金属学基础知识
金属学基础知识

比工程塑料的铸造性能好。
2. 锻造性能锻造性能是指材料是否易于进行压力加工的性能,取决于材料的塑性和变形抗力,塑性越好,变形抗力越小,材料的锻造性能越好。
例如,纯铜在室温下就有良好的锻造性能,碳素钢在加热状态锻造性能良好,铸铁则不能锻造。
热塑性塑料可经挤压和压塑成型,与金属挤压和模压成型相似。
3. 焊接性能两块材料在局部加热至熔融状态下能牢固地焊接在一起的能力称为该材料的焊接性能。
碳素钢的焊接性能主要由化学成分决定,其中含碳量的影响最大。
例如,低碳钢具有良好的焊接性,而高碳钢、铸铁的焊接性不好。
4. 热处理性能生产上,热处理既可用于提高材料的力学性能及某些特殊性能,以进一步充分发挥材料的潜力,亦可用于改善材料的加工工艺性能,如改善切削加工、拉拔挤压加工和焊接性能等。
常用的热处理方法有退火、正火、淬火、回火及表面热处理(表面淬火及化学热处理)等。
5. 切削加工性能材料接受切削加工的难易程度称为切削加工性能。
切削加工性能主要用切削速度、加工表面光洁度和刀具使用寿命来衡量。
影响切削加工性能的因素有工件的化学成分、组织、硬度、导热性及加工硬化程度等。
一般认为,具有适当硬度(170~230HBW)和足够脆性的金属材料切削性能良好,所以灰铸铁比钢切削性能好,碳素钢比高合金钢切削性能好。
改变钢的成分(如加入少量铅、磷等元素)和进行适当的热处理(如低碳钢进行退火,高碳钢进行球化退火)可改善钢的切削加工性能。
1.2 金属学基础知识1.2.1 纯金属的晶体结构1.2.1.1 晶体与非晶体1. 晶体固态下原子(或分子)呈规则排列而形成的聚集状态,称为晶体,如纯铝、纯铁、纯铜等都属于晶体。
2. 非晶体原子(或分子)呈无规则的无序堆积的聚集状态,称为非晶体,如松香、玻璃、沥青、石蜡等都属于非晶体。
绝大多数金属和合金在固态下都属于晶体。
1.2.1.2 晶体结构1. 晶格晶体内部原子是按一定的几何规律排列的。
为便于理解,把金属内部的原子近似地看成是刚性小球,则金属晶体就可看成是由刚性小球按一定几何规则紧密堆积而成的物体,如图1-5(a)所示。
金属学基础知识

一般具有规则的外形; 在不同的方向上具有不同的性能,即表现出晶体的各向异性。
非晶体:内部质点无规则的堆积在一起的物质称为非晶体。
没有固定的熔点; 表现出各向同性;
晶体与非晶体在一定条件下可互相转化。
晶体中原子排列示意图
a) 原子对垛模型
2.试验原理
试样被冲断过程中吸收 的能量即冲击吸收功( Ak )等于摆锤冲击试 样前后的势能差。
1.1.2 金属材料的力学性能
(四)硬度
1.定义
金属材料抵抗更硬的物体压入其表面的能力。
布氏硬度
洛氏硬度
1.1.2 金属材料的力学性能
1.1.3 钢的基本组织
常压下物质由分子、原子或离子构成,通常有固态、气态 和液态三种聚集状态。 晶体:内部质点按一定的几何规律呈周期性规则排列的物质称为晶体。
σb=
Fb A0
1.1.2 金属材料的力学性能
(二)塑性
1. 定义 金属材料断裂前发生永久
变形的能力。
2.衡量指标 伸长率:试样拉断后,标距的伸长与原始标距的百分比。 试样拉断后,颈缩处的横截面积的缩减量与 断面收缩率:
原始横截面积的百分比。
1.1.2 金属材料的力学性能
(三)冲击韧性
1.定义
金属材料抵抗冲击载荷 作用而不破坏的能力。
b)晶格
c)晶胞
常见金属晶格类型
体心立方晶胞 面心立方晶胞
a) 刚球模型
b)质点模型
a)刚球模型
b)质点模型
密排六方晶胞
金属结晶过程(多晶体)
相:合金中具有同一聚集状态,成分和性能均一,并以界面互 相分开的组成部分。
金属学基础知识

共析钢、亚共析钢、过共析钢1. 共析钢碳溶解在铁的晶格中形成固溶体,碳溶解到α——铁中的固溶体叫铁素体,溶解到γ——铁中的固溶体叫奥氏体。
铁素体和奥氏体都具有良好的塑性。
当铁碳合金中的碳不能全部溶入铁素体或奥氏体中时,剩余出来的碳将和铁形成化合物——碳化铁(Fe3C)这种化合物的晶体组织叫渗碳体,它的硬度极高,塑性几乎为零。
从反映钢的组织结构和钢的含碳量和钢的温度之间关系的铁碳平衡状态图上可见,当碳的含量正好等于0.77%时,即相当于合金中渗碳体(碳化铁)约占12%,铁素体约占88%时,该合金的相变是在恒温下实现的。
即在这种特定比例下的渗碳体和铁素体,在发生相变时,如果消失两者同时消失(加热时),如果出现则两者又同时出现,在这一点上这种组织和纯金属的相变类似。
基于这个原因,人们就把这种由特定比例构成的两相组织当作一种组织来看待,并且命名为珠光体,这种钢就叫做共析钢。
即含碳量正好是0.77%的钢就叫做共析钢,它的组织是珠光体。
2. 亚共析钢常用的结构钢含碳量大都在0.5%以下,由于含碳量低于0.77%,所以组织中的渗碳体量也少于12%,于是铁素体除去一部分要和渗碳体形成珠光体外,还会有多余的出现,所以这种钢的组织是铁素体+珠光体。
碳含量越少,钢组织中珠光体比例也越小,钢的强度也越低,但塑性越好,这类钢统称为亚共析钢。
3. 过共析钢工具用钢的含碳量往往超过0.77%,这种钢组织中渗碳体的比例超过12%,所以除和铁素体形成珠光体外,还有多余的渗碳体,于是这类钢的组织是珠光体+ 渗碳体。
这类钢统称为过共析钢。
二、有关钢材机械性能的名词1.屈服点(σs)钢材或试样在拉伸时,当应力超过弹性极限,即使应力不再增加,而钢材或试样仍继续发生明显的塑性变形,称此现象为屈服,而产生屈服现象时的最小应力值即为屈服点。
设Ps为屈服点s处的外力,Fo为试样断面积,则屈服点σs =Ps/Fo(MPa),Mpa 称为兆帕等于N(牛顿)/mm2,(MPa=106Pa,Pa:帕斯卡=N/m2)2.屈服强度(σ0.2)有的金属材料的屈服点极不明显,在测量上有困难,因此为了衡量材料的屈服特性,规定产生永久残余塑性变形等于一定值(一般为原长度的0.2%)时的应力,称为条件屈服强度或简称屈服强度σ0.2 。
初中金属重要知识点总结

初中金属重要知识点总结1. 金属的性质金属的性质通常包括导电性、导热性、延展性、强度和光泽。
金属通常具有良好的导电性和导热性,这是因为金属中存在着大量的自由电子,它们能够在金属内部自由移动,传导电流和热量。
金属还具有良好的延展性和强度,这意味着金属能够被拉伸成细丝或者压制成薄片,并且具有一定的抗拉力和抗压力。
此外,金属还具有良好的光泽,通常呈现出银白色或者金黄色的外观。
2. 金属的晶体结构金属的晶体结构通常表现为紧密堆积的排列,这种排列方式使得金属具有良好的延展性和强度。
在晶体结构中,金属原子通常排列成紧密的球状结构,具有较大的自由空间,并且具有良好的平衡性能。
3. 金属的熔点和沸点金属的熔点通常比较高,这是因为金属原子之间存在着较强的金属键,需要较高的温度才能够克服金属间的相互作用力而使金属熔化。
金属的沸点也较高,通常需要较高的温度才能使金属发生汽化。
4. 常见金属材料在学习初中金属知识时,通常会接触到一些常见的金属材料,例如铁、铝、铜、锌等。
这些金属材料在日常生活和工业生产中都有着广泛的应用。
例如,铁是最常见的金属材料之一,被广泛应用于建筑、交通工具、机械制造等领域。
铝具有较低的密度和良好的耐腐蚀性,被广泛应用于航空航天、食品包装等领域。
铜具有良好的导电性和导热性,被广泛应用于电子、电气和通信设备制造等领域。
锌具有良好的耐腐蚀性能,被广泛应用于镀锌、防腐蚀等领域。
5. 金属的提纯和合金在工业生产中,通常需要对金属进行提纯,以去除杂质和提高金属的纯度。
提纯金属的方法包括电解法、冶炼法、萃取法等。
此外,金属还可以通过合金的方式来改善其性能,合金是两种或两种以上金属元素以一定的比例混合而成的材料。
合金通常具有比单一金属更优异的性能,例如更高的强度、硬度、耐腐蚀性等。
6. 金属的加工和铸造金属通常需要经过加工和铸造才能够被制成各种物品。
金属的加工包括锻造、压延、挤压等工艺,通过这些工艺,金属可以得到所需要的形状和尺寸。
金属基本常识

金属基本常识金属是一类常见的物质,具有特殊的化学性质和物理性质,广泛应用于各个领域。
本文将介绍金属的基本常识,包括定义、分类、制备方法以及常见金属的性质和应用。
一、金属的定义和分类金属是一类具有金属光泽、良好导电导热性能和可塑性的物质。
根据金属元素的化学性质和晶体结构,金属可以分为两类:有色金属和黑色金属。
1. 有色金属有色金属指的是呈现出特定颜色的金属,如铜、铝、铅和锌等。
这些金属具有良好的导电导热性能、可塑性和耐腐蚀性。
有色金属广泛应用于电子、建筑、航空航天等领域。
2. 黑色金属黑色金属是指呈现黑色的金属,如铁、钢等。
这类金属具有高强度、良好的延展性和可塑性,常用于制造机械设备、建筑结构和交通工具等。
二、金属的制备方法金属的制备方法主要包括矿石冶炼、熔融电解和粉末冶金等。
1. 矿石冶炼矿石冶炼是指将含有金属元素的矿石通过冶炼工艺提取出金属。
例如,将含铜矿石进行烧烤、熔炼和电解的过程,最终得到纯铜。
2. 熔融电解熔融电解是指将金属盐、金属氧化物等在高温条件下熔化,通过电解的方式将金属离子还原成金属。
这种方法常用于制备高纯度的金属,如铝的制备。
3. 粉末冶金粉末冶金是指将金属粉末按一定的比例混合后,通过压制、烧结等工艺制备金属制品。
这种方法可以制备复杂形状的金属制品,如齿轮、刀具等。
三、常见金属的性质和应用以下介绍几种常见的金属及其性质和应用。
1. 铁铁是最常见的金属之一,具有良好的延展性和可塑性。
它广泛应用于建筑、制造机械设备和交通工具等领域。
2. 铜铜具有良好的导电导热性能和可塑性,是重要的工业材料。
它被广泛应用于电子、建筑、制造和工艺品等领域。
3. 铝铝具有较低的密度和良好的导电导热性能,广泛应用于航空航天、汽车制造和建筑等领域。
4. 锌锌具有良好的耐腐蚀性,在电镀、制造合金和防锈涂料等方面有广泛应用。
5. 镍镍是重要的合金元素,广泛用于制造不锈钢、合金钢和电池等。
结语金属作为一类重要的材料,对人类社会的发展起到了重要的推动作用。
有关金属的知识点总结

有关金属的知识点总结一、金属的性质1. 金属的物理性质:金属的物理性质主要包括导电性、热导性、弹性和延展性等。
大多数金属具有很好的导电性和热导性,这使得它们成为电线、电路、散热器等的理想材料。
同时,金属还具有较好的弹性和延展性,可以被加工成各种形状,用于制造不同的产品。
2. 金属的化学性质:金属的化学性质主要包括活泼性、耐腐蚀性等。
大多数金属都具有一定的活泼性,与非金属元素发生化学反应,形成氧化物、氢化物、硫化物等化合物。
另外,一些金属还具有很好的耐腐蚀性,可以用于制造耐腐蚀设备、管道等。
3. 金属的晶体结构:金属的分子结构是一种紧密排列的晶格结构,这种结构决定了金属的一些特性,比如硬度、延展性等。
晶体结构也是金属导电性和热导性的重要原因。
二、金属的分类1. 金属根据晶体结构可分为:(1)面心立方(FCC)结构金属,如铝、铜等;(2)体心立方(BCC)结构金属,如铁、钴等;(3)密堆排(HCP)结构金属,如钛、锌等。
2. 金属根据化学性质可分为:(1)活泼金属和不活泼金属;(2)有色金属和黑色金属。
3. 金属根据用途和性质可分为:(1)结构金属,如铝、镁等,主要用于机械结构部件;(2)功能金属,如铜、铁等,用于导电、传热等;(3)特种金属,如钨、铟等,用于特殊行业需求。
三、金属的生产1. 金属的提炼:金属提炼主要是指从矿石中提取出金属的过程。
一般来说,金属的提炼包括矿石的选矿、焙烧、冶炼等步骤。
提炼方法有传统的火法冶炼和现代的湿法冶炼等。
2. 金属的合金化:金属合金是由两种或两种以上的金属或非金属元素组成的固态溶体,具有比单一金属更优越的性能。
金属的合金化是为了改善金属的性能,满足特定的需求。
常见的金属合金有钢、铜合金、铝合金等。
3. 金属的加工:金属的加工是指将金属材料加工成所需形状和尺寸的过程,包括锻造、压延、挤压、粉末冶金等。
金属加工可以改善金属的性能、提高金属的强度和硬度等。
四、金属的应用1. 工业领域:金属在工业领域中应用广泛,主要用于机械制造、电子设备、航空航天等。
金属知识点总结大全

一、金属的基本性质1. 导电性:金属具有良好的导电性,其原子结构中的自由电子能够在金属内部自由流动,从而实现电流的传导。
2. 导热性:金属具有良好的导热性,可以快速将热量传导到周围环境中,因此常用于制造散热器和导热器等产品。
3. 可塑性:金属具有良好的可塑性,可以通过锻造、轧制等方式形成各种形状的产品。
4. 良好的机械性能:金属材料具有较高的强度和韧性,可以满足不同工程领域的需要。
二、金属的分类1. 基本金属:包括铁、铜、铝、镁、锌等,是工业生产中最常用的金属材料。
2. 合金:由两种或更多种金属或非金属混合而成,具有优良的物理和化学性能,如钢、铜合金、铝合金等。
3. 贵金属:如黄金、铂、银等,具有良好的抗腐蚀性和化学稳定性,常用于珠宝、电子器件等领域。
三、常见金属材料1. 铁:是最常见的金属材料,包括纯铁、钢和铸铁等,广泛应用于建筑、机械制造、汽车制造等领域。
2. 铝:具有良好的轻量化和耐腐蚀性能,常用于航空航天、汽车制造和建筑材料等领域。
3. 铜:具有良好的导电性和导热性,常用于电子器件、建筑材料等领域。
4. 钛:具有优良的耐腐蚀性和高强度,常用于航空航天、医疗器械等领域。
四、金属加工和制造1. 铸造:将金属熔化后倒入模具,冷却后得到所需的形状。
2. 锻造:通过对金属进行加热后进行锻打,使其得到所需的形状和尺寸。
3. 冷拔:通过在室温下拉制金属材料,使其形成所需的形状和尺寸。
4. 焊接:将两个金属材料通过加热或施加压力,使其相互连接。
5. 切削加工:通过旋转刀具等方式对金属材料进行加工,实现所需的形状和尺寸。
1. 建筑领域:金属材料常用于制造建筑结构、门窗、屋顶等部件。
2. 机械制造:金属材料广泛应用于制造机床、轴承、齿轮等机械零部件。
3. 电子设备:金属材料常用于制造电子器件、电路板、散热器等产品。
4. 汽车制造:金属材料是汽车制造的主要材料,常用于制造车身、发动机零部件等。
六、金属的环保和可持续发展1. 循环利用:金属材料可以通过回收再利用的方式,减少资源浪费和环境污染。
金属知识点

金属知识点金属是一类重要的材料,具有许多独特的性质和应用。
本文将从金属的物理性质、化学性质以及常见金属的应用等方面介绍金属的知识点。
一、金属的物理性质1. 密度:金属的密度一般较大,通常在4-20克/立方厘米之间。
例如,铁的密度为7.87克/立方厘米,铝的密度为2.7克/立方厘米。
2. 导电性:金属具有良好的导电性,是导电材料的主要成分之一。
金属中的自由电子能够在电场的作用下自由移动,形成电流。
3. 热导性:金属的热导性能较好,能够快速传递热量。
这也是为什么许多散热器、锅具等都采用金属材料制作的原因。
4. 延展性和塑性:金属具有良好的延展性和塑性,可以通过加热和加工等方式改变形状。
例如,铜线可以拉制成细丝,铝片可以轧制成薄板。
5. 磁性:金属中的某些元素具有磁性。
例如,铁、镍、钴等属于铁磁性材料,可以被磁场吸引。
二、金属的化学性质1. 氧化反应:金属与氧气反应,形成金属氧化物。
例如,铁与氧气反应生成铁氧化物,常见的铁锈即为铁氧化物的一种。
2. 酸碱反应:金属与酸或碱反应,产生相应的盐和气体。
例如,铝与盐酸反应生成氯化铝和氢气,钠与水反应生成氢气和氢氧化钠。
3. 腐蚀性:一些金属容易被环境中的氧气、水、酸等腐蚀。
例如,铁易被氧气和水腐蚀,形成铁锈;铜易被硫化氢腐蚀,形成铜绿。
三、常见金属及其应用1. 铁:铁是最常见的金属之一,广泛应用于建筑、制造业、交通运输等领域。
铁制品包括钢材、铁器等,例如建筑结构、汽车、铁路轨道等。
2. 铝:铝是轻质金属,具有良好的导电性和导热性,广泛应用于航空航天、汽车、电子等领域。
铝制品包括铝合金材料、铝箔等。
3. 铜:铜是导电性能最好的金属之一,广泛应用于电子、电力、通信等领域。
铜制品包括电线、电缆、电子元件等。
4. 锌:锌具有良好的防腐性,常用于镀锌钢板、锌合金等的制造。
此外,锌还可以用于制造电池、合金材料等。
5. 铅:铅是密度较大的金属,具有良好的耐腐蚀性和阻尼性能。
金属学基础

性材料:断裂前断口不发生明显塑性变形的材料 • 对同一材料,随试验温度降低,韧性断裂可以转
变为脆性断裂,即材料由韧性材料变为脆性材料 ,这种现象称为韧脆性转移。韧脆转移的温度称 为韧脆转变温度(金属材料的最低工作温度)。
第一章金属学基础
§1.1 金属的力学性能 §1.2 金属的物理性能 §1.3 金属的晶体结构
§1.4 金属的结晶 §1.5 合金的结构与结晶
§1.6 铁碳合金相图 §1.7 金属受力时结构和性能的变化
第一节金属的力学性能
• 通常机械零件或工程结构在工作中都要受到 外力的作用,金属在外力作用下所表现的性 能叫做力学性能。
• 金属导电能力大小的顺序与热导率基本相同
第三节 金属的晶体结构
一、晶体与非晶体
晶体的特点是: ①原子在三维空间呈有规则地周期性重复排列。 ②具有一定的熔点,绝大多数固体金属属于晶体:如 铁的熔点为1538℃,铜的熔点为1083℃。 ③晶体的性能随着原子的排列方位而改变,即单晶体 具有各向异性。
§1-3 金属的晶体结构 非晶体的特点是:
抗拉强度:
线弹性阶段
O
伸长率:d
l1 l l0
0
100%
Dl
s
b
Fb A0
断面
收缩率 y A0 A1 100%
:
A0
• 2.塑性 • 塑性是金属在外力作用下,断裂前发生不
可逆永久变形的能力。 • 试验方法为拉伸试验 • 金属材料的塑性指标:δ;ψ
三、韧性
• 又称韧度,是指金属在断裂前吸收变形能量的能 力。
Ⅰ、点缺陷 :空位和间隙原子
关于金属的知识点总结

关于金属的知识点总结一、金属的性质1. 导电性和热传导性金属具有良好的导电性和热传导性,因此广泛应用于电子设备和热传导设备中。
金属内部的电子可以自由移动,从而形成电流和导热。
例如,铝、铜和铁等金属是常见的导电材料。
2. 延展性和塑性金属具有良好的延展性和塑性,可以被拉伸成细丝或者压制成薄片。
这使得金属可以用来制造各种各样的产品,如金属线、金属箔等。
3. 色泽和光泽大多数金属具有一定的色泽和光泽。
例如,黄金呈现出金黄色的光泽,银则呈现出银白色的光泽。
4. 密度和硬度金属的密度和硬度一般较高。
例如,铁和铝的密度分别为7.87g/cm³和2.7g/cm³,硬度也较高。
5. 融点和沸点金属的融点和沸点一般较高,具有良好的热稳定性。
例如,铁的融点为1535°C,铝的融点为660°C。
二、金属的分类根据金属的性质和化学特性,金属可以分为两大类别:有色金属和黑色金属。
1. 有色金属有色金属指的是那些具有相对较高的反射率和一定的色泽的金属。
常见的有色金属包括铜、铝、铅、锌、镍、锡、钛等。
有色金属一般用于制造装饰品、电线、管道、合金等产品。
2. 黑色金属黑色金属指的是那些具有黑色或者暗色的金属。
常见的黑色金属包括铁、钢、铬、锰、钨等。
黑色金属一般用于制造建筑材料、机械设备、汽车零件等产品。
三、金属的应用金属广泛应用于各个领域,包括工业制造、建筑建材、电子设备、汽车制造、航空航天等。
1. 工业制造金属是工业制造中最重要的原材料之一。
金属制品广泛用于机械设备、仪器仪表、轴承、齿轮、管道等产品的制造。
2. 建筑建材金属也被广泛用于建筑建材中。
例如,铝合金被用于制造窗户和门框、铁和钢被用于制造支撑结构、屋顶和楼梯等。
3. 电子设备金属是电子设备中不可或缺的材料。
例如,铜被用于制造电线和电缆,铝被用于制造散热器和外壳,金被用于制造电子元件等。
4. 汽车制造金属在汽车制造中扮演着重要角色。
金属学知识点总结

第一章金属的晶体结构1、除化学成分外,金属的内部结构和组织状态也是决定金属材料性能的重要因素。
2、将阵点用直线连接起来形成空间格子,称之为晶格。
3、晶胞中原子排列的紧密程度通常用两个参数来表征:配位数、致密度。
4、原子所占体积与晶胞体积之比称为致密度。
5、体心立方结构有两种间隙:一种是八面体间隙,另一种是四面体间隙。
6、在晶体中,由一系列原子所组成的平面称为晶面,任意两个原子之间连线所指的方向称为晶向。
7、晶体的点缺陷有三种:空位、间隙原子和置换原子。
8、塑性变形时,由于局部区域的晶体发生滑移即可形成位错。
9、刃型位错的柏氏矢量与其位错线相垂直,螺型位错的柏氏矢量与其位错线相平行。
10、把单位体积中所包含的位错线的总长度称为位错密度。
11、晶体的面缺陷包括晶体的外表面和内界面两类。
12、晶体的内界面缺陷有:晶界、亚晶界、孪晶界、堆垛层错和相界等。
13、金属:是具有正的电阻温度系数的物质,其电阻随温度的升高而增加。
14、晶体:原子在三维空间作有规则的周期性排列的物质称为晶体。
15、晶体结构:是指晶体中原子在三维空间有规律的周期性的具体排列方式。
16、点阵:能清楚地表明原子在空间排列规律性的原子的几何点,称之为点阵。
17、晶胞:晶格中能够完全反映晶格特征的最小的几何单元,称为晶胞。
用来分析晶体中原子排列的规律性。
18、配位数:是指晶体结构中与任一个原子最邻近、等距离的原子数目。
19、螺型位错:设想在立方晶体右端施加一切应力,使右端上下两部分沿滑移面发生了一个原子间距的相对切边,这种晶体缺陷就是螺型位错。
20、表面能:由于在表面层产生了晶格畸变,其能量就要升高,这种单位面积上升高的能量称为比表面能,简称表面能。
21、什么是晶体?晶体有何特性?答:晶体:原子在三维空间作有规则的周期性排列的物质称为晶体。
1)晶体具有一定的熔点。
在熔点以上,晶体变为液体,处于非晶体状;在熔点以下,液体又变为晶体。
2)晶体的另一个特点是在不同的方向上测量其性能,表现出或大或小的差异,称为各向异性或异向性。
金属学基础知识

高炉产品
铸造生铁---这类生铁断口呈暗灰色。 含硅量较高,用于机械制造厂生产铸件。 炼钢生铁---这类生铁断口呈暗灰色。含 硅量较低(1.5%),用于在炼钢炉中炼钢。 高炉冶炼的副产品是煤气和炉渣。煤气 有很高的经济价值。高炉炉渣主要成分是氧 化钙、二氧化硅。可以用来制造水泥渣棉、 渣砖等建筑材料。
图1—1为退火低碳钢拉伸曲线 示意图。曲线的纵坐标为载荷(P), 横坐标是绝对伸长(△L),由图可 见,载荷比较小时,试样伸长随 载荷增加成正比例增加,保持直 线关系。载荷超过户。后,拉伸 曲线开始偏离直线。载荷在Pe以 下阶段,试样在加载时发生变形, 卸载后变形能完全恢复,该阶段 为弹性变形阶段。当载荷超过Pe 后,试样在继续产生弹性变形的 同时,将产生塑性变形,进入弹 塑性变形阶段。此时,若在
第一节 拉伸曲线和应力应变曲线 拉伸试验是工业上最广泛使 用的力学性能试验方法之一。试 验时在拉伸机上对圆柱试样或板 状试样两端缓慢地施加载荷,使 试样受轴向拉力沿轴向伸长,一 般进行到拉断为止。 一般试验机都带有自动汜录 装置,可把作用在试样上的力和 所引起的试样伸长自动记录下来, 绘出载荷—伸长曲线,称拉伸曲 线或拉伸图。 P
铁矿石在570º C---1200º C之间受到一氧 化碳气体和红热焦碳的还原,形成了海棉状 铁,这种铁在1000º C---1200º C的高温下 会 从一氧化碳和焦碳中溶入大量的碳---含碳量 可达百分之四。因而铁的熔点下降,于是就 形成了生铁。生铁的熔点约为1200º C。因次 经过溶碳作用之后,生铁以液体状态滴入炉 缸。
2 金属的化学性能 耐腐蚀性 抗氧化性
二 金属的工艺性能
1 2 3 4 铸造性 锻压性 焊接性 切削加工性
三 金属的力学性能
金属所有知识点总结

金属所有知识点总结一、金属的基本性质1. 金属的结构和成分金属的晶体结构通常是紧密堆积的球形原子构成的各向同性结构。
金属的晶体结构通常是面心立方结构(如铝、铜、铂等金属)、体心立方结构(如铁、钒、钽等金属)或者简单立方结构(如钾、银、钠等金属)。
2. 金属的物理性质金属的物理性质主要包括金属的硬度、导电性、导热性、光泽和延展性。
金属通常具有较好的硬度和刚性,同时具有良好的导电导热性能。
此外,金属通常具有光泽并且可以被延展成薄片并制成不同形状。
3. 金属的化学性质金属的化学性质主要包括金属的化学活性、与其他物质的反应性以及在化学反应中的离子性等特点。
大部分金属具有较强的还原性,可以与非金属元素形成氧化物或盐等化合物。
同时,金属通常在化学反应中以正离子的形式存在。
4. 金属的熔点和沸点金属的熔点和沸点是金属固态、液态和气态状态的转变温度。
金属通常具有较高的熔点和沸点,能够在一定的温度下形成稳定的固态结构。
二、金属的种类根据金属的晶体结构和性质,可以将金属分为不同的类别,主要包括有色金属、贵金属、稀有金属、黑色金属等不同类别。
1. 有色金属有色金属是指具有明显颜色的金属,包括铜、铝、镍、锌、铅等。
有色金属通常具有良好的导电导热性能,并且在电子工业、建筑工业和航空航天等领域有广泛的应用。
2. 贵金属贵金属是指珍贵且稀有的金属,包括金、银、铂、钯、铱等。
贵金属通常具有良好的稳定性和化学反应性,因此被广泛用于首饰、电子产品、化工催化剂等方面。
3. 稀有金属稀有金属是指地壳中含量较少的金属,包括钨、锆、铌、钽等。
稀有金属通常具有高熔点和高硬度,被广泛应用于合金、耐磨材料、电子器件等方面。
4. 黑色金属黑色金属主要指铁、锰、铬、钴等。
黑色金属具有较高的熔点和较好的磁性,广泛应用于冶金、机械加工、建筑结构等领域。
三、金属的应用领域金属在现代社会的生产生活中有着广泛的应用。
1. 金属材料金属材料是工程技术中使用最广泛的材料之一,用于制造机械设备、汽车船舶、建筑结构等。
金属知识点归纳总结

金属知识点归纳总结一、金属的基本性质1. 导电性:金属具有良好的导电性能,可以轻易传递电子,在电路中广泛应用。
2. 热导性:金属具有良好的热导性能,能够快速传导热量,因此常被用于锅具、散热器等。
3. 延展性:金属具有很高的延展性,可以被拉伸成铜丝、铝箔等细长材料。
4. 强度:金属具有较高的抗拉强度和硬度,可以用于制造机械零件、建筑结构等。
5. 反射性:金属具有良好的光反射性,被用于制造镜子、光学部件等。
6. 密度:金属的密度较高,是坚固材料选用的首选。
二、常见金属材料1. 铁:铁是地壳中含量最丰富的金属元素,被广泛用于制造钢铁材料。
2. 铝:铝具有优良的抗腐蚀性和轻质特性,被广泛用于航空航天、汽车制造等领域。
3. 铜:铜是一种重要的导电材料,广泛用于电气设备、通讯设备等领域。
4. 锌:锌具有良好的阻隔性,被用于防腐蚀材料的涂层。
5. 镍:镍具有良好的耐磨性和抗腐蚀性,广泛用于化工设备、航空发动机等领域。
6. 钛:钛具有良好的耐高温性能和抗腐蚀能力,被广泛用于航空航天、医疗设备等高端领域。
三、金属加工1. 铸造:铸造是将金属熔化后注入模具中凝固成型的工艺,用于制造大型铸件、汽车零部件等。
2. 锻造:锻造是将金属加热后进行锻打成型的工艺,用于制造轴类零件、锻造工具等。
3. 深冲:深冲是将金属板料放入冲床中进行冲压成型的工艺,用于制造汽车车身、家用电器外壳等。
4. 焊接:焊接是将金属材料通过热能和压力进行熔接的工艺,用于制造管道、船舶结构等。
5. 长条材:长条材是将金属材料通过拉拔、挤压等工艺制成的长条状材料,用于制造线材、型材等。
四、金属应用1. 建筑领域:金属材料被广泛应用于建筑结构、屋面材料、门窗等。
2. 交通运输:金属材料被广泛应用于汽车、飞机、船舶等交通工具的制造中。
3. 电子产品:金属材料被广泛应用于手机、电脑、家电等电子产品的外壳和内部零部件中。
4. 医疗设备:金属材料被广泛应用于手术器械、人工骨骼等医疗设备中。
金属学的基础知识
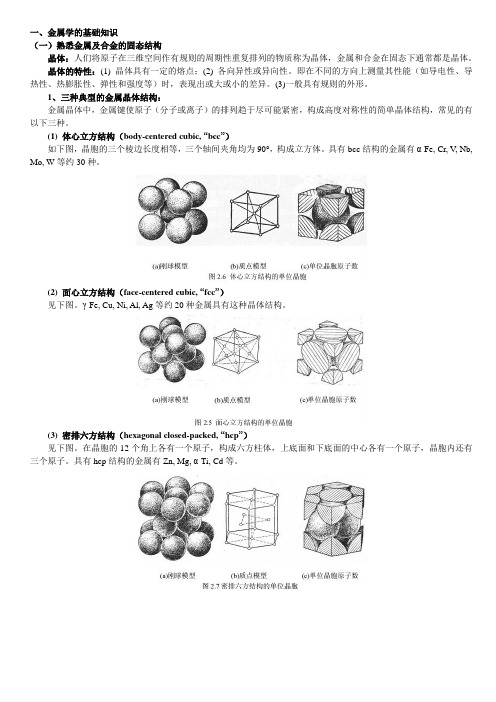
(一)熟悉金属及合金的固态结构晶体:人们将原子在三维空间作有规则的周期性重复排列的物质称为晶体,金属和合金在固态下通常都是晶体。
晶体的特性:(1) 晶体具有一定的熔点;(2) 各向异性或异向性。
即在不同的方向上测量其性能(如导电性、导热性、热膨胀性、弹性和强度等)时,表现出或大或小的差异。
(3)一般具有规则的外形。
1、三种典型的金属晶体结构:金属晶体中,金属键使原子(分子或离子)的排列趋于尽可能紧密,构成高度对称性的简单晶体结构,常见的有以下三种。
(1) 体心立方结构(body-centered cubic, “bcc”)如下图,晶胞的三个棱边长度相等,三个轴间夹角均为90°,构成立方体。
具有bcc结构的金属有α-Fe, Cr, V, Nb, Mo, W等约30种。
(2) 面心立方结构(face-centered cubic, “fcc”)见下图。
γ-Fe, Cu, Ni, Al, Ag等约20种金属具有这种晶体结构。
(3) 密排六方结构(hexagonal closed-packed, “hcp”)见下图。
在晶胞的12个角上各有一个原子,构成六方柱体,上底面和下底面的中心各有一个原子,晶胞内还有三个原子。
具有hcp结构的金属有Zn, Mg, α-Ti, Cd等。
多晶型转变(同素异构转变):大部分金属只有一种晶体结构,但也有少数金属如Fe、Mn、Ti、Co等具有两种或几种晶体结构,即具有多晶型。
当外部条件(如温度和压强)改变时,金属内部由一种晶体结构向另一种晶体结构的转变称为多晶型转变或同素异构转变。
如Fe在912℃以下为bcc结构,称为α-Fe,在912-1394℃,具有fcc结构,称为γ-Fe,而从1394℃至熔点,又转变为bcc结构,称为δ-Fe。
2、合金的晶体结构:在液态下,大多数合金的组元均能相互溶解,称为均匀的液体,因而只具有一个液相。
但凝固后,由于各组元的晶体结构、原子结构等不同,各组元之间的相互作用不同,在固态合金中可能出现不同的相结构(phase structure),主要有固溶体(solid solution)和金属化合物(intermetallic compound)两大类。
工程材料学_第一章-金属学基础知识

晶向(crystal direction) :
通过晶体中任意两个原子中心连线来表示晶体结构的空间的各 个方向。 晶胞原子数:一个晶胞内包含的原子数目。
原子半径:晶胞中原子密度最大的方向上相邻两原子之间
平衡距离的一半,与晶格常数有一定的关系。 配位数:晶格中任一原子处于相等距离并相距最近原子数
的性能、塑性变形及其组织 转变均有极为重要的作用 。
通过冷塑性变形,提高位错
密度使得金属强度、硬度提
高的方法称为加工硬化。
面缺陷-晶界与亚晶界
大角度晶界---晶界
小角度晶界---亚晶界
大角度晶界---晶界
小角度晶界---亚晶界
小角度晶界---亚晶界
大角度晶界---晶界
金属的晶体结构
合金与合金的相结构
•单相合金组织(homogeneous structure )与多相合金组织 (Heterogenous structure):显微组织为单相的称为单相组织,为 多相的称为多相组织。
•合金组织的相:构成合金组织的各个相称为合金组织的相。 • 相结构:相组成物的晶体结构称为合金的相结构
二、合金的相结构
点位置的异类原子
线缺陷
位错( dislocation ):晶格的一部分相对
于另一部分发生的局部滑移现象,或者说 局部原子发生有规律的位置错排现象
面缺陷
晶界( grain boundary ) 亚晶界( sub-boundary )
点缺陷
置换原子
间隙原子
化合物离子晶体两种常见的缺陷
晶格空位
(1)晶面(crystal face)和晶向( crystal directions ):
晶向指数(indices of directions)和晶面指数(indices of crystal-plane)是分
高三金属知识点

高三金属知识点金属是物质世界中常见的一类物质,具有良好的导电性、热传导性、延展性和塑性等特点,广泛应用于工业、建筑、电子、交通等领域。
在高三的学习中,了解金属的知识点,对于理解相关学科内容和解决问题都具有重要意义。
下面将介绍高三金属知识点的相关内容。
一、金属元素与金属晶体结构金属元素是指具有金属特性的化学元素。
金属晶体结构是指金属元素在固态下形成的晶体结构。
常见的金属晶体结构有面心立方结构、体心立方结构和六方密堆积结构。
二、金属的物理性质1. 密度:金属的密度通常较大,其数值随原子质量的增大而增大。
2. 熔点和沸点:金属的熔点通常较高,但也有一些低熔点金属。
金属具有良好的导热性,热传导速度快。
3. 导电性和热传导性:金属具有良好的导电性和热传导性,能够传递电能和热能。
4. 弹性和塑性:金属在受力后能够发生形变,具有一定的延展性和塑性。
5. 光泽性:金属表面可反射光线,呈现出光泽。
三、金属的化学性质1. 金属的活泼性:金属元素的活泼性是指其在化学反应中易于失去电子形成阳离子的倾向。
金属活泼性由活泼性顺序来进行比较。
2. 金属的腐蚀:金属在氧气、水和酸等环境中会发生腐蚀反应,导致金属的破坏。
3. 金属的氧化反应:金属与氧气发生氧化反应,产生金属氧化物。
不同金属的氧化物具有不同的性质。
四、金属的提取与提纯1. 金属的矿石:金属一般以矿石的形式存在于地壳中,矿石是含有可提取金属的矿石矿物。
2. 金属的提取方法:金属的提取方法包括熔炼、化学法、电解等。
3. 金属的提纯:金属提取后,需要进行提纯处理,以提高金属的纯度和性能。
五、金属的应用1. 工业应用:金属在工业生产中应用广泛,如铜用于电线、铝用于制造飞机和汽车等。
2. 建筑应用:金属用于建筑领域,如钢结构、铝合金门窗等。
3. 电子应用:金属在电子领域具有重要应用,如导线、电子器件等。
4. 交通运输:金属在汽车、火车、船舶等交通工具中起到关键作用。
综上所述,金属是一种重要的物质,具有独特的物理性质和化学性质。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
共析钢、亚共析钢、过共析钢
1. 共析钢
碳溶解在铁的晶格中形成固溶体,碳溶解到a――中的固溶体叫铁素体,
溶解到丫一一中的固溶体叫奥氏体。
铁素体与奥氏体都具有良好的塑性。
当铁碳合金中的碳不能全部溶入铁素体或奥氏体中时,剩余出来的碳将与铁形成化合物——碳化铁(Fe3C)这种化合物的晶体组织叫渗碳体,它的硬度极高,塑性几乎为零。
从反映钢的组织结构与钢的含碳量和钢的温度之间关系的铁碳平衡状态图上可见,当碳的含量正好等于0.77%时,即相当于合金中渗碳体(碳化铁)约占12%,铁素体约占88%时,该合金的相变是在恒温下实现的。
即在这种特定比例下的渗碳体和铁素体,在发生相变时,如果消失两者同时消失(加热时),如
果出现则两者又同时出现,在这一点上这种组织与纯金属的相变类似。
基于这个原因,人们就把这种由特定比例构成的两相组织当作一种组织来看待,并且命名为珠光体,这种钢就叫做共析钢。
即含碳量正好是 0.77%的钢就叫做共析钢,它的组织是珠光体。
2. 亚共析钢
常用的结构钢含碳量大都在0.5%以下,由于含碳量低于 0.77%,所以组织中的
渗碳体量也少于 12%,于是铁素体除去一部分要与渗碳体形成珠光体外,还会有多余的出现,所以这种钢的组织是铁素体+珠光体。
碳含量越少,钢组织中珠光体
比例也越小,钢的强度也越低,但塑性越好,这类钢统称为亚共析钢。
3. 过共析钢
工具用钢的含碳量往往超过 0.77%,这种钢组织中渗碳体的比例超过 12%,所以除与铁素体形成珠光体外,还有多余的渗碳体,于是这类钢的组织是珠光体+
渗碳体。
这类钢统称为过共析钢。
二、有关钢材机械性能的名词
1•屈服点(<rS
钢材或试样在拉伸时,当应力超过弹性极限,即使应力不再增加,而钢材或试样仍继续发生明显的塑性变形,称此现象为屈服,而产生屈服现象时的最小应力值即为屈服点。
设Ps为屈服点s处的外力,Fo为试样断面积,则屈服点 d s =Ps/Fo(MPa,) Mpa
称为兆帕等于 N (牛顿)/mm2 , ( MPa=106Pa, Pa:帕斯卡=N/m2 )
2•屈服强度(d 0.2
有的金属材料的屈服点极不明显,在测量上有困难,因此为了衡量材料的屈服
特性,规定产生永久残余塑性变形等于一定值(一般为原长度的0.2%)时的应力,
称为条件屈服强度或简称屈服强度 d 0.2。
4. 抗拉强度(db)材料在拉伸过程中,从开始到发生断裂时所达到的最大应力值。
它表示钢材抵抗断裂的能力大小。
与抗拉强度相应的还有抗压强度、抗弯强度等。
设Pb为材料被拉断前达到的最大拉力,Fo为试样截面面积,则抗拉强度 d b= Pb
/Fo ( MPa)。
4.伸长率(3)
材料在拉断后,其塑性伸长的长度与原试样长度的百分比叫伸长率或延伸率。
5. 屈强比((T s/ )r b 钢材的屈服点(屈服强度)与抗拉强度的比值,称为屈强比。
屈强比越大,结构
零件的可靠性越高,一般碳素钢屈强比为0.6-0.65,低合金结构钢为 0.65-0.75合金
结构钢为 0.84-0.86。
6. 硬度硬度表示材料抵抗硬物体压入其表面的能力。
它是金属材料的重要性能指标之一。
一般硬度越高,耐磨性越好。
常用的硬度指标有布氏硬度、洛氏硬度和维氏硬度。
⑴布氏硬度(HB )以一定的载荷(一般 3000kg)把一定大小(直径一般为 10mm)的淬硬钢球压入材料表面,保持一段时间,去载后,负荷与其压痕面积之比值,即为布氏硬度值(HB),
单位为公斤力 /mm2 (N/mm2)。
⑵洛氏硬度(HR)
当 HB>450 或者试样过小时,不能采用布氏硬度试验而改用洛氏硬度计量。
它是用一个顶角 120°的金刚石圆锥体或直径为 1.59、3.18mm 的钢球,在一定载荷下压入被测材料表面,由压痕的深度求出材料的硬度。
根据试验材料硬度的不同,分三种不同的标度来表示:
HRA :是采用60kg载荷和钻石锥压入器求得的硬度,用于硬度极高的材料(如硬质合
HRB :是采用 100kg 载荷和直径 1.58mm 淬硬的钢球,求得的硬度,用于硬度较低的材料(如退火钢、铸铁等)。
HRC :是采用150kg载荷和钻石锥压入器求得的硬度,用于硬度很高的材料(如淬火钢
等)。
⑶维氏硬度(HV )
以 120kg 以内的载荷和顶角为 136°的金刚石方形锥压入器压入材料表面,用材料压痕凹
坑的表面积除以载荷值,即为维氏硬度值( HV)
三、有关钢的热处理的名词
1. 钢的退火
将钢加热到一定温度并保温一段时间,然后使它慢慢冷却,称为退火。
钢的退火是将钢加热到发生相变或部分相变的温度,经过保温后缓慢冷却的热处理方法。
退火的目的,是为了消除组织缺陷,改善组织使成分均匀化以及细化晶粒,提高钢的力学性能,减少残余应力;同时可降低硬度,提高塑性和韧性,改善切削加工性能。
所以退火既为了消除和改善前道工序遗留的组织缺陷和内应力,又为后续工序作好准备,故退火是属于半成品热处理,又称预先热处理。
2. 钢的正火
正火是将钢加热到临界温度以上,使钢全部转变为均匀的奥氏体,然后在空气中自然冷却的热处理方法。
它能消除过共析钢的网状渗碳体,对于亚共析钢正火可细化晶格,提高综合力学性能,对要求不高的零件用正火代替退火工艺是比较经济的。
3. 钢的淬火
淬火是将钢加热到临界温度以上,保温一段时间,然后很快放入淬火剂中,使其温度骤然降低,以大于临界冷却速度的速度急速冷却,而获得以马氏体为主的不平衡组织的热处理方法。
淬火能增加钢的强度和硬度,但要减少其塑性。
淬火中常用的淬火剂有:水、油、
碱水和盐类溶液等。
4. 钢的回火
将已经淬火的钢重新加热到一定温度,再用一定方法冷却称为回火。
其目的是消除淬火产生的内应力,降低硬度和脆性,以取得预期的力学性能。
回火分高温回火、中温回火和低温回火三类。
回火多与淬火、正火配合使用。
⑴调质处理:淬火后高温回火的热处理方法称为调质处理。
高温回火是指在500-650C之
间进行回火。
调质可以使钢的性能,材质得到很大程度的调整,其强度、塑性和韧性都较好,具有良
好的综合机械性能。
⑵时效处理:为了消除精密量具或模具、零件在长期使用中尺寸、形状发生变化,常在低温回火后(低温回火温度 150-250 C)精加工前,把工件重新加热到100-150 C,保持5 -20 小时,这种为稳定精密制件质量的处理,称为时效。
对在低温或动载荷条件下的钢材构件进行时效处理,以消除残余应力,稳定钢材组织和尺寸,尤为重要。
6. 钢的表面热处理
⑴表面淬火:是将钢件的表面通过快速加热到临界温度以上,但热量还未来得及传到心部之前迅速冷却,这样就可以把表面层被淬火在马氏体组织,而心部没有发生相变,这就实现了表面淬硬而心部不变的目的。
适用于中碳钢。
⑵化学热处理:是指将化学元素的原子,借助高温时原子扩散的能力,把它渗入到工件的表面层去,来改变工件表面层的化学成分和结构,从而达到使钢的表面层具有特定要求的组织和性能的一种热处理工艺。
按照渗入元素的种类不同,化学热处理可分为渗碳、渗氮、氰化和渗金属法等四种。
渗碳:渗碳是指使碳原子渗入到钢表面层的过程。
也是使低碳钢的工件具有高碳钢的表面层,再经过淬火和低温回火,使工件的表面层具有高硬度和耐磨性,而工件的中心部分仍然保持着低碳钢的韧性和塑性。
渗氮:又称氮化,是指向钢的表面层渗入氮原子的过程。
其目的是提高表面层的硬度与耐磨性以及提高疲劳强度、抗腐蚀性等。
目前生产中多采用气体渗氮法。
氰化:又称碳氮共渗,是指在钢中同时渗入碳原子与氮原子的过程。
它使钢表面具有渗碳与渗氮的特性。
渗金属:是指以金属原子渗入钢的表面层的过程。
它是使钢的表面层合金化,以使工件表面具有某些合金钢、特殊钢的特性,如耐热、耐磨、抗氧化、耐腐蚀等。
生产中常用的有渗铝、渗铬、渗硼、渗硅等。
