天然药化
天然药化

1、具反映该天然药物(中药)临床疗效的生物活性;不代表疗效为活性成分。 2、化学上单一结构的化合物(单体)。 3、在植物中有效成分的多样性和复杂性
4、 有效成分与无效成分的相对性
• 有效部位:主要含有效成分的中药提取分离部分称为有效部位。有
• 新药开发难度加大: 筛选命中率万分之一,
中药存在的主要问题
• 产品水平急待提高 • 规范建设有待完善 • 基础性研究有待加强 • 产业规模需要扩展 • 应用市场需要开拓
中药化学研究的现状
• 已对200多种中药与天然药物进行了比较全 面系统的化学研究,其中包括一些最常用 的中药,如: • 人参、三七、大黄、甘草、黄连、白术、 广藿香、苍术、丹参、天麻、贝母、芍药、 党参、肉苁蓉、川芍、乌头、黄芩、知母、 紫草、厚朴、五味子、防风、羌活、麻黄、 沉香、灵芝、淫羊霍、黄花蒿等等。
(二)国内发展史
炼丹术与升华药物的实践发现、汞齐法技术的实 践、黑火药的配伍实践、酶解、酸解、碱解及氧化制 品的实践、提取分离纯化方法制取纯成分的实践 明代李挺在《医学入门》(1575)中就记载了 用发酵法从五倍子中得到没食子酸的过程。1711年 由洪遵所著《集验方》一书,记载了用升华法制备 纯化樟脑的过程。这些方法都早于国外,故有“医 药化学源于中国”的高度评价。
385( 383) 414( 415)
2313( 2309) 879( 861)
11118( 11146) 1574( 1581) 80 12772( 12807)
我国中药与天然药物资源的统计(1995年)
类 别 种 数
11146 115 292 52 43 456 10188 1581 80
天然药物化学的定义

天然药物化学的定义天然药物化学是研究天然产物的化学结构、化学特性和生物学活性,以及这些产物在药物发现和开发中的应用的分支学科。
天然药物化学包括从天然资源中分离、纯化和鉴定生物活性化合物的技术和方法,以及用于合成类似分子的有机合成和机制研究。
随着对复杂药物发现和开发的需求不断增加、分析技术不断提高,天然药物化学在药物研究和开发中的地位越来越重要。
天然药物化学研究的目的是了解天然产物的化学结构、生物学活性和药理学特征,为发现新的天然产物药物和开发药物带来启示。
天然药物化学家通过从各种生物体中分离和纯化有生物活性的天然物质,如植物、微生物和动物,来收集有关它们的化学信息。
然后,天然药物化学家将这些物质的结构鉴定和解决分子的化学结构、化学特性和背景知识,以便了解其在药物发现和开发中的应用。
这种专业的知识使它们能够优化这些化合物,以增加它们的效力或减少它们的毒副作用,并改善它们的化学稳定性和制剂属性。
天然药物化学在天然产物的化学分析方面极为重要。
这种类型的化学分析使用多种技术和方法来分离、提纯和鉴定天然产物。
例如,对于复杂的混合物,天然药物化学家可以使用高效液相色谱(HPLC)或气相色谱(GC)等技术来提取单个分离物。
然后,他们可能会使用核磁共振(NMR)或质谱(MS)等技术来获取有关该分子的化学和结构信息,并开发分子的结构-活性关系。
天然药物化学的主要目标是从复杂的混合物中分离出一种或多种有生物活性的化合物,并了解它们的药理学属性。
另一个研究天然药物化学的领域是通过有机合成复制自然产物结构来创建新的天然产物类似物。
这种方法被称为半合成法。
利用这种方法,天然药物化学家可以调整原来的天然产物的结构,以优化它们的药理学性质,或创造新的药物。
即使天然药物化合物有助于药物研究和开发,但它们并不总是合适的药物治疗方案。
因此,天然药物化学家使用化学合成技术创造类似分子,以获得更好的药理学性质或更好的制剂性质。
总之,天然药物化学是一个广泛的领域,涵盖了从天然产物中分离、纯化和鉴定生物活性化合物的技术和方法,以及用于合成类似分子的有机合成和机制研究。
天然药化完整版

1、两相溶剂萃取的原理的利用混合物中各成分在两相溶剂中的()A 比重不同B 分配系数不同C 分离系数不同D 萃取常熟不同E 介电常数不同2、原理为氢键吸附的色谱是A 离子交换色谱B 凝胶滤过色谱C 聚酰胺色谱D 硅胶色谱E氧化铝色谱3分馏法分离适用于A 极性大成分B 极性小成分C 升华性成分D 挥发性成分E内脂类成分4、聚酰胺薄层色谱,下列展开剂中展开能力最强的是A 30%乙醇B 无水乙醇C 70%乙醇D 丙酮E 水5、可将天然药物水提液中的亲水性成分萃取出来的溶剂是A 乙醚B 醋酸乙酯C 丙酮D 正丁醇E 乙醇6、红外光谱的单位是A cm-1B nmC m/zD mmE g7、生物碱沉淀反应的条件是A 酸性水溶液B 碱性水溶液C 中性水溶液D 盐水溶液E 醇溶液8、下列生物碱碱性最强是的A 莨菪碱B 东莨菪碱C 山莨菪碱D N-去甲基莨菪碱E 樟柳碱9、溶解游离亲脂性生物碱的最好溶剂为A 水B 甲醇C 正丁醇D 氯仿E 苯10、游离麻黄碱所具有的性质是A 黄色B 升华性C 挥发性D 发泡性E 溶血性11、最难被算水解的是A 氧苷B 氮苷C 硫苷D 碳苷E 氰苷12、提取苷类成分时,为抑制或破坏酶常加入一定量的A 硫酸B 酒石酸C 碳酸钙D 氢氧化钠E 碳酸钠13、大黄根在新鲜植物体的生长阶段,夏季存在的主要成分类型是A 蒽醌类B 蒽庝类C 蒽酚类D 氧化蒽酚类E 蒽二酚类14、由于此题涉及到图形,无法绘出,因此飘过···15、在羟基蒽醌的红外光谱中,有1个羟基峰的化合物是A 大黄素B 大黄酚C 大黄素甲醚D 茜草素E 羟基茜草素16、下列黄酮类型酸性最强的是A 7-OH黄酮B 4-OH黄酮C 7,4-二OH黄酮D 5,6-OH黄酮E 6,8-二OH 黄酮17、四氢硼钠反应用于鉴别A黄酮、黄酮醇B异黄酮C杏耳酮D黄色素E二氢黄酮、二氢黄酮醇18.硅胶吸附TLC,以苯-甲酸甲酯-甲酸(5︰4︰1)为展开剂,下列化合物Rf值最大的是A.山奈素B.槲皮素C.山奈素-3-O-葡萄糖苷D.山奈素-3-O-芸香糖苷E.山奈素-3-O-鼠李糖苷19.1H-NMR中,推断黄酮类化合物类型主要是依据A.B环H-3′的特征B.C环质子的特征C.A环H-5的特征D.A环H-7的特征E.B环H-2′和H-6′的特征20. 黄酮苷类化合物不能采用的提取方法是A.酸提碱沉B.碱提酸沉C.沸水提取D.乙醇提取E.甲醇提取21.香豆素的基本母核为A. 苯并α-吡喃酮B. 对羟基桂皮酸C. 反式邻羟基桂皮酸D. 顺式邻羟基桂皮酸E.苯并γ-吡喃酮22.鉴别香豆素首选的显色反应为A. 三氯化铁反应B. Gibb’s反应C. Emerson反应D. 异羟肟酸铁反应E. 三氯化铝反应23. 挥发油折光率一般在:A. 1.330~1.430B. 1.440~1.530C. 1.430~1.610D. 1.510~1.610E. 1.330~1.61024.分离挥发油中的羰基成分,常采用的试剂为:A. 亚硫酸氢钠试剂B. 三氯化铁试剂C. 2%高锰酸钾溶液D. 异羟肟酸铁试剂E. 香草醛浓硫酸试剂25.不符合甾体皂苷元结构特点的是A. 含A、B、C、D、E和F六个环B. E环和F环以螺缩酮形式连接C. E环是呋喃环,F环是吡喃环D. C10、C13、C17位侧链均为β-构型E. 分子中常含羧基,又称酸性皂苷26.可用于分离甾体皂苷和三萜皂苷的方法是A. 正丁醇提取法B. 明胶沉淀法C. 分段沉淀法D. 胆甾醇沉淀法E. 乙醇沉淀法27.甲型强心苷甾体母核的C-17位上连接的基团是A. 甲基B. 五元饱和内酯环C. 五元不饱和内酯环D. 六元饱和内酯环E. 六元不饱和内酯环28.水解强心苷不使苷元发生变化用A. 0.02~0.05mol/L盐酸B. 氢氧化钠/水C. 3~5%盐酸D. 碳酸氢钠/水E. 氢氧化钠/乙醇29.强心苷甾体母核的反应不包括A. Tschugaev反应B. Salkowski反应C. Chloramine T反应D. Raymond反应E. Liebemann-Burchard反应30. 在水液中不能被乙醇沉淀的是A. 蛋白质B. 多肽C. 多糖D. 酶E. 鞣质B型题[31-50](共10分,每题0.5分)[31-35]A. 离子交换色谱B. 聚酰胺色谱C. 凝胶色谱D. 氧化铝色谱E. 硅胶分配色谱31.黄酮类化合物的分离优先采用32.蛋白质、多糖类化合物的分离优先采用33.有机酸类化合物的分离优先采用34. 生物碱类化合物的分离优先采用35. 皂苷类化合物的分离优先采用[36-40]A. 杂化方式B. 诱导效应C. 共轭效应D. 空间效应E. 分子内氢键36. 东莨菪碱碱性比莨菪碱弱是因为37. 秋水仙碱碱性弱的原因是由于38. 麻黄碱碱性强于去甲麻黄碱是由于39. 小檗碱碱性强的原因是由于40. 伪麻黄碱碱性强于麻黄碱是由于[41-45]A. 三氯化铁试剂B. 2%高锰酸钾溶液C. 异羟肟酸铁试剂D. 2,4-二硝基苯肼试剂E. 硝酸铈铵试剂41. 检查挥发油中是否含有不饱和化合物常选用42. 检查挥发油中是否含有羰基成分常选用43. 检查挥发油中是否含有酚羟基成分常选用44. 检查挥发油中是否含有酯或内酯成分常选用45. 检查挥发油中是否含有醇类成分常选用[46-50]A.向红位移B.向紫位移C.向低场方向位移D.向高场方向位移E.没有变化46.B环上增加羟基等供电子基,将使紫外光谱带Ⅰ47.A环上增加羟基等供电子基,将使紫外光谱带Ⅱ48.A环上增加酚羟基,将使A环上氢质子共振信号49.母核上酚羟基甲基化或苷化后,将使相应的紫外吸收带50.7-OH成苷后,将使邻位H-6、H-8质子共振信号C型题[51-70](共10分,每题0.5分)[51-55]A.3-OH及5-OH B.邻二酚羟基C.二者均是D.二者均不是51.可在HCl酸性条件下与AlCl3试剂反应的黄酮类化合物52.可与AlCl3试剂反应的黄酮类化合物53.AlCl3+HCl紫外光谱与甲醇谱相同,示黄酮(醇)类化合物无54.AlCl3+HCl紫外光谱与AlCl3谱相同,示黄酮(醇)类化合物无55.AlCl3+HCl紫外光谱与AlCl3谱不同,示黄酮(醇)类化合物有[56-60]A. Ⅰ型强心苷B. Ⅱ型强心苷C. 二者均有D. 二者均无56.通过温和酸水解可以切断糖与苷元之间苷键的是57.通过强烈酸水解可以切断糖与苷元之间苷键的是58.与醋酐-浓硫酸试剂显色的是59.呫吨氢醇试剂显色的是60.与α-萘酚-浓硫酸作用界面出现紫色环的是[61-65]A. 还原性B. 旋光性C. 二者均是D. 二者均不是61.苷元62.原生苷63.糖64.苷的水解液65.次级苷[66-70]A. 青蒿素B. 穿心莲内酯C. 二者均有D. 二者均无66.具有内酯特性的化合物是67.属于倍半萜类化合物的是68.属于二萜类化合物的是69.与三氯化铁试剂反应的是70.属于三萜类化合物的是X型题[71-75](共10分,每题2分)71. 加入另一种溶剂改变溶液极性,使部分物质沉淀分离的方法有A.水提醇沉法B.醇提水沉法C.酸提碱沉法D.醇提醚沉法E.明胶沉淀法72. 羟基蒽醌UV光谱中有苯甲酰基结构引起的吸收谱带为A. 230nmB. 240~260nmC. 262~295nmD. 305~389nmE. 400nm以上73. 可以用于Ⅰ-型强心苷中α-去氧糖检测的试剂是A. 对二甲胺基苯甲醛B. 亚硝酰氰化钠C. 三氯化铁-冰醋酸D. 冰醋酸-乙酰氯E. 苦味酸钠74. 皂苷在那些溶剂中溶解度较大A. 热水B. 含水稀醇C. 热乙醇D. 乙醚E. 苯75. 生物碱分子结构与其碱性强弱的关系正确的是:A. 氮原子价电子的P电子成分比例越大,碱性越强B. 氮原子附近有吸电子基团则使碱性增强C. 氮原子处于酰胺状态则碱性极弱D. 生物碱的立体结构有利于氮原子接受质子,则其碱性增强E. 氮原子附近取代基团不利于其共轭酸中的质子形成氢键缔合,则碱性强三、填空题[1-5](共10分,每题2分)1. 天然药物化学成分的主要分离方法有:、、、、、及等。
天然药化名词解释

6.苷类;亦称苷或配糖体,是由糖或糖的衍生物与苷元脱水形成的一类化合物。
7.苷键;糖与糖及糖的衍生物形成的化学键。
8.单糖;多羟基醛或多羟基酮类化合物。
9.端基碳;单糖成环后形成的一个新的手性碳原子(不对称碳原子)成为端基碳,生成的一对异构体称为端基差向异构体。
28.诱导剂;因其诱导的化合物。 29,黄酮类化合物:泛指两个具有酚羟基的苯环(A-与B-环)通过中央三碳原子相互连结而成的一系列化合物。
29.萜类化合物;从化学结构来看,它是异戊二烯的聚合体及其衍生物,其骨架一般以五个碳为基本单位,少数也有例外。
42.乙型强心苷元;位侧链为不饱和内脂,为六元环的αβ-γ内脂,-δ-内脂,称为乙型强心苷元。
43.甾体皂苷;是一类有螺甾烷类化合物与糖结合的寡糖苷。
44.呋甾烷醇皂苷;由F环裂环而衍生的皂苷称为呋甾烷醇皂苷。
45.强心苷;是存在植物中具有强心作用的甾体苷类化合物。
46.生物碱;是含负氧化态的氮原子、存在于生物有机体中的环状化合物。
30.萸类化合物;凡由五元环与七元环骈合而成的芳环骨架都称为萸类化合物。
31.二倍半萜Байду номын сангаас化合物;是由5个异戊二烯单位构成,含25个碳原子的化合物类群。
32.吉拉德试剂;是一类带有季氨基团的酰肼,常用的是GirardT和GirarrdP。
33.挥发油;又称精油,是一类具有芳香气味的油状液体的总称。
38.次皂苷;当原生苷由于水解或酶解,部分糖被降解时,所生成的苷叫次皂苷。
39.溶血指数;是指在一定条件下能使血液中红细胞完全溶解的最低浓度。
天然药化名词解释

HR-MS:高分辨率质谱,能测量Li到U等60多种元素;及部分同位素。
苷化位移糖与苷元成苷后,苷元的α-C、β-C和糖的端基碳的化学位移值均发生了改变,这种改变称为苷化位移二次代谢产物由植物体产生的、对维持植物生命活动来说不起重要作用的化合物,如萜类、生物碱类化合物等。
分子旋光法(Klynemethods或Klyne法):测定甙键构型,α或β- 甙,将甙和甙元的分子旋光差与组成该甙的糖的一对甲甙的分子旋光度进行比较,数值上相接近的便是与之有相同甙键的甙。
挥发油又称精油,是存在于植物中的一类具有芳香气味、可随水蒸气蒸馏出来而又与水不相混溶的挥发性油状成分的总称生源异戊二烯法则认为IPP及DMAPP是萜类在生物体内形成的活性前体,其真正的基本单元是甲戊二羟酸经验异戊二烯法则认为萜类碳架是由异戊二烯单位以头-尾或非头-尾顺序相连而成,都是异戊二烯的聚合体或其衍生物硝酸银络合色谱根据挥发油分子中双键的数目和位置不同,与硝酸银形成π络合物难易程度和稳定性不同而得到分离。
络合的稳定性规律:末端双键>顺式双键>反式双键(洗脱的先后顺序:反式双键>顺式双键>末端双键)正相色谱以极性物质做固定相,非极性物质作流动相,即流动相的极性<固定相的极性反相色谱如果采用相对非极性固定相和极性流动相,则称为反相苷一种豆科甘草属多年生草本植物苷元糖苷类化合物中,与糖缩合的非糖部分。
苷键是苷类分子特有的化学键,具有缩醛性质,易被化学或生物方法裂解。
原生苷指原存在于植物体内的苷.次生苷指原生苷水解后生成的苷.低聚糖是由2-10个单糖形成的低度聚合糖多聚糖由许多单糖分子或其衍生物缩合而成的高聚物称为多糖,又称为高聚糖HPLC:高效液相色谱是色谱法的一个重要分支,以液体为流动相,采用高压输液系统,将具有不同极性的单一溶剂或不同比例的混合溶剂、缓冲液等流动相泵入装有固定相的色谱柱,在柱内各成分被分离后,进入检测器进行检测,从而实现对试样的分析。
天然药化

1.有效成分:指天然药物中,具有一定的生物活性、能代表天然药物临床疗效的单一化合物。
2.pH梯度萃取法:指根据所分离成分的酸碱性的差别,而用不同的碱或者酸性溶剂进行萃取分离的过程。
3.萜的定义:是一类由甲戊二羟酸衍生的、具有(C5H8)n通式的碳氧化合物及其含氧的饱和程度不等的衍生物。
4.挥发油:常温下可挥发,又称精油,是一类可随水蒸汽蒸馏、具有芳香气味的油状液体的总称。
5.强心苷:是存在于植物中具有强心作用的甾体苷类化合物。
6.生物碱:分子中含有负氧化态氮原子且氮原子多处于杂环上可与酸成盐具有较强生理活性的一类化合物。
7.香豆素:指邻羟基桂皮酸内酯类成分的总称。
8.溶血指数:指在一定条件下能使血液中红细胞完全溶解的最低浓度。
9.有效部位与有效成分之间的区别:有效部位是一类或几类成分的混合体,而有效成分是单一化合物。
10.醋酸-丙二酸途径(AA-MA途径):合成脂肪酸类、酚类、蒽醌类11.莽草酸途径:香豆素、苯丙素、木脂素、黄酮12.甲戊二羟酸途径(MV A途径)和脱氧木酮糖磷酸酯途径(DXP途径):主要生成萜类、甾体类化合物13.氨基酸途径(Amino Acid Pathway):合成生物碱,氨基酸脱酸成胺类,再经过一系列化学反应转化成生物碱。
14.复合途径:(1)醋酸-丙二酸-莽草酸途径(2) 醋酸-丙二酸-甲戊二羟酸途径(3) 氨基酸-甲戊二羟酸途径(4) 氨基酸-醋酸-丙二酸途径(5) 氨基酸--莽草酸途径15.连续回流提取法(Continuous Refluxing):优点:最节省溶剂、效率高。
缺点:对热不稳定成分不宜用,时间长。
16.纸色谱(PC)也叫纸分配色谱(PPC)原理:分配色谱支持剂:纤维素(纸)固定相:水(纸纤维吸附)流动相:水饱和的有机溶剂,如:水饱和正丁醇、n-BuOH-HOAc-H2O(4:1:5上层,BAW)、n-BuOH-HOAc-H2O(3:1:1上层, TBA)Rf值:化合物极性越小,Rf值越大;反之,化合物极性越大,Rf值越小。
天然药物化学(ppt)

二、分离纯化
(一)溶剂法
酸碱法:是将总提取物溶于有机溶剂,用酸水、碱水 分别萃取,难溶于水的有机碱性成分可与酸成盐溶于水, 从而达到分离纯化的目的。 溶剂分配法:利用混合物中各组分在两相溶剂中分配 系数差进行分离纯化的方法。
(二)沉淀法
基于有些天然药物化学成分能与某些试剂生成沉 淀;或降低某些成分在溶液中的溶解度而自溶液中析出 的一种分离方法。
多孔凝胶过滤色谱
第五节 天然药物化学成分结构鉴定方法
结构鉴定的程序一般是: (1)确定纯度 (2)测定物理常数 (3)确定分子量、分子式 (4)波谱分析 (5)确定结构式
确定化合物结构常用几种光谱分析技术: ① 紫外光谱 ② 红外光谱 ③ 磁共振 ④ 质谱
紫外光谱
测定范围:通常在200~600nm的紫外可见光区 原理:基于分子中的电子可因光照射由基态跃迁到激
第四节 天然药物化学成分的提取分离方法
一、天然药物化学成分的提取
(一)溶剂提取法 1、溶剂
原理:相似者相溶,根据欲提取成分的性质确定,充分地提取 所需成分、沸点适中、易回收、安全低毒。 常用溶剂:以溶剂极性弱到强的顺序排列为: 石油醚<四氯化碳<苯< 二氯甲烷<氯仿<氯仿<乙醚<乙酸 乙酯<正丁醇<丙酮<乙醇<甲醇<水
天然药物化学(ppt)
优选天然药物化学
第一节 天然药物化学的性质与任务
一、天然药物化学的性质
1、概念:“天然药物化学”是应用现代科学理论 与方法研究天然药物中的化学成分的学科. 2、性质:“天然药物化学”是从分子水平研究天 然药物的药效物质基础及其防治疾病规律的一门综 合性学科。
“天然药物化学”是药学二级学科“药物化学”下设置的三级学 科. “天然药物化学”是药学类专业规定设置的一门主要专业课程.
天然药化

超临界流体萃取技术
在超临界状态下,将超临界流体与待分离的物质接触,使 其有选择性地把极性大小、沸点高低和分子量大小的成分 依次萃取出来。当然,对应各压力范围所得到的萃取物不 可能是单一的,但可以控制条件得到最佳比例的混合成分, 然后借助减压、升温的方法使超临界流体变成普通气体, 被萃取物质则完全或基本析出,从而达到分离提纯的目的, 所以超临界流体萃取过程是由萃取和分离组合而成的。 ----快速、高效、简便、无污染;萃取温度低、溶解性质可 控、可联用;对水溶性物质的溶解能力差;适用于生物碱、 挥发油、有机酸、萜类的提取。 •
2 ) 具有一定的理化常数
3 ) 具有生理活性
小蘗碱(Berberine)
2. 有效部位(Active Extracts)
指具有生物活性的有效部位,如:总生物碱、总皂苷或总黄酮等。
3. 无效成分(Anactive Constituents )
与有效成分共存的其它成分
4. 杂
质
中药麻黄: 有效成分-左旋麻黄素 有效部位-总生物碱 无效成份-挥发油 杂质-淀粉、树脂、叶绿素
(三)
其他提取方法
水蒸气蒸馏法 混合物的沸点比任意组分的低;适用于具有挥发性的、 能随水蒸气蒸馏而不被破坏,且难溶于水的成分 升华法 固体物质在受热后不经过熔融直接转化为蒸气,蒸气 遇冷又凝结成固体的现象。如樟木中的樟脑、茶叶中的咖 啡因等。 超临界流体萃取技术(SFE) 物质处于其临界温度(Tc)和临界压力(Pc)以上状 态时,成为单一相态,此相态称为超临界流体 (Supercritical fluid, SF)。 利用处于状态的流体具有特异增加的溶解能力而发展 出来的化工分离新技术
溶剂提取法
4. 选择溶剂注意点
1) 对有效成分溶解度大,对杂质溶解度小 2) 不与化学成分起化学变化 3) 经济、易得、使用安全
天然药化结构式.doc
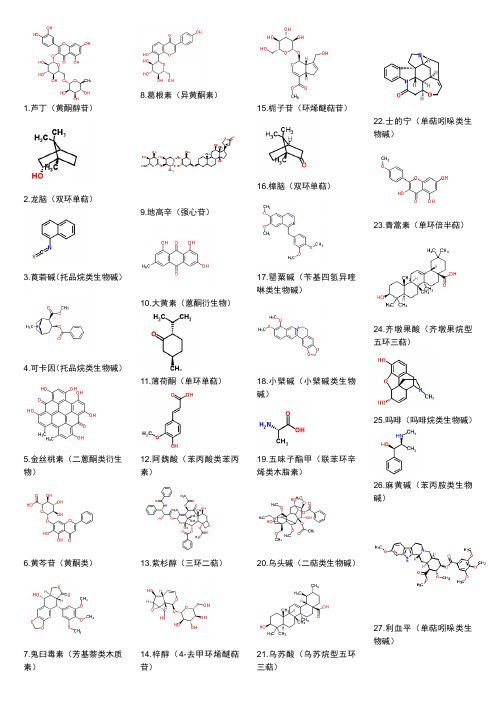
1.芦丁(黄酮醇苷)
2.龙脑(双环单萜)
3.莨菪碱(托品烷类生物碱)
4.可卡因(托品烷类生物碱)
5.金丝桃素(二蒽酮类衍生物)
6.黄芩苷(黄酮类)
7.鬼臼毒素(芳基萘类木质素)
8.葛根素(异黄酮素)
9.地高辛(强心苷)
10.大黄素(蒽酮衍生物)
11.薄荷酮(单环单萜)
12.阿魏酸(苯丙酸类苯丙
素)
13.紫杉醇(三环二萜)
14.梓醇(4-去甲环烯醚萜
苷)
15.栀子苷(环烯醚萜苷)
16.樟脑(双环单萜)
17.罂粟碱(苄基四氢异喹
啉类生物碱)
18.小檗碱(小檗碱类生物
碱)
19.五味子酯甲(联苯环辛
烯类木脂素)
20.乌头碱(二萜类生物碱)
21.乌苏酸(乌苏烷型五环
三萜)
22.士的宁(单萜吲哚类生
物碱)
23.青蒿素(单环倍半萜)
24.齐墩果酸(齐墩果烷型
五环三萜)
25.吗啡(吗啡烷类生物碱)
26.麻黄碱(苯丙胺类生物
碱)
27.利血平(单萜吲哚类生
物碱)。
天然药化

1、常用提取用溶剂亲脂性由强到弱的顺序是:石油醚>苯>氯仿>乙醚>乙酸乙酯>丙酮>乙醇>甲醇>水。
亲水性强,则极性强2、在硅胶吸附薄层色谱上,用石油醚-甲酸乙酯-甲酸(15:5:1)为展开剂,Rf值大小顺序:大黄酚>大黄素甲醚>大黄素>芦荟大黄素>大黄酸。
3、开链萜烃具有(C5H8)n通式。
4、色谱法按分离原理可分为:吸附色谱和分配色谱。
5、羟基蒽醌类化合物的酸性强弱与结构中酚羟基的数目和结合位置有关。
6、皂苷水溶液的发泡性与PH有关,可利用此性质区别三萜皂苷和甾体皂苷。
7、苷和糖的混合物通过活性炭吸附柱,先用烯醇洗去糖类,再用浓醇洗脱苷类。
8、聚酰胺吸附色谱分离化合物时,影响分离结果的主要基团是:酚羟基,羰基,芳香共轭双键。
9、生物碱沉淀反应一般应再酸性环境中进行,常用生物碱沉淀试剂有:碘化物复盐,重金属盐,大分子酸类。
10、溶剂提取中药成分,常用方法有:浸渍法,渗滤法,煎煮法,回流提取法,连续提取法。
11、苷是由糖与非糖两部分组成的化合物。
12、硅胶G吸附薄层色谱分离化合物时,展开剂为氯仿-醋酸乙酯-浓氨试液(8:2:0.2),其Rf值大小为:苦参碱>氧化苦参碱>大黄素。
13、植物中生物总碱常用的提取方法为:水或酸水提取法,醇提取法,亲脂性有机溶剂提取法。
14、黄酮类化合物多呈酸性,是由于其多数带有酚羟基;黄酮类成分也具有较弱的碱性,是由于其结构中Υ-吡喃酮环上的-1位氧原子的存在。
15、用氯仿提取生物碱时,若先用碱水润湿药材,则能提得碱性较强的生物碱;若先用水润湿药材,则能提得弱碱性生物碱。
16、区别5-羟基黄酮和7-羟基黄酮的反应是:Gibb’s反应。
17、极性大的化合物Rf值小,因为极性强,吸附力大,极性较强的物质,在水中的溶解度大,其Rf值就小。
相反,极性较弱的物质,在有机溶剂中的溶解度较大,其Rf值就大些。
天然药化——精选推荐

第一章总论1.天然药化是运用现代科学理论与方法研究天然药物中化学成分的一门学科。
其研究内容包括各类天然药物的化学成分(主要是生理活性成分或药效成分)的结构特点、物理化学性质、提取分离方法、主要类型化学成分的结构鉴定以及主要类型化学成分的生物合成途径等。
2. 二次代谢:以一次代谢产物作为原料或前体,又进一步经历不同的代谢过程,并非在所有植物中都能发生,对维持植物生命活动又不起重要作用;称之为二次代谢过程。
产物:生物碱、萜类等3.主要生物合成途径:醋酸-丙二酸途径(AA-MA):脂肪酸类、酚类、蒽酮类;甲戊二羟酸途径(MVA):萜类、甾体类;桂皮酸途径及莽草酸途径:骨架的苯丙素类、香豆素类、木质素类、木脂体类C6-C3-C6骨架的黄酮类化合物氨基酸途径:生物碱类。
可作为生物碱前体的氨基酸:脂肪族有鸟氨酸、赖氨酸芳香族有苯丙氨酸、酪氨酸及色氨酸复合途径。
4.中草药有效成分的提取方法及其使用范围和优缺点1)溶液提取法2)水蒸气蒸馏法:适用于具有挥发性的、能随水蒸汽蒸馏而不被破坏、且难溶或不溶于水的成分的提取3)升华法:适用具有升华性质的成分5.化合物分子的极性越大,表现亲水性越强,亲脂性就越弱常见溶剂的极性强弱顺序:环己烷<石油醚<苯二氯甲烷<氯仿<乙醚<乙酸乙酯<正丁醇<丙酮<乙醇<甲醇<水1)比水重的有机溶剂:氯仿、二氯甲烷2)能与水分层的有机溶剂:环己烷~正丁醇;能与水分层的极性最大的有机溶剂:正丁醇3)与水可以以任意比例混溶的有机溶剂:丙酮~乙醇4)常用来从水中萃取苷类,水溶性生物碱类的有机溶剂是正丁醇6.改变极性分离1)在药材浓缩水提取液中加入数倍量高浓度乙醇,以沉淀除去多糖、蛋白质等水溶性杂质(水/醇法)2)在浓缩乙醇提取液中加入数倍量水稀释,放置以沉淀除去树脂、叶绿素等水不溶性杂质(醇/水法)3)在乙醇浓缩液中加入数倍量乙醚(醇/醚)或丙酮(醇/丙酮法),可使皂苷沉淀析出改变PH分离 1)提取黄酮、蒽醌类酚酸性成分采用碱提酸沉法(碱/酸)2)提取生物碱类用酸提碱沉法(酸/碱)7.根据物质在两相溶剂中的分离比不同进行分离(1).液-液萃取法适用β>=100,过程运用课本23页pH<3时,酸性物质多呈非离解状态、碱性物质则呈离解状态存在;pH>12,则酸性物质多呈离解状态、碱性物质则呈非离解状态存在。
天然药化-绪论

三 常用 的提 取分 离方
法
有效成分
碱性化合物:生物碱 酸性化合物:黄酮、醌类、苯丙素、
有机酸、葡萄糖醛酸 两性化合物:氨基酸、蛋白质、结
构中既有碱性基团也有酸性基团 中性化合物:分子结构中既无碱性
基团也无酸性基团的化合物,如帖 类和挥发油、甾体等
三 常用 的提 取分 离方
无效成分
相似相溶原则
(一)
有效 成分 的提
萜类、甾体等脂环类及芳香类化合物极性较 小,易溶于氯仿、乙醚等脂溶性溶剂中;
糖苷、氨基酸、短肽等成分极性较大,易溶 于水及含水醇中;
酸性、碱性及两性化合物,存在状态随溶液 pH不同而不同,故溶解度随溶液pH而改变。
取
(一)
有效 成分 的提
取
2、水蒸气蒸馏法
(二)
有效 成分 的分 离与 精制
酸碱溶剂法
(二)
有效 成分 的分 离与 精制
2. 根据物质在两相溶剂中的配比不同 进行分离
常用的有液-液萃取法、液滴逆流色 谱 法 (DCCC) 、 高 速 逆 流 色 谱 法 (HSCCC) 、 气液分配色谱法(GC)及液-液分配色谱法 (LC)等。
主要是利用不同的成分在两相溶剂中 溶解度的不同进行分离。
有效成分,右旋麻黄素具有消炎作用。
概
HO
CH3
述
HH
NHCH3
l-麻黄素
例如:
中药甘草(Glycyrrhiza uralensis的根及
一
根茎)含有多种皂苷类、黄酮类、淀粉等
成分,其中甘草酸具有抗炎、抗过敏、治
疗胃溃疡作用,是甘草的主要活性成分。
概
述
COOH
O H
天然药物化学就业

天然药物化学就业
天然药物化学专业毕业生可以有多种就业选择。
以下是一些常见的就业岗位:
1. 药物研发公司:在制药公司的研发部门工作,负责天然药物的研发和筛选,参与新药开发项目。
2. 科研机构:在大学、医院或独立的药物化学研究机构从事天然药物化学研究,如天然产物提取、分离纯化、结构鉴定等科研工作。
3. 化学分析实验室:在化工企业或其他实验室从事天然药物化学分析工作,负责分析天然药物的组成、含量、纯度等。
4. 药物监管机构:在药品监督管理部门从事天然药物的审核、注册、监管等工作,确保药物的质量和安全性。
5. 药品销售与市场推广:在药品销售公司、药品代理商等企业从事天然药物产品的销售与市场推广工作。
6. 教育与科普机构:在高校从事天然药物化学专业的教师工作,或者在相关机构从事天然药物化学的科普宣传工作。
此外,天然药物化学专业的毕业生还可以选择进一步深造,攻读硕士或博士学位,从事科研工作或教育工作,并有机会在相关领域内取得更高的职位和待遇。
天然药物化学

天然药物化学在当今世界,药物学领域一直是备受关注的研究领域之一,其中天然药物化学更是备受推崇。
天然药物化学是指从天然来源(如植物、微生物、动物等)中提取出的具有药用价值的化学物质,如生物碱、黄酮类化合物、多糖等。
这些天然药物化合物具有丰富的化学结构和药理活性,常被用于治疗各种疾病。
天然药物的来源天然药物来自于大自然,其来源种类繁多。
植物中含有大量的生物活性成分,如植物类生物碱、黄酮类化合物、甾体类化合物等,常被用于中药的配方中。
微生物也是天然药物的重要来源,如青霉素、链霉素等抗生素就是来自于微生物的产物。
此外,动物也可以产生一些具有药用价值的分子,比如蛇毒、蜂毒等。
天然药物化学的研究方法天然药物化学的研究方法主要包括分离提取、结构鉴定、生物活性评价等。
首先,研究人员会通过不同的分离技术(如柱层析、液-液萃取等)从天然来源中提取出目标化合物。
然后,利用质谱、核磁共振等技术对化合物的结构进行鉴定,确定其分子式、分子量、结构等信息。
最后,通过生物学实验评价化合物的药理活性,如抗菌活性、抗癌活性等。
天然药物的应用与展望天然药物在治疗疾病中发挥着重要作用,尤其是在抗癌、抗感染等领域。
许多天然药物化合物被广泛用于临床治疗,如阿司匹林、紫杉醇等。
未来,天然药物化学仍将是一个重要的研究领域,研究人员将致力于发现新的天然药物,挖掘其潜在的药理活性,为人类健康做出更大的贡献。
通过对天然药物化学的研究,可以更好地理解天然药物在治疗疾病中的机制,为新药研发提供更多的启示。
天然药物化学的发展必将推动药物领域的进步,为保障人类健康作出更多的贡献。
天然药物化学
蓝色国土
二、研究内容
天然药化是运用现代科学的理论与 方法研究天然物中有效成分的结构特 点。理化性质,提取分离方法,结构 鉴定及生物合成途径等内容的一门实 践科学。
内容
说明: 1、区别与中药的传统加工方法。
2、指出这门学科的学习重点。 3、这一学科的特点,实践性强。 毒草
何谓: 有效成分:有生理活性、有药效,能 治 病的成分叫有效成分。
无效成分:无生理活性、无药学,不 能治病
的成分叫无效成分。 有毒成分:能导致疾病的成分叫有毒 成分。
三、研究目的: 1、探讨天然药物防病治病的原理,推 动中 西医结合。 这方面的成就很多如: (1)中药元胡中的13种生物碱为我国 首次 发现并鉴定结构的。说明了我们的 能力 与水平。 (提高方面)
(2)民间草药鹤草芽驱蛔,其成分 鹤草酚;
也是我国发现,现已合成成功。 ( 发掘方面)
发掘
2、从天然药物中研制开发新药。
这是我们学习天然药物化学的主要目的。
有人预测,未来的天然药物将与化学药物
平分秋色。与生物药一起成三足鼎立之势。
新药
3、开辟新的药源
(1)西药药源的扩大 在天然药物的研究中发现了各种生理活性 的成分, 如:抗菌消炎药,西药有抗菌素,现在发现 天然药物中有很多成分有抗菌消炎的作用。
梦想 热情
精彩人生
出口一斤参豆子价格一定比土 豆高,效益巨增,你们说生活 能不好吗?生活的质量能不提 高吗?请在网上告诉我你的梦 想。天然药化有能力在过去 发掘二棵“摇钱树”,还将继 续 发掘更多的“摇钱树”和其它。
摇钱树பைடு நூலகம்
太空种子长出的植物会有什 么成分和作用。太空上有什 么天然物?随着科学的发展, 相信这个学科将会迎来更加 兴旺、蓬勃发展的新时代, 也将永远兴盛不衰。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
Gibbs试剂
Emerson试剂
出蓝色
香豆素溶液呈现
红色
醌类化合物
Feigl反应—醌的通性 在碱性条件下,经加热可与醛类及邻二硝基苯反 应生成紫色络合物。
无色亚甲蓝显色
碱性条件下呈色
苯醌和萘醌因醌核上有活泼质子可反应在白色背景
(纸)上蓝色斑点。而蒽醌无 可区别含羟基的蒽醌与蒽酚衍生物。羟基醌类在 碱性条件下会出现一些颜色,如橙 红 紫红等
当B环上有羟基或甲氧基颜色加深
对二氢黄酮类化合物专 在试管中加入适量含有式样的乙醇液再加 属性较高 适量四氢硼纳的甲醇液一分钟后加浓盐酸, 生成紫色至紫红色
铅盐
镁盐 锆盐 氯化锶
黄酮类化合物的鉴定和 提纯
乙酸铅只能与具有邻二酚羟基或兼有3-OH, 4—酮基或5—OH,4-酮基产生黄色沉淀,碱式 乙酸铅可沉淀酚类化合物故可用于提取
• 定义
存在于植物中具有强心作用的甾体苷类化合物
• 功能
治疗充血性心力衰竭及节律障碍等心脏疾病
• 存在部位
存在于许多有毒植物中。在动物中至今未发现强心 苷的存在。
结构: 强心苷元
C-3和C-14取代 基 C-3:羟基大多是β 构型 C-14:羟基都是β 构型 C-10上的取代 基
甲基:β构型 醛基,羟甲基,羧 基:β构型
酶催化水解
• 用酶水解苷键可以保持苷元的结构不变,还可以保留部分 苷键得到次级苷或低聚糖。 • 转化糖酶只水解β-果糖苷键 • 麦芽糖酶只水解α-D-葡萄糖苷键 • 纤维素酶只水解β-D-葡萄糖苷键 • 杏仁苷酶只水解β-六碳醛糖苷键 • 蜗牛酶只水解β–苷键
显色反应
• 不饱和内酯环产生的反应 甲型强心苷C-17侧链有个不饱和五 元环,在碱性溶液里,双键转位形 成活性次甲基。从而能与某些试剂 发生显色反应。 • Legal反应 亚硝酰铁氰化钠 深 红或蓝 • Baljet反应 苦味酸 橙或橙红 • 2-去氧糖产生的反应 Keller-Kiliani反应 : 强心苷溶于少 量三价铁离子的冰乙酸,沿壁滴加 浓硫酸,乙酸层渐呈现蓝色或蓝绿 色,则表示有2-去氧糖存在。
糖和苷
Molisch反应 鉴定单糖
试剂 显色剂 现象
浓硫酸 α-萘酚
邻苯二甲酸 苯胺
糖类在浓硫酸作用下形成糠醛及其衍 生物可与α-萘酚形成紫色环。
香豆素类(苯骈α-吡喃酮)
异羟肟酸铁反应—内酯环反应
与酚类试剂反应
酚羟基对位或者6号 位无取代基 香豆素乙醇溶液在 碱性条件下,呈现
碱性条件下,香豆素内酯开 环,并与盐酸羟胺缩合成异 羟肟酸,再在酸性条件下与 三价铁离子络合成盐而显红 色。
(Brontrager)
与活性次甲基试剂反应
区别蒽醌与苯醌萘醌。苯醌及蒽醌化合物当环上有未
被取代时,在碱性条件下可与含有活性次甲基的醇溶液 发生蓝绿色或蓝紫色反应
与金属离子反应
初步鉴定蒽醌的取代情况
黄酮类化合物
盐酸—镁粉 四氢硼纳
鉴定黄酮类最常用的的 将试样溶于甲醇中,加入适量镁粉振摇,滴加 几滴浓盐酸,即可显色。多说呈现红色至紫色。 颜色反应
挥发油(官能团鉴定)
酚类 不饱和化合物 和薁类衍生物
将挥发油溶于乙醇中,加 入三氯化铁产生颜色反应 蓝色,蓝紫色或绿色
在挥发油的三氯甲烷溶 红色褪去→含有不饱和 液中滴加溴的三氯甲烷 化合物 溶液 继续滴加溴的三氯甲烷 蓝色,紫色或绿色→含 溶液 有薁类化合物 挥发油的无水甲醇溶液 蓝色或紫色→有薁类衍 加浓硫酸 生物
+
同时接有脱氧糖 和葡萄糖
糖
脱氧糖直接与苷 元相连,而后再 接葡萄糖。
仅接葡萄糖和仅接脱氧糖。
C-13上的取代 基
都是甲基
六碳醛糖 6-去氧糖 6-去氧糖甲醚 五碳 醛糖
仅存在强心苷和 2,6-二去氧糖
C-17侧链不饱 五元环:甲型 和内脂(β构型)
C21甾苷中
六元环:乙型
2,6-二去氧糖 加醚
• 五元内酯环
乙酰解
• 反应用的试剂:为乙酸酐与不同酸的混合液。 • 反应机理:与酸催化水解相似,它是以CH3CO+为 进攻基团。而不是质子。 • 规律:苷发生乙酰解的速度与糖苷键的位置有关。 从二糖的乙酰解速率可以看出,苷键的乙酰解一 般以1-6苷键最易断裂,其次为1-4苷键,1-3 苷键 较难开裂,而以1-2苷键最难开裂。
3-OH位β构型强心作用大于α构型的异 构体 3-OH位构型对强心作用无明显作用。
A/B反式异构物
生物制药一班 李东保 整理编制
红色变紫色(加热 100℃) 甾体(加热60℃)
绿色 蓝色 灰蓝色
氯仿-浓硫酸反应 (Shlkowski) (适用于甾体类)
冰乙酸-乙酰氯反应
样品溶于三 氯甲烷,加 入浓硫酸后 呈现颜色反 应
氯仿层:红色 或蓝色
硫酸层:绿 色荧光
样品溶于冰 淡红色或紫 乙酸,加入 红色 乙酰氯及氯 化锌结晶数 粒,稍加热。
(纸上操作) (适用于甾体类)
将样品溶液滴在滤纸 红色渐变紫色(加热 上,喷三氯乙酸乙醇 100℃)甾体类 溶液
(60℃)
三氯乙酸乙醇溶液和 氯胺T水溶液按比例 混合喷在纸上与强心 苷反应
黄绿,蓝色,灰 蓝色
三萜类 三氯乙酸反应(Rosen-
Heimer)纸上操作 (适用于甾体类)
将样品溶液滴在 滤纸上,喷三氯 乙酸乙醇溶液 三氯乙酸乙醇溶 液和氯胺T水溶液 按比例混合喷在 纸上与强心苷反 应
强心苷苷键水解
酸催化水解 (不一定能 得到苷元)
(1)温和酸水解:用稀酸在含水醇中经短时间加热回流,可水解 去氧糖苷键,2-羟基糖的苷不断裂。 (2)剧烈酸水解:2-羟基糖的苷,由于2-位羟基存在。产生了互 变,水解困难。需要增加酸浓度,延长时间,加压。由于比较强 烈往往得到的是缩水苷元。 (3)盐酸丙酮水解:于丙酮溶液中,室温下与HCL长时间反应糖 分子中的2-OH 3-OH与丙酮反应进而水解,得到相应苷元。 强心苷的苷键为缩醛结构,不被碱水解。 酶的水解有一定的专一性。但是蜗牛酶是一种混合酶,几乎能水 解所有苷键,可将强心苷分子中的糖链逐步水解,只到得到苷元。 由于苷元类型不同,乙型强心苷较甲型强心苷更容易为酶水解。
羰基化合物 内酯类化合物
用硝酸银的氨溶液检查挥 发油 挥发油的乙醇溶液中加氨 基脲 2,4-二硝基苯肼 在挥发油的吡啶溶液中, 加入亚酰氰化钠及氢氧化 钠溶液
银镜反应→有醛类物质 结晶物生成→有醛或酮 红色逐渐消失→α,β不饱 和内酯类化合物
强心苷的生物活性
• • • • • C/D环为反式或14-OH脱水生成脱水苷元,强心作用消失。 C-17位为β构型{苦味}有活性α构型{甜味}没有活性 内酯环双键被饱和,强心作用减弱,毒性减弱。 C-10位甲基氧化成羟甲基或醛基,强心作用加强。 甲型强心苷元中 A/B顺式异构物
温故而知新可以为师矣
甾类及其苷类
第一节 概述
甾体化合物
第二节 强心苷
概述
定义 功能
存在部位
化学结构和实例
结构 五元内酯环强心苷类 六元内酯环强心苷类
强心苷理化性质
苷键水解 显色反应
强心苷的生物活性
甾体化合物结构中都具有环戊烷骈多氢菲的甾核。 根据甾核的C-17的侧链结构不同可将甾类成分分为 许多类型。本章主要介绍强心苷(C17侧链为不饱和内 酯环)。根据C-17上的内酯环不同又可分为甲型(五 元环)和乙型(六元环)
碱催化水解 酶催化水解
苷键的裂解解 • 酸催化水解 苷键原子质子化难易程度
按苷键原子的不同,酸水易难程度为:N-苷>O-苷>S-苷>C-苷。 当N处于酰胺或嘧啶位置时,N-苷难于用浓酸水解。 p-π共轭作用。芳香苷(如酚苷)因苷元部分有供电子结构,水解比脂肪苷(如萜 苷、甾苷等)容易得多。 2-去氧糖>2-羟基糖>2-氨基糖。由易到难 呋喃糖苷较吡喃糖苷易水解 酮糖较醛糖易水解 吡喃糖苷中,吡喃环C5上的取代基越大越难水解,故有:五碳糖>甲基五碳糖 >六碳糖>七碳糖>5位接-CO一滴实液,喷以乙酸镁的甲醇溶液, 在紫光下,二氢黄酮(醇)显天蓝色。黄酮 黄酮(醇)
(醇)显黄色(橙黄色)
鉴定黄酮类化合物中的 是否有3-OH 或者5-OH
3-OH或5-OH存在时,与二氧化锆甲醇溶 液生成黄色络合物。当加入枸橼酸5-OH 黄酮黄色褪色显著。
鉴定邻二酚羟基结构的 取适量试样,,加入甲醇使其溶解,再加入适 量氯化锶甲醇溶液再滴加几滴用氨蒸气饱和了 黄酮类 用于酚类显色剂
铜络合物:显示绿色结晶 铁络合物:赤红色结晶 Sabety 反应 取挥发油一滴溶 于1毫升三氯甲 烷中,加入5%溴 的三氯甲烷溶液 产生紫色或绿色
薁衍 生物
Ehrlich 与Ehrlich试剂反 试剂 应生成紫色或红 (对色。 二甲氨 基苯甲 醛 +浓 硫酸)
三萜类 醋酐—浓硫酸反 (Liebermann-Burchard)
• 洋地黄强心苷
• 洋地黄毒苷,亲脂性强,口服吸 收完全,可注射可口服,多用于 慢性病例。 羟基洋地黄毒苷,亲脂性低(C16引入羟基)难以吸收,乙酰化 后,脂溶性提高易于吸收,脱酰 基后,易于经肾排泄易于控制。 异羟基洋地黄毒苷,C-12引入羟 基,亲脂性降低,口服不易吸收, 制成注射液用于急性病例。 去乙酰毛花洋地黄苷,亲水性强, 适于注射,毒性小为速效强心苷。 G-毒毛花苷,又称乌本苷(乌本 苷元+L-鼠李糖苷),为速效强心 苷,并作为测定强心苷生物效价 的标准品。
(适用于甾体类)
将样品溶于醋酐中, 黄→ 加浓硫酸-酸酐(1: 20),产生颜色反应。
红 →紫 → 蓝
甾体皂苷也有该反应,污绿色 但颜色变化快。 将三氯甲烷滴于滤纸 上,喷五氯化锑的三 氯甲烷溶液
五氯化锑反应 (纸上操作) (适用于甾体类)
