高中化学第一章1.3化学反应热的计算练习新人教版选修13
高中化学选择性必修1 第一章 化学反应的热效应 第二节 反应热的计算同步练习含详解答案

全面解读盖斯定律及其应用同步练习(答题时间:40分钟)一、选择题1. 下列叙述不正确的是()A. 化学反应的反应热不仅与反应体系的始态和终态有关,也与反应的途径有关B. 盖斯定律遵循能量守恒定律C. 利用盖斯定律可间接计算难以通过实验测定的反应的反应热D. 利用盖斯定律可以计算有副反应发生的反应的反应热2. 盖斯定律指出:化学反应的反应热只与反应的始态(各反应物)和终态(各生成物)有关,而与反应进行的具体途径无关。
物质A在一定条件下可发生一系列转化,由如图判断下列关系错误的是()A. A→F,ΔH=-ΔH6B. ΔH1+ΔH2+ΔH3+ΔH4+ΔH5+ΔH6=1C. C→F,|ΔH|=|ΔH1+ΔH2+ΔH6|D. ΔH1+ΔH2+ΔH3=-ΔH4-ΔH5-ΔH63. 已知N2和H2合成氨的反应是放热反应,破坏1mol N≡N键消耗的能量为Q1kJ,破坏1mol H-H键消耗的能量为Q2kJ,形成1mol N-H键放出的能量为Q3kJ,下列关系式中正确的是()A. Q1+3Q2>6Q3B. Q1+3Q2<6Q3C. Q1+Q2<Q3D. Q1+Q2=Q34. 发射火箭时使用的燃料可以是液氢和液氧,已知下列热化学方程式:①H2(g)+12O2(g)=H2O(l)ΔH1=-285.8kJ·mol-1②H2(g)=H2(l)ΔH2=-0.92kJ·mol-1③O2(g)=O2(l)ΔH3=-6.84kJ·mol-1④H2O(l)=H2O(g)ΔH4=+44.0kJ·mol-1则反应H2(l)+12O2(l)=H2O(g)的反应热ΔH为()A. +237.46kJ·mol-1B. -474.92kJ·mol-1C. -118.73kJ·mol-1D. -237.46kJ·mol-1*5. 已知:①2C(s)+O2(g)=2CO(g)ΔH=-221.0kJ·mol-1;②2H2(g)+O2(g)=2H2O(g)ΔH=-483.6kJ·mol-1。
高中化学《反应热的计算》练习题(附答案解析)

高中化学《反应热的计算》练习题(附答案解析)学校:___________姓名:___________班级:_____________一、单选题1.已知:①2CO(g)+O2(g)=2CO2(g) ΔH=-566 kJ/mol;②Na2O2(s)+CO2(g)=Na2CO3(s)+1/2O2(g) ΔH=-226 kJ/mol根据以上热化学方程式判断,下列说法正确的是()A.CO的燃烧热为 283 kJB.反应①正反应活化能与逆反应活化能之差为+566 kJ/molC.反应 2Na2O2(s)+2CO2(s)=2Na2CO3(s)+O2(g) ΔH>-452 kJ/molD.CO(g)与 Na2O2(s)反应放出 509 kJ 热量时,电子转移数为 6.02×10232.已知反应:①101kPa时,2C(s)+O2(g)=2CO(g);△H=-221 kJ/mol②稀溶液中,H+(aq)+OH-(aq)=H2O(1);△H=-57.3 kJ/mol③红磷的化学式为P,白磷的化学式为P4,已知P4(s)+5O2(g)="P4O10(s)" △H=-3093.2 kJ/mol4P (s)+5O2(g)="P4O10(s)" △H=-2954.0 kJ/mol下列结论正确的是()A.由于红磷转化为白磷是放热反应,等质量的红磷能量比白磷低B.稀硫酸与稀NaOH溶液反应的中和热△H=57.3 kJ/molC.碳的燃烧热大于-110.5 kJ/molD.稀醋酸与稀NaOH溶液反应生成1 mol水,△H 大于-57.3 kJ/mol3.1mol氨气(化学式为:NH3)分解成氮气和氢气要吸收46.19kJ的热量,下列热化学方程式中正确的是()A.2NH3=N2+3H2-46.19kJB.2NH3(g)=N2(g)+3H2(g)-46.19kJC.NH3(g)=1/2N2(g)+3/2H2(g)-46.19kJD.2NH3(g)=N2(g)+3H2(g)+92.38kJ4.氢气和氟气反应生成氟化氢的过程中能量变化如图所示。
人教版高中化学选修4练习:第一章第三节化学反应热的计算 word版含答案

第一章 化学反应与能量第三节 化学反应热的计算1.在298 K 时下述反应的有关数据:C(s)+12O 2(g)===CO(g) ΔH 1=-110.5 kJ·mol -1 C(s)+O 2(g)===CO 2(g) ΔH 2=-393.5 kJ·mol -1则C(s)+CO 2(g)===2CO(g)的ΔH 为( )A .+283.5 kJ·mol -1B .+172.5 kJ·mol -1C .-172.5 kJ·mol -1D .-504 kJ·mol -1解析:由已知热化学方程式可得:2C(s)+O 2(g)===2CO(g)ΔH =2ΔH 1=-221 kJ·mol -1①CO 2(g)===C(s)+O 2(g) ΔH -ΔH 2=+393.5 kJ·mol -1②依据盖斯定律,反应①+②可得:C(s)+CO 2(g)===2CO(g)ΔH =-221 kJ·mol -1+393.5 kJ·mol -1=+172.5 kJ·mol -1。
答案:B2.根据盖斯定律判断如下图所示的物质转变过程中,正确的等式是( )A .ΔH 1=ΔH 2=ΔH 3=ΔH 4B .ΔH 1+ΔH 2=ΔH 3+ΔH 4C .ΔH 1+ΔH 2+ΔH 3=ΔH 4D .ΔH 1=ΔH 2+ΔH 3+ΔH 4解析:由盖斯定律知:ΔH 1=ΔH 2+ΔH 3+ΔH 4,D 项正确。
答案:D3.已知丙烷的燃烧热ΔH =-2 215 kJ·mol -1,若一定量的丙烷完全燃烧后生成1.8 g 水,则放出的热量约为( )A .55 kJB .220 kJC .550 kJD .1 108 kJ解析:丙烷分子式是C 3H 8,1 mol 丙烷完全燃烧会产生4 mol水,则丙烷完全燃烧产生1.8 g 水,反应放出的热量为 1.818×4×2 215 kJ =55.375 kJ 。
人教版高中化学选择性必修1第一章化学反应的热效应第二节反应热的计算第2课时反应热的计算练习含答案

第一章化学反应的热效应第二节反应热的计算第2课时反应热的计算基础过关练题组一反应热的相关计算1.(2024河南中原名校联考)工业上PCl3可通过下列反应制取:P4(g)+6Cl2(g) 4PCl3(g)(已知P4为正四面体结构,如图),断裂1 mol P—P、1 mol Cl—Cl、1 mol P—Cl需要吸收的能量分别为a kJ、b kJ、c kJ,该反应的ΔH为()A.(12c-6a-6b) kJ·mol-1B.(4a+6b-12c) kJ·mol-1C.(a+6b-12c) kJ·mol-1D.(6a+6b-12c) kJ·mol-12.(2024浙江台州月考)合成氨工业中的氢气可由天然气和水反应制备,其主要反应为CH4(g)+2H2O(g) CO2(g)+4H2(g)ΔH=+162 kJ·mol-1,断裂化学键所需能量如表,则断裂1 mol C—H所需吸收的能量为()C OA.207 kJB.414 kJC.632 kJD.828 kJ3.(教材习题改编)已知:①2H2(g)+O2(g) 2H2O(l)ΔH1=-571.6kJ/molO2(g) H2O(g)ΔH2=-241.8 kJ/mol②H2(g)+12③CH4(g)+2O2(g) CO2(g)+2H2O(l)ΔH3=-890.3 kJ/mol请回答下列问题:(1)H2的燃烧热为kJ/mol;等质量的H2和CH4完全燃烧生成H2O(l),放出热量较多的是。
(2)112.0 L(标准状况)H2和CH4的混合气体充分燃烧生成H2O(l),放出3 242.5 kJ热量,则混合气体中CH4的体积分数为。
(3)写出CH4燃烧生成CO2和水蒸气的热化学方程式:。
题组二反应热的判断与大小比较4.(2024湖南长沙雅礼中学月考)下列各组热化学方程式中,ΔH的比较正确的是() ①C(s)+O2(g) CO2(g)ΔH1C(s)+1O2(g) CO(g)ΔH22②S(s)+O2(g) SO2(g)ΔH3S(g)+O2(g) SO2(g)ΔH4③H2(g)+1O2(g) H2O(l)ΔH522H2(g)+O2(g) 2H2O(l)ΔH6④CaO(s)+H2O(l) Ca(OH)2(s)ΔH7CaCO3(s) CaO(s)+CO2(g)ΔH8A.ΔH1<ΔH2B.ΔH3<ΔH4C.ΔH5<ΔH6D.ΔH7>ΔH85.(经典题)(2024广东深圳红岭中学质检)已知:①2H2(g)+O2(g)2H2O(g)ΔH1②3H2(g)+Fe2O3(s) 2Fe(s)+3H2O(g)ΔH2O2(g) Fe2O3(s)ΔH3③2Fe(s)+32O2(g) Al2O3(s)ΔH4④2Al(s)+32⑤2Al(s)+Fe2O3(s) Al2O3(s)+2Fe(s)ΔH5下列关于上述反应焓变的判断正确的是()A.ΔH1>0B.ΔH5>0C.ΔH4<ΔH3D.ΔH1=ΔH2+ΔH3能力提升练题组反应热知识的综合应用1.(2024重庆部分重点中学调研)以太阳能为热源,热化学硫碘循环分解水制氢流程如图。
第一章 化学反应的热效应 知识点讲解及练习-高中化学人教版(2019)选择性必修1

一、基础概念:1、体系:容器内的反应物及发生的反应看作一个反应体系。
2、环境:反应容器和反应物质之外的都看作环境。
3、热量:4、反应热:5、焓变:=反应的焓变,用△H表示。
6、7、单位:热量:kJ、焓变:kJ/mol、反应热:kJ/mol8、△H:放热反应:△H<0,吸热反应:△H>09、内能:是体系内物质的各种能量的总和,受温度、压强和物质的聚集状态等影响。
10、能量变化的主要原因:化学键断裂和形成时的能量变化是化学反应中能量变化的主要原因。
11、(能量守恒)任何化学反应都有能量变化,所以在一个确定的化学反应关系中,反应物的总焓变与反应产物的总焓变一定不同。
12、△H的单位中“mol-1”的含义:对于一个化学反应:aA + bB = cC + dD,△H的单位中“mol-1”既不是指“每摩尔A”也不是指“每摩尔B、C、D”,而是指“每摩尔反应”。
13、能量越低越稳定。
三态之间的能量关系:s < l < g 。
14、键能越大越稳定。
15、反应条件对△H无影响。
eg. H2(g)+Cl2(g)=2HCl(g)在光照条件下和点燃条件下,△H相同。
16、与反应条件无关,吸热反应不一定需要加热,放热反应,也可能需要加热。
17、18、19、断键:吸20、二、放热反应和吸热反应:1、概念:图像能量大小关系反应物能量总和大于生成物能量总合反应物能量总和小于生成物能量总合化学键角度反应物断键吸收的总能量小于生成物成键放出的总能量反应物断键吸收的总能量大于生成物成键放出的总能量2、记住常见的放热反应和吸热反应:反应类型吸热反应放热反应类型①盐类水解反应&弱电解质的电离②大多数分解反应③以H2、CO、C为还原剂的反应④Ba(OH)2•8H2O和NH4Cl反应①所有的燃烧反应②所有的酸碱中和反应③铝热反应④大多数化合反应⑤活泼金属单质、金属氧化物与水或酸的反应金属的缓慢氧化、食品腐败、糖类在体内消化吸收3、判断正误:✗化学反应中的能量变化都表现为热量变化✗物质燃烧不一定是放热反应✗伴有能量变化的过程都是化学变化✗凡吸热反应均需加热等条件✗在化学变化中,发生物质变化的同时不一定发生能量变化4、热量测量装置图:三、中和热和燃烧热1、中和热:思考?1)测定中和热需要测哪些数据?2)如何根据这些数据计算反应热?3)为了减少误差,应采取哪些措施?实验仪器?量热计或者简易量热计(大烧杯、小烧杯、碎泡沫破碎料、泡沫塑料板或硬纸板)、量筒、温度计、环形玻璃搅拌棒。
高中化学(新人教版)选择性必修一课后习题:反应热的计算(课后习题)【含答案及解析】

反应热的计算课后篇素养形成必备知识基础练1.相同温度时,下列两个反应的反应热分别用ΔH 1和ΔH 2表示,则( ) ①H 2(g)+12O 2(g)H 2O(g) ΔH 1=-Q 1 kJ·mol -1②2H 2O(l)2H 2(g)+O 2(g) ΔH 2=+Q 2 kJ·mol -1已知Q 1、Q 2均大于零。
A.Q 1>Q 2B.Q 1=Q 2C.2Q 1<Q 2D.Q 2=2Q 1解析将①式改写成2H 2(g)+O 2(g)2H 2O(g) ΔH 3=-2Q 1 kJ·mol -1③,将②式改写成2H 2(g)+O 2(g)2H 2O(l)ΔH 4=-Q 2 kJ·mol -1④。
③式中各物质的化学计量数与④式相同,但③式中H 2O 为气态,④式中H 2O 为液态,生成液态水比生成等物质的量的气态水所放出的热量多,故2Q 1<Q 2。
2.已知H —H 、H —O 和O O 的键能分别为436 kJ·mol -1、462.8 kJ·mol -1和497.3 kJ·mol -1。
下列热化学方程式正确的是( ) A.H 2O(g)H 2(g)+12O 2(g) ΔH =-481.9 kJ·mol -1 B.H 2O(g)H 2(g)+12O 2(g) ΔH =+481.9 kJ·mol -1C.2H 2(g)+O 2(g)2H 2O(g) ΔH =+481.9 kJ·mol -1D.2H 2(g)+O 2(g)2H 2O(g) ΔH =-481.9 kJ·mol -1解析1 mol 气态水分解产生1 mol H 2(g)和12 mol O 2(g)的能量变化为2×462.8 kJ-436 kJ-12×497.3 kJ=240.95 kJ 。
因此气态水分解的热化学方程式可表示为H 2O(g)H 2(g)+12O 2(g) ΔH =+240.95kJ·mol -1。
人教版高中化学选择性必修第1册 第一章 化学反应的热效应 第二节 反应热的计算 (2)

和 燃烧热的数据 。
2.根据教材中的例题,有关反应热的计算的主要类型有:
(1)根据反应热计算一定量物质完全燃烧 放出 的热量;
(2)利用 盖斯定律 计算某化学反应的ΔH。
微思考2怎样利用盖斯定律和已知反应的反应热计算其他
反应的反应热?
提示:若某个化学反应的ΔH=+a kJ·mol-1,则其逆反应的
A项正确;根据盖斯定律和能量守恒定律可知,B、C两项正确;
ΔH1+ΔH6=-(ΔH2+ΔH3+ΔH4+ΔH5),D项错误。
3.已知:
①2H2(g)+O2(g)══2H2O(g) ΔH1
②3H2(g)+Fe2O3(s)
③2Fe(s)+O2(g)
④2Al(s)+ O2(g)
⑤2Al(s)+Fe2O3(s)
ΔH=E(生成物)-E(反应物)
已知:
①H2(g)+ O2(g)══H2O(g) ΔH1=-241.8 kJ·mol-1
②H2O(g)══H2O(l) ΔH2=-44 kJ·mol-1
根据①和②,如何求出氢气的燃烧热?
提示:要计算H2的燃烧热,即求热化学方程式H2(g)+ O2(g)
CO(g)的反应热 ΔH。
ΔH3+ΔH2
,则:ΔH3= ΔH1-ΔH2 。
微思考1如何从能量守恒的角度,解释化学反应的热效应只
与反应体系的始态和终态有关?
提示:由于在指定状态下,各种物质的焓值都是确定的,因此
无论经过哪些步骤从反应物转化为生成物,它们的差值是不
反应热的计算 专题练习【化学人教版高中(新课标)同步测试】

反应热的计算 专题训练1.在298 K 、1.01×105 Pa ,将22 g CO 2通入0.75 L 1.0 mol·L -1 NaOH 溶液中充分反应,测得反应放出的热量为a kJ 。
已知该条件下1 mol CO 2通入1 L 2.0 mol·L -1 NaOH 溶液中充分反应放出的热量为b kJ 。
则CO 2与NaOH 反应生成NaHCO 3的热化学方程式为( ) A .CO 2(g)+NaOH(aq)NaHCO 3(aq) ΔH=-(2b-a) kJ·mol -1B .CO 2(g)+NaOH(aq)NaHCO 3(aq) ΔH=+(4a-b) kJ·mol -1C .CO 2(g)+NaOH(aq)NaHCO 3(aq) ΔH=-(4a-b) kJ·mol -1D .CO 2(g)+NaOH(aq)NaHCO 3(aq) ΔH=+(2b-a) kJ·mol -1【答案】C【解析】根据题意可知,22g CO 2通入1mol•L -1 NaOH 溶液750mL 中充分反应,测得反应放出akJ 的热量,写出热化学反应方程式,再利用1mol CO 2通入2mol•L -1NaOH 溶液1L 中充分反应放出b kJ 的热量写出热化学反应方程式,最后利用盖斯定律来书写CO 2与NaOH 溶液反应生成NaHCO 3的热化学方程式。
【详解】根据题意,22g CO 2通入1mol•L -1NaOH 溶液750 mL 中充分反应,n(CO 2)=2244=0.5mol ,n(NaOH)=1mol•L -1×0.75 L=0.75 mol ,该反应既生成碳酸钠又生成碳酸氢钠,方程式为2CO 2+3NaOH═ NaHCO 3+Na 2CO 3 +H 2O ,由0.5molCO 2反应放出热量为aKJ ,则2molCO 2反应放出热量为4a kJ ,即热化学反应方程式为2CO 2(g)+3NaOH(aq)═NaHCO 3 (aq)+Na 2CO 3(aq)+H 2O(l) △H=-4a kJ/mol ①。
化学反应热的计算 专题练习题 带答案

高二年级化学选修四同步小题狂练第一章第三节化学反应热的计算一、单选题1.已知下列热化学方程式:(1)CH3COOH(l)+2O2(g)=2CO2(g)+2H2O(l)△H1=−870.3kJ⋅mol−1(2)C(s)+O2(g)=CO2(g)△H2=−393.5kJ⋅mol−1O2(g)=H2O(l)△H3=−285.8kJ⋅mol−1(3)H2(g)+12则反应2C(s)+2H2(g)+O2(g)=CH3COOH(l)的△H为()kJ⋅mol−1.A. +488.3B. −244.15C. −488.3D. +244.152.已知:H2O(g)=H2O(l)△H1=−Q1kJ⋅mol−1(Q1>0)C2H5OH(g)=C2H5OH(l)△H2=−Q2kJ⋅mol−1(Q2>0)C2H5OH(g)+3O2(g)=2CO2(g)+3H2O(g)△H3=−Q3kJ⋅mol−1(Q3>0)依据盖斯定律,若使23g液态乙醇完全燃烧并恢复至室温,则放出的热量为(单位:kJ)()A. Q1+Q2+Q3B. 0.5(Q1+Q2+Q3)C. 0.5Q1−1.5Q2+0.5Q3D. 1.5Q1−0.5Q2+0.5Q33.已知:①CH3COOH(l)+2O2(g)=2CO2(g)+2H2O(l)△H1②C(s)+O2(g)=CO2(g)△H2③2H2(g)+O2(g)=2H2O(l)△H3④2CO2(g)+4H2(g)=CH3COOH(l)+2H2O(l)△H4下列关于上述反应的焓变判断正确的是()A. H2的燃烧热为△H3B. 2C(s)+2H2(g)+O2(g)=CH3COOH(l)△H=2△H2+△H3−△H1C. △H4−△H1+2△H3=0D. 2molH2(g)燃烧生成水蒸气的△H<△H34.在298K、100kPa时,已知:2H2O(g)=O2(g)+2H2(g)△H1Cl2(g)+H2(g)=2HCl(g)△H22Cl2(g)+2H2O(g)=4HCl(g)+O2(g)△H3则△H3与△H1和△H2间的关系正确的是()A. △H3=△H1+2△H2B. △H3=△H1+△H2C. △H3=△H1−2△H2D. △H3=△H1−△H25.天然气燃烧不完全会产生有毒气体CO,又知CO和CH4燃烧的热化学方程式分别为2CO(g)+O2(g)=2CO2(g)H=−566kJ⋅mol−1CH4(g)+2O2(g)=CO2(g)+2H2O(l)H=−890kJ⋅mol−1又知由H2与O2反应生成液态H2O比生成气态H2O多放出44kJ⋅mol−1的热量.则下列热化学方程式正确的是()A. 2CH4(g)+72O2(g)=CO2(g)+CO(g)+4H2O(l)△H=−1214kJ⋅mol−1B. 2CH4(g)+72O2(g)=CO2(g)+CO(g)+4H2O(g)△H=−1038kJ⋅mol−1C. 3CH4(g)+5O2(g)=CO2(g)+2CO(g)+6H2O(l)△H=−1538kJ⋅mol−1D. 3CH4(g)+5O2(g)=CO2(g)+2CO(g)+6H2O(g)△H=−1840kJ⋅mol−6.已知胆矾溶于水时溶液温度降低.胆矾分解的热化学方程式为CuSO4⋅5H2O(s)=CuSO4(s)+5H2O(l)△H=+Q1kJ⋅mol−1.室温下,若1mol无水硫酸铜溶解为溶液放热Q2 kJ,则()A. Q1>Q2B. Q1=Q2C. Q1<Q2D. 无法比较7.在1200℃时,天然气脱硫工艺中会发生下列反应H2S(g)+32O2(g)=SO2(g)+H2O(g)△H12H2S(g)+SO2(g)=32S2(g)+2H2O(g)△H22H2S(g)+O2(g)=2S(g)+2H2O(g)△H32S(g)=S2(g)△H4则△H4的正确表达式为()A. △H4=23(3△H3−△H1)−△H2 B. △H4=23(△H1+△H2)+△H3C. △H4=23(△H1+△H2)−△H3 D. △H4=23(△H1−△H2)−△H38.某科学家利用二氧化铈(CeO2)在太阳能作用下将H2O、CO2转变成H2、CO.其过程如下:下列说法不正确的是()A. 该过程中CeO2没有消耗B. 该过程实现了太阳能向化学能的转化第2页,共13页C. 图中△H1=△H2+△H3O2(g)=H2O(g)的反应热大于△H3D. H2(g)+129.如下图所示,△H1=−393.5kJ⋅mol−1,△H2=−395.4kJ⋅mol−1,下列说法正确的是A. 石墨和金刚石的转化是物理变化B. 金刚石的稳定性强于石墨C. 1 mol石墨的总键能比1 mol金刚石的总键能大1.9kJD. C(s,石墨)=C(s,金刚石),该反应的△H<010.已知:①2C(s)+O2(g)=2CO(g)△H=−220kJ⋅mol−1②氢气燃烧的能量变化示意图:下列说法正确的是()A. 1molC(s)完全燃烧放出110 kJ的热量O2(g)=H2O(g)△H=−480kJ⋅mol−1B. H2(g)+12C. C(s)+H2O(g)=CO(g)+H2(g)△H=+130kJ⋅mol−1D. 欲分解2 mol H2O(l),至少需要提供4×462 kJ的热量二、填空题11.研究NOx、SO2、CO等大气污染气体的处理方法具有重要意义.(1)氮氧化物是造成光化学烟雾和臭氧层损耗的主要气体.已知:①CO(g)+NO2(g)=NO(g)+CO2(g)△H=−a kJ⋅mol−1(a>0)②2CO(g)+2NO(g)=N2(g)+2CO2(g)△H=−b kJ⋅mol−1(b>0)若用标准状况下3.36LCO还原NO2至N2(CO完全反应)的整个过程中转移电子的物质的量为______ mol,放出的热量为______ kJ(用含有a和b的代数式表示).(2)用CH4催化还原NO x也可以消除氮氧化物的污染.例如:①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)△H1=−574kJ⋅mol−1①②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g)△H2=?②若1molCH4还原NO2至N2的整个过程中放出的热量为867kJ,则△H2=______ .12.(1)已知:①H2O(g)=H2O(l)△H1=−Q1kJ/mol②C2H5OH(g)=C2H5OH(l)△H2=−Q2kJ/mol③C2H5OH(g)+3O2(g)=2CO2(g)+3H2O(g)△H3=−Q3kJ/mol若使1mol乙醇液体完全燃烧,最后恢复到室温,则放出的热量为______ kJ(2)大气中的部分碘源于O3对海水中I−的氧化,将O3持续通入NaI溶液中进行模拟研究.O3将I−氧化成I2的过程由3步反应组成:a.I−(aq)+O3(g)=IO−(aq)+O2(g)△H1b.IO−(aq)+H+(aq)=HOI(aq)△H2c.HOI(aq)+I−(aq)+H+(aq)=I2(aq)+H2O(l)△H3总反应的化学方程式为______ ,其反应热△H=______ .13.已知X、Y、Z、W是短周期元素中的四种非金属元素,它们的原子序数依次增大.X元素的原子形成的离子就是一个质子,Z、W在元素周期表中处于相邻的位置,它们的单质在常温下均为无色气体,Y原子的最外层电子数是内层电子数的2倍.(1)请写出Z在元素周期表中的位置______ .(2)由X、Y、Z、W四种元素可组成酸式盐,该化合物的水溶液与足量NaOH溶液在加热条件下反应的离子方程式为______ .(3)工业上用E检验输送氯气的管道是否漏气,可观察到大量白烟,同时有单质Z生成,写出化学方程式______ ,该反应中氧化剂与还原剂的物质的量比为:______ .(4)Z的氢化物与NaClO反应可得到肼(N2H4),该反应的化学方程式为______ .(5)肼可作为火箭发动机的燃料,与氧化剂N2O4应生成N2和水蒸气.已知:①N2(g)+2O2(g)=N2O4(1)△H1=−195kJ⋅mol−1②N2H4(1)+O2(g)=N2(g)+2H2O(g)△H2=−534.2kJ⋅mol−1写出肼和N2O4反应的热化学方程式______ .14.磷单质及其化合物的有广泛应用.由磷灰石[主要成分Ca5(PO4)3F]在高温下制备白磷(P4)的热化学方程式为:4Ca5(PO4)3F(s)+2lSiO2(s)+30C(s)=3P4(g)+20CaSiO3(s)+30CO(g)+SiF4(g)△H已知相同条件下:第4页,共13页4Ca5(PO4)3F(s)+3SiO2(s)=6Ca3(PO4)2(s)+2CaSiO3(s)+SiF4(g)△H12Ca3(PO4)2(s)+10C(s)=P4(g)+6CaO(s)+10CO(g)△H2SiO2(s)+CaO(s)=CaSiO3(s)△H3用△H1、△H2和△H3表示△H,△H=______(2)次磷酸钠(NaH2PO2)可用于化学镀镍.①NaH2PO2中P元素的化合价为______ 4Ca5(PO4)3F(s)+2lSiO2(s)+30C(s)=3P4(g)+ 20CaSiO3(s)+30CO(g)+SiF4(g)△H.②化学镀镍的溶液中含有Ni2+和H2PO2ˉ,在酸性等条件下发生下述反应:Ni2++______ H2PO2ˉ+______ →______ Ni+______ H2PO3ˉ+______请在横线上写出配平反应式所需要的系数及缺少的物质(系数为1时不能省略不填)答案和解析【答案】1. C2. D3. B4. A5. D6. A7. C8. C 9. C 10. C11. 0.3;3(2a+b);−1160kJ/mol8012. (3Q1−Q2+Q3);2I−+O3+2H+=I2+O2+H2O;△H1+△H2+△H313. 第二周期第ⅤA族;NH4++HCO3−+2OH−=NH3↑+2H2O+CO32−;8NH3+3Cl2=6NH4Cl+N2;3:2;2NH3+NaClO=N2H4+NaCl+H2O;2N2H4(l)+N2O4(l)=3N2(g)+4H2O(g)△H=−873.4kJ/mol 14. △H1+3△H2+18△H3;+1;1;H2O;1;1;2H+【解析】1. 解:利用盖斯定律将(2)×2+(3)×2−(1)可得:2C(s)+2H2(g)+O2(g)=CH3COOH(l)则△H=2×(−285.8kJ⋅mol−1)+2×(−393.5kJ⋅mol−1)−(−870.3kJ⋅mol−1)=−488.3kJ⋅mol−1.故选C.根据盖斯定律将(2)×2+(3)×2−(1)可得2C(s)+2H2(g)+O2(g)=CH3COOH(l)的反应热.本题考查反应热的计算,题目难度不大,注意盖斯定律的运用.2. 解:①H2O(g)=H2O(l)△H1=−Q1kJ⋅mol−1(Q1>0),②C2H5OH(g)=C2H5OH(l)△H2=−Q2kJ⋅mol−1(Q2>0),③C2H5OH(g)+3O2(g)=2CO2(g)+3H2O(g)△H3=−Q3kJ⋅mol−1(Q3>0),根据盖斯定律可知,①×3−②+③得C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(l)△H=(−3Q1+Q2−Q3)kJ/mol,即1mol液态乙醇完全燃烧并恢复至室温,则放出的热量为(3Q1−Q2+Q3)kJ,则23g液态乙醇完全燃烧并恢复至室温,则放出的热量为0.5×(3Q1−Q2+Q3)kJ=(1.5Q1−0.5Q2+ 0.5Q3)kJ,故选D.23g液态乙醇为0.5mol,利用已知的反应得出C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(l)的反应热,利用物质的量与反应放出的热量成正比来解答.本题考查学生利用盖斯定律计算反应热,明确已知反应和目标反应的关系是解答本题的关键,题目难度中等.△H3,3. 解:A.③2H2(g)+O2(g)=2H2O(l)△H3中,不是1molH2燃烧时的能量变化,则H2的燃烧热为12故A错误;第6页,共13页B.由盖斯定律可知,②×2+③−①得到2C(s)+2H2(g)+O2(g)=CH3COOH(l),则2C(s)+2H2(g)+O2(g)=CH3COOH(l)△H=2△H2+△H3−△H1,故B正确;C.由盖斯定律可知,③×2−①得到④,则2△H3−△H1=△H4,即△H4+△H1−2△H3=0,故C错误;D.燃烧为放热反应,焓变为负,生成物中气态水的能量比液态水的能量高,则2molH2(g)燃烧生成水蒸气的△H>△H3,故D错误;故选B。
高中化学(必修一)第一章 反应热与焓变练习题(含答案解析)

高中化学(必修一)第一章 反应热与焓变 练习题(含答案解析)学校:___________姓名:___________班级:___________考号:___________一、单选题1.强酸与强碱的稀溶液发生中和反应时:H +(aq) +OH - (aq) =H 2O(l) △H= -57.3kJ/mol 。
向1 L0.5 mol/L 的NaOH 溶液中分别加入下列物质至恰好完全反应:△稀醋酸△浓硫酸△稀硝酸。
下列说法正确的是 A .三者放出的热量均为28. 65kJ B .浓硫酸反应放出的热量小于28. 65kJ C .稀硝酸反应放出的热量为28.65kJD .稀醋酸放出的热量大于28. 65kJ2.C 、CO 、4CH 和25C H OH 是常用的燃料,1 mol 上述物质分别完全燃烧生成()2CO g 及()2H O l 时,放出的热量依次为393.5 kJ 、283.0 kJ 、890.3 kJ 和1366.8 kJ 。
相同质量的这4种燃料完全燃烧,放出热量最多的是。
A .CB .COC .4CHD .25C H OH3.下列反应属于吸热反应的是 A .KOH+HF=KF+H 2O B .NH 4Cl+NaOH ΔNH 3+H 2O+NaCl C .CaO+H 2O=Ca(OH)2D .C+O 2ΔCO 24.肼(H 2N -NH 2)燃烧涉及的共价键的键能与热化学方程式信息见下表:则2N(g)→N 2(g)+Q ,Q 为A .1882kJB .941kJC .483kJD .241.5kJ5.N 2(g)与H 2(g)化合生成NH 3(g)的能量变化如图,下列说法正确的是A.N2与H2的键能数值总和为1080B.N2(g)+3H2(g)2NH3(g)+46 kJC.1 mol H2(g)的能量比2 mol H(g)的能量低D.若使用催化剂会改变反应的热效应6.MgCO3和CaCO3的能量关系如图所示(M=Ca、Mg):已知:离子电荷相同时,半径越小,离子键越强。
高中化学(必修一)第一章 反应热的计算练习题(含答案解析)

高中化学(必修一)第一章反应热的计算练习题(含答案解析)学校:___________姓名:___________班级:___________考号:___________一、单选题1.质量相同的氢气,分别与足量的氧气点燃充分反应,在(1)生成液态水,(2)生成水蒸气两种情况下A.反应(1)放出的热量多B.反应(2)放出的热量多C.(1)、(2)放出的热量一样多D.无法比较两个反应放出的热量2.化学反应中的能量变化,通常表现为热量的变化,如Ba(OH)2·8H2O 与NH4Cl的反应要吸收热量,在化学上叫作吸热反应。
其原因是。
A.反应物NH4Cl所具有的能量比较低B.反应物Ba(OH)2·8H2O所具有的能量比较低C.反应物所具有的总能量高于生成物所具有的总能量D.反应物所具有的总能量低于生成物所具有的总能量低3.已知:25℃、101kPa时,1g H2完全燃烧生成液态水放出142.9kJ的热量,下列热化学方程式中书写正确的是A.2H2(g) + O2(g) = 2H2O(l)ΔH = -142.9kJ/molB.H2(g)+12O2(g)= H2O(l)ΔH = -285.8kJ/molC.2H2(g) + O2(g) = 2H2O(g)ΔH = -571.6kJ/molD.H2(g) +12O2(g) = H2O(g)ΔH = +285.8kJ/mol4.下列有关测定中和反应反应热实验的说法正确的是A.用铜丝代替玻璃搅拌器,测得的℃H偏小B.强酸的稀溶液与强碱的稀溶液反应生成1molH2O的℃H均为−57.3 kJ∙mol−1C.已知冰的熔化热为6.0 kJ∙mol−1,冰中氢键键能为20.0kJ·mol-1,假设1mol冰中有2mol氢键,且熔化热完全用于破坏冰中的氢键,则最多只能破坏1mol冰中15%的氢键D.若H2的燃烧热为a kJ∙mol−1,则燃烧热的热化学方程式H2(g)+Cl2(g)=2HCl(g) ℃H=−a kJ∙mol−15.盖斯定律表明,在一定条件下,化学反应的反应热只与反应体系的始态和终态有关,而与反应的途径无关。
高中化学《化学反应热的计算》练习题(附答案解析)

高中化学《化学反应热的计算》练习题(附答案解析)学校:___________姓名:___________班级:___________一、单选题1.在同温、同压下,下列各组热化学方程式中,△H 1>△H 2 的是 ( )A .2H 2O(g)=2H 2(g)+O 2(g)△H 1 2H 2O(l)=2H 2(g)+O 2(g) △H 2B .S(g)+O 2(g)=SO 2(g)△H 1 S(s)+O 2(g)=SO 2(g)△H 2C .2C(s)+O 2(g)=2CO(g)△H 1 2C(s)+2O 2(g)=2CO 2 (g)△H 2D .H 2(g)+Cl 2(g)=2HCl(g)△H 1 2HCl(g)=H 2(g)+Cl 2(g)△H 22.已知:断裂1molN N ≡键需吸收945.6kJ 能量,形成1molH N -键可放出391kJ 能量。
若()21molN g 和()23molH g 完全反应生成()3NH g 可放出92.4kJ 能量,则断裂1molH H -键需吸收的能量为( )A .45kJB .436kJC .466.8kJD .497.6kJ3.已知:碳的燃烧热ΔH 1=akJ ·mol -1;S(s)+2K(s)=K 2S(s)ΔH 2=bkJ ·mol -12K(s)+N 2(g)+3O 2(g)=2KNO 3(s);ΔH 3=ckJ ·mol -1黑火药是中国古代的四大发明之一,其爆炸的热化学方程式为:S(s)+2KNO 3(s)+3C(s)=K 2S(s)+N 2(g)+3CO 2(g)ΔH=xkJ ·mol -1。
则x 为( )A .3a+b -cB .c+3a -bC .a+b -cD .c+a -b 4.已知N N ≡键的键能是1945kJ mol ﹒-,H H -键的键能是1436kJ mol N H ﹒,--键的键能是1391kJ mol ﹒-,则()()()223N g 3H g 2NH g +=的H ∆为( )A .-93 kJ/molB .-208 kJ/molC .+93 kJ/molD .+208 kJ/mol5.已知石墨和金刚石燃烧的热化学方程式如下:C(石墨,s)+O 2(g) → CO 2(g)-393.8 kJ ;C(金刚石,s)+O 2(g) → CO 2(g)-395.2 kJ下列说法中正确的是( )A .石墨燃烧得到的CO 2分子能量大于金刚石燃烧得到的CO 2分子能量B .相同条件下,石墨比金刚石稳定C .等质量的石墨储存的能量大于金刚石D .石墨转化为金刚石是一个放热过程6.已知完全燃烧7.80g 乙炔气体生成 二氧化碳气体和液态水时,释放389.9kJ 的热。
高中化学选修一第一章《化学反应的热效应》经典练习

一、选择题1.下列有关反应热的说法不正确的是()A.在稀溶液中:H+(aq)+OH-(aq)=H2O(l),ΔH=-57.3kJ/mol,若将含0.5molH2SO4的稀硫酸与含1.1molNaOH的稀溶液混合,放出的热量等于57.3kJB.甲烷的燃烧热ΔH=-890kJ·mol-1,则甲烷燃烧的热化学方程式为:CH4(g)+2O2(g)=CO2(g)+2H2O(l)ΔH=-890kJ·mol-1C.H-H键、O=O键和O-H键的键能分别为436kJ/mol,496kJ/mol和462kJ/mol,则反应2H2+O2=2H2O的△H=-1832kJ/molD.已知:S(s)+O2(g)=SO2(g)ΔH1=-Q1kJ·mol-1,S(g)+O2(g)=SO2(g)ΔH2=-Q2kJ·mol-1,则Q1<Q2答案:C【详解】A. 将含0.5molH2SO4的稀硫酸与含1.1molNaOH的稀溶液混合时,反应生成水的物质的量为:0.5mol×2=1mol,根据中和热的热化学方程式可知,放出的热量等于57.3kJ,故A正确;B.甲烷的燃烧热ΔH=-890 kJ·mol-1,表示1 mol甲烷气体完全燃烧生成CO2气体和液态水时放出890 kJ的热量,则甲烷燃烧的热化学方程式为:CH4(g)+2O2(g)=CO2(g)+2H2O(l)ΔH=-890 kJ·mol-1,故B正确;C.因为没有注明各物质的聚集状态,所以不能计算反应过程中的能量变化值,故C错误;D.S(g)变化为S(s)要释放出热量,所以S(g)完全燃烧时比S(s)完全燃烧放出的热量多,则Q1<Q2,故D正确;答案选C。
2.101Kpa时,已知反应:①2C(s)+O2(g)=2CO(g) ΔH=-221kJ/mol②CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH=-802.3kJ/mol③稀溶液中,H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3kJ/mol下列结论中正确的是A.碳的燃烧热ΔH=-110.5kJ/molB.甲烷的燃烧热ΔH=-802.3kJ/molC.稀醋酸与稀氢氧化钠溶液反应生成1mol水,放出57.3kJ热量D.稀硫酸与稀氢氧化钠反应的中和热ΔH=-57.3kJ/mol答案:D【详解】A.反应①中,C(s)燃烧生成一氧化碳,所以1mol C(s)不充分燃烧产生的热量不是碳的燃烧热,A不正确;B.反应②中,甲烷燃烧的产物为H2O(g),而不是H2O(l),所以甲烷的燃烧热ΔH<-802.3kJ/mol,B不正确;C.由于醋酸为弱电解质,电离时吸热,所以稀醋酸与稀氢氧化钠溶液反应生成1mol水,放出小于57.3kJ热量,C不正确;D.稀硫酸与稀氢氧化钠反应生成1mol H2O(l),放出的热量即为中和热,其中和热ΔH=-57.3kJ/mol,D正确;故选D。
2023版新教材高中化学第一章化学反应的热效应第一节反应热第一课时反应热焓变课时作业新人教版选择性必

第一节反应热第一课时反应热焓变必备知识基础练1.下列说法中错误的是( )A.化学反应必然伴随发生能量变化B.化学反应中的能量变化主要是由化学键变化引起的C.化学反应中的能量变化通常表现为热量的变化D.人体运动消耗的能量与化学反应无关2.下列反应中,属于放热反应的是( )A.C与CO2反应B.高温煅烧石灰石C.生石灰与水反应D.Ba(OH)2·8H2O与NH4Cl反应3.下列有关中和热测定实验的叙述中,错误的是( )A.应准确读取酸碱混合后溶液的最高温度作为最终温度B.酸碱混合时,量筒中NaOH溶液应缓缓倒入量热计中,不断用玻璃棒搅拌C.用温度计测量盐酸的温度后,用水冲洗干净,再测量氢氧化钠溶液的温度D.为了保证0.50 mol·L-1的盐酸完全被中和,通常使氢氧化钠溶液稍稍过量4.在如图所示的量热计中,将100 mL 0.50 mol·L-1CH3COOH溶液与100 mL 0.55 mol·L -1NaOH溶液混合,温度从25.0 ℃升高到27.7 ℃。
下列说法错误的是( )A.若量热计的保温瓶绝热效果不好,则所测ΔH偏大B.搅拌器一般选用导热性差的玻璃搅拌器C.若选用同浓度同体积的盐酸,则溶液温度将升高至不超过27.7℃D.所加NaOH溶液过量,目的是保证CH3COOH溶液完全被中和5.下列有关能量变化的叙述正确的是( )A.NaHCO3与盐酸反应属于放热反应B.C(石墨,s)=C(金刚石,s)ΔH>0,说明石墨比金刚石稳定C.需要加热才能进行的反应一定是吸热反应D.同温同压下,H2(g)+Cl2(g)===2HCl(g)在光照和点燃条件下的ΔH不同6.已知:H2(g)+Br2(g)===2HBr(g) ΔH=-72 kJ·mol,其它相关数据如表:H2(g) Br2(g) HBr(g) 1 mol分子中的化学键断裂时需要吸收的能量/kJ 436 a 369A.404 B.260 C.230 D.2007.如图所示,ΔE1=393.5 kJ,ΔE2=395.4 kJ,下列说法正确的是( )A.1 mol石墨完全转化为金刚石需吸收1.9 kJ热量B.石墨和金刚石之间的转化是物理变化C.金刚石的稳定性强于石墨D.1 mol金刚石具有的总能量高于1 mol CO2的总能量8.下列反应的能量变化与示意图不相符的是( )A.生石灰与水的反应B.灼热的炭与水蒸气的反应C.盐酸和碳酸氢钠的反应D.氢氧化钡与氯化铵的反应9.50 mL 0.50 mol·L-1盐酸与50 mL 0.55 mol·L-1 NaOH 溶液进行中和反应,通过测定反应过程中所放出的热量可计算中和热,下列说法正确的是( )A.在测定中和热的实验中,至少需要测定并记录的温度是3次B.大烧杯上如不盖硬纸板,测得的中和热ΔH会偏大C.用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得中和热ΔH会偏小D.测定中和热的实验中,环形玻璃搅拌棒材料若用铜代替,则测量出的中和热ΔH< -57.3 kJ·mol-110.分解水获得H2的能量变化如图所示,下列说法正确的是( )A.分解水属于吸热反应B.断开H—O键放出能量C.形成H—H键吸收能量D.反应物的总能量大于生成物的总能量11.下列图像能准确表示氢气燃烧的热量变化的是( )12.如图为反应2H2(g)+O2(g)===2H2O(g)的能量变化示意图。
人教版初中高中化学选修一第一章《化学反应的热效应》经典练习题(含答案解析)

一、选择题1.下图为N2分子在催化剂作用下发生一系列转化的示意图,下列叙述正确的是()A.若N≡N键能是a kJ·mol-1,H—H键能是b kJ·mol-1,H—N键能是c kJ·mol-1,则每生成2 mol NH3,放出(6c-a-3b)kJ热量B.NH3分子和H2O分子的中心原子杂化类型不同C.催化剂a、b表面均发生了极性共价键的断裂D.在催化剂b作用下发生转化得到的两种生成物,均为直线形分子答案:A【详解】A.反应热就是断键吸收的能量和形成化学键所放出的能量的差值,则根据键能数据可知,该反应的反应热△H=akJ/mol+3bkJ/mol-2×3ckJ/mol,则每生成2 mol NH3,放出(6c-a-3b)kJ热量,选项A正确;B.水分子中价电子数=2+12(6-2×1)=4,水分子中含有2个孤电子对,所以氧原子采取sp3杂化,氨气中价层电子对个数=3+12(5-3×1)=4且含有1个孤电子对,所以N原子采用sp3杂化,杂化方式相同,选项B错误;C.催化剂a表面是氢气氮气反应生成氨气,催化剂a表面发生了非极性键(氢氢键和氮氮键)的断裂,催化剂b表面发生了非极性共价键(氧氧双键)的断裂,选项C错误;D.在催化剂b作用下发生转化得到的两种生成物H2O和NO,NO为直线形分子,H2O为V形分子,选项D错误;答案选A。
2.断裂1mol化学键所需的能量如表,火箭燃料肼(H2N—NH2)的有关化学反应的能量变化如图所示,则下列说法错误的是化学键N—N O=O N≡N N—H键能(kJ)154500942aA.N2(g)比O2(g)稳定B.N2H4(g)+O2(g)=N2(g)+2H2O(g)ΔH1=-534kJ·mol-1C.图中的ΔH3=+2218kJ·mol-1D.表中的a=194答案:D【详解】A.化学键的断裂要吸收能量,N≡N键能942kJ,O=O键能500kJ,所以N≡N键能大,破坏需吸收更多的能量,相对于破坏氧气中O=O难,N2(g)比O2(g)稳定,故A正确;B.根据图中内容,可以看出N2H4(g)+O2(g)=N2(g)+2H2O(g)ΔH1=-534kJ·mol-1,故B正确;C.根据图中内容,可以看出N2H4(g)+O2(g)=2N(g)+4H(g)+2O(g),△H3=△H1−△H2=−534kJ/mol-(-2752kJ/mol)=+2218kJ/mol,故C正确;D.根据图中内容,可以看出N2H4(g)+O2(g)=2N(g)+4H(g)+2O(g),△H3=−534kJ/mol-(-2752kJ/mol)=2218kJ/mol,化学反应的焓变等于产物的能量与反应物能量的差值,旧键断裂吸收能量,新键生成释放能量,设断裂1molN−H键所需的能量为akJ/mol,旧键断裂吸收的能量:154kJ/mol+4akJ/mol+500kJ/mol=2218kJ/mol,解得a=391,故D错误;答案选:D。
新人教版高中化学选修一第一章《化学反应的热效应》测试卷(答案解析)(1)

一、选择题1.(0分)[ID :138099]键能是化学键断开需吸收的能量或形成所放出的能量。
N 4在21世纪才被发现,跟你们的年龄差不多。
N 4是正四面体结构,有六个N-N 单键,N-N 键能为193kJ/mol ,而N 2有一个N N ≡键,键能为946kJ/mol 。
下列叙述正确的是A .2molN 2变成1molN 4需要吸收能量734kJB .2molN 2的总能量高于1molN 4的总能量C .N 4比N 2更稳定,因为N 4的键能更小D .如图所示,A 为N 4,B 为2N 22.(0分)[ID :138006]根据以下三个热化学方程式:2H 2S(g)+3O 2(g)=2SO 2(g)+2H 2O(l) ΔH =-Q 1kJ·mol -12H 2S(g)+O 2(g)=2S(s)+2H 2O(l) ΔH =-Q 2kJ·mol -12H 2S(g)+O 2(g)=2S(s)+2H 2O(g) ΔH =-Q 3kJ·mol -1判断Q 1、Q 2、Q 3三者关系正确的是A .Q 1>Q 2>Q 3B .Q 1>Q 3>Q 2C .Q 3>Q 2>Q 1D .Q 2>Q 1>Q 33.(0分)[ID :138002]水煤气变换反应为:CO(g)+H 2O(g)=CO 2(g)+H 2(g)。
我国学者结合实验与计算机模拟结果,研究了在金催化剂表面上水煤气变换的反应历程,如图所示,其中吸附在金催化剂表面上的物种用·标注。
下列说法正确的是A .水煤气变换反应的∆H>0B .步骤③的化学方程式为:CO·+OH·+H 2O(g)=COOH·+H 2O·C .步骤⑤只有非极性键H-H 键形成D .该历程中最大能垒(活化能)E 正=1.86eV4.(0分)[ID :138001]甲烷的燃烧热为890kJ /mol ,但当41molCH 不完全燃烧生成CO 和()2H O l 时,放出的热量为607kJ ,如果41molCH 与一定量2O 燃烧生成CO 、2CO 、2H O ,并放出819.25kJ 的热量,则一定量2O 的质量为( )A.40g B.56g C.60g D.无法计算5.(0分)[ID:138071]下列各组热化学方程式中,△H1>△H2的是①C(s)+O2(g)=CO2(g) △H1 C(s)+12O2(g)=CO(g) △H2②S(s)+O2(g)=SO2(g) △H1 S(g)+O2(g)=SO2(g) △H2③H2(g)+12O2(g)=H2O(l) △H1 2H2(g)+O2(g)=2H2O(l) △H2④CaCO3(s)=CaO(s)+CO2(g) △H1 CaO(s)+H2O(l)=Ca(OH)2(s) △H2A.①B.④C.②③④D.①②③6.(0分)[ID:138054]天然气可催化重整制备合成气(CO、H2),其有关反应如下:①CH4(g)+CO2(g)=2CO(g)+2H2(g)ΔH1②CH4(g)=C(s)+2H2(g)ΔH2=+75kJ·mol-1③C(s)+12O2(g)=CO(g)ΔH3=-111kJ·mol-1④C(s)+O2(g)=CO2(g)ΔH4=-394kJ·mol-1下列说法正确的是()A.反应②在较低温度下能自发进行B.CO的燃烧热为283kJ·mol-1C.若3molC(s)燃烧生成1molCO(g)和2molCO2(g),则损失的热量为111kJD.在上述反应①中,ΔH1=-247kJ·mol-1[7.(0分)[ID:138046]下列说法正确的是 ()A.需要加热才能发生的反应一定是吸热反应B.化学反应中放热是产生了新的能量C.任何放热反应在常温下一定能发生D.反应物和生成物所具有的总能量决定了反应是放热还是吸热8.(0分)[ID:138036]反应A(g)+B(g)→C(g)△H,分两步进行:①A(g)+B (g)→X(g)△H1;②X(g)→C(g)△H2。
高中化学新人教版选择性必修112反应热的计算作业
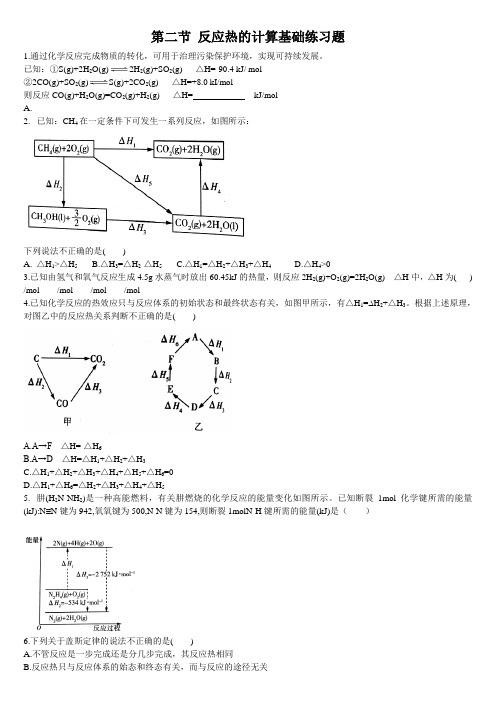
第二节反应热的计算基础练习题1.通过化学反应完成物质的转化,可用于治理污染保护环境,实现可持续发展。
已知:①S(g)+2H2O(g)2H2(g)+SO2(g) △H=-90.4 kJ/ mol②2CO(g)+SO2(g)S(g)+2CO2(g) △H=+8.0 kI/mol则反应CO(g)+H2O(g)=CO2(g)+H2(g) △H= kJ/molA.2.已知:CH4在一定条件下可发生一系列反应,如图所示:下列说法不正确的是( )A.△H1>△H5B.△H3=△H2-△H5C.△H1=△H2+△H3+△H4D.△H4>03.已知由氢气和氧气反应生成4.5g水蒸气时放出60.45kJ的热量,则反应2H2(g)+O2(g)=2H2O(g) △H中,△H为( ) /mol /mol /mol /mol4.已知化学反应的热效应只与反应体系的初始状态和最终状态有关,如图甲所示,有△H1=∆H2+△H3。
根据上述原理,对图乙中的反应热关系判断不正确的是( )A.A→F△H=-△H6B.A→D△H=△H1+△H2+△H3C.△H1+△H2+△H3+△H4+△H5+△H6=0D.△H1+△H6=△H2+△H3+△H4+△H55.肼(H2N-NH2)是一种高能燃料,有关肼燃烧的化学反应的能量变化如图所示。
已知断裂1mol化学键所需的能量(kJ):N≡N键为942,氧氧键为500,N-N键为154,则断裂1molN-H键所需的能量(kJ)是()6.下列关于盖斯定律的说法不正确的是( )A.不管反应是一步完成还是分几步完成,其反应热相同B.反应热只与反应体系的始态和终态有关,而与反应的途径无关C.有些反应的反应热不能直接测得,可通过盖斯定律间接计算得到D.根据盖斯定律,热化学方程式中△H直接相加即可得总反应热7.氧气(O2)和臭氧(O3)是氧元素的两种同素异形体,已知热化学方程式4Al(s)+3O2(g)=2Al2O3(s) △H1①4A1(s)+2O2(g)=2Al2O3(s) △H2②3O2(g)=2O3(g) △H3③则△H1、△H2、△H3的关系正确的是( )A.△H1-△H2=△H3B.△H1+△H2=△H3C.△H2-△H1=△H3D.△H1+△H2+△H3=08.已知:2H2(g)+O2(g)=2H2O(1) ∆H1=-572 kJ/molC(s)+O2(g)=CO2(g) ∆H2=-393 5 kJ/mol,C2H5OH(1)+3O2(g)=2CO2(g)+3H2O(1) △H3=-1 367 kJ/mol则2C(s)+3H2(g)+1/2O2(g)=C2H5OH(1) △H为( )A.+278 kJ/molB.-278 kJ/molC.+401.5 kJ/molD.-401.5 kJ/mol9.根据盖斯定律判断如图所示的物质转变过程中焓变的关系正确的是( )A.△H1=△H2=△H3=△H4B.△H1+△H2=△H3+△H4C.△H1+△H2+△H3=△H4D.△H1=△H2+△H3+△H410.灰锡(以粉末状存在)和白锡是锡的两种同素异形体。
高中化学第1章化学反应的热效应第2节反应热的计算作业含解析第一册

第2节反应热的计算A级·基础达标练一、选择题1.已知H2(g)+Cl2(g)===2HCl(g)ΔH=-184。
6 kJ·mol-1,则反应HCl(g)===错误!H2(g)+错误!Cl2(g)的ΔH为(D)A.+184。
6 kJ·mol-1B.-92.3 kJ·mol-1C.-369。
2 kJ·mol-1D.+92.3 kJ·mol-1解析:依据热化学方程式的书写原则和方法,已知热化学方程式为H2(g)+Cl2(g)===2HCl(g)ΔH=-184。
6 kJ·mol-1,改变方向,焓变变为正值,方程式系数除以2,焓变也除以2,得热化学方程式为:HCl(g)===错误!H2(g)+错误!Cl2(g)ΔH=+92.3 kJ·mol-1,故选D。
2.已知298 K时,合成氨反应N2(g)+3H2(g)2NH3(g)ΔH=-92。
0 kJ·mol-1,将此温度下的1 mol N2和3 mol H2放在一密闭容器中,在催化剂存在时进行反应,测得反应放出的热量为(假定测量过程中没有能量损失) (D)A.一定大于92.0 kJ B.无法确定C.一定等于92.0 kJ D.一定小于92。
0 kJ解析:合成氨是可逆反应,反应物不能完全转化,热化学方程式中的焓变是生成物与反应物的能量差,1 mol N2和3 mol H2不能完全转化为氨气,所以放热少于92 kJ,故选D。
3.已知:①H2(g)+错误!O2(g)===H2O(g)ΔH1=a kJ·mol-1②2H2(g)+O2(g)===2H2O(g)ΔH2=b kJ·mol-1③H2(g)+12O2(g)===H2O(l)ΔH3=c kJ·mol-1④2H2(g)+O2(g)===2H2O(l)ΔH4=d kJ·mol-1则a、b、c、d的关系正确的是(C)A.a〈c<0B.b〉d>0C.2a=b<0D.2c=d>0解析:反应①和③相比,③放出热量多,a大于c,A项错;氢气的燃烧是放热反应,b和d均为负值,B项错;反应②是①的二倍,故b=2a,而且燃烧放热,即b=2a<0,C项正确;氢气的燃烧是放热反应,c和d均为负值,故D项错误。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第三节化学反应热的计算基础巩固1下列说法正确的是( )A.化学反应的反应热与反应过程有密切的关系B.化学反应的反应热取决于反应体系的始态和终态C.盖斯定律只是一条简单的自然规律,其实际作用不大D.有的化学反应过程没有能量变化答案:B2已知热化学方程式2H2(g)+ O2(g)2H2O(l)ΔH1<0,则关于2H2O(l)2H2(g)+O2(g) ΔH2的说法不正确的是( )A.热化学方程式中的化学计量数只表示分子数B.该反应的ΔH2应大于零C.该反应的ΔH2=-ΔH1D.该反应可表示36 g液态水完全分解生成气态氢气和氧气的热效应答案:A3已知:H2SO4(aq)与Ba(OH)2(aq)反应的ΔH=-1 584.2 kJ·mol-1;HCl(aq)与NaOH(aq)反应的ΔH=-55.6 kJ·mol-1。
则生成BaSO4的焓变ΔH等于( )A.-1 528.6 kJ·mol-1B.-1 473 kJ·mol-1C.+1 473 kJ·mol-1D.+1 528.6 kJ·mol-1答案:B4在298 K、100 kPa时,已知:①2H2O(g)O2(g)+2H2(g) ΔH1②Cl2(g)+H2(g)2HCl(g) ΔH2③2Cl2(g)+2H2O(g)4HCl(g)+O2(g) ΔH3则ΔH3与ΔH1、ΔH2间的关系正确的是( )A.ΔH3=ΔH1+2ΔH2B.ΔH3=ΔH1+ΔH2C.ΔH3=ΔH1-2ΔH2D.ΔH3=ΔH1-ΔH2答案:A5相同温度时,下列两个反应的反应热分别用ΔH1和ΔH2表示,则( )①H2(g)+O2(g)H2O(g) ΔH1=-Q1kJ·mol-1;②2H2O(l)2H2(g)+O2(g) ΔH2=+Q2 kJ·mol-1。
A.Q1>Q2B.Q1=Q2C.2Q1<Q2D.Q2=Q1解析:将①式改写成③式:2H2O(g)2H2(g)+O2(g) ΔH3=+2Q1kJ·mol-1,③式中的化学计量数与②式相同,但③式中H2O为气态,②式中H2O为液态,生成液态水比生成等物质的量的气态水所放出的热量多,故2Q1<Q2。
答案:C6已知化学反应的热效应只与反应物的初始状态和生成物的最终状态有关,下列各反应热关系中不正确的是( )A.A→FΔH=-ΔH6B.A→DΔH=ΔH1+ΔH2+ΔH3C.ΔH1+ΔH2+ΔH3+ΔH4+ΔH5+ΔH6=0D.ΔH1+ΔH6=ΔH2+ΔH3+ΔH4+ΔH5解析:D项ΔH1+ΔH6=-(ΔH2+ΔH3+ΔH4+ΔH5)。
答案:D7已知热化学方程式:①C2H2(g)+O2(g)2CO2(g)+H2O(l)ΔH1=-1 301.0 kJ·mol-1②C(s)+O2(g)CO2(g)ΔH2=-393.5 kJ·mol-1③H2(g)+O2(g)H2O(l)ΔH3=-285.8 kJ·mol-1则反应④2C(s)+H2(g)C2H2(g)的ΔH为( )A.+228.2 kJ·mol-1B.-228.2 kJ·mol-1C.+1 301.0 kJ·mol-1D.+621.7 kJ·mol-1解析:热化学方程式①②③和④之间存在如下关系:2×②+③-①=④。
所以2ΔH2+ΔH3-ΔH1=ΔH=-2×393.5 kJ·mol-1-285.8 kJ·mol-1+1 301.0 kJ·mol-1=+228.2 kJ·mol-1。
答案:A8(1)已知:Fe2O3(s)+3C(石墨,s)2Fe(s)+3CO(g)ΔH=+489.0 kJ·mol-1①;CO (g)+O2(g)CO2(g) ΔH=-283.0 kJ·mol-1②;C(石墨,s)+O2(g)CO2(g) ΔH=-393. 5 kJ·mol-1③;则Fe(s)与O2(g)反应生成Fe2O3(s)反应的热化学方程式为。
(2)25 ℃、101 kPa下:①2Na(s)+O2(g)Na2O(s) ΔH1=-414 kJ·mol-1;②2Na(s)+O2(g)Na2O2(s)ΔH2=-511 kJ·mol-1;25 ℃、101 kPa下,Na2O2(s)与Na(s)反应生成Na2O(s)的热化学方程式为。
解析:(1)由盖斯定律知:③×6-①×2-②×6即得到反应4Fe(s)+3O2(g)2Fe2O3(s) ΔH=-1 641.0 kJ·mol-1。
(2)由盖斯定律知①×2-②即得到反应Na2O2(s)+2Na(s)2Na2O(s) ΔH=-317 kJ·mol-1。
答案:(1)4Fe(s)+3O2(g)2Fe2O3(s)ΔH=-1 641.0 kJ·mol-1(2)Na2O2(s)+2Na(s)2Na2O(s)ΔH=-317 kJ·mol-19已知下列热化学方程式:①H2(g)+O2(g)H2O(l)ΔH=-285.8 kJ·mol-1②H2(g)+O2(g)H2O(g)ΔH=-241.8 kJ·mol-1③C(s)+O2(g)CO(g)ΔH=-110.5 kJ·mol-1④C(s)+O2(g)CO2(g)ΔH=-393.5 kJ·mol-1回答下列问题:(1)上述反应中属于放热反应的是。
(2)H2的燃烧热ΔH= ;C的燃烧热ΔH= 。
(3)燃烧10 g H2生成液态水,放出的热量为。
(4)写出CO燃烧的热化学方程式: 。
解析:(1)放热反应的ΔH<0,故①②③④都是放热反应。
(2)1 mol可燃物完全燃烧生成稳定氧化物所放出的热量为燃烧热,由方程式知H2、C的燃烧热(ΔH)分别为-285.8 kJ·mol-1、-393.5 kJ·mol-1。
(3)10 g H2的物质的量为 5 mol,燃烧生成液态水,放出的热量为 5 mol×285.8 kJ·mol-1=1 429 kJ。
(4)由方程式④-③得CO(g)+O2(g)CO2(g) ΔH=-283 kJ·mol-1。
答案:(1)①②③④(2)-285.8 kJ·mol-1-393.5 kJ·mol-1(3)1 429 kJ(4)CO(g)+O2(g)CO2(g)ΔH=-283 kJ·mol-110已知在298 K下的热化学方程式:C(石墨,s)+O2(g)CO2(g)ΔH1=-393.5 kJ·mol-12CO(g)+O2(g)2CO2(g)ΔH2=-566.0 kJ·mol-1。
298 K时,1 mol C(石墨,s)转化为CO(g)的反应焓变是。
答案:ΔH=-110.5 kJ·mol-111已知:①Fe2O3(s)+3C(s)2Fe(s)+3CO(g)ΔH=+494 kJ·mol-1②CO(g)+O2(g)CO2(g)ΔH=-283 kJ·mol-1③C(s)+O2(g)CO(g)ΔH=-110 kJ·mol-1则反应Fe2O3(s)+3C(s)+O2(g)2Fe(s)+3CO2(g)的ΔH= kJ·mol-1。
理论上反应(填上述方程式序号,下同)放出的热量足以供给反应所需要的热量。
解析:依据盖斯定律,按“①+②×3”可得反应的ΔH=-355 kJ·mol-1。
反应②③为放热反应,可提供给①反应所需的能量。
答案:-355 ②③①12用O2将HCl转化为Cl2,可提高效益,减少污染。
传统上该转化通过如图所示的催化循环实现。
其中,反应①为:2HCl(g)+CuO(s)H2O(g)+CuCl2(s) ΔH1反应②生成 1 mol Cl2(g)的反应热为ΔH2,则总反应的热化学方程式为(反应热用ΔH1和ΔH2表示)。
答案:2HCl(g)+O2(g)H2O(g)+Cl2(g)ΔH=ΔH1+ΔH2能力提升1(2017江苏化学)通过以下反应可获得新型能源二甲醚(CH3OCH3)。
下列说法不正确的是( )①C(s)+H2O(g)CO(g)+H2(g) ΔH1=a kJ·mol-1②CO(g)+H2O(g)CO2(g)+H2(g) ΔH2=b kJ·mol-1③CO2(g)+3H2(g)CH3OH(g)+H2O(g)ΔH3=c kJ·mol-1④2CH3OH(g)CH3OCH3(g)+H2O(g)ΔH4=d kJ·mol-1A.反应①、②为反应③提供原料气B.反应③也是CO2资源化利用的方法之一C.反应CH3OH(g)CH3OCH3(g)+H2O(l)的ΔH=kJ·mol-1D.反应2CO(g)+4H2(g)CH3OCH3(g)+H2O(g)的ΔH=(2b+2c+d) kJ·mol-1解析:A项,反应①生成CO(g)和H2(g),生成的CO(g)继续发生反应②生成CO2(g)和H2(g),反应③的原料为CO2(g)和H2(g),正确;B项,反应③可将温室气体CO2转化为燃料CH3OH,正确;C项,反应④中生成的H2O为气体,选项所给反应中生成的H2O为液体,故选项中反应的ΔH≠kJ·mol-1,错误;D项,依据盖斯定律:反应②×2+反应③×2+反应④,可得热化学方程式2CO(g)+4H2(g)CH3OCH3(g)+H2O(g) ΔH=(2b+2c+d) kJ·mol-1,正确。
答案:C2肼(H2NNH2)是一种高能燃料,有关化学反应的能量变化如图所示,已知断裂1 mol化学键所需的能量(kJ):N≡N键为942、O O键为500、N—N键为154,则断裂1 mol N—H键所需的能量(kJ)是( )A.194B.391C.516D.658解析:利用图示可知肼和氧气变成原子时断键需要的能量为 2 752 kJ-534 kJ=2 218 kJ。
肼和氧气断键变为原子时要断裂1个N—N键,4个N—H键,1个O O键,所以1×154+4×(N—H键能)+1×500 kJ=2 218 kJ,解得N—H键能为391,单位kJ。
答案:B3已知:C(s)+H2O(g)CO(g)+H2(g)ΔH=a kJ·mo l-1;2C(s)+O2(g)2CO(g)ΔH=-220 kJ·mol-1。
