化学平衡移动
高中化学必修2 化学平衡的移动1

高温、高压 催化剂
2 NH 3 Q
(1)当增大N2的浓度时,N2的反应速率增 大,而NH3的速率不变,正反应速率增 大,平衡向正反应方向移动
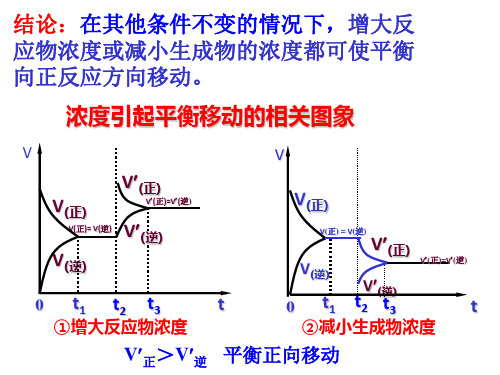
结论:在其它条件不变时,增大反应物的浓度 或减小生成物的浓度,化学平衡向正反 应移动;反之,向逆反应方向移动。
图像:
(2)当增大压强时,容器的体积减小,N2、H2、 NH3的浓度同时增大,但是,H2和N2的反 应速率增大比NH3的大,正反应速率增大快, 平衡向正反应方向移动。
C、3molC+1molD D、1molA+0.5molB+1.5molC+0.5molD (2)恒温、恒压下的等效平衡 判断方法:将生成物按方程式完全归于反应物 ,其各反应物的物质的量之比相同时,即能达 到同一平衡状态;否则为不同的平衡状态。
结论:增大压强,平衡向气体分子数目减小的 方向移动。 图像: V正
v
V正 V逆
V逆
t
(3)当升高温度时,正逆反应速率都增大,但 向吸热方向速率增大较快,总体向正反应 方向移动。 结论:当其它条件不变时,升高温度,反应 向吸热方向移动。
图像:
V正
v
V正
V逆V逆t来自(4)催化剂:使正逆反应速率同时增大相同 的倍数。
化学平衡的移动
复习回顾:
一定条件下,可逆反应进行到 1、化学平衡: 一定程度时,正反应速率和逆 反应速率相等,反应物的浓度 和生成物的浓度不再改变的状态 2、条件: 3、标志: 一定条件(温度、压强) 正逆反应速率相等 反应物浓度和生成物浓度不再 改变
一、化学平衡的移动 化学平衡移动的原因
N 2 3H 2
结论:催化剂只能加快反应速率,但不能改 变化学平衡。
化学平衡的移动与平衡常数

化学平衡的移动与平衡常数化学平衡是指在反应物和生成物之间达到动态平衡的状态,其中反应物被转化为生成物,而生成物又被转化回反应物。
在这个过程中,反应物和生成物的浓度会发生变化,而平衡常数则是用来描述反应物与生成物之间浓度比例的一个重要指标。
一、化学平衡的移动方向在化学平衡下,反应物和生成物的浓度通常会发生变化,移动的方向取决于浓度的变化趋势。
根据勒夏特列原理,如果在系统中添加了物质或者改变了温度、压力等条件,平衡反应会重新调整以适应这些改变,使得系统保持稳定。
1. 浓度变化引起的平衡移动当我们向平衡反应的反应体系中添加了更多的反应物,反应会朝着生成物的方向移动,以减小反应物的浓度。
相反地,如果我们添加了更多的生成物,反应则会朝着反应物的方向移动,以减小生成物的浓度。
这种移动方向是为了保持平衡条件。
2. 温度变化引起的平衡移动温度对平衡反应的移动方向也有影响。
根据利用吉布斯自由能进行分析,当增加温度时,反应物中的吸热反应会被加剧,因此反应会向吸热方向移动。
相反地,当降低温度时,反应物中的放热反应会被加剧,反应会向放热方向移动。
这种移动的方向是为了维持平衡状态。
二、平衡常数的意义与计算平衡常数用来描述反应物和生成物之间浓度比例的关系。
在平衡状态下,反应物浓度与生成物浓度之间的比例由平衡常数确定。
平衡常数的大小表示了反应的偏向程度,具体计算公式如下:Kc = [C]^c[D]^d / [A]^a[B]^b其中,[A]、[B]、[C]、[D] 分别表示反应物 A、B 和生成物 C、D的浓度,a、b、c、d 分别表示它们的化学计量数。
平衡常数 Kc 的值越大,表示反应偏向生成物的方向;Kc 的值越小,则表示反应偏向反应物的方向。
三、平衡常数对化学平衡的影响平衡常数不仅反映了反应物和生成物之间的浓度比例关系,还决定了反应物和生成物的转化率。
反应物和生成物的浓度与平衡常数之间的关系可以用来预测平衡位置和反应的可逆性。
化学反应的平衡移动

化学反应的平衡移动在化学反应中,平衡是指反应物和生成物的浓度或分压达到一定的比例,使反应达到一个动态平衡的状态。
平衡的移动是指改变反应条件,如温度、压力、浓度等,导致反应平衡位置的改变。
本文将探讨化学反应中平衡移动的原因、影响因素以及与平衡移动相关的应用。
一、化学反应的平衡移动原因化学反应的平衡移动是基于Le Chatelier原理,即“系统在受到扰动时,会产生使该扰动缓解的变化”。
根据这个原理,当化学反应受到外界条件的改变时,系统会通过移动平衡位置来缓解这种扰动。
具体而言,以下是一些导致平衡移动的原因:1. 温度变化:改变反应温度会影响反应速率和平衡位置。
一般而言,通过增加或降低温度,反应平衡位置可以相应地向生成物或反应物方向移动。
2. 压力变化:只对气态反应有效,改变反应体系的总压力会导致反应平衡位置的变化。
通过增加或减少总压力,反应平衡位置可以向分子数较多的一方移动。
3. 浓度变化:改变反应物或生成物的浓度会导致反应平衡位置发生变化。
增加反应物浓度会使反应平衡位置向生成物方向移动,而增加生成物浓度会使反应平衡位置向反应物方向移动。
4. 催化剂的使用:催化剂可以影响反应速率,但对反应平衡位置没有直接的影响。
二、影响化学反应平衡移动的因素除了上述的原因外,还有其他因素可以影响化学反应平衡移动。
以下是一些重要的因素:1. 反应物和生成物的物态:固态反应物和生成物不会因体积的变化而引起平衡移动,而气态和溶液态的反应物和生成物则会受到压力和浓度的影响。
2. 反应的平衡常数:平衡常数描述了反应体系在平衡状态下物质浓度之间的比例。
平衡常数越大,反应偏向生成物的概率越大;平衡常数越小,反应偏向反应物的概率越大。
3. 反应速率:平衡是反应速率相等时达到的,因此改变反应速率会导致平衡位置的移动。
例如,通过增加反应物的浓度或降低生成物的浓度,可以加快反应速率,导致平衡位置向生成物方向移动。
三、平衡移动的应用1. 工业应用:平衡移动的原理在工业生产中广泛应用。
高三化学 平衡移动 化学平衡的移动
①此原理只适用于已达平衡的可逆反应 ②平衡移动方向与条件改变方向相反。 ③移动的结果只能是减弱外界条件的该 变量,但不能抵消。
练习1:反应 2 A(g) 2B(g) + C(g) △H >0 达平衡时,要使V正降低,A的浓度增大,应采取
的措施是( C )
A. 加压
B. 减压
C. 降温
D. 增大C的浓度
能否引起平衡移动?(① ③ )
①增大水蒸气浓度
②加入更多的碳
③增加H2浓度 改变条件后能使CO浓度有何变化?
强调:气体或溶液浓度的改变会引起反应速
率的变化,纯固体或纯液体用量的变化不会
引起反应速率改变,化学平衡不移动
压强对化学平衡的影响:
(1)结论
aA (g) + bB(g)
当 a+b=c+d
cC(g) + dD(g)
(2)若X为气体,增大压强,X的物质的量不变,则可知
Y是_气___体___, Z是__固__体___或液体
4、在密闭容器中进行下列反应
CO2(g)+C(s)
2CO(g)
达平衡后,改变条件,指定物的浓度及平衡如何变化:
(1)减小密闭容器体积,保持温度不变,则平
衡 逆向移动; c(CO2)
增大。
(2温)
Ⅰ、恒温恒容下,充入与反应无关的气体,气体的浓度保 持恒定,正逆反应速率不变,故平衡不移动。
Ⅱ、恒温恒压下,充入与反应无关的气体。平衡混合气体 的浓度减小,正逆反应速率均减小,故相当于减小压强。
2.恒温下, 反应aX(g) bY(g) + cZ(g),达到平 衡后, 把容器体积压缩到原来的一半且达到新
V逆
化学平衡移动规律总结

化学平衡移动规律总结化学反应是物质转化的过程,而化学平衡则是在反应物和生成物浓度达到一定比例时的状态。
化学平衡的移动规律是指在一定条件下,平衡位置如何随着外界条件的改变而发生变化的规律。
下面将从温度、压力、浓度和催化剂四个方面来总结化学平衡的移动规律。
一、温度影响在化学反应中,温度的改变会影响反应物和生成物的速率以及平衡位置。
根据Le Chatelier定律,当温度升高时,反应速率会增加。
对于吸热反应,升高温度会使平衡位置向右移动,生成物浓度增加;而对于放热反应,升高温度会使平衡位置向左移动,生成物浓度减少。
二、压力影响在气相反应中,压力的改变对平衡位置有一定影响。
根据Le Chatelier定律,当压力增加时,平衡位置会向反应物浓度较小的一侧移动,以减少压力。
对于反应物和生成物摩尔数相等的反应,压力的改变不会影响平衡位置。
而对于摩尔数不相等的反应,压力的增加会使平衡位置向摩尔数较小的一侧移动。
三、浓度影响在溶液中的反应中,溶液浓度的改变会导致平衡位置的移动。
根据Le Chatelier定律,当浓度增加时,平衡位置会向生成物浓度较小的一侧移动,以减少浓度差。
而当浓度减少时,平衡位置会向生成物浓度较大的一侧移动,以增加浓度差。
四、催化剂影响催化剂可以加速化学反应的速率,但不参与反应。
催化剂的加入不会改变平衡位置,因为它同样影响反应物和生成物的速率。
催化剂提供了一个更低的活化能路径,使反应更容易进行,但并不改变反应的平衡位置。
化学平衡的移动规律可以通过调节温度、压力和浓度来实现。
根据Le Chatelier定律,当这些条件发生改变时,平衡位置会向着减少影响的一侧移动,以达到新的平衡状态。
催化剂的加入可以提高反应速率,但不会改变平衡位置。
这些规律的理解和应用对于理解和控制化学反应过程具有重要意义。
化学平衡的移动

化学平衡的移动平衡移动原理阐明了浓度、压强、温度对平衡移动的影响。
在恒温条件下改变浓度、压强,平衡可能发生移动,但平衡常数不变;改变温度,平衡常数有相应改变。
(1)浓度、压强对平衡移动的影响恒温下,改变反应物或(和)生成物的浓度,均能导致平衡移动。
对于有气态物质参与的反应,在恒温、恒容条件下,气态反应物或(和)生成物浓度的改变,就是相应各气态物质压强的改变,平衡将发生相应移动。
若在恒温条件下,改变有气态物质参与反应的总压强,则气态反应物、生成物的浓度或分压将以同等倍数增大或减小,对于气态反应物和生成物物质的量不同的反应,平衡将发生移动。
我们以N2+3H2=2NH3为例讨论如下。
①恒温、恒容下加N2(改变浓度),平衡向正反应方向移动的结果是:c2(N2)>c1(N2),c2(H2)<c1(H2),c2(NH3)>c1(NH3)。
H2转化率增大与c(NH3)增大是一致的,但N2的转化率却下降了。
恒温、恒容下加H2,平衡发生移动,c(NH3)增大和N2转化率增大一致,但H2的转化率下降。
结论是:恒温、恒容下增大一种反应物浓度,可提高其他反应物的转化率,而增大了浓度的反应物本身的转化率下降。
或者说,恒温、恒容条件下改变一种反应物的浓度,不可能出现所有反应物(若不止一种)转化率都升高或下降的情况。
②恒温下加大总压,如使p→2p。
在加压瞬间,N2、H2、NH3的浓度或分压强都增大1倍,平衡将向正反应方向移动。
若和2c1相比,N2、H2浓度或分压强减小,NH3增大。
即c3(NH3)>2c1(NH3),2c1(N2)>c3(N2)>c1(N2),H2同N2。
平衡移动结果若和原先c1相比,N2、H2、NH3浓度都增大了,只是NH3浓度或分压强增大更多。
即N2、H2转化率都增大了。
③恒温减压,如使p→p/2。
在减压瞬间,N2、H2、NH3的浓度或分压强都减半,平衡向逆反应方向移动。
化学平衡移动原理

2.0 9.2 16.4 35.5 53.6 69.4
结果:增大压强,NH3含量增加,平衡向右移动
6000C, 反应2SO3(g)
2SO2(g)+O2(g)的实
验数据
压强 / MPa
0.1
0.5
1.0
10
SO3的分解率/﹪
26.3
14.2
10.5
4.6
结果:增大压强,SO3含量增加,平衡向左移动
v N2 + 3H2
500℃左右比室温更有利于 合成氨反应
四. 对2HI(g)
B
H2(g)+I2(g)平衡体
系, 增大
平衡体系的压强可使颜色变 深
例:对于反应2A+B
2C,在反应过程中
C的百分含量随温度变化如图,则
C%
a
b
0
T0
T
(1)T0对应的V正与V逆的关系是 相等
。
(2)正反应为 放 热反应。
(3)a、b两点正反应速率的关系是b>a 。
改变反应条件时平衡移动的方向
改变反应条件
平 衡移 动
平衡移动结果
增大反应物浓度
①
减小反应物浓度
正向移动 逆向移动
反应物浓度减少 反应物浓度增大
增大压强
②
减小压强
向气体体积缩小 的方向移动
向气体体积增 大的方向移动
压强减小 压强增大
③ 升高温度 降低温度
向吸热方向移动 温度降低 向放热方向移动 温度升高
对平衡体系中的固态和 纯液态物质,其浓度可 看作一个定值,增加或 减小固态或液态纯净物 的量并不影响V正、V逆 的大小,所以化学平衡 不移动。
工业上往往根据上述原 理,通过适当增加相对 廉价的反应物或及时分 离出生成物的方法提高 产量、降低成本。例如, 在硫酸工业中常通入过 量的空气使二氧化硫充 分氧化,以得到更多的 三氧化硫。
化学平衡的移动与影响因素

化学平衡的移动与影响因素化学平衡是指当反应物生成产物的速率与产物生成反应物的速率相等时,反应处于平衡状态。
在化学平衡中,各种因素可能会对平衡的位置产生影响,导致反应向前或向后移动。
本文将介绍化学平衡移动的几种情况以及影响平衡位置的主要因素。
一、影响化学平衡移动的因素1.浓度的变化:当增加某个物质的浓度时,根据Le Chatelier原理,系统会偏离原来的平衡位置,以减小浓度差。
例如,在以下反应中:A + B ⇌ C,如果A的浓度增加,平衡会向右移动,生成更多的产物C,以减小A的浓度差。
2.压力的变化:当反应涉及气体时,改变压力也会影响平衡的位置。
增加压力会导致系统向压力较小的一方移动,减小压力差。
反之,减小压力会导致系统向压力较大的一方移动。
例如,在以下反应中:2H2(g) + O2(g) ⇌ 2H2O(g),增加压力会使平衡向右移动,生成更多的水蒸气,以减小压力差。
3.温度的变化:温度的变化对平衡的位置也具有显著影响。
一般而言,增加温度会导致平衡位置向反应吸热的一方移动,以吸收多余的热量。
反之,降低温度会导致平衡向反应放热的一方移动。
例如,在以下反应中:N2(g) + 3H2(g) ⇌2NH3(g),增加温度会使平衡向左移动,生成更多的氮气和氢气,以吸收多余的热量。
二、化学平衡移动的情况1.向生成物的方向移动:当增加某个反应物浓度、减小产物浓度、增加压力或增加温度时,平衡会向生成物的方向移动。
这意味着产生更多的产物并减小了原有的浓度差、压力差或温度差。
2.向反应物的方向移动:当增加某个产物浓度、减小反应物浓度、减小压力或降低温度时,平衡会向反应物的方向移动。
这会导致产生更多的反应物,并减小原有的浓度差、压力差或温度差。
三、示例分析让我们以以下反应为例:N2(g) + 3H2(g) ⇌ 2NH3(g)1.当增加氮气或氢气浓度时,平衡将向产生氨气的方向移动,生成更多的氨气以减小浓度差。
2.当增加氨气浓度时,平衡将向生成氮气和氢气的方向移动,减小氨气的浓度差。
化学平衡的移动和等效平衡

化学平衡的移动和等效平衡一.化学平衡的移动1.移动规律:遵循勒夏特列原理。
(1)浓度:增大反应物浓度或减小生成物浓度,平衡向正反应方向移动;减小反应物浓度或增大生成物浓度,平衡向逆反应方向移动。
(2)压强:增大压强,平衡向气体体积减小的方向移动;减小压强,平衡向气体体积增大的方向移动。
(3)温度:升高温度,平衡向吸热反应方向移动;降低温度,平衡向放热反应方向移动。
(4)催化剂:不能使平衡移动,但能减小达到新平衡所需要的时间。
2.例题:(1)反应2A(g)2B(g)+C(g);△H>0,达平衡时,要使v正降低、c(A)增大,应采取的措施是()。
A.加压B.减压C.升温D.降温(2)在容积固定的密闭容器中存在如下反应:A(g) + B(g) 3 C(g);(正反应为放热反应)某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,并根据实验数据作出下列关系图:下列判断一定错误的是()。
A、图I研究的是不同催化剂对反应的影响,且乙使用的催化剂效率较高B、图Ⅱ研究的是压强对反应的影响,且甲的压强较高C、图Ⅱ研究的是温度对反应的影响,且甲的温度较高D、图Ⅲ研究的是不同催化剂对反应的影响,且甲使用的催化剂效率较高[小结] 图像题的解题技巧:①四看:看横纵坐标表示的量,看图像的起点,看图像的转折点,看图像的走势;②联系:将题目的已知条件、图像得出的结论和平衡移动原理联系起来,看是否吻合,即可得出结论。
二.等效平衡规律1.恒温、恒容条件下的体积可变的等效平衡如果按方程式的化学计量关系转化为方程式同一半边的物质,其物质的量与对应组分的起始加入量相同,则建立的化学平衡状态时等效的。
例题:在密闭容器中,加入3molA和1 molB,一定条件下发生反应3A(g)+B(g)2C(g)+D(g),达平衡时,测得C的浓度为w mol/L,若保持容器中压强和温度不变,重新按下列配比作起始物质,达到平衡时,C的浓度仍然为w mol/L的是( )A.6molA+2mol B B 1.5mol A+0.5mol B+1mol C+0.5mol DC. 3mol A+1mol B+2mol C+1mol D D 2mol C+1mol D2.恒温、恒容条件下体积不变的等效平衡如果按方程式的化学计量关系转化为方程式同一半边的物质,其物质的量与对应组分的起始加入量成比例,则建立的化学平衡状态时等效的。
化学平衡的移动化学反应进行的方向

重点内容化学平衡的移动,化学反应进行的方向;2内容讲解一、化学平衡的移动1、含义:可逆反应达到平衡状态后,反应条件如浓度、压强、温度改变,使正和逆不再相等,原平衡被破坏;一段时间后,在新的条件下,正、逆反应速率又重新相等,即V正'=V逆',此时达到了新的平衡状态,称为化学平衡的移动;应注意:v正'≠v 正,v逆'≠v逆;2、影响因素:1浓度:其它条件不变时,增大反应物浓度或减小生成物浓度,平衡向正反应方向移动;增大生成物浓度或减小反应物浓度,平衡向逆反应方向移动;在下列反应速率v 对时间t的关系图象中,在t1时刻发生下述相应条件的变化,则正、逆反应速率的改变情况如图所示:①增大反应物浓度;②减小生成物浓度;③增大生成物浓度;④减小反应物浓度注:①由于纯固体或纯液体的浓度为常数,所以改变纯固体或纯液体的量,不影响化学反应速率,因此平衡不发生移动;②增大或减小一种反应物A的浓度,可以使另一种反应物B的转化率增大或减小,而反应物A的转化率减小或增大;2压强:其它条件不变时,对于有气体参加的可逆反应,且反应前后气体分子数即气体体积数不相等,则当缩小体积以增大平衡混合物的压强时,平衡向气体体积数减小的方向移动;反之当增大体积来减小平衡混合物的压强时,平衡向气体体积数增大的方向移动;若反应前后气体分子数即气体体积数相等的可逆反应,达到平衡后改变压强,则平衡不移动;对于反应mAg+nBg pCg+qDg,在下列v-t图中,在t1时刻发生下述相应条件的变化,则正、逆反应速率的改变情况如图所示:① m +n > p +q,增大压强;② m +n > p +q,减小压强;③ m +n < p +q,增大压强;④ m +n < p +q,减小压强;⑤ m +n = p +q,增大压强;⑥ m +n = p +q,减小压强;3温度:其它条件不变时,升高温度,平衡向吸热反应△H>0方向移动;降低温度,平衡向放热反应△H<0方向移动; 在下列v-t图中,在t1时刻发生下述相应条件的变化,则正、逆反应速率的改变情况如图所示:①正反应△H>0,升高温度;②正反应△H>0,降低温度;③正反应△H<0,升高温度;④正反应△H<0,降低温度;4催化剂:对于可逆反应,催化剂同等程度地改变正、逆反应速率,所以化学平衡不移动;在下列-图中,在t1时刻加入了催化剂,则正、逆反应速率的改变情况如图所示:3、化学平衡移动原理勒夏特列原理如果改变影响平衡的条件之一如浓度、压强、温度,平衡将向着能够减弱这种改变的方向移动;注:①影响平衡移动的因素只有浓度、压强或温度;②原理的研究对象是已达平衡的体系在解决问题时一定要特别注意这一点,原理的适用范围是只有一项条件发生变化的情况温度或压强或一种物质的浓度,当多项条件同时发生变化时,情况比较复杂;③平衡移动的结果只能减弱但不可能抵消外界条件的变化;④当反应条件改变时,化学平衡不一定发生移动;例如:改变压强,对反应前后气体体积数相等的反应无影响此时浓度也改变,同等程度增大或减小;因此,在浓度、压强、温度三个条件中,只有温度改变,化学平衡一定发生移动;二、化学反应进行方向的判据:1、焓判据:在一定条件下,对于化学反应, ⊿H<0即放热反应,有利于反应自发进行;2、熵判据:在一定条件下,自发过程的反应趋向于由有序转变为无序,导致体系的熵增大,这个原理叫“熵增原理”;综合判据:△H <0 △S>0 一定自发△H >0 △S<0 一定自发△H >0 △S>0 不一定高温自发△H <0 △S<0 不一定低温自发说明:1判断某一反应进行的方向,必须综合考虑体系的焓变与熵变;2在讨论反应方向问题时,是指一定温度、压强下,没有外界干扰时体系的性质;如果允许外界对体系施加某种作用如:通电、光照,就可能出现相反的结果;3反应的自发性只能用于判断反应的方向,不能确定反应是否一定会发生和反应发生的速率;即反应的自发性只提供反应发生的可能性趋势,而不提供有关反应是否能现实发生的信息;经典例题1.可逆反应Cs+H2Og COg+H2g △H<0,在一定条件下达到平衡,改变下列条件:1投入焦炭粉末 2增加CO 3降温 4加压5使用催化剂正、逆反应速率各怎样变化化学平衡怎样移动分析与解答:改变反应条件,正、逆反应的速率变化是一致的,只是变化程度大小不同而引起平衡的移动;浓度对固体物质无意义,催化剂同等程度地改变正、逆反应速率,对化学平衡移动没有影响;因此,答案如下“×”表示无影响:2、在某容器中,可逆反应2SO2g+O2g 2SO3g已建立化学平衡,容器中的压强是100kPa;在恒温下使容器体积比原来扩大1倍,重新达到平衡时,容器中的压强是A.小于200kPaB.大于200kPaC.等于200kPaD.等于400kPa分析与解答:扩大容器体积,必然减小气态物质的浓度,而使压强减小,平衡向着体积增大的方向移动;答案是B;3、将H2g和Br2g充入恒容密闭容器,恒温下发生反应:H2g+Br2g2HBrg △H<0 平衡时Br2g的转化率为a;若初始条件相同,绝热下进行上述反应,平衡时Br2g的转化率为b;a与b的关系是A.a>b B.a=b C.a<b D.无法确定分析:正反应为放热反应,前者恒温,后者相对前者,温度升高;使平衡向左移动,从而使Br2的转化率降低;所以b<a; 答案:A4、碘钨灯比白炽灯使用寿命长;灯管内封存的少量碘与使用过程中沉积在管壁上的钨可以发生反应;下列说法正确的是A.灯管工作时,扩散到灯丝附近高温区的WI2g会分解出W,W重新沉积到灯丝上B.灯丝附近温度越高,WI2g的转化率越低C.该反应的平衡常数表达式是D.利用该反应原理可以提纯钨分析与解答:该反应的正反应为放热反应,温度升高,化学平衡向左移动,选项A正确;灯丝附近温度越高,WI2的转化率越高,选项B错误;平衡常数应为生成物浓度除以反应物浓度:,选项C错误;利用该反应,可往钨矿石中加入I2单质,使其反应生成WI2富集,再通过高温加热WI2生成钨,从而提纯W,选项D正确; 答案:AD5、黄铁矿主要成分为FeS2是工业制取硫酸的重要原料,其煅烧产物为SO2和Fe3O4;1将 mol SO2g和 mol O2g放入容积为 1 L的密闭容器中,反应:在一定条件下达到平衡,测得计算该条件下反应的平衡常数K和SO2的平衡转化率写出计算过程; 2已知上述反应是放热反应,当该反应处于平衡状态时,在体积不变的条件下,下列措施中有利于提高SO2平衡转化率的有_________填字母A、升高温度B、降低温度C、增大压强D、减小压强E、加入催化剂F、移出氧气分析与解答:考查学生对可逆反应、化学平衡、化学平衡常数和影响化学平衡的外界条件的了解;考查学生计算平衡常数和平衡转化率的能力以及学生对化学平衡知识的综合应用及知识迁移能力;2由于正反应为放热反应,故降低温度可使平衡向右移动,提高SO2的平衡转化率;加入催化剂只能缩短达到平衡的时间,不能使平衡发生移动,故不能改变反应物的平衡转化率;恒容条件下,增大压强,若充入O2,可使平衡向右移动,能提高SO2的平衡转化率;若充入SO2,可使平衡向右移动,但SO2的平衡转化率将下降;若充入SO3,将使平衡向左移动,使SO2的平衡转化率下降;若充入无关气体,并不影响反应物与生成物的浓度,故平衡不移动;因此,增大压强不一定会使SO2的平衡转化率增大;同理,减小压强也不一定会使SO2的平衡转化率增大;。
化学平衡化学平衡移动

[总结]改变反应条件时平衡移动的方向
改变反应条件
增大反应物浓度
平衡移动方向
向减少反应物的浓度方向移动
减小反应物浓度
增 大 压 强 减 小 压 强 升 高 温 度 降 低 温 度 加 催 化 剂
向增大反应物的浓度方向移动
向气体体积缩小的方向移动 向气体体积增大的方向移动 向吸热反应方向移动 向放热反应方向移动 平衡不移动
化学平衡的移动
V正=V逆≠0 平衡1
条 件 改 变
′ V′ 正≠V逆
不平衡
平衡2 建立新平衡
一 定 时 间
破坏旧平衡
【定义】可逆反应中,旧化学平衡被破坏,新 化 学平衡建立过程,叫做化学平衡的移动。
影响化学平衡移动的因素 1、浓度对化学平衡的影响
在其他条件不变时,增大反应物浓度或减小
生成物浓度,化学平衡向正反应方向移动; 减小反应物浓度或增大生成物的浓度,化学 平衡向逆反应方向移动。
在其它条件不变的情况下,增大压强,会使化学平衡
向着气体体积缩小的方向移动,减小压强,会使化学
平衡向着气体体积增大的方向移动。
3、压强对化学平衡的影响:
3、压强对化学平衡的影响:
4、催化剂对化学平衡的影响
同等程度改变化学反应速率,V’正= V’逆 只改变反应到达平衡所需要的时间,而不影响 化学平衡的移动 v
(3)对于水溶液中的反应,水的浓度可视为1,不写入 平衡常数的关系式中
(4)同一化学反应,可以用不同的化学反应式来 表示,每个化学方程式都有自己的平衡常数关系 式及相应的平衡常数,方程式不同,平衡常数不 同。 例:N2O4(g) 2NO2(g)
[NO2 ]2 K [N2O4 ]
K [NO2 ] [N2O4 ]1/2
化学平衡移动

分离和提纯产物
利用化学平衡移动原理,通过改变条件使目 标产物从反应体系中分离出来,实现产物的 提纯和精制。
节能减排
通过合理设计工艺流程和操作条件,减少副 反应和废弃物的生成,降低能源消耗和环境 污染。
在环境保护中的应用
治理污染
利用化学平衡移动原理,通过添加试
大气污染治理
利用化学平衡移动原理,通过控制大
05
化学平衡移动的实验研究
实验目的和原理
实验目的
通过实验研究化学平衡移动的影响因素和规律,加深对化学平衡原理的理解。
实验原理
化学平衡是指在一定条件下,可逆反应的正反应速率和逆反应速率相等,反应物 和生成物的浓度保持不变的状态。当外界条件改变时,平衡状态会被打破,反应 会向着减弱这种改变的方向进行,直到建立新的平衡。
对于有气体参加的可逆反应,改变压力会使 平衡向着气体体积减小的方向移动。例如, 在合成氨的反应中,增大压力会使平衡向右 移动,提高氨的产率。
06
结论与展望
研究结论
沉淀溶解平衡的移动
通过改变沉淀溶解平衡的条件(如温度、浓度、压力或添加其他物质),可以使平衡发生移动。实验结果表 明,当改变条件时,平衡会向着减弱这种改变的方向移动。
3
氧化还原平衡
当改变氧化剂或还原剂的浓度时,氧化 还原平衡会向着能够减弱这种改变的方 向移动。例如,增大氧化剂浓度时,还 原剂会被氧化;增大还原剂浓度时,氧 化剂会被还原。
03
化学平衡移动的应用
在工业生产中的应用
优化生产条件
通过控制温度、压力、浓度等条件,使化学 平衡向有利于生成目标产物的方向移动,提 高产物的产量和质量。
实验步骤和操作
实验操作 配置不同浓度的弱酸或弱碱溶液。
化学平衡的移动

四、催化剂对化学平衡的影响
催化剂降低了反应的活 化能,正反应的活化能降低, 逆反应的活化能也降低,正 反应的活化分子百分数增加 几倍,逆反应的活化分子百 分数也增加几倍,正逆反应
速率增加的倍数相等,加催
化剂,不能使平衡发 生移动,只影响到达平衡
的时间。
4、使用催化剂对化学平衡的影响
V
速 率
V
速 率
V
V(逆) V( 正 )
V(正)= V(逆) V(正)=V(逆)
V
V( 正 )
V(正) = V(逆)
V(正)
V(逆)
V(正)
V( 逆 )
V(正)=V(逆)
V( 逆 )
0
t1
t2
t3
t
0
t1
t2 t3
t
①增大生成物浓度
②减小反应物浓度
结论:增加生成物浓度或减小反应物的浓度都可使 V逆>V正 平衡逆反应方向移动 平衡向逆反应方向移动 浓度引起平衡移动的v-t图分析
二、影响化学平衡的因素
(一)浓度
条件改变 原因 V正 > V逆 V正 < V逆 V正 < V逆 V正 > V逆 移动方向 正反应方向 逆反应方向 逆反应方向
①增大反应物浓度
②增大生成物浓度 ③减小反应物浓度 ④减小生成物浓度
正反应方向
1、浓度的变化对化学平衡的影响
V
V(正) V( 正 )
V(正)= V(逆) V(正)=V(逆)
2HI(g)
V V(正) V正= V逆
V(逆)
0
V(逆)
⑤增大压强
t
0
⑥减小压强
t
V正=V逆 平衡不移动
压强引起平衡移动的相关v-t图分析
化学平衡的移动

化学平衡的移动一化学平衡的移动在一定条件下,可逆反应达到了平衡状态,如果改变影响平衡的条件(如浓度、压强、温度等)化学平衡状态被破坏(正、逆反应速率不再相等),直至正逆反应速率再次相等,在新的条件下达到新的化学平衡状态。
注:看平衡向哪个方向移动,要看改变条件的瞬间。
正逆反应速率的相对大小。
二、影响化学平衡的因素1)浓度:增大反应物浓度或减小生成物浓度,平衡向正反应方向移动;减小反应物浓度或增大生成物浓度,平衡向逆反应方向移动。
2)温度:其他条件不变时,升高温度,平衡向着吸热方向移动;降低温度,平衡向着放热方向移动。
3)压强:其他条件不变时,对于有气体参加的反应,增大压强,会使平衡向着气体体积减小的方向移动;减小压强,会使平衡向着气体体积增大的方向移动。
但是压强改变,对于有气体参与而反应前后气态物质系数不变的反应来说,平衡不移动。
4)催化剂:同等程度增大正逆反应速率,故平衡不移动勒夏特列原理如果改变影响平衡的条件之一(如温度、压强以及参加反应的化学物质的浓度),平衡将向着减弱这种改变的方向移动。
例题1:在新制的氯水中存在平衡:Cl2+H2O++Cl-+HClO,若向氯水中投入少量碳酸钙粉末,溶液中发生的变化是()A.H+浓度减小,HClO浓度减小B.H+浓度增大,HClO浓度增大C.H+浓度减小,HClO浓度增大D.H+浓度增大,HClO浓度减小例题2.对已达化学平衡的下列反应2X(g)+Y(g),减小压强时,对反应产生的影响是()A.逆反应速率增大,正反应速率减小,平衡向逆反应方向移动B.逆反应速率减小,正反应速率增大,平衡向正反应方向移动C.正、逆反应速率都减小,平衡向逆反应方向运动D.正、逆反应速率都增大,平衡向正反应方向移动例题3:关节炎是因为在关节滑液中形成了尿酸钠晶体,尤其是在寒冷季节易诱发关节疼痛,其化学机理如下:①HUr+H2O Ur-+H3O+,尿酸尿酸根离子②Ur-(aq)+Na+(aq)NaUr(s)。
化学平衡移动

4.影响化学平衡的条件
浓度、压强、温度、催化剂等。
(1)、浓度
c(反应物)增大,v正突增为v’正, v逆不变,出现 v’正> v’逆,平衡正移,使v’正渐减, v’逆渐增,直至v’ 正= v’逆 时平衡, 且此时有v’正= v’逆> v正= v逆。
转化率:对于反应 mA(g)+nB(g) pC(g)+qD(g) 若增大的是c(A),则A的转化率减小,B的转化率增大
外界条件对化学反应速率与化学平衡的影响
可逆反应m A (g) +n B (g)
条件变化 增大c(A) 增大c(C) 反应特征
p C (g) +q D (g) △H=+Q kJ· mol-1
化学反应速率
υ正
加快 加快 减慢 减慢 加快 加快
υ逆
加快 加快 减慢 减慢 加快 加快
υ正与υ逆的关 系
υ正 > υ逆 υ正 < υ逆 υ正 < υ逆 υ正 > υ逆 υ正 > υ逆 υ正 = υ逆 υ正 < υ逆
五、化学学平衡移动
1.化学平衡移动的概念 当改变已经达到化学平衡的可逆反应的条件时,平衡 状态被破坏,随反应的进行重新达到新平衡的过程叫做化 学平衡移动。 2、勒夏持列原理:如果改变影响平衡的一个条件(如浓度、
压强和温度等),平衡就向着能够减弱这种改变的方向移动。 其中包含: ①影响平衡的因素:浓度、压强、温度三种; ②原理的适用范围:只适用于一项条件发生变化的情况(即温 度或压强或一种物质的浓度),当多项条件同时发生变化时,情 况比较复杂; ③平衡移动的结果:只能减弱(不可能抵消)外界条件的变化。 平衡移动:是一个“平衡状态→不平衡状态→新的平衡状态” 的过程。一定条件下的平衡体系,条件改变后,可能发生平衡移 动。
化学平衡的移动与控制

化学平衡的移动与控制化学平衡是指在化学反应中,反应物和生成物之间的浓度或压力保持恒定的状态。
在一定条件下,反应处于平衡状态时,正向反应和逆向反应的速率相等。
掌握化学平衡的移动和控制是化学研究和工业生产中的重要内容之一。
本文将介绍化学平衡的移动和控制的基本原理和一些常用的方法。
一、化学平衡的移动1. 温度的影响温度是化学反应速率和平衡位置的主要因素之一。
根据Le Chatelier 原理,当化学反应放出热量时(即反应是放热反应),增加温度会使平衡位置向生成物一侧移动,反之亦然。
这是因为通过增加温度,系统吸收热量,以吸收的热量作为平衡移动的动力。
2. 压力的影响对于气态反应来说,压力对平衡位置的移动有显著影响。
当反应物的摩尔数大于生成物时,增加压力会使平衡位置向生成物一侧移动,反之亦然。
这是因为通过增加压力,系统会使摩尔数较少的物质生成更多的物质,以减少系统所受的压力。
3. 浓度的影响对于溶液中的反应来说,溶液的浓度对平衡位置的移动也有影响。
当反应物的浓度大于生成物时,增加反应物的浓度会使平衡位置向生成物一侧移动,反之亦然。
这是因为通过增加反应物的浓度,系统会使浓度较低的物质生成更多的物质,以达到浓度均衡。
二、化学平衡的控制1. Le Chatelier原理的应用Le Chatelier原理是控制化学平衡的重要原理。
根据该原理,在系统受到外界扰动时,会产生一种趋向于减小该扰动的平衡移动。
所以,我们可以通过增加或减少反应物或生成物的浓度、改变温度或压力等方式来控制平衡位置的移动。
2. 催化剂的应用催化剂是一种可以加速化学反应速率但不参与反应的物质。
在化学平衡中,催化剂可以影响反应的正向和逆向反应速率,但对平衡位置没有直接影响。
通过使用适当的催化剂,可以实现平衡位置的控制,使反应更加高效和完全。
3. 连续流动反应器的应用连续流动反应器是一种可以实现平衡位置控制的重要装置。
通过在反应过程中连续加入反应物和移除生成物,可以使反应在更高的转化率下进行,使得平衡位置向生成物一侧移动。
化学平衡的移动

A
B
升高温度ห้องสมุดไป่ตู้平衡常数减小
0~3 s内,反应速率为:v(NO2)=0.2 mol·L-1
C
D
续表
t1时仅加入催化剂,平衡正向移动
达平衡时,仅改变x,则x为c(O2)
答案 A 由图像可知,该可逆反应的正反应为放热反应,升高温度,平
衡向逆反应方向移动,平衡常数减小,A项正确;v(NO2)= c(NtO2 ) =
根据以上规律判断,下列结论正确的是 ( ) A.反应Ⅰ:ΔH>0,p2>p1
B.反应Ⅱ:ΔH<0,T1<T2 C.反应Ⅲ:ΔH>0,T2>T1或ΔH<0,T2<T1 D.反应Ⅳ:ΔH<0,T2>T1 答案 C A项,反应Ⅰ中温度降低,A的平衡转化率升高,说明平衡向正 反应方向移动,故正反应是放热反应,ΔH<0;压强增大,平衡向正反应方 向移动,A的平衡转化率升高,故p2>p1。B项,T1时先达到平衡,说明T1>T2, 温度降低,n(C)增大,说明平衡向正反应方向移动,故正反应是放热反应, ΔH<0。C项,反应Ⅲ中,若ΔH>0,温度升高,平衡向正反应方向移动,C的 百分含量增大,则T2>T1;若ΔH<0,温度升高,平衡向逆反应方向移动,C的 百分含量减小,则T2<T1。D项,反应Ⅳ中,若T2>T1,则温度升高,A的平衡转 化率增大,说明平衡向正反应方向移动,故正反应是吸热反应,ΔH>0。
1.30
下列说法正确的是 ( )
A.m>n
B.Q<0
C.温度不变,压强增大,Y的质量分数减小
D.体积不变,温度升高,平衡向逆反应方向移动
1.00
化学选修四(化学反应原理)----化学平衡的移动

课题:化学平衡的移动基础自测化学平衡的移动1.化学平衡的移动就是改变外界条件,破坏原有的平衡状态,建立起新的平衡状态的过程。
2.图示3.平衡移动的方向(1)若v(正)>v(逆),则平衡向正反应方向移动。
(2)若v(正)=v(逆),则平衡不移动。
(3)若v(正)<v(逆),则平衡向逆反应方向移动。
[特别提醒](1)外界条件改变,平衡不一定发生移动。
①若条件改变,未引起化学反应速率的变化,则平衡一定不移动,如增加固体的用量。
①若条件改变,引起了化学反应速率的变化,但v(正)、v(逆)同等程度的改变,则平衡不发生移动。
①若条件改变,引起v(正)≠v(逆),则平衡一定发生移动。
(2)平衡发生移动,说明外界条件一定发生改变。
浓度变化对化学平衡的影响1.浓度对化学平衡的影响在其他条件不变的情况下,改变参与反应物质的浓度对化学平衡的影响:(1)增大反应物的浓度或减小生成物的浓度,使得v(正)大于v(逆),平衡向正反应方向移动。
(2)减小反应物的浓度或增大生成物的浓度,使得v(正)小于v(逆),平衡向逆反应方向移动。
2.平衡移动图像(vt图)(1)平衡正向移动(2)平衡逆向移动压强变化对化学平衡的影响1.压强改变与化学反应速率、化学平衡移动间的关系2.在其他条件不变的情况下压强对化学平衡的影响(1)增大压强,化学平衡向气体体积减小的方向移动。
(2)减小压强,化学平衡向气体体积增大的方向移动。
3.平衡移动图像(vt图)以m A(g)+n B(g)p C(g)+q D(g)为例(1)若m+n>p+q(2)若m+n<p+q(3)若m+n=p+q温度变化对化学平衡的影响1.温度对化学平衡的影响(1)在其他条件不变的情况下,升高温度,平衡向吸热的方向移动。
(2)在其他条件不变的情况下,降低温度,平衡向放热的方向移动。
2.平衡移动图像(vt图)(1)若a A+b B c C+d DΔH<0(2)若a A+b B c C+d DΔH>0催化剂与化学平衡平衡移动原理1.催化剂与化学平衡(1)催化剂对化学平衡的影响催化剂能同等程度的增大正、逆反应的速率,对化学平衡移动无影响,但能缩短达到平衡所需要的时间。
高中化学 平衡移动最全知识总结

一、化学平衡的移动1.化学平衡的移动(1)定义达到平衡状态的反应体系,条件改变,引起平衡状态被破坏的过程。
(2)化学平衡移动的过程2.影响化学平衡移动的因素(1)温度:在其他条件不变的情况下,升高温度,化学平衡向吸热反应方向移动;降低温度,化学平衡向放热反应方向移动。
(2)浓度:在其他条件不变的情况下,增大反应物浓度或减小生成物浓度,化学平衡向正反应方向移动;减小反应物浓度或增大生成物浓度,化学平衡向逆反应方向移动。
(3)压强:对于反应前后总体积发生变化的化学反应,在其他条件不变的情况下,增大压强,化学平衡向气体体积减小的方向移动;减小压强,化学平衡向气体体积增大的方向移动。
(4)催化剂:由于催化剂能同时同等程度地增大或减小正反应速率和逆反应速率,故其对化学平衡的移动无影响。
3.勒夏特列原理在密闭体系中,如果改变影响化学平衡的一个条件(如温度、压强或浓度等),平衡就向能够减弱这种改变的方向移动。
二、外界条件对化学平衡移动的影响1.外界条件的变化对速率的影响和平衡移动方向的判断在一定条件下,浓度、压强、温度、催化剂等外界因素会影响可逆反应的速率,但平衡不一定发生移动,只有当v正≠v逆时,平衡才会发生移动。
对于反应mA(g)+nB(g)pC(g)+qD(g),分析如下:2.浓度、压强和温度对平衡移动影响的几种特殊情况(1)改变固体或纯液体的量,对平衡无影响。
(2)当反应混合物中不存在气态物质时,压强的改变对平衡无影响。
(3)对于反应前后气体体积无变化的反应,如H2(g)+I2(g)2HI(g),压强的改变对平衡无影响。
但增大(或减小)压强会使各物质的浓度增大(或减小),混合气体的颜色变深(或浅)。
(4)恒容时,同等程度地改变反应混合物中各物质的浓度时,应视为压强的影响,增大(减小)浓度相当于增大(减小)压强。
(5)在恒容容器中,当改变其中一种气态物质的浓度时,必然会引起压强的改变,在判断平衡移动的方向和物质的转化率、体积分数变化时,应灵活分析浓度和压强对化学平衡的影响。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
Fe3++3SCN- Fe(SCN)3
编号 步骤(1)
现象 步骤(2)
现象 结论
1 滴加饱和FeCl3溶液
颜色加深 滴加NaOH溶液
颜色变浅
2 滴加KSCN溶液
颜色加深 滴加NaOH溶液
颜色变浅
2020/8/15
结论3:增大反应物浓度,化学平衡向正 反应方向移动。
v
0
2020/8/15
V’
V正
正
V’
思考:
对于可逆反应:
(g)
(g) H﹤0
(1)升高温度, v(正)、v(逆)均增大,但从平衡移动 方向来看, 谁增大幅度大?
(2)降低温度,谁降低的幅度大?
2020/8/15
V逆
逆
增大反应物浓度
V’正=V’
逆
t
结论4:减小反应物浓度,化学平衡向逆 反应方向移动。
v
2020/8/15
V正
V逆
V’
逆
V’正=V’
V’
逆
正
减小反应物浓度
t
总结一: 增大反应物浓度 减小生成物浓度
增大生成物浓度 减小反应物浓度
化学平衡向正反应方向 移动
化学平衡向逆反应方向 移动
(1)只要是增大浓度,不论增大的是反应物浓度 还是生成物浓度,新平衡状态下的反应速率一定 大于原平衡状态。 (2)减少浓度,新平衡条件下的速率一定小于原 平衡状态。
2020/8/15
结论1:增大生成物浓度,正逆速率均增 大,化学平衡向逆反应方向移动。
v
0
2020/8/15
V’
V正
逆
V’正=V’
V逆
V’
正
逆
t
增大生成物浓度
结论2:减小生成物浓度,化学平衡向正 反应方向移动。
v
0
2020/8/15
V正
V逆
V’
正
V’
减小生成物逆浓度
V’正=V’
逆
t
• 2.反应物浓度对化学平衡的影响
平衡状态Ⅰ 条件 改变
v(正)=v(逆)
各组分浓度一定
非平衡状态
(非平衡状态) 一段时 间后
v(正)≠v(逆)
各组分浓度
不断在变化
条件② 平衡状态Ⅱ
v`(正)=v`(逆)
各组分浓度保持
新的一定
2020/8/15
化学平衡移动方向的判断
(1)若外界条件改变,引起V(正)>V(逆), 化学平衡向正方向移动
影响化学平衡的因素
第一课时
2020/8/15
化学平衡移动:
当反应达到平衡后,正逆反应速率相 等,假如改变条件后正逆反应速率不再相 等,就要在新的条件下建立新的平衡,这 时我们就说平衡发生了移动。
2020/8/15
化学平衡的移动:
可逆反应中旧化学平衡的破坏、新化学平衡的建 立过程.
化学平衡的移动
条件①
2020/8/15
思考:
• 改变固体或纯液体的量,化学平衡会不 会发生移动?
2020/8/15
3、温度对化学平衡的影响:
NO2球实验: 将装有二氧化氮和四氧化二氮的NO2球,
一端置于冷水中,另一端置于热水中。
2020/8/15
二、温度对化学平衡的影响
结论: 在其他条件不变的情况下, 升高温度,化学平衡向吸热反应方向移动; 降低温度,化学平衡向放热反应方向移动。
(2)若外界条件改变,引起V(正)<V(逆), Fra bibliotek学平衡向逆方向移动
(3)若外界条件改变,引起V(正)=V(逆), 化学平衡不移动
2020/8/15
影响化学平衡移动的因素
• 1.生成物浓度对化学平衡的影响
Cr2O72-+H2O
橙色
2黄Cr色O42-+2H+
编号
1
2
步骤
滴加浓H2SO4
滴加NaOH
K2Cr2O7溶液 橙黄色变为橙色 橙黄色变为黄色
