醇的性质和应用 获奖课件
合集下载
醇的性质与应用 PPT课件

[问题4]下图为乙醇和氢溴酸反应的实验装置,该实验 过程中并没有直接加入氢溴酸,氢溴酸是如何获得的? 实验中可观察到试管I中的溶液由无色变橙黄色、试管II 中溶液分层,下层为无色油状液体。推测可能的原因?
[问题5]实验时为什么需要往试管I、试管II中加入少量 蒸馏水?及烧杯中注入的自来水有何作用?设计实验证 明该实验过程中有溴乙烷生成?
有机化学基础
专题4、烃的衍生物
第二单元 醇 酚 第一部分、醇的性质和应用
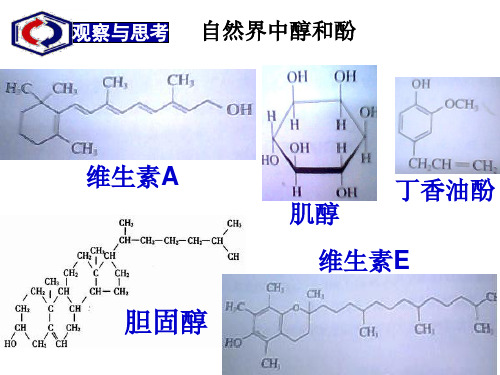
[问题1]分别写出胆固醇、维生素A、丁香油酚三种有 机化合物的分子式以及结构中具有的官能团名称?
[问题2]三只烧杯中分别加入乙醚、无水乙醇、水,从 煤油中取出一块金属钠,切去表层后分成三等份,分别 放入三只烧杯中,观察现象?推测乙醚、乙醇、水中氢 原子的活泼性强弱?实验中产生的气体成分?如何证明?
反应物
反应条件
Na
不需要
与O2催化氧化 Cu或Ag、加热 CH3COOH 浓硫酸、加热
HX
加热
脱水
浓硫酸、1400C
反应
浓硫酸、1700C
反应类型
断键方式
[问题11]饱和一元醇的通式?写出最简单的饱和一元 醇的分子式?阅读教材第70页了解这种物质性质?
[问题12]阅读教材第71页了解根据醇羟基的分类方式, 并了解几种常见的多元醇的物理性质。
[问题6]在下列试管中将乙醇和浓硫酸混合后,加热至 1400C可生成乙醚,试写出反应的化学方程式,判断 该反应的反应类型,分析反应中可能的断键方式?
[问题7]若将乙醇与浓硫酸混合液加热至1700C,可观 察到KMnO4溶液最终完全褪色,若证实使溶液褪色的 是乙烯气体,写出反应的方程式,反应类型?分析反 应中可能的断键方式?
《醇的性质与应用》课件

醇中的互变异构
不含双键的单一醇分子 会出现结构互变,分子 中的氢原子可以在醇分 子的羟基之间移动,形 成不同的同分异构体。
醇的物理性质
1
溶解性
由于醇分子中含有羟基,与水分子
密度和熔点
2
之间有氢键作用,因此醇在水中非 常容易溶解。
较短的醇一般是无色液体,密度比
水轻,而较长的醇则为无色固体。
3
沸点
随着碳链长度的增加,醇的沸点也
黏度
4
逐渐升高。
由于醇分子间有氢键作用,因此醇 的黏度通常比烃类高,黏稠度也相
应增加。
醇的应用领域
消毒剂
醇常用于口腔消毒、医疗器械和生活用品消毒 等领域。
燃料和能源
乙醇是一种重要的替代燃料,可以替代剂等都是 以醇为原料制造的。
饮品工业
醇是酒精饮料的重要成分,如啤酒、葡萄酒等。
醇的生产方法
合成法
不同的醇可以通过醇醚 法、加氢还原法、合成 气法等多种方法生产。
自然法
一些天然植物和动物中 也含有少量的醇,如蜂 蜜中的甘油、水果中的 乙醇等。
蒸馏法
蒸馏是最基本的分离纯 化方法之一,可以用于 提取和纯化醇。
醇的安全使用注意事项
1 易燃易爆
醇是易燃易爆的化合物,携带、储存和使用过程中要非常小心。
是一种无色黏稠液体,在化妆品、香水、口香 糖和食品等众多领域有着广泛用途。
苯酚
是一种无色晶体,在合成树脂、染料、农药和 香料等方面有着广泛应用。
醇的化学性质
醇对酸的反应
当醇与酸反应时,醇分 子中的氢离子被酸分子 中的阴离子取代,生成 酯和水。
醇对卤素的反应
在醇的存在下,卤素可 以通过亲电取代反应与 醇发生反应,生成卤代 烷和水。
苏教版高中化学选修5《醇的性质和应用》名师课件

实验步骤:
1. 铜片弄成四周稍高,至于三脚架上, 用酒精灯持续加热; 2. 当铜片红热时,用胶头滴管滴一滴 无水乙醇,观察现象,待烧干再滴一 滴乙醇,观察现象。
2CH3CH2OH+O2
Cu △
2CH3CHO+H2O
有机化学中的氧化还原反应
氧化反应:有机物分子中加入氧原子或失去氢原子 还原反应:有机物分子中加入氢原子或失去氧原子
CH3CH2OH 氧化 CH3CHO 氧化 CH3COOH
乙醇
乙醛
乙酸
问题讨论
下列醇不能被铜催化氧化的是 ;能被催化氧
化为醛的是
。
A.CH3OH C.CH3CHCH3
OH
B. CH3CH2CH2OH D. OH
CH3CCH3
CH3
Q4:酒喝多了会醉酒,警察如何检验酒驾?
实验步骤:
往左侧的重铬酸 钾溶液中滴加 2ml无水乙醇, 振荡,再滴加 1ml稀硫酸,观 察现象。
往右侧的酸性高 锰酸钾溶液中滴 加2ml无水乙醇, 振荡,加热,观 察现象。
2K2Cr2O7 + 3C2H5OH+8H2SO4 → 2Cr2(SO4)3 +3CH3COOH +2K2SO4+11H2O (绿色)
5C2H5OH+4KMnO4+6H2SO4→5CH3COOH+4MnSO4+2K2SO4+11H2O 无色
清《中除药血大中辞毒典素》,亦对说受葛花损“的解肝酒脏醒细脾,胞治起伤修酒复发营热养烦的渴作,不用思。饮研食究,发欧现逆,吐灵酸,芝吐能血帮,助肠 人凤葛花下体中血快的”速皂。分角苷解(出gan乙),醇异脱黄氢酮类酶具和有乙氧醛化还脱原氢作酶用,,加可速以酒快精速氧分化解,人可使体乙内醇的失酒去精毒。性,
部分专题4第二单元第一课时醇的性质和应用PPT课件

返回
1.下列说法不. 正确的是
()
A.乙醇分子中有1/6的氢原子与其他氢原子不一样
B.乙醇分子可认为是乙烷分子中的一个氢原子被一
个羟基取代产生的
C.乙醇分子中的每个碳原子都形成了四个键,但显
示的化合价不是+4价
D.乙醇的相对分子质量为46,相对分子质量为46的
就是乙醇
返回
解析:A.羟基上的一个氢原子与氧原子相连,其他氢原子 与碳原子相连;B.CH3—CH3去掉一个氢原子,换上—OH 便是CH3—CH2—OH;C.化合价与共用电子对的偏向有关, 乙醇分子中的二个碳原子都不是有四对共用电子对偏向的 原子;D.CH3—O—CH3的相对分子质量也是46。 答案:D
2.醇与钠反应生成醇钠与氢气,醇与卤化氢(HX)反 应生成卤代烃,醇可发生消去反应,一些醇可氧化生成相 应的醛或酮。乙醇在浓硫酸、170℃时生成乙烯,在140℃ 时生成乙醚。
返回
3.甲醇有剧毒,饮用少量可使眼睛失明,大量 使人死亡。
4.乙二醇可作为汽车发动机的抗冻剂,丙三醇具 有吸湿性,有护肤作用,是重要的化工原料。
返回
1.乙醇与钠反应生成H2 化学方程式为: 2CH3CH2OH+2Na―→2CH3CH2ONa+H2↑ 。 2.乙醇与氢卤酸发生取代反应 化学方程式为: CH3CH2OH+HBr―△―→CH3CH2Br+H2O 。
返回
3.乙醇的脱水反应 (1)分子内脱水(消去反应),化学方程式为: CH3CH2OH―浓―1H7―02S℃―O→4 CH2===CH2↑+H2O 。 (2)分子间脱水(取代反应),化学方程式为: 2CH3CH2O―浓―1H4―02S℃―O→4 CH3CH2—O—CH2CH3+H2O 。
返回
(3)丙三醇(甘油)结构简式: CH2OHCHOHCH2OH , 无色黏稠有 甜 味的液体,吸湿性强,它跟水、乙醇以任意比 例互溶,甘油水溶液的凝固点很低,用于制造硝化甘油。
1.下列说法不. 正确的是
()
A.乙醇分子中有1/6的氢原子与其他氢原子不一样
B.乙醇分子可认为是乙烷分子中的一个氢原子被一
个羟基取代产生的
C.乙醇分子中的每个碳原子都形成了四个键,但显
示的化合价不是+4价
D.乙醇的相对分子质量为46,相对分子质量为46的
就是乙醇
返回
解析:A.羟基上的一个氢原子与氧原子相连,其他氢原子 与碳原子相连;B.CH3—CH3去掉一个氢原子,换上—OH 便是CH3—CH2—OH;C.化合价与共用电子对的偏向有关, 乙醇分子中的二个碳原子都不是有四对共用电子对偏向的 原子;D.CH3—O—CH3的相对分子质量也是46。 答案:D
2.醇与钠反应生成醇钠与氢气,醇与卤化氢(HX)反 应生成卤代烃,醇可发生消去反应,一些醇可氧化生成相 应的醛或酮。乙醇在浓硫酸、170℃时生成乙烯,在140℃ 时生成乙醚。
返回
3.甲醇有剧毒,饮用少量可使眼睛失明,大量 使人死亡。
4.乙二醇可作为汽车发动机的抗冻剂,丙三醇具 有吸湿性,有护肤作用,是重要的化工原料。
返回
1.乙醇与钠反应生成H2 化学方程式为: 2CH3CH2OH+2Na―→2CH3CH2ONa+H2↑ 。 2.乙醇与氢卤酸发生取代反应 化学方程式为: CH3CH2OH+HBr―△―→CH3CH2Br+H2O 。
返回
3.乙醇的脱水反应 (1)分子内脱水(消去反应),化学方程式为: CH3CH2OH―浓―1H7―02S℃―O→4 CH2===CH2↑+H2O 。 (2)分子间脱水(取代反应),化学方程式为: 2CH3CH2O―浓―1H4―02S℃―O→4 CH3CH2—O—CH2CH3+H2O 。
返回
(3)丙三醇(甘油)结构简式: CH2OHCHOHCH2OH , 无色黏稠有 甜 味的液体,吸湿性强,它跟水、乙醇以任意比 例互溶,甘油水溶液的凝固点很低,用于制造硝化甘油。
高中化学苏教版选修五4-2-1 醇的性质和应用 课件(共44张PPT)

(2)注意事项 应先加 P2O5, 后加 95%乙醇溶液, 由于 P2O5 具有强烈吸水性, 产生大量白雾。
2.利用浓硫酸作催化剂 (1)实验装置
(2)注意事项 ①配制体积比为 1∶3 的乙醇与浓硫酸混合液时,要注意在烧 杯中先加入 95%乙醇,然后滴加浓硫酸,边滴加边搅拌,冷却 备用(相当于浓硫酸的稀释),浓硫酸起催化剂和脱水剂的作用。 ②加热混合液时,温度要迅速上升到并稳定于 170 ℃左右,因 为在 140 ℃时主要产物是乙醚。 ③由于反应物都是液体而无固体,所以要向烧瓶中加入碎瓷 片,以防液体受热时发生暴沸。 ④温度计的水银球要置于反应液的中央位置,因为需要测量的 是反应液的温度。
第二单元
醇
酚
第1课时 醇的性质和应用
1.写出溴乙烷在碱性条件下水解的化学方程式。 提示 H2 O CH3CH2Br+NaOH― ― → CH3CH2OH+NaBr。 △
2.通过必修模块的学习,你了解乙醇具有哪些性质? 提示 乙醇能发生催化氧化反应、能与活泼金属反应。
1.掌握乙醇的结构和性质。 2.掌握实验室由乙醇制乙烯的反应原理和实验方法。 3.了解醇类的官能团、结构特点、一般通性和几种典型醇的 用途。
(2)脱水反应 乙醇在浓硫酸的作用下加热到 170 ℃ 时,反应的化学方程式 浓硫酸 为 CH3CH2OH― ― ― ― ― →CH2==CH2↑+H2O,浓硫酸 170 ℃ 作 催化剂、脱水剂 。
(3)取代反应 ①乙醇与浓氢溴酸混合加热生成溴乙烷的化学方程式为 △ CH3CH2OH+HBr― ― →CH3CH2Br+H2O。 一般情况下,醇比较容易获得,卤代烷常用醇与 氢卤酸 反应 制得。
②酯化反应 乙醇与乙酸发生酯化反应的化学方程式为
浓硫酸作 催化剂、吸水剂 。 ③分子间脱水成醚 浓硫酸 2CH3CH2OH― ― ― ― ― →CH3CH2OCH2CH3+H2O。 140 ℃
化学课件《醇的性质和应用》优秀ppt 苏教版

97.有三个人是我的朋友爱我的人.恨我的人.以及对我冷漠的人。 爱我的人教我温柔;恨我的人教我谨慎;对我冷漠的人教我自立。――[J·E·丁格] 98.过去的事已经一去不复返。聪明的人是考虑现在和未来,根本无暇去想过去的事。――[英国哲学家培根] 99.真正的发现之旅不只是为了寻找全新的景色,也为了拥有全新的眼光。――[马塞尔·普劳斯特] 100.这个世界总是充满美好的事物,然而能看到这些美好事物的人,事实上是少之又少。――[罗丹] 101.称赞不但对人的感情,而且对人的理智也发生巨大的作用,在这种令人愉快的影响之下,我觉得更加聪明了,各种想法,以异常的速度接连涌入我的脑际。――[托尔斯泰] 102.人生过程的景观一直在变化,向前跨进,就看到与初始不同的景观,再上前去,又是另一番新的气候――。[叔本华] 103.为何我们如此汲汲于名利,如果一个人和他的同伴保持不一样的速度,或许他耳中听到的是不同的旋律,让他随他所听到的旋律走,无论快慢或远近。――[梭罗] 104.我们最容易不吝惜的是时间,而我们应该最担心的也是时间;因为没有时间的话,我们在世界上什么也不能做。――[威廉·彭] 105.人类的悲剧,就是想延长自己的寿命。我们往往只憧憬地平线那端的神奇【违禁词,被屏蔽】,而忘了去欣赏今天窗外正在盛开的玫瑰花。――[戴尔·卡内基] 106.休息并非无所事事,夏日炎炎时躺在树底下的草地,听着潺潺的水声,看着飘过的白云,亦非浪费时间。――[约翰·罗伯克] 107.没有人会只因年龄而衰老,我们是因放弃我们的理想而衰老。年龄会使皮肤老化,而放弃热情却会使灵魂老化。――[撒母耳·厄尔曼] 108.快乐和智能的区别在于:自认最快乐的人实际上就是最快乐的,但自认为最明智的人一般而言却是最愚蠢的。――[卡雷贝·C·科尔顿] 109.每个人皆有连自己都不清楚的潜在能力。无论是谁,在千钧一发之际,往往能轻易解决从前认为极不可能解决的事。――[戴尔·卡内基] 110.每天安静地坐十五分钟·倾听你的气息,感觉它,感觉你自己,并且试着什么都不想。――[艾瑞克·佛洛姆] 111.你知道何谓沮丧---就是你用一辈子工夫,在公司或任何领域里往上攀爬,却在抵达最高处的同时,发现自己爬错了墙头。--[坎伯] 112.「伟大」这个名词未必非出现在规模很大的事情不可;生活中微小之处,照样可以伟大。――[布鲁克斯] 113.人生的目的有二:先是获得你想要的;然后是享受你所获得的。只有最明智的人类做到第二点。――[罗根·皮沙尔·史密斯] 114.要经常听.时常想.时时学习,才是真正的生活方式。对任何事既不抱希望,也不肯学习的人,没有生存的资格。
《醇的性质和应用》课件

储存醇类物质时应远离火源和热 源,使用防爆电气设备,并配备 灭火器材。
个人防护措施
1 2
佩戴防护服
在处理醇类物质时,应穿戴化学防护眼镜、化学 防护服和化学防护手套。
通风
保持良好的通风条件,以降低醇蒸汽在空气中的 浓度。
3
使用个人防护器材
根据需要选择合适的个人防护器材,如呼吸器、 护目镜等。
THANK YOU
溶剂
醇可用作有机合成中的溶剂,用于溶解和提取各种物质。
化学原料
醇可用于合成多种化学品,如酯类、醚类、醛类等。
食品和饮料
01
02
03
调味料
某些醇具有特殊的风味, 可作为食品和饮料的调味 料。
香料
醇是许多香精和香料的主 要成分,用于增加食品和 饮料的香气。
防腐剂
某些醇具有抗菌和防腐作 用,可用于延长食品的保 质期。
03
醇的化学性质
氧化反应
叔醇可以被氧化生成羧酸 。
氧化生成羧酸
仲醇可以被氧化生成醛。
在催化剂的作用下,伯醇 可以被氧化生成酮。
氧化生成醛 氧化生成酮
酯化反应
与羧酸反应
醇可以与羧酸反应生成酯和 水。
与羧酸酐反应
醇可以与羧酸酐反应生成酯 和水。
与酰氯反应
醇可以与酰氯反应生成酯和 氯化氢。
取代反应
醇的毒性主要与其代谢产物和干 扰细胞代谢有关,长期接触高浓 度醇可能导致肝肾损伤、神经元 死亡等。
毒性症状
接触醇后可能出现头痛、恶心、 呕吐、腹痛、乏力等症状,严重 时可能导致昏迷或死亡。
防火和防爆
01
燃烧特性
醇类物质是易燃的,其闪点较低 ,一般在21℃以下。
爆炸条件
醇的性质和应用4(课件PPT)

和100mL乙醚,再分别向三支试管中放入一小块金属 钠,观察实验现象
用上面的方案可判断出乙醇与钠反应中乙醇分子中 断裂的是氧氢键,而不是碳氢键,其原理是什么?
2CH3CH2 O H+2Na→2CH3CH2ONa+H2↑
煤油
H—O—H
钠沉在底部、有气泡冒出
浮、熔、游、有“嘶嘶” 声
无明显现象
结论:
乙醇与钠反应时,乙醇分子中氧氢键断裂
课堂练习
1.写出下列反应的化学方程式
(1)乙醇与金属钾的反应
(2)
与金属钠的反应
(3)2-丙醇与HCl的反应
【课堂练习】
2.A、B、C三种醇同足量的金属钠完全反 应,在相同的条件下,产生相同体积的氢气, 消耗这三种醇的物质的量之比为2:6:3 ,则A、
B、C三种醇分子里羟基数之比是( B )
A.3:2:1 B.3:1:2 C.2:1:3 D.2:6:3
3.已知一氯戊烷有8种同分异构体,可推知戊
醇(属醇类)的同分异构体的数目是( D )
A.5种 B.6种 C.7种 D.8种
4、教学必须从学习者已有的经验开始。——杜威 5、构成我们学习最大障碍的是已知的东西,而不是未知的东西。——贝尔纳 6、学习要注意到细处,不是粗枝大叶的,这样可以逐步学习摸索,找到客观规律。——徐特立 7、学习文学而懒于记诵是不成的,特别是诗。一个高中文科的学生,与其囫囵吞枣或走马观花地读十部诗集,不如仔仔细细地背诵三百首诗。——朱自清 8、一般青年的任务,尤其是共产主义青年团及其他一切组织的任务,可以用一句话来表示,就是要学习。——列宁 9、学习和研究好比爬梯子,要一步一步地往上爬,企图一脚跨上四五步,平地登天,那就必须会摔跤了。——华罗庚 10、儿童的心灵是敏感的,它是为着接受一切好的东西而敞开的。如果教师诱导儿童学习好榜样,鼓励仿效一切好的行为,那末,儿童身上的所有缺点就会没有痛苦和创伤地不觉得难受地逐渐消失。——苏霍姆林斯基
用上面的方案可判断出乙醇与钠反应中乙醇分子中 断裂的是氧氢键,而不是碳氢键,其原理是什么?
2CH3CH2 O H+2Na→2CH3CH2ONa+H2↑
煤油
H—O—H
钠沉在底部、有气泡冒出
浮、熔、游、有“嘶嘶” 声
无明显现象
结论:
乙醇与钠反应时,乙醇分子中氧氢键断裂
课堂练习
1.写出下列反应的化学方程式
(1)乙醇与金属钾的反应
(2)
与金属钠的反应
(3)2-丙醇与HCl的反应
【课堂练习】
2.A、B、C三种醇同足量的金属钠完全反 应,在相同的条件下,产生相同体积的氢气, 消耗这三种醇的物质的量之比为2:6:3 ,则A、
B、C三种醇分子里羟基数之比是( B )
A.3:2:1 B.3:1:2 C.2:1:3 D.2:6:3
3.已知一氯戊烷有8种同分异构体,可推知戊
醇(属醇类)的同分异构体的数目是( D )
A.5种 B.6种 C.7种 D.8种
4、教学必须从学习者已有的经验开始。——杜威 5、构成我们学习最大障碍的是已知的东西,而不是未知的东西。——贝尔纳 6、学习要注意到细处,不是粗枝大叶的,这样可以逐步学习摸索,找到客观规律。——徐特立 7、学习文学而懒于记诵是不成的,特别是诗。一个高中文科的学生,与其囫囵吞枣或走马观花地读十部诗集,不如仔仔细细地背诵三百首诗。——朱自清 8、一般青年的任务,尤其是共产主义青年团及其他一切组织的任务,可以用一句话来表示,就是要学习。——列宁 9、学习和研究好比爬梯子,要一步一步地往上爬,企图一脚跨上四五步,平地登天,那就必须会摔跤了。——华罗庚 10、儿童的心灵是敏感的,它是为着接受一切好的东西而敞开的。如果教师诱导儿童学习好榜样,鼓励仿效一切好的行为,那末,儿童身上的所有缺点就会没有痛苦和创伤地不觉得难受地逐渐消失。——苏霍姆林斯基
醇的性质和应用上课ppt课件
饱和一元醇通式:
CnH2n+1OH或 CnH2n+2O
阅读教材第71页有关甲醇、乙二醇 和丙三醇的介绍,总结三种醇的 物理性质和常见用途。
认识到了贫困户贫困的根本原因,才 能开始 对症下 药,然 后药到 病除。 近年来 国家对 扶贫工 作高度 重视, 已经展 开了“ 精准扶 贫”项 目
新
知
可上网查看相 关危害新闻哦!
思考
⑴如何区分乙醇溶液和无水乙醇?
取少量酒精,加入无水硫酸铜, 若出现蓝色,则证明是工业酒精.
⑵如何实现由乙醇溶液向无水乙醇转化?
乙醇溶液 加CaO生成Ca(OH)2 无水乙醇
(96%)
蒸馏
(99.5%)
认识到了贫困户贫困的根本原因,才 能开始 对症下 药,然 后药到 病除。 近年来 国家对 扶贫工 作高度 重视, 已经展 开了“ 精准扶 贫”项 目
3CH3CH2OH+2K2Cr2O7+8H2SO4→
(橙红色)
3CH3COOH+2Cr2(SO4)3+2K2SO4+11H2O
(绿色)
= =
认识到了贫困户贫困的根本原因,才 能开始 对症下 药,然 后药到 病除。 近年来 国家对 扶贫工 作高度 重视, 已经展 开了“ 精准扶 贫”项 目
知识拓展
(1). 2R—CH2—OH + O2
认识乙醇与氢卤酸的反应。
1.组装如图所示装置。在试管I中依 次加入2 mL蒸馏水、4 mL浓硫酸、 2 mL 95%的乙醇和3 g 溴化钠粉末, 在试管II中注入蒸馏水,烧杯中注入 自来水。加热试管I至微沸状态数分 钟后,冷却,观察并描述实验现象。
2.在该反应中,采用蒸馏水、浓硫 酸和溴化钠固体的目的是获得与乙 醇作用的氢溴酸。根据上述实验现 象,你能判断出乙醇与氢溴酸反应 的产物吗?请设计实验证明试管II中 收集到的是卤代烃吗?
《醇的性质与应用》公开课课件

日化产品
化妆品
醇类化合物常用于化妆品中,如保湿霜、香水 等。
清洁剂
醇类化合物可用作清洁剂的成分,如洗手液、 洗洁精等。
口腔护理
某些醇类具有抗菌作用,可用于口腔护理产品,如漱口水、牙膏等。
05 醇的安全与防护
醇的毒性
醇的毒性分类
根据醇的毒性,可以分为低毒、中毒和高毒 三类。
毒性作用机制
醇的毒性作用机制主要与其代谢产物和影响 细胞代谢有关。
01
根据烃基的不同,醇可以分为脂肪醇和芳香醇。
02
根据醇分子中羟基的数目,可以分为一元醇、二元 醇和多元醇。
03
根据醇的来源,可以分为天然醇和合成醇。
醇的结构与性质
01
醇的结构特点是含有羟基,这使得醇具有一些独特的
性质,如亲水性、能与水形成氢键等。
02
醇的化学性质主要包括取代反应、氧化反应和酯化反
感谢您的观看
03
醇可以与酰氯反应生成酯。
脱水反应
1 2
分子内脱水
醇在一定条件下可以发生分子内脱水,生成烯烃。
分子间脱水
醇在一定条件下可以发生分子间脱水,生成醚。
3
氧化脱水
醇在一定条件下可以发生氧化脱水,生成醛或酮。
04 醇的应用
工业生产
燃料添加剂
醇可作为燃料添加剂,提高燃料的燃烧效率,减少污染物排放。
溶剂
影响因素
除了碳原子数,醇在水中的溶解度还受到其他因素的影响,如羟基的数目、温度等。一般来说,羟基数目越多, 溶解度越大;温度越高,溶解度越大。
03 醇的化学性质
酸性
酸性较弱
醇的酸性较弱,其电离常数通常在10^-10至10^-13 之间,远弱于水。
醇的性质与应用课件

醇的沸点通常在60-150°C之间,随着碳原子数的增加而升高。一元醇的沸点 随着碳原子数的增加而逐渐升高,但碳原子数相同时,支链越多,沸点越低。
影响因素
醇的沸点主要受分子间作用力和分子内氢键的影响。分子间作用力越大,沸点 越高;分子内氢键的存在也会增加沸点。
熔点
熔点范围
醇的熔点一般在-78°C至100°C之 间。一元醇的熔点随着碳原子数 的增加而升高,碳原子数相同的 情况下,支链越多,熔点越低。
溶解度
溶解度范围
醇在水中的溶解度通常较大,但在有机溶剂中的溶解度较小。一元醇的溶解度随 着碳原子数的增加而减小。
影响因素
溶解度主要受分子极性和溶剂性质的影响。极性溶剂对极性物质的溶解度较大, 非极性溶剂对非极性物质的溶解度较大。
03 醇的化学性质
醇的氧化
氧化生成酮
氧化生成醛
氧化生成羧酸
氧化生成酯
燃料
某些醇类化合物如乙醇可作为燃料, 用于替代传统的化石燃料,减少环境 污染。
食品添加 剂
01
02
03
调味
醇类化合物具有芳香味道, 常被用作食品添加剂,如 香精、香料等,增加食品 的口感和香味。
防腐
某些醇类化合物具有抗菌、 防腐作用,如丙二醇、山 梨醇等,可用于食品保鲜 和防腐。
营养强化
乙醇可以作为维生素和矿 物质的载体,用于食品营 养强化,提高食品的营养 价值。
醇的卤化
直接卤化
醇与卤素或卤化氢发生直接卤化反应, 生成卤代烃。
间接卤化
醇先进行氧化或酯化等反应,再与卤 素或卤化氢发生卤化反应,生成卤代 烃。
04 醇的应用
工业生产
溶剂
化工原料
醇类化合物由于其良好的溶解性能, 常被用作工业生产的溶剂,如甲醇、 乙醇等。
影响因素
醇的沸点主要受分子间作用力和分子内氢键的影响。分子间作用力越大,沸点 越高;分子内氢键的存在也会增加沸点。
熔点
熔点范围
醇的熔点一般在-78°C至100°C之 间。一元醇的熔点随着碳原子数 的增加而升高,碳原子数相同的 情况下,支链越多,熔点越低。
溶解度
溶解度范围
醇在水中的溶解度通常较大,但在有机溶剂中的溶解度较小。一元醇的溶解度随 着碳原子数的增加而减小。
影响因素
溶解度主要受分子极性和溶剂性质的影响。极性溶剂对极性物质的溶解度较大, 非极性溶剂对非极性物质的溶解度较大。
03 醇的化学性质
醇的氧化
氧化生成酮
氧化生成醛
氧化生成羧酸
氧化生成酯
燃料
某些醇类化合物如乙醇可作为燃料, 用于替代传统的化石燃料,减少环境 污染。
食品添加 剂
01
02
03
调味
醇类化合物具有芳香味道, 常被用作食品添加剂,如 香精、香料等,增加食品 的口感和香味。
防腐
某些醇类化合物具有抗菌、 防腐作用,如丙二醇、山 梨醇等,可用于食品保鲜 和防腐。
营养强化
乙醇可以作为维生素和矿 物质的载体,用于食品营 养强化,提高食品的营养 价值。
醇的卤化
直接卤化
醇与卤素或卤化氢发生直接卤化反应, 生成卤代烃。
间接卤化
醇先进行氧化或酯化等反应,再与卤 素或卤化氢发生卤化反应,生成卤代 烃。
04 醇的应用
工业生产
溶剂
化工原料
醇类化合物由于其良好的溶解性能, 常被用作工业生产的溶剂,如甲醇、 乙醇等。
醇的性质与应用课件

储存与运输。
在储存与运输过程中,应建立完 善的安全管理制度和应急预案, 以应对可能发生的事故和危险情
况。
06
CATALOGUE
醇的发展趋势与展望
醇的应用前景展望
01
醇在化工、医药、食品、能源 等领域的应用越来越广泛,随 着科技的进步,醇的应用前景 将更加广阔。
02
随着环保意识的提高,醇作为 可再生能源的代表,未来在替 代传统化石能源方面将发挥重 要作用。
醇的实验室制备方法
酯水解法
01
酯类物质在酸性或碱性条件下水解生成醇。
卤代烃水解法
02
卤代烃与碱反应生成醇。
烷基化反应
03
芳烃与卤代烷在催化剂作用下生成醇。
醇的生产安全与环保
安全措施
生产过程中应采取必要的安全措 施,如穿戴防护服、定期检查设 备等,以防止事故发生。
环保要求
醇的生产过程中会产生废气、废 水等污染物,应采取有效的环保 措施,如处理废水、回收废气等 ,以减少对环境的污染。
药物合成
醇是许多药物合成的中间体或原料,如抗生素、镇痛药等。
药用辅料
某些醇类物质可作为药用辅料,如甘油常用于制作栓剂、软膏等 。
生物活性分子
某些醇类物质具有生物活性,如多酚类化合物具有抗氧化、抗炎 等作用。
醇在化学工业中的应用
1 2
有机合成
醇是许多有机合成反应ຫໍສະໝຸດ 中间体或原料,如酯化 反应、氧化反应等。
醇的通式为R-OH, 其中R代表烃基。
醇的分类
一元醇
多元醇
只有一个羟基的醇,如乙醇、甲醇等 。
含有多个羟基的醇,如甘油、葡萄糖 等。
二元醇
含有两个羟基的醇,如乙二醇、丙二 醇等。
在储存与运输过程中,应建立完 善的安全管理制度和应急预案, 以应对可能发生的事故和危险情
况。
06
CATALOGUE
醇的发展趋势与展望
醇的应用前景展望
01
醇在化工、医药、食品、能源 等领域的应用越来越广泛,随 着科技的进步,醇的应用前景 将更加广阔。
02
随着环保意识的提高,醇作为 可再生能源的代表,未来在替 代传统化石能源方面将发挥重 要作用。
醇的实验室制备方法
酯水解法
01
酯类物质在酸性或碱性条件下水解生成醇。
卤代烃水解法
02
卤代烃与碱反应生成醇。
烷基化反应
03
芳烃与卤代烷在催化剂作用下生成醇。
醇的生产安全与环保
安全措施
生产过程中应采取必要的安全措 施,如穿戴防护服、定期检查设 备等,以防止事故发生。
环保要求
醇的生产过程中会产生废气、废 水等污染物,应采取有效的环保 措施,如处理废水、回收废气等 ,以减少对环境的污染。
药物合成
醇是许多药物合成的中间体或原料,如抗生素、镇痛药等。
药用辅料
某些醇类物质可作为药用辅料,如甘油常用于制作栓剂、软膏等 。
生物活性分子
某些醇类物质具有生物活性,如多酚类化合物具有抗氧化、抗炎 等作用。
醇在化学工业中的应用
1 2
有机合成
醇是许多有机合成反应ຫໍສະໝຸດ 中间体或原料,如酯化 反应、氧化反应等。
醇的通式为R-OH, 其中R代表烃基。
醇的分类
一元醇
多元醇
只有一个羟基的醇,如乙醇、甲醇等 。
含有多个羟基的醇,如甘油、葡萄糖 等。
二元醇
含有两个羟基的醇,如乙二醇、丙二 醇等。
化学课件《醇的性质与应用》优秀ppt 苏教版30页PPT

45、自己的饭量自己知道。——苏联
41、学问是异常珍贵的东西,从任何源泉吸 收都不可耻。——阿卜·日·法拉兹
42、只有在人群中间,才能认识自 己。——德国
43、重复别人所说的话,只需要教育; 而要挑战别人所说的话,则需要头脑。—— 玛丽·佩蒂博恩·普尔
44、卓越的人一大优点是:在不利与艰 难的遭遇里百折不饶。——贝多芬
化学课件《醇的性质与应用》 优秀pp 苏教版26、机遇对于有准备的头脑有特别的 亲和力 。 27、自信是人格的核心。
28、目标的坚定是性格中最必要的力 量泉源 之一, 也是成 功的利 器之一 。没有 它,天 才也会 在矛盾 无定的 迷径中 ,徒劳 无功。- -查士 德斐尔 爵士。 29、困难就是机遇。--温斯顿.丘吉 尔。 30、我奋斗,所以我快乐。--格林斯 潘。
41、学问是异常珍贵的东西,从任何源泉吸 收都不可耻。——阿卜·日·法拉兹
42、只有在人群中间,才能认识自 己。——德国
43、重复别人所说的话,只需要教育; 而要挑战别人所说的话,则需要头脑。—— 玛丽·佩蒂博恩·普尔
44、卓越的人一大优点是:在不利与艰 难的遭遇里百折不饶。——贝多芬
化学课件《醇的性质与应用》 优秀pp 苏教版26、机遇对于有准备的头脑有特别的 亲和力 。 27、自信是人格的核心。
28、目标的坚定是性格中最必要的力 量泉源 之一, 也是成 功的利 器之一 。没有 它,天 才也会 在矛盾 无定的 迷径中 ,徒劳 无功。- -查士 德斐尔 爵士。 29、困难就是机遇。--温斯顿.丘吉 尔。 30、我奋斗,所以我快乐。--格林斯 潘。
醇的性质和应用--上课41页PPT

谢谢!
61、奢侈是舒适的,否则就不是奢侈 。——CocoCha nel 62、少而好学,如日出之阳;壮而好学 ,如日 中之光 ;志而 好学, 如炳烛 之光。 ——刘 向 63、三军可夺帅也,匹夫不可夺志也。 ——孔 丘 64、人生就是学校。在那里,与其说好 的教师 是幸福 ,不如 说好的 教师是 不幸。 ——海 贝尔 65、接受挑战,就可以享受胜利的喜悦 。—法而稳定的权力在使用得当时很 少遇到 抵抗。 ——塞 ·约翰 逊 2、权力会使人渐渐失去温厚善良的美 德。— —伯克
3、最大限度地行使权力总是令人反感 ;权力 不易确 定之处 始终存 在着危 险。— —塞·约翰逊 4、权力会奴化一切。——塔西佗
5、虽然权力是一头固执的熊,可是金 子可以 拉着它 的鼻子 走。— —莎士 比
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
橙色
绿色
实验探究:乙醇与钠反应
实 验 步 骤
钠的保存方法
实 验 现 象
少量钠保存在煤油里
1、向两个小烧杯中各加入 约适量的水、无水乙醇;
钠+水
钠+乙醇
沉在底部, 浮、熔、 2、向上述两种试剂中分别 游、响 表面有气泡产生 不发出响声 投入米粒大小的金属钠 不熔化成小球
2C2H5OH+2Na
2C2H5ONa+H2
思考:
1.为什么实验中的硫酸不能使用98%的浓硫酸,而 用蒸馏水稀释过的浓硫酸? 98%的浓硫酸具有强氧化性,而HBr有还原性, 会发生副反应生成溴单质。 2.长导管、试管II和烧杯中的水起到了什么作用? 对溴乙烷起到冷凝作用,试管II中的水还可以除 去溴乙烷中的乙醇。
乙醇的化学性质
实验探究五 乙醇的消去反应
①催化剂:加快化学反应速率
②吸水剂:吸收生成的水分,增大反应进行的程度
7. 加热的目的: ①加快反应速率;②及时将产物乙酸乙酯蒸出,以 利于平衡向生成乙酸乙酯的方向移动
8.为什么不能将导管插到液面下?
防止发生倒吸
酯化反应的反应机理 同位素示踪法
O CH3—C—OH+H—O—C2H5 a、 O
浓H2SO4 18 浓H2SO4
脂环醇 脂环醇
芳香醇
CH2OH OH
2
2
乙醇的化学性质
实验探究六 酒为什么越陈越香?
1、在试管中先加入3mL乙醇,再慢慢加入2mL浓硫酸,摇动试管混合均 匀,用手感觉温度变化。 2、再加入2mL冰醋酸,如图连好装置。接上导管到3mL饱和碳酸钠的液 面上(不接触液面)。
3、用酒精灯小心加热,观察现象。
世界卫生组织的 事故调查显示, 大约50%-60%的交 通事故与酒后驾 驶有关。
③与强氧化剂反应
资料卡片 酸性高锰酸钾或
交通警察检查司机是否 重铬酸钾溶液等 酒后驾车的装置中,含有橙色 CH3COOH CH3CH2OH 的酸性重铬酸钾,当其遇到乙 C2H5OH 醇时橙色变为绿色,由此可以 K2Cr2判断司机是否酒后驾车。 O7 Cr2(SO4)3
O CH3—C—O—C2H5 + H2O O
18
CH3—C—OH+H—O—C2H5
b、 O CH3—C—O—H+HO—C2H5
CH3—C—O—C2H5 + H2O
O CH3—C—O—C2H5 + H2O
浓H2SO4
反应机理: 酸去羟基 醇去氢
酯化反应属于哪一类型有机反应类型?
O CH3—C—OH+H—O—C2H5
18 浓H2SO4
O CH3—C—O—C2H5 + H2O
18
酯化反应属于取代反应中的一种, 也可看作是分子间脱水的反应。
谢谢!
酯化反应:酸和醇作用,生成酯和水的反应
2.酯化反应
物 质 乙 酸 乙 醇 乙酸乙酯
沸点(0C) 117.9 78.5 77
密度(g/mL) 1.05 0.7893 0.90
水溶性 易溶 易溶 微溶于水 不溶于盐溶液
1、为什么要先加酒精,后加浓硫酸? 浓硫酸稀释放出热量;若酒精加在后,则会沸腾飞溅 混合物的加入顺序:乙醇、浓硫酸、冰醋酸。 2、乙酸乙酯为什么浮在液面上? 乙酸乙酯不溶于碳酸钠溶液,且密度比水小。 3、为什么要加碎瓷片?
专题4 烃的衍生物
第二单元 醇 酚
醇、酚在结构上有什么不同?
书P66【观察与思考】
醇——烃分子中饱和碳原子上的氢原子被羟基取代形成的化合物 酚——分子中羟基与苯环碳原子直接相连的有机化合物
OH CH3CHCH3 OH
OH
CH3
不是酒精是乙醇
长途客运汽车站,一个男子拎着一大桶东西 急匆匆地奔过来,正挤着人群想上车,售票 员问:“哎哎,这是什么东西?” 男子一边喘气一边往上挤说:“酒精”.
乙醇和浓硫酸混合加热 到170℃左右
H H C H H C H 1700C
浓H2SO4
CH2=CH2
+H2O
OH
羟基和氢脱去结合成水
H H H
C—C—H
H O—H
消去(脱水)
有机化合物在适当的条 件下,由一个分子脱去一个 小分子(如水、卤化氢等分 子),而生成不饱和(双键 或叁键)化合物的反应,叫 做消去反应。
催化剂 ∆
H-C-C-O-H
|③
H
H
2C2H5OH+2Na→2C2H5ONa+H2↑ 2C2H5OH+O2
C2H5OH
浓H2SO4
170℃
2CH3CHO+2H2O
CH2=CH2↑+H2O
CH3CH2OCH2CH3+H2O C2H5Br + H2O
2C2H5OH
浓H2SO4
140℃
C2H5OH + HBr △
乙 二 醇 球 棍 模 型
物理性质:无色、粘稠、甜味、液体、低凝固点
化学性质:与乙醇相似。
用途:抗冻剂、原料、发雾剂。
丙 三 醇 球 棍 模 型
物理性质:无色、粘稠、甜味、液体、凝固点 低、吸湿性强。 化学性质:与乙醇相似。 用途:制印泥、化妆品,防冻剂,制炸药(消 化甘油)。
醇的分类
一元醇:如 甲醇、乙醇
启迪思考: 能发生消去反应的醇的分子结构特点是什么? 是不是所有的醇都能发生消去反应?
碳原子上要有氢原子
脱水反应--(分子间脱水)
乙醇的脱水反应条件(例如温度)不同,脱水的 方式也不同,生成物也不同。如乙醇和浓硫酸共热 到140℃左右,每两个乙醇分子间会脱去一个水分 子而生成乙醚。
2CH3CH2OH
乙醇的化学性质
实验探究一
乙醇燃烧时火焰的颜色?
乙醇在空气里能够燃烧,发出淡蓝色 的火焰,同时放出大量的热。
1. 燃烧
C2H5 OH + 3 O2
点燃
2CO2 +3H2O
乙醇燃烧时哪些化学键发生断裂呢?
⑤
焊接银器、铜器时,表面会生成发黑的氧化膜, 银匠说,可以先把铜、银在火上烧热,马上蘸 一下酒精,铜银会光亮如初!这是何原理?
防止液体暴沸
物 质 乙 酸 乙 醇 乙酸乙酯
沸点(0C) 117.9 78.5 77
密度(g/mL) 1.05 0.7893 0.90
水溶性 易溶 易溶 微溶于水 难溶于盐溶液
4、蒸出的乙酸乙酯中含有哪些杂质? 乙醇,乙酸。 5、饱和碳酸钠溶液的作用?
溶解乙醇、中和乙酸、降低乙酸乙酯的溶解度。
6、反应中浓H2SO4的作用是什么?
浓H2SO4
1400C
CH3CH2OCH3CH2 + H2O
书P69“信息提示” 启迪思考: 通过分子内脱水反应和分子间脱水反应, 试比较这两个反应的异同点,有什么心得?
小结:乙醇的化学性质
乙醇分子结构
H H
|
④|
化学性质
氢被活泼金属置换 催 化 氧 化
断键位置
① ①③ ②④ ①或② ②
|
② ①
分子内脱水(消去) 分子间脱水(取代) 与HX反应
乙 醇 制 法
1、发酵法 2、乙烯水化法
乙醇的用途
乙 醇
溶 剂 燃料 化工原料
甲 醇 的 球 棍 模 型
甲醇别名甲基醇、木醇、木精 ,结构简式 CH3OH ,有类似乙醇气味的无色透明、易燃、易 挥发的液体 。 甲醇有毒、有麻醉作用,对视神 经影响很大,严重时可引起失明。甲醇是最常用的 有机溶剂之一,能与水和多种有机溶剂互溶。
乙 醇 结 构
分子式: C2H6O H H 结构式: H C—C—O—H H H
乙醇分子的比例模型
醇的官能团--羟基 写作-OH
结构简式:CH3CH2OH 或C2H5OH
结构与性质分析
⑤
H H
-C原子 -C原子
H
④
C—C—O—H H
③
H② ①
官能团--羟基(-OH)
乙醇分子是由乙基(—C2H5)和羟基(— OH)组成的,羟基比较活泼,它决定着乙醇的主 要性质。
实验现象:试管II中有油状物产生,溶液分层
【实验原理】
乙醇与氢卤酸的反应
学生表演 H―C―C―B H―C―C―OH + H B
H H H H
― r
r
+ H―OH
H
H
H
H
NaBr + H2SO4 == NaHSO4 + HBr
说明: ⑴该反应与卤代烃的水解反应是相反的关系,碱性时易于 卤代烃与水的水解反应,酸性时易于醇与HX的取代。 ⑵常用醇、卤化钠、浓硫 →C2H5Br+NaHSO4+H2O
乙醇钠
⑤
此反应中,乙醇哪 些键断裂?
乙醇的化学性质
实验探究四 乙醇与氢卤酸的反应
试管 I 试管 II 导管 a
在试管 I 中依次加入 2 mL 蒸馏水、4 mL浓硫酸、2 mL 95%的乙醇和3 g 溴化钠粉末, 在试管II中注入蒸馏水,烧杯 中注入自来水。加热试管 I 至 微沸状态数分钟后,冷却,观 察并描述实验现象。
“不行,不行,这可是易燃物,不能带上车 的.”售票员反皱着眉头. 这男子又嚷道:“这是乙醇.”
“干嘛不早说?呵呵,快上!”售票员笑着 抱怨.客车终于启动了.
乙醇的物理性质
颜 色: 气 味: 状 态: 挥发性: 无色透明 特殊香味 液体 易挥发 比水小
密 度:
溶解性: 跟水以任意比互溶 能够溶解多种无机物和有机物
H 结构简式 CH3CHO
H―C―C― ―O H
醛基
生活中,你的亲朋好友有没有喝酒的? 同学们有没有发现一个有趣的现象, 喝了酒之后,有的人容易脸红?你知 道是为什么吗?
