预防艾滋病母婴传播上报流程
预防艾滋病母婴传播相关报表上报流程及要求
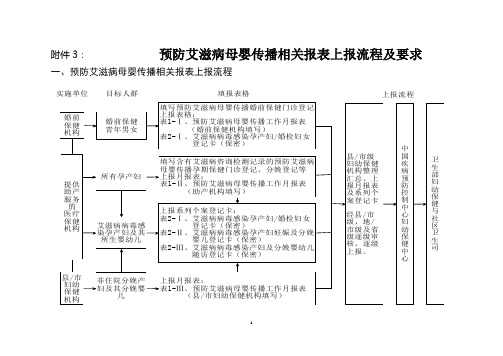
附件 3:预防艾滋病母婴传播相关报表上报流程及要求 预防艾滋病母婴传播相关报表上报流程及要求目标人群 填报表格 填写预防艾滋病母婴传播婚前保健门诊登记 上报表格: 表1-Ⅰ、预防艾滋病母婴传播工作月报表 (婚前保健机构填写) 表2-Ⅰ、艾滋病病毒感染孕产妇/婚检妇女 登记卡(保密) 填写含有艾滋病咨询检测记录的预防艾滋病 母婴传播孕期保健门诊登记、分娩登记等 上报月报表: 表1-Ⅱ、预防艾滋病母婴传播工作月报表 (助产机构填写) 上报系列个案登记卡: 表2-Ⅰ、艾滋病病毒感染孕产妇/婚检妇女 登记卡(保密) 表2-Ⅱ、艾滋病病毒感染孕产妇妊娠及分娩 婴儿登记卡(保密) 表2-Ⅲ、艾滋病病毒感染产妇及分娩婴幼儿 随访登记卡(保密) 县/市级 妇幼保健 机构整理 汇总、上 报月报表 及系列个 案登记卡 经县/市 级、地/ 市级及省 级逐级审 核、逐级 上报。
上报流程一、预防艾滋病母婴传播相关报表上报流程实施单位 婚前 保健 机构婚前保健 青年男女所有孕产妇 提供 助产 服务 的 医疗 保健 机构艾滋病病毒感 染孕产妇及其 所生婴幼儿中 国 疾 病 预 防 控 制 中 心 妇 幼 保 健 中 心卫 生 部 妇 幼 保 健 与 社 区 卫 生 司县/市 妇幼 保健 机构非住院分娩产 妇及其分娩婴 儿上报月报表: 表1-Ⅲ、预防艾滋病母婴传播工作月报表 (县/市妇幼保健机构填写)1二、预防艾滋病母婴传播相关报表上报时限 预防艾滋病母婴传播相关报表上报时限 (一) 预防艾滋病母婴传播工作月报表 (表 1–Ⅰ、 1–Ⅱ、 表 表 1–Ⅲ) 各级医疗保健机构应于次月 5 日前将预防艾滋病母婴传播 工作月报表(本机构填写部分)上报至本辖区的县(市、区)级 妇幼保健机构。
各级妇幼保健机构收集、整理、汇总和审核后, 形成 “预防艾滋病母婴传播工作月报(汇总)表”(表 1) ,于次 月 15 日前逐级上报至中国疾病预防控制中心妇幼保健中心。
预防艾滋病、梅毒和乙肝母婴传播相关报表、上报流程和要求

附件6预防艾滋病、梅毒和乙肝母婴传播相关报表上报流程及要求一、预防艾滋病、梅毒和乙肝母婴传播相关报表上报流程二、预防艾滋病、梅毒和乙肝母婴传播报表上报时限及要求(一)预防艾滋病、梅毒和乙肝母婴传播工作报表(表1)。
1.报告对象:所有婚前保健人群及孕产妇人群2.报告时限及要求:各级医疗卫生机构应按时将预防艾滋病、梅毒和乙肝母婴传播工作报表(本机构填写部分)上报至本辖区的县(市、区)级妇幼保健机构。
县(市、区)级妇幼保健机构除完成本机构应填报内容外,还应负责收集、整理、汇总本地区工作汇总数据,审核后尽快完成网络报告。
地(市、州)级妇幼保健机构应负责收集、整理、征求意见稿汇总所辖各县(市、区)工作汇总数据,审核后尽快完成网络报告。
省级妇幼保健机构应于每月15日前完成本省(自治区、直辖市)工作月报表的审核、汇总与网络报告,并上报至中国疾病预防控制中心妇幼保健中心。
(二)预防艾滋病、梅毒和乙肝母婴传播个案卡(表2—表4)。
1.报告对象:所有诊断为艾滋病感染的婚检妇女、孕产妇及其所生的18月龄以内的儿童(表2)。
所有诊断为梅毒感染的孕产妇及其所生的18月龄以内的儿童(表3)。
所有乙肝病毒表面抗原阳征求意见稿性孕产妇及其新生婴儿(表4-I ),以及其中血清HBV DNA ≥2×105 IU/ml 或HBeAg 阳性产妇所生的12月龄内的儿童(表4-II )。
上述报告对象不包括以终止妊娠为直接目的而就医时发现的感染病例。
2.报告时限及要求:表2-I 、3-I 和4-I 应于明确艾滋病、梅毒和乙肝感染状态后的5日内填写完成。
对既往已确诊感染者,也应在本次了解其感染状态后5日内填写完成。
表2-Ⅱ、3-Ⅱ和4-I (“三-九”部分)应当分别于艾滋病、梅毒或乙肝感染孕产妇分娩后及出院前填写完成,对发生自然流产、人工终止妊娠、死亡或失访等其他妊娠结局的艾滋病或梅毒感染孕产妇,应当在获知其结局后的5日内填写完成。
预防艾滋病、梅毒和乙肝母婴传播检测服务流程)

预防艾滋病、梅毒和乙肝母婴传播检测服务流程为了更好地为孕产妇提供预防艾滋病、梅毒和乙肝母婴传播的综合防治服务,最大程度地减少因艾滋病、梅毒和乙肝母婴传播造成的儿童感染,改善妇女、儿童的生活质量及健康水平,做到早发现、早干预、早随访,使更多育龄妇女、孕产妇及其家庭受益,从而规范我院预防艾滋病、梅毒和乙肝母婴传播的服务流程,服务流程及措施如下:1、产科门诊接诊医师,要对来院初次产前检查的孕妇进行预防艾滋病、梅毒和乙肝母婴传播的有关知识宣传,对有需求的服务对象要单独进行咨询和指导,提高服务对象对预防艾滋病、梅毒和乙肝感染及母婴传播服务的认识和利用。
实行首诊负责制。
2、产科门诊接诊医师开具检验申请单,由孕妇到收费处付款后到检验科验血。
3、检验科依据申请单如实检验,当出现疑似阳性的结果时,要及时复检,结果仍然疑似阳性时,要通知科主任,不能消除疑似阳性结果的,要及时与送检医师联系,做好沟通与准备工作,选择合适的理由为受检者作进一步复检和确定实验。
4、对于已经证实的阳性结果,检验科工作人员要直接将报告单送交送检医师,有送检医师处理。
5、送检医师要为检测结果为阴性的孕产妇提供改变危险行为、避免艾滋病、梅毒和乙肝感染等重要信息;为检测结果为阳性的孕产妇提供保密的咨询服务,告知预防母婴传播干预措施信息,与感染孕产妇商讨并由其知情选择妊娠结局,提供必要的转介服务等,与感染孕产妇沟通,在其同意情况下进行配偶/性伴的告知和检测指导。
要认真做好登记工作。
6、检验报告单应采用向内对折的方式相互递送,检验人员与医师的告知应在保密的状态下进行。
有关工作人员不得对检验结果进行相关人员以外的交流。
7、妇产科、检验科要将登记本进行保密性保管,无关人员不得翻录查阅。
艾滋病、梅毒和乙肝孕妇产前检测流程图产科医师开具检验申请单——受检孕妇或其家人到收费处交费——持交费后的检验申请单到检验科采血——(检验结果为阴性的由孕妇自行取报告就诊)检验结果疑似或确证为阳性的,检验人员直接与送检医师联系。
艾梅乙、检测服务流程图

附件1(产科门诊、病房上墙)预防艾滋病、梅毒和乙肝母婴传播服务流程图1. 预防艾滋病、梅毒和乙肝母婴传播服务流程)附件2-I(检验科上墙)孕产妇艾滋病抗体检测及服务流程图2. 孕妇艾滋病抗体检测及服务流程附件2-II(检验科上墙)产时艾滋病抗体检测及服务流程说明:# 再次确认结果阴性报告“阴性”,结果阳性报告“阳性”,结果仍为“不确定”继续随访, 4周后再次进行确认试验;仍为不确定结果,报告“阴性”。
必要时可进行HIV核酸检测作为辅助诊断。
图3 产时艾滋病抗体检测及服务流程)(适用于孕期未接受HIV检测的产妇)附件3(检验科上墙)孕产妇梅毒检测及服务流程图4.孕产妇梅毒检测及服务流程艾滋病感染孕产妇及所生儿童抗艾滋病病毒用药方案预防艾滋病母婴传播抗病毒药物的应用可分为预防性抗病毒用药方案和治疗性抗病毒用药方案。
对于处于艾滋病临床I期或II期,免疫功能相对较好,CD4+T淋巴细胞计数>350/mm3的艾滋病感染孕产妇,建议采用预防性抗病毒用药方案;对处于艾滋病临床Ⅲ期或Ⅳ期,CD4+T淋巴细胞计数≤350/mm3的艾滋病感染孕产妇,建议采用治疗性抗病毒用药方案。
一、预防性应用抗病毒药物(一)孕产妇预防性应用抗病毒药物。
1.孕期和分娩时。
从妊娠14周或14周后发现艾滋病感染后尽早开始服用齐多夫定(AZT)300mg +拉米夫定(3TC)150mg +洛匹那韦/利托那韦(克力芝)(LPV/r)400/100mg,每天2次;或者AZT300mg+3TC150mg,每天2次,依非韦伦(EFV)600mg,每天1次,直至分娩结束。
2.分娩后。
若选择人工喂养,产妇可在分娩结束后停止抗病毒药物的应用;若选择母乳喂养,产妇持续应用抗病毒药物至停止母乳喂养后1周。
(二)婴儿应用抗病毒药物。
婴儿可以选择应用以下两种抗病毒药物方案中的任一种。
1.奈韦拉平(NVP)方案:新生儿出生体重≥2500g,服用NVP 15mg(即混悬液1.5ml),每天1次;出生体重<2500g且≥2000g,服用NVP 10mg(即混悬液1.0ml),每天1次;出生体重<2000g,服用NVP 2mg/kg(即混悬液0.2ml/kg),每天1次;至出生后4~6周。
艾梅乙检测服务流程图

艾梅乙检测服务流程图 IMB standardization office【IMB 5AB- IMBK 08- IMB 2C】附件1(产科门诊、病房上墙)预防艾滋病、梅毒和乙肝母婴传播服务流程图1.预防艾滋病、梅毒和乙肝母婴传播服务流程)附件2-I(检验科上墙)孕产妇艾滋病抗体检测及服务流程图2.孕妇艾滋病抗体检测及服务流程附件2-II(检验科上墙)产时艾滋病抗体检测及服务流程说明:# 再次确认结果阴性报告“阴性”,结果阳性报告“阳性”,结果仍为“不确定”继续随访, 4周后再次进行确认试验;仍为不确定结果,报告“阴性”。
必要时可进行HIV核酸检测作为辅助诊断。
图3产时艾滋病抗体检测及服务流程)(适用于孕期未接受HIV检测的产妇)附件3(检验科上墙)孕产妇梅毒检测及服务流程图4.孕产妇梅毒检测及服务流程艾滋病感染孕产妇及所生儿童抗艾滋病病毒用药方案预防艾滋病母婴传播抗病毒药物的应用可分为预防性抗病毒用药方案和治疗性抗病毒用药方案。
对于处于艾滋病临床I期或II期,免疫功能相对较好,CD4+T淋巴细胞计数>350/mm3的艾滋病感染孕产妇,建议采用预防性抗病毒用药方案;对处于艾滋病临床Ⅲ期或Ⅳ期,CD4+T淋巴细胞计数≤350/mm3的艾滋病感染孕产妇,建议采用治疗性抗病毒用药方案。
一、预防性应用抗病毒药物(一)孕产妇预防性应用抗病毒药物。
1.孕期和分娩时。
从妊娠14周或14周后发现艾滋病感染后尽早开始服用齐多夫定(AZT)300mg+拉米夫定(3TC)150mg+洛匹那韦/利托那韦(克力芝)(LPV/r)400/100mg,每天2次;或者AZT300mg+3TC150mg,每天2次,依非韦伦(EFV)600mg,每天1次,直至分娩结束。
2.分娩后。
若选择人工喂养,产妇可在分娩结束后停止抗病毒药物的应用;若选择母乳喂养,产妇持续应用抗病毒药物至停止母乳喂养后1周。
(二)婴儿应用抗病毒药物。
婴儿可以选择应用以下两种抗病毒药物方案中的任一种。
预防艾滋病、梅毒和乙肝母婴传播工作报表填表说明

征求意见稿预防艾滋病、梅毒和乙肝母婴传播工作报表填表说明一、填报要求1.该表为月报表,统计每月第一天至当月最后一天的数据。
2.月报表中提及的产妇是指≥28孕周分娩,包括≥28孕周引产者;活产儿是指孕满28周或体重达到1000克及以上的新生儿,出生时具有心跳、呼吸、脐带搏动、随意肌收缩4项生命征象之一者。
3.婚前保健部分由婚前保健机构填报,孕前保健部分由孕前保健机构填报,孕期部分由提供孕期保健服务机构填报,预防母婴传播服务部分由助产机构填报,非住院分娩部分由区县妇幼保健机构填报。
4.所有数据以相关登记或信息系统记录为依据。
5.既往感染者按本次妊娠最早接受检测的时期统计。
6.同一个孕产妇多次检测的,计1人。
二、指标解释1.接受婚前/孕前保健人数:指在婚前孕前保健机构接受婚前孕前医学检查服务的人数,分别填报男性和女性人数。
2.其中接受艾滋病检测人数:指接受婚前孕前医学检查服务的人群中接受艾滋病检测的人数,分别填报男性和女性人数。
3.其中艾滋病感染人数:指接受艾滋病检测的婚前孕前医学检查人群中,确认艾滋病病毒感染的人数,分别填报男性和女性人数。
4.接受初次产前保健的孕妇数:指本次妊娠中第一次接受孕期保健服务的孕妇人数。
5.接受艾滋病检测孕妇数:指在孕期接受过艾滋病检测的孕妇总人数。
6.其中艾滋病感染孕妇数:指所有在艾滋病补充试验结果为阳性的孕妇数,无论其妊娠结局如何。
7.接受梅毒检测孕妇数:指所有接受梅毒检测的孕妇人数。
8.其中梅毒感染孕妇数:指所有在孕期诊断梅毒感染的孕妇,无论其妊娠结局如何。
9.接受乙肝检测孕妇数:指当月所有接受乙肝病毒血清标志物(乙肝病毒表面抗原或两对半)检测的孕妇人数。
10.其中乙肝感染孕妇数:所有在孕期诊断乙肝感染的孕妇人数,无论其妊娠结局如何。
11.住院分娩产妇数:指在本机构住院分娩的产妇总人数。
12.孕产期接受艾滋病检测产妇数:指本机构住院分娩产妇中在孕期和产时接受过艾滋病检测的人数。
预防艾滋病梅毒和乙肝母婴传播婚前保健和孕产期保健服务规范及流程

预防艾滋病、梅毒和乙肝母婴传播婚前保健和孕产期保健服务规范及流程一、婚前保健经许可开展婚前保健的医疗机构在提供婚前保健服务时,主动提供预防艾滋病、梅毒和乙肝母婴传播咨询。
应以知情不拒绝为原则,对婚前保健人群开展艾滋病检测、梅毒血清学检测和乙肝检测。
对检测结果有反应或阳性反应者(艾滋病为有反应,梅毒和乙肝为阳性反应)进行告知,并提供咨询和指导。
具体服务流程如下:(-)艾滋病病毒筛查试验有反应者应及时采集第二份血样标本,并对两份样本进行复检,如复检均有反应或其中一份样本有反应,应将两份样本一并送至所在区疾病预防控制中心艾滋病确证实验室进行补充试验,区疾病预防控制中心应在收到标本后五个工作日内将抗体确证试验结果反馈给送检机构。
对确认艾滋病病毒感染者,应协同区疾病预防控制中心做好个案流行病学调查和告知工作,并完成表2-1 “艾滋病感染妇女基本情况”。
(-)梅毒血清学试验阳性者应转介至有性病诊疗资质的医疗机构进行复检。
(三)乙肝病毒表面抗原阳性者告知预防母婴传播干预措施,对配偶科普乙肝疫苗免费接种政策。
二、孕产期保健各级各类医疗保健机构(包括社区卫生服务中心)应在提供初次孕产期保健服务时,主动提供预防艾滋病、梅毒和乙肝母婴传播咨询。
以知情不拒绝为原则,采集孕妇血样标本进行艾滋病抗体初筛试验、梅毒血清学检测(梅毒螺旋体血清学试验)、乙肝病毒感染血清学标志物(乙肝五项)检测。
社区卫生服务中心将血样标本送至所在区妇幼保健机构或区卫生健康行政部门指定机构进行艾滋病抗体初筛试验。
(一)检测服务流程对艾滋病病毒筛查试验有反应、梅毒和乙肝筛查试验阳性的孕产妇检测服务流程如下:1.艾滋病病毒筛查试验有反应孕产妇应及时采集第二份血样标本,并对两份样本进行复检,如复检均有反应或其中一份样本有反应,应将两份样本一并送至所在区疾病预防控制中心艾滋病确证实验室进行补充试验。
区疾病预防控制中心应在收到标本后五个工作日内将抗体确证试验结果反馈给送检机构。
预防艾滋病、梅毒和乙肝母婴传播服务流程

预防艾滋病、梅毒和乙肝母婴传播服务流程预防艾滋病、梅毒和乙肝母婴传播服务流程是一项重要的工作,旨在降低艾滋病、梅毒和乙肝母婴传播的风险,保障母婴健康。
以下是预防艾滋病、梅毒和乙肝母婴传播服务流程的详细介绍。
一、宣传教育1. 普及艾滋病、梅毒和乙肝的相关知识,提高公众对这三类疾病的认识和了解。
2. 宣传预防母婴传播的重要性,强调采取有效措施可以降低母婴传播的风险。
3. 针对不同人群,如孕妇、产妇、家属、医护人员等,开展有针对性的宣传教育活动。
二、孕期管理1. 孕早期检测:对所有孕妇进行艾滋病、梅毒和乙肝的筛查,确保尽早发现感染。
2. 定期随访:对感染艾滋病、梅毒和乙肝的孕妇进行定期随访,监测病情变化。
3. 药物治疗:根据病情,为感染艾滋病、梅毒和乙肝的孕妇提供相应的药物治疗。
4. 健康指导:为孕妇提供健康指导,包括营养、生活方式等方面的建议,以提高母婴健康水平。
三、分娩期管理1. 选择适宜的分娩方式:根据孕妇和胎儿的具体情况,选择适宜的分娩方式,以降低母婴传播的风险。
2. 安全接生:确保分娩过程中的安全,避免感染的发生。
3. 预防性用药:为感染艾滋病、梅毒和乙肝的孕妇所生儿童提供预防性用药,降低感染风险。
四、产后管理1. 随访:对感染艾滋病、梅毒和乙肝的孕妇所生儿童进行定期随访,监测健康状况。
2. 喂养指导:为感染艾滋病、梅毒和乙肝的孕妇所生儿童提供科学的喂养指导,确保营养均衡。
3. 疫苗接种:为感染艾滋病、梅毒和乙肝的孕妇所生儿童提供疫苗接种,提高免疫力。
五、综合干预1. 家庭支持:为感染艾滋病、梅毒和乙肝的孕妇及其家庭提供心理支持和关爱,减轻心理负担。
2. 社会支持:争取社会各界对预防艾滋病、梅毒和乙肝母婴传播工作的支持和参与,提高服务质量。
3. 政策支持:争取政府相关政策支持,为预防艾滋病、梅毒和乙肝母婴传播工作提供保障。
通过以上五个方面的服务流程,可以有效降低艾滋病、梅毒和乙肝母婴传播的风险,保障母婴健康。
预防艾滋病、梅毒和乙肝母婴传播服务流程图

附件1预防艾滋病、梅毒和乙肝母婴传播服务流程图1. 预防艾滋病、梅毒和乙肝母婴传播服务流程附件2孕产妇艾滋病抗体检测及服务流程确认试验、CD4T淋巴细胞计数及病毒载量检测均在疾控中心进行。
孕期每三个月和产后4-6周对孕产妇各进行一次CD4T淋巴细胞计数的检测,同时在发现孕产妇感染艾滋病时和孕晚期各进行一次病毒载量的检测。
图2. 孕妇艾滋病抗体检测及服务流程附件3孕期末艾滋病抗体检测及服务流程说明:# 再次确认结果阴性报告“阴性”,结果阳性报告“阳性”,结果仍为“不确定”继续随访, 4周后再次进行确认试验;仍为不确定结果,报告“阴性”。
必要时可进行HIV核酸检测作为辅助诊断。
图3 产时艾滋病抗体检测及服务流程(适用于孕期未接受HIV检测的产妇)附件4艾滋病感染孕产妇所生儿童艾滋病感染早期诊断检测及服务流程早期诊断地址:北京市昌平区昌百路155号,性艾中心参比实验室。
邮编:102206图4.艾滋病感染孕产妇所生儿童艾滋病感染早期诊断检测及服务流程附件5艾滋病感染孕产妇所生儿童艾滋病抗体检测及服务流程各级医疗保健机构应在艾滋病感染确诊孕产妇后、感染孕产妇分娩后及感染孕产妇所生儿童满1、3、6、9、12和18月龄时分别进行随访,并上报个案卡,共8张个案卡图5. 艾滋病感染孕产妇所生儿童艾滋病抗体检测及服务流程附件6孕产妇梅毒检测及服务流程梅毒阳性孕妇每月监测RPR1次,监测治疗效果图6.孕产妇梅毒检测及服务流程附件7梅毒感染孕产妇所生儿童的随访与先天梅毒感染状态监测梅毒阳性孕产妇所生儿童随访时间3、6、9、12、15、18月龄*非梅毒螺旋体试验包括RPR、TRUST等方法#梅毒螺旋体试验包括TPPA、TPHA及应用该原理的快速检测等方法图7. 梅毒感染孕产妇所生儿童的随访及先天梅毒感染状态监测图。
艾梅乙、检测服务流程图

附件1(产科门诊、病房上墙)预防艾滋病、梅毒和乙肝母婴传播服务流程图1.预防艾滋病、梅毒和乙肝母婴传播服务流程)附件2-I(检验科上墙)孕产妇艾滋病抗体检测及服务流程图2.孕妇艾滋病抗体检测及服务流程附件2-II(检验科上墙)产时艾滋病抗体检测及服务流程说明:# 再次确认结果阴性报告“阴性”,结果阳性报告“阳性”,结果仍为“不确定”继续随访, 4周后再次进行确认试验;仍为不确定结果,报告“阴性”。
必要时可进行HIV核酸检测作为辅助诊断。
图3产时艾滋病抗体检测及服务流程)(适用于孕期未接受HIV检测的产妇)附件3(检验科上墙)孕产妇梅毒检测及服务流程图4.孕产妇梅毒检测及服务流程艾滋病感染孕产妇及所生儿童抗艾滋病病毒用药方案预防艾滋病母婴传播抗病毒药物的应用可分为预防性抗病毒用药方案和治疗性抗病毒用药方案。
对于处于艾滋病临床I期或II期,免疫功能相对较好,CD4+T淋巴细胞计数>350/mm3的艾滋病感染孕产妇,建议采用预防性抗病毒用药方案;对处于艾滋病临床Ⅲ期或Ⅳ期,CD4+T淋巴细胞计数≤350/mm3的艾滋病感染孕产妇,建议采用治疗性抗病毒用药方案。
一、预防性应用抗病毒药物(一)孕产妇预防性应用抗病毒药物。
1.孕期和分娩时。
从妊娠14周或14周后发现艾滋病感染后尽早开始服用齐多夫定(AZT)300mg+拉米夫定(3TC)150mg+洛匹那韦/利托那韦(克力芝)(LPV/r)400/100mg,每天2次;或者AZT300mg+3TC150mg,每天2次,依非韦伦(EFV)600mg,每天1次,直至分娩结束。
2.分娩后。
若选择人工喂养,产妇可在分娩结束后停止抗病毒药物的应用;若选择母乳喂养,产妇持续应用抗病毒药物至停止母乳喂养后1周。
(二)婴儿应用抗病毒药物。
婴儿可以选择应用以下两种抗病毒药物方案中的任一种。
1.奈韦拉平(NVP)方案:新生儿出生体重≥2500g,服用NVP15mg(即混悬液),每天1次;出生体重<2500g且≥2000g,服用NVP10mg(即混悬液),每天1次;出生体重<2000g,服用NVP2mg/kg(即混悬液kg),每天1次;至出生后4~6周。
预防艾滋病、梅毒和乙肝母婴传播信息管理工作制度

预防艾滋病、梅毒和乙肝母婴传播信息管理工作制度为建立健全预防艾滋病、梅毒和乙肝母婴传播信息管理工作,完善信息资料收集、管理和及时上报,确保信息安全,特制定本制度。
1、承担婚前保健和孕产妇保健的医疗保健机构,应建立艾滋病、梅毒和乙肝检测咨询信息的等相关登记资料,定期收集和汇总相关信息,每月准时上报相关报表至县妇幼保健院。
2、各镇卫生院、县医院、县妇幼保健院应及时收集、整理和汇总本辖区内艾滋病、梅毒和乙肝的相关检测、咨询信息,上报预防艾滋病、梅毒和乙肝母婴传播工作月报表及个案登记卡,审核上报科室报表的准确性、完整性,按要求准时上报妇幼保健院。
3、县妇幼项目办公室负责人负责收集、整理、报告、审核全县预防艾滋病、梅毒和乙肝母婴传播工作月报表及个案登记卡,完成全县预防艾滋病、梅毒和乙肝母婴传播工作月报表及系列个案登记卡的网络直报、审核工作,准时上报全县报表。
4、县妇幼项目办公室人员定期对本县数据信息的及时性、完整性与准确性进行核查,开展针对数据错报、漏报、重报等情况的质量控制,提高数据信息质量。
预防艾滋病梅毒和乙肝母婴传播工作实施方案

防止艾滋病、梅毒和乙肝母婴传播服务流程
孕产妇艾滋病抗体检测及服务流程
说明:# 再次确认结果阴性报告“阴性”,结果阳性报告“阳性”,结果仍为“不确定”继续随访, 4周后再次进行确认试验;仍为不确定结果,报告“阴性”。
必要时可进行HIV核酸检测作为辅助诊断。
孕产妇梅毒检测及服务流程
艾滋病感染孕产妇所生小朋友艾滋病感染初期
诊断检测及服务流程
艾滋病感染孕产妇所生小朋友艾滋病抗体
检测及服务流程
梅毒感染孕产妇所生小朋友旳随访与先天梅
毒感染状态监测
说明:* 非梅毒螺旋体抗原血清学试验包括RPR、TRUST等方法。
#梅毒螺旋体抗原血清学试验包括TPPA、TPHA及应用该原理的快速检测等方法。
预防艾滋病、梅毒、乙肝各种制度

预防艾滋病、梅毒、乙肝母婴传播信息管理制度一、管理对象辖区各级医疗保健机构二、管理目的规范艾滋病、梅毒、乙肝各种信息资料管理程序,提高信息管理质量。
三、管理要求1、各级医疗卫生机构应当建立记录艾滋病、梅毒、乙肝检测咨询信息的婚前保健、孕产妇保健、产时保健等相关登记2、各级医疗保健机构应每月5日将收集、整理和汇总相关检测、咨询信息上报县妇幼保健院。
3、各级医疗机构对检测发现的艾滋病或梅毒感染孕产妇进行随访和个案信息调查,按照预防艾滋病、梅毒、乙肝母婴传播相关报表上报要求及时填写上报县妇幼保健院。
4、各级医疗保健机构应当认真核对各类原始登记与记录,确保相关报表信息符合逻辑、完整、准确。
5、县妇幼保健院汇总、审核各医疗机构的月报和个案卡上报到市妇幼保健院。
6、确保信息的保密性。
预防艾滋病、梅毒、乙肝母婴传播医护人员职业暴露及防护工作制度医务人员预防艾滋病感染的防护措施应当遵照标准预防原则,对所有病人的血液、体液及被血液、体液污染的物品均视为具有传染性病源物质,医务人员接触这些物质时,必须采取防护措施:一、医务人员接触病源物质时,应当采取以下防护措施:1、医务人员进行有可能接触病人血液、体液的诊疗和护理操作时必须戴手套,操作完毕,脱去手套后立即洗手,必要时进行手消毒。
2、在诊疗、护理操作过程中,有可能发生血液、体液飞溅到医务人员的面部时,医务人员应当戴手套,具有防渗透性能的口罩、防护眼镜;有可能发生血、体液大面积飞溅或者有可能污染医务人员的身体时,还应当穿具有防渗透性能的隔离衣或者围裙。
3、医务人员手部皮肤发生破损,在进行有可能接触病人的血液、体液的诊疗和护理操作时必须戴双层手套。
4、医务人员在进行侵袭性诊疗、护理操作过程中,要注意防止针头、缝合针、刀片等锐器刺伤或者划伤。
5、使用后的锐器应当直接放入耐刺、防渗漏的利器盒,或者利用针头处理设备进行安全处置,也可以使用具有安全性能的注射器、输液器等医用锐器,以防刺伤。
预防艾滋病母婴传播工作职责

五、预防艾滋病母婴传播 试剂及药品管理:
1、预防艾滋病母婴传播工作需要的试剂由省级负责采购 分配。 2、省妇幼保健院负责逐级收集试剂(包括采血一次性耗 材)、药品需求信息、制订年度需求计划。省疾病预防控 制中心负责集中采购 3、试剂(包括采血一次性耗材)直接由供货厂家下发到 市州妇幼保健院,由市州妇幼保健院按照各区县活产数下 发至区县。 4、药品下发到各市州妇幼保健院,放臵在市级妇幼保健 院药房并由专人管理。由市州妇幼保健院根据各防艾滋病母婴传播 信息管理:
二、电话及电子邮件上报流程 1. 重申所有医疗保健机构每发现1例HIV阳性(初筛阳性)孕产妇必 须立即电话上报至辖区的县、区妇幼保健机构。 2. 妇幼保健机构在接到辖区内的电话上报后必须立即进行调查, 了解并指导其进行母婴阻断的干预,并在24小时内逐级电话上报 至省级妇幼保健院妇女保健科,同时督促其立即进行HIV确诊试验。 3. 妇幼保健机构在获得确认试验阳性结果后必须在3天内进行个案 调查,填写相关信息报表并通过电子邮箱上报至省妇幼保健院妇 女保健科cswumin@,(艾滋病病毒感染孕产妇妊娠及所 生婴儿登记卡(表2–Ⅱ)应于艾滋病病毒感染孕产妇出现妊娠结 局或产褥期(分娩至42日)后3日内上报;艾滋病病毒感染产妇及 所生儿童随访登记卡(表2–Ⅲ)应于艾滋病病毒感染产妇所生儿 童满1、3、6、9、12、18个月后 3日内上报)。 4. 每月10日前市(州)妇幼保健机构必须将本市(州)的工作月 报表通过电子邮件上报至省妇幼信息科。
预防艾滋病母婴传播工作职责
1
存在的问题
(1)HIV检测覆盖面仍窄,孕期检测率低:我省6各示范 区孕产妇孕期检测率仅达72.7%,且大部分的为产时检 测,从而错失抗病毒药物的良好时机。 (2)抗病毒药物应用率低:孕产妇抗病毒药物应用率为 44 %,婴儿抗病毒药物应用率为35%,这与检测发现阳 性时间晚有关,同时与部分地区抗病毒药物获得性低 有关。 (3)信息上报不及时,(大多数HIV阳性孕产妇的个案 卡都在产后1-2月才上报)不完整( 一部分HIV阳性孕 产妇丈夫的信息资料缺失)。 (4)部分地区项目工作负责人更换频繁,影响信息上 报的及时性和准确性。
艾梅乙流程

附件1预防艾滋病、梅毒和乙肝母婴传播服务流程图1. 预防艾滋病、梅毒和乙肝母婴传播服务流程附件2孕产妇艾滋病抗体检测及服务流程图2. 孕妇艾滋病抗体检测及服务流程图3 产时艾滋病抗体检测及服务流程(适用于孕期未接受HIV检测的产妇)附件3孕产妇梅毒检测及服务流程图4.孕产妇梅毒检测及服务流程附件4艾滋病感染孕产妇及所生儿童抗艾滋病病毒用药方案预防艾滋病母婴传播抗病毒药物的应用可分为预防性抗病毒用药方案和治疗性抗病毒用药方案。
对于处于艾滋病临床I期或II 期,免疫功能相对较好,CD4+T淋巴细胞计数>350/mm3的艾滋病感染孕产妇,建议采用预防性抗病毒用药方案;对处于艾滋病临床Ⅲ期或Ⅳ期,CD4+T淋巴细胞计数≤350/mm3的艾滋病感染孕产妇,建议采用治疗性抗病毒用药方案。
一、预防性应用抗病毒药物(一)孕产妇预防性应用抗病毒药物。
1.孕期和分娩时。
从妊娠14周或14周后发现艾滋病感染后尽早开始服用齐多夫定(AZT)300mg +拉米夫定(3TC)150mg +洛匹那韦/利托那韦(克力芝)(LPV/r)400/100mg,每天2次;或者AZT300mg+3TC150mg,每天2次,依非韦伦(EFV)600mg,每天1次,直至分娩结束。
2.分娩后。
若选择人工喂养,产妇可在分娩结束后停止抗病毒药物的应用;若选择母乳喂养,产妇持续应用抗病毒药物至停止母乳喂养后1周。
(二)婴儿应用抗病毒药物。
婴儿可以选择应用以下两种抗病毒药物方案中的任一种。
1.奈韦拉平(NVP)方案:新生儿出生体重≥2500g,服用NVP15mg(即混悬液1.5ml),每天1次;出生体重<2500g且≥2000g,服用NVP 10mg(即混悬液1.0ml),每天1次;出生体重<2000g,服用NVP 2mg/kg(即混悬液0.2ml/kg),每天1次;至出生后4~6周。
2.齐多夫定(AZT)方案: 新生儿出生体重≥2500g,服用AZT 15mg(即混悬液1.5ml),每天2次;出生体重<2500g且≥2000g,服用AZT 10mg(即混悬液1.0ml),每天2次;出生体重<2000g,服用AZT 2mg/kg(即混悬液0.2ml/kg),每天2次;至出生后4~6周。
消除艾滋病、梅毒和乙肝母婴传播评估流程及主要指标

附件1消除艾滋病、梅毒和乙肝母婴传播评估流程及主要指标一、评估流程(一)省级自评。
各省(区、市)围绕国家、省级预防母婴传播行动计划及实施方案,对照有关要求和评估指标体系,对本省份消除母婴传播工作开展自评,撰写消除母婴传播自评报告。
(二)申请国家级评估。
以省(区、市)为整体,13个消除主要指标达标的省份可向国家卫生健康委申请开展国家级评估。
其中,3个结果指标需至少达到1年(提交申请的前一年达标),10个过程指标需持续达到2年(提交申请的前两年均达标)。
申请材料应包括《关于申请开展消除艾滋病、梅毒和乙肝母婴传播国家级评估的请示》、省级消除母婴传播工作进展报告、消除评估数据一览表。
(见附件2)。
(三)初步审核。
国家卫生健康委妇幼司组织有关专家对各省份提交的申请材料进行初步审核。
审核通过的,择期启动现场评估;审核不通过的,将有关意见反馈给申请省份,由其改进工作或补充完善资料后再次提出申请。
(四)现场评估。
国家卫生健康委妇幼司组建评估专家组,提前与申请省份做好沟通,确定现场评估时间、地区和流程等事宜。
1.评估现场选择。
综合考虑被评省份消除母婴传播工作情况以及常住人口、卫生资源、交通、代表性等因素,抽取包括省会城市在内的3个市(地、州)作为评估现场。
2.评估方法。
主要采用听取工作汇报、查阅资料、群体和个人访谈、现场调研等形式开展评估。
重点查看各级妇幼保健院、疾病预防控制中心、抗病毒治疗和性病防治机构、开展助产服务的公立医院和非公立医疗机构、基层医疗卫生机构以及相关社会组织。
另外,将在每个县(市、区)抽取2-3名艾滋病、梅毒或乙肝感染孕产妇进行深入访谈。
3.反馈评估情况。
现场评估结束后,评估专家组向被评省(区、市)现场反馈评估情况,指出工作成效和亮点,明确存在的问题和不足,提出下一步工作建议。
(五)形成评估结果。
国家卫生健康委妇幼司结合初步审核和现场评估情况,研究形成消除母婴传播评估通过或不予通过的结论,向申请省份反馈评估结果。
