2020-2021备战高考化学备考之有机化合物压轴突破训练∶培优 易错 难题篇及答案
2020-2021高考化学培优易错试卷(含解析)之有机化合物

2020-2021高考化学培优易错试卷(含解析)之有机化合物一、有机化合物练习题(含详细答案解析)1.(1)写出以乙炔为原料制备PVC (聚氯乙烯)的过程中所发生的反应类型:____________、_____________。
PE (聚乙烯)材料目前被公认为安全材料,也可用于制作保鲜膜和一次性餐盒。
辨别PE 和PVC 有三种方法,一是闻气味法:具有刺激性气味的是___________________;二是测密度法:密度大的应是___________________;三是燃烧法:PE 的单体和PVC 的单体在足量空气中燃烧的实验现象的明显区别是__________。
(2)PVDC ()是一种阻隔性高、韧性强、化学稳定性好的理想包装材料,广泛用于肉制品、豆制品等的包装。
写出合成PVDC 的单体的同分异构体的结构简式_________。
(3) “白色污染”是指各种塑料制品对环境的污染。
焚烧塑料会生成有毒物质二噁英,二噁英是含有如图所示母体的系列化合物,下列关于如图所示物质的说法不正确的是___________________(填序号)。
a .该物质在氧气中完全燃烧的产物是2CO 和2H Ob .该物质属于烃c .该物质的一卤代物只有2种【答案】加成反应 加聚反应 聚氯乙烯 聚氯乙烯 乙烯更易燃烧,氯乙烯燃烧有白雾(HCl 的小液滴)生成 ClCH CHCl = b【解析】【分析】(1)22C H 与HCl 加成生成2CH CHCl =,2CH CHCl =聚合生成聚氯乙烯;聚氯乙烯因会释放出氯化氢而具有刺激性气味;依据阿伏加德罗定律的推论,气体的密度之比等于其相对分子质量之比,由此可确定聚氯乙烯与聚乙烯的密度关系;氯乙烯燃烧时产生。
(2)PVDC 的单体为22CH CCl =,由此确定其同分异构体。
(3) a .该物质含碳、氢、氧三种元素;b .该物质中含有氧元素;c .该物质苯环上有2种不同性质的氢原子。
2020-2021高考化学备考之有机化合物压轴突破训练∶培优 易错 难题篇含答案

2020-2021高考化学备考之有机化合物压轴突破训练∶培优易错难题篇含答案一、有机化合物练习题(含详细答案解析)1.有机物种类繁多,结构复杂。
(1)下列各图均能表示甲烷的分子结构,其中甲烷的球棍模型是__(填序号,下同),表现甲烷的空间真实结构是__。
(2)下列有机物中所有原子可以在同一个平面上的是___(填序号)(3)如图是由4个碳原子结合成的6种有机物(氢原子没有画出)①上述有机物中与(c)互为同分异构体的是__(填序号)。
②写出有机物(a)的名称__。
③有机物(a)有一种同分异构体,试写出其结构简式__。
④写出与(c)互为同系物的最简单有机物和溴水反应的化学方程式:__;生成物的名称是___。
(4)某单烯烃与氢气加成后生成异戊烷,该烯烃的结构简式有__种。
(5)“立方烷”是一种新合成的烃,其分子为正方体结构。
如图表示立方烷,正方体的每个顶点是一个碳原子,氢原子均省略,一条短线表示一个共用电子对。
碳原子上的二个氢原子被氨基(-NH2)取代,同分异构体的数目有_种。
【答案】C D ABD bf 异丁烷 CH3CH2CH2CH3 CH2=CH2+Br2→CH2Br-CH2Br 1,2-二溴乙烷 3 3【解析】【分析】【详解】(1)甲烷的球棍模型是C,甲烷的电子式是B;A是分子结构示意图;D是比例模型;其中比例模型更能形象地表达出H、C的相对位置及所占比例;电子式只反映原子最外层电子的成键情况;(2)乙烯和苯分子中所有原子共平面,甲烷是正四面体结构,所以C不可能原子共面;D 苯环和碳碳双键之间的碳碳单键可以旋转,所有原子可以共平面;(3)①c为C4H8与它分子式相同,结构不同的为b、f,②由图示可知a为烷烃,含有4个C原子,主链含有3个C,甲基在2号C,是异丁烷③含有4个碳原子的烷烃有CH3CH(CH3)CH3和CH3CH2CH2CH3,a为CH3CH(CH3)CH3,则其同分异构体为:CH3CH2CH2CH3;④c为丁烯,单烯烃碳原子数目最少的是CH2=CH2;(4)加成反应不改变碳链结构,异戊烷CH3-CH2-CH(CH3)2两个甲基与碳相连的价键是相同的,所以烯烃的双键位置有三种,烯烃的结构就有三种;(5)在一个面上有邻位和对位两种;不在一个面上,有1种,即立方体体对角线一个顶点一个-NH2。
2020-2021高考化学有机化合物(大题培优 易错 难题)附答案

2020-2021高考化学有机化合物(大题培优易错难题)附答案一、有机化合物练习题(含详细答案解析)1.肉桂酸是合成香料、化妆品、医药、浆料和感光树脂等的重要原料,其结构简式是。
I.写出肉桂酸的反式结构: __________。
II.实验室可用下列反应制取肉桂酸。
已知药品的相关数据如下:苯甲醛乙酸酐肉桂酸乙酸互溶溶解度(25℃,g/100g 水)0.3遇水水解0.04相对分子质量10610214860实验步骤如下:第一步合成:向烧瓶中依次加入研细的无水醋酸钠、5.3g 苯甲醛和6.0g乙酸酐,振荡使之混合均匀。
在150~ 170℃加热1小时,保持微沸状态。
第二步粗品精制:将上述反应后得到的混合物趁热倒入圆底烧瓶中,并进行下列操作:请回答下列问题。
(1)检验粗产品中含有苯甲醛的实验方案是:取粗产品于试管中,加水溶解,滴入NaOH 溶液,将溶液调至碱性, _________。
(2)步骤①中肉桂酸与Na2CO3溶液反应的化学方程式是_________。
(3)若最后得到4.81g纯净的肉桂酸,则该反应中肉桂酸的产率是_________。
(4)符合下列条件的肉桂酸的同分异构体有_________种。
i.苯环上含有三个取代基;ii.该同分异构体遇FeCl3显色且能发生银镜反应。
写出其中任意一种同分异构体的结构简式: _________。
【答案】加入银氨溶液共热,若有银镜出现,说明含有苯甲醛(用新制氢氧化铜悬浊液鉴别也给分)65% 10 、、、、、、、、、【解析】【分析】I.两个相同原子或基团在双键两侧的为反式异构体;II. (1)根据醛基检验的方法进行分析;(2)步骤①中肉桂酸与Na2CO3溶液反应生成肉桂酸钠、二氧化碳和水;(3)根据反应,进行计算;(4)根据肉桂酸的结构简式结合条件进行分析。
【详解】I.两个相同原子或基团在双键两侧的为反式异构体,肉桂酸的反式结构为;II. (1)检验粗产品中含有苯甲醛的实验方案是:取粗产品于试管中,加水溶解,滴入NaOH 溶液,将溶液调至碱性,加入银氨溶液共热,若有银镜出现,说明含有苯甲醛(或加入新制氢氧化铜悬浊液,加热,产生砖红色沉淀,说明含有苯甲醛);(2)步骤①中肉桂酸与Na2CO3溶液反应生成肉桂酸钠、二氧化碳和水,反应的化学方程式是;(3)根据反应,5.3g 苯甲醛和6.0g 乙酸酐(过量)反应理论上可得肉桂酸的质量为5.3g 148/106/g mol g mol⨯=7.4g ,若最后得到4.81g 纯净的肉桂酸,则该反应中肉桂酸的产率是4.81g 100%657.4g⨯=%; (4)肉桂酸,符合条件的肉桂酸的同分异构体:i.苯环上含有三个取代基; ii.该同分异构体遇FeCl 3显色且能发生银镜反应,则含有酚羟基和醛基;符合条件的同分异构体的结构简式有、、、、、、、、、。
2020-2021高考化学有机化合物(大题培优 易错 难题)附答案

2020-2021高考化学有机化合物(大题培优易错难题)附答案一、有机化合物练习题(含详细答案解析)1.某些有机化合物的模型如图所示。
回答下列问题:(1)属于比例模型的是___(填“甲”、“乙”、“丙”、“丁”或“戊”,下同)。
(2)表示同一种有机化合物的是___。
(3)存在同分异构体的是___,写出其同分异构体的结构简式___。
(4)含碳量最低的是___,含氢量最低的分子中氢元素的质量百分含量是___(保留一位小数)。
(5)C8H10属于苯的同系物的所有同分异构体共有___种。
【答案】乙、丙甲、丙戊 CH3CH2CH2CH2CH3、CH3CH(CH3)CH2CH3、C(CH3)4甲、丙 16.7% 4【解析】【分析】甲、丁、戊分别是甲烷、丁烷、戊烷的球棍模型,乙、丙分别是乙烷和甲烷的比例模型。
【详解】(1)乙、丙能表示的是原子的相对大小及连接形式,属于比例模型;(2)甲、丙分别是甲烷的球棍模型与比例模型,属于同一种有机化合物;(3)存在同分异构体的是戊(戊烷),其同分异构体的结构简式CH3CH2CH2CH2CH3、CH3CH(CH3)CH2CH3、C(CH3)4;(4)烷烃的通式为C n H2n+2,随n值增大,碳元素的质量百分含量逐渐增大,含碳量最低的是甲烷,含氢量最低的分子是戊烷,氢元素的质量百分含量是126012×100%=16.7%;(5)C8H10属于苯的同系物,侧链为烷基,可能是一个乙基,如乙苯;也可以是二个甲基,则有邻二甲苯、间二甲苯和对二甲苯三种,则符合条件的同分异构体共有4种。
2.化合物W是合成一种抗心律失常药物的中间物质,一种合成该物质的路线如下:(1)ClCH 2CH 2C1的名称是____________。
(2)E 中不含氧的官能团的名称为____________。
(3)C 的分子式为__________,B→C 的反应类型是____________。
(4)筛选C→D 的最优反应条件(各组别条件得到的D 的产率不同)如下表所示: 组别 加料温度 反应溶剂 AlCl 3的用量(摩尔当量)① -30~0℃ 1 eq ② -20~-10℃1 eq③-20~-10℃ ClCH 2CH 2Cl1 eq上述实验筛选了________和________对物质D 产率的影响。
2020-2021备战高考化学知识点过关培优 易错 难题训练∶化学反应原理综合考查及详细答案

2020-2021备战高考化学知识点过关培优易错难题训练∶化学反应原理综合考查及详细答案一、化学反应原理综合考查1.丙烯腈(CH2=CHCN)是一种重要的化工原料,工业上可用“丙烯氨氧化法”生产,主要副产物有丙烯醛(CH2=CHCHO)和乙腈(CH3CN)等,回答下列问题:(1)以丙烯、氨、氧气为原料,在催化剂存在下生成丙烯腈(C3H3N)和副产物丙烯醛(C3H4O)的热化学方程式如下:①C3H6(g)+NH3(g)+32O2(g)=C3H3N(g)+3H2O(g) ΔH=-515kJ/mol①C3H6(g)+O2(g)=C3H4O(g)+H2O(g) ΔH=-353kJ/mol两个反应在热力学上趋势均很大,其原因是________;有利于提高丙烯腈平衡产率的反应条件是________;提高丙烯腈反应选择性的关键因素是________。
(2)图(a)为丙烯腈产率与反应温度的关系曲线,最高产率对应温度为460℃。
低于460℃时,丙烯腈的产率________(填“是”或者“不是”)对应温度下的平衡产率,判断理由是________;高于460℃时,丙烯腈产率降低的可能原因是________(双选,填标号)A.催化剂活性降低B.平衡常数变大C.副反应增多D.反应活化能增大(3)丙烯腈和丙烯醛的产率与n(氨)/n(丙烯)的关系如图(b)所示。
由图可知,最佳n (氨)/n(丙烯)约为1理由是_______________。
进料氨、空气、丙烯的理论体积约为________。
【答案】两个反应均为放热量大的反应降低温度,降低压强,催化剂不是该反应为放热反应,平衡产率应随温度升高而降低 AC 1 该比例下丙烯腈产率最高,而副产物丙烯醛产率最低 1:7.5:1【解析】【分析】(1)依据热化学方程式方向可知,两个反应均放热量大,即反应物和生成物的能量差大,因此热力学趋势大;有利于提高丙烯腈平衡产率需要改变条件使平衡正向进行,提高丙烯腈反应选择性的关键因素是催化剂;(2)因为该反应为放热反应,平衡产率应随温度升高而降低,即低于460℃时,对应温度下的平衡转化率曲线应该是下降的,但实际曲线是上升的,因此判断低于460℃时,丙烯腈的产率不是对应温度下的平衡转化率;产率降低主要从产率的影响因素进行考虑;(3)根据图像可知,当n(氨)/n(丙烯)约为1时,该比例下丙烯腈产率最高,而副产物丙烯醛产率最低,根据化学反应氨气、氧气、丙烯按1:1.5:1的体积比加入反应达到最佳状态,依据氧气在空气中约占20%计算条件比。
备战高考化学备考之有机化合物压轴突破训练∶培优 易错 难题篇含详细答案

备战高考化学备考之有机化合物压轴突破训练∶培优易错难题篇含详细答案一、有机化合物练习题(含详细答案解析)1.酪氨酸是一种生命活动不可缺少的氨基酸,它的结构简式如下:(1)酪氨酸能发生的化学反应类型有________(填字母)。
A.取代反应 B.氧化反应C.酯化反应 D.中和反应(2)在酪氨酸的同分异构体中,同时满足如下三个条件的,除酪氨酸外还有________种。
①属于氨基酸且“碳骨架”与酪氨酸相同;②与氯化铁溶液能发生显色反应;③氨基(—NH2)不与苯环直接相连。
(3)已知氨基酸能与碱反应,写出酪氨酸与足量的NaOH溶液反应的化学方程式:___________________。
【答案】ABCD 5【解析】【分析】【详解】(1)该有机物中含有羟基、氨基和羧基,所以具有羧酸、氨基酸和酚的性质,能和羧酸或氨基酸发生取代反应,酚也能发生取代反应;能和氢氧化钠发生中和反应,能与醇发生酯化反应;酚羟基及氨基能发生氧化反应,故答案为ABCD;(2)在酪氨酸的同分异构体中,①属于氨基酸且“碳骨架”与酪氨酸相同;②与氯化铁溶液能发生显色反应则含有酚羟基;③氨基(—NH2)不与苯环直接相连。
同时满足条件,除酪氨酸外还有共5种;(3)酪氨酸与足量的NaOH溶液反应生成和水,反应的化学方程式为:。
2.含氧有机化合物是重要的化学工业原料。
完成下列填空:(1)工业上,乙醇可以通过粮食发酵制取,也可由乙烯在一定条件下和__________反应制取。
(2)乙醇催化氧化生成乙醛,乙醛中的官能团为____________。
乙醛与环氧乙烷()互为____________。
(3)写出CH3COOH和CH3CH2OH发生酯化反应的化学方程式。
____________________________【答案】水醛基同分异构体浓硫酸3323232ΔCH COOH+CH CH OH→CH COOCH CH+H O【解析】【分析】(1)工业上,乙醇可以通过粮食发酵制取,也可由乙烯在一定条件下和水反应制取;(2)乙醛中的官能团为醛基-CHO, 乙醛与环氧乙烷()分子式相同,互为同分异构体;(3)CH3COOH和CH3CH2OH发生酯化反应的化学方程式:浓硫酸3323232ΔCH COOH+CH CH OH→CH COOCH CH+H O;【详解】(1)工业上,乙醇可以通过粮食发酵制取,也可由乙烯在一定条件下和水反应制取,故答案为:水;(2)乙醛中的官能团为醛基-CHO, 乙醛与环氧乙烷()分子式相同,互为同分异构体,故答案为:醛基;同分异构体;(3)CH3COOH和CH3CH2OH发生酯化反应的化学方程式:浓硫酸3323232ΔCH COOH+CH CH OH→CH COOCH CH+H O,故答案为:浓硫酸3323232ΔCH COOH+CH CH OH→CH COOCH CH+H O。
2020-2021高考化学备考之有机化合物压轴突破训练∶培优 易错 难题篇及答案
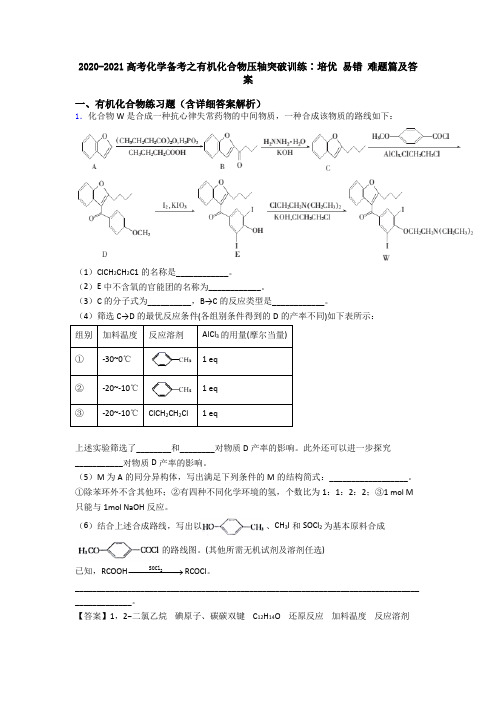
2020-2021高考化学备考之有机化合物压轴突破训练∶培优 易错 难题篇及答案一、有机化合物练习题(含详细答案解析)1.化合物W 是合成一种抗心律失常药物的中间物质,一种合成该物质的路线如下:(1)ClCH 2CH 2C1的名称是____________。
(2)E 中不含氧的官能团的名称为____________。
(3)C 的分子式为__________,B→C 的反应类型是____________。
(4)筛选C→D 的最优反应条件(各组别条件得到的D 的产率不同)如下表所示: 组别 加料温度 反应溶剂AlCl 3的用量(摩尔当量) ①-30~0℃ 1 eq ②-20~-10℃ 1 eq ③ -20~-10℃ ClCH 2CH 2Cl 1 eq上述实验筛选了________和________对物质D 产率的影响。
此外还可以进一步探究___________对物质D 产率的影响。
(5)M 为A 的同分异构体,写出满足下列条件的M 的结构简式:__________________。
①除苯环外不含其他环;②有四种不同化学环境的氢,个数比为1:1:2:2;③1 mol M 只能与1mol NaOH 反应。
(6)结合上述合成路线,写出以、CH 3I 和SOCl 2为基本原料合成的路线图。
(其他所需无机试剂及溶剂任选)已知,RCOOH 2SOCl −−−−−→RCOCl 。
____________________________________________________________________________________________。
【答案】1,2−二氯乙烷 碘原子、碳碳双键 C 12H 14O 还原反应 加料温度 反应溶剂氯化铝的用量322CH I ClCH C 1OH H K C −−−−−−→、+4KMnO (H )−−−−−−→2SOCl−−−−−→【解析】【分析】A 发生取代反应生成B ,B 发生还原反应生成C ,C 发生取代反应生成D ,D 发生取代反应生成E ,E 发生取代反应生成W ;(1)该分子中含有2个碳原子,氯原子位于1、2号碳原子上;(2)E 中含有的官能团是醚键、碳碳双键、羰基、碘原子、酚羟基;(3)根据结构简式确定分子式;B 分子去掉氧原子生成C ;(4)对比表中数据不同点确定实验筛选条件;还可以利用氯化铝量的不同探究氯化铝对D 产率的影响;(5)M 为A 的同分异构体,M 符合下列条件:①除苯环外不含其他环;②有四种不同化学环境的氢,个数比为1:1:2:2;③l mol M 只能与1 molNaOH 反应,说明含有1个酚羟基;根据其不饱和度知还存在1个碳碳三键;(6)以、CH 3I 和SOCl 2为基本原料合成,可由和SOCl 2发生取代反应得到,可由发生氧化反应得到,可由和CH 3I 发生取代反应得到。
2020-2021高考化学备考之化学反应原理压轴突破训练∶培优 易错 难题篇附答案(1)

2020-2021高考化学备考之化学反应原理压轴突破训练∶培优易错难题篇附答案(1)一、化学反应原理1.氨基磺酸(H2NSO3H)是一元固体强酸,俗称“固体硫酸”,易溶于水和液氨,不溶于乙醇,在工业上常用作酸性清洗剂、阻燃剂、磺化剂等。
某实验室用尿素和发烟硫酸(溶有SO3的硫酸)制备氨基磺酸的流程如图:已知“磺化”步骤发生的反应为:①CO(NH 2)2(s)+SO3(g)H2NCONHSO3H(s) ΔH<0②H 2NCONHSO3H+H2SO42H2NSO3H+CO2↑发生“磺化”步骤反应的装置如图1所示:请回答下列问题:(1)下列关于“磺化”与“抽滤”步骤的说法中正确的是____。
A.仪器a的名称是三颈烧瓶B.冷凝回流时,冷凝水应该从冷凝管的B管口通入C.抽滤操作前,应先将略小于漏斗内径却又能将全部小孔盖住的滤纸平铺在布氏漏斗中,稍稍润湿滤纸,微开水龙头,抽气使滤纸紧贴在漏斗瓷板上,再转移悬浊液D.抽滤结束后为了防止倒吸,应先关闭水龙头,再拆下连接抽气泵和吸滤瓶之间的橡皮管(2)“磺化”过程温度与产率的关系如图2所示,控制反应温度为75~80℃为宜,若温度高于80℃,氨基磺酸的产率会降低,可能的原因是____。
(3)“抽滤”时,所得晶体要用乙醇洗涤,则洗涤的具体操作是____。
(4)“重结晶”时,溶剂选用10%~12%的硫酸而不用蒸馏水的原因是____。
(5)“配液及滴定”操作中,准确称取2.500g氨基磺酸粗品配成250mL待测液。
取25.00mL待测液于锥形瓶中,以淀粉-碘化钾溶液做指示剂,用0.08000mol•L-1的NaNO2标准溶液进行滴定,当溶液恰好变蓝时,消耗NaNO2标准溶液25.00mL。
此时氨基磺酸恰好被完全氧化成N2,NaNO2的还原产物也为N2。
①电子天平使用前须____并调零校准。
称量时,可先将洁净干燥的小烧杯放在称盘中央,显示数字稳定后按____,再缓缓加样品至所需质量时,停止加样,读数记录。
2020-2021【化学】化学有机化合物的专项培优 易错 难题练习题(含答案)

2020-2021【化学】化学有机化合物的专项培优易错难题练习题(含答案)一、有机化合物练习题(含详细答案解析)1.华法林(Warfarin)又名杀鼠灵,为心血管疾病的临床药物。
其合成路线(部分反应条件略去)如下所示:回答下列问题:(1)A 的名称为________,E 中官能团名称为________。
(2)B 的结构简式为________。
(3)由 C 生成 D 的化学方程式为___________(4)⑤的反应类型为_________,⑧的反应类型为________。
(5)F 的同分异构体中,同时符合下列条件的同分异构体共有___________种。
a.能与 FeCl3溶液发生显色反应 b.含有-CHO其中核磁共振氢谱为五组峰的结构简式为___________【答案】甲苯酯基取代反应加成反应 13【解析】【分析】由A的分子式及产物的性质,可确定A为,在光照条件下发生-CH3上的取代反应生成B(),B发生水解反应生成C(),C催化氧化生成D(),D 与CH3COCH3在NaOH、加热条件下发生羟醛缩合反应,生成和水。
【详解】(1)A为,名称为甲苯,E为,官能团名称为酯基。
答案为:甲苯;酯基;(2)由以上分析知,B 的结构简式为。
答案为:;(3)C()催化氧化生成D(),化学方程式为。
答案为:;(4)⑤为与(CH3CO)2O在浓硫酸的催化作用下反应生成和CH3COOH,则反应类型为取代反应,⑧为与反应生成,反应类型为加成反应。
答案为:取代反应;加成反应;(5)F 的同分异构体中,同时符合:a.能与 FeCl3溶液发生显色反应、b.含有-CHO条件的同分异构体共有13种。
它们为苯环上有-OH(酚)、-CH2CHO两个取代基的异构体3种,苯环上有-OH(酚)、-CHO、-CH3三个取代基的异构体10种。
其中核磁共振氢谱为五组峰的结构简式为。
答案为:13;。
【点睛】F的13种同分异构体,含有3个取代基的异构体为,,(其中,-CH3位于序号所在的位置),(共3种)。
2020-2021高考化学培优易错试卷(含解析)之有机化合物及详细答案

2020-2021高考化学培优易错试卷(含解析)之有机化合物及详细答案一、有机化合物练习题(含详细答案解析)1.有机物种类繁多,结构复杂。
(1)下列各图均能表示甲烷的分子结构,其中甲烷的球棍模型是__(填序号,下同),表现甲烷的空间真实结构是__。
(2)下列有机物中所有原子可以在同一个平面上的是___(填序号)(3)如图是由4个碳原子结合成的6种有机物(氢原子没有画出)①上述有机物中与(c)互为同分异构体的是__(填序号)。
②写出有机物(a)的名称__。
③有机物(a)有一种同分异构体,试写出其结构简式__。
④写出与(c)互为同系物的最简单有机物和溴水反应的化学方程式:__;生成物的名称是___。
(4)某单烯烃与氢气加成后生成异戊烷,该烯烃的结构简式有__种。
(5)“立方烷”是一种新合成的烃,其分子为正方体结构。
如图表示立方烷,正方体的每个顶点是一个碳原子,氢原子均省略,一条短线表示一个共用电子对。
碳原子上的二个氢原子被氨基(-NH2)取代,同分异构体的数目有_种。
【答案】C D ABD bf 异丁烷 CH3CH2CH2CH3 CH2=CH2+Br2→CH2Br-CH2Br 1,2-二溴乙烷 3 3【解析】【分析】【详解】(1)甲烷的球棍模型是C,甲烷的电子式是B;A是分子结构示意图;D是比例模型;其中比例模型更能形象地表达出H、C的相对位置及所占比例;电子式只反映原子最外层电子的成键情况;(2)乙烯和苯分子中所有原子共平面,甲烷是正四面体结构,所以C不可能原子共面;D 苯环和碳碳双键之间的碳碳单键可以旋转,所有原子可以共平面;(3)①c为C4H8与它分子式相同,结构不同的为b、f,②由图示可知a为烷烃,含有4个C原子,主链含有3个C,甲基在2号C,是异丁烷③含有4个碳原子的烷烃有CH3CH(CH3)CH3和CH3CH2CH2CH3,a为CH3CH(CH3)CH3,则其同分异构体为:CH3CH2CH2CH3;④c为丁烯,单烯烃碳原子数目最少的是CH2=CH2;(4)加成反应不改变碳链结构,异戊烷CH3-CH2-CH(CH3)2两个甲基与碳相连的价键是相同的,所以烯烃的双键位置有三种,烯烃的结构就有三种;(5)在一个面上有邻位和对位两种;不在一个面上,有1种,即立方体体对角线一个顶点一个-NH2。
2020-2021高考化学二轮 有机化合物 专项培优 易错 难题及详细答案

2020-2021高考化学二轮有机化合物专项培优易错难题及详细答案一、有机化合物练习题(含详细答案解析)1.合成乙酸乙酯的路线如下:CH2=CH2C2H5OH CH3CHO CH3COOHCH3COOCH2CH3。
请回答下列问题:(1)乙烯能发生聚合反应,其产物的结构简式为_____。
.(2)乙醇所含的官能团为_____。
(3)写出下列反应的化学方程式.。
反应②:______,反应④:______。
(4)反应④的实验装置如图所示,试管B中在反应前加入的是_____。
【答案】 -OH 2CH3CH2OH+O22CH3CHO+2H2O CH3CH2OH+CH3COOH CH3COOCH2CH3+H2O 饱和碳酸钠溶液【解析】【分析】(1)乙烯能发生聚合反应生成聚乙烯;(2)反应②是乙醇的催化氧化生成乙醛和水;反应④是乙酸和乙醇在浓硫酸加热反应生成乙酸乙酯和水。
(3)反应②为乙醇催化氧化生成乙醛和水,反应④为乙酸和乙醇在浓硫酸加热反应生成乙酸乙酯和水。
【详解】(1)乙烯在一定条件下能发生加聚反应生成聚乙烯,其结构简式为,故答案为:;(2)乙醇的结构简式CH3CH2OH,含有的官能团为:-OH,故答案为:-OH;(3)反应②为乙醇催化氧化生成乙醛和水,其反应方程式为:2CH3CH2OH+O22CH3CHO+2H2O;反应④为乙酸和乙醇在浓硫酸加热反应生成乙酸乙酯和水,反应的化学方程式为:CH3CH2OH +CH3COOH CH3COOCH2CH3+H2O,故答案:2CH 3CH 2OH+O 22CH 3CHO+2H 2O ;CH 3CH 2OH+CH 3COOHCH 3COOCH 2CH 3+H 2O ;反应④为乙酸和乙醇在浓硫 酸加热反应制取乙酸乙酯,因为乙酸和乙醇沸点低易挥发,且都能溶于水,CH 3COOCH 2CH 3不溶于水,密度比水小,所以试管B 中在反应前加入的是饱和碳酸钠溶液,它可以降低乙酸乙酯的降解性,同时可以吸收乙酸,溶解乙醇,故答案:饱和碳酸钠溶液。
2020-2021高考化学压轴题之有机化合物(高考题型整理,突破提升)附答案

2020-2021高考化学压轴题之有机化合物(高考题型整理,突破提升)附答案一、有机化合物练习题(含详细答案解析)1.合成乙酸乙酯的路线如下:CH2=CH2C2H5OH CH3CHO CH3COOHCH3COOCH2CH3。
请回答下列问题:(1)乙烯能发生聚合反应,其产物的结构简式为_____。
.(2)乙醇所含的官能团为_____。
(3)写出下列反应的化学方程式.。
反应②:______,反应④:______。
(4)反应④的实验装置如图所示,试管B中在反应前加入的是_____。
【答案】 -OH 2CH3CH2OH+O22CH3CHO+2H2O CH3CH2OH+CH3COOH CH3COOCH2CH3+H2O 饱和碳酸钠溶液【解析】【分析】(1)乙烯能发生聚合反应生成聚乙烯;(2)反应②是乙醇的催化氧化生成乙醛和水;反应④是乙酸和乙醇在浓硫酸加热反应生成乙酸乙酯和水。
(3)反应②为乙醇催化氧化生成乙醛和水,反应④为乙酸和乙醇在浓硫酸加热反应生成乙酸乙酯和水。
【详解】(1)乙烯在一定条件下能发生加聚反应生成聚乙烯,其结构简式为,故答案为:;(2)乙醇的结构简式CH3CH2OH,含有的官能团为:-OH,故答案为:-OH;(3)反应②为乙醇催化氧化生成乙醛和水,其反应方程式为:2CH3CH2OH+O22CH3CHO+2H2O;反应④为乙酸和乙醇在浓硫酸加热反应生成乙酸乙酯和水,反应的化学方程式为:CH3CH2OH +CH3COOH CH3COOCH2CH3+H2O,故答案:2CH 3CH 2OH+O 22CH 3CHO+2H 2O ;CH 3CH 2OH+CH 3COOHCH 3COOCH 2CH 3+H 2O ;反应④为乙酸和乙醇在浓硫 酸加热反应制取乙酸乙酯,因为乙酸和乙醇沸点低易挥发,且都能溶于水,CH 3COOCH 2CH 3不溶于水,密度比水小,所以试管B 中在反应前加入的是饱和碳酸钠溶液,它可以降低乙酸乙酯的降解性,同时可以吸收乙酸,溶解乙醇,故答案:饱和碳酸钠溶液。
2020-2021备战高考化学备考之化学反应原理综合考查压轴突破训练∶培优 易错 难题篇附答案(1)

2020-2021备战高考化学备考之化学反应原理综合考查压轴突破训练∶培优易错难题篇附答案(1)一、化学反应原理综合考查1.(15分)甲烷水蒸气催化重整(SMR)是传统制取富氢混合气的重要方法,具有工艺简单、成本低等优点。
回答下列问题:(1)已知1000 K时,下列反应的平衡常数和反应热:①CH 4(g)C(s)+2H2(g) K1=10.2 ΔH1②2CO(g)C(s)+CO 2(g) K2=0.6 ΔH2③CO(g)+H 2O(g)CO2(g)+H2(g) K3=1.4 ΔH3④CH 4(g)+2H2O(g)CO2(g)+4H2(g) K4 ΔH4(SMR)则1000 K时,K4=____________;ΔH4=_________(用ΔH1、ΔH2、ΔH3来表示)。
(2)在进入催化重整装置前,先要对原料气进行脱硫操作,使其浓度为0.5 ppm以下。
脱硫的目的为______________。
(3)下图为不同温度条件下电流强度对CH4转化率的影响。
由图可知,电流对不同催化剂、不同温度条件下的甲烷水蒸气催化重整反应均有着促进作用,则可推知ΔH4____0(填“>”或“<”)。
(4)下图为不同温度条件下6小时稳定测试电流强度对H2产率的影响。
由图可知,随着温度的降低,电流对H2产率的影响作用逐渐____________(填“增加”“减小”或“不变”),600 ℃时,电流对三种催化剂中的____________(用图中的催化剂表示式回答)影响效果最为显著,当温度高于750 ℃时,无论电流强度大小,有无催化剂,H 2产率趋于相同,其原因是______________。
(5)我国科学家对甲烷和水蒸气催化重整反应机理也进行了广泛研究,通常认为该反应分两步进行。
第一步:CH 4催化裂解生成H 2和碳(或碳氢物种),其中碳(或碳氢物种)吸附在催化剂上,如CH 4→C ads /[C(H)n ]ads +(2–2n)H 2;第二步:碳(或碳氢物种)和H 2O 反应生成CO 2和H 2,如C ads /[C(H)n ]ads +2H 2O→CO 2 +(2+2n)H 2。
2020-2021高考化学备考之化学反应原理综合考查压轴突破训练∶培优 易错 难题篇及答案

2020-2021高考化学备考之化学反应原理综合考查压轴突破训练∶培优 易错难题篇及答案一、化学反应原理综合考查1.水蒸汽催化重整生物油是未来工业化制氢的可行方案。
以乙酸为模型物进行研究,发生的主要反应如下:Ⅰ.CH 3COOH (g )+2H 2O (g )⇌2CO 2(g )+4H 2(g ) △H 1 Ⅱ.CH 3COOH (g )⇌2CO (g )+2H 2(g ) △H 2 Ⅲ.CO 2(g )+H 2(g )⇌CO (g )+H 2O (g ) △H 3 回答下列问题:(1)用△H 1、△H 2表示,△H 3=___。
(2)重整反应的含碳产物产率、H 2产率随温度、水与乙酸投料比(S/C )的变化关系如图(a )、(b )所示。
①由图(a )可知,制备H 2最佳的温度约为___。
②由图(b )可知,H 2产率随S/C 增大而___(填“增大”或“减小”)。
(3)向恒容密闭容器中充入等物质的量的CH 3COOH 和H 2O 混合气体,若仅发生反应Ⅰ至平衡状态,测得H 2的体积分数为50%,则CH 3COOH 的平衡转化率为___。
(4)反应体系常生成积碳。
当温度一定时,随着S/C 增加,积碳量逐渐减小,其原因用化学方程式表示为___。
【答案】21H -H 2V V 800℃ 增大 40% C(s)+H 2O (g)CO(g)+H 2(g)【解析】 【分析】 【详解】(1)根据题干信息分析,反应Ⅲ=12(反应Ⅱ-反应Ⅰ),由盖斯定律可得213-2H H H ∆∆∆=,故答案为:21-2H H ∆∆; (2)①由图(a)可知,制备H 2在800℃时,达到最高转化率,则制备氢气最佳的温度约为800℃,故答案为:800℃;②由图(b)可知,S/C 增大时,反应I 平衡向正反应方向移动,反应III 平衡向逆反应方向移动,使体系中的H 2的量增大,故答案为:增大;(3)设CH 3COOH 和H 2O 的物质的量均为1mol ,平衡时,反应了CH 3COOH x mol ,列三段式有:()()()()()()()3222CH COOH g +2H O g 2CO g + 4H g mol 1100mol x 2x 2x 4x mol 1-x1-2x2x4xƒ起始转化平衡测得H 2的体积分数为50%,则41112242x x x x x =-+-++,计算得x=0.4mol ,醋酸的转化率为:0.4mol100%1mol⨯=40%,即CH 3COOH 平衡转化率为40%,故答案为:40%; (4)当温度一定时,随着S/C 增加,积碳量逐渐减小,是由于积碳与水蒸气反应生成了CO 和H 2,反应的化学方程式为C(s)+H 2O (g)CO(g)+H 2(g),故答案为:C(s)+H 2O (g)CO(g)+H 2(g);2.丙烯腈(CH 2=CHCN )是一种重要的化工原料,工业上可用“丙烯氨氧化法”生产,主要副产物有丙烯醛(CH 2=CHCHO )和乙腈(CH 3CN )等,回答下列问题:(1)以丙烯、氨、氧气为原料,在催化剂存在下生成丙烯腈(C 3H 3N )和副产物丙烯醛(C 3H 4O )的热化学方程式如下:①C 3H 6(g)+NH 3(g)+32O 2(g)=C 3H 3N(g)+3H 2O(g) ΔH =-515kJ/mol ①C 3H 6(g)+O 2(g)=C 3H 4O(g)+H 2O(g) ΔH =-353kJ/mol两个反应在热力学上趋势均很大,其原因是________;有利于提高丙烯腈平衡产率的反应条件是________;提高丙烯腈反应选择性的关键因素是________。
2020-2021备战高考化学压轴题之有机化合物(备战高考题型整理,突破提升)含答案

2020-2021备战高考化学压轴题之有机化合物(备战高考题型整理,突破提升)含答案一、有机化合物练习题(含详细答案解析)1.有机物种类繁多,结构复杂。
(1)下列各图均能表示甲烷的分子结构,其中甲烷的球棍模型是__(填序号,下同),表现甲烷的空间真实结构是__。
(2)下列有机物中所有原子可以在同一个平面上的是___(填序号)(3)如图是由4个碳原子结合成的6种有机物(氢原子没有画出)①上述有机物中与(c)互为同分异构体的是__(填序号)。
②写出有机物(a)的名称__。
③有机物(a)有一种同分异构体,试写出其结构简式__。
④写出与(c)互为同系物的最简单有机物和溴水反应的化学方程式:__;生成物的名称是___。
(4)某单烯烃与氢气加成后生成异戊烷,该烯烃的结构简式有__种。
(5)“立方烷”是一种新合成的烃,其分子为正方体结构。
如图表示立方烷,正方体的每个顶点是一个碳原子,氢原子均省略,一条短线表示一个共用电子对。
碳原子上的二个氢原子被氨基(-NH2)取代,同分异构体的数目有_种。
【答案】C D ABD bf 异丁烷 CH3CH2CH2CH3 CH2=CH2+Br2→CH2Br-CH2Br 1,2-二溴乙烷 3 3【解析】【分析】【详解】(1)甲烷的球棍模型是C,甲烷的电子式是B;A是分子结构示意图;D是比例模型;其中比例模型更能形象地表达出H、C的相对位置及所占比例;电子式只反映原子最外层电子的成键情况;(2)乙烯和苯分子中所有原子共平面,甲烷是正四面体结构,所以C不可能原子共面;D 苯环和碳碳双键之间的碳碳单键可以旋转,所有原子可以共平面;(3)①c为C4H8与它分子式相同,结构不同的为b、f,②由图示可知a为烷烃,含有4个C原子,主链含有3个C,甲基在2号C,是异丁烷③含有4个碳原子的烷烃有CH3CH(CH3)CH3和CH3CH2CH2CH3,a为CH3CH(CH3)CH3,则其同分异构体为:CH3CH2CH2CH3;④c为丁烯,单烯烃碳原子数目最少的是CH2=CH2;(4)加成反应不改变碳链结构,异戊烷CH3-CH2-CH(CH3)2两个甲基与碳相连的价键是相同的,所以烯烃的双键位置有三种,烯烃的结构就有三种;(5)在一个面上有邻位和对位两种;不在一个面上,有1种,即立方体体对角线一个顶点一个-NH2。
2020-2021备战高考化学备考之有机化合物压轴突破训练∶培优 易错 难题篇及详细答案

2020-2021备战高考化学备考之有机化合物压轴突破训练∶培优易错难题篇及详细答案一、有机化合物练习题(含详细答案解析)1.含绒量是决定羽绒服质量优劣最重要的指标,按照我国实施的羽绒服新国标,羽绒服的含绒量要在50%以上,一些不法厂家填充“飞丝”或“人造羊毛来假冒羽绒,严重损害消费者的利益。
“飞丝”由鸭毛、鹅毛甚至鸡毛经粉碎而成,人造羊毛的主要成分是聚丙烯腈纤维。
请回答下列问题:Ⅰ.鸭绒、蚕丝、人造羊毛都是高分子化合物,下列说法正确的是________(填序号)。
A.通过灼烧的方法可鉴别羽绒服中填充的是鸭绒还是飞丝B.将人造羊毛和棉花进行混纺可提高纤维的性能C.鸭绒、蚕丝、人造羊毛都有固定的熔沸点D.鸭绒、蚕丝、人造羊毛燃烧过程中不会产生有毒气体Ⅱ.合成聚丙烯腈纤维的方法很多,如以乙炔为原料,其合成过程如下:CH≡CH+HCN CH2=CHCN聚丙烯腈(1)反应①的反应类型为__________。
(2)写出反应②的化学方程式:__________________,其反应类型为_________。
(3)CH2=CHCN在一定条件下可与苯乙烯()反应得到一种优良的塑料,该塑料的结构简式为__________。
【答案】B 加成反应 nCH2=CHCN加聚反应(或)【解析】【分析】I.根据物质的组成成分、元素组成、物质的性质分析解答;II.乙炔与HCN发生加成反应产生CH2=CHCN,CH2=CHCN发生加聚反应产生聚丙烯腈。
CH2=CHCN与苯乙烯()在一定条件下可发生加聚反应产生高聚物、。
【详解】Ⅰ.A.鸭绒和飞丝的主要成分都属于蛋白质,在灼烧过程中都有烧焦羽毛的气味,故不能用灼烧的方法鉴别,A错误;B.人造羊毛属于合成纤维,优点在于强度高、弹性好、耐磨、耐化学腐蚀、不发霉、不怕虫蛀、不缩水等,其缺点在于不透气、不吸汗等,棉花则具有吸汗、透气性强的优点,但又有不耐磨、不耐腐蚀的缺点,若把它和棉花混纺,这样制成的混纺织物兼有两类纤维的优点,B正确;C.高分子化合物都属于混合物,混合物没有固定的熔、沸点,C错误;D.鸭绒飞丝、人造羊毛组成成分是蛋白质,含有C、H、O、N元素,有的蛋白质还含有S 元素,在燃烧过程中会释放出如SO2、CO、氮氧化物等有毒气体,D错误;故合理选项是B;Ⅱ.(1) CH≡CH 与HCN发生加成反应生成CH2=CHCN,故①反应的反应类型为加成反应;(2)CH2=CHCN在引发剂作用下发生加聚反应生成聚丙烯腈,反应方程式为:nCH2=CHCN;(3)CH2=CHCN在一定条件下可与苯乙烯()在一定条件下发生加聚反应产生高聚物或。
备战高考化学备考之有机化合物压轴突破训练∶培优 易错 难题篇及答案

备战高考化学备考之有机化合物压轴突破训练∶培优易错难题篇及答案一、有机化合物练习题(含详细答案解析)1.合成乙酸乙酯的路线如下:CH2=CH2C2H5OH CH3CHO CH3COOHCH3COOCH2CH3。
请回答下列问题:(1)乙烯能发生聚合反应,其产物的结构简式为_____。
.(2)乙醇所含的官能团为_____。
(3)写出下列反应的化学方程式.。
反应②:______,反应④:______。
(4)反应④的实验装置如图所示,试管B中在反应前加入的是_____。
【答案】 -OH 2CH3CH2OH+O22CH3CHO+2H2O CH3CH2OH+CH3COOH CH3COOCH2CH3+H2O 饱和碳酸钠溶液【解析】【分析】(1)乙烯能发生聚合反应生成聚乙烯;(2)反应②是乙醇的催化氧化生成乙醛和水;反应④是乙酸和乙醇在浓硫酸加热反应生成乙酸乙酯和水。
(3)反应②为乙醇催化氧化生成乙醛和水,反应④为乙酸和乙醇在浓硫酸加热反应生成乙酸乙酯和水。
【详解】(1)乙烯在一定条件下能发生加聚反应生成聚乙烯,其结构简式为,故答案为:;(2)乙醇的结构简式CH3CH2OH,含有的官能团为:-OH,故答案为:-OH;(3)反应②为乙醇催化氧化生成乙醛和水,其反应方程式为:2CH3CH2OH+O22CH3CHO+2H2O;反应④为乙酸和乙醇在浓硫酸加热反应生成乙酸乙酯和水,反应的化学方程式为:CH3CH2OH +CH3COOH CH3COOCH2CH3+H2O,故答案:2CH3CH2OH+O22CH3CHO+2H2O;CH3CH2OH+CH3COOH CH3COOCH2CH3+H2O;反应④为乙酸和乙醇在浓硫酸加热反应制取乙酸乙酯,因为乙酸和乙醇沸点低易挥发,且都能溶于水,CH3COOCH2CH3不溶于水,密度比水小,所以试管B中在反应前加入的是饱和碳酸钠溶液,它可以降低乙酸乙酯的降解性,同时可以吸收乙酸,溶解乙醇,故答案:饱和碳酸钠溶液。
2020-2021高考化学备考之有机化合物压轴突破训练∶培优 易错 难题篇及详细答案

2020-2021高考化学备考之有机化合物压轴突破训练∶培优易错难题篇及详细答案一、有机化合物练习题(含详细答案解析)1.霉酚酸酯(MMF)是器官移植中抑制细胞增殖最常用的药物。
它能在酸性溶液中能发生如下反应:(1)有机物(I)在铂催化下与足量的氢气发生加成反应生成物质X,X所含的官能团的名称是__________;X的结构简式为__________。
(2)有机物(II)的化学式为_______;分子中化学环境不同的氢原子共有_____种。
(3)下列关于MMF说法正确的是__________(选填字母编号)。
a.能溶于水b.1 mol MMF最多能与3 mol NaOH完全反应c.能发生取代反应和消去反应d.镍催化下1 mol MMF最多能与6 mol H2发生加成反应(4)1 mol的有机物(I)在单质铜和氧气的作用下可以氧化为醛基的—OH有____mol;有机物(II)在加热和浓硫酸的条件下发生消去反应的化学方程式为_________。
【答案】羧基、羟基 C6H13O2N 5 b 1【解析】【分析】(1)有机物(I)在铂催化下与足量的H2发生加成反应生成物质X,和H2发生加成反应的是苯环和碳碳双键,根据有机物(Ⅰ)结构判断X的结构,根据X的结构判断含有的官能团。
(2)根据断键方式和原子守恒判断有机物(Ⅱ)的化学式,断键物质为酯基,根据氢原子的物质判断其种类。
(3)根据MMF的结构判断其性质,MMF中含有的官能团是酚羟基、碳碳双键、酯基,可能具有酚、酯和烯烃的性质。
(4)连有醇羟基的碳原子上有2个氢原子时,醇羟基才能发生催化氧化生成醛;醇若能发生消去反应,消去反应后生成物含有碳碳双键。
【详解】(1)有机物(Ⅰ)在铂催化下与足量的H2发生加成反应生成物质X,能和H2发生加成反应的是苯环和碳碳双键,X的结构简式为,可见X含有的官能团是羧基和羟基;(2)在酸性、加热条件下,MMF能发生水解反应生成有机物(Ⅰ)和有机物(Ⅱ),断键部位是酯基,根据原子守恒判断有机物(Ⅱ),所以有机物(Ⅱ)的结构简式为,所以该有机物的分子式为C6H13O2N;该分子中化学环境不同的氢原子共有5种;(3)a.该有机物中含有酯基,酯类物质是不易溶于水的,a错误;b.该有机物能和氢氧化钠反应的是酯基和酚羟基,所以1 molMMF最多能与3 molNaOH 完全反应,b正确;c.苯环酚羟基的邻对位上不含有氢原子,所以不能和溴水发生取代反应;该分子没有醇羟基,所以不能发生消去反应,c错误;d.能与H2发生加成反应的有苯环和碳碳双键,所以镍催化下1 molMMF最多能与4 mol H2发生加成反应,d错误;故合理选项是b;(4)该有机物分子中只有醇羟基能被催化氧化生成醛基,所以1 mol的有机物(Ⅰ)在单质铜的催化下可以氧化为醛基的-OH有1 mol;有机物(Ⅱ)在加热和浓硫酸的发生消去反应生成含有碳碳双键的有机物,反应方程式为。
2020-2021高考化学压轴题之有机化合物(高考题型整理,突破提升)及详细答案
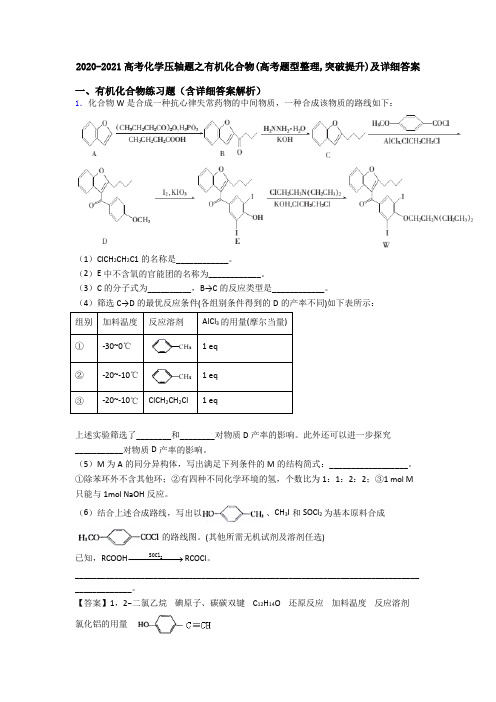
2020-2021高考化学压轴题之有机化合物(高考题型整理,突破提升)及详细答案一、有机化合物练习题(含详细答案解析)1.化合物W 是合成一种抗心律失常药物的中间物质,一种合成该物质的路线如下:(1)ClCH 2CH 2C1的名称是____________。
(2)E 中不含氧的官能团的名称为____________。
(3)C 的分子式为__________,B→C 的反应类型是____________。
(4)筛选C→D 的最优反应条件(各组别条件得到的D 的产率不同)如下表所示: 组别 加料温度 反应溶剂AlCl 3的用量(摩尔当量) ①-30~0℃ 1 eq ②-20~-10℃ 1 eq ③ -20~-10℃ ClCH 2CH 2Cl 1 eq上述实验筛选了________和________对物质D 产率的影响。
此外还可以进一步探究___________对物质D 产率的影响。
(5)M 为A 的同分异构体,写出满足下列条件的M 的结构简式:__________________。
①除苯环外不含其他环;②有四种不同化学环境的氢,个数比为1:1:2:2;③1 mol M 只能与1mol NaOH 反应。
(6)结合上述合成路线,写出以、CH 3I 和SOCl 2为基本原料合成的路线图。
(其他所需无机试剂及溶剂任选)已知,RCOOH 2SOCl −−−−−→RCOCl 。
____________________________________________________________________________________________。
【答案】1,2−二氯乙烷 碘原子、碳碳双键 C 12H 14O 还原反应 加料温度 反应溶剂 氯化铝的用量322CH I ClCH C 1OH H K C −−−−−−→、+4KMnO (H )−−−−−−→2SOCl−−−−−→【解析】【分析】A 发生取代反应生成B ,B 发生还原反应生成C ,C 发生取代反应生成D ,D 发生取代反应生成E ,E 发生取代反应生成W ;(1)该分子中含有2个碳原子,氯原子位于1、2号碳原子上;(2)E 中含有的官能团是醚键、碳碳双键、羰基、碘原子、酚羟基;(3)根据结构简式确定分子式;B 分子去掉氧原子生成C ;(4)对比表中数据不同点确定实验筛选条件;还可以利用氯化铝量的不同探究氯化铝对D 产率的影响;(5)M 为A 的同分异构体,M 符合下列条件:①除苯环外不含其他环;②有四种不同化学环境的氢,个数比为1:1:2:2;③l mol M 只能与1 molNaOH 反应,说明含有1个酚羟基;根据其不饱和度知还存在1个碳碳三键;(6)以、CH 3I 和SOCl 2为基本原料合成,可由和SOCl 2发生取代反应得到,可由发生氧化反应得到,可由和CH 3I 发生取代反应得到。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
2020-2021备战高考化学备考之有机化合物压轴突破训练∶培优易错难题篇及答案一、有机化合物练习题(含详细答案解析)1.合成乙酸乙酯的路线如下:CH2=CH2C2H5OH CH3CHO CH3COOHCH3COOCH2CH3。
请回答下列问题:(1)乙烯能发生聚合反应,其产物的结构简式为_____。
.(2)乙醇所含的官能团为_____。
(3)写出下列反应的化学方程式.。
反应②:______,反应④:______。
(4)反应④的实验装置如图所示,试管B中在反应前加入的是_____。
【答案】 -OH 2CH3CH2OH+O22CH3CHO+2H2O CH3CH2OH+CH3COOH CH3COOCH2CH3+H2O 饱和碳酸钠溶液【解析】【分析】(1)乙烯能发生聚合反应生成聚乙烯;(2)反应②是乙醇的催化氧化生成乙醛和水;反应④是乙酸和乙醇在浓硫酸加热反应生成乙酸乙酯和水。
(3)反应②为乙醇催化氧化生成乙醛和水,反应④为乙酸和乙醇在浓硫酸加热反应生成乙酸乙酯和水。
【详解】(1)乙烯在一定条件下能发生加聚反应生成聚乙烯,其结构简式为,故答案为:;(2)乙醇的结构简式CH3CH2OH,含有的官能团为:-OH,故答案为:-OH;(3)反应②为乙醇催化氧化生成乙醛和水,其反应方程式为:2CH3CH2OH+O22CH3CHO+2H2O;反应④为乙酸和乙醇在浓硫酸加热反应生成乙酸乙酯和水,反应的化学方程式为:CH 3CH 2OH +CH 3COOHCH 3COOCH 2CH 3+H 2O ,故答案:2CH 3CH 2OH+O 22CH 3CHO+2H 2O ;CH 3CH 2OH +CH 3COOH CH 3COOCH 2CH 3+H 2O ; 反应④为乙酸和乙醇在浓硫 酸加热反应制取乙酸乙酯,因为乙酸和乙醇沸点低易挥发,且都能溶于水,CH 3COOCH 2CH 3不溶于水,密度比水小,所以试管B 中在反应前加入的是饱和碳酸钠溶液,它可以降低乙酸乙酯的降解性,同时可以吸收乙酸,溶解乙醇,故答案:饱和碳酸钠溶液。
2.为探究乙烯与溴的加成反应,甲同学设计并进行如下实验:先取一定量的工业用乙烯气体(在储气瓶中),使气体通入溴水中,发现溶液褪色,即证明乙烯与溴水发生了加成反应;乙同学发现在甲同学的实验中,褪色后的溶液里有少许淡黄色浑浊物质,推测在工业上制得的乙烯中还可能含有少量还原性气体杂质,由此他提出必须先除去杂质,再让乙烯与溴水反应。
请回答下列问题:(1)甲同学设计的实验________(填“能”或“不能”)验证乙烯与溴发生了加成反应,其理由是________(填序号)。
①使溴水褪色的反应不一定是加成反应②使溴水褪色的反应就是加成反应③使溴水褪色的物质不一定是乙烯④使溴水褪色的物质就是乙烯(2)乙同学推测此乙烯中一定含有的一种杂质气体是________,它与溴水反应的化学方程式是________________。
在实验前必须全部除去,除去该杂质的试剂可用________。
(3)为验证乙烯与溴发生的反应是加成反应而不是取代反应,丙同学提出可用pH 试纸来测试反应后溶液的酸性,理由是_____________________________________________________________________________。
【答案】不能 ①③ 2H S 22H S Br 2HBr S ++↓ NaOH 溶液(答案合理即可) 若乙烯与2Br 发生取代反应,必定生成HBr ,溶液的酸性会明显增强,若乙烯与2Br 发生加成反应,则生成22CH BrCH Br ,溶液的酸性变化不大,故可用pH 试纸予以验证【解析】【分析】根据乙同学发现在甲同学的实验中,褪色后的溶液里有少许淡黄色浑浊物质,推测在工业上制得的乙烯中还可能含有少量还原性气体杂质,该淡黄色的浑浊物质应该是具有还原性的硫化氢与溴水发生氧化还原反应生成的硫单质,反应方程式为22H S Br 2HBr S =++↓,据此分析解答。
【详解】(1)根据乙同学发现在甲同学的实验中,褪色后的溶液里有少许淡黄色浑浊物质,推测在工业上制得的乙烯中还可能含有少量还原性气体杂质,则可能是该还原性气体与溴水发生氧化还原反应,使溴水褪色,则溴水褪色不能证明是乙烯与溴水发生了加成反应,所以①③正确,故答案为:不能;①③;(2)淡黄色的浑浊物质是具有还原性的硫化氢与溴水发生氧化还原反应生成的硫单质,反应方程式为22H S Br 2HBr S =++↓;选用的除杂试剂能够除去硫化氢气体,但是不能与乙烯反应,也不能引入新的气体杂质,根据除杂原则,可以选用NaOH 溶液,故答案为:2H S ;22H S Br 2HBr S =++↓;NaOH 溶液(答案合理即可);(3)若乙烯与2Br 发生取代反应,必定生成HBr ,溶液的酸性会明显增强,若乙烯与2Br 发生加成反应,则生成22CH BrCH Br ,溶液的酸性变化不大,故可用pH 试纸予以验证,故答案为:若乙烯与2Br 发生取代反应,必定生成HBr ,溶液的酸性会明显增强,若乙烯与2Br 发生加成反应,则生成22CH BrCH Br ,溶液的酸性变化不大,故可用pH 试纸予以验证。
3.苏联科学家欧巴林教授在其著作中曾说:“生命起源于甲烷”,英国科学家巴纳尔教授则认为生命是从二氧化碳和水开始的。
与之相关的转化关系如图所示(部分反应条件已略去):(1)A 的结构式为________;C 中官能团的电子式为________;反应②的反应类型为________。
(2)写出下列物质的结构简式:D ________;H ________。
(3)C→D 的化学方程式为__________;二氧化碳和水经光合作用生成葡萄糖的化学方程式为_________。
(4)在自然界中纤维素与水可在甲烷菌的催化作用下生成甲烷和二氧化碳,写出该反应的化学方程式并配平:_____。
【答案】H —C≡C—H 加成反应 CH 3CHO 2CH 3CH 2OH +O 22CH 3CHO +2H 2O 6CO 2+6H 2O C 6H 12O 6+6O 2 (C 6H 10O 5)n +n H 2O 3n CH 4↑+3n CO 2↑【解析】【分析】根据题中物质的转化关系可知,A 为HC≡CH,与氢气发生加成反应得到B ,B 为CH 2=CH 2,B 与水加成得到C ,C 为CH 3CH 2OH ,C 被氧化得到D ,D 为CH 3CHO ,D 被氧化得到E ,E 为CH 3COOH ,E 与C 发生酯化反应得到F ,F 为CH 3COOCH 2CH 3,A 与氯化氢加成得到G ,G 为CH 2=CHCl ,G 发生加聚反应得到H ,H 为。
【详解】(1) A 为HC≡CH,A 的结构式为H —C≡C—H ;C 为CH 3CH 2OH ,官能团的电子式为;反应②是乙炔与氯化氢发生加成反应生成氯乙烯,反应类型为加成反应;(2) D 的结构简式为CH 3CHO ;H 的结构简式为;(3)C→D 的化学方程式为2CH 3CH 2OH +O 22CH 3CHO +2H 2O ;二氧化碳和水经光合作用生成葡萄糖的化学方程式为6CO 2+6H 2O C 6H 12O 6+6O 2;(4)在自然界中纤维素与水可在甲烷菌的催化作用下生成甲烷和二氧化碳,反应的化学方程式为:(C 6H 10O 5)n +n H 2O3n CH 4↑+3n CO 2↑。
【点睛】本题考查有机物推断,解题时注意有机物官能团的相互转化,解题关键是掌握官能团的性质,难度不大,注意有机基础知识的灵活运用。
4.电石法(乙炔法)制氯乙烯是最早完成工业化的生产氯乙烯的方法。
反应原理为HC≡CH+HCl 2HgCl /100-180−−−−−→℃活性炭CH 2=CHCl(HgCl 2/活性炭作催化剂)。
某学习小组的同学用下列装置测定该反应中乙炔的转化率(不考虑其他副反应)。
铁架台及夹持仪器未画出。
(已知2CH CHCl =的熔点为-159.8℃,沸点为-134℃。
乙炔、氯乙烯、氯化氢均不溶于液体A)(1)各装置的连接顺序为(箭头方向即为气流方向):_________→________→_________→h→_________→______→_________→__________ (2)戊装置除了均匀混合气体之外,还有_________和_________的作用。
(3)乙装置中发生反应的化学方程式为_________________________________。
(4)若实验所用的电石中含有1.28gCaC 2,甲装置中产生0.02mol 的HCl 气体。
则所选用的量筒的容积较合理的是_______(填字母代号)。
A .500mlB .1000mlC .2000ml(5)假定在标准状况下测得庚中收集到的液体A 的体积为672ml(导管内气体体积忽略不计),则乙炔的转化率为_________。
【答案】b f e g c d j 干燥气体 观察气体流速22222CaC 2H O Ca(OH)C H +→+↑ B 50%【解析】【分析】(1)根据反应过程可知,装置乙的作用为制取乙炔,利用装置丁除去杂质后,在戊装置中干燥、控制气体流速以及使气体混合均匀,在装置丙中发生反应后生成氯乙烯,利用装置己和庚测定气体的体积,据此连接装置;(2)装置乙中制得的乙炔,利用装置丁除去杂质后,与装置甲制得的HCl 在戊装置中干燥、控制气体流速以及使气体混合均匀后在装置丙中发生反应后生成氯乙烯,由此确定装置戊的作用;(3)乙装置中发生的反应为电石与水生成乙炔和氢氧化钙;(4)碳化钙的物质的量为 1.28g 0.02mol 64g /mol=,可计算出0.02molHCl 反应产生的氯乙烯在标准状况下的体积,再考虑乙炔不能全部转化及乙炔、氯乙烯、氯化氢均不溶于液体A , 据此选择量筒的体积;(5)碳化钙的物质的量为 1.28g 0.02mol 64g /mol=,可计算出乙炔与0.02molHCl 气体的总体积,乙炔、氯乙烯、氯化氢均不溶于液体A ,由此可计算出乙炔的转化率。
【详解】(1)根据给定装置图分析可知甲装置用于制取氯化氢,乙装置用于制取乙炔,丙装置用于氯乙烯的制备,丁装置用于除去乙炔中的杂质,戊装置用于干燥、控制气体流速以及使气体混合均匀,己和庚用于测定气体的体积,所以装置的连接顺序为:b ;f ;e ;g ; c ;d ;j ;(2)戊装置用于干燥、控制气体流速以及使气体混合均匀等;(3)碳化钙与水反应的化学方程式为:22222CaC 2H O Ca(OH)C H +→+↑;(4)碳化钙的物质的量为 1.28g 0.02mol 64g /mol=,与0.02molHCl 反应产生的氯乙烯在标准状况下的体积为0.02mol ×22.4L/mol=0.448L=448ml ,考虑乙炔不能全部转化及乙炔、氯乙烯、氯化氢均不溶于液体A , 所以应选取1000mL 的量筒;(5)碳化钙的物质的量为 1.28g 0.02mol 64g /mol=,故乙炔与0.02molHCl 气体的总体积在标准状况下为(0.02mol+0.02mol) ×22.4L/mol=0.896L=896mL ,乙炔、氯乙烯、氯化氢均不溶于液体A ,所以乙炔的转化率为224mL 10050448mL ⨯=%%。
