二苯基乙二酮结构和电子光谱的理论研究
安息香衍生物二苯乙二酮的合成及表征

研究结论
01
安息香衍生物二苯乙二酮的合成方法具有较高的效率
和选择性,为该类化合物的制备提供了新的途径。
02
通过表征手段证实了合成产物的结构和性质,表明合
成方法具有较高的可靠性和准确性。
03
该合成方法在实验室条件下具有良好的可重复性,为
进一步优化和扩大生产规模奠定了基础。
研究展望
深入研究合成方法的反应机理和影响因素,以 提高合成效率和产物纯度,降低生产成本。
04
安息香衍生物二苯乙二酮的 表征结果
红外光谱分析结果
红外光谱分析是一种常用的化学分析方法,通过测量物质对红外光的吸收 特性来推断物质的结构。
对于安息香衍生物二苯乙二酮,红外光谱分析可以检测到苯环的振动峰、 羰基的伸缩振动峰以及可能的取代基的振动峰。
通过与标准谱图对比,可以初步确定安息香衍生物二苯乙二酮的结构。
合成步骤
准备原料
混合与加热
准备好所需的苯甲醛、苯乙 酮、催化剂和其他辅助试剂。
将苯甲醛、苯乙酮和催化剂 按照一定的比例混合,加热 至适当的温度,通常在80120℃之间。
反应与冷却
保持一定的反应时间,使原 料充分反应,然后冷却至室 温。
分离与纯化
通过蒸馏或其他分离方法, 去除多余的试剂和副产物, 得到纯化的安息香衍生物二 苯乙二酮。
苯甲醛、苯乙酮和催化剂之间的配比也需优化,以达到最佳的合成效 果。
03
安息香衍生物二苯乙二酮的 表征技术
红外光谱分析
总结词
红外光谱分析是一种常用的表征手段 ,用于确定分子中的官能团和化学键 。
详细描述
通过红外光谱分析,可以检测到安息 香衍生物二苯乙二酮分子中的特征振 动模式,从而确定其化学结构和组成 。
二苯基乙二酮的制备

安息香衍生物二苯乙二酮的合成及表征一、实验目的:1.学习安息香氧化制备α—二酮的原理与方法。
2.掌握薄层色谱的原理,薄层板的制作。
3.学习薄层色谱法跟踪反应进程。
二、实验原理:(一)薄层色谱的有关知识薄层色谱法是以薄层板作为载体,让样品溶液在薄层板上展开而达到分离的目的,故也称为薄层层析。
它是快速分离和定性分析少量物质的一种广泛使用的实验技术,可用于精制样品、化合物鉴定、跟踪反应进程和柱色谱的先导(即为柱色谱摸索最佳条件)等方面。
1.薄层色谱常用的吸附剂硅胶和氧化铝是薄层层析常用的固相吸附剂。
化合物极性越大,它在硅胶和氧化铝上的吸附力越强,所以吸附剂均制成活性精细粉末。
活化通常是加热粉末以脱去水分。
硅胶是酸性的,用来分离酸性或中性的化合物。
氧化铝有酸性、中性和碱性的,可用于分离极性或非极性的化合物。
商用的硅胶和氧化铝薄层板可以买到,这些薄板常用玻璃或塑料制成。
溶剂在薄层板上爬升的距离越长,化合物的分离效果越好。
宽的薄层板也可用于量较大的样品,具有1~2 mm厚的大板可用于50~1000 mg样品的分离制备。
2.样品的制备与点样样品必须溶解在挥发性的有机溶剂中,浓度最好是1~2 %。
溶剂应具有高的挥发性以便于立即蒸发。
丙酮、二氯甲烷和氯仿等是常用的有机溶剂。
分析固体样品时,可将20~40mg样品溶到2mL 的溶剂中。
在距薄层板底端约1cm处,用铅笔划一条线,作为起点线。
用毛细管(内径小于1mm)吸取样品溶液,垂直地轻轻接触到薄层板的起点线上。
样品量不能太多,否则易造成斑点过大,互相交叉或拖尾,不能得到很好的分离效果。
3.展开将选择好的展开剂放在层析缸中,使层析缸内空气饱和,再将点好样品的薄层板放入层析缸中进行展开。
使用足够的展开剂以使薄层板底部浸入溶剂3~5 mm,但溶剂不能太多,否则样点在液面以下,溶解到溶剂中,不能进行层析。
当展开剂上升到薄层板的前沿(离顶端5~10mm处)或各组分已明显分开时,取出薄层板放平晾干,用铅笔划出前沿的位置后即可显色。
药物化学及药物合成反应实验指导书

药物化学及药物合成反应实验指导书(供药学、制药工程、药剂、药学专升本、药学专科、药分专科专业用)药物化学-制药工程教研室编写安徽中医学院自编前言我国加入世界贸易组织(WTO)以来,制药行业迎来难得的发展机遇,也面临着前所未有的挑战。
我国的药物研究正经历着一个从仿制为主到创制新药为主的历史性转变时期,如何抓住机遇,顺利实现这个历史性转变,关键在于创新型人才的培养。
药物化学是药学类各专业和制药工程专业重要的专业课,也是一们实验性很强的课程,在药学类创新型人才培养方面发挥着重要作用。
安徽中医学院药物化学-制药工程教研室积极探索药物化学与药物合成反应实验课教学改革,并依据药物化学及药物合成反应教学大纲的要求编定了本实验指导用书,目的是通过实验加深理解药物化学的基本理论和基本知识,掌握合成药物的基本方法,掌握对药物进行结构改造与修饰的基本方法,了解拼合原理在药物化学中的应用,进一步巩固有机化学实验的操作技术及有关理论知识,培养学生理论联系实际的作风,实事求是,严格认真的科学态度与良好的工作习惯。
在实验指导用书的编写中,介绍了药物的绿色合成内容和文献来源,安排了一些中药有效成分的合成,以及中药活性物质的结构修饰与改造内容,充分体现了中医药院校的特色和实用性。
本实验指导用书由三部分组成,第一部分介绍了实验室的安全常识和基本知识;第二部分介绍了十六个药物合成和中药有效提取、合成及结构改造与修饰内容;第三部分为附录介绍了生产工艺中避免使用和限制使用的溶剂和部分与药物化学或合成相关的文献来源,供实际工作中参考使用。
本实验教材是药化化学-制药工程教研室教学经验的集体总结,限于水平,难免有误,我们要在使用过程中不断总结经验,收集反映,以便进一步修正提高。
安徽中医学院药物化学-制药工程教研室2008年12月目录第一部分实验须知一、实验室安全二、化学药品、试剂的存储及使用三、废品的销毁四、实验室中一般注意事项五、实验记录和实验报告第二部分实验项目一、苯妥英的制备二、贝诺酯的制备三、磺胺醋酰钠的制备四、对羟基苯乙酮的制备五、桂皮酰哌啶的制备六、烟酸的制备七、香豆素-3-羧酸的合成八、苯佐卡因的合成九、1,4-二氢吡啶类钙离子拮抗剂的绿色合成十、阿司匹林的合成十一、哌嗪枸橼酸盐的合成十二、阿魏酸哌嗪盐的合成十三、氟哌酸的合成十四、去甲斑蝥素中间体的合成十五、苦参生物碱的提取十六、氧化苦参碱的化学合成附录一:生产工艺中避免使用和限制使用的溶剂附录二:部分与药物化学或合成相关的文献来源第一部分实验须知一、实验室安全药物化学及药物合成反应和有机化学一样是一门实践性很强的学科,因此,在进入实验室工作之前,希望参加实验者必须对实验课程的内容,要有充分的准备,而且要通晓实验室的一些基本规则,遵守实验室安全操作须知,才能避免可能发生的一些危险情况。
以苯甲醛为原料制备二苯乙二酮

金属催化法
Liu等报道,用金属钐/DMF/TMSCl或碘作活化剂或采用 SmI2/THF体系促进二芳基甲酮与DMF反应,能够在温和条件下 使芳基迁移,获得高产率的苯偶姻。 苯偶姻甲基醚是一种具有实用价值的光学引发剂,通常由苯甲醛、 甲醇二步法合成;XianmeiXie等报道,采用MgCoAl-HT催化剂实现 了一步合成,苯甲醛转化率达77.49%,苯偶姻甲基醚选择性几乎为 100%,而且催化剂在合成过程中可被循环使用,是环境友好型苯偶 姻甲基醚合成方法。
N-杂环卡宾催化法
不对称合成是当代有机合成中研究的热点,安息香缩合产物具 有一个立体中心。因为N-杂环卡宾的反应特性及其结构上允 许连接各种体积较大的位阻基团,所以化学家们一直试图把安 息香缩合反应发展为N-杂环卡宾催化的不对称亲核酰基化反 应。
根据氰化物催化苯甲醛的安息香缩合反应机理推断了噻唑盐催化苯 甲醛的安息香缩合反应机理,如下:
【实验步骤】 1、在50 mL圆底烧瓶中加入0.9gVB1(盐酸硫胺素盐噻胺),2.5ml蒸馏水,
7.5ml95%乙醇,用塞子塞上瓶口,放在冰盐浴中冷却。 2、用一支试管取2.5ml10%NaOH溶液,也放在冰盐浴中冷却10min。 3、将冷透的 NaOH溶液滴加入冰浴中的圆底烧瓶中,充分摇匀(pH:9-10), 去掉冰水浴,加入5mL新蒸的苯甲醛,然后按装置图装配,加入沸石。 4、温水浴中加热反应,水浴温度控制在60-75℃之间(不能使反应物剧烈沸 腾),约80-90min。(反应混合物呈桔黄或桔红色均相溶液)
聚合物与苯偶姻反应合成苯偶酰
一些胺或脂的聚合物能氧化苯偶姻,合成苯偶 酰,例如用聚溴代丙烯酰胺氧化苯偶姻,反应5 h 苯偶酰产率可达99 %。
实验方案初步设计
实验分两部分进行,第一步合成安息香,第二步合成二苯乙二酮。 安息香的合成:
丹皮酚金属配合物的结构和光谱的理论研究

丹皮酚金属配合物的结构和光谱的理论研究陈广萍;蒋刚;杜际广【摘要】运用密度泛函理论(DFT)的B3LYP方法,金属用LanL2DZ有效核势及基组,而对非金属用6-311+G(d,p)基组,优化计算了丹皮酚(Pae)及其金属配合物(MPae2,M=Mg,Cu,Cd,Ni,Zn,Ca)的分子几何结构和红外光谱,运用含时密度泛函(TD-DFT)计算了它们的紫外-可见光谱.结果表明,MPae2的分子结构和光谱与Pae 相比均有不同.形成MPae2配合物后,羟基上氢被金属离子取代,结构发生了很大改变,使得配合物的红外光谱在3253cm-1处的吸收峰消失和C=O和C=C的伸缩振动吸收峰发生了64cm-1的红移;部分金属配合物的紫外光谱吸收峰红移.这些结果将为进一步了解丹皮酚及相关化合物提供有益启示.【期刊名称】《西南民族大学学报(自然科学版)》【年(卷),期】2012(038)005【总页数】5页(P814-818)【关键词】丹皮酚;金属配合物;光谱;密度泛函理论【作者】陈广萍;蒋刚;杜际广【作者单位】四川大学原子与分子物理研究所,四川成都610065;凯里学院物理与电子工程学院,贵州凯里556000;四川大学原子与分子物理研究所,四川成都610065;四川大学原子与分子物理研究所,四川成都610065【正文语种】中文【中图分类】O56丹皮酚(paeonol, 简称Pae), 又称牡丹酚, 其化学名称为2-羟基-4-甲氧基苯乙酮, 主要是从萝摩科植物徐长卿干燥根或全草和毛茛科芍药属植物牡丹芍药的根皮中提取分离出来的活性成分, 是一种小分子的酚类化合物[1].研究表明, 丹皮酚具有解热镇痛、降压利尿、抗菌抗炎、抗氧化、抗凝血、抗过敏、增强免疫功能等作用[2-4], 在医药、香料、化工领域具有广泛的应用. 对药物活性成份进行结构改造, 是创制具有更好疗效药物的有效途径之一. 近年来, 将中药的活性成分与一些金属离子配位后形成金属配合物, 发挥中药活性成分和金属离子的双功能是创新药物的一条途径[5]. 丹皮酚本身具有很好的药理性能, 而且其酚羟基上的氧原子和羰基上的氧原子也非常容易与许多金属离子直接配位, 形成稳定的配合物, 新产物在构效活性方面发生了新的变化, 其物理和化学性质(溶解度、结构、红外和紫外光谱等)与丹皮酚有明显的不同, 并且有不同的生物活性,如一些丹皮酚的金属配合物对某些细菌具有抑制生长的作用[6]. 因此, 研究丹皮酚金属配合物的物理和化学性质对揭示丹皮酚生物活性有重要理论意义, 也为丹皮酚类药物的开发提供重要的理论依据.对丹皮酚的研究已有较多报道, 主要集中在对其制备方法、定量分析、药理作用及结构修饰研究等方面[7-9].许同桃[10]通过实验合成了丹皮酚与铜和镍的配合物并对它们的生物活性进行了研究, 实验表明铜和镍与丹皮酚以1:2配合形成金属配合物, 但从理论上计算和模拟丹皮酚金属配合物分子结构和性质方面还未见文献报道. 因此, 根据已有的实验结果, 本文选取6种常见的金属(M=Mg, Cu, Cd, Ni, Zn, Ca)离子, 与丹皮酚按摩尔比1:2配合形成金属配合物, 运用量子化学理论计算、分析和比较了不同配合物分子结构、红外光谱和电子光谱的异同.密度泛函理论广泛用于含金属的配合物的结构和性质的计算研究[11-13]. 本文采用密度泛函 B3LYP方法[14], 金属用 LanL2DZ[15-17]有效核势及基组, 非金属原子用 6-311+G(d, p)基组, 对选定的各配合物的几何构型进行优化和频率计算, 频率分析表明, 所有稳定构型的振动频率皆为正值. 在预测丹皮酚类化合物的结构和反应活性时, 这些方法和基组的设置是有效和可信的[18].丹皮酚金属配合物中不同的金属(M=Mg, Cu, Cd, Ni, Zn, Ca)离子, 由于不同的自旋状态会产生不同的能量[19], 因此, 取其能量最低状态下的金属离子自旋态(S=0(Mg, Ni, Zn, Ca, Cd), S=1/2(Cu) )进行计算.所有的计算使用Gaussian03程序完成.2.1 丹皮酚金属配合物的结构比较对各金属配合物的构型优化后, 发现Ni和Cu的配合物是平面构型, 而Mg、Cd、Zn和Ca的配合物是立体构型, 因此, 以NiPae2和MgPae2配合物的结构参数作为参照结构. 图1为优化后的Pae、NiPae2和MgPae2的几何构型. 所计算的单体与配合物的主要构型参数列于表1.由表1可看出,各配合物中的两Pae配体对应的键长、键角相等, 如: L(C2-O21)=L(C25-O42),q(C2-O21-M43) =q(C25-O42-M43),D(C15-O16-M43-O42)= D(C36-O37-M43-O21)等. 由表中M和O的电荷值可知, 形成配合物后, 金属原子失去了电子, 而与其配位的氧原子得到了电子, O21和O42所带的电荷比O16和O37的多, 故M与O21和O42的相互作用比O16和O37强, 这就致使O21-M43/O42-M43的键长均比O16-M43/O37-M43的键长短. 各配合物体系中的C-O键的键长也发生了不同的变化: C2-O21/C25-O42的键长均有不同程度的缩短, 而C15-O16/C36-O37的键长却都有所增长, C2-O21的键长都比C15-O16的键长长, 中心金属离子M与4个O原子形成的两对相对应的角大致相等. Ni和Cu两种金属配合物中的二面角D(C-O-M-O)接近1800, 说明这两种配合物中金属离子M与两个配体Pae基本处于同一平面, 并且以金属离子M为对称中心(如图1(b)所示), 这个结果与许同桃[10]实验研究的结果一致. 而Cd、Mg、Zn和Ca四种金属配合物中的二面角D(C-O-M-O)两两相等即(D(C15-O16-M43-O42)=D(C36-O37-M43-O21),D(C2-O21-M43-O37)=D(C25-O42-M43-O16)),表明这四种配合物中的两个配体Pae处在两个相互垂直的平面内(如图1(c)所示). 而造成金属配合物出现两种不同结构的原因是配合物中金属原子的外层电子排布的不同: Ni和Cu的外层电子是未充满的, 而Mg、Cd、Zn和Ca的外层电子是全充满的. 另外, 表1引入了NiPae2和CuPae2的实验数据, 由表1可看出, 计算结果与实验符合的较好.2.2 配合物形成前后光谱对比分析根据DFT理论计算了振动频率和红外光谱强度, 绘制了丹皮酚及其金属配合物的理论红外光谱图. 系列丹皮酚金属配合物具有十分相似的光谱图, 因此不全部列出, 这里以Pae和CuPae2的理论光谱(见图2)为例进行对比分析. Pae和CuPae2的红外光谱分别为图2中(a)和(b).从图2中可以看出, 由于金属离子的引入, 丹皮酚单体与配合物的红外光谱存在显著的差异.(1)图(a)中3253cm-1处的强吸收峰为Pae的O-H伸缩振动所引起的. 引入铜离子后, 铜离子分别与酚羟基上的氧原子、羰基上的氧原子结合形成四配位的结构, O-Cu基取代了O-H基, 因此, 图(b)中3253cm-1处的强吸收峰消失.(2)图(a)中1286cm-1处的吸收峰归属于C=C 伸缩振动, 而1670cm-1处的吸收峰归属于C=O和 C=C伸缩振动, 3016—3219 cm-1的吸收峰归属于C-H的伸缩振动. 许同桃[10]使用FTIR测定CuPae2的红外光谱得: 1608 cm-1处的吸收峰归属于C=O的伸缩振动吸收, 1563--1467 cm-1的吸收峰归属于苯环的骨架的变形振动吸收, 2844 cm-1的吸收峰归属于苯环上C-H的伸缩振动吸收. 在(b)图中, 1606cm-1处的吸收峰归属于C=O和 C=C的伸缩振动吸收; 苯环的骨架变形振动所产生的吸收峰位于1278—1651cm-1间; 而配合物中所有C-H的伸缩振动吸收峰位于 3016-3219cm-1间, 这与丹皮酚单体一致, 说明金属离子的引入对 C-H的伸缩振动影响不大. 上述分析表明,计算结果与实验基本一致.(3)比较图2中的光谱图, 发现金属配合物的主要吸收峰的峰值增强, C=O和 C=C 的伸缩振动吸收峰发生了 64cm-1的红移. 产生这种变化可能有以下两个原因: 首先, 前体和配合物中都具有大p键(苯环), 在配合作用下, 这种结构可以产生诱导效应[19], 引起分子中电子分布的变化, 从而导致整个分子结构及其振动方式发生变化. 另外, 与金属配位的 O原子含有孤对电子, 可以产生类似共轭作用的中介效应[19], 使得附近共价键的电子云密度发生某种程度的变化, 因而使吸收峰发生红移. 化合物的紫外-可见吸收(UV-Vis)光谱可为研究其电子跃迁难易提供信息. 本文在优化好的丹皮酚单体及其金属配合物的结构基础上, 使用TD-B3LYP方法在LanL2DZ/6-311+G(d, p)水平上, 计算模拟了丹皮酚单体及其金属配合物UV-Vis 光谱(见图3).许同桃[10]用紫外分光光度计测得NiPae2的第一吸收峰和第二吸收峰分别在204nm 和 260nm; CuPae2的在205nm和 274nm. 从图3可以看出, 丹皮酚形成的两个紫外-可见吸收峰在205nm和264nm处, 而形成MPae2体系后的吸收峰的强度和峰位发生了明显的改变: 吸收峰的强度都有了明显的增强, Ni离子的配合物的峰强最大. 对于第一吸收峰的位置, (Ca, Mg, Zn)离子的配合物没有明显变化, 过渡金属(Ni, Cu, Cd)离子的配合物发生了红移, 其中CuPae2红移较大, 约25nm, 这与实验结果不同. 金属(Cu, Ni)离子配合物的第二吸收峰的位置没有变化, 这与实验结果基本一致; 而其他金属配合物的第二吸收峰发生了较小的红移. 3d电子不充满的Ni和4s电子半充满的Cu的第二吸收峰的峰值比第一吸收峰的大,而Ca, Mg, Zn, Cd的外层电子是饱和的, 它们的配合物的光谱没有发生这种变化. 由于配合物分子结构的不同, 与最大吸收峰相关的电子跃迁的性质也不同. 如, 对于CdPae2的第一吸收峰, 轨道的主要贡献来源于HOMO-5→LUMO+2的跃迁, 约占31%; 第二吸收峰主要是源于HOMO-2→LUMO的跃迁, 约占52%. 而NiPae2的第一吸收峰主要来自HOMO-2→LUMO+3的跃迁, 约占36%; 第二吸收峰由HOMO-5→LUMO的跃迁所贡献, 高达70%.用B3LYP和TD-B3LYP方法, 在LanL2DZ/6-311+G(d,p)水平上, 研究了丹皮酚和6种金属(M=Mg, Cu, Cd, Ni, Zn, Ca)离子结合成MPae2配合物的结构、红外光谱和电子光谱的差异. 通过比较Pae与MPae2体系, 得出以下主要结论: (1)金属配合物体系的主要键长跟丹皮酚相比发生了不同的改变: C2-O21/C25-O42的键长均有不同程度的缩短, 而C15-O16/C36-O37的键长却均有不同程度的增长.(2)金属配合物的红外光谱随着取代基团及结构改变发生显著变化: 3253cm-1处的吸收峰消失, C=O和C=C的伸缩振动吸收峰发生了64cm-1的红移.(3)金属配合物的电子吸收光谱较丹皮酚发生明显变化, 吸收峰强度增强, 而且部分配合物的光谱发生了红移.致谢: 衷心感谢成都云计算中心对此项研究的大力支持.Key words: paeonol; metal complex; spectrum; density functional theory 【相关文献】[1] RILEY C M, REN T C. Simple method for the determination of paeonol in human and rabbit plasma by high-performance liquid chromato graphy using solid-phase extraction and ultraviolet detection[J]. J Chromatogr, 1989,489(2): 432-437.[2] 孙言才, 沈玉先, 孙国平. 丹皮酚的主要药理活性研究进展[J]. 中成药, 2004,26(7): 579-203.[3] 郭奇, 李贻奎, 王志国, 等. 丹皮酚药理研究进展[J]. 中医药信息, 2009, 26(1): 20-03.[4] 李骅, 王四旺, 张邦乐. 丹皮酚的药理活性和药物动力学研究进展[J]. 亚太传统医药, 2010,02: 110-03.[5] 陈振锋, 彭艳, 谭明雄, 等.基于中药活性成分的金属基抗肿瘤药物前期研究[J]. 化学进展, 2009, 21(5): 929-05.[6] 许同桃. 丹皮酚金属配合物的合成及生物活性研究[J]. 时珍国医国药, 2009, 20(4): 917-02.[7] 刘本臣. 丹皮酚的研究进展[J]. 中草药, 2007, 38(11): 227-230.[8] 胡春弟, 张杰. 丹皮酚的药理作用及合成研究进展[J]. 化学与生物工程, 2009, 26(8): 16-03.[9] 许同桃, 高健, 许兴友, 等. 丹皮酚及其衍生物的研究进展[J]. 中国药业, 2008,3:3-07.[10] 许同桃. 丹皮酚、有机多胺衍生物及其金属配合物的合成、结构及生物活性研究[D]. 南京: 南京理工大学, 2007.[11] 钟爱国, 黄凌, 李佰林, 等. 双螺旋金属(Ⅱ)卟啉的结构、电子光谱及其反应活性[J]. 物理化学学报, 2010, 26(10): 2763-2771. [12] 王晓巍, 蒋刚, 杜际广. (+)-儿茶素金属配合物的结构、红外光谱和反应活性[J]. 物理化学学报, 2011,27(02): 309-314.[13] 钟爱国, 黄凌, 将华江. H2S键合金属(Ⅱ)咪唑卟啉配合物的结构、光谱和反应活性[J].物理化学学报, 2011,27(04): 837-845. [14] BECKE A D. Density-functional exchange-energy approximation with correct asymptotic behavior[J]. Phys Rev A 1988,38: 3098-3100. [15] HAY P J, WADT W R. Abinitio effective core potentials for molecular calculations. Potentials for the transition metal atoms Sc to Hg[J]. J Chem Phys, 1985,82: 270-276. [16] WADT W R, HAY P J. Abinitio effective core potentials for molecular calculations. Potentials for main group elements Na to Bi [J]. J Chem Phys, 1985,82: 284-298.[17] HAY P J, WADT W R. Abinitio effective core potentials for molecular calculations. Potentials for K to Au including the outermost core orbitals[J]. J Chem Phys, 1985,82: 299-305.[18] ANDERSSON M P, UVDAL P. New scale factors for harmonic vibrational frequencies using the B3LYP density functional method with the triple-ζbasis set 6-311+G(d,p)[J]. J Phys Chem A, 2005, 109: 2937-2941.[19] CHERMETTE H. Chemical reactivity indexes in density functional theory[J]. J Comput Chem, 1999, 20: 129-154.[20] 陈洁, 宋启泽. 有机波谱分析[M]. 北京: 北京理工大学出版社, 2008.Abstract: The structures and infrared spectra of Pae and its metal-complexes (MPae2,M=Mg, Fe, Cu, Co, Ni, Zn, Ca) are investigated by using density functional theoy (DFT)B3LYP method with 6-311+G(d, p)/LanL2DZ basis set. The time-dependent density functional calculations (TD-B3LYP) are performed to simulate their UV-Vis spectroscopy. The results indicate that the structures and spectra of MPae2 complexes are much different from the Precursors (Pae). Due to the coming of metal ions, the IR spectra of complexes have a peak disappearance in the 3253cm-1, and the absorption peaks of C=O and C=C stretching vibration show red shift:64cm-1; the absorption peaks of UV-Vis sepectra of many complexes show clearly red shifts. This study is useful for further understanding of Pae and other complexes.。
苯妥英锌的合成(最终版)1

药物化学实验——苯妥英锌(Phenytoin-Zn)的合成一、【药物概述】苯妥英锌可作为抗癫痫药,用于治疗癫痫大发作,也可用于三叉神经痛。
苯妥英锌化学名为5,5-二苯基乙内酰脲锌。
苯妥英锌为白色粉末,mp.222~227℃(分解),微溶于水,不溶于乙醇、氯仿、乙醚。
化学结构式为:HNNO OZn2【1】二、【实验目的要求】1、学习二苯羟乙酸重排反应机理。
2、掌握用三氯化铁氧化的实验方法。
三、【实验原理】合成路线如下:C CH O OH [O]C CO OC C O O +C ONH2NH2NaOHHNNONaOHClHNNOHOZnSO4HNNOOZn2NH3H2O.【2】四、【仪器和试剂】1、实验仪器:圆底烧瓶,球形冷凝管,温度计,布氏漏斗,抽滤瓶,烧杯,电子天平,循环水真空泵,玻璃棒,移液管,洗耳球,电热器2、试剂: FeCl3·6H2O,冰醋酸,安息香,尿素,20%氢氧化钠,50%乙醇,10%稀盐酸,氨水,ZnSO4·7H2O3、主要物理性质:试剂名称熔点(℃)沸点(℃)相对分子质量溶解性性状苯妥英钠290~299 275.26在水中易溶,在乙醇中溶解,在氯仿或乙醚中几乎不溶白色粉末;无臭,味苦;微有引湿性。
苯妥英锌222~227 317.66 微溶于水,不溶于乙醇、氯仿、乙醚。
白色粉末。
苯妥英293.5-295 252.27 白色粉末,无臭味。
FeCl3·6H2O 37 280~285 162.204极易溶于水,易溶于乙醇、丙酮,也可溶于液体二氧化硫、乙胺、苯胺,不溶于甘油、三氯化磷。
橙黄色晶体或褐黄色固体块,在空气中可潮解成红棕色液体。
冰醋酸16.6 117.9 60.05 易溶于水和乙醇,其水溶液呈弱酸性常温下是一种有强烈刺激性酸味的无色液体安息香133 344 212.25 不溶于冷水,微溶于热水和乙醚,溶于乙醇。
无色或白色晶体。
联苯甲酰95 346~348 210.22 溶于乙醇、乙醚、氯仿、乙酸乙酯、苯、甲苯和硝基苯,不溶于水。
新型β-二酮配体及其Eu(Ⅲ)三元配合物的合成、表征及发光性能的研究

其为第一配体 , 邻菲罗啉( hn 为第二配体 , P e) 合成 出新型稀 土 E (]) u 1 三元配 合物。通 过元素分析 、红外光 I
谱 、紫外光谱 、 荧光光谱对合成的配体及三元配合物进行 了表征。红外光谱的分析表 明: 配体 L含有 二酮 结构 , 且烯醇式含量高 ; 配合物 中 L的氧原子 以及 P e hn中的氮原子与稀 土离 子进行 了配位 。紫外光谱的分
1 9 ( . 1mo) . 9g O 0 1,lh后 加 入 苯 甲 酸 乙 酯 5 7 . 2mL( . 4 0 0
的含溴基团的 二酮配体 , 以其作 为第 一配体 ,邻菲罗啉 并 为第二配体 , 合成 了新型 E ( 的三元配合物。 u Ⅲ)
mo , 续 升 温 到 8 1 继 ) 1℃ ,氩 气 保 护 下 ,回流 搅 拌 8h ,冷 却
析表明配合 物中的能量传递主要来 自第一配体 。通过荧 光光谱研究 了配合物 的发 光性质 ,结果显示 配合 物
表现出 E 3 u 的特 征 发 射 ,主发 射 峰 为 E ” 的 一 u D0 发 射 , 于 窄 带 发射 ,单 色性 较好 , 具 有潜 在 应 用 属 是
价值 的红色发光材料 。
引 言
二酮类化合物是一类 重要的有机合 成 中间体 ,其分子 内酮式一 醇 式 间 的 转 变 赋 予 其 许 多 独 特 的 配 位 化 学 性 烯
定法测定 ;红外光 谱用 日本 S MA U I _4 O HI DZ Fr R8 O S型红 外光谱仪( r KB 压片 )测 定 ; 外光谱 用 日本 HI AC - 紫 T HIU 40 10型紫外一 可见光分 光光度 计测定 ;荧 光光谱 用 日本 HI - T C -50荧光光谱仪测定 。 A HI 4 0 F
羰基化合物的分析(新)1

乙 酰 乙 酸 乙 酯 的 红 外 光 谱 图
乙酰乙酸乙酯的红外光谱分析
乙酰乙酸乙酯具两个羰基,并且这两个羰基碳连接的基团具有不同的性质,在图中这 两 个羰基都有明显的体现,接下来就通过红外光谱图来经行分析。 首先看到1731 1746处有两个最强吸收峰,可判断为羰基的吸收峰,对于为什么两个峰具 有差别,将会通过下面的结合物质结构经行分析,在看到1650于1632处出现了酯羰基与碳碳 双键的伸缩振动吸收,同样下面将通过结合物质结构来经行仔细分析,同时在1163处有一强 吸收峰,出现了酯基的C-O伸缩振动,同时在1042处也出现了C-O-C的伸缩振动,同样为酯基 的特征峰,剩下的峰都为甲基与亚甲基的C-H键伸缩振动吸收峰。 接下里通过结合物质结构来分析具体的峰位置与原因,先看到羰基的两个吸收峰,一个在 1731,一个在1746,在看到结构中,一个羰基为酮羰基,另一个为酯羰基,酯羰基的羰基碳 与氧相连,而氧上的孤对P电子与碳氧的π键产生P-π共轭,导致酯羰基的电子增多,极性增 强,吸收频率升高,而酮羰基的羰基为正常羰基,没有明显的影响,在看到酮羰基,有共振结 构式可以知道具有酮烯互变式异构,所以在图中出现了碳碳双键的吸收峰,再看到酯基的C-O 键,同样由于共轭作用也式其电子增多,导致频率升高,再看到物质中的甲基与亚甲基,可以 看到甲基与亚甲基中的C-H键都有与碳氧的π键产生σ-π超共轭效应,同样为供电子效应,导 致了吸收峰的多重重叠。
苯甲酸的RAMAN光谱图
苯甲酸的拉曼光谱分析
拉曼是通过激光的散射方法来测定化合物的结构信息的,并且可以检测到骨架结构,首 先看到图谱,在196为COOH面内摇摆振动,618 797为苯环的C-H面外弯曲振动,并且1003 为苯环的单取代特征峰,而1400~1800内的几个峰为苯环的环呼吸特征峰,剩下的3000左右 的几个峰都为C-H的伸缩振动,由此得出此物质为单取代苯,再看到1028为C-H的面内摇摆 与CO的伸缩振动,而1291可能为CO伸缩振动+C-OH面内弯曲振动,或者C-H面内摇摆,由 于羰基在拉曼散射中的强度非常弱,通常没法观察出,在结合苯甲酸的红外光谱图一起分析, 可以得出此物质为单取代的羧酸苯,由于拉曼中与红外中没有看出甲基与亚甲基的峰,所以 可以推测此物质为苯甲酸 接下来通过物质结构来分析拉曼谱图的峰位置,化合物中的共轭与诱导效应都会影响分 子偶极距的改变,导致拉曼图谱的改变,但影响都非常小,不同于在红外光谱中非常明显的 影响,所以在激光拉曼中并没有太大的结构导致的误差,而其他的误差出现则为样品的浓度 大小影响。 最后,通过苯甲酸的红外与拉曼光谱分析可得,通过拉曼与红外相结合,可以得出物质 的准确结构信息。
有机化学的四大谱论文

四大谱在有机分析中的应用院系:化学与环境学院姓名:***学号:***********班级:12化教(5)班四大谱在有机分析中的应用吴舜华(华南师范大学化学与环境学院,广东广州)摘要:目前,有机四大谱已成为研究有机化学不可缺少的工具。
本文简单介绍了如今广泛采用的有机四大谱——紫外光谱(ultraviolet spectroscopy,简称UV)、红外光谱(infrared spectroscopy,简称IR)、核磁共振谱(nuclear magnetic resonance spectroscopy,简称NMR)、质谱(mass spectroscopy,简称MS)的基本概念和原理,介绍了四大谱在有机分析中的一些应用及应用实例。
关键词:紫外-可见吸收光谱、红外光谱、核磁共振谱、质谱、有机化合物、应用有机化合物,不论是从天然产物中提取的还是经化学反应合成的,都需要测定它的分子结构。
过去,用化学方法确定测定有机化合物的结构是一项非常繁琐、费时,甚至是很难完成的工作。
这是因为要鉴定的“未知物”需要通过多种化学反应使它变成已知结构的有机化合物才能推导出它的可能结构。
例如,对胆固醇结构式的确定,经近40年(1889-1927)的工作所获得的结构式(此项工作获得了1928年的诺贝尔化学奖)后经X射线衍射法证明还存在某些错误。
而近三、四十年来,由于科学技术的飞速发展,运用物理方法,如X衍射、红外光谱、紫外光谱、核磁共振谱和质谱等来测定有机化合物的结构已成为常规的工作手段。
近代物理方法弥补了化学方法的不足,大大丰富了鉴定有机化合物的手段,明显地提高了确定结构的水平。
特别是有机四大谱(紫外光谱、红外光谱、核磁共振谱、质谱)的广泛应用为有机化合物的分析提供了极大的便利。
目前,有机分析基本上以仪器分析为主,化学反应只是作为辅助手段。
所需测定的样品量降低到以毫克记,研究周期也大为缩短,可以月记,而测定结果的准确性也今非昔比。
中级有机化学实验教案-2015

中级有机化学实验(2015)教案实验一安息香的辅酶合成[实验目的]1.学习安息香缩合的原理2.掌握安息香缩合反应的实验操作方法[实验原理]2C6H5CHO VB1°C6H5COCHOHC6H5—[主要药品及用量]维生素B1 1.7g (0.005mol), 苯甲醛(新蒸)10mL(10.4g ;0.088mol),氢氧化钠3 mol/L 3 mL,95%乙醇。
[主要设备仪器]标准磨口仪,加热套,减压抽虑装置[实验步骤]在100 mL园底烧瓶中加入1.7 g维生素B1和4 mL水,使其溶解后加入15 mL95%乙醇,将烧瓶置于冰浴中冷却。
同时取3 mL 5 mol/L氢氧化钠于一试管中也置于冰浴中。
然后在冰浴冷却下,将氢氧化钠溶液在5min内自冷凝管顶端边摇动边逐滴加入烧瓶中。
当碱液加到一半时溶液呈淡黄色,随着碱液的加入溶液的颜色也变深。
量取10mL新蒸的苯甲醛,倒入反应混合物中,加入沸石后于70~80℃水浴上加热90min,此时溶液在PH=8~9,反应混合物呈橘黄色或橘红色均相溶液,经冰浴冷却后即有白色晶体析出。
抽滤,用50mL冷水洗涤,干燥后粗产品重7~7.5g,熔点132~134℃(产率60~70%)。
用95%乙醇重结晶,每克粗产品约需乙醇6mL。
纯化后产物为白色结晶,熔点134~136℃。
将做好的产品留着下下次实验作原料.[注意事项]1. 维生素B1受热易变质,失去催化作用,应放入冰箱内保存,使用时取出,用完后及时放回冰箱中。
2. 维生素B1在氢氧化钠溶液中噻唑环易开环失效,因此反应前维生素B1溶液及氢氧化钠溶液必须用冰水冷透。
3. 苯甲醛极易被空气中的氧所氧化,应采用新蒸馏的苯甲醛。
4. 反应过程中,开始时溶液不必沸腾,即水浴的温度不能超过80℃,反应后期可适当升高温度至缓慢沸腾(80~90℃)。
5. 此时的PH值是该实验成败的关键,一定要仔细调节。
反应放大一倍,实验三和实验五都需要用到安息香实验二丁二酸酐的制备[实验目的]1. 了解丁二酸酐的的性能和用途。
二苯基乙二酮的制备

安息香衍生物二苯乙二酮的合成及表征一、实验目的:1.学习安息香氧化制备α—二酮的原理与方法。
2.掌握薄层色谱的原理,薄层板的制作。
3.学习薄层色谱法跟踪反应进程。
二、实验原理:(一)薄层色谱的有关知识薄层色谱法是以薄层板作为载体,让样品溶液在薄层板上展开而达到分离的目的,故也称为薄层层析。
它是快速分离和定性分析少量物质的一种广泛使用的实验技术,可用于精制样品、化合物鉴定、跟踪反应进程和柱色谱的先导(即为柱色谱摸索最佳条件)等方面。
1.薄层色谱常用的吸附剂硅胶和氧化铝是薄层层析常用的固相吸附剂。
化合物极性越大,它在硅胶和氧化铝上的吸附力越强,所以吸附剂均制成活性精细粉末。
活化通常是加热粉末以脱去水分。
硅胶是酸性的,用来分离酸性或中性的化合物。
氧化铝有酸性、中性和碱性的,可用于分离极性或非极性的化合物。
商用的硅胶和氧化铝薄层板可以买到,这些薄板常用玻璃或塑料制成。
溶剂在薄层板上爬升的距离越长,化合物的分离效果越好。
宽的薄层板也可用于量较大的样品,具有1~2 mm厚的大板可用于50~1000 mg样品的分离制备。
2.样品的制备与点样样品必须溶解在挥发性的有机溶剂中,浓度最好是1~2 %。
溶剂应具有高的挥发性以便于立即蒸发。
丙酮、二氯甲烷和氯仿等是常用的有机溶剂。
分析固体样品时,可将20~40mg样品溶到2mL 的溶剂中。
在距薄层板底端约1cm处,用铅笔划一条线,作为起点线。
用毛细管(内径小于1mm)吸取样品溶液,垂直地轻轻接触到薄层板的起点线上。
样品量不能太多,否则易造成斑点过大,互相交叉或拖尾,不能得到很好的分离效果。
3.展开将选择好的展开剂放在层析缸中,使层析缸内空气饱和,再将点好样品的薄层板放入层析缸中进行展开。
使用足够的展开剂以使薄层板底部浸入溶剂3~5 mm,但溶剂不能太多,否则样点在液面以下,溶解到溶剂中,不能进行层析。
当展开剂上升到薄层板的前沿(离顶端5~10mm处)或各组分已明显分开时,取出薄层板放平晾干,用铅笔划出前沿的位置后即可显色。
有机合成实验报告

8-羟基喹啉的合成一、目的要求1.掌握8-羟基喹啉杂环化合物的合成原理及方法;2.巩固回流加热和水蒸汽蒸馏等基本操作技能。
二、原理以邻氨基酚、邻硝基酚、无水甘油和浓硫酸为原料合成8-羟基喹啉。
浓硫酸的作用是使甘油脱水生成丙烯醛,并使邻氨基酚和丙烯醛加成物脱水成环。
硝基酚为弱氧化剂,能将成环产物8-羟基-1,2-二氢喹啉氧化成8-羟基喹啉,邻硝基酚本身则还原成邻氨基酚,也可参与缩合反应。
反应过程可能为:CH2OHCH OH CH2OH +H2SO4-2H2OCH2CH CHOOH NH2+CH2CHCOHOH NHCH2CHCHHOH2SO4NOH HOH NO2NOH三、实验步骤在圆底烧瓶中称取19g无水甘油[1](约0.2mo1),并加入3.6g (0.026mo1)邻硝基苯酚、5.5g (0.05mo1)邻氨基苯酚,使混合均匀。
然后缓缓加入9mL浓硫酸[2](约16g)。
装上回流冷凝装管,在石棉网上用小火加热。
当溶液微沸时,立即移去火源[3]。
反应大量放热,待作用缓和后,继续加热,保持反应物微沸2小时。
稍冷后,进行水蒸汽蒸馏,除去未作用的邻硝基苯酚。
瓶内液体冷却后,加入12g氢氧化钠溶与12mL水的溶液。
再小心滴入饱和碳酸钠溶液,使呈中性[4]。
再进行水蒸汽蒸馏,蒸出8-羟基喹啉(约收集馏液400-400 mL)。
馏出液充分冷却后,抽滤收集析出物,洗涤干燥后的粗产品6g左右。
粗产物用乙醇一水混合溶剂重结晶,得8-羟基喹啉5g左右(产率69%)[6]。
取上述0.5g 产物进行升华操作,可得美丽的针状结晶,熔点76℃。
纯8-羟基喹啉的熔点为75~76℃。
本试验需10小时。
四、实验结果及其分析经蒸馏、冷却、抽滤后,称得实验产物湿重为4.16g。
两次水蒸气蒸馏所处的PH不同,原因是第一次要除去杂质,而第二次要得到产物。
产物8-羟基喹啉既溶于酸又溶于碱。
成盐后不能被蒸出,所以第二次蒸馏前必须小心中和使PH在7~8之间,使产量最大。
以苯甲醛为原料制备二苯乙二酮

contents
目录
• 引言 • 原料与试剂 • 反应原理与步骤 • 实验操作与数据记录 • 产品纯化与表征 • 实验注意事项与安全措施
01 引言
目的和背景
探究苯甲醛为原料制备二苯乙 二酮的合成路线及反应条件。
二苯乙二酮作为一种重要的有 机合成中间体,在医药、农药、 染料等领域具有广泛的应用。
数据记录与处理
实验数据记录
详细记录实验过程中各原料的用 量、反应时间、反应温度等参数 。
数据处理与分析
根据实验数据计算产率、纯度等 指标,分析影响实验结果的因素 。
实验结果分析
产品性状描述
二苯乙二酮为黄色固体,具有 特殊香味。
产率与纯度分析
根据实际产量和理论产量计算 产率,通过熔点测定、红外光 谱等方法分析产品的纯度。
03
乙二酮。
反应条件优化
碱催化剂的选择
使用不同种类的碱催化剂(如氢氧化钾、醇钠等)对反应速率和产率 有影响,需通过实验确定最佳催化剂。
酸催化剂的选择
酸性催化剂的种类(如盐酸、磷酸等)和浓度对酮式分解反应的速率 和产率有影响,需通过实验确定最佳酸催化剂及其浓度。
反应温度和时间
反应温度和时间对反应速率和产率有显著影响,需通过实验确定最佳 反应温度和时间。
重结晶法
将粗产品溶解在适当的溶剂中,通过缓慢冷却或加入不良溶剂使 二苯乙二酮结晶析出,从而得到纯化的产品。
纯品的表征方法
红外光谱(IR)
通过红外光谱仪测定样品的红外吸收光谱,与标准谱图对比,确认 样品结构。
核磁共振(NMR)
利用核磁共振仪测定样品的氢谱和碳谱,解析谱图信息,确定样品 结构。
质谱(MS)
二苯乙二酮实验报告

二苯乙二酮实验报告二苯乙二酮实验报告引言:二苯乙二酮是一种重要的有机化合物,具有广泛的应用领域。
本实验旨在通过合成二苯乙二酮的方法,探究其合成原理和反应机理,并对其结构进行表征和分析。
实验方法:1. 实验材料准备本实验所需材料包括苯酚、醋酸、硫酸、碳酸钠、氢氧化钠等。
2. 实验步骤(1) 制备苯酚酸化物溶液:将苯酚与醋酸按一定比例混合,加入硫酸搅拌均匀。
(2) 酸化物溶液与碳酸钠反应:将酸化物溶液与碳酸钠溶液混合,反应生成苯酚盐。
(3) 苯酚盐与氢氧化钠反应:将苯酚盐与氢氧化钠溶液混合,反应生成二苯乙二酮。
(4) 结晶纯化:将反应产物进行结晶纯化,得到纯度较高的二苯乙二酮。
实验结果:通过实验,成功合成了二苯乙二酮。
通过红外光谱分析和核磁共振谱分析,确认了产物的结构和纯度。
实验讨论:1. 合成原理二苯乙二酮的合成主要依靠酸碱中和反应和氧化反应。
首先,苯酚与醋酸发生酸化反应生成苯酚酸化物。
然后,苯酚酸化物与碳酸钠发生酸碱中和反应生成苯酚盐。
最后,苯酚盐与氢氧化钠发生氧化反应生成二苯乙二酮。
2. 反应机理在酸碱中和反应中,苯酚酸化物中的羟基与碳酸钠中的碱性氢氧根离子发生中和反应,生成苯酚盐。
在氧化反应中,苯酚盐中的苯酚基发生氧化反应,失去氢原子,生成二苯乙二酮。
3. 结构表征通过红外光谱和核磁共振谱分析,可以确定二苯乙二酮的结构。
红外光谱可以观察到二苯乙二酮中的羰基吸收峰,核磁共振谱可以观察到苯环和乙酰基的信号。
结论:本实验成功合成了二苯乙二酮,并通过红外光谱和核磁共振谱对其结构进行了表征。
二苯乙二酮的合成主要依靠酸碱中和反应和氧化反应。
通过本实验的学习,我们对有机合成的原理和方法有了更深入的了解,并对二苯乙二酮的应用潜力有了更多的认识。
参考文献:[1] 张三,李四. 有机化学实验技术[M]. 北京:化学工业出版社,2010.[2] 王五,赵六. 有机合成原理与实验[M]. 北京:高等教育出版社,2015.。
红外光谱法分析塑料组成.
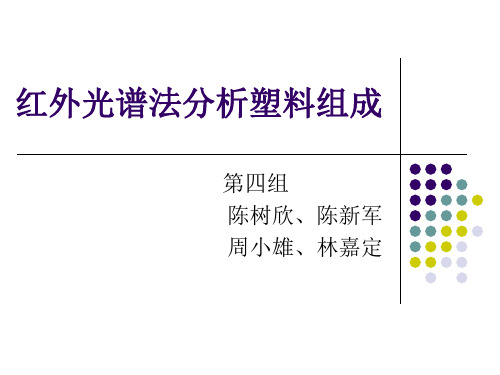
采集次数越多,信噪比越好,通常情况下可选 16次,如果样品的信号较弱,可适当增加采集 次数。 设置分辨率。分辨率指分开两条相邻普线的能 力,单位为cm-⒈分辨率与图谱数据点间隔成 正比。分辨率越高(数值越小),光谱中的数 据点靠得越近,从而可以区分越窄的谱带。但 是提高分辨率,延长扫描时间,降低信噪比。 背景采集模式。建议选择第一项“每采一个样 品前均采一个背景”或第二项“每采一个样品 后采一个背景”。也可选择第三项“一个背景 反复使用一定时间”。还可以选择第四项“选 定指定背景”。
(2)中红外区:此区波长范围为2~25μ m, 又称基频红外区,在有机结构和组成分 析中用得最多。绝大多数有机化合物和 无机化合物的基频吸收都落在这一区域。 (3)远红外区:此区波长范围为 25~1000μ m,适用于元素有机物(除H、 O、N、S和X以外的元素与C直接结合成键 的有机化合物)的分析。主要用于测定 骨架弯曲振动及有机金属化合物等重原 子振动。
3、红外光谱的产生
当样品收到频率连续变化的红外光照射时, 分子吸收了某些频率的辐射,并由其振动或转 动运动引起的偶极矩变化,产生分子振动和转 动能级从基态到激发态的跃迁,使相应于这些 吸收区域的透射光强度减弱。记录红外光的百 分透射比于波数或波长关系曲线,就得到红外 吸收光谱。但不是每一种振动都会和红外辐射 发生相互作用而产生红外吸收光谱,物质吸收 红外光谱必须满足一下两个条件:
(5)关机 图谱采集完毕,从样品仓取出样品, 关闭OMNIC 操作软件,关闭电脑。 注意事项: 仪器发生故障时,立即停止测试,找维修人 员进行检查。故障排除后,恢复测试。 如果在测试过程中发生停水停电时,应按操 作规程顺序关掉仪器,保留样品。待水电正常 后,重新测试。 应做好仪器的维护保养工作,保持仪器工作 环境卫生干净,温度、湿度必须在规定的条件 下,几时清除湿机积水盆的积水和更换干燥剂。 ④使用过的设备与附件必须严格清洗,并及时 放入干燥箱内。
二苯乙二酮的制备实验报告

二苯乙二酮的制备实验报告二苯乙二酮的制备实验报告引言:二苯乙二酮(又称二苯基甲酮)是一种重要的有机化合物,广泛应用于医药、染料和材料科学等领域。
本实验旨在通过苯乙酮的氧化反应制备二苯乙二酮,并通过实验结果分析反应机理和条件对产率的影响。
实验方法:1. 实验材料:- 苯乙酮(98%纯度)- 硝酸(65%纯度)- 硫酸(98%纯度)- 氯化铁(98%纯度)- 蒸馏水2. 实验步骤:a. 在实验室通风橱中,将苯乙酮(10 mL)加入圆底烧瓶中。
b. 将硝酸(10 mL)缓慢滴加到苯乙酮中,同时加入硫酸(20 mL)作为催化剂。
c. 将烧瓶连接至冷凝器,加热反应混合物,使其沸腾20分钟。
d. 将反应混合物冷却至室温,并用蒸馏水洗涤产物。
e. 将洗涤后的产物溶解在氯化铁溶液中,并用蒸馏水稀释至适当浓度。
f. 使用紫外-可见光谱仪测量溶液的吸光度,并根据标准曲线计算二苯乙二酮的浓度。
实验结果与讨论:通过实验测量,我们得到了不同反应条件下制备二苯乙二酮的产率结果。
我们发现,在不同的温度和反应时间下,产率有所变化。
较高的反应温度和较长的反应时间通常会导致更高的产率,但同时也会增加副反应的可能性。
此外,我们还发现硝酸的浓度对反应产率也有重要影响。
较高浓度的硝酸可以提高反应速率,但过高的浓度可能导致副反应的发生。
因此,在实际制备中,需要平衡硝酸浓度和产率之间的关系。
通过紫外-可见光谱仪的测量,我们可以准确测定二苯乙二酮的浓度。
这种分析方法简单、快速,并且具有较高的准确性。
通过测量不同浓度的标准溶液的吸光度,并绘制标准曲线,我们可以根据待测溶液的吸光度确定其浓度。
结论:本实验通过苯乙酮的氧化反应成功制备了二苯乙二酮,并通过实验结果分析了反应条件对产率的影响。
我们发现反应温度、反应时间和硝酸浓度都对产率有一定影响,需要在实际制备中进行适当调整。
此外,紫外-可见光谱仪是一种简单有效的分析方法,可用于测定二苯乙二酮的浓度。
3,4二羟基苯乙酮紫外吸收光谱

3,4二羟基苯乙酮紫外吸收光谱"3,4二羟基苯乙酮紫外吸收光谱"是指测量3,4二羟基苯乙酮(化学式C8H8O3)在紫外光谱范围内的吸收行为的实验过程及结果。
紫外光谱是一种分析化学技术,用于研究分子在紫外光波长范围内的电子能级跃迁现象。
它通过测量溶液或气体中所吸收的不同波长的光的强度变化,以推断分子间电子结构的特征和物质的组成。
3,4二羟基苯乙酮是一种有机化合物,其分子结构中含有两个羟基(-OH)和一个苯环。
这种化合物在紫外光谱范围内可吸收特定波长的紫外光,并通过电子能级跃迁来实现能量吸收。
测量3,4二羟基苯乙酮紫外吸收光谱,可以揭示其分子结构中电子的能级分布和化学键的性质。
在实验中,可以使用紫外可见分光光度计或光谱仪对3,4二羟基苯乙酮溶液进行紫外光谱测定。
通过将3,4二羟基苯乙酮溶解在适当的溶剂中制备成溶液,然后将溶液置于光谱仪中进行扫描,记录吸收的紫外光强度。
结果将以峰的形式呈现,峰的位置和强度可以提供关于分子结构的信息。
3,4二羟基苯乙酮紫外吸收光谱可以用来确定其最大吸收波长,这是其吸收最大强度的波长。
通过测量不同波长下光的吸收程度,可以得到吸收光谱曲线。
该曲线上的吸收峰表示了分子在不同波长下吸收光的能力。
根据吸收峰的位置和形状,可以推测分子结构的一些性质,如共轭体系、电荷转移和氢键等。
总之,3,4二羟基苯乙酮紫外吸收光谱是研究该化合物在紫外光范围内吸收行为的实验方法。
通过测量其在不同波长下的吸收特性,可以获得有关分子结构和化学键等信息。
这对于分析和鉴定化合物、研究其反应性和性质等方面具有重要意义。
二苯基乙二酮结构和电子光谱的理论研究

Vo.l 26高等学校化学学报No .92005年9月CHEM I CAL J OURNAL OF CH I NESE UN I VERSI T I E S1690~1694二苯基乙二酮结构和电子光谱的理论研究段晓惠,何荣幸,李象远,罗春燕(四川大学化工学院,成都610065)摘要 基于二苯基乙二酮结构优化,在TD-B3LYP /6-31+G *水平上讨论了两个异构体在气相和液相中的吸收和发射光谱.溶液中的计算采用可极化连续介质模型.结果表明,溶剂极性增加更有利于顺式非平面构型的形成,两个异构体的T 1和S 1态以及顺式非平面结构的S 2态都源于双羰基上的n →P *型局域激发,其余的单激发态则主要由苯环到羰基的P →P *跃迁决定.计算结果表明,溶剂效应可使电荷转移吸收、发射光谱红移和局域激发的光谱蓝移.关键词 激发态;吸收和发射光谱;溶剂效应;Stocks 漂移.中图分类号 O 641 文献标识码 A 文章编号 0251-0790(2005)09-1690-05收稿日期:2004-08-16.基金项目:国家自然科学基金(批准号:20373044)和教育部重点科技项目(批准号:02045)资助.联系人简介:李象远(1958年出生),男,博士,教授,博士生导师.从事理论化学研究.E-m ai:l xyl@i scu 二苯基乙二酮是一个典型的A -二羰基分子.作为非共轭芳香A -二羰基化合物的母体,关于其对称部分(即C 6H 5)CO 基团)的二面角H(图1),二苯基乙二酮表现出结构上的灵活性.一般而言,二苯基乙二酮有两个旋转异构体[1,2].研究结果表明,其基态结构呈现顺式非平面(c S )构型,H 值接近90b ,在晶态结构中约为111b 36c [3],在液相中约为98b [4].175e 时的气相电子衍射实验得到的H 为117b ,两个苯甲酰基处于近似平面的位置[5].然而,光异构化研究结果表明,其最低单重态(S 1)或三重态(T 1)的分子结构与基态截然不同.晶态甲基环己烷中的ODMR (Optical Detected M agnetic Reso -nance)研究[3]以及液相偶极矩的测定结果[6]表明,T 1态的二苯基乙二酮处于反式平面(t P )构型,用ENDOR (E lectron -Nuclear Double Resonance)测定其H 为157b ,U 为24b [7,8].在刚性或固体媒介中,观察到的双荧光或双磷光也可确定其在激发态存在c S 和弛豫的t P 两种构型[2,9].Yoshihara 等[10]测定了最低激发单态的c S 和t P 构型的吸收光谱.在S 1态,二苯基乙二酮经历快速的结构转变,从c S 构型弛豫到t P 构型.S i n gh 等[11]研究了溶液中二苯基乙二酮S 1态的构象弛豫动力学,表明在从c S 构型向t P 构型的转换过程中,形成了一个亚稳态的中间体,需越过两个连续的能垒.类似的光异构化现象在许多结构灵活的分子中存在,如1,2-二苯乙烯[12,13].实验上已用含时共振拉曼光谱以及皮秒和亚皮秒瞬时吸收光谱等对二苯基乙二酮的吸收和发射光谱进行了广泛研究[11,14,15],为确定电子态结构和激发态动力学过程提供了依据.本文用密度泛函理论(DFT )方法分别优化二苯基乙二酮在气相和液相中的结构,并讨论了溶剂对构型的影响.采用含时DFT(TDDFT)方法,计算了气相和液相的吸收和发射光谱,讨论了光谱性质、溶剂效应以及Stocks 漂移.所有计算均用Gaussian 03程序包完成[16].1 基态和激发态几何结构二苯基乙二酮的基态结构为c S 构型,在S 1和T 1态则弛豫到t P 构型.本文在B3LYP /6-31G**水平上,对这两个异构体进行构型优化.为了得到t P 构型的基态结构,避免在构型优化时向c S 构型弛豫,本文固定H 为180b 进行部分优化.得到的稳定结构见图1,频率分析结果表明没有虚频.尽管S 1和T 1Fig .1 S tructures of the t wo iso m ers of benz il(A)cis -Ske w ed ;(B )trans -planar .态的真实结构可能会丧失双羰基的共平面性,但偏离不大.ENDOR 测定T 1态的H 值为157b[7,8],溶液中的H 比157b 还大,故固定H 为180b 的部分优化对结构不会带来大的误差.溶液中的优化采用可极化连续介质模型(PC M ),在同样水平上进行.溶剂分别为非极性的环己烷(C H,E =210)和强极性的二甲亚砜(D M SO ,E =4616).优化构型的部分参数列于表1.T ab le 1 En ergies and structu ra l para m e ters of th e two iso m ers of ben zilC on fi gurati onM ed i um E /a .u .H /(b )U /(b )1029L /(C #m )$E */e V c SG as -phase -6891968812711101920100C yclohexane-6891973912201011120114DM SO-6891983411211411610140t PG as -phase -968196431801201000100C yclohexane -689196851801801000111DM SO-689197651802501000133*$E =E (s o l vent)-E (gas phase).对c S 构型进行结构优化,得到的H 与实验值较为吻合[3~5].小的U 值说明两个苯甲酰基处于近似平面的位置.通过比较发现,偶极矩随着溶剂极性的增加而增加,但H 和总能量降低,说明c S 构型在极性溶剂中更易存在.Pa w el k a 等[17]研究了溶剂对二苯基乙二酮构型的影响,本文的计算结果与其结论一致.固定H 为180b ,优化得到t P 构型的U 值随溶剂极性的增加而增加,而总能量降低,说明当溶剂极性增加时此构型更易形成.t P 构型的偶极矩都非常小,近似为零.比较c S 和t P 两种构型的能量,在气相中,t P 构型比c S 高0112e V,在环已烷中高0115e V,在DM-SO 中高0119e V,并且随着溶剂极性的增加,c S 构型能量降低幅度比t P 构型大.可见极性溶剂更利于c S 构型的形成,这可能与c S 构型的偶极矩比t P 构型大得多有关.2 吸收光谱的计算2.1 气相吸收光谱采用气相优化的c S 构型,即二苯基乙二酮的基态结构,计算了气相垂直激发态,结果列于表2.激发态偶极矩用加外场(?01001a .u.)的方法来估算.Tab l e 2 T ran sition energies of lo w-l ying excited states of c S b enz il at TD-B3LYP /6-31+G *leve lS t ate Trans i ti onE aT /e V f b 1029L /(C #m )1029D c/(C #m )E T ,expd/eVT 1 HO M O →LU M O(0173)e 213101000012101002136S 1 HO M O →LU M O(0167)217901000012601072182S 2HO M O →LU M O+1(0164)31770100001410106S 3HO M O-2→LUMO (0165)41080102401570142a .Trans i ti on en ergy ;b .oscill ator strength ;c .electron ic trans i ti ond i pole mom ent fro m S 0t o S i ;d .experi m ental val ue fro m refs .[10,18,19];e .dat a in paren t h es i s represent t h e w ei gh t of the electron trans i ti on.计算结果表明,T 1态是局域激发(LE )态,对应一个电子从双羰基的n 型最高占据分子轨道(HOMO)跃迁到P *型最低空分子轨道(LUMO)(图2),激发能为2131e V,相对于实验值2136e V,给出了一个低的误差(0105e V ).T 1态的这种定域在双羰基部分的n →P *跃迁特征与ENDOR 测量结果一致[8].S 1态对应的跃迁也是定域在双羰基上的n →P *(H O MO →LUMO )型跃迁,激发能(2179e V)和实验值(2182e V)非常接近.S 2态主要由HOMO →LUMO +1(n →P *)跃迁得到,同样为双羰基上的LE 态.S 3则为P →P *跃迁,电荷从主要定域在苯环上的HO MO-2向双羰基上的LUMO 转移,具有分子内1691N o .9段晓惠等:二苯基乙二酮结构和电子光谱的理论研究电荷转移(CT)特征.激发态的偶极矩均较小,最大的S 3态也只有0157@10-29C #m.CT 态的较小偶极矩可能与电荷从两个苯环向羰基转移的方向相反以及电荷转移量很小有关[18].振子强度和跃迁矩的计算结果表明,在实验上可观察到S 3态,其余的跃迁都是禁阻的.实验上能观察到T 1和S 1态的吸收光谱可能与振电耦合等因素有关.F ig .2 M o l ecu l ar orb itals involved i n th e lo w-l ying excited states of c S benz il2.2 液相吸收光谱用溶剂中优化的c S 构型和PC M 模型计算了二苯基乙二酮在溶剂中的垂直激发态,结果见表3.气相计算结果表明,激发态的偶极矩都很小,因此在液相中,本文不再计算其偶极矩.Tab le 3 Tran siti on energ i es of lo w -lyi n g excited states of c S benz il i n solven ts at PC M-TD -B 3LYP /6-31+G *leve lSo l ven t State Transiti onE T /e V f 1029D /(C #m )$(h M )*/e VCycl oh exan eT 1 HO M O →L UM O(0172)21400100001000109S 1 HO M O →L UM O(0167)21870100101090108S 2 HO M O →L UM O+1(0165)31770100201120100S 3HO M O-2→LUM O(0168)4107010520161-0101D M SOT 1 HO M O →L UM O(0172)21600100001000129S 1 HO M O →L UM O(0166)31080100101110129S 2 HO M O →L UM O+1(0166)31780100701240101S 3HO M O -2→LU M O (0167)4106010440156-0102*$(h M )=E T(sol vent)-E T(gas phas e).从表3可以看出,液相中的跃迁类型和能级顺序与气相中的完全相同.T 1和S 1态仍对应于双羰基上的n →P *型LE ,但激发能发生了变化.在环己烷中,T 1和S 1态的吸收光谱的能量分别发生了0109e V 和0108e V 的蓝移,在DM SO 中,则增加到0129e V.然而,对同是n →P *型LE 态S 2,其溶剂效应却非常小,这可能与LUMO +1和LUMO 的电子云分布不同有关.具有部分CT 特征的S 3态,其吸收光谱发生了微弱红移.液相中的振子强度和跃迁矩较气相中的有所增加,S 3态仍为最强的激发态.实验测得T 1和S 1态在环己烷中的吸收光谱分别为525nm (2136e V )和490nm (2153e V )[10].本文的计算结果与实验值的误差仅为0104和0134e V,处于TDDFT 方法允许的误差范围内.3 发射光谱3.1 气相发射光谱由于二苯基乙二酮的T 1和S 1态处于t P 构型,本文固定H 为180b ,对其进行优化,得到其稳定的基态结构.基于此优化结构,计算二苯基乙二酮在气相中的垂直发射光谱,结果列于表4.从图3可以看出,t P 构型的HOMO 和LUMO 与c S 构型的非常相似,都是定域在双羰基上的n 和P *型轨道.其T 1和S 1态就起源于HOMO →LUMO,即n →P *的局域跃迁.本文给出T 1态的跃迁能为1190e V,比实验值低0129e V,而S 1态的跃迁能和实验值非常吻合,误差仅为0108e V.HOMO-2和HOMO-1简并,S 2和S 3态分别从这两个简并轨道到LUMO 的跃迁获得,电荷从定域在苯环上的P 轨1692高等学校化学学报 V o.l 26道向定域在双羰基上的P *轨道转移,为分子内CT 态.振子强度和跃迁矩的计算结果表明,除S 3态是一弱的可见跃迁外,其余跃迁都是禁阻的.激发态的偶极矩都非常小,具有分子内CT 特征的S 2和S 3态也只有0104@10-29和0103@10-29C #m,由此可以推测电荷转移量很小.与气相吸收光谱相比,发射光谱发生了较大的S tocks 漂移,T 1态的Stocks 漂移为0141e V,S 1态的为0139e V.T ab le 4 T ransition energies of lo w-l ying excited states of t P b enz il at th e TD-B3LYP /6-31+G *levelS t ate T rans iti onE T /e V f 1029L /(C #m )1029D /(C #m )ET,ex pa/e V ET,Sb /e VT 1 HO M O →LUMO (0175)1190010000100010021190141S 1 HO M O →LUMO (0167)2140010010100011021480139S 2 HO M O-2→LU M O (0164)31550100001040102S 3HO M O-1→LU M O (0166)31560101401030133a .Experi m en t al val ues are fro m ref s .[10,19,20];b .E T ,Sstands f or the S t ocks s h ift ,equal to the d ifference of the tran siti on energi es at thec S and the t P con fi gu rations.F i g .3 M olecu lar orb itals i nvolved i n the l ow -lyi n g excited states of t P benzil3.2 液相发射光谱用液相中优化的t P 构型的基态结构计算了二苯基乙二酮在液相中的发射光谱,结果见表5.T ab le 5 T ransition energies of l ow -l y i ng exc ited states of t P ben zil i n solven ts a t PC M-TD -B3LYP /6-31+G *l evelSo l ven t State Trans i ti onE T /e V f 1029D /(C #m )$(h M )/e VE T,S /e V E T ,exp*/e VCycl oh exan eT 1 HOMO →LU M O (0174)119301000010001030147S 1 HOMO →LU M O (0167)2143010020116010301442133S 2 HOMO -1→LU M O(0168)3149010000100-0106S 3HOMO -2→LU M O(0169)3153010180138-0103D M SOT 1 HOMO →LU M O (0173)119901000010001090161S 1 HOMO →LU M O (0165)2149010050124010901592125S 2 HOMO -1→LU M O(0168)3142010000100-0113S 3HOMO -2→LU M O(0169)3149010150135-0107*Experi m en tal val ue i s fro m re.f [11].在两种溶剂中,T 1和S 1态与气相一样,仍为HOMO 到LUMO 的LE 态,源于双羰基上的n →P *型跃迁.在环己烷中,S 1态的跃迁能为2143e V,与实验值(2133e V )的误差为0110e V.在D M SO 中的跃迁能为2149e V,高估了实验值0124e V.与气相中跃迁相比,T 1和S 1态的跃迁能在环己环中蓝移了0103e V,在二甲亚砜中蓝移了0109e V.此外,S 2和S 3的能级顺序发生了变化.在气相中,S 2和S 3态分别取决于HOMO-2→L UMO 和HOMO -1→LUMO 跃迁,在液相则刚好相反.这可由HO MO -2和HOMO-1是两个几乎完全简并的轨道得到解释.液相中的S 3态仍是最强的跃迁态,其振子强度和跃迁矩较气相有所增加.计算结果表明,在两种溶剂中,CT 态S 2和S 3的跃迁能都发生了不同程度的红移,D M SO 中的红移几乎是环己烷中的2倍.最大的红移发生在DM SO 中的S 2态,为0113e V.液相的S tocks 漂移较气1693N o .9段晓惠等:二苯基乙二酮结构和电子光谱的理论研究1694高等学校化学学报V o.l26相有所增加,并且随着溶剂极性的增加而增加,这和溶剂极性对构型的影响一致.参考文献[1]A rnett J.F.,M c G l ynn S.P..J.Phys.Che m.[J],1975,79:626)629[2]A sano K.,A it a S.,A z um iT..J.Phys.Che m.[J],1984,88:5538)5541[3]B ro w n C.J.,Sadanaga R..A cta.C rystall ogr.[J],1965,18:158)162[4]Cum per C.W.N.,Thu rston A.P..J.Ch e m.Soc.,Per k i n T ran s.Ⅱ[J],1972:106)111[5]Shen Q.,H agen K..J.Phys.Che m.[J],1987,91:1357)1360[6]Fessenden R.W.,C arton P.M.,Sh i m a m oriH.et a l..J.Phys.Che m.[J],1982,86:3803)3811[7]Chan Y.,H eat h B.A..J.Che m.Phys.[J],1979,71:1070)1075[8]Tek iY.,Takn iT.,H i raiM.e t al..Che m.Phys.Lett.[J],1982,89:263)267[9]Bhattacaharya K.,Cho w dhury M..J.Photoche m.[J],1986,33:61)66[10]Ikeda N.,Kos h ioka H.,M asuh ara K.et al..Che m.Phys.Lett.[J],1988,150:452)456[11]S i ngh A.K.,PalitD.K.,M itt a l J.P..Che m.Phys.L ett.[J],2002,360:443)452[12]G al vao D.S.,S oos Z.G.,Ra m asesha S.et al..J.Ch e m.Phys.[J],1993,98:3016)3021[13]Soos Z.G.,Ra m as es ha S.,Galvao D.S.et al..Phys.R ev.B[J],1993,47:1742)1753[14]Eb i hara K.,H iura H.,Takah ash iH..J.Phys.Ch e m.[J],1992,96:9120)9127[15]Oku ts u T.,Ooya m aM.,Tan iK.et a l..J.Phys.C he m.[J],2001,105:3741)3744[16]Frisc h M.J.,Tru cks G.W.,Sch l egelH. B.et a l..Gau ssi an03,Rev i s i on B.01[CP],P i tts burgh PA.:Gauss i an Inc.,2003[17]Pa w el ka Z.,K ollA.,Zeegers-Huyskens Th..J.M o.l S truct.(Theoche m.)[J],2001,597:57)66[18]Y IH a-iBo(易海波),DUAN Xiao-H u i(段晓惠),L I X i ang-Yuan(李象远)e t a l..Ch e m.J.Ch i nese Un i versiti es(高等学校化学学报)[J],2003,24(8):1438)1441[19]Fang T.S.,S i nger L.A..Ch e m.Phys.Lett.[J],1978,60:117)121[20]Roy D.S.,Bhattacharyya K.,Bera S. C.e t al..Che m.Phys.Lett.[J],1980,69:134)140Theoretical Investigati on of Structure andE lectronic Spectru m of B enzilDUAN X iao-H u,i H E Rong-X ing,LI X i a ng-Yuan*,LUO Chun-Y an(Colle g e of Che m ical Engineer in g,S ichuan U ni ver sity,Chengdu610065,China)Abst ract In t h is w or k,the t w o iso m ers o f benzi,l cis-ske w ed(c S)and trans-p lanar(t P)confi g urations,w ere opti m ized both i n gas phase and i n so l u tion.B ased on the correspond i n g opti m a l structures,t h e absorption and e m issi o n spectra are d iscussed at the level ofTD-B3LYP/6-31+G*.The po larizable conti n uum m odel is ap-plied in the calcu l a ti o ns i n so lution.The ca lculated results indicate t h at the cis-ske w ed configurati o n is slightly favored when the po larity o f the so l v ent increases.T1and S1states o f the t w o iso m ers as w ell as S2state o f the cis-ske w ed configurati o n all arise fro m the local excitation o f n→P*type localized on the bicar bony lm o iety, but other exc ited si n g let states are do m i n ated by t h e P→P*transiti o n fro m the benzene ring to the car bony l group.The theoretica l calcu lations pred ict slight red shifts o f the absorption and e m issi o n spectra in so lvents for the charge transfer sta tes and b l u e shifts for the loca l exc itati o n states.K eywords Excitation sta te;Absorption and e m issi o n spectra;Solvent effects;Stocks shift(Ed.:I,X)。
抗癫痫药物5,5-二苯基乙内酰脲的制备实验报告参考模板
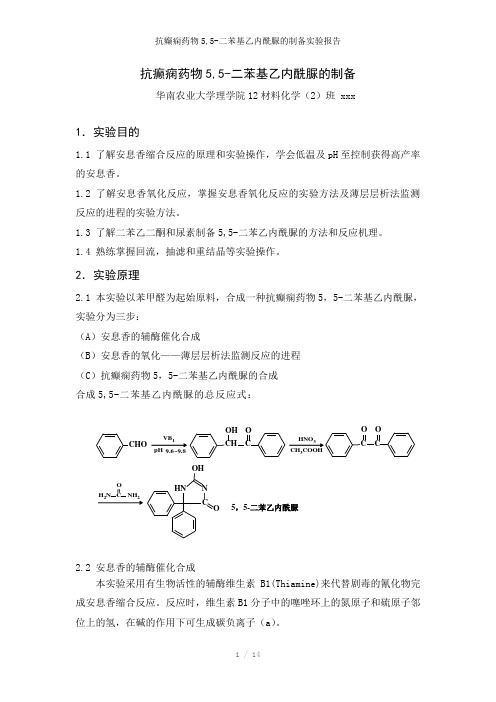
抗癫痫药物5,5-二苯基乙内酰脲的制备华南农业大学理学院12材料化学(2)班 xxx1.实验目的1.1 了解安息香缩合反应的原理和实验操作,学会低温及pH 至控制获得高产率的安息香。
1.2 了解安息香氧化反应,掌握安息香氧化反应的实验方法及薄层层析法监测反应的进程的实验方法。
1.3 了解二苯乙二酮和尿素制备5,5-二苯乙内酰脲的方法和反应机理。
1.4 熟练掌握回流,抽滤和重结晶等实验操作。
2.实验原理2.1 本实验以苯甲醛为起始原料,合成一种抗癫痫药物5,5-二苯基乙内酰脲,实验分为三步:(A )安息香的辅酶催化合成(B )安息香的氧化——薄层层析法监测反应的进程 (C )抗癫痫药物5,5-二苯基乙内酰脲的合成 合成5,5-二苯基乙内酰脲的总反应式:CHO1CH COH O pH 33CCO O C ONH H N N C HN OHO5,5-二苯乙内酰脲2.2 安息香的辅酶催化合成本实验采用有生物活性的辅酶维生素B1(Thiamine)来代替剧毒的氰化物完成安息香缩合反应。
反应时,维生素B1分子中的噻唑环上的氮原子和硫原子邻位上的氢,在碱的作用下可生成碳负离子(a )。
然后碳负离子(a)与苯甲醛作用生成中间体(b),(b)可以分离得到,经过异构化脱去质子得到中间体烯胺(c),(c)与另一分子苯甲醛作用得到安息香。
2.3 安息香的氧化——薄层层析法监测反应的进程有许多方法可以将安息香氧化成二苯基乙二酮,其中用硝酸氧化法较为简便。
简单的薄层层析法虽然不能准确地说明反应混合物中各组分的含量,但是它却可以方便而又清楚地告诉我们氧化反应的进程。
在反应过程中,通过不断取样进行分析来监测反应的进程有着实际应用意义。
如果反应进行时,不加以监测,为了反应安全,往往采取延长反应时间的办法,这不仅浪费了时间和能源,而且已经得到的产物往往还会进一步反应变化,使收率和产品纯度都较低。
2.4 抗癫痫药物5,5-二苯基乙内酰脲的合成二苯基乙二酮是一个不能烯醇化的α-二酮,当用碱处理时发生了碳架的重排,得到二苯基乙醇酸。
二苯基乙二酮的绿色合成方法分析

二苯基乙二酮的绿色合成方法分析
蔡峰;熊东;朱明伟;郑亿琦;李玉军
【期刊名称】《山西化工》
【年(卷),期】2024(44)5
【摘要】为进一步探究二苯基乙二酮的绿色合成方法,参考相关资料,以空气氧化法取代传统的硝酸氧化法进行实验,确定实验最优参数组合为:催化剂用量为催化剂摩尔分数15%、反应温度100℃、反应时间90 min。
在此基础上,进行循环实验后,得到了产率和纯度均较高的二苯基乙二酮产物,表明本次实验取得初步进展,预计其在实际生产中也将具有潜在应用价值。
【总页数】2页(P23-24)
【作者】蔡峰;熊东;朱明伟;郑亿琦;李玉军
【作者单位】不详
【正文语种】中文
【中图分类】O621.3
【相关文献】
1.[Bmim]Br-AlCl3离子液体催化合成二-(3,4-二甲氧基苯基)乙二酮
2.4-苯基-5-乙氧羰基-6-甲基-3,4-二氢嘧啶-2(1H)-酮的绿色合成研究
3.3,3'-二对乙氧基苯基-3,3'-二羟基-2,2'-二茚叉基-1,1'-二酮的合成
4.2,5-二甲氧基苯基烷基酮,4-叔丁基-2,5-二甲氧基苯基烷基酮,2,5-二甲基苯基烷基酮及其还原产物和加成产物的合成及光谱研究
5.[2′-溴-6′-(乙氧基甲基)-3′,4′-二甲氧基-苯基]-(2,3-二溴-4,5-二甲氧基-苯基)-甲酮的合成及其PTP1B酶抑制活性研究
因版权原因,仅展示原文概要,查看原文内容请购买。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
Vo.l 26高等学校化学学报No .92005年9月CHEM I CAL J OURNAL OF CH I NESE UN I VERSI T I E S1690~1694二苯基乙二酮结构和电子光谱的理论研究段晓惠,何荣幸,李象远,罗春燕(四川大学化工学院,成都610065)摘要 基于二苯基乙二酮结构优化,在TD-B3LYP /6-31+G *水平上讨论了两个异构体在气相和液相中的吸收和发射光谱.溶液中的计算采用可极化连续介质模型.结果表明,溶剂极性增加更有利于顺式非平面构型的形成,两个异构体的T 1和S 1态以及顺式非平面结构的S 2态都源于双羰基上的n →P *型局域激发,其余的单激发态则主要由苯环到羰基的P →P *跃迁决定.计算结果表明,溶剂效应可使电荷转移吸收、发射光谱红移和局域激发的光谱蓝移.关键词 激发态;吸收和发射光谱;溶剂效应;Stocks 漂移.中图分类号 O 641 文献标识码 A 文章编号 0251-0790(2005)09-1690-05收稿日期:2004-08-16.基金项目:国家自然科学基金(批准号:20373044)和教育部重点科技项目(批准号:02045)资助.联系人简介:李象远(1958年出生),男,博士,教授,博士生导师.从事理论化学研究.E-m ai:l xyl@i scu 二苯基乙二酮是一个典型的A -二羰基分子.作为非共轭芳香A -二羰基化合物的母体,关于其对称部分(即C 6H 5)CO 基团)的二面角H(图1),二苯基乙二酮表现出结构上的灵活性.一般而言,二苯基乙二酮有两个旋转异构体[1,2].研究结果表明,其基态结构呈现顺式非平面(c S )构型,H 值接近90b ,在晶态结构中约为111b 36c [3],在液相中约为98b [4].175e 时的气相电子衍射实验得到的H 为117b ,两个苯甲酰基处于近似平面的位置[5].然而,光异构化研究结果表明,其最低单重态(S 1)或三重态(T 1)的分子结构与基态截然不同.晶态甲基环己烷中的ODMR (Optical Detected M agnetic Reso -nance)研究[3]以及液相偶极矩的测定结果[6]表明,T 1态的二苯基乙二酮处于反式平面(t P )构型,用ENDOR (E lectron -Nuclear Double Resonance)测定其H 为157b ,U 为24b [7,8].在刚性或固体媒介中,观察到的双荧光或双磷光也可确定其在激发态存在c S 和弛豫的t P 两种构型[2,9].Yoshihara 等[10]测定了最低激发单态的c S 和t P 构型的吸收光谱.在S 1态,二苯基乙二酮经历快速的结构转变,从c S 构型弛豫到t P 构型.S i n gh 等[11]研究了溶液中二苯基乙二酮S 1态的构象弛豫动力学,表明在从c S 构型向t P 构型的转换过程中,形成了一个亚稳态的中间体,需越过两个连续的能垒.类似的光异构化现象在许多结构灵活的分子中存在,如1,2-二苯乙烯[12,13].实验上已用含时共振拉曼光谱以及皮秒和亚皮秒瞬时吸收光谱等对二苯基乙二酮的吸收和发射光谱进行了广泛研究[11,14,15],为确定电子态结构和激发态动力学过程提供了依据.本文用密度泛函理论(DFT )方法分别优化二苯基乙二酮在气相和液相中的结构,并讨论了溶剂对构型的影响.采用含时DFT(TDDFT)方法,计算了气相和液相的吸收和发射光谱,讨论了光谱性质、溶剂效应以及Stocks 漂移.所有计算均用Gaussian 03程序包完成[16].1 基态和激发态几何结构二苯基乙二酮的基态结构为c S 构型,在S 1和T 1态则弛豫到t P 构型.本文在B3LYP /6-31G**水平上,对这两个异构体进行构型优化.为了得到t P 构型的基态结构,避免在构型优化时向c S 构型弛豫,本文固定H 为180b 进行部分优化.得到的稳定结构见图1,频率分析结果表明没有虚频.尽管S 1和T 1Fig .1 S tructures of the t wo iso m ers of benz il(A)cis -Ske w ed ;(B )trans -planar .态的真实结构可能会丧失双羰基的共平面性,但偏离不大.ENDOR 测定T 1态的H 值为157b[7,8],溶液中的H 比157b 还大,故固定H 为180b 的部分优化对结构不会带来大的误差.溶液中的优化采用可极化连续介质模型(PC M ),在同样水平上进行.溶剂分别为非极性的环己烷(C H,E =210)和强极性的二甲亚砜(D M SO ,E =4616).优化构型的部分参数列于表1.T ab le 1 En ergies and structu ra l para m e ters of th e two iso m ers of ben zilC on fi gurati onM ed i um E /a .u .H /(b )U /(b )1029L /(C #m )$E */e V c SG as -phase -6891968812711101920100C yclohexane-6891973912201011120114DM SO-6891983411211411610140t PG as -phase -968196431801201000100C yclohexane -689196851801801000111DM SO-689197651802501000133*$E =E (s o l vent)-E (gas phase).对c S 构型进行结构优化,得到的H 与实验值较为吻合[3~5].小的U 值说明两个苯甲酰基处于近似平面的位置.通过比较发现,偶极矩随着溶剂极性的增加而增加,但H 和总能量降低,说明c S 构型在极性溶剂中更易存在.Pa w el k a 等[17]研究了溶剂对二苯基乙二酮构型的影响,本文的计算结果与其结论一致.固定H 为180b ,优化得到t P 构型的U 值随溶剂极性的增加而增加,而总能量降低,说明当溶剂极性增加时此构型更易形成.t P 构型的偶极矩都非常小,近似为零.比较c S 和t P 两种构型的能量,在气相中,t P 构型比c S 高0112e V,在环已烷中高0115e V,在DM-SO 中高0119e V,并且随着溶剂极性的增加,c S 构型能量降低幅度比t P 构型大.可见极性溶剂更利于c S 构型的形成,这可能与c S 构型的偶极矩比t P 构型大得多有关.2 吸收光谱的计算2.1 气相吸收光谱采用气相优化的c S 构型,即二苯基乙二酮的基态结构,计算了气相垂直激发态,结果列于表2.激发态偶极矩用加外场(?01001a .u.)的方法来估算.Tab l e 2 T ran sition energies of lo w-l ying excited states of c S b enz il at TD-B3LYP /6-31+G *leve lS t ate Trans i ti onE aT /e V f b 1029L /(C #m )1029D c/(C #m )E T ,expd/eVT 1 HO M O →LU M O(0173)e 213101000012101002136S 1 HO M O →LU M O(0167)217901000012601072182S 2HO M O →LU M O+1(0164)31770100001410106S 3HO M O-2→LUMO (0165)41080102401570142a .Trans i ti on en ergy ;b .oscill ator strength ;c .electron ic trans i ti ond i pole mom ent fro m S 0t o S i ;d .experi m ental val ue fro m refs .[10,18,19];e .dat a in paren t h es i s represent t h e w ei gh t of the electron trans i ti on.计算结果表明,T 1态是局域激发(LE )态,对应一个电子从双羰基的n 型最高占据分子轨道(HOMO)跃迁到P *型最低空分子轨道(LUMO)(图2),激发能为2131e V,相对于实验值2136e V,给出了一个低的误差(0105e V ).T 1态的这种定域在双羰基部分的n →P *跃迁特征与ENDOR 测量结果一致[8].S 1态对应的跃迁也是定域在双羰基上的n →P *(H O MO →LUMO )型跃迁,激发能(2179e V)和实验值(2182e V)非常接近.S 2态主要由HOMO →LUMO +1(n →P *)跃迁得到,同样为双羰基上的LE 态.S 3则为P →P *跃迁,电荷从主要定域在苯环上的HO MO-2向双羰基上的LUMO 转移,具有分子内1691N o .9段晓惠等:二苯基乙二酮结构和电子光谱的理论研究电荷转移(CT)特征.激发态的偶极矩均较小,最大的S 3态也只有0157@10-29C #m.CT 态的较小偶极矩可能与电荷从两个苯环向羰基转移的方向相反以及电荷转移量很小有关[18].振子强度和跃迁矩的计算结果表明,在实验上可观察到S 3态,其余的跃迁都是禁阻的.实验上能观察到T 1和S 1态的吸收光谱可能与振电耦合等因素有关.F ig .2 M o l ecu l ar orb itals involved i n th e lo w-l ying excited states of c S benz il2.2 液相吸收光谱用溶剂中优化的c S 构型和PC M 模型计算了二苯基乙二酮在溶剂中的垂直激发态,结果见表3.气相计算结果表明,激发态的偶极矩都很小,因此在液相中,本文不再计算其偶极矩.Tab le 3 Tran siti on energ i es of lo w -lyi n g excited states of c S benz il i n solven ts at PC M-TD -B 3LYP /6-31+G *leve lSo l ven t State Transiti onE T /e V f 1029D /(C #m )$(h M )*/e VCycl oh exan eT 1 HO M O →L UM O(0172)21400100001000109S 1 HO M O →L UM O(0167)21870100101090108S 2 HO M O →L UM O+1(0165)31770100201120100S 3HO M O-2→LUM O(0168)4107010520161-0101D M SOT 1 HO M O →L UM O(0172)21600100001000129S 1 HO M O →L UM O(0166)31080100101110129S 2 HO M O →L UM O+1(0166)31780100701240101S 3HO M O -2→LU M O (0167)4106010440156-0102*$(h M )=E T(sol vent)-E T(gas phas e).从表3可以看出,液相中的跃迁类型和能级顺序与气相中的完全相同.T 1和S 1态仍对应于双羰基上的n →P *型LE ,但激发能发生了变化.在环己烷中,T 1和S 1态的吸收光谱的能量分别发生了0109e V 和0108e V 的蓝移,在DM SO 中,则增加到0129e V.然而,对同是n →P *型LE 态S 2,其溶剂效应却非常小,这可能与LUMO +1和LUMO 的电子云分布不同有关.具有部分CT 特征的S 3态,其吸收光谱发生了微弱红移.液相中的振子强度和跃迁矩较气相中的有所增加,S 3态仍为最强的激发态.实验测得T 1和S 1态在环己烷中的吸收光谱分别为525nm (2136e V )和490nm (2153e V )[10].本文的计算结果与实验值的误差仅为0104和0134e V,处于TDDFT 方法允许的误差范围内.3 发射光谱3.1 气相发射光谱由于二苯基乙二酮的T 1和S 1态处于t P 构型,本文固定H 为180b ,对其进行优化,得到其稳定的基态结构.基于此优化结构,计算二苯基乙二酮在气相中的垂直发射光谱,结果列于表4.从图3可以看出,t P 构型的HOMO 和LUMO 与c S 构型的非常相似,都是定域在双羰基上的n 和P *型轨道.其T 1和S 1态就起源于HOMO →LUMO,即n →P *的局域跃迁.本文给出T 1态的跃迁能为1190e V,比实验值低0129e V,而S 1态的跃迁能和实验值非常吻合,误差仅为0108e V.HOMO-2和HOMO-1简并,S 2和S 3态分别从这两个简并轨道到LUMO 的跃迁获得,电荷从定域在苯环上的P 轨1692高等学校化学学报 V o.l 26道向定域在双羰基上的P *轨道转移,为分子内CT 态.振子强度和跃迁矩的计算结果表明,除S 3态是一弱的可见跃迁外,其余跃迁都是禁阻的.激发态的偶极矩都非常小,具有分子内CT 特征的S 2和S 3态也只有0104@10-29和0103@10-29C #m,由此可以推测电荷转移量很小.与气相吸收光谱相比,发射光谱发生了较大的S tocks 漂移,T 1态的Stocks 漂移为0141e V,S 1态的为0139e V.T ab le 4 T ransition energies of lo w-l ying excited states of t P b enz il at th e TD-B3LYP /6-31+G *levelS t ate T rans iti onE T /e V f 1029L /(C #m )1029D /(C #m )ET,ex pa/e V ET,Sb /e VT 1 HO M O →LUMO (0175)1190010000100010021190141S 1 HO M O →LUMO (0167)2140010010100011021480139S 2 HO M O-2→LU M O (0164)31550100001040102S 3HO M O-1→LU M O (0166)31560101401030133a .Experi m en t al val ues are fro m ref s .[10,19,20];b .E T ,Sstands f or the S t ocks s h ift ,equal to the d ifference of the tran siti on energi es at thec S and the t P con fi gu rations.F i g .3 M olecu lar orb itals i nvolved i n the l ow -lyi n g excited states of t P benzil3.2 液相发射光谱用液相中优化的t P 构型的基态结构计算了二苯基乙二酮在液相中的发射光谱,结果见表5.T ab le 5 T ransition energies of l ow -l y i ng exc ited states of t P ben zil i n solven ts a t PC M-TD -B3LYP /6-31+G *l evelSo l ven t State Trans i ti onE T /e V f 1029D /(C #m )$(h M )/e VE T,S /e V E T ,exp*/e VCycl oh exan eT 1 HOMO →LU M O (0174)119301000010001030147S 1 HOMO →LU M O (0167)2143010020116010301442133S 2 HOMO -1→LU M O(0168)3149010000100-0106S 3HOMO -2→LU M O(0169)3153010180138-0103D M SOT 1 HOMO →LU M O (0173)119901000010001090161S 1 HOMO →LU M O (0165)2149010050124010901592125S 2 HOMO -1→LU M O(0168)3142010000100-0113S 3HOMO -2→LU M O(0169)3149010150135-0107*Experi m en tal val ue i s fro m re.f [11].在两种溶剂中,T 1和S 1态与气相一样,仍为HOMO 到LUMO 的LE 态,源于双羰基上的n →P *型跃迁.在环己烷中,S 1态的跃迁能为2143e V,与实验值(2133e V )的误差为0110e V.在D M SO 中的跃迁能为2149e V,高估了实验值0124e V.与气相中跃迁相比,T 1和S 1态的跃迁能在环己环中蓝移了0103e V,在二甲亚砜中蓝移了0109e V.此外,S 2和S 3的能级顺序发生了变化.在气相中,S 2和S 3态分别取决于HOMO-2→L UMO 和HOMO -1→LUMO 跃迁,在液相则刚好相反.这可由HO MO -2和HOMO-1是两个几乎完全简并的轨道得到解释.液相中的S 3态仍是最强的跃迁态,其振子强度和跃迁矩较气相有所增加.计算结果表明,在两种溶剂中,CT 态S 2和S 3的跃迁能都发生了不同程度的红移,D M SO 中的红移几乎是环己烷中的2倍.最大的红移发生在DM SO 中的S 2态,为0113e V.液相的S tocks 漂移较气1693N o .9段晓惠等:二苯基乙二酮结构和电子光谱的理论研究1694高等学校化学学报V o.l26相有所增加,并且随着溶剂极性的增加而增加,这和溶剂极性对构型的影响一致.参考文献[1]A rnett J.F.,M c G l ynn S.P..J.Phys.Che m.[J],1975,79:626)629[2]A sano K.,A it a S.,A z um iT..J.Phys.Che m.[J],1984,88:5538)5541[3]B ro w n C.J.,Sadanaga R..A cta.C rystall ogr.[J],1965,18:158)162[4]Cum per C.W.N.,Thu rston A.P..J.Ch e m.Soc.,Per k i n T ran s.Ⅱ[J],1972:106)111[5]Shen Q.,H agen K..J.Phys.Che m.[J],1987,91:1357)1360[6]Fessenden R.W.,C arton P.M.,Sh i m a m oriH.et a l..J.Phys.Che m.[J],1982,86:3803)3811[7]Chan Y.,H eat h B.A..J.Che m.Phys.[J],1979,71:1070)1075[8]Tek iY.,Takn iT.,H i raiM.e t al..Che m.Phys.Lett.[J],1982,89:263)267[9]Bhattacaharya K.,Cho w dhury M..J.Photoche m.[J],1986,33:61)66[10]Ikeda N.,Kos h ioka H.,M asuh ara K.et al..Che m.Phys.Lett.[J],1988,150:452)456[11]S i ngh A.K.,PalitD.K.,M itt a l J.P..Che m.Phys.L ett.[J],2002,360:443)452[12]G al vao D.S.,S oos Z.G.,Ra m asesha S.et al..J.Ch e m.Phys.[J],1993,98:3016)3021[13]Soos Z.G.,Ra m as es ha S.,Galvao D.S.et al..Phys.R ev.B[J],1993,47:1742)1753[14]Eb i hara K.,H iura H.,Takah ash iH..J.Phys.Ch e m.[J],1992,96:9120)9127[15]Oku ts u T.,Ooya m aM.,Tan iK.et a l..J.Phys.C he m.[J],2001,105:3741)3744[16]Frisc h M.J.,Tru cks G.W.,Sch l egelH. B.et a l..Gau ssi an03,Rev i s i on B.01[CP],P i tts burgh PA.:Gauss i an Inc.,2003[17]Pa w el ka Z.,K ollA.,Zeegers-Huyskens Th..J.M o.l S truct.(Theoche m.)[J],2001,597:57)66[18]Y IH a-iBo(易海波),DUAN Xiao-H u i(段晓惠),L I X i ang-Yuan(李象远)e t a l..Ch e m.J.Ch i nese Un i versiti es(高等学校化学学报)[J],2003,24(8):1438)1441[19]Fang T.S.,S i nger L.A..Ch e m.Phys.Lett.[J],1978,60:117)121[20]Roy D.S.,Bhattacharyya K.,Bera S. C.e t al..Che m.Phys.Lett.[J],1980,69:134)140Theoretical Investigati on of Structure andE lectronic Spectru m of B enzilDUAN X iao-H u,i H E Rong-X ing,LI X i a ng-Yuan*,LUO Chun-Y an(Colle g e of Che m ical Engineer in g,S ichuan U ni ver sity,Chengdu610065,China)Abst ract In t h is w or k,the t w o iso m ers o f benzi,l cis-ske w ed(c S)and trans-p lanar(t P)confi g urations,w ere opti m ized both i n gas phase and i n so l u tion.B ased on the correspond i n g opti m a l structures,t h e absorption and e m issi o n spectra are d iscussed at the level ofTD-B3LYP/6-31+G*.The po larizable conti n uum m odel is ap-plied in the calcu l a ti o ns i n so lution.The ca lculated results indicate t h at the cis-ske w ed configurati o n is slightly favored when the po larity o f the so l v ent increases.T1and S1states o f the t w o iso m ers as w ell as S2state o f the cis-ske w ed configurati o n all arise fro m the local excitation o f n→P*type localized on the bicar bony lm o iety, but other exc ited si n g let states are do m i n ated by t h e P→P*transiti o n fro m the benzene ring to the car bony l group.The theoretica l calcu lations pred ict slight red shifts o f the absorption and e m issi o n spectra in so lvents for the charge transfer sta tes and b l u e shifts for the loca l exc itati o n states.K eywords Excitation sta te;Absorption and e m issi o n spectra;Solvent effects;Stocks shift(Ed.:I,X)。
