最新高中化学奥赛辅导有机化学部分全套课件汇总
高中化学有机化学PPT课件

利用金属(如铁、锌等)在酸性条件下还原硝基化合物为胺类。此 方法操作简便,但需注意防止过度还原和副反应的发生。
硫化物还原法
在碱性条件下,用硫化物(如硫化钠、硫氢化钠等)还原硝基化合物 为胺类。此方法适用于对酸敏感的硝基化合物的还原。
06
杂环化合物及生物活性物质简介
杂环化合物分类及命名
分类
的发展和进步。
谢谢您的聆听
THANKS
化学性质
相对稳定,主要发生自由基取代反应,如 卤代反应。
烯烃结构和性质
结构特点
含有一个或多个碳碳双键。
物理性质
随碳原子数增加,沸点、熔点逐渐升高, 但密度比相应烷烃小。
化学性质
较为活泼,可发生加成、氧化、聚合等反 应。
炔烃结构和性质
01
02
03
结构特点
含有一个或多个碳碳三键。
物理性质
与烯烃相似,但更为活泼。
可能包含各种元素。
结构特点
有机物分子结构复杂,具 有同分异构现象;无机物
分子结构相对简单。
性质特征
有机物大多具有可燃性、 难溶于水、反应速率较慢 等性质;无机物性质各异, 有些具有与有机物相似的
性质。
有机化学发展简史
萌芽时期
古代人们对天然动植物和矿物的
研究,为有机化学的萌芽奠定了
基础。
01
创立时期
高中化学有机化学PPT课件
CONTENTS
• 有机化学基本概念 • 烃类化合物性质与反应 • 烃衍生物性质与反应 • 羰基化合物性质与反应 • 含氮化合物性质与反应 • 杂环化合物及生物活性物质简
介 • 有机合成路线设计策略探讨
01
有机化学基本概念
2021届苏高中化学竞赛理论辅导课件-有机化学(提升)03对映异构(共34张PPT)

高中化学竞赛理论辅导
有机化学
(提升部分)
第3章 对映异构
镜象 实物
对映异构(属立体异构) 手性
一、具有一个手性中心的分子
CH3 C*H COOH 乳酸
OH
镜子
COOH
C
H
OH
CH3
对映体
COOH
C
HO
H
CH3
手性分子
手性中心 手性碳原子C*
结论 具有一个手性碳原子的化合物必定 是手性化合物,有一对对映体。(C连四 个不同的基团)
① H、H、H
CH3
③CH CH3 H C H 3① ②CH 2CH 3
② H、H、C
③> ② > ①
③ H、C、C
若手性碳原子上连有的基团含有双键或 三键,则可看成连接两个或三个相同的原子。
CHO H CH3
CH2OH
CHO 、 CH2OH 哪个大?
O CH
O
CH >
O
OH CH H
-I > -Br > -Cl > -SO3H > -SH > -F > -OCOR > -OR
S
HO CH3 CH
H C OH CH3
CH3 HO H CH3 OH
H
COOH HO H
CH3
S
CH3 HO H HO H
CH3
Fischer投影式 Newman投影式、锯架式
CHO H OH HO H
CH2OH
H OH CHO
HO H CH2OH
HO H
H OH
OHCCH2OH
Newman投影式 Fischer投影式
最新中学化学竞赛辅导课件+《有机化学部分》word版本

4. 与水加成
直接水合制乙醇的工业法
H3PO4 /硅藻土 CH 2 CH 2 + H2O 300℃, 70atm
CH 3CH 2OH
CH
CH
+
H2O
HgSO4 H 2SO 4
O
CH 3 C H
RC
CH
+
H2O
HgSO4 H 2SO 4
O
R C CH 3
CH CH 2 OH
RC CH 2 OH
5. 加次卤酸
RCC3H Cl
3. 与硫酸的加成
❖ 烯烃与硫酸在较低温度下形成硫酸氢酯, 硫酸氢酯在水存在下加热水解生成醇 — — 间接水合法
CH2 CH2 + H2SO4(98%) CH3CH2OSO3H H2O CH3CH2OH + H2SO4
(CH3)2C CH2 + H2SO4(50%) (CH3)3COSO3H H2O (CH3)3COH + H2SO4
+
71%
CH3CH2C CH2 CH3 29%
遵从Zaitsev (Saytzeff)规律
3. 与金属的反应
无 水 乙 醚
R X + M g
R M g X G r ig n a r d 试 剂
Grignard 试剂的反应
RMgX +
Et2O C O 无水
H2O H
R C OH
R C OMgX
五.芳香烃的主要化学性质
有机化合物的命名
系统命名法
命名法
普通命名法
俗名
系统命名法
❖ IUPAC命名法 ❖ 中文系统命名法(CCS):由中国化
学会根据IUPAC命名法的原则, 结合中文特点而制定的 ❖ 系统命名法化合物名称的构成: 立体化学名+取代基名+母体名
高中化学奥赛培训教程全集---之有机化学.doc
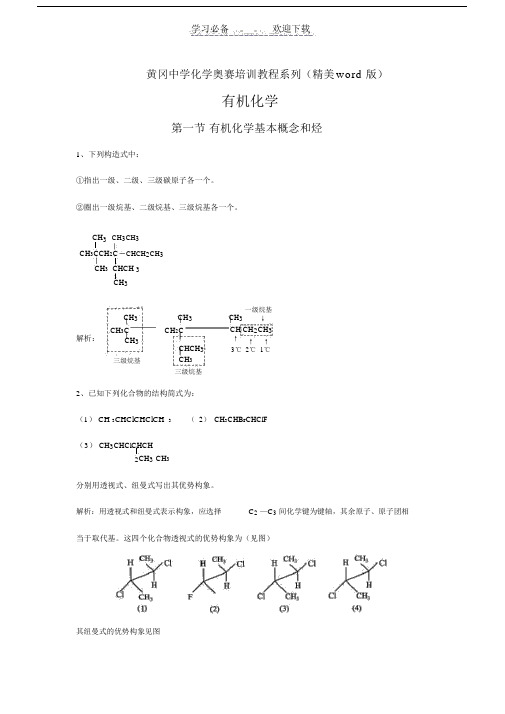
学习必备 欢迎下载黄冈中学化学奥赛培训教程系列(精美 word 版)有机化学第一节 有机化学基本概念和烃1、下列构造式中:①指出一级、二级、三级碳原子各一个。
②圈出一级烷基、二级烷基、三级烷基各一个。
CH 3 CH 3CH 3 CH 3CCH 2C CHCH 2CH 3CH 3 CHCH 3CH 3CH 3 CH 3 CH 3 一级烷基↓解析: CH 3CCH 2CCH CH 2CH 3CH 3CHCH 3↑ ↑ ↑3℃ 2℃ 1℃三级烷基CH 3三级烷基2、已知下列化合物的结构简式为: (1) CH 3CHClCHClCH 3 ( 2) CH 3CHBrCHClF( 3) CH 3CHClCHCH2CH 3 CH 3分别用透视式、纽曼式写出其优势构象。
解析:用透视式和纽曼式表示构象,应选择C 2 —C 3 间化学键为键轴,其余原子、原子团相当于取代基。
这四个化合物透视式的优势构象为(见图)其纽曼式的优势构象见图3、( 2000 年广东省模拟题)用烃 A 分子式为C10H16,将其进行臭氧化后,水解得到HCHO 和 A 催化加氢后得烃B, B 化学式为 C10H20,分子中有一个六元环,用键线式写出A,B 的结构。
解析:从 A 催化加氢生成的 B 的化学式可推知,原 A 分子中有两个C=C 键和一个六元环。
从水解产物可知, C1与 C6就是原碳环连接之处HCHO 的羰基,只能由C3支链上双键臭氧化水解生成。
所以 A 的结构为, B 的结构为。
4、下列化合物若有顺反异构,写出异构体并用顺、反及E、 Z 名称命名。
5、(河南省98 年竞赛题)写出符合C6H10的所有共轭二烯烃的异构体,并用E—Z命名法命名。
解析:6、用化学方法鉴别下列化合物:CH 3CH2CH2CH3,CH 3CH 2CH=CH 2, CH 3CH 2C≡ CH 。
解析:( 1)用 Br 2, CH 3CH 2CH=CH 2与 CH 3CH2 C≡ CH 可褪色, CH 3CH 2CH 2CH 3不反应。
高中化学竞赛——大学有机化学课件38

《有机化学》教学课件(76-04-1.0版)—第三十八讲
返回首页
第二部分: ——完成反应(写主产物或条件/试剂) 知识点——化学性质 NO2 (考查知识面) ? ? KMnO4 ? 稀、冷
Fe/HCl
KMnO4/H+ ?
①O3 ? ②Zn/H2O ? ?
-NO2 NH4HS
CH2=CHCH=CH2 + CH2=CHCN
返回首页
有 机 化 学 主 线
紫外
红外 核磁共振
质谱
物理分析方法 理论 写 命名 写 结构 决定
基础
IR和 1HNMR
应用 鉴别 分离
完成 性质 有机合成 进行 结
推测
注意
性 质
立体化学
反应机理
结构理论
构
关联
《有机化学》教学课件(76-04-1.0版)—第三十八讲
返回首页
第一部分——综合题 (一)命名或写结构式 !(考查基础知识) 知识点:习惯法、衍生法、系统法。
O -酮酸 CH3–C–CH2COOH O CH3–C–CH2–CH2COOH -酮酸 HOOCCH2–CH2COOH CH2–CH2 CH2–CH2 -二酸
CHCOOH 环烷烃甲酸
≥-二酸 HOOCCH2–CH2–CH2COOH
《有机化学》教学课件(76-04-1.0版)—第三十八讲
返回首页
H2/Ni
CH2NH2
《有机化学》教学课件(76-04-1.0版)—第三十八讲
返回首页
第三部分: ——反应机理 (考查理解能力) 知识点——反应机理 1)自由基取代 (P122)
2)亲电加成(AE) (P133) 3)正碳离子重排 (P137;P279;P180;P334) 4)亲核取代(SN) (P237;P239) 5)亲核加成(AN) (P340、P356) 6)芳环上的亲电取代(ArSE) 7)羟醛缩合 (P356-357) (P185;P227)
高中化学有机化学ppt课件

03有机物主要由碳、氢元素组成,还可能含有氧、氮、硫、磷等元素;无机物则可能包含各种元素。
组成元素有机物分子结构复杂,具有同分异构现象;无机物分子结构相对简单。
结构特点有机物大多具有可燃性、难溶于水、反应速率较慢等性质;无机物性质各异,有些具有与有机物相似的性质。
性质特征有机物与无机物区别古代人们对天然动植物和矿物的利用,如木材、药材、染料等。
萌芽时期18世纪末至19世纪初,贝采利乌斯等化学家提出有机化学概念,并合成尿素等有机化合物。
创立时期19世纪中后期,合成染料、香料、药物等有机化合物的出现,推动了有机化学的快速发展。
发展时期20世纪以来,随着物理和化学方法的不断进步,有机化学在合成、结构、反应机理等方面取得了巨大成就。
现代时期有机化学发展简史有机化合物分类及命名分类根据碳骨架形状,有机化合物可分为链状化合物和环状化合物;根据官能团类型,可分为烃类、醇类、醛类、酮类、羧酸类等。
命名有机化合物的命名遵循一定的规则和原则,包括选取主链、编号原则、官能团优先顺序等。
常见的命名法有普通命名法、系统命名法和衍生命名法等。
01结构特点碳原子间以单键相连,其余价键被氢原子饱和。
02物理性质随碳原子数增加,沸点、熔点逐渐升高,密度逐渐增大。
03化学性质相对稳定,主要发生取代反应,如卤代反应。
含有一个或多个碳碳双键。
结构特点物理性质化学性质随碳原子数增加,沸点、熔点逐渐升高,密度逐渐增大。
较为活泼,可发生加成反应、氧化反应、聚合反应等。
030201含有一个或多个碳碳三键。
结构特点随碳原子数增加,沸点、熔点逐渐升高,密度逐渐增大。
物理性质非常活泼,可发生加成反应、氧化反应、聚合反应等。
化学性质1 2 3含有苯环或其他芳香环结构。
结构特点具有特殊芳香味,沸点、熔点较高,密度较大。
物理性质相对稳定,可发生取代反应、加成反应等。
化学性质芳香烃结构和性质卤代烃结构和性质卤代烃的分子结构由烃基和卤素原子组成,卤素原子与烃基通过共价键连接。
最新高中化学竞赛有机化学基础课件

CH3COOH
pKa
4.76
ClCH2COOH 2.86
Cl2CHCOOH 1.36
Cl3CCOOH 0.63
取代羧酸的酸性与在烃基同一位置上引入-I基团的数目有关, 数目越多,酸性越强。
CH3CH2CH2COOH ClCH2CH2CH2COOH CH3CHClCH2COOH CH3CH2CHClCOOH
有机化学的任务
1.发现新现象(新的有机物,有机物的新的来源、 新的合成方法、合成技巧,新的有机反应等) 2.研究新的规律(结构与性质的关系,反应机理等) 3.提供新材料 (提供新的高科技材料,推动国民经 济和科学技术的发展) 4.探索生命的奥秘(生命与有机化学的结合)。
§有机化合物的特点
有机化合物的特点通常可用五个字概括:“多、燃、 低、难、慢”。
C
H
Cl
H
μ = 5.34 × 10-30 C.m
非极性共价键:两个相同原子组成的共价键,成键电子云 均匀分布在两核周围。
Cl2 ; H2 极性共价键:不同原子组成的共价键,成键电子云均偏向 电负性大的原子一边。HCl ;H2O
键的极性:键的极性大小取决于成键两原子电负性的 差值,与外界条件无关,是永久的性质。
转。
3、键的可极化度:较大。
3、键的可极化度:较小。
二、共价键的属性
1、键长:以共价键键合的两个原子核间的距离为键长。
2、键角:同一原子上的两个共价键之间的夹角。 3、键能:气态时原子A和原子B结合成1molA-B双原子分子 (气态)所放出的能量。
4、键的极性和键矩 键矩:极性共价键正或负电荷中心的电荷(q)与两个电 荷中心之间的距离(d)的乘积叫键矩(u)。
电负性: s sp sp2 sp3 p
高中化学《有机化学》总复习课件

CH3CH3 + H2 CH2=CH2 + H2 CH≡CH
水解
C2H5Br
HBr
消 去
H2O
CH3CH2OH
O2
O2 加H2
H2O CH3CHO
CH3COOC2H5
C2H5OH 水解
O2
CH3COOH
Na C2H5ONa
分子间脱水
C2H5—O—C2H5
延伸转化关系举例
CH H2 CH2 Br2 CH2Br 水解 CH2OH 脱H2 CHO O2 COOH
类 别 结构特点
烷烃 单键(C-C)
双键(C=C) 烯烃 二烯烃
(-C=C-C=C-)
主要性质
1.稳定:通常情况下不与强酸、 强碱、强氧化剂反应 2.取代反应(卤代) 3.氧化反应(燃烧) 4.加热分解 1.加成反应;与H2、X2、H X、H2O 2.氧化反应(燃烧;被KMnO4[H+] 氧化) 3.加聚反应 (加成时有1,4加成和1,2加成)
有机物:含碳元素的化合物 (除CO、CO2、碳酸盐、氰化物及金
属碳化物等)。
烃:仅含碳和氢两种元素的有机物称为碳氢 化合物.
烷烃:碳原子之间都以碳碳单键结合成链状 烃叫烷烃,也叫做饱和烃 .
烯烃 分子中含有碳碳双键的一类链烃叫做烯烃.
炔烃 分子里含有碳碳三键的一类链烃叫做炔烃.
芳香烃 分子里含有苯环的一类烃叫做芳香烃.
△
CH3CHO+2Cu(OH)2
CH3COOH+Cu2O↓+2H2O
醛
羧酸
有机反应类型——还原反应
还原反应:有机物分子里“加氢”或“去氧”的
反应其中加氢反应又属加成反应
高中化学奥赛辅导有机化学全套课件

“有机化学”部分
初赛基本要求:
有机化合物基本类型—烷、烯、炔、环烃、芳香烃、 卤代烃、醇、酚、醚、醛、酸、酯、胺、酰胺、硝基 化合物、磺酸的系统命名、基本性质及相互转化。异 构现象。C=C加成。取代反应。芳环香烃取代反应及 定位规则。芳香烃侧链的取代反应和氧化反应。碳链 增长与缩短的基本反应。分子的手性及不对称碳原子 的R、S构型判断。糖、脂肪、蛋白质的基本概念、通 式和典型物资、基本性质、结构特征以及结构表达式。
a
c
CC
a>b
b
b
c>d
(Z)-构型
Zusammen (同)
a
d
CC
b
c
(E)-构型
Entgegen(对)
次序规则:
(1)取代基的原子按原子序数大小排列,大者为“较 优”基团。
I>Br>Cl>S>P>F>O>N>C>D(氘1中子)>H -Br > -OH > -NH2 > -CH3 > -H
(2)若两个基团第一个原子相同(如C ),则比较与 它直接相连的几个原子,余类推。如:
(A) 若只有一个不饱和碳上有侧链,该不饱和碳编号为1; (B) 若两个不饱和碳都有侧链或都没有侧链,则碳原子编
号顺序除双键所在位置号码最小外,还要同时以侧链位 置号码的加和数为最小.
CH3
1
6
2
5
3
4
1-甲基-1-环己烯
H3C 3 2 1
4
6
5
3-甲基-1-环己烯
CH3
6 CH3
5
1
4
2
3
2024年高中化学竞赛大学有机化学课件6(附加条款版)

高中化学竞赛大学有机化学课件6(附加条款版)高中化学竞赛大学有机化学课件6一、引言化学竞赛作为高中阶段学生提高化学素养、培养化学思维的重要途径,一直受到广泛关注。
有机化学作为化学竞赛的重要组成部分,对于参赛选手来说至关重要。
本课件旨在帮助高中化学竞赛选手更好地掌握大学有机化学知识,提高竞赛成绩。
二、有机化学基本概念1.有机化合物:含有碳元素的化合物,通常与生命活动密切相关。
2.有机反应:有机化合物在一定条件下发生的化学变化,包括合成、分解、取代、加成等。
3.有机化合物结构:碳原子之间的成键方式,包括单键、双键、三键以及环状结构等。
4.有机化合物的分类:根据分子结构、官能团、反应类型等不同特点进行分类。
三、有机化学基本反应1.烷烃的卤代反应:烷烃与卤素单质在光照条件下发生取代反应,卤代烷。
2.烯烃的加成反应:烯烃与卤素单质、水、卤化氢等发生加成反应,卤代烷、醇等化合物。
3.炔烃的加成反应:炔烃与卤素单质、水、卤化氢等发生加成反应,卤代烷、醛、羧酸等化合物。
4.醇的氧化反应:醇在酸性条件下与氧化剂如酸性高锰酸钾、铬酸等反应,醛、酮等化合物。
5.醛、酮的还原反应:醛、酮与还原剂如氢气、锂铝氢化剂等反应,醇。
6.羧酸的酯化反应:羧酸与醇在酸性条件下反应,酯。
7.芳香烃的取代反应:芳香烃在一定条件下与取代基发生取代反应,取代芳香烃。
四、有机化学合成策略1.反应途径的选择:根据目标产物的结构特点,选择合适的反应途径。
2.反应条件的优化:通过调整反应温度、压力、催化剂等条件,提高反应产率和选择性。
3.保护基的应用:在合成过程中,通过引入保护基,保护敏感官能团,提高反应可控性。
4.反应顺序的安排:合理安排反应顺序,避免不必要的副反应,提高合成效率。
五、有机化学竞赛实例分析1.合成题目分析:分析题目所给的反应物和产物,确定反应类型和合成路线。
2.反应机理探讨:根据反应类型,推导反应机理,理解反应过程。
3.实验操作注意事项:分析实验操作步骤,注意实验安全,提高实验技能。
高中化学竞赛全套课件

化学反应与能量转化
化学反应的能量守恒定律
化学反应中,反应物的总能量等于生成物的总能量,能量守恒是 化学反应的基本规律。
熵变与自发反应
熵变是反应能否自发进行的判据,熵增加的反应更容易自发进行。
催化剂的作用
催化剂可以降低反应的活化能,加速化学反应的速率。
周期与族
元素周期表分为七个周期和十八个族 ,每个周期和族的元素具有相似的性 质和电子排布规律。
化学键与分子结构
01
02
03
离子键与共价键
离子键是由电子转移形成 的,共价键则是通过共享 电子形成的。
分子轨道理论
分子轨道理论解释了分子 中电子的排布和运动,是 理解分子结构和化学键的 重要理论。
分子几何构型
数据处理
掌握实验数据的记录、整理、分析和 处理方法,能够根据实验结果得出正 确的结论。
实验报告撰写与评价
实验报告撰写
能够按照规定的格式和要求,撰写内容完整、条理清晰的实验报告,包括实验 目的、材料与方法、结果与讨论等部分。
实验评价
能够对实验过程和结果进行客观的评价,发现实验中存在的问题并提出改进意 见,促进实验技能的提高。
铁元素及其化合物
铁是过渡金属之一,广泛 用于制造钢铁和其他合金 ,存在于铁锈、氧化铁和 许多其他化合物中。
铝元素及其化合物
铝是轻金属之一,广泛用 于制造铝制品和其他合金 ,存在于明矾、氧化铝和 许多其他化合物中。
无机化学反应类型与规律
置换反应
一种物质取代另一种物质的 过程,例如金属与酸的反应 。
复分解反应
两种物质相互交换成分生成 另外两种物质的过程,例如 酸与碱的反应。
高中化学竞赛——大学有机化学31ppt课件

O
K2Cr2O7 H2SO4
苯胺黑(黑色染料)
漂白粉 显紫色(可用于苯胺的鉴别) 溶液
《有机化学》教学课件(76-04-1.0版)—第三十一讲
返回首页
芳胺容易被氧化,要想氧化芳胺环上的其它官能团 而不损害氨基,就必须先将氨基“保护”起来。
保护氨基的方法:先进行酰基化反应,待其它反应 完成后,再将酰基水解掉。
返回首页
C H N H 成盐3 :2 C · H · N + H H C 用l 3 途:C 3 遇H 分强离N H 碱提+ 纯C !3 l - - 2 强酸弱· H 碱C l 盐)
NH2 +H2SO4
NH2·H2SO4
(二)烷基化和酰基化
胺
遇 到
醇、 酚
1、烷基化
伯卤代烃和有活泼 卤原子的芳卤化物
.. RNH2 +RCH2Cl
②>④ > ① > ③
2、①丙胺、②2-氨基-1-丙醇、③3-氨基-1-丙醇 ① > ③> ②
3、①丙胺、②3-氯丙胺、③1-氯丙胺、④2-氯丙胺 ①>②>④>③
4、①苯胺、②对氯苯胺、③对硝基苯胺、④对溴苯胺、
⑤对甲氧基苯胺、⑥2,4-二硝基苯胺 ⑤>①>④>②>③>⑥
《有机化学》教学课件(76-04-1.0版)—第三十一讲
2、化学性质——★还原
NO2 H
酸性条件下:
NO H
NHOH H
NO2
NH2
Fe或HSn2//NHiCl
返回首页
NH2
★注意:
NO2 SnCl2/浓HCl
-CHO △
NH2 -CHO
在中性或碱性介质中的还原非常复杂,在此记住:
2
NO2 ZFne/NaOH
