测定空气中氧气含量的装置(全)之欧阳家百创编
测定空气中氧气含量的装置(全)

测定空气中氧气含量的常见的装置(全)江苏省特级教师赵美荣序号装置实验操作图1 用凸透镜将太阳光聚焦到白磷,使白磷燃烧,一段时间后,白磷燃烧。
燃烧完毕,待冷却至室温,打开弹簧夹,烧杯中的水倒吸进入瓶内。
图2 闭合电源开关,电阻丝发热,温度达到40 ℃时白磷燃烧,产生大量白烟。
装置冷却后,由于左侧中氧气被消耗,气体压强减小,水会在左侧中上升,且上升到1刻度处。
图3 先关闭弹簧夹a,将螺旋状的铜丝在酒精灯的灼烧后迅速插入大试管,接触试管底部的过量的白磷,然后立即塞紧橡皮塞。
由于白磷的着火点低,白磷燃烧,产生大量的白烟。
燃烧完毕,待冷却至室温,打开弹簧夹,烧杯中的水倒吸进入瓶内。
图4 用水浴加热的办法使白磷燃烧,足以使白磷着火燃烧。
燃烧完毕,待冷却至室温,打开弹簧夹,烧杯中的水倒吸进入瓶内。
图5 在一封闭的试管内放一颗白磷,用酒精灯微微加热白磷,白磷燃烧,有大量白烟生成,注射器被推向外侧(右侧)。
待装置冷却,注射器逐渐向内侧(左侧)移动,根据注射器停止时的位置,确定空气中氧气的体积。
图6 在一端封闭的粗玻璃管内放一颗白磷,用胶塞塞住,并推入到玻璃管中部,记下位置。
用酒精灯微微加热白磷,白磷燃烧,有大量白烟生成,胶塞被推向外侧(右侧)。
待装置冷却,胶塞逐渐向内侧(左侧)移动,根据胶塞停止时的位置,确定空气中氧气的体积。
图7 用生石灰和水反应时放出的热量使白磷燃烧。
烧杯上方玻璃管(预先固定好)中部有一可左右滑动的活塞,活塞左端管内密封有空气,活塞右端的玻璃管口跟空气连通,实验开始前活塞处在刻度5 cm处。
图8 在一个耐热活塞的底部放一小块(足量)白磷,然后迅速将活塞下压,使空气内能增大,温度达到40℃。
白磷燃烧,产生大量白烟,冷却至原来温度时,松开手,活塞最终将回到刻度4处。
图10 在一玻璃管的两端,通过橡皮塞装上两只注射器,玻璃管内装几团细的铜丝,把一个注射器内的空气体积调到50mL的位置,另一只注射器不留空气加热玻璃管的铜丝部位。
【整理】触电事故典型案例之欧阳家百创编

落实安全规章制度欧阳家百(2021.03.07)强化安全防范措施触电事故典型案例高压线下吊运作业,汽车扒杆碰线触电,电死扶绳汽车司机。
1984 年 3 月 28 日下午,某厂运输车间运水泥构件,汽车吊扒升到距 10 千伏高压线约 100 毫米处,因承重摆动扒杆而碰触高压线,致使扶钢丝绳的汽车司机触电死亡。
这次作业违反了“在 10 千伏高压线下作业,安全间距不应小于 2 米”的规定,且由非司机开车,导致悲剧的发生。
水沟焊管搭接回路线,手脚潮湿触电命归天。
1988 年 7 月 31 日上午,某厂职工子弟中学校办工厂,在承包工程的室外地沟里进行对接管道作业的青年管工拉着焊机二次回路线,往焊管上搭接时触电,倒地后将回路线压在身下触电身亡。
该管工在雨后有积水的管沟内摆对接管时,脚上穿的塑料底布鞋、手上戴的帆布手套均已湿透。
当右手拉电焊机回路线往钢管上搭接时,裸露的线头触到戴手套的左手掌上,使电流在回线——人体——手把线(已放在地上)之间形成回路,电流通过心脏。
尤其是触电倒下后,在积水的沟内,人体成了良好的导体,那时人体电阻在 1000 欧左右,电焊机空载二次电压在 70 伏左右,则通过人体的电流 70 毫安。
而成人通常的致颤电流即致命电流为 50 毫安。
70 毫安电流使其心脏不能再起压送血液的作用,所以血液循环停止造成死亡。
环境的不安全因素加之缺乏安全用电知识使年仅 23 岁的青工死于非命。
类似的事故还有 1998 年 7 月 17 日下午某厂一铆工在进行点焊固定工件作业时触电身亡。
原因是非电焊工干点焊;所用焊把末端因绝缘破损而漏电;天气高温炎热,又为保产品质量,工作地点不能使用降温风扇,以致所穿戴的工作服、防护手套被汗湿透。
上述这些因素使入厂才一上,虚岁才 20 的小伙子离开了人间。
拆低压不停上方高压电,遭电击高处坠丧落了命。
1993 年 11 月 7 日上午,某厂动力外线班班长与徒弟一起执行拆除动力线任务。
测定空气中氧气含量的装置(全)

测定空气中氧气含量的常见的装置(全)实验操作用凸透镜将太阳光聚焦到白磷,使 白磷燃烧,一段时间后,白磷燃烧燃烧完毕,待冷却至室温,打开弹 簧夹,烧杯中的水倒吸进入瓶内。
闭合电源开关,电阻丝发热,温度 达到40 C 时白磷燃烧,产生大量白 烟。
装置冷却后,由于左侧中氧气被消 耗,气体压强减小,水会在左侧中 上升,且上升到1刻度处。
先关闭弹簧夹a ,将螺旋状的铜丝在 酒精灯的灼烧后迅速插入大试管, 接触试管底部的过量的白磷,然后 立即塞紧橡皮塞。
燃烧完毕,待冷却至室温,打开弹 簧夹,烧杯中的水倒吸进入瓶内。
用水浴加热的办法使白磷燃烧,足 以使白磷着火燃烧。
燃烧完毕,待冷却至室温,打开弹 簧夹,烧杯中的水倒吸进入瓶内。
由于白磷的着火点低,白磷燃烧, 产生大量的白烟。
装置图2图3图4在一封闭的试管内放一颗白磷,用酒精灯微微加热白磷,白磷燃烧,有大量白烟生成,注射器被推向外侧(右侧)。
待装置冷却,注射器逐渐向内侧(左侧)移动,根据注射器停止时的位置,确定空气中氧气的体积。
在一端封闭的粗玻璃管内放一颗白磷,用胶塞塞住,并推入到玻璃管中部,记下位置。
待装置冷却,胶塞逐渐向内侧(左侧)移动,根据胶塞停止时的位置, 确定空气中氧气的体积。
用生石灰和水反应时放出的热量使白磷燃烧。
烧杯上方玻璃管(预先固定好)中部有一可左右滑动的活塞,活塞左端管内密封有空气,活塞右端的玻璃管口跟空气连通,实验开始前活塞处在刻度5 cm处。
在一个耐热活塞的底部放一小块(足量)白磷,然后迅速将活塞下压,使空气内能增大,温度达到40C。
白磷燃烧,产生大量白烟,冷却至原来温度时,松开手,活塞最终将回到刻度4处。
用酒精灯微微加热白磷,白磷燃烧,有大量白烟生成,胶塞被推向外侧(右侧)。
1-1图5图7在一玻璃管的两端,通过橡皮塞装 上两只注射器,玻璃管内装几团细 的铜丝,把一个注射器内的空气体 积调到50mL 的位置,另一只注射器 不留空气加热玻璃管的铜丝部位。
煤矿安全监控系统及检测仪器使用管理规范之欧阳家百创编

煤矿安全监控系统及检测仪器使用管理规范(AQ1029—2019)欧阳家百(2021.03.07)中华人民共和国应急管理部发布1 范围本标准规定了煤矿安全监控系统及检测仪器的装备、设计和安装、传感器设置、使用与维护、系统及联网信息处理、管理制度与技术资料等要求。
本标准适用于全国井工煤矿,包括生产、新建和改、扩建矿井。
2 规范性引用文件下列文件对于本文件的应用是必不可少的。
凡是注日期的引用文件,仅注日期的版本适用于本文件。
凡是不注日期的引用文件,其最新版本(包括所有的修改单)适用于本文件。
AQ6201煤矿安全监控系统通用技术要求MT/T423 空气中甲烷校准气体技术条件3 术语和定义下列术语和定义适用于本文件。
3.1煤矿安全监控系统 coal mine safety monitoring system具有模拟量、开关量、累计量采集、传输、存储、处理、显示、打印、声光报警、控制等功能,用于监测甲烷浓度、一氧化碳浓度、风速、风压、温度、烟雾、馈电状态、风门状态、风筒状态、局部通风机开停、主要通风机开停等,并实现甲烷超限声光报警、断电和甲烷风电闭锁控制等,由主机、传输接口、分站、传感器、断电控制器、声光报警器、电源箱、避雷器等设备组成的系统。
3.2传感器 transducer将被测物理量转换为电信号输出的装置。
3.3甲烷传感器 methane transducer连续监测矿井环境气体中及抽放管道内甲烷浓度的装置,一般具有显示及声光报警功能。
3.4风速传感器 air velocity transducer连续监测矿井通风巷道中风速大小的装置。
3.5风压传感器 wind pressure transducer连续监测矿井通风机、风门、密闭巷道、通风巷道等地点通风压力的装置。
3.6一氧化碳传感器 carbon monoxide transducer连续监测矿井中煤层自然发火及胶带输送机胶带等着火时产生的一氧化碳浓度的装置。
测定空气中氧气含量实验的改进与思考

2020年第9期教育与装备研究实验教学测定空气中氧气含量实验的改进与思考金隆㊀欧阳根乐摘㊀要:浙教版‘科学“教材中 测定空气中氧气含量 的实验存在操作困难㊁结果不稳定和不利分组实验等问题㊂利用白磷燃点较低的特点,结合医用西林瓶㊁输液管等常见器材,改进实验设计,降低了实验操作难度,便于学生参与实验,提升了实验可见度和可信度,有效解决了教材实验中存在的问题㊂关键词:初中科学;测定空气中氧含量;实验改进;思考金隆,浙江省天台县教育局教研室书记;欧阳根乐,浙江省天台县外国语学校,一级教师㊂㊀㊀一㊁问题提出测定空气中氧气含量的实验是浙教版‘科学“八年级下册第3章 空气与生命 第1节 空气与氧气 中的一个探究性实验,活动设计如图1所示[1]㊂图1㊀教材中 测定空气中氧气含量的实验 活动设计该实验活动通过燃烧红磷消耗空气中的氧气,并将其转化的产物五氧化二磷固体粉末经水吸收及沉淀后,读出集气瓶内进入的水位所占原剩余容积的比例(即氧气在空气中的体积比),初步测出空气中的氧气体积含量㊂但在实验过程中存在如下问题[2]㊂①红磷着火点为260ħ,点燃需加热较长时间,且点燃后还在外界空气中燃烧一段时间,往往造成红磷在瓶内燃烧的量不够,难以最大程度地消耗瓶内氧气,使测量值偏低㊂②利用固定在双孔橡胶塞上的药匙加热点燃红磷,燃烧后不便于塞入集气瓶;塞入时由于燃烧的高温造成瓶内空气膨胀外溢,使测量值受影响;由于操作者对燃烧的紧张情绪,可能没塞紧橡皮塞,气密性较差,在瓶内燃烧结束后的静置冷却过程中,外界空气进入瓶内,使得测量值偏小甚至实验失败㊂③冷却需要较长时间㊂更多时候,操作者为了节约授课时间,未待集气瓶完全冷却便打开止水夹,瓶内部分气体沿导管逸出,使测量值偏小㊂④集气瓶容积较大,且瓶颈与瓶身并非等径圆柱体,在容积等份上存在困难㊂⑤实验后,导管中的气体也被压入集气瓶,使测量值偏低㊂⑥该实验有一定操作难度,且燃烧后产生有毒物质,所以基本以教师演示为主,无法进行学生的分组实验或随堂实验,可见度较差,学生主体地位不能充分发挥㊂75实验教学教育与装备研究2020年第9期㊀㊀二㊁实验的改进(一)实验器材及药品医用西林瓶(5mL)㊁输液导管及开关㊁小烧杯(2个)㊁镊子㊁小刀㊁白磷㊁水和开水㊂(二)实验装置(见图2)图2㊀改进后的实验装置(三)实验步骤①取输液导管灌满水,关闭开关,连接好西林瓶瓶塞,待用㊂②往西林瓶中加入少量水(用以吸收五氧化二磷),在瓶壁上将瓶内剩余的容积即空气部分五等分㊂用镊子夹取并缓慢切取绿豆大小的白磷,小心地放入瓶内,盖紧㊂③在两个烧杯中分别加入半杯左右的冷水(室温)和开水,冷水中滴加几滴红墨水㊂④按图2所示连接实验装置,注意保持插入冷水中的导管口浸没在水中㊂⑤将西林瓶部分浸入热水加热,稍倾斜瓶身,使白磷露出水面,引燃㊂⑥充分燃烧后,将西林瓶浸入冷水中快速冷却㊂⑦当瓶内白烟褪尽,取出西林瓶静置于桌面,打开输液管上的开关,观察西林瓶内的液位变化,如图3所示㊂(四)实验注意事项白磷是危化品,毒性大且易自燃,接触过白磷的实验用品必须进行适当的处理:小刀和镊子要在通风厨中用酒精灯灼烧;吸水纸在通风厨中烧掉;水槽要冲洗数遍㊂人若不小心接触白磷,要立即用水冲洗,然后用2%的CuSO4溶液(或2%的AgNO3溶液)轻抹,再用3%5%图3㊀西林瓶内的液位变化的NaHCO3溶液湿敷,禁止用油脂性的烧伤药膏㊂建议取放白磷操作均由专业教师完成,实验完成后西林瓶由授课教师收回统一处理㊂㊀㊀三㊁实验改进后的效果及反思(一)效果白磷着火点为40ħ,不需明火高温加热㊂改进后的实验过程中,燃烧均在密闭的西林瓶内发生,不会出现无产物外泄而污染环境的现象㊂西林瓶容积小,密闭性好,反应后的进水现象明显,测量误差也更小㊂改进后的实验便于采用分组的随堂实验方式进行教学,提高了可见度,增加了可信度,深化了基于科学本质的科学课堂教学改革,也进一步发挥了学生的主体地位㊂总的来说,改进后的实验科学合理㊁材料易得㊁操作简便㊁安全环保㊁现象明显㊂(二)反思观察和实验是科学的基础,问题导向下的改进和创新实验是我们科学教育人永恒追求的话题和努力的方向㊂改进实验利用 瓶瓶罐罐当仪器,拼拼凑凑做实验 ,使普遍的统一的科学概念㊁原理㊁规律和经验事实由 千言万语说不清 变成 一做实验就分明 ㊂这种改变,也更让学生体悟科学源于生活,科学就在身边,科学并不神秘㊂参考文献:[1]朱清时.义务教育教科书.科学(八年级下册)[M].浙江:浙江教育出版社,2014:71-72.[2]王耀村.初中科学创新实验[M].浙江:浙江科学技术出版社,2018:88-96.85。
测定空气中氧气含量的实验装置

测定空气中氧气含量的实验装置空气中氧气含量的实验装置是用于测定空气中氧气含量的仪器,也被称为氧气分析仪。
本文将介绍氧气分析仪的原理、使用方法、应用范围以及注意事项。
一、原理氧气分析仪的原理是利用电化学方法,即将空气通过一个电极间隙,使氧气被还原成氧离子,然后测量电极间的电压差。
电极的材料一般是铂,它在氧气存在下可以被还原,在电子供给下可以氧化成耗氧的离子,根据离子传输过程中的电势差测得氧气含量。
二、使用方法1. 准备工作:将氧气分析仪和相应的电极、电缆等组装好,插好电源;根据需要调整仪器的测量范围。
2. 开始测量:将电极浸泡在待测气体中,开启仪器的预热功能并等待一段时间。
然后开始实际测量,并记录下测量结果。
3. 清洗和保养:使用完氧气分析仪后,需要对其进行清洗和保养,以延长其使用寿命。
三、应用范围氧气分析仪主要应用于以下领域:1. 环境监测:测量空气中氧气含量,了解环境污染的程度。
2. 工业生产:在某些工业生产过程中,需要测量空气中氧气含量,以保证生产的稳定性。
3. 医疗保健:氧气分析仪也被用于医疗保健领域,如测量氧气瓶中氧气含量等。
四、注意事项1. 氧气分析仪使用前要仔细阅读使用说明书并遵循相应的安全操作规程。
2. 在使用前,检查仪器的电极和电缆是否完好,并根据需要校准仪器。
3. 使用时要注意保持电极的清洁和干燥,以避免误差产生。
4. 处理氧气分析仪时要特别注意,避免损坏或电极污染。
通过对氧气分析仪的原理、使用方法、应用范围以及注意事项的介绍,我们可以更好地了解氧气分析仪的特点和使用方法,使得我们在实验操作过程中更加准确、安全和有效。
测定空气中氧气含量的装置(全)
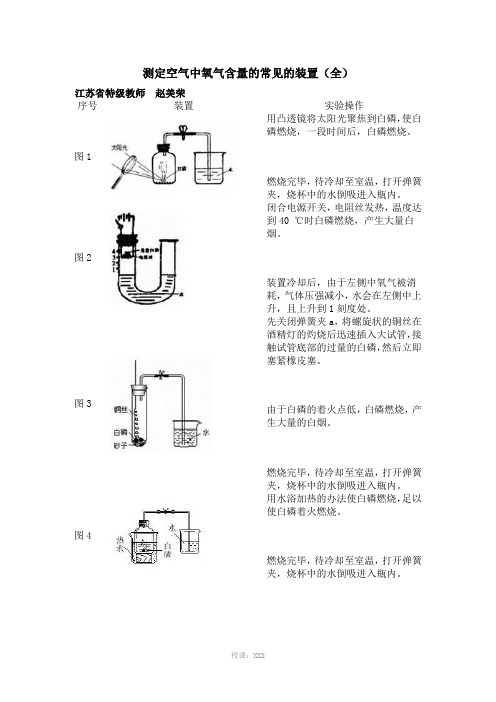
测定空气中氧气含量的常见的装置(全)江苏省特级教师赵美荣序号装置实验操作图1 用凸透镜将太阳光聚焦到白磷,使白磷燃烧,一段时间后,白磷燃烧。
燃烧完毕,待冷却至室温,打开弹簧夹,烧杯中的水倒吸进入瓶内。
图2 闭合电源开关,电阻丝发热,温度达到40 ℃时白磷燃烧,产生大量白烟。
装置冷却后,由于左侧中氧气被消耗,气体压强减小,水会在左侧中上升,且上升到1刻度处。
图3 先关闭弹簧夹a,将螺旋状的铜丝在酒精灯的灼烧后迅速插入大试管,接触试管底部的过量的白磷,然后立即塞紧橡皮塞。
由于白磷的着火点低,白磷燃烧,产生大量的白烟。
燃烧完毕,待冷却至室温,打开弹簧夹,烧杯中的水倒吸进入瓶内。
图4 用水浴加热的办法使白磷燃烧,足以使白磷着火燃烧。
燃烧完毕,待冷却至室温,打开弹簧夹,烧杯中的水倒吸进入瓶内。
图5 在一封闭的试管内放一颗白磷,用酒精灯微微加热白磷,白磷燃烧,有大量白烟生成,注射器被推向外侧(右侧)。
待装置冷却,注射器逐渐向内侧(左侧)移动,根据注射器停止时的位置,确定空气中氧气的体积。
图6 在一端封闭的粗玻璃管内放一颗白磷,用胶塞塞住,并推入到玻璃管中部,记下位置。
用酒精灯微微加热白磷,白磷燃烧,有大量白烟生成,胶塞被推向外侧(右侧)。
待装置冷却,胶塞逐渐向内侧(左侧)移动,根据胶塞停止时的位置,确定空气中氧气的体积。
图7 用生石灰和水反应时放出的热量使白磷燃烧。
烧杯上方玻璃管(预先固定好)中部有一可左右滑动的活塞,活塞左端管内密封有空气,活塞右端的玻璃管口跟空气连通,实验开始前活塞处在刻度5 cm处。
图8 在一个耐热活塞的底部放一小块(足量)白磷,然后迅速将活塞下压,使空气内能增大,温度达到40℃。
白磷燃烧,产生大量白烟,冷却至原来温度时,松开手,活塞最终将回到刻度4处。
图10 在一玻璃管的两端,通过橡皮塞装上两只注射器,玻璃管内装几团细的铜丝,把一个注射器内的空气体积调到50mL的位置,另一只注射器不留空气加热玻璃管的铜丝部位。
测定空气中氧气含量地装置(全)
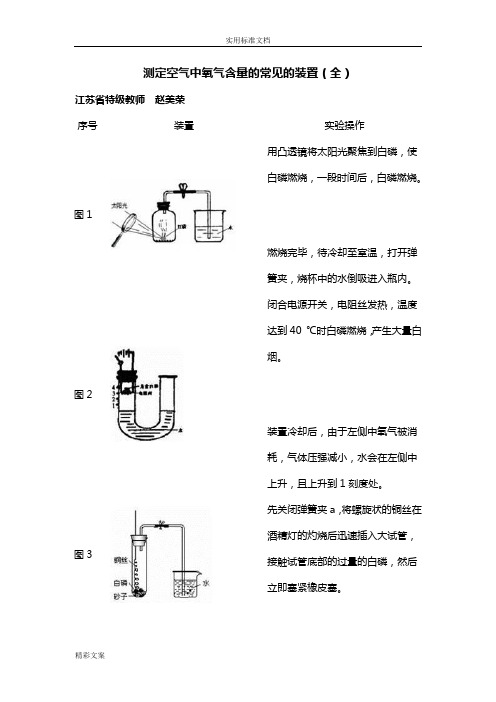
测定空气中氧气含量的常见的装置(全)江苏省特级教师赵美荣序号装置实验操作图1 用凸透镜将太阳光聚焦到白磷,使白磷燃烧,一段时间后,白磷燃烧。
燃烧完毕,待冷却至室温,打开弹簧夹,烧杯中的水倒吸进入瓶内。
图2 闭合电源开关,电阻丝发热,温度达到40 ℃时白磷燃烧,产生大量白烟。
装置冷却后,由于左侧中氧气被消耗,气体压强减小,水会在左侧中上升,且上升到1刻度处。
图3 先关闭弹簧夹a,将螺旋状的铜丝在酒精灯的灼烧后迅速插入大试管,接触试管底部的过量的白磷,然后立即塞紧橡皮塞。
由于白磷的着火点低,白磷燃烧,产生大量的白烟。
燃烧完毕,待冷却至室温,打开弹簧夹,烧杯中的水倒吸进入瓶内。
图4 用水浴加热的办法使白磷燃烧,足以使白磷着火燃烧。
燃烧完毕,待冷却至室温,打开弹簧夹,烧杯中的水倒吸进入瓶内。
图5 在一封闭的试管内放一颗白磷,用酒精灯微微加热白磷,白磷燃烧,有大量白烟生成,注射器被推向外侧(右侧)。
待装置冷却,注射器逐渐向内侧(左侧)移动,根据注射器停止时的位置,确定空气中氧气的体积。
图6 在一端封闭的粗玻璃管内放一颗白磷,用胶塞塞住,并推入到玻璃管中部,记下位置。
用酒精灯微微加热白磷,白磷燃烧,有大量白烟生成,胶塞被推向外侧(右侧)。
待装置冷却,胶塞逐渐向内侧(左侧)移动,根据胶塞停止时的位置,确定空气中氧气的体积。
图7 用生石灰和水反应时放出的热量使白磷燃烧。
烧杯上方玻璃管(预先固定好)中部有一可左右滑动的活塞,活塞左端管内密封有空气,活塞右端的玻璃管口跟空气连通,实验开始前活塞处在刻度5 cm处。
图8 在一个耐热活塞的底部放一小块(足量)白磷,然后迅速将活塞下压,使空气内能增大,温度达到40℃。
白磷燃烧,产生大量白烟,冷却至原来温度时,松开手,活塞最终将回到刻度4处。
图10 在一玻璃管的两端,通过橡皮塞装上两只注射器,玻璃管内装几团细的铜丝,把一个注射器内的空气体积调到50mL的位置,另一只注射器不留空气加热玻璃管的铜丝部位。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
测定空气中氧气含量的常见的装置(全)欧阳家百(2021.03.07)江苏省特级教师赵美荣序号装置实验操作图1用凸透镜将太阳光聚焦到白磷,使白磷燃烧,一段时间后,白磷燃烧。
燃烧完毕,待冷却至室温,打开弹簧夹,烧杯中的水倒吸进入瓶内。
图2闭合电源开关,电阻丝发热,温度达到40 ℃时白磷燃烧,产生大量白烟。
装置冷却后,由于左侧中氧气被消耗,气体压强减小,水会在左侧中上升,且上升到1刻度处。
图3先关闭弹簧夹a,将螺旋状的铜丝在酒精灯的灼烧后迅速插入大试管,接触试管底部的过量的白磷,然后立即塞紧橡皮塞。
由于白磷的着火点低,白磷燃烧,产生大量的白烟。
燃烧完毕,待冷却至室温,打开弹簧夹,烧杯中的水倒吸进入瓶内。
图4用水浴加热的办法使白磷燃烧,足以使白磷着火燃烧。
燃烧完毕,待冷却至室温,打开弹簧夹,烧杯中的水倒吸进入瓶内。
图5在一封闭的试管内放一颗白磷,用酒精灯微微加热白磷,白磷燃烧,有大量白烟生成,注射器被推向外侧(右侧)。
待装置冷却,注射器逐渐向内侧(左侧)移动,根据注射器停止时的位置,确定空气中氧气的体积。
图6在一端封闭的粗玻璃管内放一颗白磷,用胶塞塞住,并推入到玻璃管中部,记下位置。
用酒精灯微微加热白磷,白磷燃烧,有大量白烟生成,胶塞被推向外侧(右侧)。
待装置冷却,胶塞逐渐向内侧(左侧)移动,根据胶塞停止时的位置,确定空气中氧气的体积。
图7用生石灰和水反应时放出的热量使白磷燃烧。
烧杯上方玻璃管(预先固定好)中部有一可左右滑动的活塞,活塞左端管内密封有空气,活塞右端的玻璃管口跟空气连通,实验开始前活塞处在刻度5 cm处。
图8在一个耐热活塞的底部放一小块(足量)白磷,然后迅速将活塞下压,使空气内能增大,温度达到40℃。
白磷燃烧,产生大量白烟,冷却至原来温度时,松开手,活塞最终将回到刻度4处。
图10在一玻璃管的两端,通过橡皮塞装上两只注射器,玻璃管内装几团细的铜丝,把一个注射器内的空气体积调到50mL的位置,另一只注射器不留空气加热玻璃管的铜丝部位。
待铜丝被灼热后,把注射管缓慢地以2~3次/分的速度左右推动。
大约3~4min之后停止加热。
待玻璃管冷却至室温后,注射器内空气减少。
图11在滴管中盛适量的氢氧化钠溶液。
将燃着的硫粉迅速插入集气瓶内,硫粉燃烧,发出淡蓝色的火焰。
燃烧完毕,待冷却至室温,打开弹簧夹,烧杯中的水倒吸进入瓶内。
探究空气中氧气的含量湖北省教研室组长杨国安亲爱的同学,很高兴与你见面了!老师要告诉你一个小秘密:在《我们周围的空气》单元里,“探究空气中氧气含量的实验”可重要啦!这不,近几年来在各省市中考试题中频繁出现。
本文中的例3就是我出的一道中考题。
遗憾的是,当年我市考生平均得分率只有41%!现在,你一定很想知道,怎样才能掌握这一考点?老师告诉你,掌握这一考点有秘决:一是你要深入理解实验原理;二是你要有流畅的解题思路,找到解题的突破口。
深入理解实验原理对于探究空气成分的实验,以下几点需要你认真研读,深入理解,这是你正确解答这类题目的基础。
【实验原理】利用物质在密闭容器里燃烧或与氧气反应生成固体物质,把容器里空气中的氧气耗尽,根据气体体积的减少量来确定氧气的含量。
【实验药品】能用来测定空气中氧气含量的物质必须是易与氧气反应且没有气体生成的物质,如红磷(或白磷)等。
不能用木炭、硫来代替红磷(或白磷)。
木炭、硫燃烧的产物是气体,且消耗的氧气的体积恰好等于生成的气体的体积,密闭体系内气体的压强几乎没有变化。
【实验装置】如图1所示(当然,也可用其他合理装置)。
【实验步骤】1.在集气瓶内加入少量水(用于溶解生成的五氧化二磷,同时吸收燃烧产生的热,有利于瓶内降温),把集气瓶剩余容积划分为5等分,并做上记号。
2.用止水夹夹紧乳胶管。
把燃烧匙内的红磷放在酒精灯火焰上点燃,立即伸入瓶中并把塞子塞紧。
观察红磷燃烧时的现象。
3.待红磷熄灭并冷却后,打开止水夹,观察实验现象及水面的变化情况。
【实验现象】红磷燃烧时发出黄白色火焰,同时放出热量,随着反应的进行,瓶内充满白烟。
待集气瓶冷却到室温时,打开止水夹,烧杯中的水被吸进集气瓶中,进水的体积恰好近似于集气瓶中原空气体积的1/5。
【注意事项】1.装置不能漏气。
2.红磷要过量,以保证瓶内的氧气耗完。
3.点燃红磷后要立即伸入集气瓶中,并塞紧塞子,不能使外界空气进入瓶内。
4.止水夹要夹紧,防止红磷燃烧时气体膨胀使瓶中气体从导管逸出。
5.等到集气瓶冷却到室温时再打开止水夹,防止瓶内气温高于外界气温,使进入瓶内的水减少领悟解题思路以上内容是你正确解题的基础。
接下来,需要你积极领悟解题思路,寻找解题突破口。
只有思路流畅,你才能在平时考试或中考中游刃有余。
总体思路:测定空气中氧气含量的方法有多种,但其原理只有一种,这就是利用足量的某物质与密闭容器里空气中的氧气充分反应,通过观察进水的体积或活塞移动的体积,来确定空气中氧气的含量。
例1 某同学设计了测定空气中氧气含量的实验,装置如图1所示。
回答下列问题:⑴红磷在集气瓶中燃烧的符号表达式为。
⑵待燃烧停止,白烟消失并冷却后,打开止水夹,观察到进入集气瓶中水的体积不到总容积的1/5,你认为其原因可能是、。
(填2点即可)⑶如将红磷换成炭粉,实验能否成功?(填“能”或“不能”)。
原因是。
思路分析测定空气中氧气含量的物质,是容易与氧气反应且没有气体生成的物质。
如红磷在密闭容器中燃烧,消耗了容器里的氧气,生成了五氧化二磷固体。
木炭燃烧的产物是二氧化碳气体,木炭消耗氧气的体积与生成的二氧化碳气体的体积相同,密闭体系内气体的压强变化很小。
测定的氧气的含量小于实际含量,或是装置有问题,或是操作有问题。
如装置漏气;红磷的量不足;止水夹未夹紧;装置未冷却到室温就开始读数等。
答案⑴红磷+氧气五氧化二磷⑵装置漏气红磷的量不足⑶不能炭粉虽然消耗了氧气,但燃烧生成的二氧化碳是气体,瓶内压强变化很小,水基本不能进入集气瓶中例2 某课外活动小组的同学,用图2所示的装置粗略测定空气中氧气的体积分数。
该装置的气密性良好,活塞可左右滑动,实验前活塞处在刻度10cm处。
已知白磷在空气中燃烧的最低温度为40 ℃。
回答下列问题:⑴可观察到玻璃管内开始发生的现象是:白磷着火燃烧,活塞先向移动(填“左”或“右”,下同),后向移动。
⑵实验结束,恢复到常温后,活塞应停在约(填整数)cm 处。
思路分析烧杯中的沸水使白磷的温度上升,当白磷的温度达到40 ℃时,白磷着火燃烧。
白磷燃烧时放出的热量使密闭容器中的气体受热膨胀,活塞右移;当膨胀的体积不及消耗的氧气的体积时,活塞左移。
由于空气中的氧气约占总体积的1/5,所以,待装置冷却至室温,活塞最后停在刻度约为8cm的位置上。
答案⑴右左⑵8例 3 某同学为测定空气里氧气的含量,设计了如图 3 所示的实验装置。
该同学在“金属梯”的每一步的凹处放置一颗用滤纸吸干水后的白磷,用放大镜会聚6V手电筒光于靠近水面的一步“金属梯”处的白磷上。
回答下列问题:⑴一段时间后,可观察到的现象是_________________。
⑵“金属梯”的每一步上都放置一小颗白磷与只靠近水面的一步“金属梯”处放一大颗白磷相比,优点是______________________。
思路分析放大镜会聚6V手电筒光,使金属梯最下端凹处的白磷的温度升高,白磷着火燃烧。
白磷燃烧放出的热量,使金属梯上各步凹处的白磷由下往上依次燃烧。
由于试管中的氧气逐渐减少,试管内气体的压强也逐渐减小,试管内的水位逐渐上升。
当氧气全部耗尽时,水面不再上升。
金属梯上各步凹处放置一颗小白磷,可增大白磷与氧气的接触面积,尽可能多地消耗试管里的氧气。
答案⑴白磷像“上楼梯”般依次燃烧,开始时冒白烟,燃烧快停止时在倒置试管的上部出现黄烟。
试管内的水位先下降,然后上升到一定位置后恒定不动⑵尽可能多地消耗试管内的氧气例 4 铁能在潮湿的空气中与氧气反应生成铁锈,一位同学应用上述反应原理测定空气中氧气的含量,他选用的仪器如图4所示。
回答下列问题:⑴试管和铁丝球应该如何放置?⑵实验中观察到什么现象?⑶实验要进行一周左右的时间,才能观察到明显的现象,你知道时间较长的原因吗?思路分析在密闭容器内,细铁丝与潮湿空气中的氧气反应生成铁锈,使容器内的氧气耗尽,容器内气体压强小于容器外的大气压,水进入容器。
铁生锈的速度很慢,为了将试管中的氧气全部耗尽,需要较长的时间。
答案⑴把细铁丝放在倒立着的试管里,将烧杯移至试管下方使试管口浸没在水中,并用烧杯中的水液封试管中的空气。
(如图5所示)⑵一段时间后,试管内液面上升,试管中铁丝生锈。
⑶铁生锈是一个缓慢氧化的过程,为了保证试管中的氧气能完全与铁丝反应,实验需要较长时间。
亲爱的同学,“测定空气中氧气的含量”的原理你已十分清楚了,解题思路也相当明晰了,如果在平时考试或中考中遇到了这样一类题目,我相信你已成竹在胸了!。
