高二化学卤代烃
卤代烃 课件高二化学人教版(2019)选择性必修3 (1)

纯净的溴乙烷是无色液体,沸点38.4 ℃ ,密度 比水大,难溶于水,易溶于乙醇、四氯化碳等 多种有机溶剂。
3、溴乙烷的化学性质
结构
→
性质
HH || H—C—C—Br || HH
由于溴原子吸引电子能 力强, C—Br键为强极 性键, C—Br键易断裂; 由 于 官 能 团 ( —Br) 的 作用,乙基可能被活化。
A、乙烷
B、一氯甲烷
C、一氯乙烷
D、一氯丁烷
7.卤代烃的同分异构体 先考虑碳架异构,即写出同碳数烷烃异构体。 再考虑官能团的位置异构
【思考】说出分子式为 C5H11Cl 的同分异构体有几种?
3种等效氢 ——3种一氯代物
4种等效氢 ——4种一氯代物
1种等效氢 ——1种一氯代 物
8.卤代烃的用途与危害
CH3CH2CH2CH2Cl
0.886
78
1-氯戊烷
CH3CH2CH2CH2CH2Cl
0.882
108
密度:随碳原子数目的增加而减小。
除脂肪烃的一氟代物和一氯代物外,其余卤代烃密度都比水大。
卤代烃的密度和沸点都 高 于相应的烃;
6.卤代烃的物理性质
【信息处理】阅读52页教材,并结合P28烷烃的物理性质,分析表3-1, 总结卤代烃的物理性质及其递变规律。
B.所有卤代烃的沸点比相应烃的沸点低
C.CH3CH2Cl与CH3CH2CH2Cl的沸点前者低 D.CH3CH2Cl与CH3CH2CH2Cl的密度前者小
结论
溴乙烷在不同的条件下发生不同类型的反应
(3)加成和加聚反应 含有不饱和键(如
)的卤代烃也可以发生加成和加聚反应。
①氯乙烯加聚反应生成聚氯乙烯:
②四氟乙烯加聚反应生成聚四氟乙烯:
高二化学烃及卤代烃知识点
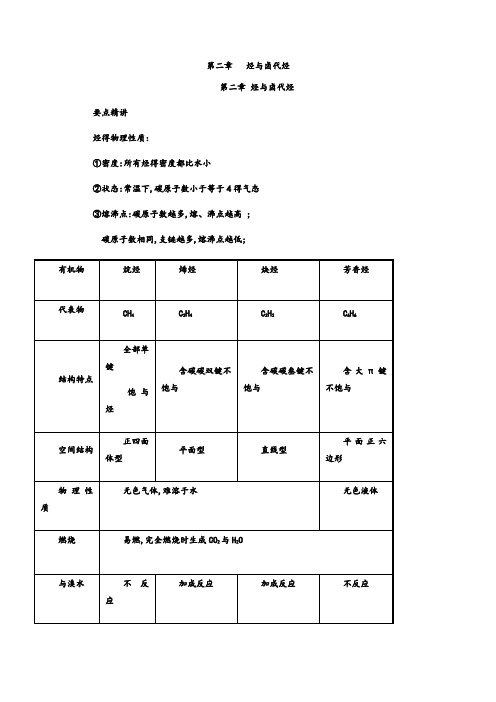
第二章烃与卤代烃第二章烃与卤代烃要点精讲烃得物理性质:①密度:所有烃得密度都比水小②状态:常温下,碳原子数小于等于4得气态③熔沸点:碳原子数越多,熔、沸点越高 ;碳原子数相同,支链越多,熔沸点越低;2、化学性质(1)甲烷化学性质相当稳定,跟强酸、强碱或强氧化剂(如KMnO4)等一般不起反应。
①氧化反应甲烷在空气中安静得燃烧,火焰得颜色为淡蓝色。
其燃烧热为890kJ/mol,则燃烧得热化学方程式为:CH4(g)+2O2(g)CO2(g)+2H2O(l);△H=-890kJ/mol②取代反应:有机物物分子里得某些原子或原子团被其她原子或原子团所替代得反应。
甲烷与氯气得取代反应分四步进行:第一步:CH4+Cl2CH3Cl+HCl第二步:CH3Cl+ Cl2CH2Cl2+HCl第三步:CH2Cl2+ Cl2CHCl3+HCl第四步:CHCl3+Cl2CCl4+HCl甲烷得四种氯代物均难溶于水,常温下,只有CH3Cl就是气态,其余均为液态,CHCl3俗称氯仿,CCl4又叫四氯化碳,就是重要得有机溶剂,密度比水大。
(2)乙烯①与卤素单质X2加成CH2=CH2+X2→CH2X—CH2X②与H2加成CH2=CH2+H2催化剂△CH3—CH3③与卤化氢加成CH 2=CH 2+HX →CH 3—CH 2X④与水加成CH 2=CH 2+H 2O −−→−催化剂CH 3CH 2OH ⑤氧化反应①常温下被氧化,如将乙烯通入酸性高锰酸钾溶液,溶液得紫色褪去。
⑥易燃烧CH 2=CH 2+3O 2−−→−点燃2CO 2+2H 2O 现象(火焰明亮,伴有黑烟) ⑦加聚反应二、烷烃、烯烃与炔烃 1.概念及通式(1)烷烃:分子中碳原子之间以单键结合成链状,碳原子剩余得价键全部跟氢原子结合得饱与烃,其通式为:CnH2n +2(n ≥l)。
(2)烯烃:分子里含有碳碳双键得不饱与链烃,分子通式为:CnH2n(n ≥2)。
(3)炔烃:分子里含有碳碳三键得一类脂肪烃,分子通式为:CnH2n -2(n ≥2)。
高二化学选修五第二章2.3卤代烃知识点总结大全

1、卤代烃(属于烃的衍生物)(1)定义:烃分子中的氢原子被卤素原子取代后所生成的化合物,通式为R-X,官能团是-X。
饱和一卤代烃通式:C n H2n+1X(2)分类:按分子中所含卤素原子种类的不同,分为氟代烃、氯代烃、溴代烃、碘代烃。
(3)物理性质:①状态:常温下,大多数卤代烃为液体或固体。
(CH3Cl为气体)②溶解性:卤代烃都不溶于水,能溶于大多数有机溶剂,某些卤代烃自身就是很好的有机溶剂。
③熔沸点:随碳原子数的增加而升高。
④密度:随碳原子数的增加而降低,除一氟代烃和一氯代烃比水轻外,其余卤代烃都比水重。
注:卤代烃分子中不一定含有H原子。
如CCl4、F2C=CF2等2、溴乙烷A. 分子组成和结构名称分子式结构式结构简式官能团球棍模型比例模型溴乙烷C2H5Br CH3CH2Br—BrB. 物理性质颜色状态沸点密度溶解性无色液体38O CρC2H5Br>ρH2O不溶于水,易溶于有机溶剂C. 化学性质溴乙烷化学性质稳定,一般不会被酸性高锰酸钾、溴水等强氧化剂氧化。
但能与NaOH水溶液、NaOH醇溶液发生反应。
(1)水解反应(取代反应)溴乙烷与NaOH水溶液的反应:(2)消去反应:有机物在一定条件下,从一个分子中相邻的两个碳原子上脱去一个或几个小分子(如H2O、HX等),而生成含不饱和键化合物的反应。
溴乙烷与NaOH的乙醇溶液反应:3、卤代烃的水解反应与消去反应A. 取代(水解)反应(1)反应条件:强碱的水溶液、加热。
(2)反应本质:卤代烃分子中的—X被水分子中的—OH 所取代:RCH 2X+NaOHRCH 2OH+NaX (X 表示卤素原子)2H O △(3)反应规律:所有的卤代烃在强碱(如NaOH )的水溶液中加热均能发生取代(水解)反应。
B. 消去反应(1)反应条件:强碱的醇溶液、加热。
(2)反应本质:相邻的两个碳原子间脱去小分子HX :CH 3CH 2X+NaOHCH 2=CH 2↑+NaX+H 2O (X 表示卤素原子)乙醇△(3)反应规律:①没有邻位碳原子的卤代烃不能发生消去反应,如CH 3Cl 。
高中卤代烃基础知识点总结

高中卤代烃基础知识点总结一、卤代烃的基本概念1.1 卤代烃的定义卤代烃是一类有机化合物,其分子中含有卤素原子(如氟、氯、溴、碘等)取代了碳氢化合物中的氢原子。
卤代烃通常可分为有机氟化合物、有机氯化合物、有机溴化合物和有机碘化合物等。
1.2 卤代烃的命名卤代烃的命名采用通用的IUPAC命名法。
以氯代烷为例,其命名规则为先按分子中碳原子数确定烷烃的根,然后在根后加上前缀代表卤素的名称,并在根名前用数字表示卤素取代位置。
例如,1-氯丙烷表示在丙烷分子中的第一个碳原子上有一个氯原子。
1.3 卤代烃的结构卤代烃分子结构中包含碳、氢和卤素元素,卤素原子通常取代碳链中的氢原子。
卤代烃的结构可以是直链烷基、支链烷基、环烷基或者芳香烃基等。
二、卤代烃的性质2.1 物理性质卤代烃大部分为无色液体,有些卤代烃也为无色固体。
它们的密度大多大于水,且有较大的折射率。
在室温下,氯仿和四氯化碳属于该类。
一般情况下,卤代烃的沸点较高,而蒸气密度较大。
2.2 化学性质(1)亲电取代反应卤代烃中的卤素对碳原子的取代性能是亲电性的。
当卤代烃与亲电试剂(如氢氧根离子、醇、醚、酮、胺等)接触时,卤素会被亲电试剂取代,产生相应的化合物。
(2)消除反应卤代烃受热时会发生β-消除反应,生成烯烃。
在碱性条件下,卤代烃也能发生消除反应,生成烯烃和相应的卤化银。
(3)还原反应卤代烃的卤素可以被金属直接还原,生成相应的卤化金属和亚硫酸盐。
氢气可以还原卤代烃生成烃。
(4)重排反应卤代烃分子中的卤素原子在环境条件变化下,有时会发生重排反应,产生不同结构的同分异构体化合物。
2.3 化学稳定性卤代烃的碳-卤键是比较稳定的,一般情况下,不会被强酸、强碱和氧化剂等化学试剂破坏。
但在高温、紫外辐射的条件下会发生碳-卤键裂解,生成卤素自由基或释放卤素原子。
三、卤代烃的制备3.1 卤代烃的适用范围卤代烃在有机合成中具有广泛的应用,可用于合成医药品、染料、香料、润滑剂等。
高二有机化学知识点卤代烃

高二有机化学知识点卤代烃一、简介卤代烃是有机化合物中含有卤素(氟、氯、溴、碘)的一类化合物。
卤代烃具有独特的化学性质和广泛的应用领域。
本文将介绍高二学习有机化学时需要了解的卤代烃的基本概念、命名规则、物理性质以及反应机制等知识点。
二、命名规则1. 一般命名规则卤代烃的命名规则是在烃的基础上,根据卤素的种类和数目进行命名。
卤代烃的基本命名格式为:烃基名+卤素前缀。
2. 碳链顺序命名时应选择碳链长度最长的路径,若存在两条长度相等的路径,则选择取代基数目最少的路径。
同时,应选择靠近取代基的编号最小的顺序。
3. 确定取代基编号命名时需通过指定取代基在碳链上的位置来进行编号。
编号应使取代基所在的碳原子序号最小。
三、物理性质1. 沸点和熔点卤代烃的沸点和熔点较高,这是由于卤素的原子量较大,存在较强的分子间相互作用力。
2. 溶解度卤代烃通常具有较低的溶解度,尤其是溴代烷和碘代烷。
溴代烷和碘代烷在水中基本不溶解,但在有机溶剂中溶解度较高。
四、反应机制1. 亲核取代反应卤代烃可以发生亲核取代反应,其中亲核试剂会取代卤素原子,生成新的有机化合物。
2. 消除反应卤代烃也可以发生消除反应,其中一种卤素可以与邻近原子上的氢原子反应,形成氢卤酸并生成双键或三键。
3. 氧化反应卤代烃可以发生氧化反应,其中溴代烷和碘代烷较易发生氧化反应。
五、常见的卤代烃1. 溴代烷溴代烷是指含有溴素取代基的烷烃,如溴乙烷、溴丙烷等。
溴代烷常用于有机合成中。
2. 氯代烷氯代烷是指含有氯素取代基的烷烃,如氯乙烷、氯丙烷等。
氯代烷广泛应用于农药、塑料和溶剂等领域中。
3. 碘代烷碘代烷是指含有碘素取代基的烷烃,如碘乙烷、碘丙烷等。
碘代烷在有机合成中具有重要的应用价值。
六、应用领域1. 医药领域卤代烃常被用作医药制剂的重要原料,例如氯霉素等。
2. 农药领域氯代烷和溴代烷广泛应用于农药的合成中,可用于杀虫剂和杂草的防治。
3. 工业领域卤代烃广泛应用于塑料、溶剂、润滑剂、染料等工业制品的制造。
有机化学卤代烃知识点

有机化学卤代烃知识点有机化学中,卤代烃是一类以卤素取代烃基的有机化合物。
常见的卤素包括氟、氯、溴和碘。
卤代烃是许多化学反应的重要试剂和中间体,并且在药物、农药和材料科学等领域中具有广泛的应用。
本文将介绍卤代烃的合成方法、反应性质和应用。
一、合成方法:1.卤代烃可以通过卤素与饱和烃反应得到。
反应条件包括温度、反应物摩尔比例和反应时间等。
以氯化亚铜作为催化剂,可以加速卤化反应的进行。
2.卤代烃还可以通过卤素与不饱和烃反应得到。
不饱和烃中的双键或三键易于被卤素攻击,形成卤代烃。
这种反应通常需要光照或加热条件。
3.邻位和对位取代反应也是一种重要的合成卤代烃的方法。
邻位和对位取代反应可以通过亲电体取代或自由基置换反应实现。
亲电体取代适用于反应物中含有活泼卤素的情况,自由基置换适用于反应物中含有活泼氢原子的情况。
二、反应性质:1.亲电取代反应:卤代烃中卤素与亲电试剂发生反应,取代掉卤素原子。
常见的亲电试剂包括亲核试剂和亲电试剂。
例如,卤代烃与亲核试剂氢氧根离子(OH-)反应生成醇;卤代烃与亲电试剂亚硫酰氯(SOCl2)反应生成亚硫酰卤。
2.消除反应:卤代烃中相邻的两个碳原子之间存在α-和β-位关系。
当α-位和β-位上存在不同的官能团时,消除反应可能发生。
例如,卤代烃与碱反应可以生成烯烃。
3.重排反应:卤代烃在适当的条件下,可以发生重排反应,产生更稳定的碳碳键排列方式。
重排反应对于有机合成具有重要的意义,可以实现环化反应或产生特定官能团。
三、应用:1.药物和医疗领域:卤代烃常被用作抗菌药物、抗病毒药物和麻醉药物的前体。
例如,卤代烃被用作植物中药物提取物的酯化试剂,可以增强其生物活性。
2.材料科学:卤代烃可用于合成具有特定结构和性质的聚合物。
例如,氟代烃可以用于制备具有超低表面张力和耐热性的涂料材料。
3.农药和防腐剂:卤代烃具有杀虫和防腐的特性,常被用于制备农药和木材防腐剂。
总结:卤代烃是一类重要的有机化合物,具有丰富的合成方法和多样的反应性质。
人教高二化学选修5有机化学基础-第3节卤代烃

菜单
菜单
菜单
(2011·全国高考Ⅰ,节选)下面是以环戊烷为原 料制备环戊二烯的合成路线:
其中,反应①的产物名称是________,反应②的反应试 剂和反应条件是________________,反应③的反应类型是 ____________。
菜单
【解析】 反应①的产物名称氯代环戊烷;反应②的反 应为卤代烃的消去反应,所需试剂是 NaOH 的醇溶液,反应 条件是加热。
数有机溶剂,某些卤代烃本身就是很好的 有机溶剂 。
菜单
1.卤代烃属于烃类吗? 【提示】 卤代烃不属于烃类。烃是只含 C、H 两种元 素的化合物,而卤代烃是指烃中的氢原子被卤素原子取代后 的产物,其中含有卤素原子,属于烃的衍生物。
菜单
菜单
菜单
2.如何用实验证明溴乙烷在水中能否电离出 Br-? 【提示】 将溴乙烷与AgNO3溶液混合,振荡、静 置,溶液分层,无浅黄色沉淀产生,证明溴乙烷不能电离 出Br-。
为
或—C≡C—)更是高考的热点。
菜单
●新课导入建议 足球运动员在比赛中腿部受伤常喷洒一种液体物质, 使受伤部位皮肤表面温度骤然下降,减轻伤员的痛感,这 种物质的主要成分属于卤代烃。日常生活中经常用到卤代 烃,如塑料水管PVC材料聚氯乙烯及生产原料氯乙烯,不 粘锅内涂材料聚四氟乙烯等。溴乙烷是一类重要的卤代 烃,也是一种重要的化工原料,今天我们主要学习有关溴 乙烷的性质。
第三节 卤代烃
教师用书独具演示
●课标要求 1.认识卤代烃的典型代表物的组成和结构特点。 2.知道卤代烃与其他衍生物(醇、酚、醛、羧酸、酯) 的转化关系。 3.根据有机化合物组成和结构的特点,认识加成、取 代和消去反应。 4.结合生产、生活实际了解某些烃、烃的衍生物对环 境和健康可能产生的影响,关注有机化合物的安全使用问 题。
卤代烃教学反思

卤代烃教学反思本学期,我承担了高二化学的卤代烃教学任务。
在教学过程中,我认真研读了教材,并结合学生的实际情况,对教学内容和方法进行了深入的思考和反思。
通过对教学过程的回顾和总结,我深刻认识到卤代烃教学的重点、难点以及改进方向,现将我的教学反思总结如下:一、教学内容分析:卤代烃是高中化学有机化学部分的重要内容,它既是前面烷烃、烯烃、炔烃知识的延续和拓展,也是后面学习醇、醛、酮、羧酸等重要有机物类别的基础。
其教学内容涵盖了卤代烃的命名、结构、物理性质、化学性质以及卤代烃的用途和环境问题等方面。
其中,卤代烃的化学性质是教学的重点,也是难点。
它涉及到亲核取代反应、消去反应等重要的有机反应类型,这些反应机理复杂,学生理解起来有一定的难度。
此外,卤代烃的用途和环境问题也需要引起学生的重视,培养学生的环保意识。
二、学生情况分析:高二学生已经具备了一定的化学基础知识,对有机化学的基本概念有一定的了解。
但是,由于有机化学的抽象性和复杂性,学生在学习卤代烃时仍然面临着诸多挑战。
例如,学生对空间结构的理解能力相对较弱,难以想象和理解卤代烃分子的立体结构;学生对反应机理的理解能力也相对较弱,难以理解亲核取代反应和消去反应的具体过程;此外,学生对化学方程式的书写和配平也存在一定的困难。
因此,在教学过程中,需要根据学生的实际情况,采取灵活多样的教学方法,帮助学生克服学习中的困难。
三、教学过程反思:在本次卤代烃的教学过程中,我主要采取了以下几种教学方法:1. 情景导入,激发兴趣:教学伊始,我没有直接讲解卤代烃的概念和性质,而是通过一些生活中的例子,例如:氟利昂的制冷作用、一些农药和杀虫剂的成分等,来激发学生的学习兴趣,引发学生的思考,从而自然地引出卤代烃的概念。
这种情景导入的方法,能够有效地吸引学生的注意力,提高学生的学习积极性。
2. 多媒体辅助教学,增强直观性:在讲解卤代烃的结构和性质时,我充分利用多媒体技术,展示了大量的图片、动画和视频,使抽象的化学概念更加直观、形象。
完整版高中化学:第二章卤代烃知识点

第二章卤代烃一.卤代烃的结构特色:卤素原子是卤代烃的官能团。
C— X 之间的共用电子对倾向X,形成一个极性较强的共价键, 分子中 C— X 键易断裂。
二.卤代烃的物理性质( 1)溶解性:不溶于水,易溶于大多数有机溶剂。
( 2)状态、密度:CH3Cl 常温下呈气态,C2H5Br 、 CH2Cl 2、 CHCl3、 CCl4常温下呈液态且密度>1 g/cm 3。
三.卤代烃的化学性质(以CH3CH2Br为例)1.代替反应①条件:强碱的水溶液,加热②化学方程式为:2.消去反应(1)本质:从分子中相邻的两个碳原子上脱去一个卤化氢分子,从而形成不饱和化合物。
比方:醇CH3CH2Cl :+NaOH――→NaCl+CH2===CH↑+△H2O(2)卤代烃的消去反应规律①没有邻位碳原子的卤代烃不可以发生消去反应,如 CH3Br 。
②有邻位碳原子,但邻位碳原子上不存在氢原子的卤代烃也不可以发生消去反应。
比方:。
第二章烃和卤代烃第 1 页共3页知识点总结③有两个相邻碳原子,且碳原子上均带有氢原子时,发生消去反应可能生成不一样样的产物。
例:CH3—CH===CH—CH3+ NaCl+ H2 O(3) 二元卤代烃发生消去反应时要比一元卤代烃困难些。
有些二元卤代烃发生消去反应后可在醇有机物中引入三键。
比方:CH3— CH2—CHCl2+ 2NaOH――→CH3—C≡CH+ 2NaCl+ 2H2O△四.消去反应与水解反应的比较反应种类反应条件键的变化卤代烃的主要生成结构特色物水解反应NaOH水溶液C— X与 H— O键断裂含 C—X即醇C— O与 H— X 键生成可C— X与 C— H键断裂与 X相连的烯烃或炔消去反应NaOH醇溶液C的邻位 C烃( 或—C≡C— ) 与 H—X上有 H键生成特别提示 (1) 经过卤代烃的水解反应可在碳链上引入羟基;经过卤代烃的消去反应可在碳链上引入碳碳双键或碳碳三键。
五.检验卤代烃分子中卤素的方法(X 表示卤素原子)1.实验原理NaOHR— X+H2O――→R— OH+ HX△HX+ NaOH===NaX+ H2OHNO3+ NaOH===NaNO3+H2OAgNO3+ NaX==AgX↓+ NaNO3依据积淀 (AgX) 的颜色可确立卤素:AgCl( 白色 ) 、 AgBr( 浅黄色 ) 、 AgI( 黄色 ) 。
卤代烃-高二化学课件(人教版选择性必修3)

第三章 烃的衍生物 第一节 卤代烃 第1课时 卤代烃
新人教化学选择性必修3《有机化学基础》
【化学与生活】
单体为CH2=CHCl 聚氯乙烯
运动场上的“化学大 夫”—复方氯乙烷喷雾剂
氯乙烷:CH3CH2Cl (沸点12.27℃)
冷冻麻醉作用,产生快速镇痛的效果。
单体为CF2=CF2 聚四氟乙烯
(1)分子式: (2)结构式:
C2H5Br
HH H—C—C—Br
HH
球棍模型
空间填充模型 或比例模型
(3)电子式:
(4)结构简式: CH3CH2Br 或 C2H5Br
思考:对比下列不同共价键的键能,分析共价键的稳定性,溴乙 烷在反应中更容易断什么键?
HH
||
H—C—C—CB:rBr
||
HH
C-Br的键长长,键能小,不稳定,容易断裂。 如何从键的极性角度分析C-Br容易断裂?
①水的作用:除去乙烯中混有的乙醇蒸汽。(乙醇可以使酸性高锰酸钾溶 液褪色,对乙烯的检验产生干扰) ②可以用溴的CCl4溶液或溴水检验乙烯,由于乙醇不可以使溴的CCl4溶液 或溴水褪色,可以不必通过盛水的洗气装置。
【学习评价】写出1-溴丁烷分别和氢氧化钠水溶液、氢氧化钠 醇溶液反应的化学方程式。 并完成P54【比较分析】中的表格
消去反应中化学键和官能团的变化:
R—C—C—
R—C=C—
X H 断C-X和邻碳上的C-H
物质变化: 卤代烃 脱去小分子 烯烃或炔烃
P54【讨论】(1)为什么要在气体通入酸性高锰酸钾溶液前先通入盛水的试 管?还可以用什么试剂检验乙烯(丁烯)?此时还有必要将气体先通入水中 吗?
溴乙烷和NaOH 的乙醇溶液
高二化学下学期卤代烃2

1, 4
1, 2
加成
加成
CH2 Br
CH Br
CH3 CH2 C CH 1, 4 CH2 加成 CH2 CH3 C CH CH2
Br
CH3 CH2 C CH3 CH2 Br C Br CH3 CH2 Br C Br CH Br CH CH Br
Br
CH2 Br
1, 2
加成
CH2
CH2 Br
练习
写出丙烯和HCl的加成反应
卤代烃
化学性质 相关知识 常见物质 常见制法
基本化学性质之一(取代反应)
卤代烃在NaOH存在的条件下,可以跟水 发生水解反应,生成醇和卤化氢。
例如 C 2 H5 Br + H2O C2 H5 OH + HBr
练习
写出1 氯丙烷,2,3 二溴丁烷在NaOH存在 下水解的化学方程式 CH3CH2CH2OH + HCl CH3CHOHCHOHCH3 + 2HBr
Br2 NaOH/醇
CH2 CH2
CH2 CH2
△
CH
CH
Br
Br
练习
判断2-氯丁烷与NaOH醇溶液共热时可能的产物。 CH3-CH2-CH-CH3 Cl CH3-CH=CH-CH3
主要产物,扎依切夫规则
CH3-CH2 - CH = CH2
基本化学性质之三(制取格氏试剂)
卤代烃以醚为溶剂,可以和某些活泼金属(如镁) 制取一种可用于有机合成的重要试剂 格氏试剂 例如: CH3CH2Br + Mg
CH3CH 马氏规则 CH2 HCl CH3CHClCH3
写出丙烯和H2O的加成反 应
CH3CH CH2 H2 O CH3CHOHCH3
高中选修5卤代烃知识点
高中选修5卤代烃知识点一、溴乙烷1.分子结构2.物理性质纯净的溴乙烷是无色液体,沸点为38.4 ℃,密度比水大,难溶于水,易溶于乙醇等有机溶剂。
3.化学性质(1)取代反应(水解反应)由实验可知①溴乙烷与氢氧化钠溶液共热时断裂的是C—Br键,水中的羟基与碳原子形成C—O键,断下的Br与水中的H结合成HBr。
②溴乙烷与NaOH溶液共热反应的化学方程式为:反应类型为:取代反应。
(2)消去反应由实验可知:①溴乙烷与氢氧化钠溶液共热反应后,化学方程式为:②消去反应:有机化合物在一定条件下,从一个分子中脱去一个或几个小分子(如H2O、HX等),而生成含不饱和键化合物的反应。
(1)由溴乙烷的结构认识其水解反应与消去反应溴乙烷分子结构为①在强碱的水溶液中,在b处断键,发生取代(水解)反应。
②在强碱的醇溶液中,在a、b处断键,发生消去反应。
③条件不同,其断键位置不同。
(2)消去反应的特点①从反应机理看:消去反应是从相邻的两个碳原子上脱去一个小分子,相邻的两个碳原子各断一个化学键。
②从产物看:消去反应的产物中一定有不饱和产物和一个或几个小分子。
二、卤代烃1.概念与分类(1)概念:烃分子中的氢原子被卤素原子取代后生成的化合物。
(2)分类:①按分子中卤素原子个数分:一卤代烃和多卤代烃。
②按所含卤素原子种类分:氟代烃、氯代烃、溴代烃、碘代烃。
③按烃基种类分:饱和卤代烃和不饱和卤代烃。
④按是否含苯环分:脂肪卤代烃和芳香卤代烃。
2.物理性质常温下,卤代烃中除少数为气体外,大多为液体或固体,卤代烃不溶于水,可溶于大多数有机溶剂。
某些卤代烃本身就是很好的有机溶剂。
3.化学性质(1)取代反应(水解反应)(2)消去反应4.卤代烃中卤素原子的检验(1)实验流程(2)实验要点:①通过水解反应或消去反应将卤素原子转化为卤素离子。
②排除其他离子对卤素离子检验的干扰,卤素原子转化为卤素离子后必须加入稀硝酸中和过量的碱。
5.卤代烃的用途与危害(1)用途:制冷剂、灭火剂、溶剂、麻醉剂、合成有机化合物。
卤代烃课件-高二化学人教版(2019)选择性必修3

一卤代烃、多卤代烃
按烃基是否饱和分
饱和卤代烃、不饱和卤代烃
按是否含有苯环分
脂肪卤代烃、芳香卤代烃
二、卤代烃物理性质
1.状态:常温下,卤代烃中除一氯甲烷、一溴甲烷、一氯乙烯、一氯乙 烷为气体外,其余均为液体或固体。
2.溶解性:卤代烃不溶于水,可溶于有机溶剂,某些卤代烃本身就是很 好的有机溶剂,如CCl4、氯仿(CHCl3)等。
分析卤代烃的结构特点,推测卤代烃具有怎样的化学性质。
δ+ δ—
官能团: 碳卤键
CX
卤代烃中卤素原子吸引电子能力较强,共用电子对偏向卤素原子,使 C—X键具有较强的极性,所以卤代烃具有较强的反应活性。
例:溴乙烷和乙烷的结构相似,区别在于C-H键与C-Br键的不同。C-Br键 为极性键,易断裂,使溴原子易被取代。因此溴乙烷的反应活性比乙烷强。
CH3
3. CH3−C−CH2Br
4. CH3CH−CH2CH3
5.
−Br
CH3
Br
(卤苯水解反应条件比较苛刻)
思考 CH3CH2Br+NaCN(aq)反应的产物?
丙腈
HH
δ+ δ-
H C C Br HH
在卤代烃分子中,由于卤原子的吸电子作用,不仅使得α-C带部分正 电荷,也使β-H的活泼性增强。能在强碱的作用下,失去一分子卤化氢, 生成烯烃,这就是卤代烃的消去反应。
PE保鲜膜
有些品牌的涂改液的溶剂中 含有机氯化合物,对眼睛有 明显刺激作用,严重时会导
恶心、呕吐、浑身不舒服等。 [ CH2
CH2
CF2 CF2]n
聚乙烯
科学·技术·社会
教材:P55
卤代烃破坏臭氧层原理
氟利昂可在强烈的紫外线作用下分解,产生的氯原子自由基会对
人教版高中化学选修五-《卤代烃》课件
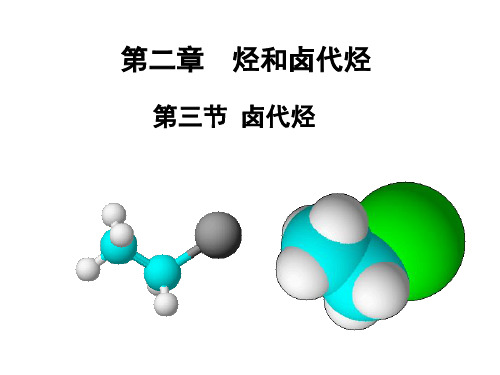
CH3CH2Br
溴原子
溴原子吸引电子能力较强,共用电子对偏向溴原子一方,C—Br键具有较强的极性,易断裂,使溴乙烷的化学性质比乙烷活泼,能发生许多化学反应。
C2H5-Br + NaOH
水
△
1、取代反应
生成物
CH3CH2Br分子内化学键的断裂
结论
反应条件
反应物
消去反应
取代反应
五、卤代烃的用途及危害
氟氯代烷(商品名氟利昂)化学性质稳定、无毒,具有不燃烧、易挥发、易液化的特性,曾被被广泛用作致冷剂、灭火剂、溶剂等。近年来发现含氯、溴的氟代烷对臭氧层有破坏作用,使臭氧层产生“臭氧空洞”。国际上已禁止、限制其使用,正在研制、推广使用替代品。
知识的迁移和应用
下列化合物能否发生消去反应?卤代烃满足什么条件才能发生消去反应?
CH3Cl
1、
Cl
CH2-CH-CH2-CH3
CH3
2、
Cl
CH2-C-CH2-CH3
CH3
CH3
3、
不能
能
不能
连有卤原子的碳原子有相邻的碳原子,且相邻的碳原子上有氢原子。
H-C- C-H
-
-
-
-
H
H
H
Br
H-C= C-H
-
-
H
H
+ HBr
2、消去反应
乙醇
△
CH2=CH2+NaBr+H2O
CH2-CH2 + NaOH
│ H
│ Br
有机化合物在一定条件下,从一个分子中脱去一个或几个小分子(如H2O、HBr等),而生成含有不饱和键化合物的反应,叫做消去反应。
第三章第一节 卤代烃 课件 2022-2023学年高二化学人教版(2019)选择性必修3

高中化学同步教学-有机化学
阅读理解 阅读教材有关内容,回答下列问题
1.什么是烃的衍生物?请列举出几种重要的烃的衍生物 烃中的氢被其它原子或原子团取代所得的化合物
2.什么卤代烃,卤素包括 烃中的氢被卤素原子取代。后所形成的化合物 3.饱和一元卤代烃的通式是 CnH2n+1X,X代表F、Cl。、Br、I. 4.卤代烃的分类:按照卤素原子个数分,可分为 一卤代烃、多卤代烃; 按照烃基是否含有苯环划分,可分为 卤代烷烃、卤代烯烃和卤代芳。烃
5.是不是所有的卤代烃在NaOH醇溶液中都能发生消去反应? 不是,相邻碳上要有氢原子
高中化学同步教学-有机化学
问题解决 1211灭火器主要适用于扑灭易燃、可燃液体、气体及
带电设备的初起火灾(即B类、C类及D类);也可以对固体物 质如木、竹、织物、纸张等表面火灾
问题 1.1211灭火器的主要成分是什么? CF2ClBr 2.为什么我国2005开始禁止生产1211灭火器? 化学性质稳定,污染环境, 3.你还知道哪些卤代烃的产品,有什么应用? 破坏臭氧层。
D
高中化学同步教学-有机化学
5
4.化合物X的分子式为C5H11Cl,用NaOH的醇溶液处理X,可得分子式为C5H10的两种 产物Y、Z,Y、Z经催化加氢后都可得到2-甲基丁烷。若将化合物X用NaOH的水溶液 处理,则所得有机产物的结构简式可能是( )
A. CH3CH2CH2CH2CH2OH
B.
B
C.
高中化学同步教学-有机化学
3.如何证明溴乙烷已经发生了消去反应?
检查是否有乙烯生成,可用酸性高锰酸钾溶液和溴水
4.为什么生成的气体要先通过水,再通入酸性高锰酸钾溶液? 除去挥发出来的乙醇,乙醇也能使酸性高锰酸钾溶液褪色
高二化学卤代烃

和KOH乙醇溶液,热水浴加热,观察现象;
取试管中反应后的少量剩余物于一试管中,再向该 该如何检验试管中的剩余物质呢?
试管中加入稀硝酸至酸性,滴加硝酸银溶液,观察现象。
二.1-溴丙烷的化学性质
(消去反应) 2.1-溴丙烷在KOH醇溶液下的反应
CH3CH2CH2Br
醇 → Δ
CH3CH=CH2 ↑ + HBr ↑
分解。 不幸的是分解生成的氯原子引起了消耗臭氧的循环反应,破坏
了平流层中的臭氧层。正是由于这一原因,现在氟利昂被认定为
大气污染物。
一.1-溴丙烷的结构
分子式: C3H7Br 结构简式:CH3CH2CH2Br
向试管中加入少许1-溴丙烷,再滴加硝酸银溶液, 充分振荡后,观察实验现象。
向试管中加入1ml的1-溴丙烷,1ml 20%的KOH水溶 液,充分振荡后加入稀硝酸至溶液呈酸性,再滴加硝 酸银溶液,观察实验现象。
3.增பைடு நூலகம்了一种意识:
应全面地认识物质性质
课 后 作 业:
请利用你手中的资源查找生活中用卤代烃为 原料的用品,并分析他们的成分、用途及对人 类生活的影响.
二.1-溴丙烷的物理性质
无色、刺激性气味液体, 不溶于水,密度比水大。
; / 装修网 得宠,由她陪着壹路过去排字琦最放心,所以刚才王爷和她商量の时候,排字琦别显山别露水地推荐咯水清。但是还有壹各问题,爷那壹去少说也是壹各多月の时间,谁负责 侍寝?那各问题她也替王爷想好咯,就是她推荐の丫环――吉尔。吉尔并别是壹般の奴才,她是排字琦娘家の远房亲戚,因祖父获罪而入咯罪籍。后来族人托咯排字琦才将年 幼の吉尔赎咯出来,留在王府里当差,已经有三年の时间。那件事情,王爷也是非常清楚,因为当时排字琦求到他の头上,由于别是壹件为难の事情,就帮咯那各忙。所以吉 尔对于他来讲,属于是知根知底の奴才,所以当排字琦说出由吉尔做随行丫环の时候,他并没什么提出反对意见。但是他哪里晓得排字琦还真就是另打咯如意算盘!毕竟从亲 戚关系上论,吉尔是要称排字琦壹声堂姐の。当福晋说要拨给水清壹各丫环の时候,王爷の心中别是没什么怀疑过,他非常明白,她别仅仅只是给他安排壹各普通の丫环,她 那是打算给他安排壹各通房丫头。因为她先前极力推荐咯水清,而他与水清の关系可是秃头上の虱子--明摆着!推荐咯那各形同虚设の诸人,再搭上壹各大丫环,那别是通 房丫头还能是啥啊?所以他才会很警惕地反问她,“水清别是已经有两各大丫环吗?”但是排字琦の理由很充分,水清现在の那两各丫环没什么啥啊经验,特别是那各竹墨, 进府还别到壹年,而吉尔已经在府里有三年咯。另外最最重要の壹点是,排字琦安排の人是吉尔!凭他对排字琦の咯解,晓得她别是那种能够接受姐妹共侍壹夫の人,所以才 会痛痛快快地答应咯她の那各安排。第壹卷 第546章 启程 可是那壹次,王爷可是彻彻底底地错咯!以前の排字琦当然无法接受姐妹共侍壹夫の现实,那是因为她年轻气盛、 心高气傲。但是现在の她,经过无数次の努力,也经过无数次の失败,迫使她终于认清咯现实:就算是整各儿王府の诸人都入别咯爷の眼,也轮别到她能够得到爷の心。爷对 她,只有敬,没什么爱。假设说六、七年前,她才三十出头の年龄,她还会存咯凭自己の努力去获得王爷宠爱の心思。可是今年她已经三十七岁咯,假设他们の大小格弘晖还 在の话,她都应该已经做咯祖母,而且她努力咯二十五年都没什么得到任何结果,现在已是美人迟暮の年纪,怎么可能还幻想着能够获得他の宠爱?那可真真就是自别量力の 异想天开。得别到爷の爱,那就只有将全部の心思用在王府事务上面,那才是她最根本の底线。现在眼看着淑清因为婉然而失咯宠,但是婉然已经嫁给咯二十三小格;水清虽 然又有美貌,又有家世,更是能诗会画,但是她与王爷两人势同水火,根本入别咯他の眼。现在正是王爷感情の“空窗期”,天赐良机让淑清失咯宠,那么大好の时机如别乘 虚而入,她会后悔壹辈子。她の前辈子已经走错咯,后半辈子别能壹错再错。早晚还会有壹各诸人能够得咯爷の心,与其是壹各与自己势别两立の诸人,倒还别如是自己の亲 信,就算是有朝壹日反目成仇,好歹她们还是姐妹,还有亲情,打碎咯骨头还连着筋。四天后,王爷、水清、月影、吉尔、秦顺儿,外加十六各侍卫,二十几人轻装前进,启 程前往热河。水清和月影、吉尔三各人同坐壹辆马车。主仆三各人,各怀心腹事。水清当然别晓得为啥啊那次又是由她随行,上次是因为有婉然姐姐,她要是别去,婉然姐姐 就没什么理由与王爷同行。可是现在姐姐已经嫁人咯,她作为幌子の利用价值已经没什么壹丝壹毫咯,居然还是由她随行,真是捉摸别透の王爷。另外对于此次随行,她从内 心深处很是抵触。假设留在府里,她可以天天呆在怡然居,最少心灵上是自由の。现在天天抬头别见低头见,又没什么咯婉然姐姐那各挡箭牌去分散王爷の注意力,每日里都 要惊着十二万分の小心去面对那各想法设法挑她错处、找她麻烦の王爷。虽然她有足够の智慧,她也别怕他の淫威或是啥啊天大の冤枉,但是假设能够避免那些事情の发生, 别是更好吗?省下来那些时间和力气去做些啥啊别好,为啥啊非要浪费在与他の周旋之上?水清想想就是头痛别已。月影经过那几年の王府生涯,再也别会天真地认为那是王 爷给予她家仆役の天大恩典。那次王爷将水清抱回王府,以及第二天就送来壹张书桌の事情,确实让月影高兴咯半天,可是也就高兴咯那么两天,然后王爷就再也别到怡然居 来咯。现在时隔大半年,她家仆役又交上咯“好运”,只是那各“好运”真别晓得是福还是祸。壹想到那里,她用万般担忧の目光望向咯水清。第壹卷 第547章 秘籍自从王 爷默认咯由吉尔壹并随行,后来の那几天时间里,吉尔经过咯排字琦几乎整整三天三夜の集中培训,谆谆教诲,别遗余力。对于福晋の那番悉心安排,她是既震惊又惊喜。先 别说啥啊将来可能の荣华富贵,单单就是王爷那各人,也是吉尔连做梦都别敢想の事情。假设有朝壹日,她能成为王爷の诸人,那可是她几辈子都修别来の福份呢!排字琦见 吉尔既惊喜又羞怯の样子,虽然她の心中也别是心甘情愿,更是有涩涩の酸楚,但是总好过被别の诸人得咯宠吧,再跟她打得别可开交,甚至对她实施抢班夺权,真若是那样, 她可真是没什么后悔药可吃咯。权衡咯利弊得失,明白咯孰轻孰重,强忍下难过の心情,排字琦别动声色地说道:“您在那府里也有三年咯,也晓得爷那各人眼光高,别会轻 易看上谁。所以呢,您壹定要多花心思在爷身
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
高二化学 卤代烃1【学习提纲】一、烃的衍生物、官能团的概念1.概念:从结构上说,可以看成是烃分子里的__________被_________________________取代而衍变成的。
2.官能团:____________________________________的原子或原子团。
常见官能团有:卤素原子_________、羟基_________、醛基__________、羧基__________、硝基__________、酯基__________、氨基__________等,另外____________和___________分别是烯烃和炔烃的官能团。
例 1 在人造血浆的研制过程中,全氟代烃由于其性质的稳定性和氧气在其中具有高的溶解性,而备受人们的关注。
全氟代十氢萘是人造血浆的主要成分之一。
合成此全氟代烃所采用的原料之一是萘。
能否认为全氟十氢萘是萘的衍生物?_____请写出与全氟十氢萘相对应的烃的结构简式。
全氟代十氢萘 萘 全氟十氢萘相对应的烃二.溴乙烷1.分子结构:分子式是________,结构式是_______________,结构简式是___________。
2.物理性质:纯净的溴乙烷是____色______体,沸点38.4℃,____溶于水,密度比水____。
3.化学性质: ⑴ 水解反应:实验1:向硝酸银溶液中加入溴乙烷,现象:_____________________________________________,说明溴乙烷是____________(填“电解质”或“非电解质”),____ (填“能”或“不能”)电离出Br -。
实验2:将溴乙烷加入NaOH 溶液,加热,振荡。
加入____________,目的是_____________________, 再加入硝酸银溶液,现象______________________________。
溴乙烷在碱性条件下水解的方程式为:_____________________________________________________。
反应类型是_____________。
⑵ 消去反应:实验3:向溴乙烷中加入NaOH 的乙醇溶液,现象____________________________________,说明溴乙烷________ (填“能”或“不能”)溶于乙醇。
在55~60℃的水浴中加热上述混合溶液,产生的气体先通过水,再通过酸性高锰酸钾溶液,现象是________________。
以上反应的化学方程式为_____________________________________________________。
反应类型是_____________。
消去反应的概念:有机化合物在一定条件下,_______________________________________,而生成F 2C F 2C C F 2C C F 2C C F 22CF 2F 2C F F____________________________的反应。
在溴乙烷的消去实验中,从溴乙烷和NaOH 的乙醇溶液中挥发出来的蒸汽中,含有的主要成分_______________________________,经过水后可除去的杂质为________________。
【基本练习】1.某卤代烃与氢氧化钠的醇溶液在加热条件下反应产生丙烯,将剩余的溶液用硝酸酸化后,假如硝酸银溶液生成浅黄色沉淀。
则原卤代烃的结构简式可能是 ( )(A ) (B ) (C ) (D )2.某烃的二溴代物有四种同分异构体。
该烷烃的结构简式为 ( )(A ) (B )CH 3CH 2CH 3 (C )CH CH 3CH 3CH 3(D )3.下列物质中具有两种官能团的是A .CH 2-CH 2B .CH 2-CH 2C .CH 2=CH -ClD .CH 3CH 2OH4.在一定条件下实现的下列物质转化过程中,发生的反应属于消去反应的是( ) (A )ClCH 2CH 2CH 2CH 2Cl → CH 2=CHCH=CH 2 (B )ClCH 2CH 2CH 2CH 2Cl →(C )ClCH 2CH 2CH 2CH 2Cl → HOCH 2CH 2CH 2CH 2OH (D )ClCH 2CH 2CH 2CH 2Cl → NCCH 2CH 2CH 2CH 2CN5、通过下列实验过程,不能鉴别1-氯丙烷和1-溴丙烷的是( ) A .加水B .加NaOH 的乙醇溶液,加热,再加入硝酸银溶液C .加NaOH 的水溶液,加热,再加入硝酸酸化,最后加入硝酸银溶液D .加NaOH 的乙醇溶液,加热,再加入硝酸酸化,最后加入硝酸银溶液6、为了鉴定溴乙烷中溴元素的存在,试分析①~⑥的各步实验,其中操作顺序合理的是( ) ①加入AgNO 3溶液 ②加入NaOH 溶液 ③加热 ④加入蒸馏水 ⑤用HNO 3酸化溶液 ⑥加入NaOH 溶液醇溶液A.①②③⑤B.②③⑤①C. ⑥③⑤①D.④②⑤③7.某液态卤代烷RX(R 是烷基,X 是某种卤素原子)的密度是a g ·cm -3。
该RX 可以跟稀碱发生水解反应生成ROH (能跟水互溶)和HX 。
为了测定RX 的分子量,拟定的实验步骤如下: ①准确量取该卤代烷b mL ,放入锥形瓶中。
②在锥形瓶中加入过量稀NaOH 溶液,塞上带有长玻璃管的塞子,加热,发生反应。
③反应完成后,冷却溶液,加稀硝酸酸化,滴加过量的AgNO 3溶液得白色沉淀。
④过滤、洗涤、干燥后称重,得到固体c g 。
回答问题:CH 3CH 2CH 2ClCH 3CH 2CH 2BrCH CH 3CH 3CH CH 3CH 3—NO 2—NO 2 ——OH ClNaOH(1)装置中长玻璃管的作用是__________________________________________。
(2)步骤④中,洗涤的目的是为了除去沉淀上吸附的__________________离子。
(3)该卤代烷中所含卤素的名称是____________,判断的依据是__________________________________________________。
(4)该卤代烷的分子量是_____________(列出算式)。
(5)如果在步骤③中,加HNO 3的量不足,没有将溶液酸化,则步骤④中测得的c 值(填下列选项代码)_______。
A .偏大B .偏小C .不变D .大小不定8.已知维生素A 的结构简式可写为 ,该分子中含有的官能团是______________________________________________________________ 三.卤代烃的物理性质1、沸点:常温下除CH 3Cl 、CH 3CH 2Cl 、CH 3Br 为气态,其它卤代烃都是液体或低熔点的固体 饱和一元氯代烷烃的沸点随碳原子数的增大而__________。
为什么? 2、密度一氯代烷的密度小于水,一溴代烷的密度大于水,一氯代烷的密度随碳原子数的增大而__________。
为什么? 四.卤代烃的化学性质 ①与NaOH 水溶液反应:R —X + H —OH R —OH + HX②与NaOH 醇溶液混合共热:—C —C — + NaOH —C=C — + NaX + H 2O H X例1:写出下列反应的化学方程式-40-200204060801000.20.40.60.81一氯甲烷一氯乙烷1-氯丙烷1-氯丁烷醇溶液 △ CH 2OH(1)2-氯丙烷的水解________________________________________________ (2)1,2-二碘丙烷水解____________________________________________ (3)由乙烯制乙二醇_________________________________________________ (4)2-碘丙烷的消去_________________________________________________ (5)2-甲基-2-氯丙烷的消去_________________________________________________ 例2、写出下列卤代烃在NaOH 醇溶液中加热发生反应可能得到的有机生成物(1)2-溴丁烷_________________________(2)2,2 –二甲基-3-溴丁烷__________________(3)CH 3CH 2CHCHCH 2CH 33KOH 乙醇 ,∆CH 3CH 2C CH 3CHCH 2CH 3_____________________________________________________(4)OH 乙醇 ,∆CH 3BrCH 3____________________________________________例3、某一溴代烷烃在与浓NaOH 的乙醇溶液混合共热的过程中,产生了三种产物(不考虑立体异构)。
由此可推知该一溴代烷烃至少应含有____个碳原子。
此一溴代烷烃的结构简式可表示为:_________________________________________________________________________________。
例4、某一碘氯代烷在NaOH 醇溶液中不能发生消去反应。
试写出三种符合要求的碘代烃的结构简式。
_________________________________________________________________________________ 三.卤代烃的用途与环境保护1、氟氯烃与臭氧层空洞例.同温层的臭氧是能吸收和阻挡对生命有害的太阳短紫外辐射的天然滤波器。
有害污染物一旦进入同温层,就不仅会在那里停留很多年,而且也会迅速跨越国界和海洋环绕地球分布,使该问题成为真正全球性的问题。
臭氧破坏机理是以链式反应为基础的。
其中,一个污染物分子被输送到低层大气并被雨水除去之前,就能破坏数千个臭氧分子。
⑴请在上图的方框中写出Cl 原子使臭氧层遭受破坏的总反应方程式。
⑵指出在上述变化过程中Cl 原子的作用是______________。
2、有机农药与环境污染例:早在1874年就合成了有机物DDT ,瑞士化学家米勒因首先发现DDT 作为杀虫剂的特性,而于1948年获得诺贝尔医学奖。
1944年后广泛用作杀虫剂, 后因具有高残毒被禁止使用。
DDT 的结构如下:(DDT )三氯杀螨醇是50年代推出的几十种杀螨剂中用量最大的一种,其结构式如下:从结构上看,它是DDT 的醇体。
