新编文档-3 突破全国卷专题讲座(九) 常见有机物的结构与性质(共19张PPT)-精品文档
高考化学二轮复习:常见有机物的结构与性质课件

A.分子式为C14H14O4
志不真则心不热,心不热则功不贤。
无钱之人脚杆硬,有钱之人骨头酥。
心志要坚,意趣要乐。
②
B.不能使酸性重铬酸钾溶液变色
有志始知蓬莱近,无为总觉咫尺远。
三军可夺帅也,匹夫不可夺志也。
C.能够发生水解反应
志高山峰矮,路从脚下伸。
D.能够发生消去反应生成双键
ห้องสมุดไป่ตู้
)
【审答流程—信息提炼】
常见有机物的结构与性质
(考查频次:5年10考)
研磨真题·培养审题力
【典例】(2020·全国Ⅰ卷)紫花前胡醇(
)可从中药材当归和白芷
人不可以有傲气,但不可以无傲骨
中提取得到,能提高人体免疫力,有关该化合物,下列叙述错误的是(
丈夫清万里,谁能扫一室。
谁不向前看,谁就会面临许多困难。
天才是由于对事业的热爱感而发展起来的,简直可以说天才。
如右:
下列关于金丝桃苷的叙述,错误的是(
A.可与氢气发生加成反应
B.分子含21个碳原子
C.能与乙酸发生酯化反应
D.不能与金属钠反应
)
4.D
该物质含有苯环和碳碳双键,一定条件下可以与氢气发生加成反应,A正确;
根据该物质的结构简式可知该分子含有21个碳原子,B正确;该物质含有羟基,
可以与乙酸发生酯化反应,C正确;该物质含有普通羟基和酚羟基,均可以与金
【典例解析】B 该化合物的分子式为C14H14O4,故A正确;紫花前胡醇结构中含
有碳碳双键,双键比较活泼,酸性重铬酸钾溶液有强氧化性,双键很容易被氧化,
故酸性重铬酸钾溶液自身会被还原从而变色,故B错误;紫花前胡醇结构中含有
才自清明志自高。
高中化学 有机物的结构与性质

[备考要点] 1.掌握有机物的组成与结构。
2.掌握烃及其衍生物的性质与应用。
3.掌握糖类、油脂、蛋白质的结构与性质。
4.理解合成高分子的结构与特点。
考点一有机物的结构与性质1.常见有机物及官能团的主要性质种类通式官能团主要化学性质烷烃C n H 2n +2无在光照时与气态卤素单质发生取代反应烯烃C n H 2n (单烯烃)碳碳双键:(1)与卤素单质、H 2或H 2O 等能发生加成反应;(2)能被酸性KMnO 4溶液等强氧化剂氧化炔烃C n H 2n -2(单炔烃)碳碳三键:—C ≡C—卤代烃一卤代烃:R—X—X(X 表示卤素原子)(1)与NaOH 水溶液共热发生取代反应生成醇;(2)与NaOH 醇溶液共热发生消去反应醇一元醇:R—OH羟基:—OH(1)与活泼金属反应产生H 2;(2)与卤化氢或浓氢卤酸反应生成卤代烃;(3)脱水反应:乙醇140℃分子间脱水生成醚170℃分子内脱水生成烯;(4)催化氧化为醛或酮;(5)与羧酸或无机含氧酸反应生成酯醚R—O—R醚键:性质稳定,一般不与酸、碱、氧化剂反应酚Ar—OH(Ar 表示芳香基)羟基:—OH(1)呈弱酸性,比碳酸酸性弱;(2)苯酚与浓溴水发生取代反应,生成白色沉淀2,4,6-三溴苯酚;(3)遇FeCl 3溶液呈紫色(显色反应);(4)易被氧化醛醛基:(1)与H 2发生加成反应生成醇;(2)被氧化剂(O 2、多伦试剂、斐林试剂、酸性高锰酸钾等)氧化为羧酸羧酸羧基:(1)具有酸的通性;(2)与醇发生酯化反应;(3)不能与H 2发生加成反应;(4)能与含—NH 2的物质生成酰胺酯酯基:(1)可发生水解反应生成羧酸(盐)和醇;(2)可发生醇解反应生成新酯和新醇氨基酸RCH(NH 2)COOH氨基:—NH 2,羧基:—COOH两性化合物,能形成肽键()蛋白质结构复杂无通式肽键:,氨基:—NH 2,羧基:—COOH(1)具有两性;(2)能发生水解反应;(3)在一定条件下变性;(4)含苯基的蛋白质遇浓硝酸变黄发生颜色反应;(5)灼烧有特殊气味糖C m (H 2O)n羟基:—OH ,醛基:—CHO ,羰基:(1)氧化反应,含醛基的糖能发生银镜反应(或与新制氢氧化铜反应);(2)加氢还原;(3)酯化反应;(4)多糖水解;(5)葡萄糖发酵分解生成乙醇油脂酯基:(1)水解反应(在碱性溶液中的水解称为皂化反应);(2)硬化反应2.常考官能团1mol 所消耗的NaOH 溶液、H 2物质的量的确定(1)最多消耗NaOH 溶液______mol 。
有机物的性质和结构PPT教学课件

CH3-CHCl-CH2-CHCl-CH3 (D) Cl-CH2-CHCl-CCl3 Cl-CH2-CHCl-CH2-CHCl-CCl3
Cl-CH2-CHCl-CH2-CHCl-CH2-CHCl-CCl3
023.中山市华侨中学第三次模考卷5
5.一个做匀减速直线运动的物体,经3.0s速度减 为零,若测出它在最后1.0s内的位移是1.0m。那么 该物体在这3.0s内的平均速度是 ( B )
A.1.0m/s B.3.0m/s C.5.0m/s D.9.0m/s
011.08届启东市第一次调研测试卷1
1.某车队从同一地点先后从静止开出n辆汽车,在 平直的公路上沿一直线行驶,各车均先做加速度为a 的匀加速直线运动,达到速度v后做匀速直线运动, 汽车都匀速行驶后,相邻两车距离均为s,则相邻两 车启动的时间间隔为 ( D )
试写出-CH3、 CH3+ 、 -OH、OH-的电子式。
2.官能团
能决定有机物化学特性的原子或原子团。
名称 符号 名称
双、叁键 卤素原子
-C C-
-C≡ C-
X
硝基
磺酸基
羟基 -OH 氨基
醛基 -CHO 羧基
符号
-NO2
-SO3H
-NH2 -COOH
例、与H2完全加成后,不可能生成
C 2,2,3-三甲基戊烷的烃是(
A.若A不t 变,则a也不变 B.若A>0且保持不变,则a逐渐变大 C.若A不变,则物体在中间位置处的速度为 vt v0
2 D.若A不变,则物体在中间位置处的速度为 vt 2 v02
2
gk006.2008年高考物理广东卷1
第九章 课时3 有机物的结构与性质 课件 2021届高三一轮复习化学(共50张PPT)

甲苯为—CH3 与
的组合。
(2)碳碳单键能旋转,而碳碳双键不能旋转。
(3)凡有机物分子结构中有碳的 4 条单键结构(如—CH3、—CH2
—等),则所有原子一定不在同一平面上。
(4)平面与平面连接时,如果两个平面结构通过单键相连,由于
碳碳单键能旋转,两个平面可能共平面,如苯乙烯
( 多有 16 个。
)分子中共平面的原子至少有 12 个,最
液变色,可以鉴别;D 项,乙醇能使酸性高锰酸钾溶液褪色,
乙酸不能使酸性高锰酸钾溶液褪色,可以鉴别。
答案:A
随堂检测反馈
1.(全国卷Ⅱ)分子式为 C5H10O2 并能与饱和 NaHCO3 溶液反应
放出气体的有机物有(不含立体异构)
()
A.3 种 B.4 种 C.5 种
D.6 种
解析:分子式为 C5H10O2 并能与饱和 NaHCO3 溶液反应放
答案:A
知识点二 核心素养迁移 ——同分异构体数目判断
考必备•清单
判断同分异构体数目的常用方法和思路 基团 将有机物看作由基团连接而成,由基团的异构体数目可 连接 推断有机物的异构体数目。如丁基有四种,C4H9— 法 OH、C4H9—Cl分别有四种
将有机物分子中的不同原子或基团换位思考。如乙烷分 换位
的同分异构体(不考虑立体异构)数目为
()
A.9
B.10
C.11
D.12
解析:由分子式可知碳原子达饱和,能与钠反应生成 H2
说明分子中含有羟基,含有 4 个碳原子的碳链结构有
有 3 种和 1 种,所以符合条件的同分异构体的数目共有:
4+4+3+1=12 种。
答案:D
法中正确的是
()
A.b 的同分异构体只有 d 和 p 两种
高三化学专题复习09·常考有机物的结构、性质及用途
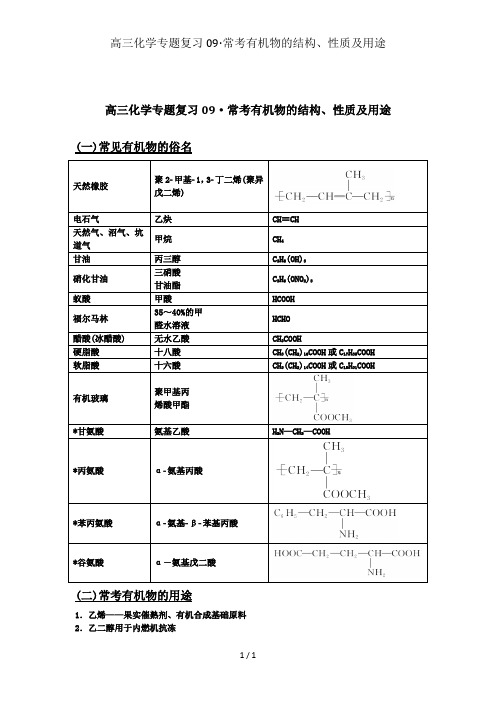
高三化学专题复习09·常考有机物的结构、性质及用途(一)常见有机物的俗名
CH≡CH
CH3(CH2)14COOH或C15H31COOH
H2N—CH2—COOH
(二)常考有机物的用途
1.乙烯——果实催熟剂、有机合成基础原料
2.乙二醇用于内燃机抗冻
3.甘油用于制硝化甘油,溶剂,润滑油
4.维生素C、E等——抗氧化剂
5.植物纤维可用作食品干燥剂
6.葡萄糖——用于制镜业、糖果业、医药工业等
7.消毒杀菌:氯气,漂白粉(水消毒);高锰酸钾(稀溶液皮肤消毒),酒精(皮肤,75%)碘酒;苯酚(粗品用于环境消毒,制洗剂,软膏用于皮肤消毒);甲醛(福尔马林用于环境消毒)
等;ClO2可用于自来水的杀菌消毒
(三)常见有机物的结构与性质
1.几种烃的结构、性质的比较
苯
苯环中的碳碳键是介于碳碳单键
(CH3COOCH2CH3)
油脂
(。
第九章 课时3 有机物的结构与性质 课件 2021届高三一轮复习化学(共50张PPT)

探题源•规律
[典例] (2019·全国卷 Ⅲ)下列化合物的分子中,所有原子
可能共平面的是
()
A.甲苯
B.乙烷
C.丙炔
D.1,3丁二烯
[解析] 甲烷分子是正四面体结构,含有甲基(—CH3)的分
子所有原子不能共平面。A 错误,甲苯中含有甲基,分子中所
有原子一定不能共平面;B 错误,乙烷中所有原子一定不共平
()
A.8种
B.10种
C.12种
D.14种
解析:可利用“定一移一”法,正丁烷有两种等效氢,Br定
位1号碳原子时,有
,Br定位2号碳原子时,
有
,异丁烷有两种等效氢,Br定位1号碳原子
时,有
,Br定位2号碳原子时,有
4+4+3+1=12(种)。
答案:C
,共
2.分子式为 C4H9OCl,且能与钠反应产生氢气的有机物可能
甲苯为—CH3 与
的组合。
(2)碳碳单键能旋转,而碳碳双键不能旋转。
(3)凡有机物分子结构中有碳的 4 条单键结构(如—CH3、—CH2
—等),则所有原子一定不在同一平面上。
(4)平面与平面连接时,如果两个平面结构通过单键相连,由于
碳碳单键能旋转,两个平面可能共平面,如苯乙烯
( 多有 16 个。
)分子中共平面的原子至少有 12 个,最
代表物
典型化学反应
葡萄糖 与新制Cu(OH)2悬浊液加热产生砖 红色沉淀
探题源•规律
[典例] (2019·漳州八校联考)某有机物的结构如图所示,
这种有机物不可能具有的性质是
()
①可以与氢气发生加成反应 ②能使酸性KMnO4溶液褪 色 ③能跟NaOH溶液反应 ④能发生酯化反应 ⑤能发生加
高考命题25常见有机物的组成、结构、性质 (共45张)

褪色 褪色
无色无味
3.糖类、蛋白质的特征反应
银镜
红色沉淀 蓝 烧焦羽毛
4.有机物分子中原子共面、共线的判断
正四面体 结构,分子 (1)四面体结构模型:甲烷分子为_____________
中有且只有 3 个原子共面。 (2)共面模型 ①乙烯:平面结构,分子中所有原子都在同一平面内,键角
120° _____________ 。
淀粉、纤维素的化学式都可以用(C6H10O5)n 表示 误认为两者是同分异构体。其实两者分子中的 n 取值不同, 两者不属于同分异构体。 误以为糖类都能水解 其实不然,单糖不能水解。 C2.常见有机物的结构
4.[2017· 全国Ⅰ]化合物
(b)、
(d)、,下列说法正确的是( D ) A.b 的同分异构体只有 d 和 p 两种 B.b、d、p 的二氯代物均只有三种 C.b、d、p 均可与酸性高锰酸钾溶液反应 D.b、d、p 中只有 b 的所有原子处于同一平面
平面六边形 结构,分子中所有原子在同一平面内, ②苯:_____________
120° 键角_____________ 。
平面三角形 结构,分子中所有原子在同一平面 ③甲醛:_____________
内。
直线形 (3)共线模型:乙炔分子为_____________ 结构,分子中 4 个
原子在一条直线上。
第一部分
知识专题突破篇
专题十一 常见有机物及其应用(必修)
[考纲要求]
1.了解有机化合物中碳的成键特征。了解有机
化合物的同分异构现象。 能正确书写简单有机化合物的同分异构 体。 2.掌握常见有机反应类型。 3.了解甲烷、乙烯、苯等有机化合物的主要性质及应用。 4.了解氯乙烯、苯的衍生物等在化工生产中的重要作用。
化学专题三 有机物的结构与性质

专题三有机物的结构与性质一、各类有机物(或代表物)的物理性质及用途1. 脂肪烃(烷烃、烯烃、炔烃)的物理性质及规律、用途田气和煤矿坑道气(又叫瓦斯气)的主要成分。
用途:作清洁能源(高效、低耗、污染小)和化工原料。
乙烯:通常为无色、稍有气味的气体,密度比空气略小,难溶于水,易溶于有机溶剂。
用途:乙烯是非常重要的化工原料,乙烯的产量可以用来衡量一个国家的石油化工发展水平;乙烯是一种植物生长调节剂,可作为果实催熟剂。
乙炔:通常为无色、无味的气体,密度比空气略小,微溶于水,易溶于有机溶剂。
用途:化工原料。
脂肪烃:来源于石油、天然气和煤等。
2.苯的物理性质和用途:苯为____色、________气味的液体,有毒,____溶于水,密度比水____,熔点为5.5 ℃,沸点为80.1 ℃。
用途:苯、甲苯、二甲苯、乙苯等是基本的有机原料,可用于合成炸药、染料、药品、农药、合成材料等。
来源:芳香烃来源于煤的提炼和石油化学工业中的催化重整。
3.卤代烃的物理性质和用途:常温下,少数如一氯甲烷为气体,大多数卤代烃为液态或固态,沸点比同碳原子数的烃沸点要高,所有卤代烃都不溶于水,可溶于大多数有机溶剂。
一氯(氟)代烷的密度小于1,一溴(碘)代烷的密度大于1。
用途:作制冷剂、灭火剂、有机溶剂、麻醉剂及化工合成的中间体等。
危害:造成“臭氧空洞”。
溴乙烷:无色液体,沸点为38.4 ℃,密度比水大,难溶于水,易溶于乙醇等有机溶剂。
4.醇的物理性质和用途:低级脂肪醇易溶于水,随碳数增多,溶解性逐渐降低。
因为与水形成了氢键,甲醇、乙醇、丙醇、乙二醇、丙三醇等小分子醇类均可以与水任意比互溶。
一元脂肪醇的密度一般小于水。
直链饱和一元醇的沸点随着分子中碳原子数的递增而逐渐升高。
醇分子间存在氢键,所以相对分子质量相近的醇和烷烃相比,醇的沸点远远高于烷烃。
乙醇:常温下,无色、有特殊香味的液体,密度比水小,与水互溶,易挥发。
用途:用作酒精灯、内燃机等的燃料,用作化工原料,医疗上常用体积分数为75%的乙醇溶液作消毒剂。
高中常见的有机物结构和性质的总结.docx

高中常见有机化合物结构与性质总结物质类别特征结构(官能团)断键位置反应类型试剂条件反应产物烷坯—c— C—-C-H 取代x2,光照1-c-x 1烯桂)c=< >=<加成X2的CCI4溶液—c — c —HX-C-C-H2O,催化剂-C-C-H 0H加成,还原H2,催化剂—c — c —加聚一定条件 1 1 十c— Ct1 1氧化酸性KMnO4溶液一C三c- -c = c-或-c = c-加成x2的CCI4溶液X X—f 二f—或X X I 1X XHX,催化剂,加热H X 或Y十H X加成,还原H2,催化剂H H 或-卜卜H H氧化酸性KMnO4溶液芳香坯◎取代X2, FeX3HNO3,浓H2SO4,加热<§^NO2◎加成出,Ni,加热0取代HNO3,浓H2SO4,加热/N0202N^^^R'N O2氧化酸性KMnO4溶液<§^COOH物质类别特征结构(官能团)断键位置反应类型试剂条件反应产物卤代坯—X1-c-x1取代NaOH水溶液,加热 1 -C-OH1 —c— C—消去NaOH乙醇溶液,加热>=<醇—0H1-C-O-H1取代、置换Na1一C-ONa1取代、酯化竣酸,浓H2SO4,加热1 II—f—0— c—1 -C-O-H1H氧化。
2,Cu,加热0 II -C-H1-C-OH1取代浓HX溶液,加热1-c-x11 1-C-C-OHA 1消去浓H2SO4,加热>=< —CH2—0H 氧化酸性KMnO4溶液(或酸性K2Cr2O7溶液)—COOH酚取代澳水z BrBr^O^OH r Br取代、置换Na屮和NaOH溶液氧化空气醛0II -C-H 0II -C-H 氧化。
2,催化剂,加热(或银氨溶液,或新制C U(OH)2浊液)II -C-OHII -C-H 加成、还原H2,催化剂,加热OH-C-H竣酸II一C-OHII _ C-O-H取代、置换Na 0II一C-ONa中和NaOH溶液II .一 C + OHi取代、酯化醇,浓H2SO4,加热0II —C —0—R酯0II -C-O-R0 II .一C'O-R 取代、水解稀H2SO4,加热(或NaOH溶液,加热)0 IIJ - C-OHI HO-R乙酸能使紫色石蕊溶液变红色乙醇能和紫色石蕊溶液互溶苯会和紫色右蕊试液分层,苯在上层硝基苯和紫色石蕊试液会分层,硝基苯在下层甲烷燃烧CH4+202->C02+2H20(条件为点燃)甲烷隔绝空气高温分解甲烷分解很复杂,以下是最终分解。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
专题9 有机化合物
4.(2018·济南模拟)下列有关说法正确的是( ) A.蔗糖、淀粉、蛋白质、油脂都是营养物质,都属于高分子 化合物,都能发生水解反应 B.人造纤维、合成纤维、碳纤维、光导纤维的主要成分都是 纤维素 C.乙醇、乙酸、乙酸乙酯都能发生取代反应,乙酸乙酯中的 少量乙酸可用饱和 Na2CO3 溶液除去 D.甲烷、乙烯和苯在工业上都可通过石油分馏得到 解析:选 C。蔗糖与油脂不属于高分子化合物,A 错误;合成
—X、—NO2 取代 碳上的氢原子
剂)、浓 HNO3(浓硫酸作催化剂)
取代反应
水解型
酯、油脂,酸溶液作 催化剂 酯、油脂,碱溶液作
生成相应酸和醇 生成相应酸的盐和
催化剂
相应醇
酯化型 —OH、—COOH(浓 生成相应的酯和水 硫酸、加热)
专题9 有机化合物
反应类型 官能团种类、试剂、反应条件 实质或结果
专题9 有机化合物
突破全国卷专题讲座(九) 常见有机物的 结构与性质
专题9 有机化合物
[备考分析] 常见有机物是与我们的生活、生产紧密相关的物质,属于高考 必考内容,主要包括甲烷、乙烯、苯、乙醇、乙酸、葡萄糖、 蔗糖、淀粉、油脂、蛋白质共十种物质。内容相对独立、零碎, 不具备系统性。学习中重点抓住“结构决定性质”这一思想, 掌握典型物质的重要性质并灵活应用于生产、生活实际才能较 好的应对这一类问题。
专题9 有机化合物
[命题解读] 该类题的解题策略:熟练掌握以下四方面基础知识,灵活运用。 1.常见有机物的知识体系
甲烷(CH4)
烃乙烯(CH2===CH2)
有机化合物
苯( ) 乙醇(CH3CH2OH)
烃的衍生物
乙酸(
)
糖类、油脂、蛋白质
专题9 有机化合物
2.常见有机物的组成和结构
有机物
分子式
结构简式
官能团
甲烷 乙烯
CH4 C2H4
CH4 CH2===CH2
碳碳双键
苯
C6H6
乙醇 乙酸 葡萄糖 纤维素 淀粉
C2H6O C2H4O2 C6H12O6
C2H5OH
羟基
CH3COOH
羧基
CH20O5)n
(C6H10O5)n
专题9 有机化合物
物质 乙酸(CH3COOH)
葡萄糖(C6H12O6) 淀粉
蛋白质
特性或特征反应 酸性:使石蕊试液和 pH 试纸变红
酯化:与乙醇反应 与银氨溶液反应,析出单质银 与新制的 Cu(OH)2 悬浊液反应,产生 砖红色沉淀
遇碘水显蓝色 遇浓硝酸显黄色 灼烧有烧焦羽毛气味
专题9 有机化合物
4.重要的有机反应类型 反应类型 官能团种类、试剂、反应条件
实质或结果
加成反应
与 X2(X=Cl、Br,
下同)、H2、HBr、H2O(后三种
需要有催化剂等条件)
碳碳双键消失
加聚反应
(催化剂)
众多小分子相互加 成
专题9 有机化合物
反应类型 官能团种类、试剂、反应条件 实质或结果
饱和烃:X2(光照); 苯环上的氢原子:X2(Fe 作催化
纤维、碳纤维、光导纤维主要成分均不是纤维素(糖类),B 错
A.甲物质可以在引发剂作用下生成有机高分子化合物 B.1 mol 乙物质可与 2 mol 钠完全反应生成 1 mol 氢气 C.丙物质能够使酸性高锰酸钾溶液褪色 D.甲、乙、丙三种物质都可以发生加成反应
专题9 有机化合物
解析:选 D。甲物质分子中含有碳碳双键,可在一定条件下发 生加聚反应生成有机高分子化合物,A 项正确;乙物质分子中 含有两个羟基,1 mol 乙物质可与 2 mol 金属钠完全反应生成 1 mol H2,B 项正确;丙物质分子中含有碳碳双键,可使酸性 高锰酸钾溶液褪色,C 项正确;乙物质不能发生加成反应,D 项错误。
专题9 有机化合物
物质 苯(C6H6) 乙醇(C2H5OH)
特性或特征反应 氧化:燃烧,不能使 KMnO4(H+)褪色 取代:与液 Br2 在催化剂作用下反应; 与浓 HNO3 在浓 H2SO4 催化下反应
加成:与 H2 在催化剂作用下反应 置换:与 Na 反应
氧化:燃烧;与 O2 催化氧化反应;与 KMnO4(H+)或 K2Cr2O7(H+)反应
专题9 有机化合物
解析:选 C。甲为甲烷,不能使酸性 KMnO4 溶液褪色;乙为 乙烯,它使溴水褪色的原因是与 Br2 发生了加成反应;丁为乙 醇,在浓 H2SO4 的作用下能和乙酸发生酯化反应;丙为苯, 苯分子中的碳碳键是介于碳碳单键和碳碳双键之间的独特的 键。
专题9 有机化合物
2.(2018·济南模拟)“神十一”宇航员使用的氧气瓶是以聚酯 玻璃钢为原料。甲、乙、丙三种物质是合成聚酯玻璃钢的基本 原料。下列说法中错误的是( )
有机物
分子式
专题9 有机化合物
结构简式
官能团
油脂
酯基
蛋白质和氨基酸
氨基、羧基
专题9 有机化合物
3.常见有机物的化学性质
物质
特性或特征反应
甲烷(CH4) 乙烯(C2H4)
氧化:燃烧,不能使 KMnO4(H+)褪色 取代:与 Cl2(光照)反应
氧化:燃烧,能使 KMnO4(H+)褪色 加成:使 Br2 的 CCl4 溶液褪色
专题9 有机化合物
3.以下有关物质结构的描述正确的是( ) A.甲苯分子中的所有原子可能共平面
B.
分子中的所有原子可能共平面
C.乙烷分子中的所有原子可能共平面 D.二氯甲烷分子为正四面体结构
解析:选 B。由于甲苯、乙烷分子中含 —CH3,碳原子形成 的四个键为空间四面体结构,所有原子不可能全部共面;苯和 乙烯均为平面结构,故苯乙烯分子中的所有原子可能共平面; 二氯甲烷分子中 C—H 键与 C—Cl 键键长不相同,故不可能 为正四面体结构。
催化 C2H5OH、O2(催化剂、 生成乙醛和水 氧化 加热)
氧化反应 KMnO4
氧化型
CH2===CH2, C2H5OH
CH2===CH2 被氧 化生成 CO2, C2H5OH 被氧化生 成乙酸
专题9 有机化合物
[突破训练] 1.如图是四种常见有机物的比例模型示意图。下列说法正确 的是( )
A.甲能使酸性 KMnO4 溶液褪色 B.乙可与溴水发生取代反应而使溴水褪色 C.丙中的碳碳键是介于碳碳单键和碳碳双键之间的独特的键 D.丁在稀硫酸作用下可与乙酸发生取代反应
