人教版中考化学试题汇编:36 工艺流程图题
中考化学真题分类汇编考点工艺流程含答案

中考化学真题分类汇编考点工艺流程含答案 Standardization of sany group #QS8QHH-HHGX8Q8-GNHHJ8-HHMHGN#3 3 3考点34 工艺流程一、选择题(2018·内蒙古呼和浩特)8.黄铁矿的主要成分为二硫化亚铁(FeS2),工业上可利用黄铁矿煅烧的产物冶炼铁和生产浓硫酸,其工业流程如下:下列说法错误的是A.反应②不是置换反应,反应③④为化合反应B.反应①中各元素的化合价均发生了改变C.该工业生产过程产生的废气中的SO2可以用熟石灰溶液吸收D.向制得的100克98%的浓硫酸中加入100克蒸馏水,配制49%的稀硫酸【答案】D(2018·新疆乌鲁木齐)含硫煤燃烧会产生大气污染。
为防治该污染,某工厂设计的新的治污方法不仅吸收了 SO2,同时还得到了某种化工产品。
该工艺流程如图所示,下列叙述不正确的是A. 该流程中可得到化工产品H2SO4B. 图中 FeSO4 → Fe2(SO4)3 的反应类型是复分解反应C. 该流程中化合价发生改变的元素为 Fe、S 和 OD. 图中吸收 SO2 的化学反应方程式为:Fe2(SO4)3 + SO2 + 2H2O == 2FeSO4 + 2H2SO4【答案】B(2018辽宁葫芦岛)(分)合成气是工业生产中的一种原料气,主要成分是一氧化碳和氢气。
它可以冶炼钢铁、生产二甲醚等。
请根据图示回答。
(注:图中括号内化学式表示相应物质的主要成分)(1)请写出利用合成气炼铁的化学方程式(写一个即可)(2)二甲醚(CH3OCH3)被称为21世纪新型燃料,能实现高效清洁燃烧,请写出二甲醚在空气中充分燃烧生成二氧化碳和水的化学方程式。
(3)合成气在不同催化剂作用下,可以合成不同的物质。
仅用合成气为原料不可能得到的物质是(填字母序号)A.甲醇(CH3OH) B.乙二醛(HC2O2)C.尿素〔CO(NH2)2]21.(1)3CO+ Fe2O32Fe + 3CO2(或3H2+ Fe2O32Fe + 3H2O)(2分)(2)CH3OCH3+3O32CO2+3H2O(2分)(3)C(1分)(2018·江苏无锡)17.(分)MgSO47H2O是一种重要的化工原料,某工厂以一种镁矿石(主要成分为SiO2和MgCO3,还含有少量FeCO3)为原料制备MgSO47H2O的主要流程如图:已知:SiO2既不溶于水也不溶于稀硫酸。
中考化学综合题专练∶流程图及答案

一、中考初中化学流程图1.以下是印刷线路板的生产及废液的处理过程:请回答下列问题:(1)写出步骤②中发生的一个反应:______________________(2)滤渣的成份有________,步骤③中发生反应的化学方程式是______________________(3)该流程中可以循环、回收利用的物质是:________________。
【答案】Fe+CuCl2==Cu+FeCl2Fe、Cu Fe+2HCl==FeCl2+H2↑FeCl2【解析】(1)金属活动顺序表:K Ca Na Mg Al Zn Fe Sn Pb H Cu Hg Ag Pt Au,在金属活动顺序表中,排在氢前边的金属能和酸发生置换反应生成盐和氢气。
金属的位置越靠前,金属的活动性越强。
位置靠前的金属能将位于其后的金属从它的盐溶液中置换出来。
将铁放入氯化铜、氯化铁、氯化亚铁的溶液中,铁能与氯化铁反应生成氯化亚铁,与氯化铜反应生成氯化亚铁和铜;反应方程式为:2FeCl3 + Cu= CuCl2 +2FeCl2,Fe+CuCl2==Cu+FeCl2,(2) 步骤②反应后的固体即为滤渣,成份有生成的铜和过量的铁,步骤③中铁和盐酸反应生成氯化亚铁和氢气,反应的化学方程式是Fe+2HCl==FeCl2+H2↑(3) 步骤②与步骤③生成的氯化亚铁可以在一定条件下转化成氯化铁,可循环利用。
2.人类的生存和发展离不开能源和资源.(1)家用燃料的更新过程如下:煤→液化石油气或管道煤气→天然气,下列有关家用燃料更新的理由,正确的是________(选填字母).A天然气属于可再生能源B气体燃料比固体燃料利用率更高C天然气作为燃料可避免温室效应的发生D煤仅仅用作燃料烧掉浪费资源(2)水是生命之源,合理利用和保护水资源是我们义不容辞的责任.①设法除去硬水中的________,可以使硬水软化成软水.②公共场所可利用“活性炭+超滤膜+紫外线”组合工艺获得直饮水,其中活性炭主要起________作用.(3)海水中有大量可以利用的化学资源,其中所含的氯化镁是金属镁的重要来源之一.从海水中提取金属镁,可按如图流程进行:①下列有关说法正确的是________(选填字母).A步骤I通过一步反应即可实现.B步骤II、III、IV的目的是从海水中提纯氯化镁C步骤V中化学能转化为电能D在此流程中涉及的基本反应类型有4种②在此流程中可以循环利用的物质是________.(4)家中蒸馒头常用的纯碱中含有少量氯化钠,某实验小组要测定该纯碱中碳酸钠的质量分数,取12g纯碱样品放入烧杯中,逐滴加入稀盐酸至不再产生气泡,此时烧杯中没有不溶物,共消耗稀盐酸72.4g,测得反应后溶液的质量为80g.请帮助实验小组完成以下计算(写出计算过程):①根据质量守恒定律计算生成二氧化碳的质量________②样品中碳酸钠的质量分数是多少________?【答案】BD 可溶性的钙、镁化合物吸附 B 氯化氢 4.4g 88.3%【解析】【分析】【详解】(1)A、天然气是三大化石燃料之一,属于不可再生能源,A错误;B、由于气体燃料与空气接触面更大,燃烧更充分,故气体燃料比固体燃料利用率更高,B 正确;C、天然气作为燃料也生成二氧化碳,所以不可避免温室效应的发生,C错误;D、煤仅仅用作燃料烧掉浪费资源,还可以深加工成各种产品,减少环境污染,D正确。
全国各地中考化学分类:流程图综合题汇编

一、中考初中化学流程图1.我国每年报废的手机超过1亿部。
废旧手机的电路板中含有铝、铁、铜、银、金等多种金属,随意丢弃既会造成资源浪费,也会污染土壤和水体。
化学兴趣小组为回收其中的铜,设计并进行了如下实验。
已知:Cu+H2O2+H2SO4=CuSO4+2H2O;不考虑金、银发生类似反应。
(1)将电路板粉碎成粉末的目的是___________________________________________。
(2)步骤①所得滤液中的溶质除硫酸外,还有__________________________。
(3)步骤②中的实验现象是:固体部分溶解,_____________________。
(4)步骤④中反应的化学方程式是______________________________________。
(5)检验步骤④稀硫酸已过量的方法是____________________________________________。
【答案】增大接触面积,使反应更充分,加快反应速率FeSO4和Al2(SO4)3溶液由无色变为蓝色Fe+H2SO4=FeSO4+H2↑取步骤④的滤液,加入铁粉,若有气泡冒出,则稀硫酸已过量【解析】(1)将电路板粉碎成粉末的目的是增大反应物接触面积,加快反应速率;(2)步骤①所得滤液中的溶质除硫酸外,还有稀硫酸和铝、铁反应生成的硫酸铝(Al2(SO4)3)和硫酸亚铁(FeSO4);(3)步骤②中铜和过氧化氢、硫酸反应生成硫酸铜和水,能够观察到固体部分溶解,溶液由无色变成蓝色;(4)步骤④中铁和稀硫酸反应生成硫酸亚铁和氢气,反应的化学Fe+H SO==FeSO+H 。
方程式是:24422.硝酸钙可用于无土栽培等。
一种利用石灰石制备硝酸钙晶体的流程如下:已知:硝酸会挥发、受热会分解。
(1)气体X为_______(填化学式)。
(2)“制浆”所得的混合物属于_______(填字母)。
a 溶液b 悬浊液c 乳浊液(3)写出“中和”步骤主要反应的化学方程式:________。
中考化学流程图综合题汇编及详细答案

一、中考初中化学流程图1.如图是常见物质的转化关系图(个别产物可能略去).其中A、B常温下均为液态,且组成元素相同;F是大理石的主要成分.请回答:(1)A的名称是_____,在反应①中,物质X起_____作用;(2)说出物质Z的一个用途_____;(3)反应②的化学方程式为_____;(4)反应⑥的化学方程式为_____;(5)反应①﹣⑥涉及的基本反应类型有_____种.【答案】双氧水或过氧化氢溶液催化做导线等 CaO+H2O = Ca(OH)2CuSO4+2NaOH=Na2SO4+Cu(OH)2↓ 3种【解析】【分析】已知F是大理石的主要成分,则F是碳酸钙,最后得到了蓝色沉淀,由此可以推出D为氢氧化钙,则可想到是生石灰和水化合生成了氢氧化钙,又因为已知A、B常温下均为液态,且组成元素相同,可以推知B是水,A是双氧水,双氧水在二氧化锰的催化作用下可生成水和氧气,所以X是二氧化锰,C是氧气,最后生成的蓝色沉淀是氢氧化铜,则往前推一下可知H是硫酸铜,再往前推测可知E是氧化铜,则Z是铜。
【详解】(1)A的名称是过氧化氢溶液,在反应①中,二氧化锰是过氧化氢溶液分解的催化剂,物质X起催化作用;(2)物质Z是铜,它的一个用途是做电线;(3)反应②是氧化钙和水反应生成氢氧化钙,反应的化学方程式为CaO+H2O = Ca(OH)2;(4)反应⑥是氢氧化钠和硫酸铜反应生成氢氧化铜和硫酸钠,反应的化学方程式为CuSO4+2NaOH=Na2SO4+Cu(OH)2↓;(5)反应①过氧化氢生成氧气和水是分解反应;反应②是氧化钙和水反应生成氢氧化钙、反应③是氧气和铜反应生成氧化铜都是化合反应,④⑤⑥都是复分解反应,涉及的基本反应类型有3种.2.CaCO3在生产生活中有广泛的用途。
(1)烧石灰石可制得活性CaO,反应的化学方程式为_________________________。
为测定不同煅烧温度对CaO活性的影响,取石灰石样品分为三等份,在同一设备中分别于800℃、900℃和1000℃条件下煅烧,所得固体分别与等质量的水完全反应,测得反应液温度随时间的变化如图所示。
中考化学综合题专题复习【流程图】专题解析附答案解析

一、中考初中化学流程图1.高炉炼铁所需的原料有铁矿石、焦炭、石灰石等,其过程可用下图简要表示:已知气体①、气体②和固体③均属于氧化物。
(1)气体②的化学式为_____。
根据氧化物的性质推测炉渣的主要成分为_____(填化学式)。
(2)炼铁高炉底部通过不同高度的出口分离铁水与炉渣(如图2所示)。
能实现渣铁分离的原因是是因为炉渣具有_____、_____的性质。
(3)反应Ⅰ~Ⅴ中属于化合反应的有_____个,属于分解反应的有_____个,属于置换反应的有_____个。
(4)高炉气体中含有多种成分,其中含量最高(占55%~60%)的是_____(填化学式),此外还含有25~30%的可燃性气体_____(填化学式),以及9~12%左右的_____(填化学式)。
【答案】CO CaSiO3熔点高密度比铁水小 3 1 0 N2 CO CO2【解析】【分析】【详解】(1)碳和氧气在点燃的条件下生成二氧化碳,二氧化碳和碳在高温的条件下生成一氧化碳,所以气体②的化学式为CO,化学反应前后,元素种类不变,所以依据氧化物的性质推测炉渣的主要成分为:CaSiO3;(2)炉渣的出口在上方,铁水的出口在下方,所以炉渣具有熔点高、密度比铁水小的性质;(3)Ⅰ是碳和氧气反应生成二氧化碳,属于化合反应,Ⅱ是二氧化碳和碳高温生成一氧化碳,属于化合反应,Ⅲ是一氧化碳和氧化铁在高温的条件下生成铁和二氧化碳,不属于基本反应类型,Ⅳ是氧化钙、二氧化硅反应生成硅酸钙,属于化合反应,Ⅴ是碳酸钙高温生成氧化钙和二氧化碳,属于分解反应,所以反应Ⅰ~Ⅴ中属于化合反应的有3个,属于分解反应的有1个,属于置换反应的有0个;(4)空气中含量最高的是氮气,所以高炉气中含有多种成分,其中含量最高(占55~60%)的是N2,此外还含有25~30%的可燃性气体CO,以及9~12%左右的CO2。
2.某合金主要成分为Zn、Fe、Cu,还含有少量这三种金属的氧化物。
利用该合金制成的机械零件废弃物制取高纯度ZnO,其部分工艺流程如下图所示。
中考化学流程图综合题汇编含详细答案

一、中考初中化学流程图1.某工业废液中含有CuSO4、ZnSO4、FeSO4,如果将废液直接排放就会造成水污染。
于是几位同学设计实验处理废液,回收工业重要原料硫酸锌和有关金属。
实验过程如下:请回答:(1)操作①的名称是_______,其中玻璃棒的作用是______。
写出加过量M发生的一个化学反应的方程式____________________。
(2)固体A中一定有_______。
判断操作④中稀硫酸足量的方法是_______。
(3)滤液 A、滤液B合起来蒸发至干目的是_________________。
【答案】过滤引流 Zn+CuSO4=ZnSO4+Cu 或Zn+FeSO4=ZnSO4+Fe Zn、Fe、Cu 继续加稀硫酸,无气泡生成提高硫酸锌的产率【解析】【分析】【详解】(1)操作1是将固体和液体分离的过程,故名称是过滤。
过滤操作中玻璃棒的作用是引流。
锌与硫酸铜反应生成硫酸锌和铜,锌与硫酸亚铁反应生成铁和硫酸锌,故反应的方程式为:Zn+CuSO4=ZnSO4+Cu 或Zn+FeSO4=ZnSO4+Fe。
(2)由图可知,加入的M物质是过量的锌,锌可以与CuSO4、FeSO4反应生成铜和铁和硫酸锌,与ZnSO4不反应,故固体A中一定有Zn、Fe、Cu。
如酸不足则不能与金属反应,则可以继续加热稀硫酸,如没有气泡没冒出,则说明稀硫酸足够。
(3)由图可知,固体C是不能被磁铁吸引,故C中含有铜和锌,故滤液B中的溶质是硫酸锌,故与滤液A混合蒸干可以提高硫酸锌的产率2.某合金主要成分为Zn、Fe、Cu,还含有少量这三种金属的氧化物。
利用该合金制成的机械零件废弃物制取高纯度ZnO,其部分工艺流程如下图所示。
已知:Zn( OH)2溶于NaOH等强碱形成可溶性盐。
回答相关问题:(1)滤渣I中一定有___________________。
(2)加酸溶解废弃物时,需要通风并远离火源,其原因是_____。
此过程中Zn还能起到除去含铜化合物的作用.写出该反应的化学方程式:_________________。
中考化学《流程图题》专项练习题(附带答案)

①步骤Ⅰ中加入足量稀硫酸后发生反应的化学方程式为______。
②溶液X中只含有一种溶质,该溶质为______。
17.(2023贵州)溶液的配制和应用在生活、生产中非常普遍。
(1)实验室用“电解水”的实验来探究水的组成,探究的理论依据是_____,反应的化学方程式是_______。
(4)反应②生成的水全部循环利用,为使该过程持续发生,反应①需要不断补充水,其原因是_______。
12.(2023广西)柠檬酸亚铁(FeC6H6O7)是一种易被吸收的补血剂。利用硫酸厂的废渣(主要含Fe2O3、Fe3O4,还有少量SiO2)制备柠檬酸亚铁,该工艺流程如图所示,回答下列问题:
资料1: ;
资料2:SiO2不溶于水,也不与稀硫酸反应。
(1)柠檬酸亚铁进入人体肠道后以_______(填阳离子符号)的形式被吸收,达到补血效果。
(2)固体C的成分是_______。
(3)步骤①②③④中涉及置换反应的是_______(填数字序号)。
(4)步骤③中发生反应的化学方程式是_______。
(5)“一系列操作”中,将柠檬酸亚铁晶体与溶液分离的操作是_______。
(4)降温至0℃的“冷冻结晶”过程,析出的两种物质中较多的是_________________。
(5)结合溶解度曲线解释,“蒸发结晶2”主要得到氯化钠的原因是_________________。
10.(2023深圳)某同学以金泥(含有Au、CuS、ZnS等)为原料制备(Au)和Cu的流程如图所示:
琴琴同学查阅资料已知:
13.(2023广州)制盐在我国有着悠久的历史。某盐湖水样品含有NaCl、Na2SO4及少量MgSO4和CaSO4,某小组从中获取NaCl和Na2SO4的主要过程如下:
中考化学流程图综合题汇编及答案

一、中考初中化学流程图1.以下是两个常见的工业流程,流程一:从只含有C u SO4的废液中回收金属铜,并得到工业原料硫酸亚铁,生产流程如下:(1)加入过量的A物质,该A物质为______。
操作a的名称是_______,操作a所用到的玻璃仪器有烧杯、玻璃棒、_________,操作a中玻璃棒的作用是_______。
(2)写出流程图中的固体成分的化学式____,B的溶液中溶质的化学式_______流程二:如图是两种常用脱硫工艺中含硫物质的转化路径(部分产物已略),请回答下列问题:(1)CaSO3中Ca、S、O元素的质量比是_______。
(2)已知原料NaOH的价格为2.9元/kg. 而Ca(OH)2的价格为0.36元/kg.两种工艺中,处理相同质量的SO2,双碱法所需的原料成本更低,其原因是______________。
【答案】铁过滤漏斗引流 Fe和Cu H2SO4 5:4 : 6 双碱法中通过反应II实现了NaOH的循环利用,减少了NaOH的用量处理等量SO2,氢氧化钙用量更少且价格便宜,所以双碱法成本更低【解析】流程一:只含有C u SO4的废液中回收金属铜,并得到工业原料硫酸亚铁,所所加试剂是过量的铁,反应方程式为Fe+CuSO4==FeSO4+Cu ,反应后得到是固体铜和铁,溶液硫酸亚铁溶液,过滤可将难溶固体与液体分离,所以应过滤,过滤用到的仪器有:烧杯、漏斗、玻璃棒、铁架台,其中,玻璃棒的作用是引流;将铜和铁的混合物中的铁除掉,得硫酸亚铁和铜,所以应加入的试剂B为稀硫酸,因为.Fe+H2SO4=FeSO4+H2↑,而铜和酸不反应;流程二:(1)化合物中元素的质量比=(相对原子质量×原子个数)之比,CaSO3中Ca、S、O元素的质量比是40:32:3×16= 5:4 : 6;(2)Na2SO3 + Ca(OH)2 =CaSO3↓+2NaOH , 2NaOH+ SO2 == Na2SO3+H2O;因此用双碱法(氢氧化钙和氢氧化钠联合使用)实现了NaOH的循环利用,减少了NaOH的用量处理等量SO2,氢氧化钙用量更少且价格便宜,所以双碱法成本更低。
中考化学 流程图综合试题含答案

一、中考初中化学流程图1.有一包白色固体样品,可能由硫酸钠、氢氧化钠、碳酸钙、氯化钡、氯化镁中的一种或几种物质组成,为探究该样品的组成,某小组取适量样品按下列流程进行试验。
请回答下列问题:(查阅资料)CO2不能直接与BaCl2和MgCl2发生反应。
(1)过滤操作中用到的玻璃仪器有烧杯、漏斗、________。
(2)滤渣a的成分是________;白色沉淀b的成分是________。
(3)滤渣a中加入足量稀盐酸的目的:________。
(4)若现象①“滤渣全部溶解”变为“滤渣部分溶解”,其他现象不变,则原样品一定存在的物质是________。
【答案】玻璃棒 CaCO3、Mg(OH)2(填名称也可) BaCO3(填名称也可)排除硫酸钡沉淀的干扰,证明样品中无硫酸钠 CaCO3、BaCl2、Na2SO4、NaOH(填名称也可)【解析】【分析】硫酸钠和氯化钡反应生成硫酸钡和氯化钠,氢氧化钠和氯化镁反应生成氢氧化镁和氯化钠,碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳,氢氧化镁和稀盐酸反应生成氯化镁和水,氢氧化钠和二氧化碳反应生成碳酸钠和水,碳酸钠和氯化钡反应生成碳酸钡和氯化钠。
【详解】(1)过滤需要玻璃棒引流,故过滤操作中用到的玻璃仪器有烧杯、漏斗、玻璃棒。
(2)样品加水溶解,硫酸钠和氯化钡反应生成硫酸钡和氯化钠,氢氧化钠和氯化镁反应生成氢氧化镁和氯化钠,碳酸钙不溶于水,过滤得到滤渣a,则滤渣a中可能含有硫酸钡、氢氧化镁和碳酸钙,加入足量的稀盐酸充分反应,滤渣全部溶解,碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳,氢氧化镁和稀盐酸反应生成氯化镁和水,硫酸钡和稀盐酸不反应,假设1.4g滤渣a均为碳酸钙,碳酸钙和稀盐酸反应的关系式为3222 CaCO+2HCl=CaCl+H O+CO 10044,则1g碳酸钙完全反应生成0.44g二氧化碳,滤渣a的质量大于1g,说明滤渣a中含有氢氧化镁,故滤渣a的成分是CaCO3、Mg(OH)2;滤液中可能含有氢氧化钠,氯化钡,氢氧化钠和二氧化碳反应生成碳酸钠和水,碳酸钠和氯化钡反应生成碳酸钡和氯化钠,故白色沉淀b的成分是BaCO3。
中考化学综合题专练∶流程图含答案

一、中考初中化学流程图1.硫铁矿烧渣(主要成份Fe2O3、Fe3O4、FeO、SiO2等,铁的氧化物均能与盐酸反应,SiO2不与酸反应)是工业生产硫酸的废渣,利用硫铁矿烧渣制备铁红(Fe2O3)等产品的部分流程如图所示:(1)焙烧时C与O2不完全燃烧产生的气体都能将铁的多种氧化物还原成铁。
试写出该气体与Fe3O4反应的化学方程式__________。
(2)酸浸、过滤后滤液中的溶质主要是__________。
(填化学式)(3)在空气中煅烧FeCO3即FeCO3与空气中的O2反应生成Fe2O3和CO2,试写出该反应的化学反应方程式为:__________。
(4)若产品a的主要成分是K2SO4,得到产品a时加入的试剂X为__________。
由此判断在此条件下K2SO4的溶解度__________NH4Cl的溶解度(选填“<”或“>”或“=”)。
(5)可选用下列__________(填字母)洗涤产品a。
A.KCl饱和溶液 B.水 C.饱和K2SO4溶液.【答案】4CO + Fe3O43Fe + 4 CO2FeSO44FeCO3 + O2 2Fe2O 3 + 4CO2KCl<C【解析】(1)根据碳不完全燃烧产生的气体是一氧化碳,一氧化碳与四氧化三铁在高温的条件下反应生成铁和二氧化碳解答;(2)根据酸浸后发生的反应考虑生成物;(3)根据书写方程式的原则书写;(4)根据反应流程分析解答;(5)根据产品a的主要成分是硫酸钾,所选试剂能溶解其他物质但不能溶解硫酸钾解答。
(1)C与氧气不完全燃烧生成一氧化碳,一氧化碳与Fe3O4反应生成物是铁和二氧化碳,化学方程式为Fe3O4+4CO 高温3Fe+4CO2;(2)酸浸后发生的反应是铁与硫酸反应生成硫酸亚铁和氢气,所以酸浸、过滤后滤液中的溶质主要是硫酸亚铁(FeSO4);(3)在空气中煅烧FeCO3的反应物是FeCO3和氧气,生成物是Fe2O3与CO2,反应条件是高温,所以方程式为4FeCO3+O2高温2Fe2O3+4CO2;(4)由流程图可以看出酸浸、过滤后滤液中的溶质主要是硫酸亚铁,硫酸亚铁和碳酸氢铵反应生成碳酸亚铁和硫酸铵,过滤后反应Ⅱ中硫酸铵与X 反应生成硫酸钾和氯化铵,因此加入的X应为氯化钾(KCl),要过滤得到硫酸钾,说明在此条件下硫酸钾的溶解度小于氯化铵的溶解度;(5)产品a的主要成分是硫酸钾,所选试剂必须能溶解其他物质但不能溶解硫酸钾,故选C 。
九年级化学 中考复习专题 化学工艺流程图 习题练习(包含答案)

化学工艺流程图题题型之一金属资源的回收与利用1.废旧电路板中主要含有塑料、铜和锡(Sn)等,为实现对锡的绿色回收,设计如下工艺流程:已知:Sn+SnCl4===2SnCl2。
(1)塑料属于___________(填“有机物”或“无机物”)。
(2)SnCl2中锡元素的化合价是________。
(3)铜的金属活动性比锡的________(填“强”或“弱”);固体A中一定含有的金属元素是________。
(4)写出步骤②发生反应的化学方程式______________________,其基本反应类型是____________。
(5)相比于直接焚烧废旧电路板回收金属,该工艺的主要优点是___________(回答一点)。
2.金属钛广泛用于航空航天工业、化工、医疗等领域。
用钛铁矿(主要成分为FeTiO3)制取钛并获得副产品A的主要工艺流程如图1所示:图1图2请回答下列问题:(1)构成金属钛的微粒是_______(填“分子”“原子”或“离子”),H2TiO3中钛元素的化合价为______。
(2)反应②需持续通入氩气,氩气的作用是______________________。
(3)反应③的产物除红色固体A外,还有两种组成元素相同且相对分子质量相差16的气体,则该反应的化学方程式为______________________。
(4)反应①②③中属于分解反应的是___________。
(5)对反应③进行改进,可直接生产锂离子电池的电极材料LiFePO4,工艺流程如图2所示。
写出“高温煅烧”由FePO4制备LiFePO4的化学方程式_________________________________。
3.某金属冶炼厂的管道烟泥中含有少量铜、锌、硫等单质。
现欲回收铜和锌,并对硫进行环保处理,主要步骤如图所示:已知:加热的条件下,Zn、Cu都可以与氧气反应生成相应的金属氧化物。
(1)烟泥最初处理需要除油污,用洗涤剂除油污的过程中发生了_________现象。
最新中考化学试题汇编:工艺流程题(含解析)

工艺流程题1.(2022•安徽)硫酸亚铁晶体是重要的化学试剂。
传统制备方法是用铁屑与稀硫酸反应,因铁屑中含有硫、磷等杂质,与稀硫酸反应会产生刺鼻、呛人的有毒气体。
某科技小组改用铁屑与硫酸铜溶液反应制备硫酸亚铁晶体,流程如下:(1)步骤①中反应的化学方程式为___________。
(2)操作Ⅰ的名称是_______。
步骤②涉及到蒸发,蒸发时必需的仪器有铁架台(含铁圈)、酒精灯、玻璃棒、_______。
(3)用硫酸铜溶液代替稀硫酸制备硫酸亚铁晶体,优点是________。
答案44=Fe+CuSO FeSO +Cu ;过滤;蒸发皿;不产生有毒气体,安全环保。
【解析】(1)铁和硫酸铜反应会生成硫酸亚铁和铜,方程式为44=Fe+CuSO FeSO +Cu ;(2)经过操作一后得到溶液和固体,分离液体和固体的操作是过滤,故填:过滤;蒸发中除用铁架台、酒精灯、玻璃棒,还需要蒸发皿,故填:蒸发皿;(3)从题目中可了解到“铁屑中含有硫、磷等杂质,与稀硫酸反应会产生刺鼻、呛人的有毒气体”,而使用硫酸铜时,硫酸铜不与硫或磷反应,因此不会有有毒气体产生,安全环保,故填:不产生有毒气体,安全环保;2.(2022•北京)CuO 是某种无机胶黏剂的组分之一,制备的部分流程如下图。
已知:CuO 难溶于水。
(1)反应釜中发生的反应有:①42422NaOH+CuSO =Na SO +Cu(OH)↓ ②22ΔCu(OH)CuO+H O ,其中属于复分解反应的是____(填“①”或“②”)。
(2)过滤器分离出的滤液中一定含有的溶质是__________。
答案①Na2SO4【解析】(1)①42422NaOH+CuSO =Na SO +Cu(OH)↓,反应符合两种化合物相互交换成分生成另两种化合物,属于复分解反应;②22ΔCu(OH)CuO+H O ,反应符合一种物质生成两种物质,符合一变多,属于分解反应,故属于复分解反应的是①。
(2)反应釜中生成硫酸钠、氧化铜和水,故过滤器分离出的滤液中一定含有的溶质是硫酸钠,化学式为Na2SO4。
中考化学流程图综合经典题及详细答案

一、中考初中化学流程图1.《天工开物》中介绍了锌的冶炼方法:把炉甘石(ZnCO 3)和煤炭饼装入炼锌罐(如下图所示),泥封,“其底铺薪,发火煅红”“冷定毁罐取出”。
(已知:锌的熔点 为 419℃,沸点为 907℃)(1)反应区中,ZnCO 3 分解生成 ZnO 和另一种氧化物,反应的化学方程式为_________。
C 与 ZnO 发生置换反应得到 Zn ,反应中化合价升高的元素是_____。
(2)冷凝区中,锌由气态转化为液态,理论上该区应控制的温度范围是_____℃。
(3) “冷定”后方能“毁罐”取锌、从化学变化角度解释其原因:_____。
【答案】ZnCO 3加热ZnO +CO 2↑ C (或“碳”) 419~907 防止生成的锌在较高温度下又被氧化成氧化锌(或“2Zn +O 2加热2ZnO”)【解析】【分析】 碳酸锌高温生成氧化锌和二氧化碳,碳和氧化锌高温生成锌和二氧化碳,锌和氧气加热生成氧化锌。
【详解】(1)反应区中,ZnCO 3 分解生成 ZnO 和二氧化碳,反应的化学方程式为32ZnCO ZnO+CO 加热。
C 与 ZnO 发生置换反应得到Zn 和二氧化碳,故反应中化合价升高的元素是碳。
(2)锌的熔点为 419℃,沸点为 907℃,冷凝区中,锌由气态转化为液态,故该区应控制的温度范围是419~907℃。
(3)锌在较高温度被氧化成氧化锌,“冷定”后方能“毁罐”取锌,原因是防止生成的锌在较高温度下又被氧化成氧化锌。
2.酸、碱、盐在生产和生活中有广泛的应用。
(1)氢氧化钠、氢氧化钙具有相似的化学性质,是因为它们的水溶液中均含有_____(填离子符号)。
(2)同学们想除去粗盐中含的泥沙等不溶性杂质和含有的少量氯化镁、氯化钙、硫酸钠可溶性杂质,进行了探究活动:实验一:除去粗盐中不溶性杂质实验二:从滤液1中提取氯化钠固体①实验一中的操作I是_____,实验二中蒸发结晶操作中玻璃棒的作用为_____。
中考化学流程图的综合题试题及详细答案
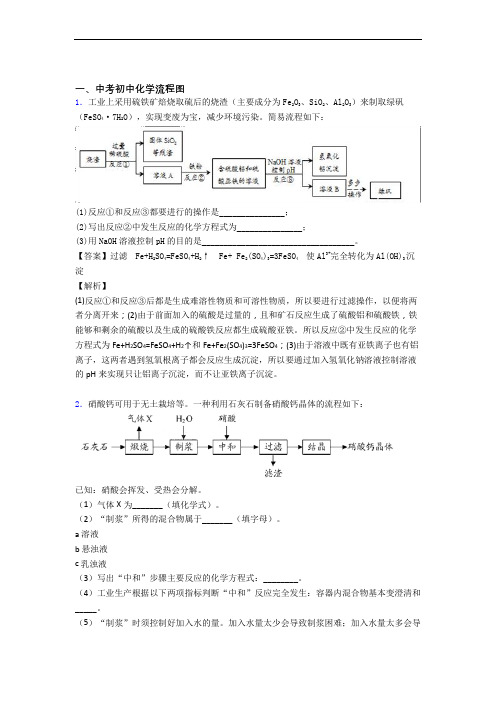
一、中考初中化学流程图1.工业上采用硫铁矿焙烧取硫后的烧渣(主要成分为Fe2O3、SiO2、Al2O3)来制取绿矾(FeSO4·7H2O),实现变废为宝,减少环境污染。
简易流程如下:(1)反应①和反应③都要进行的操作是_______________;(2)写出反应②中发生反应的化学方程式为_______________;(3)用NaOH溶液控制pH的目的是___________________________________。
【答案】过滤Fe+H2SO4=FeSO4+H2↑ Fe+ Fe2(SO4)3=3FeSO4使Al3+完全转化为Al(OH)3沉淀【解析】(1)反应①和反应③后都是生成难溶性物质和可溶性物质,所以要进行过滤操作,以便将两者分离开来;(2)由于前面加入的硫酸是过量的,且和矿石反应生成了硫酸铝和硫酸铁,铁能够和剩余的硫酸以及生成的硫酸铁反应都生成硫酸亚铁。
所以反应②中发生反应的化学方程式为Fe+H2SO4=FeSO4+H2↑和Fe+Fe2(SO4)3=3FeSO4;(3)由于溶液中既有亚铁离子也有铝离子,这两者遇到氢氧根离子都会反应生成沉淀,所以要通过加入氢氧化钠溶液控制溶液的pH来实现只让铝离子沉淀,而不让亚铁离子沉淀。
2.硝酸钙可用于无土栽培等。
一种利用石灰石制备硝酸钙晶体的流程如下:已知:硝酸会挥发、受热会分解。
(1)气体X为_______(填化学式)。
(2)“制浆”所得的混合物属于_______(填字母)。
a 溶液b 悬浊液c 乳浊液(3)写出“中和”步骤主要反应的化学方程式:________。
(4)工业生产根据以下两项指标判断“中和”反应完全发生:容器内混合物基本变澄清和_____。
(5)“制浆”时须控制好加入水的量。
加入水量太少会导致制浆困难;加入水量太多会导致_。
(6)若省去“制浆”步骤也可制得硝酸钙。
但硝酸利用率会降低、同时会产生污染气体NO x 。
产生NO x 的原因是______。
中考化学 流程图 综合题含详细答案

一、中考初中化学流程图1.Ⅰ.黄铜是Zn以主要添加元素的铜合金。
黄铜渣中约含Zn:7%、ZnO:31%、Cu:50%、CuO:5%,其余为杂质。
处理黄铜渣可得到硫酸锌,其主要流程如下(杂质不溶于水、不参与反应):已知:ZnO+H2SO4=ZnSO4+H2O; CuO+H2SO4=CuSO4+H2O(1)步骤Ⅰ中产生气体的化学方程式为___________________。
(2)溶液A中的金属阳离子有__________(填化学式)(3)步骤Ⅰ、Ⅱ中均包含的操作名称为___,此操作和步骤Ⅲ中的蒸发操作都要用到的玻璃仪器是____。
(4)溶液A_____(填“大于”、“小于”或“等于”)溶液C的质量。
Ⅱ.在探究金属活动性的实验课上,同学们把打磨光亮的铝片插入硫酸铜溶液中,过一会儿,发现了一个“意外现象”:在铝片表面看到有红色固体析出的同时,还看到有少量的气泡冒出,写出生成红色固体的化学方程式___________________.(提出问题)该气体是什么呢?(猜想与假设)猜想一:O2猜想二:H2猜想三:CO2猜想四:SO2同学们经过讨论,一致认为猜想三不成立,理由是_____________________.(实验验证)(5)有同学闻了一下该气体,发现无气味,证明猜想四也不成立,理由是___________.(6)将产生的气体经验纯后,用导管导入到点燃的酒精灯火焰上,气体安静燃烧,产生淡蓝色火焰.(实验结论)__________________.(反思与交流)CuSO4溶液可能显_______性(填“酸”或“碱”或“中”).【答案】Zn+H2SO4=ZnSO4+H2↑Zn2+、Cu2+过滤玻璃棒小于2Al+3CuSO4=3Cu+Al2(SO4)3反应物中不含碳元素二氧化硫有刺激性气味猜想一不成立,猜想二成立酸【解析】Ⅰ. (1)氧化锌和氧化铜分别与稀硫酸反应生成硫酸锌、硫酸铜和水,没有气体产生;而锌与稀硫酸反应生成硫酸锌和氢气,化学方程式为:Zn+H2SO4=ZnSO4+H2↑;(2)锌与稀硫酸反应生成硫酸锌和氢气,氧化锌与硫酸反应生成硫酸锌和水,氧化铜与硫酸反应生成硫酸铜和水,其中的金属阳离子是锌离子和铜离子;(3)由图可知,操作Ⅰ过滤除去铜和杂质,操作Ⅱ过滤是除去锌和置换出的铜;过滤和蒸发操作中均用到玻璃棒这种玻璃仪器;(4)A到C的过程中发生的反应是:Zn+CuSO4=Cu+ZnSO4,160 161由此可见溶液的质量增重了,溶液A小于溶液C的质量;Ⅱ.铝和硫酸铜反应生成硫酸铝和铜,化学方程式为:2Al+3CuSO4=3Cu+Al2(SO4)3;【猜想与假设】化学反应前后,元素种类不变,所以经过讨论,一致认为猜想三不成立,理由是:反应物中不含碳元素;【实验验证】(5)有同学闻了一下该气体,发现无气味,证明猜想四也不成立,理由是:二氧化硫有刺激性气味;氧气有助燃性,氢气有可燃性,所以(6)将产生的气体经验纯后,用导管导入到点燃的酒精灯火焰上,气体安静燃烧,产生淡蓝色火焰。
全国各地中考化学分类:流程图综合题汇编及详细答案

一、中考初中化学流程图1.高纯氧化铁可作为现代电子工业的材料,以下是硫铁矿烧渣(主要成分为Fe 2O 3、FeO 、SiO 2)为原料制备高纯氧化铁(Fe 2O 3)的生产流程示意图:[(NH 4)2CO 3溶液呈碱性,40℃以上时(NH 4)2CO 3分解]。
(1)实验室中,操作Ⅰ、操作Ⅱ用到的玻璃仪器玻璃棒、_______、烧杯等。
(2)写出通入CO 后所发生反应的化学方程式_______(任意写一个)。
(3)在该生产流程中当加入(NH 4)2CO 3后,应该控制的条件是 ______ 。
(4)滤液Ⅱ中可回收的物质在农业上可做 _____(5)写出在空气中煅烧FeCO 3的化学方程式_____。
【答案】漏斗 3CO+Fe 2O 3高温2Fe+3CO 2(或FeO+CO 高温Fe+CO 2) 温度控制在40℃以下(或控制溶液的酸碱度) 氮肥或肥料 322324FeCO +O 2Fe O +4CO 高温【解析】【分析】【详解】 (1)操作Ⅰ、操作Ⅱ都是将固体与液体分开,操作为过滤,过滤操作用到的玻璃仪器玻璃棒、漏斗、烧杯等。
(2)高温条件下,氧化铁和一氧化碳反应生成铁和二氧化碳,氧化亚铁和一氧化碳反应生成铁和二氧化碳,反应的化学方程式为:Fe 2O 3+3CO 高温2Fe+3CO 2,FeO+CO 高温Fe+CO 2。
(3)因为40℃以上时(NH 4)2CO 3分解,因此加入(NH 4)2CO 3后,温度控制在40℃以下;(NH 4)2CO 3溶液呈碱性,所以要控制酸碱性。
(4)滤液Ⅱ中可回收的产品中含有硫酸铵,在生活中可作为氮肥。
(5)在空气中煅烧FeCO 3,是碳酸亚铁和氧气在高温下生成二氧化碳和氧化铁,对应的化学反应方程式4FeCO 3+O 2高温2Fe 2O 3+4CO 2。
故答案为:(1)漏斗;(2)3CO+Fe 2O 3高温2Fe+3CO 2(或FeO+CO 高温Fe+CO 2);(3)温度控制在40℃以下(或控制溶液的酸碱度);(4)氮肥或肥料;(5)4FeCO 3+O 2 高温2Fe 2O 3+4CO 2。
全国各地中考化学分类:流程图综合题汇编及答案解析

一、中考初中化学流程图1.二氧化氯(ClO2)可用于自来水消毒。
以粗盐为原料生产ClO2的工艺主要包括:①反应Ⅰ是粗盐除杂;②反应Ⅱ是特殊条件下电解NaCl溶液制NaClO3;③反应Ⅲ是ClO2的制取。
其中反应Ⅲ制取ClO2的化学方程式为:2NaClO3+4HCl═2ClO2↑+Cl2↑+2NaCl+2H2O。
工艺流程如图,(1)加入过量氢氧化钠的目的是________。
(2)过量的试剂X是____(填化学式),操作A的名称是_______。
(3)求出沉淀ClO2中Cl的化合价为_______。
(4)加入适量HCl除为了满足电解时的微酸性外,还能除去溶液中的杂质离子,请写出其中所发生的中和反应的化学方程式:___________。
(5)该流程中可循环利用的物质是水和________。
【答案】除尽氯化镁 Na2CO3过滤 +4 NaOH+HCl=NaCl+H2O 氯化钠。
【解析】【分析】【详解】(1)氯化镁和氢氧化钠反应生成氢氧化镁沉淀和氯化钠,因此加入过量氢氧化钠的目的是除尽氯化镁。
故填:除尽氯化镁。
(2)碳酸钠和氯化钙反应生成碳酸钙沉淀和氯化钠,过量的试剂X是Na2CO3,用来除去溶液中的氯化钙;操作A的名称是过滤,通过过滤能够把液体和固体分离。
故填:Na2CO3;过滤。
(3)设ClO2中Cl元素的化合价为x,氧元素的化合价是-2,根据题意有:x+(-2)×2=0,x=+4。
故填:+4。
(4)稀盐酸和碳酸钠反应生成氯化钠、水和二氧化碳,属于复分解反应,稀盐酸和氢氧化钠反应生成氯化钠和水,属于中和反应,稀盐酸和氢氧化钠反应的化学方程式为:NaOH+HCl═NaCl+H2O。
故填:NaOH+HCl═NaCl+H2O。
(5)该流程中可循环利用的物质是水和氯化钠。
故填:氯化钠。
2.某化工厂用废硫酸制备K2SO4的流程如下:(l)生产上将CaCO3研成粉末的目的是_____;写出反应①的化学方程式:_____,操作I的名称是_____。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
2018中考化学试题汇编:考点36 工艺流程图题1. (2018•湖北黄冈)金属钨(W)可做白炽灯泡的灯丝。
用黑钨矿[主要含有FeWO4(钨酸亚铁)]制得金属钨(W)的工艺流程如下图所示:其主要反应原理如下:①4FeWO4+4Na2CO3+O24Na2WO4+2Fe2O3+4CO2②Na2WO4+2HCl(热浓)=H2WO4+2NaCl③H2WO4H2O+WO3④3H2+WO3W+3H2O下列说法不正确的是()A. 反应③属于分解反应B. 反应①②③④的产物都有氧化物C. 反应①④中有元素的化合价发生改变D. 为加快反应的速率,可将黑钨矿石碾成粉末【答案】B【解析】A、反应③是由一种物质生成两种物质,属于分解反应,故正确;B、由①②③④的化学方程式可知,在反应②中的生成物中没有氧化物,故错误;C、反应①中铁、氧的化合价从+2、0变成+3、-2;反应④中氢、钨的化合价从0、+6变成+1、0,故正确;D、将黑钨矿石碾成粉末,可增大物质间接触面积,反应速率加快,故正确。
故选B。
2.(2018•呼和浩特)实验室中同学们进行了如图所示实验,成功探究出了久置氢氧化钠固体的变质情况。
下列说法正确的是()A.甲溶液可以选择稀盐酸或CaC12溶液(查阅资料得知:CaC12溶液显中性)B.若Ⅱ、Ⅲ均有明显现象,则说明样品部分变质C.D物质可能是气体,也可能是沉淀D.溶液B中的溶质一定只含有NaOH和甲【分析】根据变质后的氢氧化钠溶液中含有碳酸钠,碳酸钠、氢氧化钠均显碱性,探究久置氢氧化钠固体的变质情况,要证明固体中含有碳酸钠、氢氧化钠,碳酸钠、氢氧化钠均显碱性,检验氢氧化钠的存在应先排除碳酸钠的干扰,进行分析判断。
【解答】解:A、甲溶液不能选择稀盐酸,因为氢氧化钠、碳酸钠均能与稀盐酸反应生成氯化钠溶液,溶液B为氯化钠溶液和盐酸的混合溶液,滴加酚酞溶液不变色,无法确定溶液中是否含有氢氧化钠,故选项说法错误。
B、甲溶液可以选用氯化钙溶液,若Ⅱ、Ⅲ均有明显现象(现象分别是产生白色沉淀、酚酞溶液变红色),分别说明含有碳酸钠、氢氧化钠,则说明样品部分变质,故选项说法正确。
C、由A选项的分析,D物质是沉淀,故选项说法错误。
D、溶液B中的溶质中一定含有碳酸钠与氯化钙反应生成的氯化钠,故选项说法错误。
故选:B。
3.(2018•呼和浩特)黄铁矿的主要成分为二硫化亚铁(FeS2),工业上可利用黄铁矿煅烧的产物冶炼铁和生产浓硫酸,其工业流程如图:下列说法错误的是()A.反应②不是置换反应,反应③④为化合反应B.反应①中各元素的化合价均发生了改变C.该工业生产过程产生的废气中的SO2可以用熟石灰溶液吸收D.向制得的100克98%的浓硫酸中加入100克蒸馏水,配制49%的稀硫酸【分析】A、反应②是一氧化碳与氧化铁反应生成铁和二氧化碳,反应③④为二氧化硫与氧气反应生成三氧化硫、三氧化硫与氧气反应生成硫酸,进行分析判断。
B、根据反应①是二硫化亚铁(FeS2)与氧气反应生成氧化铁和二氧化硫,进行分析判断。
C、根据二氧化硫能与碱溶液反应,进行分析判断。
D、根据浓硫酸的稀释方法,进行分析判断。
【解答】解:A、反应②是一氧化碳与氧化铁反应生成铁和二氧化碳,该反应的反应物均为化合物,不属于置换反应;反应③④为二氧化硫与氧气反应生成三氧化硫、三氧化硫与氧气反应生成硫酸,均属于化合反应;故选项说法正确。
B、反应①是二硫化亚铁(FeS2)与氧气反应生成氧化铁和二氧化硫,铁、硫、氧元素的化合价均发生了改变,故选项说法正确。
C、二氧化硫能与碱溶液反应,该工业生产过程产生的废气中的SO2可以用熟石灰溶液吸收,故选项说法正确。
D、稀释浓硫酸时,要把浓硫酸缓缓地沿器壁注入水中,同时用玻璃棒不断搅拌,以使热量及时地扩散;切不可把水注入浓硫酸中,应将制得的100克98%的浓硫酸加入到水中,故选项说法错误。
故选:D。
4. (2018•四川德阳)氢氧化镁是一种重要的化工原料,某矿石由MgO、Fe2O3、CuO和SiO2组成。
用它制备氢氧化镁的流程示意图如下:部分金属阳离子以氢氧化物形成沉淀时溶液的pH见下表:沉淀物Fe(OH)3Cu(OH)2Mg(OH)2开始沉淀 1.9 4.2 9.1完全沉淀 3.2 6.7 11.1(1)熟石灰主要成分的化学式是____________。
(2)溶液A中的阳离子是___________________(填离子符号)。
(3)沉淀C的成分是_____________________。
(4)溶液B与熟石灰反应的化学方程式是____________________________________。
【答案】(1). Ca(OH)2(2). Mg2+、Fe3+、Cu2+、H+(3).Fe(OH)3、Cu(OH)2(4). MgCl2+Ca(OH)2═Mg(OH)2↓+CaCl2【解析】(1)熟石灰的主要成分是氢氧化钙,化学式为Ca(OH)2;(2)矿石中加入稀盐酸,可以与氧化镁、氧化铁和氧化铜反应分别生成氯化镁、氯化铁和氯化铜,由于盐酸过量,故也含有稀盐酸,故溶液中的阳离子有Mg2+、Fe3+、Cu2+、H+;(3)pH控制在7-9时,溶液中的铁离子和铜离子会生成氢氧化镁沉淀和氢氧化铜沉淀;(4)溶液B中的主要成分是氯化镁,故氯化镁与氢氧化钙反应生成氢氧化镁沉淀和氯化钙,故反应方程式为MgCl2+Ca(OH)2═Mg(OH)2↓+CaCl2;5.(2018•安徽)废旧电路板中主要含有塑料、铜和锡(Sn)等,为实现对其中锡的绿色回收,某工艺流程如下。
已知:Sn+SnCl4=2SnCl2(1)SnCl4中锡元素的化合价是+4。
(2)铜的金属活动性比锡的弱(填“强”或“弱”),固体A中一定含有的金属元素是Cu。
(3)写出步骤②发生反应的化学方程式2SnCl2SnCl4+Sn。
(4)相比于直接焚烧废旧电路板回收金属,该工艺主要优点是保护环境(回答一点即可)。
【分析】根据物质的性质结合流程图进行分析解答,在化合物中各元素正负化合价的代数和为零,根据化学方程式的书写方法以及流程的特点进行分析解答即可。
【解答】解:(1)SnCl4中氯元素的化合价为﹣1,故锡元素的化合价为+4,故填:+4。
(2)铜的金属活动性比锡的弱,因此加入铜不能与SnCl4反应,故固体A中一定含有的金属元素是Cu,故填:弱;Cu。
(3)步骤②中SnCl2通电分解生成SnCl4和Sn,发生反应的化学方程式为2SnCl2SnCl4+Sn,故填:2SnCl2SnCl4+Sn。
(4)相比于直接焚烧废旧电路板回收金属,该工艺主要优点是保护环境,故填:保护环境。
【点评】本题考查的是常见的物质的制备的知识,完成此题,可以依据已有的物质的性质进行。
6.(2018•广西)碳酸钡是一种重要的化工产品,某厂用含二氧化硅杂质的碳酸钡原料生产碳酸钡产品,采用了以下的工艺流程:(1)为节约成本,过程中的生成物可直接应用于流程的是二氧化碳,加入过量的盐酸的目的是使碳酸钡完全反应为氯化钡(2)向氯化钡溶液中加入过量的氢氧化钾并通入二氧化碳,其中能生成碳酸钡的方程式是BaC12+2KOH+CO2=BaCO3↓+2KCl+H2O。
(3)溶液A中溶质的成分,可能的组合有KOH、KCl、BaCl2;KOH、KCl;KOH、KC1、K2CO3。
(4)操作3包括的两个操作是洗涤、干燥。
【分析】根据给出的转化关系对应的过程分析每个对应的问题,或者直接分析每个问题,从给出的信息中找对应的信息。
【解答】解:(1)根据可循环利用的物质的特点,既是某反应的生成物又是另外反应的反应物,图中向碳酸钡中加盐酸产生二氧化碳,又可以参与到制取碳酸钡的反应中,所以答案为:二氧化碳。
加盐酸过量的目的是使碳酸钡完全溶解,所以答案为:使碳酸钡完全溶解并全部转化为氯化钡;(2)向氯化钡溶液中加入过量的氢氧化钾并通入二氧化碳,其中二氧化碳与氢氧化钾生成碳酸钾和水,碳酸钾再和氯化钡发生反应,发生的反应为:BaC12+2KOH+CO2=BaCO3↓+2KCl+H2O;所以答案为:BaC12+2KOH+CO2=BaCO3↓+2KCl+H2O;(3)原料与过量的盐酸反应后的溶液中含有的溶质有氯化氢、氯化钡,在得到的溶液中加入过量氢氧化钾溶液和二氧化碳,由于氢氧化钾过量,所以溶液A 中一定含有氢氧化钾。
其中氢氧化钾先和氯化氢发生中和反应,此时溶液中不含氯化氢,只含氢氧化钾、氯化钾、氯化钡,再跟二氧化碳反应:①二氧化碳少量时,生成的碳酸钾不足以将氯化钡反应完,所以此时溶液中的溶质为:KOH、KC1、BaCl2;②二氧化碳足量时,生成的碳酸钾恰好与氯化钡完全反应,此时溶液中的溶质为:KOH、KC1;③二氧化碳过量时,生成的碳酸钾在将氯化钡反应完之后还有剩余,此时溶液中的溶质为:KOH、KC1、K2CO3;(4)经过操作2过滤后得到固体A和溶液A,其中固体A为碳酸钡,而过滤得到的固体表面还残留有少量的溶液A,所以要先洗涤沉淀然后干燥得到产品。
所以答案为:洗涤、干燥故答案为:(1)二氧化碳;使碳酸钡完全反应为氯化钡;(2)BaC12+2KOH+CO2=BaCO3↓+2KCl+H2O;(3)KOH、KCl、BaCl2;KOH、KCl;KOH、KC1、K2CO3;(4)洗涤、干燥;【点评】读图,从中获得解答题目所需的信息,所以在解答题目时先看解答的问题是什么,然后带着问题去读给出的图进而去寻找解答有用的信息,这样提高了信息扑捉的有效性。
解答的问题实际上与复杂的转化图相比,其实很简单很基础,或者可以说转化图提供的是情境,考查基本知识。
7.(2018•天津)(1)如图是利用海盐提取粗盐的过程:如图中①是蒸发池(填“蒸发”或“冷却”)。
(2)粗盐中含有少量CaCl2、MgCl2、Na2SO4和泥沙,某同学将该粗盐样品进行提纯。
①将样品加适量水溶解,然后进行过滤,除去泥沙等难溶性杂质,得到澄清溶液;②向所得的澄清溶液中依次加入稍过量的BaCl2溶液、NaOH溶液和碳酸钠溶液,除去生成的沉淀后,再滴加稍过量的稀盐酸,得到较纯净的NaCl溶液;③蒸发溶液,得到较多氯化钠固体时停止加热,他注意到不能立即把蒸发皿直接放在实验台上,以免烫坏实验台。
(3)另一同学用所得的氯化钠和蒸馏水配制溶质质量分数为6%的氯化钠溶液。
配制步骤:①称量和量取②溶解③计算④装入试剂瓶贴好标签。
配制上述溶液的正确顺序是③①②④(填序号)。
【分析】(1)根据氯化钠的溶解度受温度影响变化不大,可用蒸发结晶的方法进行分离进行分析;(2)①根据过滤是分离固体与液体的一种操作进行分析;②根据碳酸钠和氯化钙反应生成碳酸钙沉淀,和氯化钡反应生成碳酸钡沉淀等知识进行分析;③根据氯化钠溶液蒸发操作的仪器进行分析;(3)根据配制一定质量分数溶液的正确操作进行分析。
