仪器分析-极谱分析法和伏安分析法
第05章 伏安与极谱分析-2

氧化波方程 P77 de = 1/2 -0.0592/z*lg [(id-i) / i]
式中,i和id是负值
综合波方程 de = 1/2 +0.0592/z*lg [ (id)c -i) / i- (id)a ] (id)c为还原电流 (id)a为氧化电流
§5.1.4 应用
1.
定量分析
尤考维奇方程 id=ksc ks=607 zD1/2m2/3t1/6 尤考维奇常数 波高测量
Current goes to zero and then becomes anodic due to the reoxidation of the produced Fe(CN)64-. The anodic current peaks and then decreases as the accumulated Fe(CN)64- Is used up by the anodic reaction. The whole process is ended.
φ
pc
-φ
φ
pa
对可逆电极过程:
ip= K z3/2AD1/2v1/2c
ipa≈ipc,
φpc=φ1/2-1.11RT/zF φpa=φ1/2+1.11RT/zF Δφp=2.22RT/zF =φpa—φpc=56/z(mV) 经验表明,若z=1,Δφp通常在55-65mV。P96
二、应用
电极反应可逆性判断:
Cyclic Voltammogram {6.0 mM K3Fe(CN)6 and 1.0 M KNO3}
Between points D and F, the current decays. Current is reversed at point F but the current continues to be cathodic because the potentials are still negative enough to cause the reduction of Fe(CN)63-. Between H and I the potential becomes positive enough so that reduction of Fe(CN)63- can no longer occur.
第五章 伏安法和极谱分析法.

第五章伏安法和极谱分析法基本要求:1.掌握直流极谱法的基本原理及其不足之处2.掌握尤考维奇方程和极谱波方程3.理解单扫描极谱法、脉冲极谱法和阳极溶出伏安法灵敏度高的原因4.掌握循环伏安法的原理及应用伏安法(V oltammetry)和极谱分析法(Polarography)都是通过由电解过程中所得的电流-电位(电压)或电位-时间曲线进行分析的方法。
它们的区别在于伏安法使用的极化电极是固体电极或表面不能更新的液体电极,而极谱分析法使用的是表面能够周期更新的滴汞电极。
自1922年J.Heyrovsky开创极谱学以来,极谱分析在理论和实际应用上发展迅速。
继直流极谱法后,相继出现了单扫描极谱法、脉冲极谱法、卷积伏安法等各种快速、灵敏的现代极谱分析方法,使极谱分析成为电化学分析的重要组成部分。
极谱分析法不仅可用于痕量物质的测定,而且还可用于化学反应机理,电极动力学及平衡常数测定等基础理论的研究。
与两种电解过程相对应,极谱分析法也可分为控制电位极谱法(如直流极谱法、单扫描极谱法、脉冲极谱法和溶出伏安法等)和控制电流极谱法(如交流示波极谱法和计时电位法等)。
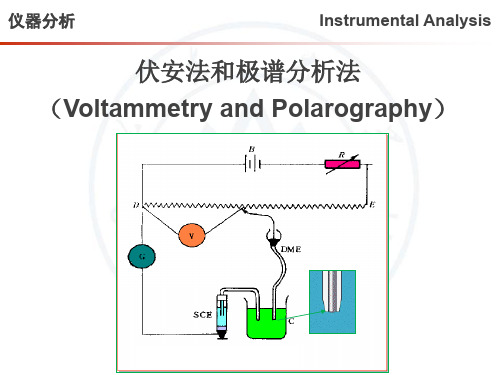
5.1 直流极谱法5.1.1 原理1.装置直流极谱法也称恒电位极谱法,其装置如图5-1所示。
它包括测量电压、测量电流和极谱电解池三部分。
图5-1 直流极谱装置示意图图5-2 饱和甘汞电极(a)和滴汞电极(b)现以测定Pb2+和Zn2+为例。
在电解池中安装一支面积小的滴汞电极,另一支面积大的饱和甘汞电极,如图5-2所示。
电解池中盛有浓度均为1.00 ×10-3mol·L-1Pb2+ 和Zn2+ 溶液以及0.1mol·L-1KCl(称为支持电解质,浓度比被测离子大50-100倍),并加入1%的动物胶(称为极大抑制剂)几滴。
电解前,通入N2除去电解液中溶解的O2。
按图5-1,以滴汞电极为阴极,饱和甘汞电极为阳极,在不搅拌溶液的静止条件下电解。
极谱与伏安分析法

2
/ Cd ( Hg )
0.059 [Cd ] lg s 2 [Cd ( Hg )]
• 式中s表示为滴汞电极的表面。 • 当继续增大外加电压,滴汞电极电位变负,电极表 面上镉离子被还原,造成电极表面上镉离子浓度的 减少,而使得其与本体溶液中镉离子浓度产生浓度 差造成极化。
极谱分析的基本原理
5、应用比较广,仪器较为简单、便宜,凡能在电极上起氧化― 还原反应的有机或无机物均可采用,有的物质虽不能在电极上 反应,但也可以间接测定。
一、直流极谱概述:
• 1 .极谱分析的一般装置: • 电解池由滴汞电极和甘汞 电极组成。滴汞电极毛细 管 内 径 为 约 0.05mm , 汞 滴有规则地滴落,增大外 加电压,记录电流 -- 电压 曲线。如图所示:
极谱分析的基本原理
• (2)极谱电流是完全受扩散控制的电解电流:(以 镉离子为例) • 当外加电压从零开始逐渐增大时,滴汞电极电位逐 渐变负,当达到镉离子的析出电位时,汞滴表面上 的镉离子开始还原形成镉汞齐,产生电解电流,此 时在汞滴表面上的镉离子与镉汞齐符合能斯特方程 式,即: 2 s
DME Cd
id it d 607 nD1 / 2 m 2 / 3t 1 / 6 c
0
• 式中t为滴下时间(s),即为尤考维奇公式。
二、极谱定量分析
二、极谱定量分析
• 2.影响扩散电流的主要因素: t id it d 607 nD1 / 2 m 2 / 3t 1 / 6 c 0 • id kc , 只有k 保持不变,极限扩散电流才与被测物质 浓度成正比。影响k 的因素主要有:
i 708 nD1 / 2 m 2 / 3 1 / 6 c
• 式中: n:电子转移数目 D:离子扩散系数(cm2/s) • m:汞流速(mg/s) :汞滴生长时间(s) c:被测物质的 浓度(mmol/L) • 在汞滴生长的周期内,由于电极(汞滴)面积不同,电流也是变 化的。当汞滴落下时,电流迅速降为0,然后上升至imax,电流起 伏较大,难于定量分析,因此需要测量整个滴下时间的平均扩散 电流, t
伏安法和极谱分析法

直流极谱法的局限性
1.用汞量和时间——直流极谱法获得一个极谱波需要数百滴汞,而
且施加直流电压的速度缓慢,约0.2V· min-1。费汞又费时间。
2 .分辨率 —— 直流极谱波呈台阶形,当两物质的半波电位差小于
200mV时两峰重叠,无法测量,因此分辨率差。
3.灵敏度——直流极谱法的充电电流大小与由浓度为10-5 mol· L-1的
极谱分析
悬汞电极 石墨电极 铂电极
伏安分析
伏安法 极谱法
通过电解过程中获得的电流-电位 或者电位-时间的曲线来进行分析 的方法。
伏安法-电位分析-电解分析区别:
方 法 测量物理量 电极面积 电位分析 电位、电动势 -电解分析 电重量、电量 大面积 伏安法 电 流 小面积
待测物 极 化 电流 浓度 无浓差极化 趋于 0 -尽量减小极化 有电流 较高浓度 完全浓差极化 有电流 稀溶液
因此
i ZFf ZFDA [M
Z
]-[ M
Z s
]
对于平面电极,扩散层厚度为
Dt
当电极电位负至产生极限扩散电流时,电极表面去极化剂 浓度趋近于零,若扣除残余电流,则
id zFAD
1/ 2
[M ] t
z
对于滴汞电极
汞滴面积
A 0.85m t
2 2 3 3
滴汞电极上扩散层厚度
(2) 充电电流(电容电流)
充电电流来 源于滴汞电 极与溶液界 面上双电层 的充电过程
滴汞电极的双电层
充电电流产 生的影响
限制了普通极 谱法的灵敏度
充电电流: ~10-7A ≈扩散电流(10-5mol· L-1)
消除方法
1)作图扣除 2)脉冲极谱
伏安和极谱分析法

电极上的电压,并记录电流的
变化——绘制i-U曲线。如左
图所示。例如:当以100-200 mV/min的速度对盛0.5mol/L CdCl2溶液施加电压时,记录 电压U对电流i的变化曲线。
-:未达分解电压U分,随外加电压U外的增加,只有一微小电流通过电
解池——残余电流ir
②-③:继续施加电压,达到Cd2+的分解电压后,滴汞表面的Cd2+便开始还 原,随即形成Cd(Hg),产生电解电流
因此只要测量波高就可求出C 1)、平行线法 通过极谱法的残余电流 部分和极限电流部分作两条 平行线,两线间的垂直距离h, 即为波高:
2)、三切线法 通过残余电流、极限电流和扩 散电流部分分别作三条切线:相交 于O和P点,过O点与P点作二条与横 坐标平行的平行线,两线间的垂直 距离为波高:此法方便,适用于不 同的波形,故应用广泛。
④-⑤:外加电压继续增加,C0趋近于0, (C-C0)趋近于C时,这时电流不再增加,达 到一个极限值──极限电流il,极谱波出现 一个平台,极限电流与残余电流之差称为 极限扩散电流id,也叫波高。 即: id =il-ir (极谱定量分析的基础) 并知: id = KC E1/2: 半波电位:扩散电流为极限扩散电流一 半时对应的电位 (极谱定性的依据).
伏安和极谱分析法
直流极谱法概述及极谱图
极谱定量分析基础 实验技术
新的极谱和伏安分析法
应用
一、什么是伏安和极谱分析法
伏安和极谱分析法是根据测量特殊形式电解过程中的电流― 电位(电势)或电流―时间曲线来进行分析的方法。是电分析化 学的一个重要分支。 1)采用一大一小的电极:大面积的去极化电极——参比电极;小 面积的极化电极; 2)电解是在静置、不搅拌的情况下进行。
郑大仪器分析第八章伏安法和极谱法

δ
(二)扩散层厚度变化 二
扫描电压较正(E0),电流为零,无浓差极化; 达到可还原物资的还原电压(E1)时,电极表面浓度迅速下降, 电流急速上升。 电极表面浓度降低至接近零(E2)后,溶液中的物质要从更远 处扩散到电极表面,扩散层变厚,虽然电压继续变负,电流 反而减小,形成尖峰状曲线。
i = k c io − c is分析中,外加电压 与两个电极电位的关系:
V = E工作 − E 参比 + iR
E工作与i的关系曲线为极谱图 电流较大时两电极系统中的参比电极将不能负荷,否则电位 不稳定,校正溶液的iR降也比较困难。因此,伏安分析多采 用三电极系统。除工作电极w、参比电极R外,还有辅助电极C (铂丝电极)对于V外回路:
溶液本体中,自 然对流或强制对 流,阻止了扩散 层进一步变厚, 所以电流不可能 衰减到零。
nFAD i1 / 2 c io i= π 1/ 2t 1/ 2
二、扩散控制伏安图
(一)扩散层厚度不变
所施加的电压值不是足够负时的情况见下图: 当电位值阶跃到E3及更负的电位值时,电极表面的O的浓度几 乎为零,这种情况叫做完全浓差极化。 对应的电流值: c io − c is
δ
一般,静止电极上 快扫时,得到峰形 极化曲线。
§8-3
直流极谱法
一、 极谱仪装置 电解池由滴汞电极和甘 汞电极组成。 上端为贮汞瓶,下接一 硅橡胶管,硅橡胶管的下 端接一毛细管(内径约为 0.05mm),汞自毛细管中 有规则地滴落。 滴汞电极称为极化电极, 参比电极为去极化电极。
改变电阻(电压) 改变电阻(电压) 电压 测量(记录电压 测量 记录电压) 记录电压
滴汞电极所以是极化电极,是因为滴汞电极的面积小, 在它表面起反应的离子数目少,电流就小;被测离子 的浓度小,电流也小,虽然电解电流这样小,但是在 极小的滴汞电极表面上,其电流密度却是很大的,所 以在滴汞电极上仍可造成显著的浓差极化,引起扩散 运动.
仪器分析:伏安分析法

1922 年 捷克科学家 海洛夫斯基 J.Heyrovsky 创立极谱法,1959年获Nobel奖 1934 年 尤考维奇 Ilkovic, 提出扩散电流理 论,从理论上定量解释了伏安曲线。 20世纪40年代以来 提出了各种特殊的伏安技 术。主要有:交流极谱法(1944年)、方波极 谱法(1952年)、脉冲极谱法(1958年)、卷 积伏安法(1970年) 20世纪40年代以来 主要采用特殊材料制备的 固体电极进行伏安分析。包括微电极、超微阵列 电极、化学修饰电极、纳米电极、金刚石电极、 生物酶电极、旋转圆盘电极等,结合各种伏安技 术进行微量分析、生化物质分析、活体分析。
极谱波的形成过程
在排除了其它电流的影响 以后,极限电流减去残余电 流后的值,称为极限扩散电 流,简称扩散电流(用id表 示)。1934年,Ilkovic推导 出了扩散电流方程式,证明 id与被测物的浓度成正比,它 是极谱定量分析的基础。当 电流等于极限电流的一半时 相应的滴汞电极电位,称为 半波电位(用E1/2表示)。半 波电位的概念是J.Heyrovsky 于1935年提出的,不同的物 质具有不同的半波电位,这 是极谱定性分析的根据。
电极表面存在 三种传质过程 1. 扩散 2. 电迁移 3. 对流
若电解采用微铂电极为 工作电极、且溶液不充 分搅拌时,会促使耗竭 区提前出现。这种现象 称极化现象。
浓差极化: 由于电解过程中电极表面离子浓 度与溶液本体浓度不同而使电极电位偏离平衡 电位的现象。 电化学极化: 因电化学反应本身的迟缓而造 成电极电位偏离可逆平衡电位的现象称为电化 学极化。 注意:由于电解过程中电极表面的浓差极化是 不可避免的现象,外加电压要严格控制工作电 极上的电位大小就要求另一支电极为稳定电位 的参比电极,实际上由于电解池的电流很大, 一般不易找到这种参比电极,故只能再加一支 辅助电极组成三电极系统来进行伏安分析。
Chapter 5 -伏安法和极谱分析法
de
2 s 0 . 0592 [ Pb ] ’ lg = 2 [Pb(Hg)]s
Instrumental Analysis
Voltammetry & Polarography
极谱波的形成
3. 极限扩散电流阶段: - 0.9 V < de< - 0.5 V
电极表面 [Pb2+]s:↓,→ 0
Instrumental Analysis
Voltammetry & Polarography
极谱分析中的干扰电流及其消除
X 迁移电流:电解池正负极对待测离子的静电吸引或排斥力
消除方法:在溶液中加入大量支持电解质
X
极谱极大(影响,消除) 电解开始后,电流随DME电位的增加而迅速增大的一个极
大值(畸峰),当 DME 电位变得更负时这种现象消失,电流下 降到正常的扩散电流值后趋于正常 消除方法:降低溶液流动性
Instrumental Analysis
பைடு நூலகம்
Voltammetry & Polarography
极谱定量分析的依据 - 扩散电流方程
Ilkovic(尤考维奇)方程式(DME):
1 2 2 3 1 6
id ,max 708 zD m t c
每滴汞寿命的最后时刻获得的最大扩散电流
id,max:最大扩散电流(μA)
证明 id与被测物的浓度成正比 ----- 极谱定量分析的基础
• 半波电位(φ1/2):电流等于极限扩散电流一半所对应的滴 汞电极电位(1935,J. Heyrovsky)
• 不同的物质具有不同的半波电位:极谱定性分析的根据
(1922年,极谱分析最早由捷克著 名物理化学家J. Heyrovsky创立, Nobel Prize in Chemsitry, 1959)
90359-仪器分析-第十五章 伏安和极谱法

[Cd 2 ]
de
(Cd )
2
[Cd (Hg)]
破坏了溶液中Cd2+浓度的均 匀性,电极表面附近的Cd2+ 浓度Cs低于溶液中的Cd2+浓
度C0,出现浓差极化现象.
b-c段
§ 10.3 直流极谱法
浓差极化的结果,使得Cd2+ 不断地由溶液中向滴汞 电极表面扩散.扩散过 来的Cd2+在电极表面不 断被还原.
扩散电流与扩散速度成正比,
lg 0.059
[Cd 2 ]
de
(Cd )
2
[Cd (Hg)]
而扩散速度与扩散层中 的浓度梯度成正比.
i C0 CS
i K (C0 C S )
c-d段
§ 10.3 直流极谱法
当外加电压继续增加,使 滴汞电极电位负到一 定的数值,此时电解 电流到达一个稳定值, 而扩散电流继续上升.
2 伏安曲线
§ 10.2 扩散电流理论
3 极限扩散电流
§ 10.2 扩散电流理论
对于反应 O+ne- = R, 要获得其极限扩散电流,需要求 解线性扩散方程式
c(x,t) D 2c(x,t)
x
x2
初始条件:t = 0 co cob
边界条件:t > 0 x 0
x
cos 0
co cob
解线性偏微分方程,得
-+-++-++--
充电电流
§ 10.3 直流极谱法
• 滴汞电极的表面积是不断改变的,必须连续地向汞滴 充以正电或负电,才能使其表面具有相当于该电位时 所应有的电荷密度值,形成连续不断的充电电流.
• 充 电 电 流 约 为 10-7A 数 量 级 , 相 当 于 浓 度 为 l0-5 mol·L-1物质所产生的扩散电流,限制普通极谱法的 灵敏度.
伏安和极谱分析法

1.残余电流
2.迁移电流 3.极谱极大 4.氧波 5.叠波、前波和氢波 三、定量分析方法
液相传质的三种基本方式 (1).扩散(Diffusion) 当溶液中粒子存在浓度梯度时,这种粒 子从高浓度向低浓度的移动过程。由于电极 反应造成的这种现象,成为“浓差极化”。 显然,这是溶质相对溶剂的运动。 2.电迁移(migrition) 在电场作用下,荷正电粒子向负极移动, 荷负电粒子向正极移动。 消除迁移电流的方法:通常是溶液中加入大 量支持电解质(或称惰性电解质),如KCl, NH4Cl和KNO3等 一般支持电解质的浓度要 比被测物质浓度达50~100倍。 3.对流(convection) 粒子随着流动的液体 而移动。显然,这是溶液中的溶质和溶剂同 时移动。有两种形式:a.自然对流 b.强制 对流。保持溶液静止,可消除对流电流。
D为扩散系数,单位为cm2/s,δ 为扩散层厚度。 由Fick第二定律,可求出线性扩散的扩散层厚 度为
Dt
δ
x
则得,极限扩散电流方程, Cottrell方程:
C id nFAD Dt
2.滴汞电极上的扩散电流-Ilkoviĉ方程
1934年,尤考维奇推导出滴汞电极上的极限扩散电流近似公式.滴汞电极上的 扩散电流是球形扩散,即溶液中的离子想球面电极中心方向进行的扩散。尤考维奇 在推导滴汞电极上的扩散电流方程时,有两点基本假设 (1)滴汞电极上可当作平 面电极来处理(扩散层很薄);(2)滴汞电极上存在对流(离子与电极的相对运 动)。推得滴汞电极上扩散层厚度为
负至-1.2 V)。 4. 汞能与许多金属生成汞齐,使其在滴汞电极上的析出电位变正,因而在碱性 溶液中,极谱法可测定碱金属、碱土金属离子。
第二节 极谱定量分析
一、扩散电流公式 1.平面电极上的扩散电流-Cottrell方程
5《仪器分析》伏安法和极谱分析法

在汞滴周围形成一扩散层,其厚度δ约0.05mm。在扩散 层内随着离开汞滴表面距离增加,浓度从小到大。
此时电流达极限值(不再随着外加电位的增加而增加), 该电流称为极限电流i1,极限电流扣除残余电流ir后为极限扩 散电流,简称扩散电流id。
对于线性扩散,根据 Fick 第一定律,每秒通过扩散而到 达电极表面的被测离子的量 f,与电极面积A和浓度梯度成正 比,即 c f DA x 电极表面 若扩散层内浓度从小到大的变化呈直线型,则电极表面的浓 度梯度可近似地表示为:
获得的实验数据是否吻合。因此,发表论文时,必须注明毛细管常数和
扩散电流常数。
(3)汞柱高度
当电活性物质浓度相同时,尤考维奇方程为:
2 3 1 6
id Km
1 m h, , h
1 2
id kh
显然,改变汞柱高度时,将引起流速和下滴时间的变化,扩 散电流也会不同。在极谱分析时,汞柱高度应保持不变。
上,当还原电位较正的B先在滴汞电极上还原产生一个大的 前波时,该前波将使A的极谱波难以测量。此时也可加入配
位剂,改变价态或用化学方法除去B的干扰。
氢波-酸性溶液中,氢离子在-1.2~ -1.4V(与酸度有关) 电位范围内在滴汞电极上还原产生氢波。 Co2+、Ni2+、Zn2
+等它们的极谱波与氢波相近,因此应在氨性溶液中进行极
法来提高检测灵敏度。
5)叠波、前波和氢波
叠波-两种物质的极谱波的半波电位之差小于0.2V 时,这 两个极谱波发生重叠,不易测定。-加入配位剂,改变半 波电位使之分开,或者化学分离。 前波-若溶液中存在两种易还原的物质 A 和B,被测物质 A
的还原电位较B负,且差值大于0.2V,而浓度比B小10倍以
第12章伏安与极谱分析法

极限扩散电流方程式为
iI nFAD1/ 2 (tm )1/ 2 c
其中: tm —从加脉冲到测量电流的时间。 A—电极面积
37
2、示差脉冲极谱法
在每一滴汞生长到一定时刻(1~2s)在线性变化 的直流电压上叠加一个恒定振幅的脉冲电压。 记录电流的方式是在每一滴汞生长期间记录两次 电流;一次是叠加脉冲前20ms,另一次是在脉冲 结束前20ms瞬间,第一次记录的直流电压的背景 电流(残余电流)。第二次记录的是叠加脉冲电 压后的电解电流,取两次电流值之差i,所得电流 即扣除了直流电压所引起的背景电流。
id= KC 极谱定量分析依据
2.半波电位Φ1/2—极限扩散 电流为1/2处对应的Φde,
一定条件下为定值,不随C 改变—极谱定性分析依据
3.锯齿形
• 因为滴汞作周期性的滴落使电极面积发生周期性变化,引
起电流起伏波动,同时产生充电电流
6
12-2扩散电流理论
一、平面电极上的扩散电流
i(t) id (t) nFAD
U外〈 U分 , ΦDME正于Φ Cd析
U外= -ΦDME (vs.SCE)
2.电流开始上升 B ΦDME=Φ Cd析
阴: ΦCdde=2+Φ+θ2Ced2++H,Cdg+=0C.0d5(H92g/)l2g〔Cd2+〕/〔Cd(Hg)〕 阳:2Hg+2Cl-=Hg2Cl2+2e 3.电流急剧上升阶段 BC 4.极限扩散电流阶段 CD
D - 被测组份扩散系数(cm2/s)
m - 汞流速度(mg/s) τ - 滴汞周期(s) C - 被测组份浓度(mmol/L)
极谱法和伏安法

极谱分析旳特殊之处: 1)采用一大一小旳电极:大面积旳去极化电极——参比电极;小面
积旳极化电极; 2)电解是在静置、不搅拌旳情况下进行。 极谱分析旳特点: l 滴汞和周围旳溶液一直保持新鲜──确保同一外加电压下旳电流旳重
设配离子与简朴离子在溶液中旳扩散系数相等,将两者旳极谱方程相减,得
1/2R zF lT n K dpR zF lT n L b []
以 1/2 对 log[Lb-] 作图,可分别求得配合物旳 Kd 和配位数 p
3. 有机物旳极谱波方程 与无机离子不同,有机物参加电极反应旳为中性分子,大多数与H+有关,
极上进行旳反应是非均相旳,其反应有一系列旳环节。 一、极谱波分类
据电极过程分类:可逆波、不可逆波、动力波和吸附波 据电极反应类型:还原波和氧化波 据反应物类型:简朴离子、配合物离子和有机物极谱波 二、电极反应环节
传质——前转化——电化学反应——后转化——新相旳生成
三、极谱波方程(推导过程从略) 1. 简朴金属离子可逆极谱波方程
若滴汞电极上发生还原反应:
0 R zlF n D D T ') 1 /2 ( R zlF ( n i T d ) i c c i c 1 /2 R zlF ( n i T d ) i c c i c
* 若滴汞电极上发生氧化反应:
0 R zl F n D D T ') 1 /2 ( R zl F ( n i T d ) i a a i a 1 /2 R zl F ( n i T d ) i a a i a
因而重叠在被测物旳极谱波上,故应加以消除。
消除:a) 通入惰性气体如H2、N2、CO2 (CO2仅适于酸性溶液); b) 在中性或碱性条件下加入Na2SO3,还原O2; c) 在强酸性溶液中加入Na2CO3,放出大量二氧化碳以除去O2;或加入 还原剂如铁粉,使与酸作用生成H2,而除去O2; d) 在弱酸性或碱性溶液中加入抗坏血酸。
四、伏安分析法

二、极谱分析法的基本原理
1、金属离子的电解
大面积的铂 片电极,溶 液充分搅拌 是减少浓差 极化和电化 学极化
2、极谱分析过程和极谱波-Pb2+(10-3mol/L)
电压由0.2 V逐渐增加到0.7 V 左右,绘制电流-电压曲线。 图中①~②段,仅有微小的电 流流过,这时的电流称为“残余电 流”或背景电流。当外加电压到达 Pb2+的析出电位时,Pb2+开始在滴 汞电极上迅速反应。 由于溶液静止,电极附近的铅离子在
3、 极谱曲线形成条件
(1) 待测物质的浓度要小,快 速形成浓度梯度。 (2) 溶液保持静止,使扩散层 厚度稳定,待测物质仅依靠扩散
到达电极表面。
(3) 电解液中含有较大量的惰性电解质,使待测离子在电
场作用力下的迁移运动降至最小。
(4) 使用两支不同性能的电极。极化电极的电位随外加电 压变化而变,保证在电极表面形成浓差极化。
(id)平均 = 607 n D 1/2 m 2/3 1/6 c
扩散电流常数:I= 607nD1/2
(n和D取决于待测物质的性质)
毛细管特性常数:K = m2/3τ1/6
(m与τ取决于滴汞电极的毛细管特性)
则,极限扩散电流可表示为:
(id)平均 = I· K· c
(2)影响扩散电流大小的因素
A、溶液搅动的影响
用于测量低浓度试样。
C、温度影响
温度系数+0.013/ C,温度控制在0.5 C范围内, 温度引起的误差小于1%。
四、极谱定量分析方法
quantitative methods of polarography
依据公式: id =K c 可进 行定量计算。 极限扩散电流 由极谱图上 量出, 用波高直接进行计算。 波高的测量 (1) 平行线法 (2) 切线法
极谱分析法与循环伏安法

(二)按电极反应的氧化或还原过程区 分——还原波和氧化波
对可逆波来说,同一 物质在相同的底液条件下, 还原波与氧化波的半波电 位1/2相同。 对不可逆波来说氧化 波和还原波的半波电位不 同。
二、极谱波方程式
极谱波是电流与电位的关系曲线, 它们之间的关系称为极谱波方程式。 不同反应类型的极谱波具有不同的 方程式,下面讨论可逆电极反应中简单 金属离子和金属配离子的极谱波方程式.
C、 叠波 二物质△E1/2<0.2V,二个极谱波重叠,形 成叠波,不易分辨。 有二种消除方法: ⑴改变物质的存在形态,如Ni2+和Zn2+的E1/2相 近,产生叠波。加入吡啶后,二络合物的分别 为-1.14V和-1.38V,相差0.24V,不再重叠。 ⑵分离或掩蔽。
§5-4
极谱波的种类及 极谱波方程式
2.亚硫酸钠法
在中性或碱性溶液中, SO32-很容易被氧化为 SO42-,加入Na2SO3可 除去溶液中溶解的氧。
第二个波 H2O2 +2H++2e-= 2H2O, φ1/2=-0.8V 酸性
由于氧波的波形倾斜,延伸 很长,影响许多物质的极谱测 定。必须除去溶解氧
2SO32-+O2= 2SO42-
影响极谱分析灵敏度的主要因素。
产生的原因:分析过程中由于汞滴不停滴下,汞滴表面 积在不断变化,因此充电电流总是存在,较难消除。
充电电流约为10-7 A的数量级,相当于10-5mol/L的被测 物质产生的扩散电流。
(二).迁移电流 migration current
产生的原因: 由于带电荷的被测离子(或带极性的分子)在静电场力 的作用下运动到电极表面所形成的电流。 消除方法: 支持电解质---惰性加强电解质supporting electrolyte。 加强电解质后,被测离子所受到的电场力减小。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
③ 电流急剧上升阶段 这在半波电位附近 ④ 极限扩散区 此时达到极限电流值, 称为极限电流。
C0 0
δ →常数, id= kC
,
i
C C0
id 称为极限扩散电流
(3)涉及概念
极化
浓差极化及形成条件
极化电极A小,反应离子数/单位面积 大,Cs→0
C低 静止
极化电极与去极化电极
表 某些金属离子在不同底液中的半波电位(V)
底液 金属离子 Al3+
1molL-1KCl 1molL-1HCl 1molL-1KOH (NaOH) 2molL-1HAc+ 2molL-1NH4Ac 1molL-1NH3+ 1molL-1NH4Cl
-1.75
-
-
-
-
Fe3+
Fe2+ Cr3+ Mn2+ Co2+ Ni2+ Zn2+
>0
-1.30 -0.85
>0
-0.99
1.46 (-0.9) -0.92 -1.70 1.43 -1.48
>0
-1.2 -1.1 -1.1 -1.1
1.49 (-0.34) 1.43
-1.47
-1.51 -1.30 -1.10 1.00
-1.26
-
-1.71
-1.66 -1.29 -1.10 -1.35
O
A k B id i 0.059 E lg ( ) n Bk A i
O
id i 0.059 E ' lg ( ) n i
当i=1/2id时的电位即为半波电位 E=E’ 即电极电位与浓度无关,故可利 用半波电位进行定性分析
在1mol/L KCl底液中,
不同浓度的Cd2+极谱波
c0 待测物原始浓度(mmol/L)
m 汞流速度(mg/s)
(2) 扩散方程讨论
n,D 取决于被测物质的特性 将607nD1/2定义为扩散电流常数,用 I 表示。 越大,测定越灵敏。
m,t 取决于毛细管特性, m2/3 t 1/6定义为毛细 管特性常数,用K 表示。则: (id)平均 = I· K· c
第四章 极谱分析与伏安分析法
Polarography and Voltammetry
一、 极谱分析装置及基本原理
1. 极谱分析的定义
伏安分析法:以测定电解过程中的电流-电
压曲线为基础的电化学分析方法
极谱分析法:采用滴汞电极作为工作电极的
伏安分析法
2. 极谱分析装置
E外=φa-φc+iR
iR很小,可忽略
灵敏度一般可达10-8 ~ 10-9 mol/L;
电流信号呈峰型,便于测量,可同时测量多
种金属离子。
应用
30多种元素的测定
6. 极谱催化波
原理与装置
平行反应过程的动力波 整个电极过程受有关化学反应动力学控制 (k) Ox相当于催化剂 催化电流与Ox在一定范围内成正比
普通极谱分析装置
特点
催化电流大,灵敏度高,10-8~10-11mol/L
选择性好
催化电流与汞高无关
温度影响较大
应用
微量至超痕量金属元素的分析
7. 循环伏安法
与单扫描法的区别
加压方式:三角波 电极:不一定是滴汞 电极
循环伏安的极化曲线 应用
电极过程可逆性的判 断 电极反应机理的研究
2. 单扫描极谱分析法
原理与装置
又称直流示波极谱法,以示波器为电信 号检测器
电压的扫描速度极快,0.25v/s 在汞滴生长后期,加线性增长的锯齿波 脉冲电压,产生的峰电流值与样品浓度成 正比
阴极射线示波器
X轴坐标:显示扫描电压; Y轴坐标:扩散电流
p= 1/2 - 0.028/n
特点
矩形脉冲电压
电解电流以t-1/2衰减,
电容电流以e-t/RC衰减, 在滴汞周期末端可消除 电容电流和毛细管噪声 的影响
特点
脉冲电解电流值大
消除了电容电流的影响
消除了毛细管噪声的影响
灵敏度高10-8-10-9mol/L
对不可逆电极反应灵敏度可提高约10倍
应用
可用于无机物和有机物的测定
减小措施
加入大量的支持电解质
(3)极谱极大
现象
产生的原因
溪流运动
消除方法
加入小量极大抑制剂 (表面活性剂)
(4) 氧波与氢波
(5) 其他概念: 可逆与不可逆波 氧化波与还原波
可逆波: 电流只受扩散控制 不可逆波: 电流受扩散速度和 电极反应速度控制
还原波(阴极波)(电 流为正) 氧化波(阳极波) 对可逆波, 还原波和氧 化波的半波电位相等
阳极采用甘汞电极, 电位不变
E外=-φc(SCE) 即阴极电位可控
3. 极谱波的形成
(1)
实验现象
用上述装置电解CdCl2,以I~E做图得
(2)极谱曲线的解析
① 残余电流
i残 为残余电流
② 电流开始上生阶段
刚达到镉的分解电压,Cd2+开始还原,电流上升
滴汞电极反应: Cd2++2e+Hg== Cd(Hg) 甘汞电极反应: 2Hg-2e+2Cl-==Hg2Cl2
i kA (cA cAe )
(2)-(3) 得:
(3)
id i k A c Ae c Ae id i kA ( 4)
根据法拉第电解定律
i kBcBe
c4)代入(2)
0.059 A ( id i ) / k A EE lg n B ( i ) / k B
极谱波图
二. 极谱定量分析基础与定性分析
1. 极谱定量分析
(1) 扩散电流方程(尤考维奇公式)
id= KC0(极谱分析定量依据)
K=607nD 1/2 m 2/3 t 1/6 id= 607nD 1/2 m 2/3 t 1/6 C0
id 每滴汞上的平均电流(uA) n 电极反应中转移的电子数 D 扩散系数,t 滴汞周期(s)
5. 溶出伏安法
原理与装置
恒电位电解富集与伏安分析相结合
预电解:被测物质在适当电压下电解,还原沉积在阴 极上
溶出:施加反向电压,使沉积在阴极上的金属氧化溶
出,并产生大的峰电流,峰电流的大小与被测物质浓度 成正比
使用普通的极谱仪即可完成(汞膜电极)
Cu,Pb,Cd的溶出伏安图
特点
灵敏度高(10-7mol.l-1)
峰高易于测量
扫描速度快,一个汞滴上可完成测试
分辨率高(只要半波电位相差35mv即可分开)
不可逆波无法测量,无需除氧
应用
与经典极谱法相当
3. 方波极谱法
原理与装置
在直流电压上叠加一个
振幅较小的方波形电压
电解电流在电压叠加区
略有下降,电容电流在电 压叠加区呈指数衰减
标准加入法
(1) 什么是半波电位
2. 极谱定性分析
当电流等于极限电流的一半时的电位,该 电位与浓度无关,是极谱定性的依据
(2) 极谱波方程式
描述极谱波上电流与电位之间关系
A+ne- = B
cAe 可还原离子在滴汞电极表面的浓度 cBe汞齐中B的浓度
由扩散电流公式:
-id = kAcA
(2)
在未达到完全浓差极化前, cAe不等于零;则:
讨论
三、干扰及其消除方法
(1)残余电流
现象
原因
微量杂质等所产生的微弱电流 电容电流(充电电流):影响极谱分析灵 敏度的主要因素
减小措施
可通过试剂提纯、预电解、除氧等
采用新技术
(2)迁移电流
现象 原因
由于带电荷的被测离子(或带极性的分子)在静电 场力的作用下运动到电极表面所形成的电流
• 面积小,电解时电流密度大,容易 发生浓差极化,这样的电极称之为 极化电极,如滴汞电极。 • 面积大,电解时电流密度小,不会 发生浓差极化,这样的电极称之为
去极化电极,如甘汞电极或大面积
汞层。
滴汞电极的特点
电极毛细管口处的汞滴很小,易形成浓差极 化; 汞滴不断滴落,使电极表面不断更新,重复 性好。(受汞滴周期性滴落的影响,汞滴面积 的变化使电流呈快速锯齿性变化); 氢在汞上的超电位较大; 金属与汞生成汞齐,降低其析出电位,使碱 金属和碱土金属也可分析。
Id正比于c的条件
依据公式: id =K c
可进行定量计算。
极限扩散电流 由 极谱图上量出, 用波高 直接进行计算。
(3) 应用方法
直接比较法
cx
hx cs hs
标准曲线法
hX Kcs V X c X Vs cs H K( ) V X VS VS cS hX cX (VS V X ) H V X hX
四、极谱分析法的发展与伏安分析法
常规极谱分析法
单扫描极谱 方波极谱 脉冲极谱 溶出伏安法
极谱催化波
循环伏安法
1. 常规极谱分析法概述
特点
灵敏度,10-2~10-4mol/L
