伏安法和极谱法
仪器分析:第15章 伏安和极谱法

ν位扫描速率(v.s-1), Ei为起始扫描电位 ,扫描时间(s)
与直流极谱法相比,电位变化速率快,使用的是固体电极。
15.6.1.1 线性扫描伏安图的基本特征
当电位较正时,不足以使被测物质在电极上还 原,电流没有变化。
当电位变负,达到被测物质的还原电位时 ,物质在电极上很快地还原。
若电位变负的速率很快,可还原物质会急 剧地还原,此时电流达最大值。
第15章 伏安和极谱法
Voltammetry and Polarography
特殊形式的 电解分析法。 以小面积的工 作电极与参比 电极组成电解池。
伏安法:固体或固态 电极作工作电极。
极谱法:滴汞电极作 工作电极。
15.1 液相传质过程
15.1.1 液相传质方式
对流:粒子随着流动的液体而移动(分自然对流和强制对流两种, 无论哪种对流,电极表面浓度会发生变化)
适用于电活性物质仅为扩散传递方式,并假定在反应中, 电活性物质的浓度基本不变的电化学体系。
电位阶跃实验装置主要由三电极系统和一个控制电位阶跃的 恒电位器组成。电位阶跃的选择通常是从电化学反应发生前 的某一电位改变到电化学反应发生后的另一电位,观察由此 引起的电流随时间变化的规律。由于该方法获得的是i-t关系 曲线,因此通常称为计时电流法或计时安培法
可见,催化电流由耦联的化学反应速率常数所控制。而且,当 C的浓度一定时,催化电流大小与被测物A的浓度呈正比,这是 物质定量的依据。
15.5 脉冲极谱
15.5.1 方波极谱法
将电压振幅小于30mV,频率 225Hz的方波,叠加在线性变 化的电位上,在电极/溶液界面 会产生充电电流,方波反向时会 产生反向的充电电流。此外,还 有Farady电流,两者都会衰减, 充电电流衰减的更快(成指数衰减), 在方波半周后期的充电电流已非常小 这时进行电流采样,主要为Farady 电流.
极谱法和伏安法

极谱分析旳特殊之处: 1)采用一大一小旳电极:大面积旳去极化电极——参比电极;小面
积旳极化电极; 2)电解是在静置、不搅拌旳情况下进行。 极谱分析旳特点: l 滴汞和周围旳溶液一直保持新鲜──确保同一外加电压下旳电流旳重
设配离子与简朴离子在溶液中旳扩散系数相等,将两者旳极谱方程相减,得
1/2R zF lT n K dpR zF lT n L b []
以 1/2 对 log[Lb-] 作图,可分别求得配合物旳 Kd 和配位数 p
3. 有机物旳极谱波方程 与无机离子不同,有机物参加电极反应旳为中性分子,大多数与H+有关,
极上进行旳反应是非均相旳,其反应有一系列旳环节。 一、极谱波分类
据电极过程分类:可逆波、不可逆波、动力波和吸附波 据电极反应类型:还原波和氧化波 据反应物类型:简朴离子、配合物离子和有机物极谱波 二、电极反应环节
传质——前转化——电化学反应——后转化——新相旳生成
三、极谱波方程(推导过程从略) 1. 简朴金属离子可逆极谱波方程
若滴汞电极上发生还原反应:
0 R zlF n D D T ') 1 /2 ( R zlF ( n i T d ) i c c i c 1 /2 R zlF ( n i T d ) i c c i c
* 若滴汞电极上发生氧化反应:
0 R zl F n D D T ') 1 /2 ( R zl F ( n i T d ) i a a i a 1 /2 R zl F ( n i T d ) i a a i a
因而重叠在被测物旳极谱波上,故应加以消除。
消除:a) 通入惰性气体如H2、N2、CO2 (CO2仅适于酸性溶液); b) 在中性或碱性条件下加入Na2SO3,还原O2; c) 在强酸性溶液中加入Na2CO3,放出大量二氧化碳以除去O2;或加入 还原剂如铁粉,使与酸作用生成H2,而除去O2; d) 在弱酸性或碱性溶液中加入抗坏血酸。
伏安法与极谱法
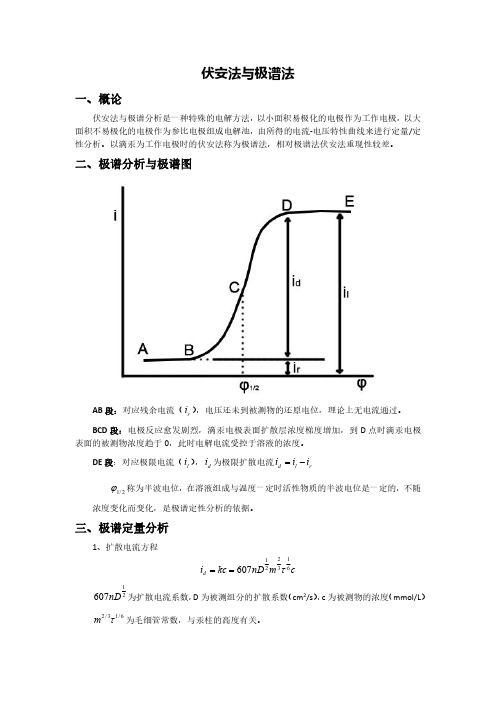
伏安法与极谱法一、概论伏安法与极谱分析是一种特殊的电解方法,以小面积易极化的电极作为工作电极,以大面积不易极化的电极作为参比电极组成电解池,由所得的电流-电压特性曲线来进行定量/定性分析。
以滴汞为工作电极时的伏安法称为极谱法,相对极谱法伏安法重现性较差。
二、极谱分析与极谱图AB 段:对应残余电流(r i ),电压还未到被测物的还原电位,理论上无电流通过。
BCD 段:电极反应愈发剧烈,滴汞电极表面扩散层浓度梯度增加,到D 点时滴汞电极表面的被测物浓度趋于0,此时电解电流受控于溶液的浓度。
DE 段:对应极限电流(l i ),d i 为极限扩散电流rl d i i i -=2/1ϕ称为半波电位,在溶液组成与温度一定时活性物质的半波电位是一定的,不随浓度变化而变化,是极谱定性分析的依据。
三、极谱定量分析1、扩散电流方程cm nD kc i d 613221607τ==21607nD 为扩散电流系数,D 为被测组分的扩散系数(cm 2/s ),c 为被测物的浓度(mmol/L )6/13/2τm 为毛细管常数,与汞柱的高度有关。
2、三切线法测量波高3、标准加入法XS X S S X hV V V H hV c c -+=)(h 为加标准溶液前的波高,H 为加标准溶液后的波高。
4、多组分分别测定:V E 2.0<∆可分别测量四、干扰电流及其消除方法残余电流迁移电流极谱极大氧电流产生微量杂质的电解电流电迁移产生的电流汞滴生长产生的对流效应导致的极谱曲线上的突发电流峰氧气在电极被还原消除作图法扣除加入大量支持电解质(惰性)加入表面活性剂使汞滴表面张力均匀通惰性气体、在中性或碱性下加Na2SO3、强酸中加入Fe 粉五、极谱法特点1、电解是在静止、不搅拌的条件下进行的2、该方法不适用于阴离子的测定,汞滴作阳极时易被氧化3、汞滴与周围溶液始终保持新鲜,保证了在不同电压下的重现性4、汞易纯化,但易堵塞毛细管。
伏安和极谱
迁移电流
电解质中阴、阳离子的静电引力或排斥力,向电极表 面移动而产生的电流
消除方法:加入大量支持电解质
三)极谱极大
定义:在极谱分析中电流随滴汞电极电位的增加迅速。
极谱极大影响半波 电位和极谱扩散电流的 测定 消除方法:可采用加入 少量表面活性物质
(四)氧波
a.为了更好地消除iR降的影响,目前多数仪 器使用三电极系统;
b. 极谱波呈S型锯齿状。
极谱分析特点∶
1.由于汞滴不断下落,电极表面不断更新。具有较高 的再现性。 2.氢在汞电极上的过电位比较高,滴汞电极电位负到 1.20V还不会有氢气析出,可在酸性溶液中测定很多物质。 3.汞是液态金属,具有均匀的表面,能与许多金属形 成汞齐,使其在滴汞电极上的析出电位变正,因而在碱 性溶液中,可测定碱金属和碱土金属离子。 4.可以进行多元素同时测定。在合适的条件下可以一 份试液中同时测定几种元素。
氧在水或溶液中的溶解度约为10-20mg.L-1,溶解氧易在
滴汞电极上还原,产生干扰 第一个波 O2+2H++2e=H2O2 酸性溶液
第二个波
H2O2 +2H++2e= 2H2O
酸性溶液
O2的两个极谱波的E1/2分别是-0.2V及-0.8V,由于氧波的 波形倾斜,延伸很长,影响许多物质的极谱测定。必须除 去溶解氧 除氧方法:1、通气法 2、亚硫酸钠法
2、特点
伏安和极谱分析法是一种特殊电解的分析方法,它是 以小面积电极作工作电极与大面积的参比电极组成电解池,
电解待测物质的稀溶液,根据所得的电流电压曲线进行分
析的方法。
是在电压连续变化的条件下的电解,研究电解过程中I~
E变化规律 电解过程中电流非常小(10-6~10-8A)。
第七章伏安法和极谱法

另外, id的一半处所对应的电 位值叫半波电位,用E1/2来表示,
在一定条件下,它是物质的特性
常数,可用它来判断物质的极谱 波的位置。
四、极谱分析的特殊之处: 1)采用一大一小的电极:大面积
的去极化电极——参比电极;小
面积的极化电极; 2)电解是在静置、不搅拌的情况
下进行。
五.极谱分析中电极的特点: (一)参比电极——大面积的饱和
1/ 2
§7—5
极谱定量分析方法
一.波高的测量:
极谱法中,波高的测量只
需相对波高即可(以mm,记录纸 表格格数表示均可)。而不需要
绝对值。
三切线法:作极限扩散电流、
上升波、残余电流的切线(三条) AB、CD、EF,AB、CD与EF交于O、
P两点,过O、P两点作平行于横
坐标的两条平行线。两线间的距 离就是波高。
经典直流极谱法的局限性:
(1) 用 汞 量 (40 ~ 80 滴 ) 及 时 间 ( 15-
30min):经典极谱法费汞、费时间;
(2)分辨率:分辨率差(V0.20V) ;
(3)灵敏度:灵敏度低(10-5 mol/L) 。
克服的办法是发展极谱分析新技术:
改进仪器: 改变记录方式:如导数、单扫描法等 改变极化方式:如方波,脉冲,单扫 描极谱法等 提高试样的分析利用率: 如催化极谱、吸附波极谱、溶出伏 安法等。
1.可逆波 在电极表面,电活性物 质的氧化态和还原态能迅速的达 到平衡,因此能完全使用能斯特 方程。反应速度很快达到平衡。 2.不可逆波 反应速度很慢,需要 加额外的电压才能进行。
(二)还原波和氧化波 1.还原波(阴极波) 2.氧化波(阳极波) 二、极谱波方程式 描述极谱图中任意一点的 电流与对应的电极电位关系的 方程式称为极谱波方程式。 (一)简单金属离子的极谱波
第15章 伏安法与极谱法..

1 2
毛细管常数
m
2 3
1 6
id kC
极限扩散电流与浓度呈正比 –极谱定量分析的基础
Instrumental Analysis
第15章 伏安法与极谱法
例1:在一定底液中测得1.25×10-3mol· L-1Zn2+的极限 扩散电流id为7.12μA。滴汞流速为1.42mg· s-1,滴下时 间为3.47s,试计算Zn2+在该溶液中的扩散系数、扩散 电流常数和毛细管常数。
b o
Cottrell(柯泰尔)方程 15. 2. 4
id nFAD
扩散层厚度
1/ 2 o
c
t
Do t
Instrumental Analysis
第15章 伏安法与极谱法
15.3 直流极谱法
极谱分析是应用浓差极化现象来 测量溶液中待测离子的浓度的。 15. 3. 1 直流极谱的装置
直流极谱法的基本装置主 要由电子线路组成的极谱 仪和电解池两部分组成, 它包括测量电压、测量电 流和极谱电解池三部分。
Instrumental Analysis
第15章 伏安法与极谱法 对于可逆极谱波,极 谱波上任何一点的电流 都是受扩散速度控制。 对于不可逆极谱波, 一般情况下在波的底部, 电流完全受电极反应的 速度所控制;在波的中 部,电流既受电极反应 速度控制也受扩散速度 控制;达到极限电流时, 完全受扩散速度控制。
第15章 伏安法与极谱法
三. 定量分析方法 1. 直接比较法 将浓度为cs的标准溶液及浓度为cx的未知溶液在 同一实验条件下,分别测得极谱波的波高hs及hx 根据:hs=kcs
hx=kcx
hx cs 求出未知液的浓度 cx hs
伏安法和极谱法

迁移电流
产生的原因:由于带电荷的被测离子(或带极性的分子) 在静电场力的作用下运动到电极表面所形成的电流。 这种由于电极对被分析离子的静电吸引力而引起的电迁 移作用,而使更多的离子趋向电极表面,并在电极上还原 所产生的电流称为迁移电流。迁移电流与被分析物质的浓 度之间并无定量关系,故应加以消除。 消除方法:加强电解质。加强电解质后,被测离子所 受到的电场力减小。 加入的惰性电解质称为“支持电解质”。它是一些能 够导电但在该条件下不能在电极上起电极反应的所谓惰性 电解质,如氯化钾、盐酸、硫酸等。一般支持电解质的浓 度要比被测物质浓度大50-100倍。
铂丝
贮汞瓶
塑料管 毛细管
图1 滴汞电极
E外=c-w+iR
c代表饱和甘汞电极(阳极)的电位, w代表滴汞电极(阴极)的电位,R为回 路中的总电阻.当电流过小时,iR可忽略 不计,Cl-会因参与反应而消耗,但由于 电解电流很小,故消耗的Cl-很少,而饱 和氯化钾溶液中很大,故饱和甘汞电极 的电位在电解过程中基本保持恒定。 图2 极谱分析基本装置 此时滴汞电极电位在数值上就等于外加电压(符号不同),其 电位会随着外加电压的变化而变化,是极化电极。
图4 极谱波
在极谱分析中,滴汞电极面积小,电流密度大,[Cd2+]小, 易发生浓差极化称为极化电极,它的电位随外加电压的变化 而变化;参比电极的表面积较大电解电流较小(微安级), [Cl-]又很大,没有明显的浓差极化现象,它的电位很稳定 ,不随外加电压而变化,称为去极化电极。极谱波的产生是 由于在极化电极上出现浓差极化现象而引起的,所以其电流 -电位曲线称之为极化曲线或极谱波,极谱的名称也是由此 而来的。
1-空气饱和,出现氧双波 2-部分除氧 3-完全除氧
图6 氧气对极谱波的影响
第十二章伏安法与极谱法

三、极谱波形成条件:
1. 待测物质的浓度要小,快速形成浓度梯度。 2. 溶液保持静止,使扩散层厚度稳定,待测物质仅依 靠扩散到达电极表面。 3. 电解液中含有较大量的惰性电解质,使待测离子在 电场作用力下的迁移运动降至最小。 4. 微电极电解。极化电极的电位随外加电压变化而变, 保证在电极表面形成浓差极化。
参比电极为去极化电极:采用SCE饱 和甘汞电极,电极面积较大,通过极谱电 解池的电流很小,电解时的电流密度小, 不会引起面积较大的参比电极电位的显著 变化,电位恒定。
⑵. 电解条件的特殊性 加入大量的支持电解质,并在溶液静止的条件下进行的非
完全的电解过程。 电解过程中,电流的大小主要取决于离子到达电极表面的
二、极谱波的形成
每加一次电压,记录一次电流。以电流为纵坐标,电压为 横坐标作图,得电流——电压曲线,称为极谱波。以电解10-3 mol/L Cd2+的 0.1 mol/L KNO3溶液为例,所得极谱波如图:
U
1. ab段:残余电流 外加电压没达到Cd2+的分解电压前,仅有微小
的电流流过电解池,称为残余电流,用ir表示。 产生的原因是:溶液中微量的更易还原的杂质
一般都可用极谱法,还常用于化学反应机理及动力学过程 的研究及配合物的组成、化学平衡常数的测定等。
四、极谱伏安分析法的分类
极谱分析法
直流极谱法 单扫描极谱法 方波极谱法 脉冲极谱法 计时电位极谱法 交流极谱法
伏安分析法
循环伏安法 溶出伏安法
阳极溶出伏安法 阴极溶出伏安法
§12-2 直流极谱法基本原理
电解电流 充电电流
(a)微量杂质等所产生的微弱电流; 溶剂及试剂中的混入的微量杂质及微量氧等在电极上还
原产生的,杂质的电解电流通常很小。 (b)充电电流(也称电容电流):影响极谱分析灵敏度的 主要因素。
第二章 伏安法和极谱法

什么是伏安法和极谱法?
根据物质在溶液中的电化学性质及其变化来测定物 质组分含量的方法,称为电分析化学法。
伏安法和极谱法是根据测量特殊形式电解过程中
的电流-电位或电流-时间曲线来进行分析的方法。 特殊的电极—电解池用一只小面 积的极化电极作为工作电极,用 一只大面积的去极化电极作为参 比电极。 特殊的电解条件—稀浓度、小 电流、静止。 第二章 伏安法及极谱法
2.4 2.3
2/3 m t 1/6
o o o 2/3 m t o o 1/6 o o o o
3.0 t 2.5 t/s 2.0 1.5
o
2.2 2.1 2.0 0
1.0
0.4
0.8
1.2 -φ/V
1.6
2.0
第二章 伏安法及极谱法
§2-2 极谱干扰电流及其消除
在极谱分析中,除扩散电流外的其它电流(对分析无用或 有害的电流)统称为干扰电流。
要小,可逆性要好。
工作电极――是一个表面积很小的极化电
极,极谱中采用滴汞电极(DME)。储汞瓶
中的汞沿着乳胶管及毛细管(内径约 0.05mm),滴入电解池中,储汞瓶高度一定,
汞滴以一定的速度(3-5秒/滴)均匀滴下。
第二章 伏安法及极谱法
滴汞电极的特点
①是一个完全的极化电极。因汞滴很小(半径0.5-1mm),表面 积很小,所以电流密度很大,当外加电压使其电位负到一 定值时,汞滴表面溶液中的离子完全被还原,浓度趋于零, 电流完全为离子的扩散所决定。 电解方程式: U 外=( E SCE Ede ) iR ESCE为定值,iR可以忽略 所以: U 外= E de (vs. SCE) 表明, DME完全受外加电压所控制,是一个完全的极化电 极。 ②DME是不断以小汞滴滴下的,速度均匀且一定,电极表面 不断更新,表面总是新鲜、光滑的,所以再现性很好。
极谱与伏安法

2. 电解条件的特殊性
电解条件的特殊性表现在分析物的浓度一般较 小,如果组分浓度太高,电流过大会使汞滴无法正 常滴落。另外,电解过程中,被测离子到达电极表 面发生电解反应有三种传质方式:电迁移、对流和 扩散,这三种方式产生三种相对应的电流,只有扩 散电流才与被测物质浓度成正比。
消除迁移电流和对流电流方法:加入支持电解 质消除迁移电流; 保持溶液静止消除对流电流。
它不随物质的浓度变化而变化。 E1/2――极谱定性分析的依据。
铅离子极谱图
三、极谱过程的特殊性
极谱过程是在特殊的电极上和特殊的条件下进行的一种电解过程。
1. 电极的特殊性:一大一小
电极的特殊性表现在极谱分析使用一支是面积很小的滴汞 电极,另一支是面积很大的饱和甘汞电极(而一般电解分 析都使用两支面积大的电极)。
二、极谱波的形成
以10-3 mol/L Pd 2+溶液和 1mol/LKCI组成电解液将三电 极系统插入,设置使汞滴以 1D/3~4s 的速度滴下 , 扫描电压 - 0.5 ~- 1.0V ,得电压~电 流曲线如右图: a-b部分为残余电流(ir); b-c-d部分为扩散电流(i); d-e部分为极限扩散电流(id)。 a b φ½ ir E e i d
极谱分析法采用滴汞电极为工作电极,
作用,汞从毛细管徐徐滴下,从而构
成滴汞电极。分析时,试液作为电解 极谱分析基本装置 溶液。调整汞柱高度,使汞滴以每滴
3~6s的速度滴下。
极谱波(polarographic wave)
如左图所示,在极谱分析中,以滴汞
电极为阴极,饱和甘汞电极为阳极进
P
行电解,当P点在分压电阻上自左向 右逐渐地均匀移动时,工作电池B施
作工作电极。参比电极常采用面积较大、不易极化的
伏安法和极谱法
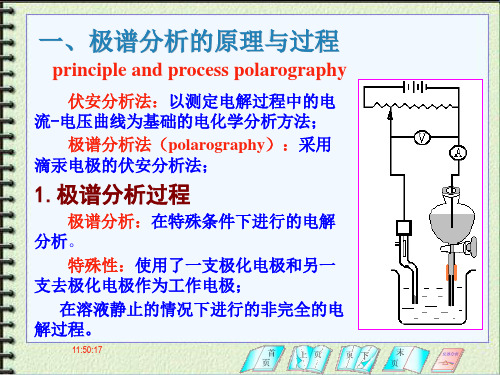
(2) m,t 取决于毛细管特性, m2/3 t 1/6定义为毛细管 特性常数,用K 表示。则:
(id)平均 = I · K· c
21:15:09
2.影响扩散电流的因素
(1)溶液搅动的影响
扩散电流常数
I= 607nD1/2 = id /( K· c) (n和D取决于待测物质的性质) 应与滴汞周期无关,但与实际 情况不符。原因,汞滴滴落使溶液
( 2)
(id)t 时电解开始后t 时,扩散电流的大小。
扩散电流方程:
(id)平均=706nD1/2m2/3 t 1/6c
(id)平均 每滴汞上的平均电流(微安);n 电极反应中转移的 电子数;D 扩散系数; t 滴汞周期(s);c 待测物原始浓度 (mmol/L);m 汞流速度(mg/s); 讨论: (1) n,D 取决于被测物质的特性 将706nD1/2定义为扩散电流常数,用 I 表示。越大,测定越 灵敏。
21:15:09
极化电极与去极化电极
如果一支电极通过无限小的电流,
便引起电极电位发生很大变化,这样的
电极称之为极化电极,如滴汞电极,反 之电极电位不随电流变化的电极叫做理 想的去极化电极,如甘汞电极或大面积 汞层。
21:15:09
极谱分析过程和极谱波-Pb2+(10-3mol/L)
电压由0.2 V逐渐增加到0.7 V 左右,绘制电流-电压曲线。 图中①~②段,仅有微小的电 流流过,这时的电流称为“残余电 流”或背景电流。当外加电压到达 Pb2+的析出电位时,Pb2+开始在滴 汞电极上迅速反应。 由于溶液静止,电极附近的铅离子在
21:15:09
2.迁移电流
21:15:09
3. 极谱波方程式
15章伏安法和极谱法

新极谱法的主要发展方向,就是怎样减少残余电流。
四、极谱分析法的应用
凡是在滴汞电极上可发生氧化还原 反应的物质,如金属离子、金属络合物
机物均可用极谱法测定。某些不发生氧
化还原反应的物质,也可用间接法测定, 因而极谱法的应用范围十分广泛。
一、单扫描极谱分析法
single sweep polarography
均与待测物质浓度(C)之间的定量关系:
尤考维奇方程
(id)平均 = 607 n D 1/2 m 2/3 1/6 c
式中:n为电极反应中电子转移数;
D为待测物质在溶液中的扩散系数(cm2/s);
m为汞滴流速(mg/s);τ为滴汞周期(s);
( id )平均的单位为微安;c 浓度单位为毫摩尔/升;
m 2/3 1/6 m毛细管常数。
3. 形成i~E曲线的条件
(1) 汞滴面积必须恒定 At=8.4910-3m2/3t2/3 dA/dt=5.710-3m2/3t - 1/3
t 越大,电极面积的变化率 越小,汞滴增长的后期,视
为不变。定时滴落。
(2) 极化电极电位必须是时间的线形函数
施加锯齿波电压。电压补偿。补偿过程如图所示。
滴汞电极的特点:
(1)使电极表面不断更新,重复性好; (2) 汞能和多种金属形成汞齐,使金属更容易析出。 (3) 氢在汞电极上过电位很高,不易产生氢离子还原的干扰;
(4)汞有毒。
极谱曲线形成条件:
(1) 待测物质的浓度要小,快速形成浓度梯度。 (2) 溶液保持静止,使扩散层厚度稳定,待测物质仅依 靠扩散到达电极表面。
峰电位:
25C
RT E P E1 / 2 1.1 nF 28 E P E1 / 2 n
第十二章 伏安法与极谱法
在实验中应谨防汞的散落和蒸发。
用后的汞要及时回收。 实验室要注意通风,并应经常检查空气中汞的含量。 只要在实验中细心操作,注意改善工作的环境条件,这一 缺点完全可以克服。
17:08:54
第十二章 伏安法与极谱法
第二节 扩散电流理论
一、电极表面传质过程
二、滴汞电极上的扩散电流
三、影响扩散电流的主要因 素
A
B
M
1/2 -/V(vs.SCE)
ir
0.059 lg 2 cCd(Hg)
0 cCd 2
其中C0Cd2+为Cd2+在滴汞表面的浓度。
17:08:54
MC段:继续增加电压,或 DME 更负。c0 将减小,即滴汞电极表面的
Cd2+ 迅速获得电子而还原,电解电流急剧增加。由于此时溶液本体的 Cd2+来不及到达滴汞表面,因此,滴汞表面浓度c0 低于溶液本体浓度c
,极谱图常呈现“锯齿状”,通常
取每一个锯齿的最大值与最小值的 中点作为平均值绘制极谱图
17:08:54
-/V(vs.SCE)
极谱电流是完全受扩散控制的电解电流 极谱的电极反应过程包括三个步骤:
(1)反应物由溶液扩散到电极表面;
(2)反应物在电极表面发生电极反应; (3)反应产物向滴汞中心扩散。 电解电流i与离子扩散速度
17:08:54
一、电极表面传质过程
液相传质方式:
对流:所谓的对流,即粒子随着流动的液体而移动。
电迁移:在电场作用下,荷正电粒子向负极移动,荷负电粒子向正
极移动。
扩散:当溶液中粒子存在浓度梯度时,这种粒子从高浓度向低浓度的
移动过程。
17:08:54
伏安与极谱分析法

1/2 id nFAD O
cb 3 πt 7
2 1 3 6 2
A 8.4910 m t (cm )
3
整个滴下时间(t从0到 )通过的电量为 0 it dt 除以滴下时间,则为单位时间内通过的电量, 即为平均极限扩散电流id:
id
1
0
it dt
1/ 2 2 / 3 1/ 6 m
15.3.4 定量分析方法
15.3.4.1 定量分析方法 1. id的测量 三切线法
2. 定量分析方法 (1)标准曲线法
(2)标准加入法
h kcx
Vx c x Vs cs H k V V x s
csVs h cx H (Vx Vs ) hVx
NH2 NH
+ 2H+ + 2e
对-氨基苯酚的循环伏安图
O + H3O+ NH O O
+ + NH4
O + 2H+ + 2e O
OH
3
4
OH
Mn+ + ne- + Hg = M(Hg)
假定电极反应是可逆的,迁移电流已经消除, 则滴汞电极电位为: RT ca θ de ln nF cs
式中cs为金属离子在电极表面的浓度,ca 为 金属在汞齐中的浓度
根据扩散电流方程式可得: id = Ksc0 未达到极限扩散电流以前,扩散电流为: i = Ks(c0 - cs) 式中c0为金属离子在本体溶液中的浓度 由上两式得: i id 1 2 Ks 607nDs / 2qm/ 3t1/ 6 cs Ks 另外,还原产物的浓度也应与通过的电流成正比
第10章伏安法与极谱法

四、扩散层厚度
线性扩散的扩散层厚度为:
D0t
10.3
一、 直流极谱的装置 以滴汞电极(DME)为 工作电极,饱和甘汞电极 (SCE)为参比电极组成电 解池。
直流极谱法
• 极谱分析使用的两个电 极都是汞电极。(滴汞电极(DME )和饱和甘汞电极(SCE)) • 滴汞电极的电位就完全随着 外加电压的改变而变化,使极谱 电解过程完全成为控制工作电极 电位的电解过程。 • 极谱电解过程中,所测电解 液必须处于静止状态,不能搅动 。
DME的特点:
1、滴汞的表面不断更新,有较好的重现性;
2、许多金属离子可以生成汞齐; 3、氢在汞电极上的过电位高,不会产生还原干扰; 4、用滴汞作为阳极时,电位一般不能正于0.4V(vs SCE) 。
P.403
表15-1
14
一、极谱波的形成
在连续电位扫描过程中记录电流信号,电流随着汞滴 的生长和滴落会出现振荡式的变化。 经整流后的极谱图呈阶梯形——伏安图(极谱波)。
一、电位阶跃法 将电极电位强制性地施加在工作电极上,测量电流随时间 或电位的变化规律。 电位阶跃法是伏安法中最基本的电化学测试技术。通常适 用于电活性物质的传递方式仅为扩散传递过程,而且假定 在电化学反应中,电活性物质的浓度基本不变。 方法: 观察从电化学反应发生前的某一电位改变到电化学反应发 生后的另一电位过程中电流随时间变化的规律——i-t曲线 。
B.
络合物极谱波 络合物的电极反应可表示为: MXp(n-pb)+ + ne- +Hg = M(Hg) + pXb_
C.
有化合物极谱波 有机物的电极反应通常都有氢离子参与。极谱波的特 点是大多数为不可逆波。许多有机化合物不溶于水,要在 有机溶剂 ( 或与水的混合液 ) 中进行测定,需要加入无机盐 类)作为支持电解质来传导电流。 电极反应可表示为: R + nH+ + ne- = RHn
伏安法与极谱

三.伏安法技术介绍
1. 取样直流伏安法 —— 定时采样
(1) 检出限:10-6 M; (2) 没扣除充电电流
2.循环伏安法
加一个三角波形扫描
(1) 可逆波
a.
i = kn3/2 Ac D v * 1/2 1/2 p
b. E = E − 1 .1 RT
Pc
1/2
nF
E = E + 1 .1 RT
Pa
平面电极上的电流大 7 倍,这是对流的原因。
3
极Hale Waihona Puke 扩散电流:id = 708zD1/ 2m2/3t1/6c
平均极限扩散电流:
尤考维奇方程
id = 607 zD1/ 2m2/3t1/6c
5.有机物的极谱波
O + ne- + mH+
R
E = E 0 + RT nF
= E 0 + RT nF
ln
c 0 ⋅ [ H ]+ m O
1/2
nF
E − E = 2 .2 RT = 59 mV
Pc
Pa
nF n
c. iPc/iPa = 1
(2) 准可逆波
120 〉 ( E − E ) 〉 59
n
Pc
Pa
n
(3) 不可逆波
a. 无回扫峰 b. Ep随v移动
(1) 检出限:10-6 M; (2) 没扣除充电电流
3.方波伏安法
存在二个缺点:
c0
R
ln
c0 O
+
mRT
c0
nF
R
ln[ H + ]
25 oC时:
E=E
+ 59
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
1-空气饱和,出现氧双波 2-部分除氧 3-完全除氧
氧气对极谱波的影响
9-2 极谱定性定量方法与应用
9-2-1 极谱定性方法
由极谱波方程式:
RT i E E1/ 2 nF ln id i
当i=id时的电位即为半波电
位,极谱波中点。
E1/ 2
E O
RT nF
ln a KM MKa
常数
一般情况下,不同金属离子
具有不同的半波电位,且不随浓
度改变,分解电压则随浓度改变
而有所不同(如右图所示),故
可利用半波电位进行定性分析。
在1mol/L KCl底液中, 不同浓度的Cd2+极谱波
1. 同一离子在不同溶液中,半波电位不同。金属络离子比 简单金属离子的半波电位要负,稳定常数越大,半波电位越 负;
2. 极限扩散电流 id
平衡时,电解电流仅受扩散运动控制,形成:极限扩散电 流id。(极谱定量分析的基础)
图中③处电流随电压 变化的比值最大,此点对 应的电位称为半波电位。 (极谱定性的依据)
3. 极谱曲线形成条件
(1) 待测物质的浓度要小,快 速形成浓度梯度。
(2) 溶液保持静止,使扩散层 厚度稳定,待测物质仅依靠扩散 到达电极表面。
方 法 测量物理量 电极面积
电位分析 电位、电动势 --
电解分析 电重量、电量 大面积
伏安法 电 流
小面积
极化
电流
无浓差极化 趋于 0 尽量减小极化 有电流 完全浓差极化 有电流
待测物 浓度 -较高浓度 稀溶液
待测物 消耗量 极小 完全消耗 极小
极谱分析过程和极谱波-Pb2+(10-3mol/L)
消除:加入可使表面张力均匀化的极大抑制剂,通常是一些 表面活性物质如明胶、PVA、Triton X-100等。
4. 氧波
产生:两个氧极谱波:
O2+2H++2e=H2O2 -0.2V (半波电位) (O2 + H2O + 2e == H2O2 +2OH-)
H2O2+2H++2e=2H2O -0.8V (半波电位) (H2O2 + 2e == 2OH-)
E1/ 2
E O
RT ln a KM nF M Ka
常数
(7)
RT i E E1/ 2 nF ln id i
25 C 时
E
E1/ 2
0.059 n
ln
id
i
i
即极谱波方程式;
由该式可以计算极谱曲线上每一点的电流与电位值。
i= id /2 时, E=E 1/2 称之为半波电位,极谱定性的依据。
伏安法与极谱法
历史: 伏安法由极谱法发展而来,后者是伏安法的特例。 1922年捷克斯洛伐克人Jaroslav Heyrovsky以滴汞电极作工
作电极首先发现极谱现象,并因此获1959年Nobel奖。随后, 伏安法作为一种电分析方法,主要用于研究各种介质中的氧化 还原过程、表面吸附过程以及化学修饰电极表面电子转移机制。 该法亦用于水相中无机离子或某些有机物的测定。
τ 0
(id
)tdt
(8)
扩散电流方程:尤考维奇(Ilkovic)公式
(id)平均=607nD1/2m2/3 t 1/6c
(id)平均 每滴汞上的平均电流(微安);n 电极反应中转移的 电子数;D 扩散系数; t 滴汞周期(s);c 待测物原始浓度 (mmol/L);m 汞流速度(mg/s); 讨论:
电压由0.2 V逐渐增加到0.7 V左 右,绘制电流-电压曲线。
图中①~②段,仅有微小的电流 流过,这时的电流称为“残余电流” 或背景电流。当外加电压到达Pb2+ 的析出电位时,Pb2+开始在滴汞电 极上迅速反应。
由于溶液静止,电极附近的铅离子在电 极表面迅速反应,此时,产生浓度梯度 (厚度约0.05mm的扩散层),电极反应受 浓度扩散控制。在④处,达到扩散平衡。
0.5MCd2+, 1MHCl 1MHCl
Cd2+的极谱图
2. 影响扩散电流的因素
(1)溶液搅动的影响 扩散电流常数
I= 607nD1/2 = id /( K·c )
(n和D取决于待测物质的性质) 应与滴汞周期无关,但与实际
情况不符。原因,汞滴滴落使溶液 产生搅动。加入动ቤተ መጻሕፍቲ ባይዱ胶(0.005% ),可以使滴汞周期降低至1.5秒。
产生:当外加电压达到待测物分解电压后,在极谱曲线上出 现的比极限扩散电流大得多的不正常的电流峰,称为极谱极 大。其与待测物浓度没有直接关系,主要影响扩散电流和半 波电位的准确测定。
其产生过程为:毛细管末端汞滴被屏蔽—表面电流密度 不均—表面张力不均—切向调整张力—搅拌溶液—离子快速 扩散—极谱极大。
c
(id )t nFAD π D t 3 / 7
(5)
考虑滴汞电极的汞滴面积是时间的函数,t 时汞滴面积,:
At=8.4910-3m2/3t2/3 (cm2)
(6)
将(6)代入(5),得:
(id)t=708nD1/2m2/3t1/6c
(7)
扩散电流的平均值:
(id
)平均
1 τ
(3) 电解液中含有较大量的惰性电解质,使待测离子在电 场作用力下的迁移运动降至最小。
(4) 使用两支不同性能的电极。极化电极的电位随外加电 压变化而变,保证在电极表面形成浓差极化。 为什么使用两支性能不同的电极? 为什么要采用滴汞电极?
4. 滴汞电极的特点
a. 电极毛细管口处的汞滴很小,易形成浓 差极化; b. 汞滴不断滴落,使电极表面不断更新, 重复性好。(受汞滴周期性滴落的影响,汞 滴面积的变化使电流呈快速锯齿性变化); c. 氢在汞上的超电位较大; d. 金属与汞生成汞齐,降低其析出电位,使碱 金属和碱土金属也可分析。 e. 汞容易提纯(但有毒)
(1) n,D 取决于被测物质的特性
将607nD1/2定义为扩散电流常数,用 I 表示。越大,测定越 灵敏。
(2) m,t 取决于毛细管特性, m2/3 t 1/6定义为毛细管
特性常数,用K 表示。则:
(id)平均 = I ·K ·c
为什么极谱曲线呈锯齿 形?
据Ilkoviĉ公式,扩散
电 流 随 时 间 t1/6 增 加 , 是扩散层厚度和滴汞面 积随时间变化的总结果。 在每一滴汞生长最初时 刻电流迅速增加,随后 变慢,汞滴下落时电流 下降,即汞滴周期性长 大和下滴使扩散电流发 生周期性变化,极谱波 呈锯齿形。
9-1-3 干扰电流与抑制
1.残余电流
(a)微量杂质等所产生的微弱电流 产生的原因:溶剂及试剂中的微量杂质及微量氧等。 消除方法:可通过试剂提纯、预电解、除氧等;
(b)充电电流(也称电容电流) 影响极谱分析灵敏度的主要因素。 产生的原因:分析过程中由于汞滴不停滴下,汞滴表面
积在不断变化,因此充电电流总是存在,较难消除。 充电电流约为10-7 A的数量级,相当于10-5~10-6mol/L的
60年代中期,经典伏安法得到很大改进,方法选择性和灵 敏度提高,而且低成本的电子放大装置出现,伏安法开始大量 用于医药、生物和环境分析中。此外伏安法与 HPLC 联用使该 法更具生机。
目前,该法仍广泛用于氧化还原过程和吸附过程的研究。
目录
9-1 极谱分析原理与过程 9-3 现代极谱分析技术
9-1-1 极谱分析原理与过程 9-1-2 扩散电流理论 9-1-3 干扰电流与抑制
其半波电位正好位于极谱分析中最有用的电位区间(0~-1.2V),因而
重叠在被测物的极谱波上,故应加以消除。
消除:a) 通入惰性气体如H2、N2、CO2 (CO2仅适于酸性溶液);
b) 在中性或碱性条件下加入Na2SO3,还原O2; c) 在强酸性溶液中加入Na2CO3,放出大量二氧化碳以除去O2; 或加入还原剂如铁粉,使与酸作用生成H2,而除去O2; d) 在弱酸性或碱性溶液中加入抗坏血酸。
(2)
A:电极面积;D 扩散系数
(id)t 时电解开始后t 时,扩散电流的大小。
在扩散场中,浓度的分布是时间t 和距电极表面距离X 的函数 c = (t, X )
c
c
( X
)X 0,t
π Dt
(3)
(3)代入(2),得:
c
(id )t nFAD π D t
(4)
由于汞滴呈周期性增长,使其有效扩散层厚度减小,线性扩散 层厚度的 3/ 7
由扩散电流公式:
id = KM cM
(3)
在未达到完全浓差极化前, cM不等于零;则:
i KM (cM cMo )
(4)
(4)-(3) 得: id i KMcMo ;
cMo
id i KM
(5)
根据法拉第电解定律:还原产物的浓度(汞齐)与通过电 解池的电流成正比,析出的金属从表面向汞滴中心扩散,则:
1.极谱分析过程
极谱分析:在特殊条件下进行的 电解分析。
特殊性:使用了一支极化电极和 另一支去极化电极作为工作电极;
在溶液静止的情况下进行的非完全 的电解过程。
伏安分析法:以测定电解过程中 的电流-电压曲线为基础的电化学分析 方法;
极谱分析法:采用滴汞电极的伏 安分析法;
极化电极与去极化电极
如果一支电极通过无限小的电流, 便引起电极电位发生很大变化,这样 的电极称之为极化电极,如滴汞电极, 反之电极电位不随电流变化的电极叫 做理想的去极化电极,如甘汞电极或 大面积汞层。
定义: 伏安法和极谱法是一种特殊的电解方法。以小面积、
易极化的电极作工作电极,以大面积、不易极化的电极为 参比电极组成电解池,电解被分析物质的稀溶液,由所测 得的电流-电压特性曲线来进行定性和定量分析的方法。 当以滴汞作工作电极时的伏安法,称为极谱法,它是伏安 法的特例。
