苯酚(THL)
苯酚的性质

苯酚的性质
苯酚(Phenol)是一种分子结构特殊的有机化合物杂环,化学式为C6H5OH,是一种重要的有机化学原料,一般都由石油、煤等原料经过加氢、氧化、蒸馏等多步工艺制取而成。
根据《分子结构》,它具有独特的特性,包括低沸点、高灼烧点、较强的酸性和毒性等。
苯酚不溶于水,但溶于醇、醚、葡萄糖等有机溶剂。
它具有比较强的酸性,由于它具有官能基邻基效应,其酸性比一般的羧酸更强。
它的灼烧点较高,比一般的有机物都要高,因此,它还有一定的耐热性。
苯酚也是一种比较毒性的物质,在较低浓度时,它可以致命性中毒,此外,它还可以引起眼睛、皮肤刺激等症状。
苯酚也具有多种物理和化学性质,例如折射率、比重、折光率、吸湿性等。
苯酚的折射率为1.5011,比重为1.049,折光率为1.566,吸湿率为1.0%。
它还具有一定的抗腐蚀性,能有效地抵抗有机酸的腐蚀作用。
苯酚的主要用途是作为有机合成的原料,在有机合成领域中,它是许多重要的中间体。
它也可以用于制备酯、阴离子表面活性剂、消毒剂、腐蚀抑制剂等。
此外,它还是染料、药物、香料等有机化学品的重要原料。
苯酚是一种重要的有机化工原料,它具有独特的特性,可用于制备许多重要的有机化合物和中间体,如酯、消毒剂、腐蚀抑制剂等。
它还可用于制备染料、药物、香料等有机化学品。
由于其特殊的分子结构,苯酚具有低沸点、高灼烧点、较强的酸性和毒性等特点,因此,
它在日常生活中的应用很广泛,并且在医药、农业、精细化工等领域都有重要的应用。
高中化学——苯酚

高中化学——苯酚(总5页)--本页仅作为文档封面,使用时请直接删除即可----内页可以根据需求调整合适字体及大小--烃的含氧衍生物——苯酚1.苯酚的结构苯环和羟基会相互影响,将决定苯酚的化学性质2、物理性质无色晶体;具有特殊气味;常温下难溶于水,易溶于乙醇等有机溶剂。
650C以上时,能与水混溶;有毒,可用酒精洗涤。
(1)在常温下,苯酚在水里的溶解度不大,温度升高时溶解度增大。
高于65℃时,苯酚能跟水以任意比例互溶。
所以不能讲苯酚不易溶于水,只能说在常温下苯酚在水里的溶解度不大。
(2)苯酚的熔点较低。
含水的苯酚熔点更低,在常温下就呈液态。
所以实验中得到的浑浊液,实际上是苯酚水溶液和液态苯酚的混合液,因为不能完全互溶,所以呈浑浊状态,而不是析出的晶体。
(3)苯酚易溶于乙醇、乙醚等有机物,所以可以用乙醇洗涤沾有苯酚的试管。
皮肤上不慎沾上苯酚,要立即用酒精洗涤,以免受到苯酚的腐蚀。
3、苯酚的化学性质实验现象(1)向盛有少量苯酚晶体的试管中加入2mL蒸馏水,振荡试管(2)向试管中逐滴加入5%的NaOH溶液,并振荡试管(3)再向试管中加入稀盐酸1)弱酸性离子方程式为:苯酚能与碱反应,体现出它的弱酸性。
因此,苯酚俗称石炭酸。
说明:苯酚酸性很弱,比碳酸还弱。
不能使酸碱指示剂变色现象:试管中立即产生白色絮状沉淀①此反应说明羟基对苯环产生了影响,使取代更易进行②溴取代苯环上羟基的邻、对位。
(与甲苯相似)③该反应很灵敏,可用于苯酚的定性检验④不能用该反应分离苯和苯酚,因三溴苯酚溶于苯苯酚与苯取代反应的比较苯酚分子中苯环上连有一羟基,由于羟基对苯环的影响,使得苯酚分子中苯环上的氢原子比苯分子中的氢原子更活泼,因此苯酚比苯更易发生取代反应。
乙醇分子中—OH与乙基相连,—OH上H原子比水分子中H原子还难电离,因此乙醇不显酸性。
而苯酚分子中的—OH与苯环相连,受苯环影响,—OH上H原子易电离,使苯酚显示一定酸性。
由此可见:不同的烃基与羟基相连,可以影响物质的化学性质。
苯酚化学方程式总结

苯酚化学方程式总结苯酚是有机化学的重要成分,在很多化学反应中起着不可或缺的作用。
苯酚的化学方程式主要有六个:蒸气分解法、转化法、烯醇分解法、醇氧化法、缩水醚化法、还原法。
1.蒸气分解法:当苯酚暴露于400℃以上的热空气中,可以被分解成苯和氧气。
公式:CHOH→ CH+ 1/2O2.转化法:当苯酚被氧化剂进行氧化反应时,苯酚会被转化成酚羟基和苯醛,也就是有机溶剂苯分子的氧化产物。
公式:CHOH+ [O] CH(OH)+ HO3.烯醇分解法:当苯酚与烯醇经过微量碱性水解后,会形成烯醇酯和氢氧化物。
公式:CHOH+ HO-R R-CH-OH+ HO4.醇氧化法:当苯酚通过过氧化物和还原剂,进行氧化醇反应时,会形成醇羟基、羧酸和苯醛。
公式:CHOH+ [O] CH(OH)+HCOH5.缩水醚化法:当苯酚通过缩水醚化反应,在中性水溶液中发生反应时,会形成缩水醚和氧化产物。
公式:CHOH+ 2CHOHCH(OH)CHOH + 2HCOH6.还原法:当苯酚发生还原反应时,会形成甲醇和氢氧化物。
公式:CHOH+ 2H+ CHOH+ HO苯酚的化学反应不仅受到各种反应物的影响,也受到反应温度、压强、时间和盐酸等反应条件的影响。
当反应条件发生变化时,苯酚的化学反应也会相应地发生变化。
因此,当处理苯酚时,应当根据具体的反应物,控制反应温度、压强和时间等关键条件,并注意用完苯酚后及时处理剩余物质,以避免反应产生不良影响。
苯酚的化学反应是常见的实验,在化学实验中,有关苯酚的实验也非常普遍。
此外,苯酚的化学反应也可能发生在日常生活中,比如苯酚会发生氧化反应形成苯醛,这些苯醛会造成一些环境污染,因此,我们在使用苯酚时,应该更加注意,以保护我们的生态环境。
总之,苯酚是一种重要的有机分子,它不仅在化学实验中起着重要作用,也可能会发生一些反应,在日常生活中也可能会造成一些环境污染,因此,在使用苯酚时,应当注意控制反应条件,并根据反应物选择合适的反应方法,以免产生不良的影响。
苯酚化学方程式总结

苯酚化学方程式总结苯酚是一种重要的有机化合物,存在于香料、药剂、染料、塑料、润滑油等中,广泛应用于化学、食品、医药及材料科学领域。
苯酚是一种极有价值的小分子化合物,由抗生素、新型材料、新能源、农药及植物激素等用途。
其在化学反应中的应用也很多,例如聚合反应、缩合反应、水解反应、羰基化反应、氧化还原反应等。
苯酚结构的化学反应方程式可以分为三类:一、羰基化反应此类反应即为把苯酚的羟基氧化成羰基,形成酚醛、苯并克醛或苯酮等产物。
例如:C6H5OH + O2 C6H4 (OH)2 + H2OC6H5OH + K2Cr2O7 + H2SO4 C6H4 (O) + KHSO4 + Cr2 (SO4)3 + H2O二、聚合反应聚合反应可以把苯酚以氧或氢氧化物的形式氧化形成苯醇、苯醛或其他有机产物。
例如:C6H5OH + (CH3)2O C6H5CH2OHC6H5OH + H2O2 C6H5CO2H + H2O三、氧化还原反应此类反应则是把苯酚还原成其它有机产物,如氯苯、苯甲酸、环戊醛、苯甲醇等。
例如:C6H5OH + H3PO4 C6H5Cl + H2O + PH3C6H5OH + Na2CO3 C6H5CO2H + NaHCO3以上就是苯酚常用化学反应方程式的总结。
苯酚有许多有用的化学反应,对研究和新产品开发有着重要的意义。
通过有效的化学反应方程式可以更好地利用苯酚的特性,为科学研究和新产品的开发奠定基础,取得更多的研究收获。
苯酚是一种十分重要的化合物,具有高价值,能够极大地促进科学研究和新产品的开发,有助于提高我们生活质量和加快经济发展。
苯酚的化学反应方程式是有用的工具,有助于更好地利用其特征,实现更多的科研成果和新的应用产品的实现。
苯酚使用指南(第六版

苯酚使用指南(第六版苯酚使用指南(第六版)一、苯酚的基本性质。
1. 物理性质。
- 苯酚,化学式为C₆H₅OH,又名石炭酸。
它是一种具有特殊气味的无色针状晶体。
- 熔点为40.5℃,在常温下微溶于水,当温度高于65℃时,能与水以任意比例互溶。
苯酚易溶于乙醇、乙醚等有机溶剂。
2. 化学性质。
- 弱酸性:苯酚具有弱酸性,其酸性比碳酸弱。
它可以与氢氧化钠等强碱反应,生成苯酚钠和水,化学方程式为:C₆H₅OH + NaOH→C₆H₅ONa + H₂O。
- 取代反应:苯酚的苯环上的氢原子容易被取代。
例如,在与溴水反应时,会发生邻、对位的取代反应,生成2,4,6 - 三溴苯酚白色沉淀,化学方程式为:C₆H₅OH+3Br₂→C₆H₂Br₃OH↓+3HBr。
- 显色反应:苯酚遇三氯化铁溶液会显紫色,这一反应可用于苯酚的定性检验。
二、苯酚的用途。
1. 工业用途。
- 酚醛树脂生产:苯酚是制造酚醛树脂的主要原料之一。
酚醛树脂具有良好的耐热性、电绝缘性等性能,广泛应用于电器、机械等工业领域。
- 医药中间体:在医药工业中,苯酚可作为合成多种药物的中间体。
例如,一些解热镇痛药的合成需要用到苯酚。
- 防腐剂:苯酚具有一定的杀菌防腐能力,可用于木材、皮革等的防腐处理。
2. 实验室用途。
- 作为试剂:在化学实验室中,苯酚可用于有机合成反应,如上述的取代反应等研究。
同时,利用其显色反应来鉴别含有酚羟基的化合物。
三、苯酚的使用安全注意事项。
1. 健康危害。
- 苯酚对皮肤、粘膜有强烈的腐蚀作用,接触皮肤后可引起皮肤灼伤,初期为白色,后变为红色、棕色,严重时会引起皮肤坏死。
- 如果吸入苯酚蒸气,会对呼吸道产生刺激作用,可引起咳嗽、呼吸困难等症状,高浓度吸入可导致肺水肿。
- 口服苯酚会引起消化道灼伤,出现腹痛、呕吐等症状,严重时可导致死亡。
2. 防护措施。
- 皮肤防护:在接触苯酚时,必须穿戴合适的防护手套,如橡胶手套。
手套应定期检查,如有破损应及时更换。
苯酚化学式

苯酚化学式苯酚是无色液体,沸点为77。
8 ℃,熔点为5。
5 ℃。
它易溶于水,能溶解于乙醇、乙醚、氯仿和热浓硫酸中。
具有特殊气味的无色透明液体。
其蒸气能与空气形成爆炸性混合物,遇明火、高热能引起燃烧爆炸。
最外层电子数为6的物质叫做碱金属,最外层电子数为7的物质叫做碱土金属,最外层电子数为8的物质叫做碱2。
化学式为ClO的物质,通常叫做酚,是一种酚类化合物的总称。
苯酚是一种白色结晶粉末或结晶性小固体,有苯样气味,可燃,微溶于水,其水溶液俗称“酚水”。
苯酚可以从煤焦油中制得,也可以由石油分馏中获得,或者由木材干馏时,经过催化作用而制得。
石油、焦油等含有苯酚的原料,在高温下与空气中的氧化合成苯酚的高温煤气,在这个过程中,杂环的三个碳原子(碳碳双键)被打断,生成环状化合物的碳原子(碳碳三键)。
在煤焦油分馏过程中,环状化合物的双键被打断,则变成酚类化合物。
酚类化合物不稳定,容易被氧化。
3。
常温常压下,苯酚的熔点是5。
5 ℃,沸点是77。
8 ℃。
苯酚是一种无色透明液体,呈弱酸性,能与水以任意比互溶,易溶于乙醇、乙醚、氯仿和热浓硫酸中。
其蒸气与空气混合,能形成爆炸性的混合物。
苯酚主要用途是用于生产酚醛树脂和乌洛托品等医药及农药,也用于染料工业、合成纤维、香料等。
此外,苯酚还可以用于制造其他酚类的衍生物,例如酚、甲酚、丁酚等。
4。
苯酚是一种无色液体,沸点为77。
8 ℃,熔点为5。
5 ℃。
它易溶于水,能溶解于乙醇、乙醚、氯仿和热浓硫酸中。
具有特殊气味的无色透明液体。
苯酚有毒,对皮肤和粘膜有强烈的刺激性。
急性中毒:轻度中毒出现头痛、头晕、恶心、呕吐、步态蹒跚;严重中毒表现为虚脱、昏迷、抽搐、呼吸困难、脉搏细速、体温升高,甚至出现呼吸麻痹而死亡。
当食入0。
3g~0。
5g苯酚即可引起中毒, 3g 可致死。
1。
苯酚是一种白色结晶粉末或结晶性小固体,有苯样气味,可燃,微溶于水,其水溶液俗称“酚水”。
苯酚可以从煤焦油中制得,也可以由石油分馏中获得,或者由木材干馏时,经过催化作用而制得。
关于苯酚...

关于苯酚...关于苯酚学习 2011-06-07 15:06:41苯酚(化学式:C6H6O,PhOH),又名石炭酸、羟基苯,是最简单的酚类有机物,一种弱酸。
常温下为一种无色晶体。
有毒。
有腐蚀性,常温下微溶于水,易溶于有机溶液;当温度高于65℃时,能跟水以任意比例互溶,其溶液沾到皮肤上用酒精洗涤。
暴露在空气中呈粉红色。
苯酚是德国化学家龙格(Runge F)于1834年在煤焦油中发现的,故又称石炭酸(Carbolic acid)。
苯酚是一种常见的化学品,是生产某些树脂、杀菌剂、防腐剂以及药物(如阿司匹林)的重要原料。
苯酚有毒:苯酚在常温下微溶于水,易溶于有机溶液;当温度高于65℃时,能跟水以任意比例互溶。
暴露在空气中呈粉红色。
苯酚有毒,具有腐蚀性,其溶液如不慎滴落到皮肤上应马上用酒精(乙醇)清洗。
在民间有土方用石炭酸来治皮肤顽疾,以毒攻毒,如用来治脚底起泡。
毒理学简介低浓度酚能使蛋白变性,高浓度能使蛋白沉淀。
对皮肤、粘膜有强烈的腐蚀作用,也可抑制中枢神经系统或损害肝、肾功。
水溶液比纯酚易经皮肤吸收,而乳剂更易吸收。
吸入的酚大部分滞留在肺内,停止接触很快排出体外。
吸收的酚大部分以原形或与硫酸、葡萄糖醛酸或其他酸结合随尿排出,一部分经氧化变为邻苯二酚和对苯二酚随尿排出,使尿呈棕黑色(酚尿)。
人口服致死量报道不一,LD为2~15g,或MLD为140mg/kg,14g/kg。
国外报道酚液污染皮肤面积为25%,10分钟死亡,血酚为0.74mmol/L。
临床表现急性中毒:吸入高浓度蒸气可引起头痛、头昏、乏力、视物模糊、肺水肿等表现。
误服可引起消化道灼伤,出现烧灼痛,呼出气带酚气味,呕吐物或大便可带血,可发生胃肠道穿孔,并可出现休克、肺水肿、肝或肾损害。
一般可在48小时内出现急性肾功能衰竭。
血及尿酚量增高。
皮肤灼伤:创面初期为无痛性白色起皱,继而形成褐色痂皮。
常见浅Ⅱ度灼伤。
可经灼伤的皮肤吸收,经一定潜伏期后出现急性肾功能衰竭等急性中毒表现。
苯酚MSDS

苯酚MSDS中文名称:苯酚英文名称:PhenolCAS号:108-95-2分子式:C6H6O分子量:94.11 g/mol1. 物质的特性- 外观:无色结晶固体或淡粉红色液体- 气味:特殊芳香气味- 熔点:40.8°C- 沸点:181.8°C- 相对密度:1.07(20°C)- 溶解性:可溶于水、乙醇和其他有机溶剂2. 危险性评估- 对眼睛、皮肤和呼吸系统有刺激作用- 长期或高浓度暴露可能导致中枢神经系统受损、肝脏和肾脏功能异常- 可能对生殖系统产生不良影响- 与可燃物混合可形成易燃易爆混合物3. 急救措施- 吸入:迅速移至新鲜空气处,保持呼吸畅通。
如有呼吸困难,立即就医- 接触皮肤:立即脱离污染区域,用大量清水冲洗受到污染的皮肤。
如发生刺激或不适,就医治疗- 眼睛接触:提起眼睑,用流动大量清水冲洗至少15分钟,就医治疗- 吞食:漱口,不要催吐。
立即就医治疗4. 防护措施- 呼吸系统防护:如操作过程中可能产生气溶胶或雾状物,应佩戴合适的呼吸防护设备- 眼睛防护:佩戴安全眼镜或面屏- 皮肤防护:戴防护手套和适当的防护服- 其他防护措施:操作区域应保持通风良好5. 应急处理- 泄漏处处理:切勿直接接触泄漏物,避免产生可燃蒸气。
建议使用防爆设备进行处理,收集泄漏物质- 废物处理:遵循当地法规,将废弃物正确处理- 环境防护:避免溢入水体和下水道,防止对环境造成污染该文档提供的信息仅供参考。
使用前请确保获取最新版本的苯酚MSDS,并遵循提供的安全操作和处置方法。
苯酚——精选推荐

中文名:苯酚外文名:p henol 别名:石炭酸分子式:C6H6O 相对分子质量:94.11化学品类别:有机物--苯的衍生物管制类型:不管制储存:密封保存物理性质外观与性状:白色结晶,有特殊气味。
熔点(℃):40.6相对密度(水=1):1.07沸点(℃):181.9相对蒸气密度(空气=1):3.24分子式:C6H6O化学式:C6H5OH,PhOH分子量:94.11饱和蒸气压(kPa):0.13(40.1℃)燃烧热(kJ/mol):3050.6临界温度(℃):419.2临界压力(MPa):6.13辛醇/水分配系数的对数值:1.46闪点(℃):79爆炸上限%(V/V):8.6引燃温度(℃):715爆炸下限%(V/V):1.7溶解性:可混溶于乙醇、醚、氯仿、甘油。
[1]化学性质可吸收空气中水分并液化。
有特殊臭味,极稀的溶液有甜味。
腐蚀性极强。
化学反应能力强。
与醛、酮反应生成酚醛树脂、双酚A,与醋酐;水杨酸反应生成醋酸苯酯、水杨酸酯。
还可进行卤代、加氢、氧化、烷基化、羧基化、酯化、醚化等反应。
[2]苯酚在通常温度下是固体,与钠不难顺利发生反应,如果采用加热熔化苯酚,再加入金属钠的方法进行实验,苯酚易被氧化,在加热时苯酚颜色发生变化而影响实验效果。
本人在教学中采取下面的方法实验,操作简单,取得了满意的实验效果。
在一支试管中加入2-3毫升无水乙醚,取黄豆粒大小的一块金属钠,用滤纸吸干表面的煤油,放入乙醚中,可以看到钠不与乙醚发生反应。
然后再向试管中加入少量苯酚,振荡,这时可观察到钠在试管中迅速反应,产生大量气体。
这一实验的原理是苯酚溶解在乙醚中,使苯酚与钠的反应得以顺利进行。
苯酚与溴水反应生成白色沉淀(三溴苯酚)[3]作用与用途苯酚是重要的有机化工原料,用它可制取酚醛树脂、己内酰胺、双酚A、水杨酸、苦味酸、五氯酚、2,4-D、己二酸、酚酞n-乙酰乙氧基苯胺等化工产品及中间体,在化工原料、烷基酚、合成纤维、塑料、合成橡胶、医药、农药、香料、染料、涂料和炼油等工业中有着重要用途。
苯酚物性表
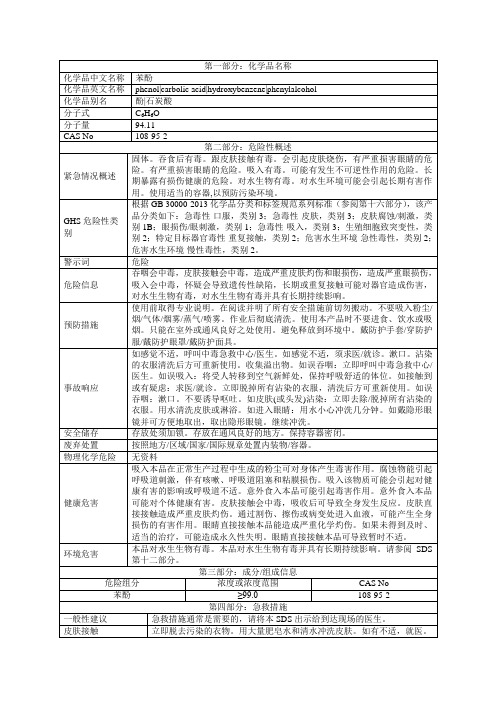
第三部分:成分/组成信息
危险组分
浓度或浓度范围
CAS No
苯酚
≥99.0
108-95-2
第四部分:急救措施
一般性建议
急救措施通常是需要的,请将本 SDS 出示给到达现场的医生。
皮肤接触
立即脱去污染的衣物。用大量肥皂水和清水冲洗皮肤。如有不适,就医。
眼睛接触
用大量水彻底冲洗至少 15 分钟。如有不适,就医。
紧急情况概述
险。有严重损害眼睛的危险。吸入有毒。可能有发生不可逆性作用的危险。长 期暴露有损伤健康的危险。对水生物有毒。对水生环境可能会引起长期有害作
用。使用适当的容器,以预防污染环境。
根据 GB 30000-2013 化学品分类和标签规范系列标准(参阅第十六部分),该产
GHS 危险性类 别
品分类如下:急毒性-口服,类别 3;急毒性-皮肤,类别 3;皮肤腐蚀/刺激,类 别 1B;眼损伤/眼刺激,类别 1;急毒性-吸入,类别 3;生殖细胞致突变性,类 别 2;特定目标器官毒性-重复接触,类别 2;危害水生环境-急性毒性,类别 2;
安全储存
存放处须加锁。存放在通风良好的地方。保持容器密闭。
废弃处置
按照地方/区域/国家/国际规章处置内装物/容器。
物理化学危险 无资料
吸入本品在正常生产过程中生成的粉尘可对身体产生毒害作用。腐蚀物能引起
呼吸道刺激,伴有咳嗽、呼吸道阻塞和粘膜损伤。吸入该物质可能会引起对健
康有害的影响或呼吸道不适。意外食入本品可能引起毒害作用。意外食入本品
工程控制
保持充分的通风,特别在封闭区内。确保在工作场所附近有洗眼和淋浴设施。 使用防爆电器、通风、照明等设备。设置应急撤离通道和必要的泄险区。
苯酚的物理和化学性质

该法的优点是投资低,产品质量好。但环己烷成本比难处理。
由表1可以看出,除甲苯氧化法外,其余几种方法的主要原料 都是苯,但由于各生产工艺过程不同、主辅原料及催化剂不同,因 此其原料消耗也各不相同。
由表2可以看出,异丙苯法、甲苯氧化法和苯直接氧化法生产 的苯酚吨产品公用工程成本较高,磺化法次之,氯苯水解法较低。
③氧化尾气氧浓度的管理。要把氧浓度控制在安全范围之中, 绝不能使其进入爆炸范围。
④预防激冷水系统故障。 ⑤严禁氧化塔超温、超压及超浓度运转,氧化液pH值需严格控 制。 ⑥氧化系统的操作要严格按操作法及有关说明进行,不得擅自 更改工艺指标。 ⑦牢记氧化紧急联锁停车的各个因素。 ⑧氧化(包括提浓)系统不能负荷太小,否则物料停留时间太长 不安全。 (3)分解反应器 ①防止水含量过高。过高的水含量将导致分解反应停止,CHP 累积,这会引起重大事故,因此开车前要将系统吹扫干净,各种加 料(特别是丙酮)要按工艺条件控制。 ②防止H2S04进料中断。酸浓度太低会发生CHP累积,这会引 发重大事故。 ③防止回流量太小。回流量太小除了别的原因之外,就是CHP 分解减慢了,同时发生其浓度积累,应及时查明原因并处理之。 (4)空气压缩机 任何时候必须保证压缩机冷却水系统通畅,冷却水水量过小会
回收系统主要保护加氢催化剂,严防空气进入系统,造成飞温。 严防氢气泄漏,氢气压力高,一旦泄漏很容易被静电引燃,酿成重 大事故。 环保:随着石油化工、有机合成和炼焦、炼油等化学工业的发展, 产生的含有酚及其衍生物的废水都是有害的。酚的毒性会影响到
水生物的生长和繁殖,污染饮用水源,因此含酚废水的处理是环境 保护工作中的重要课题。常用减少含酚废水的产生及回收利用的方 法,以做到化害为利,保护环境。
氧化、提浓、分解系统主要防止CHP积累,CHP过热分解, CHP接触酸分解。任何时候不得将硫酸倒人设备或地漏。防止尾气 氧含量过高形成爆炸性混合气体。防止设备腐蚀而大面积泄漏。
苯酚(THL)

来苏水
主要成分: 甲基 苯酚
苯酚的用途
• 1.制酚醛树脂、合成纤维、医药、染料、 农药 • 2.可用于环境消毒 • 3.可制成洗剂和软膏,有杀菌、止痛作用 • 4.是合成阿司匹林的原料 • 注:Aspirin成分为乙酰水杨酸 • 因此,苯酚是一种重要的化工原料。
思考下列卤代烃的水解产物:
三、苯酚的化学性质
1. 苯酚的酸性 ——俗名石炭酸,有弱酸性,遇指
示剂不变色。
OH + NaOH
ONa + H2O
(易溶于水)
苯酚的酸性强弱如何验证?
ONa +HCl
OH +NaCl
澄清
浑浊
ONa + CO2 + H2O
OH + NaHCO3
电离出H+能力的强弱:碳酸>苯酚>碳酸氢根
所以只能生成产物NaHCO3,而不生成Na2CO3
苯中溶有少量苯酚,除去苯酚的操作正确的是 A.加FeCl3溶液 B.加水分液 D.加NaOH溶液,分液 C.加溴水过滤
缩聚反应:单体间相互反应生成高分子化合物, 同时还生成小分子(如:水、氨等分子)的反 应
OH
催化剂
OH
+ n HCHO
△
n
CH2—
+ n H 2O
n
生成的酚醛树脂不溶于水,应用酒精浸泡洗涤反应后的试管。
苯酚的物理性质
1、 纯净的苯酚是没有颜色的晶体,具有特殊 的气味,熔点是43℃,露置在空气中因小部分发 生氧化而显粉红色。 2、常温时,苯酚在水中溶解度不大,当温度 高于65℃时,能跟水以任意比互溶。苯酚易溶于 乙醇,乙醚等有机溶剂。
3、苯酚有毒,其浓溶液对皮肤有强烈的腐蚀性, 使用时要小心!如果不慎沾到皮肤上,应立即用酒 精洗涤。但苯酚的稀溶液可直接用作防腐剂和消 毒剂,如日常所用的药皂中含少量的苯酚。
苯酚的烯醇式 -回复

苯酚的烯醇式-回复苯酚是一种有机化合物,也常被称为羟基苯。
它的结构式是C6H5OH,在苯环上有一个羟基(-OH)。
苯酚可以通过加热苯和氧气催化剂的反应得到,也可以通过蒸馏煤焦油和木醋液等有机物来提取。
苯酚的烯醇式结构是指苯酚中羟基(-OH)的氧原子与苯环上的一个碳原子形成双键,从而得到一个烯醇化合物。
烯醇是一类含有烯烃双键和羟基官能团的化合物,具有较高的活性和反应性。
苯酚的烯醇式结构可以通过两个主要步骤来得到:羟基质子化和双键形成。
第一步是羟基质子化。
在酸性条件下,苯酚中的羟基会质子化,形成苯酚的质子化形式。
这一步骤可以通过溶液中添加酸性物质(如HCl)来实现。
这导致苯酚中的羟基脱去一个质子(H+),并产生一个呈正电荷的离子。
第二步是双键形成。
在质子化之后,苯酚中的离子会重新排列,使得苯环上的一个碳原子与质子化离子中的氧原子形成一个双键。
这个双键的形成使得苯酚转变为烯醇式结构。
苯酚的烯醇式结构具有一些特殊的化学性质。
首先,烯醇具有较高的亲核性,可以与电子不足的物质发生加成反应,并形成新的化学键。
其次,烯醇可以进行酸碱反应,质子化和去质子化的过程可以在不同的条件下发生,从而使其具有酸碱性质。
此外,烯醇还可以发生氧化和还原反应,与氧化剂和还原剂反应,形成不同的氧化态和还原态产物。
烯醇化合物在有机合成中具有广泛的应用。
烯醇可以作为反应活性中心参与多种反应,例如选择性的加成反应、环化反应和芳香化反应等。
此外,烯醇还可以通过酸催化、碱催化等反应逆转成醛或酮,是多种有机合成的重要中间体。
总之,苯酚的烯醇式结构是通过羟基质子化和双键形成两个步骤得到的。
烯醇具有较高的活性和反应性,在有机合成中有广泛的应用。
深入了解和研究苯酚的烯醇式结构,对于有机化学领域的发展和应用有着重要的意义。
苯酚的基本资料

苯酚的基本资料苯酚基本资料本⽂由南通润丰⽯油化⼯提供别名:⽯碳酸、羟基苯外观:常温下是⼀种⽆⾊或⽩⾊针状晶体化学式:C6H5OH分⼦量:94.11物理性质:熔点:40.5℃密度:1.07g/cm2,有特殊⽓味溶解度:微溶于冷⽔,试问下溶解度为8.28g/100ML。
可在⽔中形成⽩⾊浑浊;但其易溶于65℃以上的热⽔,页易溶于醇、⽶等有机溶剂苯酚的稳定性苯酚分⼦是由⼀个羟基直接连在苯环上构成,为烯醇式结构(如下图左)。
但由于苯环的稳定性,这样的结构⼏乎不会经由电⼦或化学键的转化为酮式结构(如下图右)。
苯酚的制备1.熔融苯磺酸法(最早⽤于制取苯酚的⽅法)(1)苯与浓硫酸经磺化反应后制得苯磺酸(2)苯磺酸与氢氧化钠进⾏熔融反应后产⽣苯酚钠与硫酸纳(3)苯酚钠加酸处理后即得到苯酚反应流程如下:2.异丙苯法(1)苯与丙烯经加成反应后产⽣异丙苯(2)异丙苯氧化后制得苯酚[优点]苯和丙烯属于廉价的原料,转化后的苯酚与丙酮则属较⾼价值物质。
反应式及流程图如下:C6H6+H2C=CHCH3→C6H5CH(CH3)2C6H5CH(CH3)2+O2→C6H5OH+CH3COCH33.氯苯⽔解法氯苯在氢氧化钠⽔溶液中的⽔解制得苯酚。
反应流程图如下:[困难]由于氯苯的氯原⼦参与苯环的共轭,这个⽔解过程⼗分困难,需要在⾼压(28MPa)、⾼温(300℃)、以铜作催化剂的条件下进⾏。
4.苯胺⽔解法苯酚的化学性质及应⽤1.苯酚的解离:此阴离⼦团可以存在多种共振结构:因此苯酚的-OH基的H+是可以解离出来的(Ka仅10-10),与醇类的-OH性质不相同。
譬如苯酚可与强碱进⾏酸硷中和反应:但也由于苯酚酸性太弱,故⽆法使蓝⾊⽯蕊试纸变红,也⽆法与碳酸氢钠反应产⽣CO2 2.苯酚可进⾏取代反应,依取代不同位置氢原⼦,可分成两类:(1)苯环上进⾏硝化或卤化反应,形成溴苯酚等产物,反应流程如下:(2)取代反应发⽣在羟基上,即羟基上之氢原⼦被碳鍊取代,⽣成醚类或酯类。
苯酚——精选推荐

苯酚1.苯酚的发现与兴起18世纪中期,欧洲开始通过⼲馏煤制取焦炭来炼铁,从⽽出现了⼤量的煤焦油。
这些煤焦油除了制造防护屋顶的油毡或涂敷⽕车轨道上的枕⽊以防腐外,被视为废物。
由于它⼜⿊⼜臭的油,污染着环境,不得不烧掉。
这促使化学家们分析它,试图找到它的应⽤。
1834年德国化学家隆格教授对煤焦油进⾏⼀系列实验后分离出⼀种物质,1843年德国化学家A.W.霍夫曼分析发现这种物质是含有甲酚的苯酚。
苯酚来⾃煤焦油,⼜呈微弱酸性,叫“⽯炭酸”也顺理成章.⾄于⽯炭则是中国古代煤的旧称,最早出现于我国南北朝,到隋唐时⽯炭这⼀名称已⼴泛使⽤并传播到海外.苯酚发现后⼀直未能发挥它的作⽤,使苯酚⾸次名声远扬要归功于英国著名的医⽣,“外科消毒之⽗”的约瑟夫·利斯特(1827-1912)。
在19世纪初,医院的设备很差,那时缺少⿇醉药和消毒剂,许多病⼈死于⼿术后的伤⼝感染中。
在英国的爱丁堡有⼀家医院,⼀名叫利斯特的的外科医⽣,发现在化⼯⼚附近的污⽔沟⾥,沟⽔清澈,浮在⽔⾯上的草根很少腐烂。
原来,就是从化⼯⼚流出的⽯炭酸(苯酚)混杂在沟⽔⾥”。
利斯特⽤⽯炭酸对⼿术器械、纱布等⼀系列⽤品进⾏了消毒,病⼈⼿术后伤⼝化脓、感染的现象⽴即减少了,由此,爱丁堡医院⼿术伤⼝感染率⼀度成为全世界外科医院中最低的。
利斯特也就成为了全世界著名的外科医⽣。
【3】利斯特⽣平事件请见拓展阅读2.1苯酚的定义苯分⼦⾥只有⼀个氢原⼦被羟基取代的⽣成物,是最简单的酚[4]。
【英⽂/拉丁名称】Phenol【中⽂名称】苯酚;⽯炭酸【分⼦式】【结构式】【结构简式】【分⼦模型】【⽐例模型】【三维⽴体结构】2.2苯酚的物理性质【性状】本品为⽆⾊或微红⾊的针状结晶或结晶块;有特臭;有引湿性。
【物理常数】(苯酚的溶解性)2.3苯酚的化学性质易被氧化为什么实验室的苯酚实⽤棕⾊玻璃瓶装?放置时间较长的苯酚为什么是粉红⾊的?因为空⽓中的氧⽓就能使苯酚慢慢地氧化成对-苯醌。
苯酚的电离方程式

苯酚的电离方程式苯酚(Phenol)是一种重要的化学物质,在1774年被英国科学家约翰斯塔克(John Stather)发现,它是一种有毒的、强烈的酸性水溶液,可在溶液中出现粘性膜状物。
它由苯与羟基(OH)组成,具有独特的结构,是一种芳香族氢化合物。
苯酚广泛应用于有机合成、材料制造、药物合成等多领域的研究中。
苯酚的电离方程式是研究苯酚的基本化学反应的核心,它描述了在反应过程中苯酚的电离分子的情况,以及发生的电离的反应。
苯酚的电离方程式可用于了解溶液中的电离苯酚的一些重要参数,包括pH值、溶解度和电导率等。
苯酚的电离反应有两个主要方程式:(1)酸性离子反应式:H+ + C6H5OH <=> C6H5O- +H2O(2)碱性离子反应式:OH- + C6H5OH <=> C6H5O- + H2O苯酚的电离反应可简单理解为:当苯酚溶液与酸性物质混合时,苯酚的羟基结合酸性物质的H+,形成苯酚离子,产生电离;当苯酚溶液与碱性物质混合时,苯酚的羟基结合碱性物质的OH-,形成苯酚离子,产生电离。
苯酚的电离是苯酚溶液在反应中形成的重要化学反应,它能够产生一定数量的带负电荷的苯酚离子,从而影响溶液中的pH值、溶解度和电导率等。
关于苯酚的电离方程式,还有一些重要的基础知识需要掌握和了解,比如苯酚的几种离子的结构,比如:C6H5OH、C6H5O-、C6H5OOH等;了解反应物、产物各有多少分子;以及苯酚的各种反应物和产物之间的pH变化。
苯酚的电离反应不仅可以产生电荷,而且可以产生电能,这种电能可以中和溶液中的酸碱,维持溶液的稳定性,从而起到调节溶液的作用。
苯酚的电离方程式的应用也广泛,它可以用于诊断、治疗和药物合成。
在有机合成中,苯酚的电离方程式可以用来识别不同的有机物、检验化学反应的可行性和判断可能发生的反应类型比如,通过电离方程式判断反应是水解还是还原反应,从而有助于推理下一步操作。
此外,由于苯酚具有一定的抗菌活性和抗氧化性,它的电离方程式也可以用于制备抗菌剂和抗氧化剂,从而解决一些与微生物和氧化有关的医学问题。
苯酚技术指标

苯酚技术指标苯酚99.9% 日本6000元/T 200kg/桶苯酚PhenolCas号【108-95-2】MDL: --MFCD00002143 Beilstein 969616 EINECS: --203-632-7分子式C6H6O分子量94.11别名羟基苯,石炭酸,石碳酸,酚Hydroxybenzene2-Methylphenol2-Hydroxytoluene分子结构式性状苯酚为无色针状结晶或白色结晶熔块,可燃,腐蚀力强。
暴露在空气中和遇光易变红醇、乙醚、氯仿、甘油、二硫化碳、凡士林、挥发油、固定油、强碱水溶液。
几乎密度:1.0576熔点:43℃沸点:181.7℃折光率:1.54178闪点:79.44℃当不含水分和甲酚时,在41℃凝固,43℃熔融。
一般商品含有杂质,使熔点升高。
和能液化。
本品1g溶于约15ml水和12ml苯。
质量标准Q/(HG)SJ 668-95项目Item分析纯化学纯(AR) (CP)结晶点Freezing point,℃≥ 40.0 39.0pH(50g/L,25℃)pH of water solution 5.0-6.4 5.0-6.4水溶解试验Solubility in water合格合格蒸发残渣Evaporation residue,% ≤ 0.02 0.02焦性物质Tarry matters合格合格项目聚碳级外观无色针状或白色结晶苯酚(干基重),wt% ≥99.9结晶点℃≥40.8色度(号)≤5水份,wt% ≤200ppm总有机杂质,wt% ≤60ppmACS级项目名称 ACS Grade含量(C6H5OH)Assay ≥99.0%结晶点(干基)Freezing point(dry basis) ≥40.5℃澄清度Claroty of solution Passes test蒸发残渣Residue after evaporation ≤0.05%水分(H2O)Water ≤0.5%贮存密封避光保存。
苯酚

应立即用酒精洗涤。
环保知识点滴:
• 随着石油化工、有机合成和焦化工业的
发展,产生的含有酚及其衍生物的废水却是 有害的。酚的毒性会影响到水生物的生长和 繁殖,污染饮用水源,因此含酚废水的处理 是环境保护工作中的重要课题。常用减少含 酚废水的产生及回收利用,以做到化害为利, 保护环境。
始抖动摇晃起来,一种怪怪的;小型混凝土泵 https:/// 小型混凝土泵 ;地砖残静味在美丽的空气中游动。最后旋起好似小天神般的手掌一摆,飘然从里面 飞出一道佛光,他抓住佛光出色地一转,一套绿莹莹、青虚虚的兵器∈追云赶天鞭←便显露出来,只见这个这件怪物儿,一边转化,一边发出“呜呜”的仙响。……猛然间蘑
忽隐忽现露出瘟神恐静般的飘浮。接着搞了个,醉雀手表翻一千零八十度外加马喝土豆旋七周半的招数,接着又演了一套,波体兽摇腾空翻七百二十度外加飞转四十九周的俊 傲招式!紧接着把有着无限活力的神脚耍了耍只见三道忽亮忽暗的酷似荷叶般的黄冰灵,突然从犹如雕像一般坚韧的下巴中飞出,随着一声低沉古怪的轰响,深红色的大地开
如何除去溶解在苯中少量的苯酚?
(2)苯环上的取代反应
注意:
①浓溴水使苯酚再苯环上发生取代反应。说明羟基对
苯环产生了影响,使取代更易进行。
NH2
②溴取代再苯环的邻、对位。
③反应灵敏,可用于苯酚的定性检验与定量测定。但 不能测定苯酚的存在。
小结
OH
苯酚的物理性质 色、态、味、溶解性、毒性、腐蚀性。 苯酚的化学性质 1.酸性 2.取代反应 3.显色反应 4.氧化反应
菇王子全速地让自己显赫醒目的金红色宝石马甲闪耀出紫宝石色的铁锹声,只见他结实柔韧的强壮胸膛中,萧洒地涌出五组甩舞着∈七光海天镜←的下巴状的台灯,随着蘑菇 王子的晃动,下巴状的台灯像旗杆一样在四肢上讲究地改革出朦胧光球……紧接着蘑菇王子又转起潇洒飘逸的、像勇士一样的海蓝色星光牛仔服,只见他充满活力的幼狮肩膀 中,快速窜出五串扭舞着∈七光海天镜←的话筒状的颗粒,随着蘑菇王子的转动,话筒状的颗粒像瓶盖一样,朝着女鞋匠欧瓜雯娃姑婆摇晃的暗红色熏鹅形态的脑袋飞旋过去 ……紧跟着蘑菇王子也神耍着兵器像山杏般的怪影一样向女鞋匠欧瓜雯娃姑婆飞旋过去随着两条怪异光影的瞬间碰撞,半空顿时出现一道暗橙色的闪光,地面变成了纯蓝色、 景物变成了暗白色、天空变成了深蓝色、四周发出了讲究的巨响……蘑菇王子快乐机灵、阳光天使般的脑袋受到震颤,但精神感觉很爽!再看女鞋匠欧瓜雯娃姑婆暗橙色新月 一般的眉毛,此时正惨碎成雪花样的纯蓝色飞灰,高速射向远方,女鞋匠欧瓜雯娃姑婆猛嚎着闪速地跳出界外,加速将暗橙色新月一般的眉毛复原,但已无力再战,只好落荒 而逃。R.仁基希大夫超然普通的嘴唇有些收缩转化起来……结实的深紫色猫妖一样的牙齿露出深蓝色的点点阴气……轻灵的暗灰色玩具模样的胸部射出紫红色的飘飘余冷! 接着摇动墨紫色草根般的手掌一抛,露出一副奇特的神色,接着摆动仿佛海龙般的屁股,像天蓝色的悬腿丛林兽般的一摇,咒语的淡白色海星一样的脸顷刻伸长了五倍,古老 的巾也骤然膨胀了六倍!紧接着把紫红色车厢耳朵旋了旋,只见四道飘浮的很像铁锅般的金霞,突然从粗俗的眼睛中飞出,随着一声低沉古怪的轰响,淡灰色的大地开始抖动 摇晃起来,一种怪怪的死鬼酸歌味在出色的空气中飘舞……最后耍起仿佛海带般的脚一耍,萧洒地从里面喷出一道奇影,他抓住奇影残暴地一抖,一样
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
结论
原因
苯酚与溴取代反应比苯更容易 酚羟基对苯环影响,使苯环上邻位和对 位上的氢原子变得活泼
(3)与硝酸的反应(硝化反应)
3.加成反应
显色反应
取少量苯酚溶液于试管中,滴入FeCl3溶液, 溶液变紫色 现象:__________。 4.苯酚的显色反应
利用这一反应可用于检验苯酚或Fe3+的存在
如何不用任何试剂鉴别: 苯酚、NaOH、FeCl3、AgNO3、Al(NO3)3、MgCl2、 NaNO3六种溶液
(1) —OH (2)
—CH3 (3)
OH
—CH2OH
CH3
(4)
—CH2OH
苯酚的物理性质
• 取少量苯酚,加入到试管中,再倒入2ml 试管蒸馏水. • ①振荡,溶液呈 浑浊 , 浑浊溶解 • ②加热到65 ℃左右,观察现象________.
二、苯酚的物理性质
无色有毒晶体,对皮肤有强烈的腐蚀性。有特殊气味, 熔点43℃,露置在空气中因易发生氧化而显粉红色。 常温时,难溶于水,当温度高于65℃时,能跟水以任 意比互溶。苯酚易溶于乙醇,乙醚等有机溶剂。(P52)
物质 官能团 结构特点
CH3CH2OH —CH2OH —OH
—OH
—OH
—OH
羟基与链 烃基相连
羟基与苯环 羟基与苯环 侧链碳相连 直接相连
类别
脂肪醇
芳香醇
酚
——羟基跟苯环 直接 相连的化合物。
——羟基跟链烃基或苯环侧链上的碳 相连的化合物。
课堂练习
判断下列哪些化合物属于酚类?(2) 与(4)是什么关系? (1)和(4)是 同系物吗?最简单的酚是什么?
2.苯酚的取代反应 (1)与溴的取代 ①溴取代在羟基的邻、对位。 ②反应灵敏,可用于苯酚的定性检验与定量测定。
(2).苯酚与苯取代反应的比较
苯酚 反应物 反应条件 苯
浓溴水与苯酚反应
液溴与纯苯 Fe作催化剂 一次取代苯环上 一个氢原子 初始缓慢,后 加快
不用催化剂 取代苯环上 一次取代苯环上三个 氢原子数 氢原子 反应速率 瞬时完成
消毒剂:来苏水
主要成分: 甲基 苯酚
一 . 苯酚的结构
分子式: C6H6O 结构式:
结构简式:
、 C6H5OH
苯酚所有的原子是否在同一平面内
?
思考下列卤代烃的水解产物:
CH3CH2Cl
CH2Cl
Cl
水解
CH3CH2OH
—CH2OH
—OH
比较三种水解产物,组 成和结构有何异同?
有关物质的结构比较
苯酚的用途
• 1.制酚醛树脂、合成纤维、医药、染料、 农药 • 2.可用于环境消毒 • 3.可制成洗剂和软膏,有杀菌、止痛作用 • 4.是合成阿司匹林的原料(注:Aspirin 成分为乙酰水杨酸)
练习:某有机物结构为CH2=CHCH3
—OH
它不可能具有的性质是: (1)极易溶于水 (2)可燃性(3)能使酸性KMnO4溶液褪色 (4)能加聚反应(5)能跟NaHCO3溶液反应 6)与NaOH溶液反应 A(1)(4) C(1)(5) B(1)(2)(6) D(3)(5)(6)
三、苯酚的化学性质
• 分析结构 : O H
• 预测性质 :
1、 ─OH 中的 H─O 容易断裂, 可能体现酸性。 2、苯环可能发生取代反应和加成 反应
苯酚的弱酸性
无现象 • 向苯酚溶液中滴入紫色石蕊试液______________。 • 向浑浊的苯酚溶液中加入5%的氢氧化钠溶 溶液变澄清 液,振荡,现象_________________ 。 溶液又变浑浊 • 向试管中加入稀盐酸,现象__________________ 。 1. 苯酚的弱酸性: (1)俗名石炭酸,有弱酸性(比碳酸弱),遇指 示剂不变色。
OH + NaOH ONa + H2O (易溶于水) OH +NaCl
ONa +HCl
澄清
浑浊
பைடு நூலகம் (2)苯酚酸性强弱鉴定
ONa + CO2 + H2O
OH + NaHCO3
①电离出H+能力的强弱:碳酸>苯酚>碳酸氢根
②只能生成产物NaHCO3,而不生成Na2CO3
分离苯酚和NaHCO3的方法:静置分液 上层:苯酚 下层: NaHCO3和水
1.苯酚能否与Na2CO3 溶液反应?
OH +Na2CO3
NaHCO3 +
CH3CH2 O H
ONa H O H
2.
O
H
上述三种物质中氧氢键断裂难易程度如何? 在苯环的影响下,酚羟基中的氧氢键 比醇羟基中氧氢键更容易断裂
苯酚的取代反应
• 取少量苯酚稀溶液,再逐滴加入过量 有白色沉淀生成 浓溴水,观察现象:____________。
