大肠菌群检验原始记录(平板计数法)
大肠菌群原始记录2003
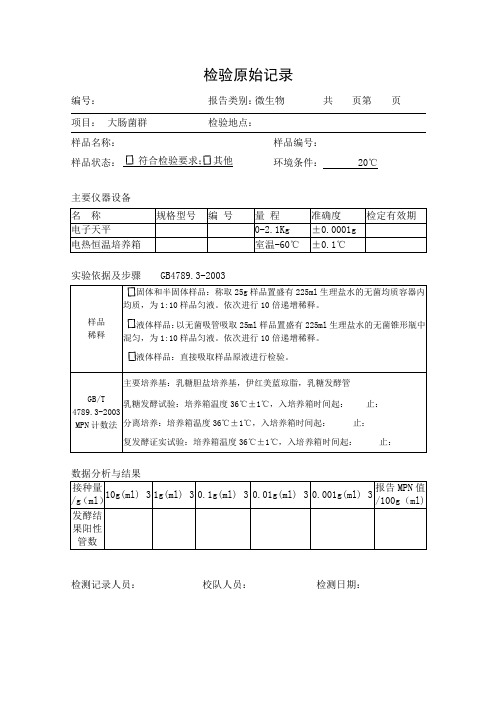
检验原始记录
编号:
报告类别: 微生物 共 页第 页 项目: 大肠菌群 检验地点:
样品名称: 样品编号: 样品状态:
符合检验要求; 其他 环境条件: 20℃
主要仪器设备
名 称
规格型号 编 号 量 程 准确度 检定有效期 电子天平
0-2.1Kg ±0.0001g 电热恒温培养箱
室温-60℃ ±0.1℃
实验依据及步骤 GB4789.3-2003 样品
稀释 固体和半固体样品:称取25g 样品置盛有225ml 生理盐水的无菌均质容器内均质,为1:10样品匀液。
依次进行10倍递增稀释。
液体样品:以无菌吸管吸取25ml 样品置盛有225ml 生理盐水的无菌锥形瓶中混匀,为1:10样品匀液。
依次进行10倍递增稀释。
液体样品:直接吸取样品原液进行检验。
GB/T 4789.3-2003
MPN 计数法 主要培养基:乳糖胆盐培养基,伊红美蓝琼脂,乳糖发酵管
乳糖发酵试验:培养箱温度36℃±1℃,入培养箱时间起: 止: 分离培养:培养箱温度36℃±1℃,入培养箱时间起: 止:
复发酵证实试验:培养箱温度36℃±1℃,入培养箱时间起: 止:
数据分析与结果
接种量/g (ml ) 10g(ml)×3 1g(ml)×3 0.1g(ml)×3 0.01g(ml)×3 0.001g(ml)×3 报告MPN 值/100g (ml) 发酵结
果阳性管数
检测记录人员:
校队人员: 检测日期:。
大肠菌群平板计数法的注意事项

大肠菌群是经常用来衡量食品卫生情况的重要指标,绝大部分食品都会要求检测的项目。
在食品微生物实验室里,大肠菌群和菌落总数的检测频次应该是最高的,但检测过程中总会有一些小问题困扰着大家,以下来讲解一下大肠菌群平板计数法的注意事项。
方法选择相比于MPN计数法,平板计数法更适用于大肠菌群含量较高的食品。
但大肠菌群多少算是含量较高呢国标里没有明确规定,但通常认为,产品大肠菌群以100CFU/g(mL)为界,超过这个含量一般认为是含量较高。
但具体什么时候选用平板计数法进行大肠菌群的检测,大部分情况还是要看你的产品执行的标准。
假如产品标准要求大肠菌群含量的单位为CFU/g(mL),那必须选用平板计数法。
若是/g(mL)或者MPN/100g(mL),就应选择MPN计数法,MPN法具体选用哪版国标此处不再赘述。
因此,根据自己产品的情况选择适当的检测方法。
培养基的要求平板计数法使用的培养基为结晶紫中性胆盐琼脂培养基,简称VRBA。
无论是国标,还是培养基的使用说明中都明确表示,VRBA是不需要进行灭菌的,煮沸2min即可使用。
特地点出这一点是因为很多朋友都在问VRBA的灭菌条件,对不灭菌的培养基不信任,害怕出现检测异常,那是因为这些小伙伴们对其中的原理不清楚。
大肠菌群的定义是在一定培养条件下能够在发酵乳糖、产酸产气的需氧和兼性厌氧的革兰氏阴性无芽孢杆菌,因此大肠菌群是不能形成芽孢的,在VRBA培养基煮沸的过程中,即使有大肠菌群存在也会被杀灭,所以从培养基带入污染的可能性是没有的。
当然盛装培养基的容器是需要进行灭菌的,以免容器引入污染。
另外,VRBA是一种选择性的培养基,含有的结晶紫对革兰氏阳性菌有比较强的抑制作用而对革兰氏阴性菌几乎没有作用,而且平板培养产生的菌落还需要进行复发酵的验证,因此VRBA培养基就不需要进行灭菌了。
但值得注意的是,VRBA需要现配现用,配制出的培养基应当在3h之内使用完毕。
稀释度的确定国标中要求选择2-3个适宜的连续稀释度。
微生物检测原始记录

室温:湿度:
样品名称
规格
检验类别
出厂检验
抽样基数
抽样方式
抽样数量
检测依据
GB/T4789.2-2010
接种时间
使用主要仪器
恒温培养箱
培养基名称
平板计数琼脂培养基
报告时间
样号
36+1℃培养24~48h
稀释度
报告数cfu/ml(g)
1:10
1:100
1:1000
空白
1
接种量ml
1
1
1
1
0.1
0.01
分析号
1
2
3
4
5
6
7
8
9
1
初发酵产酸、气
复发酵产酸、气
BGLB分离培养
2
初发酵产酸、气复发酵产酸、气BGL Nhomakorabea分离培养
检测结果
检验结论
备注:月桂基硫酸盐胰蛋白胨发酵阳性管转种培养实验:1.复发酵:+/+表示产酸、产气为阳性;-/-表示不产酸、不产气为阴性;+/-表示产酸、不产气。接种量在1ml以上者,用双料发酵管;1ml以下者,用单料发酵管。
检验员:审核人:审核时间:
大肠菌群检测原始记录
室温:湿度:
样品名称
规格
检验类别
出厂检验
抽样基数
抽样方式
抽样数量
检测依据
GB/T4789.3-2010
接种时间
使用主要仪器
恒温培养箱
报告时间
样号
培养温度、时间
培养基名称
结果判定报告数(MPN)/100ml(g)
36±1℃24h±2
大肠菌群检测中平板计数法主要操作要领

大肠菌裙检测是一项非常重要的微生物检测工作,它可以帮助我们了解环境和食品中是否存在大肠菌裙,从而保证人们的健康安全。
在大肠菌裙检测中,平板计数法是一种常用的检测方法。
下面将介绍大肠菌裙检测中平板计数法的主要操作要领。
1.准备工作在进行大肠菌裙检测之前,需要准备相应的实验器材和培养基。
实验器材包括平板计数仪、移液器、无菌培养皿等。
培养基一般选择大肠埃希氏菌(EC)培养基。
2.样品处理将待测样品取适量放入无菌容器中,进行适当的稀释。
这一步要确保样品的稀释倍数适中,以保证后续的计数结果准确。
3.接种和培养取一定量的处理过的样品,在无菌工作台上均匀涂抹于含有适量培养基的培养皿上,然后进行培养。
培养条件一般为37摄氏度,培养时间为24小时。
培养后会形成菌落,这些菌落代表了原始样品中的细菌数量。
4.计数和记录在培养后,利用平板计数仪对菌落进行计数。
计数的时候需要注意避免重复计数同一菌落,保证计数准确。
需要记录计数结果,包括菌落数量和相应的单位。
5.结果分析根据计数结果,可以对原始样品中的大肠菌裙数量进行估算。
可以通过对对照组和样品组的比较来判断样品中大肠菌裙的数量是否合格。
大肠菌裙检测中平板计数法的主要操作要领就是以上几点。
通过严格按照这些要领进行操作,可以确保检测结果的准确性和可靠性。
在进行操作过程中,还需要遵守无菌操作规范,确保实验过程中不受外界污染。
希望大家在进行大肠菌裙检测时能够严格按照操作要领进行,保证测试结果的准确性,从而更好地保障人们的健康安全。
大肠菌裙检测中的平板计数法是一种经典的微生物计数方法,它主要用于测定食品、饮用水、环境等样品中大肠菌裙的数量。
在这个过程中,我们需要注意几个关键的环节,来保证实验的准确性和结果的可靠性。
在准备工作环节,我们需要保证实验器材和培养基的质量。
实验器材一定要经过严格的消毒和清洁,以免外来细菌的污染影响实验结果。
培养基的选用也尤为重要,要选择与待测细菌的生长要求相适应的培养基,以保证细菌在培养基上的正常生长。
饮料—大肠菌群的测定—平板计数法

3.3 乳糖发酵管 3.3.1 成分
蛋白胨
20g
乳糖
10g
0.04%溴甲酚紫水溶液
25mL
蒸馏水 3.3.2 制法
1000mL
将蛋白胨及乳糖溶于水中,校正 pH7.4,加入指示剂,分装 3mL,并放入一个小倒管,115℃高
压灭菌 15min。
3.4 EC 肉汤
3.4.1 成分
1
胰蛋白胨
20g
3 号胆盐(或混合胆盐)
匀稀释液。
5.2.2 用 1 mL 灭菌吸管吸取 1:10 稀释液 1 mL,注入含有 9 mL 灭菌生理盐水或其他稀释
液的试管内,振摇试管混匀,做成 1:100 的稀释液。
5.1.3 另取 1 mL 灭菌吸管,按上条操作依次做 10 倍递增稀释液,每递增稀释一次,换用 1
支 1 mL 灭菌吸管。
5.1.4 根据饮料卫生标准要求或对检样污染情况的估计,选择三个稀释度,每个稀释度接种 3 管。
FSPYL026 饮料 大肠菌群的测定 平板计数法
F_SP_ YL_026
饮料—大肠菌群的测定—平板计数法
1 范围 本方法采用平板计数法测定饮料中的大肠菌群。
本方法适用于饮料中大肠菌群的测定,饮料中大肠菌群数系以 100 mL(g)检样内大肠
菌群最可能数(MPN)表示。
2 原理
饮料检样经处理,在需氧及兼性厌氧、37℃条件下培养,通过计数报告检样中大肠菌群 最可能数。大肠菌群系指一群能发酵乳糖,产酸产气的革兰氏阴性无芽孢杆菌。
3.2.1 成分
蛋白胨
10g
乳糖
10g
磷酸氢二钾
2g
琼脂
17g
2%伊红 Y 溶液
20mL
大肠菌群平板计数法的注意事项

大肠菌群平板计数法的注意事项大肠菌群是经常用来衡量食品卫生情况的重要指标,绝大部分食品都会要求检测的项目。
在食品微生物实验室里,大肠菌群和菌落总数的检测频次应该是最高的,但检测过程中总会有一些小问题困扰着大家,以下来讲解一下大肠菌群平板计数法的注意事项。
方法选择相比于MPN计数法,平板计数法更适用于大肠菌群含量较高的食品。
但大肠菌群多少算是含量较高呢国标里没有明确规定,但通常认为,产品大肠菌群以100CFU/g(mL)为界,超过这个含量一般认为是含量较高。
但具体什么时候选用平板计数法进行大肠菌群的检测,大部分情况还是要看你的产品执行的标准。
假如产品标准要求大肠菌群含量的单位为CFU/g(mL),那必须选用平板计数法。
若是/g(mL)或者MPN/100g(mL),就应选择MPN计数法,MPN法具体选用哪版国标此处不再赘述。
因此,根据自己产品的情况选择适当的检测方法。
培养基的要求平板计数法使用的培养基为结晶紫中性胆盐琼脂培养基,简称VRBA。
无论是国标,还是培养基的使用说明中都明确表示,VRBA是不需要进行灭菌的,煮沸2min即可使用。
特地点出这一点是因为很多朋友都在问VRBA的灭菌条件,对不灭菌的培养基不信任,害怕出现检测异常,那是因为这些小伙伴们对其中的原理不清楚。
大肠菌群的定义是在一定培养条件下能够在发酵乳糖、产酸产气的需氧和兼性厌氧的革兰氏阴性无芽孢杆菌,因此大肠菌群是不能形成芽孢的,在VRBA培养基煮沸的过程中,即使有大肠菌群存在也会被杀灭,所以从培养基带入污染的可能性是没有的。
当然盛装培养基的容器是需要进行灭菌的,以免容器引入污染。
另外,VRBA是一种选择性的培养基,含有的结晶紫对革兰氏阳性菌有比较强的抑制作用而对革兰氏阴性菌几乎没有作用,而且平板培养产生的菌落还需要进行复发酵的验证,因此VRBA 培养基就不需要进行灭菌了。
但值得注意的是,VRBA需要现配现用,配制出的培养基应当在3h之内使用完毕。
大肠菌群的测定实验报告

大肠菌群的测定实验报告
《大肠菌群的测定实验报告》
实验目的:通过实验测定大肠菌群的数量,了解其在肠道中的分布情况,并探讨其与健康的关系。
实验方法:我们采集了一组健康人群的粪便样本,并使用培养基和平板计数法对大肠菌群进行测定。
首先,我们将粪便样本均匀涂抹在培养基上,然后将培养皿放入恒温箱中进行培养。
培养后,我们对培养皿上的菌落进行计数,并根据计数结果得出大肠菌群的数量。
实验结果:经过实验测定,我们发现健康人群的大肠菌群数量在正常范围内,平均值约为10^8 CFU/g。
同时,我们还发现不同个体之间的大肠菌群数量存在一定的差异,但总体上呈现出稳定的分布情况。
实验分析:大肠菌群在肠道中起着重要的作用,它能够帮助人体消化食物、产生维生素等。
同时,大肠菌群的数量与肠道健康密切相关,过多或过少都可能导致肠道问题。
因此,通过测定大肠菌群的数量,可以帮助我们了解肠道健康状况,及时采取相应的调节措施。
结论:通过本次实验测定,我们得出了健康人群大肠菌群数量的正常范围,并认识到了大肠菌群在肠道健康中的重要作用。
希望通过这一实验结果,能够为人们提供更多关于肠道健康的参考信息,促进人们更加关注和重视肠道健康。
大肠菌群平板计数法标准号

大肠菌群平板计数法标准号大肠菌群平板计数法是指在实验室条件下,通过将待检样品分散在含有特定培养基的平板上,利用培养基对大肠菌群产生的特异性反应,以及对大肠菌群可生长的特定条件进行培养和计数,从而评估样品中大肠菌群的数量。
该方法已被广泛应用于食品、环境和医疗卫生等领域的微生物检测。
大肠菌群平板计数法标准号是《食品微生物学通则》GB 4789.3-2016。
该标准是由中国国家标准化管理委员会于2016年发布的,是用于食品微生物检测的基本规范。
根据该标准,大肠菌群平板计数法的操作流程主要包括样品制备、平板培养、菌落计数和结果表达。
下面将对每个步骤进行详细介绍。
首先,样品制备是指将待检样品进行预处理,以提高大肠菌群的检测效果。
根据不同样品的特点,可以采取不同的处理方法,如加入适量的缓冲液进行搅拌均匀、加热杀菌和稀释等。
此外,还需要注意样品制备过程中的卫生要求,以防止交叉污染。
然后,将样品均匀地分散在含有选择性培养基的平板上。
选择性培养基可以抑制非大肠菌群的生长,从而增加大肠菌群在平板上的菌落形成,方便后续的计数。
常用的选择性培养基有MacConkey琼脂、立兰肠杆菌培养基等。
接下来,将含有样品的平板置于适宜的温度和湿度条件下进行培养。
大肠菌群在一定的温度范围内可迅速繁殖,通常将培养温度控制在37摄氏度。
此外,还需要为培养提供适当的湿度,可以通过在培养箱内放置含水的培养皿或湿度控制器来实现。
菌落计数是大肠菌群平板计数法的核心步骤。
通常,在培养一定时间后,将平板上的菌落进行计数。
菌落计数可以手工进行,也可以使用计数仪来实现。
在进行计数时,需要注意区分出不同的菌落,并排除其他非大肠菌群的菌落。
最后,根据菌落计数的结果,可根据标准对样品中大肠菌群的数量进行评估。
通常,大肠菌群的计数结果以CFU/g(或CFU/mL)表示,即每克(或每毫升)样品中大肠菌群的菌落数。
需要注意的是,大肠菌群平板计数法在应用中存在一定的局限性。
微生物检验原始记录(大肠菌群)

微生物检验原始记录(大肠菌群)检验原始记录编号:报告类别:微生物共页项目:大肠菌群coliforms 检验地点:样品名称:样品编号:样品状态:符合检验要求;其他境条件:实验依据及步骤GB4789.3-2016样品稀释固体和半固体样品:称取25g样品置盛有225ml生理盐水或磷酸盐缓冲液的无菌均质容器内均质,或放入盛有225ml稀释液的无菌均质袋中拍击式均质器拍打,制成为1:10样品匀液。
依次进行10倍递增稀释。
液体样品:以无菌吸管吸取25ml样品置盛有225ml磷酸盐缓冲液或生理盐水的无菌锥形瓶(瓶内预置适当数量的无菌玻璃珠)中混匀,为1:10样品匀液。
样品匀液的ph应在6.5-7.5之间,必要时分别用1mol/lNaOH或1mol/lHcL调节。
取1mL1∶10稀释匀液沿管壁缓缓注入9ml磷酸盐缓冲液或生理盐水的无菌试管中(注意吸管或吸头尖端不要触及稀释液面),振摇试管或换用一支无菌吸管反复吹打,使其混合均匀,制成1:100样品匀液。
按上述操作顺序做10倍递增稀释液,每稀释一次,换用一支1mL灭菌吸量管。
从样品匀液制备到样品接种完毕,全过程不得超过15min。
初发酵试验(9管法)每个样品,选择3个适宜的连续稀释度的样品匀液(液体样品可以选择原液),每个稀释度接种3管月桂基硫酸盐胰蛋白胨(LST)肉汤(大肠菌群测定:如果超过1ml,则用双料LST肉汤)36℃±1℃培养24h±2h,观察倒管内是否有气泡产生。
产气者进行复发酵试验,未产气则继续培养至48±2h,产期进行复发酵试验。
未产气者为大肠菌群阴性。
复发酵试验(证实试验)用接种环从产气的LST肉汤管中分别取培养物1环,移种于煌绿糖胆盐肉汤(BGLB)管中,36℃±1℃培养48h±2h,,观察产气情况。
数据分析与结果一、菌落计数根据证实为大肠菌群的阳性管数,查MPN检索表,报告大肠菌群的最可能数。
大肠菌群平板计数限量标准

大肠菌群平板计数限量标准1. 引言大肠菌群是一类存在于人体肠道中的细菌,其计数可以作为评估肠道菌群健康状态的重要指标。
为确保食品安全和公共卫生,制定一份大肠菌群平板计数限量标准具有重要意义。
2. 目的本标准的目的是通过设定大肠菌群平板计数的限量,以减少食品和饮用水中的大肠菌群污染,保障公众健康。
3. 定义3.1 大肠菌群:指在大肠中常见的一类细菌菌群。
3.2 平板计数:采用平板培养方法,通过计数可成满足一定生长条件的菌落形成单位,来确定大肠菌群数量。
4. 大肠菌群平板计数限量标准4.1 食品中的大肠菌群平板计数限量标准:4.1.1 食品类别 | 大肠菌群平板计数限量(单位:CFU/g)鲜肉类食品| ≤100熟肉或熟制品| ≤10生鲜水果蔬菜| ≤100加工水果蔬菜| ≤10食品类加工品| ≤104.1.2 大肠菌群的检验方法:采用标准的培养基和平板计数法,培养温度为37°C,培养时间为24-48小时。
4.2 饮用水中的大肠菌群平板计数限量标准:4.2.1 饮用水类别 | 大肠菌群平板计数限量(单位:CFU/mL)自来水| ≤10包装饮用水| ≤104.2.2 大肠菌群的检验方法:采用标准的培养基和平板计数法,培养温度为37°C,培养时间为24-48小时。
5. 检测与监管5.1 大肠菌群平板计数的检测应由具备相应技术与资质的实验室进行。
5.2 相关部门应定期进行食品和饮用水的大肠菌群平板计数检测,确保其符合本标准要求。
5.3 如超出限量标准,则需要采取相应措施,例如立即终止生产、销售或使用,并进行卫生处理等。
6. 结论本标准制定了食品和饮用水中大肠菌群平板计数的限量标准,旨在确保食品安全和公共卫生。
相关部门和实验室应积极采取措施,加强对大肠菌群平板计数的监管和检测,保障公众的健康与安全。
注:CFU - 菌落形成单位 (Colony Forming Unit)。
大肠菌群平板计数法原始记录

报告日期: 规格型号 样品数量
2
3
4
5
结晶紫中性红胆盐琼脂(VRBA),36℃±1℃培养18h-24h,单位CFU/g 煌绿乳糖胆盐肉汤(BGLB),36℃±1℃培养18h-24h(产气
10-1
10-2
10-3 空白 计算公式 计算结果
大肠菌群数=阳性试管比例*平板菌落数*稀释倍数
检验员:
复核:
(+:表示产气;-:表示不产气)
报告日期: 规格型号 样品数量
10
-1
10
-2
10-3 空白 计算公式 计算结果
大肠菌群数=阳性试管比例*平板菌落数*稀释倍数
检验员:
复核:
****食品有限公司
大肠菌群平板计数法检验原始记录
编号: 检验日期: 产品名称 抽样日期 批次编号 抽样人 检测方法:GB4789.3平板计数法 稀释度 1 2 3 4 5 1
****食品有限公司
大肠菌群平板计数法检验原始记录
编号: 检验日期: 产品名称 抽样日期 批次编号 抽样人 检测方法:GB4789.3平板计数法 稀释度 1 2来自3 4 5 1 2 3 4 5
结晶紫中性红胆盐琼脂(VRBA),36℃±1℃培养18h-24h,单位CFU/g 煌绿乳糖胆盐肉汤(BGLB),36℃±1℃培养18h-24h,
大肠菌群平板计数法检测结果不确定度的评定

152 食品安全导刊 2017年8月Tlogy科技科技文苑大肠菌群是一组存在于肠道中的与粪便污染有关的细菌,通常用来作为评价食品卫生状况的指示菌。
食品中大肠菌群数量的高低与受粪便污染的程度相关,大肠菌群也可以预示食品中存在肠道致病菌的可能性。
由测量所得的测得值只是被测量的估计值,测量过程中的随机效应及系统效应会导致测量不确定度[1]。
对大肠菌群检测结果的测量不确定度进行评定,能以充分完整的信息表示检测结果,提高大肠菌群检测结果的可信度。
1 不确定度评定方法采用《GB 4789.3-2016 食品安全国家标准 食品微生物学检验 大肠菌群计数》[2]中第二法平板法进行检测,主要检测步骤如下:样品制备—10倍梯度稀释—选取2~3个合适稀释度的样品匀液接种—倾注VRBA 平板—计数典型和可疑菌落数—接种BGLB 肉汤—报告结果。
本文对奶粉样品进行大肠菌群人工污染后进行10次重复测定,以此结果为依据,分析不确定度各分量的来源和大小,并参照JJF1059.1-2012《测量结果不确定度的评定与表示》做不确定度评定。
2 各不确定度分量的评定2.1 样品制备过程中引入的不确定度样品制备过程中,可能引入不确定度的因素有样品称量、量筒量取稀释液、均质器均质等。
用均质器进行拍击均质,拍击时间和拍击速度是固定的,可以忽略由此产生的不确定度。
电子天平精度0.1 g,样品称样量25.0 g,检定证书规定的最大允许误差为±0.5 g。
则天平称量的标准不确定度μ(m样)为:用250 mL 量出式量筒量取225 mL 稀释液,制成1︰10的样品匀液。
量筒按JJG196-2006常用玻璃量器的容量允差为±2.0 mL [3],则量筒量取的标准不确定度μ(v样)为:因此,电子天平和量筒的相对标准不确定度U rel (m 样)和U rel (v 样)分别为:则样品制备过程中产生的相对标准不确定度为:大肠菌群平板计数法检测结果不确定度的评定□ 徐武俊 吕腾飞 李仕祥 刘伟平 江西出入境检验检疫局综合技术中心摘 要:通过对《GB 4789.3-2016 食品安全国家标准 食品微生物学检验 大肠菌群计数》第二法平板法中不确定度来源进行分析和计算,得出检测结果的不确定度为U=0.057 54,k=2.26,主要影响因素是样品制备、样品稀释、加样和重复检测,其中重复检测对检测结果不确定度的贡献最大。
大肠菌群平板计数法原始记录
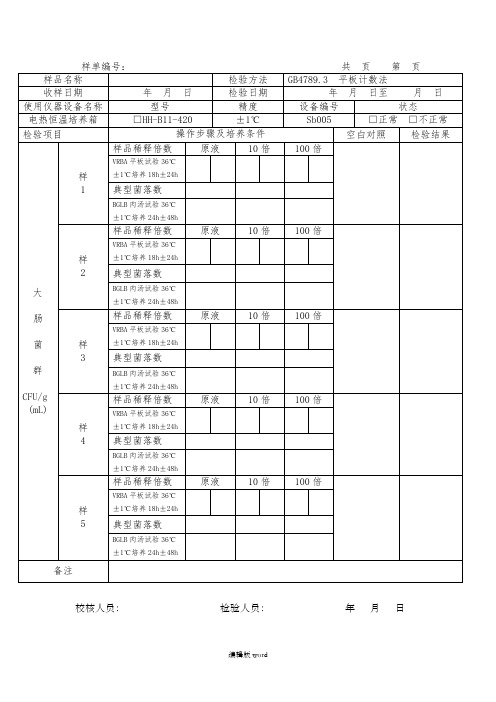
BGLB肉汤试验36℃±1℃培养24h±48h
样
2
样品稀释倍数
原液
10倍
100倍
VRBA平板试验36℃±1℃培养18h±24h
典型菌落数
BGLB肉汤试验36℃±1℃培养24h±48h
样
3
样品稀释倍数
原液
10倍
100倍
VRBA平板试验36℃±1℃培养18h±24h
典型菌落数
BGLB肉汤试验36℃±1℃培养24h±48h
样
4
样品稀释倍数
原液
10倍
100倍
VRBA平板试验36℃±1℃培养18h±24h
典型菌落数
BGLB肉汤试验36℃±1℃培养24h±48h
样
5
样品稀释倍数
原液
10倍
100倍
VRBA平板试验36℃±1℃培养18h±24h
典型菌落数
BGLB肉汤试验36℃±1℃培养24h±48h
备注
校核人员:检验人员:年月日
(此文档部分内容来源于网络,如有侵权请告知删除,文档可自行编辑修改内容,供参考,感谢您的配合和支持)
样单编号:共页第页
样品名称
检验方法
GB4789.3平板计数法
收样日期
年月日
检验日期
年月日至月日
使用仪器设备名称
型号
精度
设备编号
状态
电热恒温培养箱
□HH-B11-420
±1℃
Sb005
□正常□不正常
检验项目
操作步骤及培养条件
空白对照
检验结果
大
肠பைடு நூலகம்
菌
群
CFU/g
(mL)
大肠菌群检验原始记录(平板计数法)
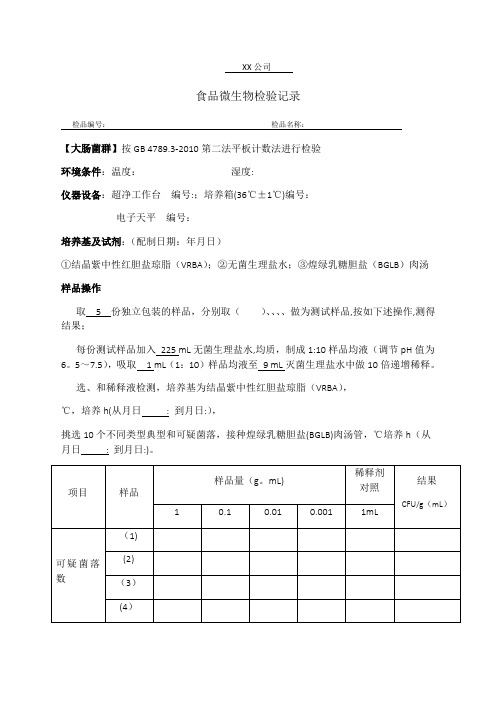
XX公司
食品微生物检验记录
检品编号:检品名称:
【大肠菌群】按GB 4789.3-2010第二法平板计数法进行检验
环境条件:温度:湿度:
仪器设备:超净工作台编号:;培养箱(36℃±1℃)编号:
电子天平编号:
培养基及试剂:(配制日期:年月日)
①结晶紫中性红胆盐琼脂(VRBA);②无菌生理盐水;③煌绿乳糖胆盐(BGLB)肉汤
样品操作
取 5 份独立包装的样品,分别取()、、、、做为测试样品,按如下述操作,测得结果;
每份测试样品加入225 mL无菌生理盐水,均质,制成1:10样品均液(调节pH值为6。
5~7.5),吸取 1 mL(1:10)样品均液至9 mL灭菌生理盐水中做10倍递增稀释。
选、和稀释液检测,培养基为结晶紫中性红胆盐琼脂(VRBA),
℃,培养h(从月日: 到月日:),
挑选10个不同类型典型和可疑菌落,接种煌绿乳糖胆盐(BGLB)肉汤管,℃培养h(从月日: 到月日:)。
标准规定:(标准号: )
n=5 c= m= CFU/g(mL)M= CFU/g(mL)结论:□符合规定□不符合规定
检验者:复核者:检验日期:。
大肠菌群平板计数法能力验证技术方案

大肠菌群平板计数法能力验证技术方案大肠菌群平板计数法是一种常用于测定大肠菌群数量的方法,广泛应用于食品卫生、环境监测以及临床诊断中。
为了保证测试结果的准确可靠,需要进行能力验证。
本文将从样品准备、实验操作、数据处理等方面,提出一种能力验证技术方案。
一、样品准备1.选择适当的样品能力验证样品应具备与真实样品类似的特性,如食品、水样或环境样品等。
可以选择一些常见的食品样品,如牛奶、肉类制品或蔬菜水果。
2.随机抽样从不同批次、不同地点或不同时间采样,确保样品的代表性。
每个样品取样量应根据实际需要确定,在保证结果准确性的前提下尽量减少消耗。
3.样品处理根据实验要求,对样品进行适当的预处理,如均质、稀释等操作。
确保样品中目标细菌的分布均匀,并避免细菌的损失或增加。
二、实验操作1.培养基准备根据大肠菌群的需求,配制适当的培养基。
常用的培养基包括发酵碱菜水平板、郑森琴水平板等。
确保培养基的质量和成分符合实验要求。
2.平板制备3.样品接种取一定量的样品,如10ml,经过适当的处理后,使用无菌吸管均匀涂布在培养基表面。
确保接种量适当,不过多或不过少。
4.孵育条件根据大肠菌群的生长要求,设置适当的孵育温度和时间。
通常情况下,37摄氏度下孵育24小时。
5.结算方法将孵育后的培养皿取出,使用显微镜观察和计数。
根据培养皿上大肠菌群的形状和颜色,判断其是否为目标菌群,并计数。
三、数据处理1.统计计数将每个培养皿上的大肠菌群数量进行统计,得到一个基本的计数值。
对于不同的样品,可以采用平均数、中位数、标准差等指标进行数据描述。
2.结果评估将实验得到的计数结果与参考值进行比较,评估实验的准确度和可靠性。
可以使用误差分析、相关系数等统计方法进行评估。
3.不确定度分析通过不确定度分析,评估实验结果的可靠程度。
可以根据具体情况选择不确定度分析方法,如C表示法、扩展不确定度法等。
4.结果报告将实验结果整理成报告,包括样品信息、实验方法、计数结果、评估结果和不确定度分析等内容。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
XX公司
食品微生物检验记录
检品编号:检品名称:
【大肠菌群】按GB 4789.3-2010第二法平板计数法进行检验
环境条件:温度:湿度:
仪器设备:超净工作台编号:;培养箱(36℃±1℃)编号:
电子天平编号:
培养基及试剂:(配制日期:年月日)
①结晶紫中性红胆盐琼脂(VRBA);②无菌生理盐水;③煌绿乳糖胆盐(BGLB)肉汤样品操作
取 5 份独立包装的样品,分别取()、、、、做为测试样品,按如下述操作,测得结果;
每份测试样品加入225 mL无菌生理盐水,均质,制成1:10样品均液(调节pH值为6.5~7.5),吸取 1 mL(1:10)样品均液至9 mL灭菌生理盐水中做10倍递增稀释。
选、和稀释液检测,培养基为结晶紫中性红胆盐琼脂(VRBA),
℃,培养h(从月日: 到月日:),
挑选10个不同类型典型和可疑菌落,接种煌绿乳糖胆盐(BGLB)肉汤管,℃培养h(从
标准规定:(标准号:)
n=5 c= m= CFU/g(mL)M= CFU/g(mL)
结论:□符合规定□不符合规定
检验者:复核者:检验日期:。
