2015届高考化学一轮复习 第二章第一节 碳、硅及其章节测试 新人教版
2015届高考化学一轮复习 第二章第1节 物质的分类限时规范特训 新人教版

【金版教程】2015届高考化学一轮复习第二章第1节物质的分类限时规范特训新人教版1. 德国著名行业杂志《应用化学》上刊登文章介绍:某中德联合研究小组设计制造了一种“水瓶”,用富勒烯(C60)的球形笼子作“瓶体”,一种磷酸盐作“瓶盖”,恰好可将一个水分子关在里面。
下列说法正确的是( )A. 水、双氧水、水玻璃都是纯净物B. 石墨和C60互称为同位素C. 磷酸钙是可溶性强电解质D. 一定条件下石墨转化为C60是化学变化答案:D解析:本题综合考查了化学基本概念,意在考查考生的应用能力。
水是纯净物,双氧水是H2O2的水溶液、水玻璃是Na2SiO3的水溶液,二者属于混合物,A错误;石墨和C60互称为同素异形体,B错误;磷酸钙是难溶性强电解质,C错误;同素异形体之间的转化是化学变化,D正确。
2. [2013·山西大同调研]分类是化学学习和研究中的常用手段,下列分类依据和结论都正确的是( )A. 浓盐酸、浓硫酸、浓硝酸均具有氧化性,都属氧化性酸B. Na2O、SO2、BaSO4在熔融状态或溶于水时均能导电,都属电解质C. NaOH、HNO3、NaNO3在水溶液中均能电离出离子,都属离子化合物D. NaOH、Na2CO3、NaCl、Na2SO4可按某种标准划为一类物质,分类标准是可溶于水答案:D解析:浓盐酸是非氧化性酸、SO2是非电解质、HNO3是共价化合物、D选项中的物质都易溶于水,只有D选项正确。
3. 某合作学习小组讨论辨析:①生活中使用的漂白粉和肥皂都是混合物,②可用过滤法分离氢氧化铁胶体和氢氧化铁沉淀的混合物,③冰、干冰、冰醋酸都是纯净物,④醋酸、烧碱、纯碱和生石灰分别属于酸、碱、盐和氧化物,⑤水玻璃、有色玻璃和果冻都是胶体,⑥汽油属于混合物,而液氯、醋酸均属于纯净物,⑦烟、雾、豆浆都是胶体。
上述说法正确的是( )A. ①②③⑤B. ①②③④⑥⑦C. ②③④⑤D. ③④⑤⑥答案:B解析:水玻璃属于溶液。
高考化学一轮复习 第一节 碳、硅及无机非金属材料习题讲解课件
精品
4
[考点达标层面] 1.解析:自然界中的硅是以化合态的形式存在,故不能从自然界
中直接获得单质硅。 答案:C 2.解析:Si 与水、浓 H2SO4、浓 HNO3 均不发生反应,但 Si 能 与氢氟酸、NaOH 溶液反应放出 H2。 答案:C
精品
5
考点二 [教材知识层面] (1)高 (2)CO2+H2O H2CO3 SiO2+4HF===SiF4↑+2H2O SiO2+2NaOH===Na2SiO3+H2O 橡胶 CO2+2NaOH===Na2CO3+H2O CO2+NaOH===NaHCO3
第一节 碳、硅及无机非金属材料
考点一 [教材知识层面]
1.
ⅣA ⅣA 空间网状
2.(1)(提示:①—c,②—a,③—e,④—b,⑤—d)
点燃
点燃
(2)①2C+O2=====2CO C+O2=====CO2
精品
1
高温 2CuO+C=====2Cu+CO2↑
高温 CO2+C=====2CO
高温 C+H2O(g) =====CO+H2
精品
11
[高考考查层面]
1.解析:玻璃的成分中含有 SiO2,能与 NaOH 溶液反应生成 粘性很强的 Na2SiO3 而发生粘连,反应方程式为 SiO2+ 2NaOH===Na2SiO3+H2O。由于钙长石和钠长石中氧原子 的物质的量分数相同,钠长石中钠与铝的原子个数比为
1∶1,扩 2 倍后可知钙长石中钙和铝的原子个数比为 1∶2。
精品
9
答案:
(1) (2) (3) (4)
B
④
D
④
A
④
③
精品
10
考点三
[教材知识层面]
高中化学 一轮复习人教版 碳、硅及其化合物和无机非金属材料 单元测试(word版)

碳、硅及其化合物和无机非金属材料一、选择题:本题共7小题,每小题2分,共14分。
每小题只有一个选项符合题意。
1.《厉害了,我的国》“中国名片”中航天、军事、天文等领域的发展受到世界瞩目,它们与化学有着密切联系。
下列说法正确的是()A.“中国天眼”的“眼眶”是钢铁结成的圈梁,属于新型无机非金属材料B.“中国歼-20”上用到的氮化镓材料属于合金材料C.“神舟十一号”宇宙飞船返回舱外表面使用的高温结构陶瓷是新型无机非金属材料D.“天宫二号”空间实验室的太阳能电池板的主要材料是二氧化硅2.化学与科学、技术、社会、环境密切相关。
下列说法正确的是()A.计算机的芯片材料是高纯度二氧化硅B.战国所著《周礼》中记载沿海古人“煤饼烧蛎房成灰”(“蛎房”即牡蛎壳),并把这种灰称为“蜃”,“蜃”的主要成分为Ca(OH)2C.“绿水青山就是金山银山”,矿物燃料经过脱硫脱硝处理,可以减少SO2、NO2的排放D.2M+N===2P+2Q,2P+M===Q(M、N为原料,Q为期望产品),不符合“绿色化学”的理念3.下列叙述正确的是()A.向含有CaCO3沉淀的水中通入CO2至沉淀恰好溶解,再向溶液中加入NaHCO3饱和溶液,又有CaCO3沉淀生成B.向Na2CO3溶液中逐滴加入含等物质的量HCl的稀盐酸,生成的CO2与原Na2CO3的物质的量之比为1 2C.等质量的NaHCO3和Na2CO3分别与足量盐酸反应,在同温同压下,生成的CO2体积相同D.向饱和BaCl2溶液中先通入CO2,再通入NH3,有BaCO3沉淀析出4.下列说法中不正确的是()A.SiO2能与HF反应,因此可用HF刻蚀玻璃B.向Na2SiO3溶液中逐滴加入稀盐酸制备硅酸凝胶C.氮化硅是一种重要的结构陶瓷材料,其化学式为Si3N4D.石英是良好的半导体材料,可以制成光电池,将光能直接转化成电能5.下列除杂方法正确的是()A.SiO2中含Al2O3杂质,可以加入足量NaOH溶液,然后过滤除去B.CO2中含有CO杂质,可以通入盛有灼热CuO的玻璃管C.CO2中含有HCl杂质,可以通过盛有饱和Na2CO3溶液的洗气瓶D.Na2CO3溶液中含有Na2SiO3杂质,可以通入足量的CO2,然后过滤6.下表各组物质之间通过一步反应不可以实现如图所示转化关系的是()选项X Y ZA NH3NO2HNO3B SiO2Na2SiO3H2SiO3C Al2O3NaAlO2Al(OH)3D CO2Na2CO3NaHCO37容器①中发生的反应①为Si(粗)+3HCl(g)===SiHCl3(l)+H2(g);容器②中发生的反应②为SiHCl3(l)+H2(g)===Si(纯)+3HCl(g)。
高三化学一轮复习碳、硅练习含答案

碳、硅一、选择题1.等物质的量的Na和Al两种金属加入足量的水中,生成26.88L(标准状况下)的气体,则下列描述错误的是()A.金属Al无剩余B.c (Na+)=c (AlO2-)C.所得溶液呈碱性D.Na的物质的量是0.6mol2.对金属制品进行抗腐蚀处理,可延长其使用寿命。
以下为铝材表面处理的一种方法:碱洗的目的是除去铝材表面的自然氧化膜,为将碱洗槽液中的铝以沉淀形式回收,最好向槽液中加入下列试剂中的()A.NH3B.CO2 C.NaOH D.HNO33.用除去表面氧化膜的细铝条紧紧缠绕在温度计上,将少许硝酸汞溶液滴到铝条表面,置于空气中,很快铝条表面产生“白毛”,且温度明显上升.下列分析错误的是()A.Al和O2化合放出热量B.硝酸汞是催化剂C.涉及了:2Al+3Hg2+→2Al3++3HgD.“白毛”是氧化铝4.硅在自然界最主要的存在形式是()①硅②二氧化硅③硅酸盐①② B. ①③ C. ②③ D. ①②③5将过量CO2分别通入下列物质的溶液中:①BaCl2;②Na2SiO3;③Ca(OH)2;④饱和Na2CO3溶液;⑤NaAlO2,最终有白色沉淀析出的是()A.①②③④⑤B.②④⑤C.①②③D.②③⑤6半导体工业中,有一句行话:“从沙滩到用户”,即由SiO2制取Si。
制取过程中不涉及的化学反应是()A.2C+SiO2Si+2CO↑B.SiO2+2NaOH Na2SiO3+H2OC.Si+2Cl2SiCl4 D.SiCl4+2H2Si+4HCl7.硅作为一种新型能源被广泛开发利用,关于其有利因素的下列说法中,你认为不正确的是()A.硅燃烧产物对环境产生的污染容易得到有效控制B.从Si(s)+O2(g)SiO2(s)ΔH=-858.6 kJ·mol-1可知,硅燃烧放出的热量多C.自然界中硅的储量丰富,可以从自然界直接获得单质硅D.硅便于运输、贮存,从安全角度考虑,硅是最佳的燃料之一8下列说法正确的是()A.高温下,可在试管内完成焦炭和石英砂(SiO2)制取硅的反应B.CO2和钠在一定条件下反应可以得到金刚石和碳酸钠,反应中氧化剂和还原剂的物质的量之比是3∶4C.现代海战通过喷放液体SiCl4(极易水解)和液氨可产生烟幕,其主要成分是NH4Cl D.从燃煤烟道灰中(含GeO2)提取半导体材料单质锗(Ge),没有发生氧化还原反应9.下列事实中能证明碳的非金属性比硅强的是①往Na2SiO3溶液中通入CO2产生白色沉淀②石墨是导体,晶体硅是半导体③制玻璃过程中发生反应:Na2CO3+SiO2=====高温Na2SiO3+CO2↑④CH4比SiH4稳定A.①④B.②③C.③④D.①②10下列物质间的转化不能通过一步反应完成的是()A. SiO2SiB. CO2 CC. SiO2H2SiO3D. Si Na2SiO311已知甲、乙、丙和X是四种中学化学中常见的物质,其转化关系如图所示,则甲和X不可能是()A.C、O2B.SO2、NaOH溶液C.Cl2、FeD.Al、NaOH溶液12如何解决好碳排放问题是关系到人类可持续发展的重大课题之一。
2015届高考化学一轮总复习讲义 第一节 碳、硅及其化合物

第一节碳、硅及其化合物明考纲要求理主干脉络1.了解碳、硅单质及其化合物的主要性质及应用。
2.了解碳、硅及其化合物对环境质量的影响。
3.了解常见无机非金属材料的性质和用途。
碳、硅单质的性质及应用1.单质的存在形态、物理性质和用途 碳 硅 存在形态 游离态和化合态化合态物理性质金刚石:熔点高、硬度大 石墨:硬度小、电的良导体灰黑色固体,有金属光泽、熔点高、硬度大,有脆性用途 金刚石用作切割刀具,石墨用作电极、铅笔芯半导体材料、太阳能电池和合金材料2.碳和硅的化学性质(1)碳单质的化学性质——还原性。
C +2O ――→CO 2、SiO 2O 2不足 C 0常温下不活泼――→CuO 、浓硫酸O 2充足C +4O 2 ①与O 2的反应:O 2不足:2C +O 2=====点燃 2CO ;O 2充足:C +O 2=====点燃 CO 2。
②与其他物质的反应:a .与CuO 反应:2CuO +C=====高温 2Cu +CO 2↑(可用于金属的冶炼);b .与CO 2反应:CO 2+C=====高温2CO ;c .与水蒸气反应:C +H 2O(g)=====高温 CO +H 2(制水煤气);d .与浓硫酸反应:C +2H 2SO 4(浓)=====△ CO 2↑+2SO 2↑+2H 2O 。
(2)硅的化学性质——还原性。
不能被浓硫酸、浓硝酸等强氧化剂氧化 Si①与氢氟酸反应:Si +4HF===SiF 4↑+2H 2↑;②与NaOH 溶液反应:Si +2NaOH +H 2O===Na 2SiO 3+2H 2↑; ③与O 2反应:Si +O 2=====△SiO 2。
1.判断以下描述的正误(正确的打“√〞,错误的打“×〞)。
(1)(2013·广东高考)高温下用焦炭还原SiO 2制取粗硅。
( )(2)(2013·浙江高考)碳有多种同素异形体,而氧不存在同素异形体。
( ) (3)(2012·新课标全国卷)单质硅是将太阳能转变为电能的常用材料。
高考化学一轮复习 第二章 第一讲 物质的组成性质和分类试题

回夺市安然阳光实验学校第一讲物质的组成、性质和分类[考纲展示]1.了解分子、原子、离子等概念的含义。
了解原子团的定义。
2.理解物理变化与化学变化的区别与联系。
3.理解混合物和纯净物、单质和化合物、金属和非金属的概念。
4.理解酸、碱、盐、氧化物的概念及其相互联系。
5.了解胶体是一种常见的分散系。
考点一物质的组成与分类[学生用书P25]一、元素、物质及微粒间的关系二、物质的分类1.概述(1)分类是学习和研究化学物质及其变化的一种常用科学方法。
(2)分类应依据一定的进行,不同,分类方法也不相同。
2.分类法常用的两种分类法是交叉分类法和树状分类法。
由于物质分类可以有不同的,那么对某一物质而言就可以按不同的分类分属于不同的物质类别。
三、常见无机化合物的分类无机化合物⎩⎪⎪⎨⎪⎪⎧氢化物:HCl、H2S、H2O、NH3等氧化物⎩⎪⎨⎪⎧不成盐氧化物:CO、NO等成盐氧化物⎩⎪⎨⎪⎧碱性氧化物:Na2O、CaO等酸性氧化物:CO2、P2O5等氧化物:Al2O3等过氧化物:Na2O2、H2O2等无机化合物⎩⎪⎪⎪⎪⎪⎪⎪⎨⎪⎪⎪⎪⎪⎪⎪⎧酸⎩⎪⎪⎪⎨⎪⎪⎪⎧按电离出的H+数⎩⎪⎨⎪⎧一元酸:HCl、HNO3等二元酸:H2SO4、H2S等三元酸:H3PO4等按酸根是否含氧⎩⎪⎨⎪⎧无氧酸:HCl、H2S等含氧酸:HClO4、H2SO4等按酸性强弱⎩⎪⎨⎪⎧强酸:HCl、H2SO4、HNO3等弱酸:CH3COOH、HF等按有无挥发性⎩⎪⎨⎪⎧挥发性酸:HNO3、HCl等难挥发性酸:H2SO4、H3PO4等碱⎩⎪⎨⎪⎧按水溶性⎩⎪⎨⎪⎧可溶性碱:NaOH、KOH、Ba(OH)2等难溶性碱:Mg(OH)2、Cu(OH)2等按碱性强弱⎩⎪⎨⎪⎧强碱:NaOH、Ba(OH)2、KOH等弱碱:NH3·H2O等盐⎩⎪⎨⎪⎧正盐:BaSO4、KNO3、NaCl等酸式盐:NaHCO3、KHSO4等碱式盐:Cu2(OH)2CO3等复盐:KAl(SO4)2·12H2O等正确理解“一定”、“不一定”,规避概念失分点(1)碱性氧化物一定是金属氧化物,但金属氧化物不一定是碱性氧化物(如Mn2O7为酸性氧化物、Al2O3为氧化物、Na2O2为过氧化物)。
高考化学一轮总复习 4.1碳、硅及无机非金属材料习题 新人教版

4.1碳、硅及无机非金属材料时间:45分钟满分:100分一、选择题(每题6分,共66分)1.下列说法正确的是( )①单质硅是将太阳能转变为电能的常用材料②合成纤维和光导纤维都是新型无机非金属材料③盛放NaOH溶液时,使用带磨口玻璃塞的玻璃瓶④Mg2+、H+、SiO2-3、SO2-4在水溶液中能大量共存⑤向含K+、Na+、Br-、SiO2-3的溶液中通入CO2后仍能大量共存⑥SiO2与酸、碱均不反应⑦SiO2不与任何酸反应,可用石英制造耐酸容器⑧SiO2是酸性氧化物,能与NaOH溶液反应⑨水玻璃可用于生产黏合剂和防火剂A.①②⑥⑦⑨ B.①⑧⑨C.②③⑧⑨ D.①④⑤⑧答案 B解析合成纤维属于有机高分子材料,②错;2NaOH+SiO2===Na2SiO3+H2O,Na2SiO3有粘性,可将玻璃瓶塞与瓶颈粘连,③错;2H++SiO2-3===H2SiO3↓,④错;CO2+H2O+SiO2-3===H2SiO3↓+CO2-3,⑤错;SiO2可与HF反应,也能与强碱溶液反应,⑥、⑦错,B正确。
2.[2017·天津市高三质检]下列说法正确的是( )A.SiO2和CO2都是酸性氧化物,都是共价化合物B.为防止月饼等富脂食品氧化变质,可在包装袋中放入硅胶C.NaHCO3溶液中含有Na2SiO3杂质,可通入少量CO2后过滤D.SiO2中含Al2O3杂质,可加入足量NaOH溶液然后过滤除去答案 A解析A项,SiO2、CO2分别为H2SiO3、H2CO3对应的酸性氧化物,都是共价化合物,正确;B项,硅胶具有吸水性,可以防止食品受潮,而不能防止食品氧化,错误;C项,除去NaHCO3溶液中的Na2SiO3杂质,应通入足量CO2,发生反应:Na2SiO3+2CO2+2H2O===2NaHCO3+H2SiO3↓,错误;D项,SiO2、Al2O3均能与NaOH溶液反应,应加入稀盐酸后过滤,错误。
3.[2017·合肥高三质检]硅及其化合物是带来人类文明的重要物质。
高考化学一轮复习 第一节 一卷冲关的课后练案 新人教版选修2

高考化学一轮复习 第一节 一卷冲关的课后练案 新人教版选修2一、选择题1.以下关于氨碱法与联合制碱法的认识,不.正确的是( ) A .氨碱法生产纯碱的原料便宜易得,步骤简单,是最早的制碱工艺B .联合制碱法又称侯氏制碱法,是侯德榜在氨碱法的基础上改造形成的C .在联合制碱法中,氯化钠的利用率比氨碱法中的高D .联合制碱法避免了氨碱法中对氯化钙的处理解析:氨碱法生产纯碱的原料为食盐和石灰石,便宜易得,但它并非最早的制碱工艺,最早的制碱方法是路布兰法。
氨碱法的产品纯度较高,制造步骤也比较简单,但氯化钠的利用率不高,生产过程中产生的氯化钙难处理,是氨碱法的一大缺点。
联合制碱法是侯德榜在氨碱法的基础上改造形成的,因此也称侯氏制碱法,该法继承了氨碱法的优点,克服了它的缺点。
答案:A2.下列使用化肥、农药的描述中正确的是( )A .高温多雨时比较适合施用钾肥B .长期施用硫铵会造成土壤板结C .石硫合剂必须与硫酸混合后才能施用D .过磷酸钙必须经硫酸处理后才能施用解析:本题考查化肥和农药的使用。
高温多雨施用钾肥容易造成流失,A 错;长期使用硫铵会造成土壤板结,B 对;石硫合剂有强碱性,不能与硫酸混合施用,C 错;过磷酸钙可以被植物吸收,不用经硫酸处理,D 错。
答案:B3.能正确表示下列反应的化学方程式是( )A .黄铁矿煅烧:2FeS 2+5O 2=====高温2FeO +4SO 2B .石英与石灰石共熔:SiO 2+CaO=====高温CaSiO 3C .氨的催化氧气:4NH 3+5O 2=====催化剂△4NO +6H 2OD .氯气与石灰乳反应:2Cl 2+2Ca(OH)2===CaCl 2+CaClO 2+2H 2O解析:黄铁矿煅烧:4FeS 2+11O 2=====高温2Fe 2O 3+8SO 2。
石英与石灰石共熔:SiO 2+CaCO 3=====高温CaSiO 3+CO 2↑。
氯气与石灰乳反应:2Cl 2+2Ca(OH)2===CaCl 2+Ca(ClO)2+2H 2O 。
高三化学一轮复习强化训练碳硅及其化合物2(含解析)

碳、硅及其化合物1.碳循环(如图)对人类生存、发展有着重要的意义。
下列说法错误的是( )1.答案 D 乙烯的年产量是衡量一个国家石油化工发展水平的标志,D错误。
2.下列说法中不正确的是( )2.答案 D 自然界中的硅元素以化合态形式存在,无游离态的单质硅存在,D错误。
3.下列反应不能一步完成的是( )2 Na2SiO32 H2SiO32 CaSiO32SiO3 SiO23.答案 B 二氧化硅不溶于水,则SiO2 H2SiO3不能一步完成,B符合题意。
4.工业制取高纯硅的反应流程如下,其中有两个反应类型相同,这两个反应的类型是( )4.答案 A 二氧化硅在高温下与碳发生反应得到CO和硅,属于置换反应;粗硅和氯气反应得到纯净的SiCl4,属于化合反应;在高温下SiCl4与氢气反应可生成硅和氯化氢,属于置换反应,因此A正确。
5.以下表示的是碳及其化合物的转化关系,其中涉及的基本反应类型依次是( )A.置换、化合、复分解、分解B.置换、复分解、化合、分解C.化合、置换、分解、复分解D.置换、化合、分解、复分解5.答案 A6.下列物品或设备:①水泥路桥②门窗玻璃③水晶项链④石英钟表⑤玛瑙手镯⑥硅太阳能电池⑦光导纤维⑧计算机芯片,所用材料为SiO2或要用到SiO2的是( )A.①②③④⑤⑦C.③④⑤⑦⑧D.①②⑦⑧6.答案 A 硅太阳能电池、计算机芯片均是硅单质的用途的体现。
7.下列单质或化合物性质的描述正确的是( )A.食品包装中常放入有硅胶和铁粉的小袋,防止食物受潮和氧化变质2和水反应直接制得2既能和NaOH溶液反应又能和氢氟酸反应,所以是两性氧化物D.自然界硅元素的贮量丰富,并存在大量的单质硅7.答案 A 硅胶具有吸水性,铁粉具有还原性,食品包装中常放入有硅胶和铁粉的小袋,可以防止食物受潮和氧化变质,A正确;SiO2与水不反应,不能与水反应直接制得硅酸,B错误;二氧化硅属于酸性氧化物,C错误;自然界硅元素的贮量丰富,但并不存在单质硅,D错误。
高中化学 一轮复习碳硅及其化合物

碳、硅及其化合物【练习题】1.判断正误(正确的打“√”,错误的打“×”)。
(1)碳有多种同素异形体,而氧不存在同素异形体( )(2)单质硅常用作半导体材料和光导纤维( )(3)硅在自然界中只以化合态的形式存在( )(4)石墨在一定条件下能转化成金刚石,该转化属于物理变化( )(5)燃料燃烧产物CO 2是温室气体之一( )(6)将某溶液与稀盐酸反应产生的气体通入澄清石灰水,石灰水变浑浊,说明该溶液中一定含有CO 2-3( ) (7)标准状况下,5.6 L CO 2气体中含有氧原子数为0.5N A ( )(8)将澄清石灰水滴入某溶液证明其中存在CO 2-3( )(9)用活性炭去除冰箱中的异味,没有发生化学反应( )(10)利用如图装置除去CO 气体中的CO 2气体( )(11)元素碳的单质只存在金刚石和石墨两种同素异形体( )(12)甲、乙、丙均含有相同的某种元素,它们之间具有转化关系:甲――→丁乙丁甲丙,若甲为焦炭,则丁可能是O 2( )(13)因为HF 与SiO 2反应,故用氢氟酸在玻璃器皿上刻蚀标记( )(14)下列转化在一定条件下能够实现:SiO 2――→HCl (aq )SiCl 4――→H 2高温Si( ) (15)石英砂可用于生产单晶硅( )(16)用NaOH 溶液不能分离氧化铁中混有的二氧化硅( )(17)物质间转化能一步实现:粗硅――→Cl 2高温SiCl 4――→H 2高温Si( ) (18)硅的最高价氧化物可用于制造光导纤维( )(19) SiO 2既能和NaOH 溶液反应,又能和氢氟酸反应,所以是两性氧化物( )(20) Si 和SiO 2都用于制造光导纤维( )(21) SiO 2可与HF 反应,因而氢氟酸不能保存在玻璃瓶中( )(22)高温下用焦炭还原SiO 2制取粗硅( )(23)硅胶作袋装食品的干燥剂的过程中没有发生化学变化( )(24) pH =2的溶液中可能大量存在Na +、NH +4、SiO 2-3( )(25)向Na 2SiO 3溶液中滴加稀盐酸的离子方程式:Na 2SiO 3+2H +===H 2SiO 3↓+2Na+( )(26)向Na 2SiO 3溶液中通入过量SO 2的离子方程式:SiO 2-3+SO 2+H 2O===H 2SiO 3↓+SO 2-3( )(27)烧结黏土制陶瓷,不涉及化学反应( )2.大气中CO 2含量的增加会加剧“温室效应”。
高考化学一轮复习 第二章 化学物质及其变化 第一

回夺市安然阳光实验学校第一讲物质的组成、性质和分类[课后达标训练]一、选择题1.(2018·新余联考)分类是科学研究的重要方法,下列物质分类不正确的是( )A.化合物:干冰、冰水共存物、烧碱、小苏打B.同素异形体:活性炭、C60、C80、石C.非电解质:乙醇、四氯化碳、氯气、葡萄糖D.混合物:漂白粉、纯净矿泉水、盐酸、大理石解析:选C。
干冰、冰水共存物、烧碱、小苏打都是由两种或两种以上元素组成的化合物,故A正确;活性炭、C60、C80、石都是由碳元素组成的不同单质,互为同素异形体,故B正确;氯气是单质,不是非电解质,故C错误;漂白粉、纯净矿泉水、盐酸、大理石都含有两种以上物质,属于混合物,故D正确。
2.胶体与溶液最简单的鉴别方法和本质区别分别是( )A.能否透过滤纸,是否有丁达尔效应B.是否无色透明,是否稳定C.是否有丁达尔效应,分散质粒子直径大小D.是否稳定,能否电泳解析:选C。
胶体分散系与其他分散系的本质区别是分散质粒子直径大小,鉴别溶液和胶体最简单的方法是丁达尔效应。
3.(2015·高考重庆卷)中华民族有着光辉灿烂的发明史,下列发明创造不涉及化学反应的是( )A.用胆矾炼铜B.用铁矿石炼铁C.烧结黏土制陶瓷D.打磨磁石制指南针解析:选D。
A.胆矾炼铜就是“湿法炼铜”,其原理是将胆矾溶于水,再将铁放入胆矾溶液中把铜置换出来,是化学反应。
B.铁矿石炼铁是将原料(铁矿石、焦炭、石灰石和空气)加入高炉中,在高炉中发生一系列化学反应,生成铁单质,是化学反应。
C.黏土烧结制成陶瓷的过程中有新物质生成,是化学反应。
D.四氧化三铁常称作“磁性氧化铁”,是磁石的主要成分,打磨磁石制指南针,只是磁石的形状发生变化,是物理变化。
4.下列生活中的做法没有利用物质化学性质的是( )A.葡萄酒中添加二氧化硫B.鲜花店的老板用浸泡了高锰酸钾的硅土延长鲜花的保存期C.用双氧水漂洗衣服上的污渍D.夏天超市用干冰给物质降温解析:选D。
高考第一轮复习——无机非金属材料的主角—碳和硅

年级高三学科化学版本人教新课标版课程标题高考第一轮复习——无机非金属材料的主角—碳和硅编稿老师刘学超一校张琦锋二校林卉审核张美玲一、考纲要求1. 了解C、Si元素的单质及其重要化合物的主要性质及应用。
2. 了解C、Si元素的单质及其重要化合物对环境质量的影响。
3. 以上知识的综合应用。
二、考题规律C和Si的单质及其化合物的知识在高考中经常有所涉及、主要以选择题的形式来考查。
1. 对C、Si元素的单质及其化合物知识的考查,主要是以实验探究、框图推断为主要命题形式。
2. 对硅及其化合物在生产、生活中的应用的考查。
通常是以新材料、新技术为背景考查常识性知识,难度较小。
三、考向预测C和Si的单质及其化合物的知识在高考中主要涉及:1. 金刚石、石墨、C60、晶体硅、二氧化碳、二氧化硅的结构和性质的比较;2. 碳和一氧化碳的还原性、一氧化碳和二氧化碳的制取、收集、检验和鉴别;3. CO2和NaOH、SiO2与C、NaOH等反应产物的确定及计算;4. 典型的碳酸盐的性质及应用;5. 化学理论在硅酸盐工业实际中的应用;6. 推测新型无机非金属材料的结构特点或分析其用途。
尤其应注意碳、硅的单质及其化合物与基本理论和实验等内容结合的题目。
一、碳、硅及其重要化合物二、碳、硅元素的单质及其化合物的特性(1)一般情况,非金属元素单质的熔、沸点低,硬度小,但硅、金刚石的熔、沸点高,硬度大,其中金刚石为硬度最大的物质。
(2)一般情况,非金属元素的单质为绝缘体,但硅为半导体,石墨为电的良导体。
(3)一般情况,较强氧化剂+较强还原剂=较弱氧化剂+较弱还原剂,而碳却还原出比它更强的还原剂:SiO2+2C Si+2CO↑,FeO+C Fe+CO↑。
(4)非金属单质与碱反应一般是非金属既作氧化剂又作还原剂,而Si与碱溶液反应却只作还原剂:Si+2NaOH+H2O=Na2SiO3+2H2↑。
(5)一般情况,较活泼金属+酸―→盐+氢气,然而Si是非金属,却能与氢氟酸发生反应:Si+4HF=SiF4↑+2H2↑。
高考化学一轮练习碳、硅、氯及其化合物人教版

排查落实练七碳、硅、氯及其化合物(教师用书独具,学生用书本部分需单独订购。
)一、碳、硅及其化合物1. 知识网络构建2. 重要反应必练写出下列反应的方程式,是离子反应的写出离子方程式①Si和NaOH溶液的反应:________________________________________________________________________②SiO2和NaOH溶液的反应:________________________________________________________________________③工业上制备粗硅:________________________________________________________________________④向Na2SiO3溶液中通入少量CO2气体:________________________________________________________________________⑤Si与氢氟酸的反应:________________________________________________________________________⑥氢氟酸腐蚀玻璃:________________________________________________________________________⑦Mg在CO2中燃烧:________________________________________________________________________⑧C与CO2高温下反应:________________________________________________________________________⑨工业制备水煤气:________________________________________________________________________ ⑩Na2CO3与SiO2在高温下反应:________________________________________________________________________ ⑪向苯酚钠溶液中通入少量CO2气体:________________________________________________________________________________________________________________________________________________ ⑫向漂白粉溶液中通入过量CO 2气体:________________________________________________________________________________________________________________________________________________3. 实验现象强化记忆①向澄清石灰水中通入CO 2气体至过量,其现象是________________________________________________________________________。
高考化学一轮复习 新人教版课时13碳、硅及其化合物
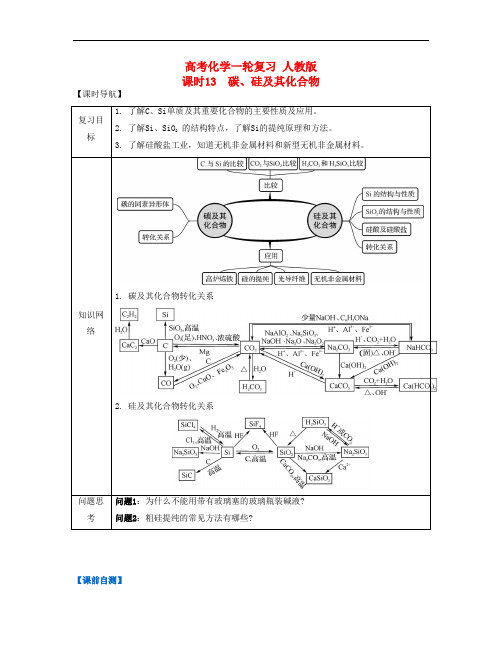
高考化学一轮复习人教版课时13 碳、硅及其化合物【课时导航】复习目标1. 了解C、Si单质及其重要化合物的主要性质及应用。
2. 了解Si、SiO2的结构特点,了解Si的提纯原理和方法。
3. 了解硅酸盐工业,知道无机非金属材料和新型无机非金属材料。
知识网络1. 碳及其化合物转化关系2. 硅及其化合物转化关系问题思考问题1:为什么不能用带有玻璃塞的玻璃瓶装碱液?问题2:粗硅提纯的常见方法有哪些?【课前自测】1. (全国各地高考试题汇集)判断下列说法是否正确,正确的划“√”,错误的划“×”。
(1)Si和SiO2都用于制造光导纤维( )(2)NH4F水溶液中含有HF,因此NH4F溶液不能存放于玻璃试剂瓶中( )(3)合成纤维和光导纤维都是新型无机非金属材料( )(4)漂白粉、石英都属于纯净物( )(5)因为晶体硅熔点高、硬度大,所以可用于制作半导体材料( )(6)二氧化硅不与强酸反应,可用石英器皿盛放氢氟酸 ( )(7)浓硫酸可刻蚀石英制艺术品( )(8)用含硅胶、铁粉透气小袋与食品一起密封保存过程中没有化学变化( )(9)氢氟酸雕刻玻璃不涉及化学变化( )(10)硬度比较:晶体硅<金刚石( )(11)烧结黏土制陶瓷不涉及化学反应( )(12)SiO2既能和氢氧化钠溶液反应又能和氢氟酸反应,所以是两性氧化物( )(13)可用磨口玻璃瓶保存NaOH溶液( )(14)水玻璃可用于生产黏合剂和防火剂( )【答案】(1)×(2)√(3)×(4)×(5)×(6)×(7)×(8)×(9)×(10)√(11)×(12)×(13)×(14)√【解析】(1)SiO2用于制造光导纤维,Si用于制造半导体材料;(2)NH4F水解产生HF,HF易和玻璃中的SiO2反应,所以NH4F溶液不能存放于玻璃试剂瓶中;(3)合成纤维不是无机非金属材料,而是有机物;(4)漂白粉是次氯酸钙和氯化钙的混合物,石英的主要成分是二氧化硅;(5)晶体硅可用于制作半导体材料是因为其位于金属与非金属交界处;(6)HF能与石英中的成分SiO2发生反应:SiO2+4HF SiF4↑+2H2O,所以石英容器不能存放氢氟酸;(7)浓硫酸不与石英的成分二氧化硅发生反应,而二氧化硅与氢氟酸反应,所以工艺师用氢氟酸刻蚀石英制艺术品;(8)硅胶具有吸水性,可防止食品受潮,属于物理变化;铁粉可防止食品被氧化,属于化学变化;(9)HF 能与玻璃的成分SiO2发生反应:SiO2+4HF SiF4↑+2H2O,因此用于雕刻玻璃,属于化学变化;(10)晶体硅与金刚石都为原子晶体,原子半径:碳<硅,键长:C—C<Si—Si,键长越短,键能越大,则硬度越大;(11)制陶瓷的原料是黏土,发生化学变化生成硅酸盐产品;(12)二氧化硅可以与碱反应生成盐和水,因此二氧化硅是酸性氧化物,二氧化硅能和氢氟酸反应是二氧化硅的特性;(13)玻璃中含有二氧化硅,能与氢氧化钠反应生成硅酸钠,使瓶塞与瓶口黏连在一起。
高考化学一轮复习 第二章第一节 碳硅及其测试

回夺市安然阳光实验学校高考化学一轮复习第二章第一节碳、硅及其章节测试新人教版1.下列关于碳和硅的叙述中,正确的是( )A.其氧化物都能与NaOH溶液反应B.其单质在加热时都能跟O2反应C.其氧化物都能溶于水生成相应的酸D.碳和硅两种元素共有两种单质解析:选B CO与NaOH溶液不反应,A错误;SiO2与水不反应,C错误;碳有多种同素异形体,D错误。
2.(2014·银川模拟)下列说法中不正确的是( )A.因SiO2不溶于水,故H2SiO3不是SiO2对应的酸B.CO2通入水玻璃可以得到硅酸沉淀C.SiO2熔点高、硬度大D.氢氟酸能够雕刻玻璃,故不能用玻璃瓶来盛装氢氟酸解析:选A H2SiO3对应的酸性氧化物是SiO2,但SiO2不能直接与水反应生成H2SiO3。
3.下列变化中,不能一步实现的是( )A.Na2SiO3―→H2SiO3 B.H2SiO3―→SiO2C.SiO2―→H2SiO3D.SiO2―→Na2SiO3解析:选C Na2SiO3――→盐酸H2SiO3;H2SiO3――→△SiO2,SiO2――→NaOH Na2SiO3,SiO2不能一步转化为H2SiO3。
4.(2014·济南联考)下列离子方程式的书写正确的是( )A.水玻璃中通入过量二氧化碳:Na2SiO3+CO2+H2O===2Na++CO2-3+H2SiO3 B.澄清石灰水中通入过量二氧化碳:Ca(OH)2+2CO2===Ca2++2HCO-3C.硅与氢氟酸的反应:Si+4H++4F-===SiF4↑+2H2↑D.二氧化硅溶于烧碱溶液中:SiO2+2OH-===SiO2-3+H2O解析:选D Na2SiO3是强电解质,应拆成Na+、SiO2-3,且应生成HCO-3,A 错;B项正确写法是CO2+OH-===HCO-3;C项,氢氟酸是弱酸,不能拆分成H+和F-。
5.硅作为一种新型能源被广泛开发利用,关于其有利因素的下列说法中,你认为不正确的是( )A.硅燃烧产物对环境产生的污染,容易得到有效控制B.从Si(s)+O2(g)=====△SiO2(s) ΔH=-858.6 kJ·mol-1可知,硅燃烧放出的热量多C.自然界中硅的储量丰富,可以从自然界直接获得单质硅D.硅便于运输、贮存,从安全角度考虑,硅是最佳的燃料之一解析:选C 硅在自然界中以化合态的形式存在,需通过化学反应才能获得单质硅。
高考化学(人教版)一轮复习知识点同步练习卷:无机非金属材料的主角硅

高考化学(人教版)一轮复习知识点同步练习卷:无机非金属材料的主角硅一、选择题(此题包括10小题,每题5分,共50分)1.化学与环境、资料、动力等关系亲密。
以下说法正确的选项是〔〕A.燃烧废旧塑料以防止〝白色污染〞B.少量CO2排放可招致酸雨的构成C.积极开发风力、太阳能发电,改善动力结构D.玛瑙、水晶、钻石、红宝石等装饰品的主要成分都是硅酸盐【答案】C2.单质Z是一种罕见的半导体资料,可由X经过如以下图所示的路途制备,其中X为Z的氧化物,Y为氢化物,分子结构与甲烷相似,回答以下效果:以下说法正确的选项是〔〕A.X为酸性氧化物,能与碱反响,不能与酸反响B.Y的化学式为SiH4C.X、Z都含有非极性共价键D.X与Mg在加热条件下反响的化学方程式为SiO2+2Mg2MgO+Si【答案】B3.硅及其化合物是带来人类文明的重要物质。
以下说法正确的选项是〔〕A.陶瓷、水晶、水泥、玻璃都属于硅酸盐B.SiO2是非金属氧化物,它不与任何酸反响C.可以用焦炭恢复二氧化硅消费硅:2C+SiO Si+2CO↑D.高纯硅可用于制造光导纤维,高纯二氧化硅可用于制造太阳能电池【答案】C4.以下物质①氢氟酸②浓硫酸③烧碱溶液④Na2CO3固体⑤硝酸⑥石灰石,其中在一定条件下能与SiO2反响的有〔〕A.①②B.全部C.①③④⑤D.①③④⑥【答案】D5.以下说法正确的选项是〔〕A.高温下,可用焦炭和石英砂〔SiO2〕制取高纯度硅B.CO2和钠在一定条件下可以失掉金刚石和碳酸钠,反响中氧化剂和恢复剂之比是4:1 C.用高纯度硅作为光导纤维的主要资料D.现代海战经过喷放液体SiCl4〔极易水解〕和液氨可发生烟幕,其主要成分是NH4Cl 【答案】D6.以下关于硅资料的说法正确的选项是〔〕A.玛瑙的主要成分是硅酸盐B.制普通玻璃的原料是石灰石、纯碱和石英砂C.光导纤维的主要成分是晶体硅D.水晶项链、玻璃、水泥和陶瓷都是硅酸盐制品【答案】B7.以下试剂可用带磨口玻璃塞的玻璃试剂瓶保管的是〔〕A.氢氟酸B.硫酸C.碳酸钠溶液D.氧氧化钠溶液【答案】B8.证明生石灰中既混有石英,又混有石灰石的正确方法是〔〕A.参与过量的盐酸,观察能否有气泡冒出B.参与过量的烧碱溶液,观察能否有固体溶解C.加热至高温,观察能否有气泡冒出,能否有硅酸钙生成D.先加过量的盐酸搅拌,观察能否有不溶物剩余及气泡出现;假定有不溶物那么滤出,投入到氢氧化钠溶液中看其能否溶解【答案】D9.以下说法正确的选项是〔〕A.在粗硅的制取中发作2C+SiO2高温2CO↑+Si,硅被恢复,所以碳的恢复性大于硅的恢复性B.硅酸钠属于盐,不属于碱,所以硅酸钠可以保管在磨口玻璃塞试剂瓶中C.用SiO2制取硅酸,应先使二氧化硅与氢氧化钠溶液反响,然后再通入CO2D.由Na2CO3+SiO2高温CO2↑+Na2SiO3可知硅酸的酸性大于碳酸【答案】C10.将足量CO2气体通入水玻璃〔Na2SiO3溶液〕中,然后加热蒸干,再在高温下充沛灼烧,最后所得的固体物质是〔〕A.SiO2B.Na2CO3、Na2SiO3C.Na2CO3、SiO2D.Na2SiO3【答案】D二、非选择题(此题包括4小题,共50分)11.(10分)含A元素的一种单质是一种重要的半导体资料,含A元素的一种化合物C可用于制造高功用的现代通讯资料——光导纤维,C与烧碱反响生成含A元素的化合物D.〔1〕与A同族但相对原子质量比A小的元素B的原子结构表示图为.〔2〕C与氢氟酸反响的化学方程式是.〔3〕将C与纯碱混合高温熔融时反响生成D,同时还生成B的最低价氧化物E;将全部的E 与全部的D在足量的水中混合后,生成了含A的化合物F.①生成D和F的化学方程式区分为、.②要将纯碱高温熔化,以下坩埚中可选用的是.A.普通玻璃坩埚B.石英玻璃坩埚C.氧化铝坩埚D.铁坩埚.【答案】〔10分,每空2分〕⑴⑵SiO2+4HF═SiF4↑+2H2O⑶①SiO2+Na2CO3Na2SiO3+CO2↑ Na2SiO3+CO2+H2O=Na2CO3+H2SiO3↓;②D。
高考化学一轮复习 第2节 硅及其化合物 无机非金属材料练习 新人教版

第二节硅及其化合物无机非金属材料1.(2010·模拟题)1798年法国化学家对绿柱石和祖母绿进行化学分析发现了铍。
已知绿柱石是一种呈绿色的硅酸盐,可表示Be x Al y[Si m O n](x、y、m、n均为自然数),其中阴离子部分结构如图所示(已知表示硅酸根离子SiO44-)。
下列说法不正确的是( )A.阴离子化学式为:Si6O1812-B.绿柱石可用氧化物形式表示为:3BeO·Al2O3·6SiO2C.绿柱石可表示为Be3Al2[Si3O12]D.绿柱石可溶于强碱和氢氟酸解析:根据表示SiO44-,可判断绿柱石的阴离子化学式为Si6O1812-,A项正确;绿柱石写为氧化物为:3BeO·A12O3·6SiO2,B项正确;C项中氧原子个数不是18,C项不正确;BeO、Al2O3、SiO2均能溶于强碱和氢氟酸,D项正确。
答案:C2.(2010·山师附中月考题)中据2001年12月的《参考消息》报道,有科学家提出硅是“21世纪的能源”、“未来的石油”的观点。
假如硅作为一种普遍使用的新型能源被开发利用,关于其有利因素的下列说法中,你认为不正确的是 ( )A.硅便于运输、贮存,从安全角度考虑,硅是最佳的燃料B.自然界中存在大量单质硅C.硅燃烧放出的热量大,且燃烧产物对环境污染程度低,容易有效控制D.自然界中硅的贮量丰富解析:由于Si的亲氧性,自然界的硅大都以SiO2或硅酸盐的形式存在,无单质硅存在。
答案:B3.(2010·改编题)下列物质中,既可与盐酸反应,又可与氢氧化钠溶液反应的是 ( )①Na2SiO3 ②AlCl3 ③NH4HCO3 ④Al2O3 ⑤NaHSO3A.①②④ B.②③⑤ C.②③④ D.③④⑤解析:Na2SiO3只能与HCl反应,AlCl3只能与NaOH反应。
答案:D4.(2010·模拟题)下列说法正确的是 ( )①合金的硬度一般比它的各成分金属的小,熔点一般比它的各成分金属的高 ②SiC俗称金刚砂,可用作砂纸、砂轮的磨料 ③漂白粉和漂粉精的有效成分都是Ca(ClO)2 ④NO在人体的血管系统内具有传送信号的功能,也是大气污染物之一 ⑤氧化铜可作为制造玻璃、搪瓷的红色颜料A.①③⑤ B.②③④ C.①②⑤ D.②③⑤解析:合金的硬度一般比它的成分金属的大,熔点一般比它的各成分金属的低,①错;氧化铜是黑色物质,不能作为红色颜料,⑤错,应是Cu2O作为红色颜料。
2015届高考化学一轮近3年真题考点分类汇编:专题十四 无机非金属材料的主角——碳和硅.pdf

专题十四 无机非金属材料的主角——碳和硅 高考试题 考点一 碳及其化合物的性质 1.(2013年广东理综,10,4分)下列叙述Ⅰ和Ⅱ均正确并且有因果关系的是( ) 选项叙述Ⅰ叙述ⅡANH4Cl为强酸弱碱盐用加热法除去NaCl中的NH4ClBFe3+具有氧化性用KSCN溶液可以鉴别Fe3+C溶解度:CaCO3<Ca(HCO3)2溶解度:Na2CO3Na2CO3非金属性: Si>CD向浓度均为0.1 mol·L-1 NaCl和NaI混合溶液中,滴加少量AgNO3溶液出现黄色沉淀Ksp(AgCl) >Ksp(AgI)解析:Fe(NO3)2溶液中,滴加稀H2SO4酸化后,相当于存在HNO3,会把Fe2+氧化为Fe3+,滴加KSCN溶液后变红色,不能确定Fe(NO3)2试样已变质,A错;SO2气体通入澄清石灰水,也会生成白色的CaSO3沉淀,B错;根据越弱越水解的规则,pH:Na2SiO3>Na2CO3,则非金属性:C >Si,C错;NaCl和NaI混合溶液中两者浓度相同,化合物类型相同,滴加AgNO3溶液时Ksp小的先生成沉淀,这里出现了AgI沉淀,所以Ksp(AgCl)>Ksp(AgI),D正确。
答案:D 9.(2012安徽蚌埠第九次联考)硅酸钠是一种重要的无机功能材料,某研究性学习小组设计的利用海边的石英砂(含氯化钠、氧化铁等杂质)制备硅酸钠的流程如下: (1)石英砂加水洗涤的目的是 。
? 研磨后加入NaOH溶液溶解的离子方程式是? 。
? (2)实验室进行蒸发操作要用到的仪器有铁架台(含铁圈)、 和 。
? (3)残渣Ⅰ的成分是 (填化学式)。
将残渣Ⅰ溶于盐酸,再加入NaOH溶液得到沉淀,将该沉淀加入到NaClO和NaOH混合溶液中可制得一种优质净水剂,完成反应的离子方程式:? + ClO-+ OH- +? Cl-+ H2O (4)按上述流程制得的硅酸钠晶体可表示为Na2O·nSiO2,若石英砂的质量为10.0 g,其中含SiO2的质量分数为90%,最终得到硅酸钠晶体15.2 g,则n=。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
2015届高考化学一轮复习 第二章第一节 碳、硅及其章节测试新人教版1.下列关于碳和硅的叙述中,正确的是( )A .其氧化物都能与NaOH 溶液反应B .其单质在加热时都能跟O 2反应C .其氧化物都能溶于水生成相应的酸D .碳和硅两种元素共有两种单质解析:选B CO 与NaOH 溶液不反应,A 错误;SiO 2与水不反应,C 错误;碳有多种同素异形体,D 错误。
2.(2014·银川模拟)下列说法中不正确的是( )A .因SiO 2不溶于水,故H 2SiO 3不是SiO 2对应的酸B .CO 2通入水玻璃可以得到硅酸沉淀C .SiO 2熔点高、硬度大D .氢氟酸能够雕刻玻璃,故不能用玻璃瓶来盛装氢氟酸解析:选A H 2SiO 3对应的酸性氧化物是SiO 2,但SiO 2不能直接与水反应生成H 2SiO 3。
3.下列变化中,不能一步实现的是( )A .Na 2SiO 3―→H 2SiO 3B .H 2SiO 3―→SiO 2C .SiO 2―→H 2SiO 3D .SiO 2―→Na 2SiO 3解析:选C Na 2SiO 3――→盐酸 H 2SiO 3;H 2SiO 3――→△ SiO 2,SiO 2――→NaOHNa 2SiO 3,SiO 2不能一步转化为H 2SiO 3。
4.(2014·济南联考)下列离子方程式的书写正确的是( )A .水玻璃中通入过量二氧化碳:Na 2SiO 3+CO 2+H 2O===2Na ++CO 2-3+H 2SiO 3B .澄清石灰水中通入过量二氧化碳:Ca(OH)2+2CO 2===Ca 2++2HCO -3C .硅与氢氟酸的反应:Si +4H ++4F -===SiF 4↑+2H 2↑D .二氧化硅溶于烧碱溶液中:SiO 2+2OH -===SiO 2-3+H 2O解析:选D Na 2SiO 3是强电解质,应拆成Na +、SiO 2-3,且应生成HCO -3,A 错;B 项正确写法是CO 2+OH -===HCO -3;C 项,氢氟酸是弱酸,不能拆分成H +和F -。
5.硅作为一种新型能源被广泛开发利用,关于其有利因素的下列说法中,你认为不正确的是( )A .硅燃烧产物对环境产生的污染,容易得到有效控制B .从Si(s)+O 2(g)=====△ SiO 2(s) ΔH =-858.6 kJ·mol -1可知,硅燃烧放出的热量多C .自然界中硅的储量丰富,可以从自然界直接获得单质硅D .硅便于运输、贮存,从安全角度考虑,硅是最佳的燃料之一解析:选C 硅在自然界中以化合态的形式存在,需通过化学反应才能获得单质硅。
6.如图是利用二氧化硅制备硅及其化合物的流程,下列说法正确的是( )A .SiO 2属于两性氧化物B .盛放Na 2CO 3溶液的试剂瓶用玻璃塞C .硅胶吸水后可重复再生D .图中所示的转化都是氧化还原反应解析:选C SiO 2是酸性氧化物;Na 2CO 3溶液呈碱性,试剂瓶不能用玻璃塞;题图中有的转化不是氧化还原反应,例如SiO 2与NaOH 溶液的反应。
7.(2014·唐山一模)下列物质:①氢氟酸;②浓H 2SO 4;③烧碱溶液;④Na 2CO 3固体;⑤氧化钙;⑥浓HNO 3。
其中在一定条件下能与SiO 2反应的有( )A .①②⑥B .②③⑥C .①③④⑤D .全部解析:选C SiO 2可与烧碱溶液、氧化钙反应,表现出酸性氧化物的性质;SiO 2可以与氢氟酸反应;在制玻璃过程中SiO 2与Na 2CO 3固体反应;SiO 2不能与浓硫酸和浓硝酸反应。
8.(2014·宿州模拟)下列叙述中正确的是( )A .因为Na 2CO 3+SiO 2=====高温 Na 2SiO 3+CO 2↑,所以硅酸的酸性比碳酸强B .碳和硅都是ⅣA 族的元素,所以二氧化碳和二氧化硅的物理性质相似C .二氧化硅既溶于氢氧化钠溶液又溶于氢氟酸,所以二氧化硅是两性氧化物D .二氧化硅和二氧化碳都是酸性氧化物,但二氧化硅不能和水反应生成硅酸解析:选D A 项的反应不是在水溶液中进行,产物中有气体生成,故不能通过此反应判断H 2CO 3与H 2SiO 3的酸性强弱,A 错误;CO 2和SiO 2的物理性质差异较大,B 错误;SiO 2与氢氟酸的反应不属于酸性氧化物与一般酸的反应,在此反应中SiO 2并没有表现出碱性氧化物的性质,C 错误。
9.有A 、B 、C 、D 四种含硅元素的物质,它们能发生如下反应:①C 与烧碱溶液反应生成A 和水;②A 溶液与钙盐反应生成白色沉淀D ;③B 在空气中燃烧生成C ;④C 在高温下与碳酸钙反应生成D 和一种气体;⑤C 在高温下与碳反应生成单质B 。
(1)根据上述变化,写出A 、B 、C 、D 的化学式。
A________________,B________________,C________________,D________________。
(2)写出①、④反应的化学方程式:①________________________________________________________________________; ④________________________________________________________________________。
解析:能与烧碱反应的含硅物质有Si 、SiO 2和H 2SiO 3,由①知A 为Na 2SiO 3;由②知D为CaSiO 3,由④知C 为SiO 2,发生的反应为SiO 2+CaCO 3=====高温 CaSiO 3+CO 2↑;由⑤知B 为Si ,发生反应的化学方程式为:SiO 2+2C=====高温 Si +2CO↑;由③验证以上推断合理。
答案:(1)Na 2SiO 3 Si SiO 2 CaSiO 3(2)①SiO 2+2NaOH===Na 2SiO 3+H 2O④SiO 2+CaCO 3=====高温 CaSiO 3+CO 2↑10.硅是无机非金属材料的主角,硅的氧化物和硅酸盐约占地壳质量的90%以上。
(1)下列物质不属于硅酸盐的是________。
A .陶瓷B .玻璃C .水泥D .生石灰(2)SiO 2是玻璃的主要成分之一,SiO 2与氢氧化钠溶液反应的化学方程式为___________,工艺师常用________(填物质名称)来雕刻玻璃。
(3)用Na 2SiO 3水溶液浸泡过的棉花不易燃烧,说明Na 2SiO 3可用作________。
Na 2SiO 3可通过SiO 2与纯碱混合高温熔融反应制得,高温熔融纯碱时下列坩埚可选用的是________。
A .普通玻璃坩埚B .石英玻璃坩埚C .氧化铝坩埚D .铁坩埚(4)工业上常利用反应2C +SiO 2=====高温 Si +2CO↑制备硅单质,该反应中所含元素化合价升高的物质是________(填化学式、下同),氧化剂是________。
解析:(1)生石灰是CaO ,为碱性氧化物且不含Si 元素,不属于硅酸盐。
(2)SiO 2与NaOH 溶液反应的化学方程式为SiO 2+2NaOH===Na 2SiO 3+H 2O 。
由于SiO 2能溶于氢氟酸,因此工艺师常用氢氟酸来雕刻玻璃。
(3)Na 2SiO 3水溶液又称“水玻璃”,具有阻燃的功能,因此可用作防火剂。
SiO 2和Na 2CO 3在高温下反应生成Na 2SiO 3和CO 2,故含SiO 2的材料(普通玻璃、石英玻璃)以及Al 2O 3等都能与Na 2CO 3在高温下反应,故不能用以上材质的坩埚熔融纯碱。
(4)题给反应中C(碳)被氧化,SiO 2中+4价的硅被还原,因此SiO 2作氧化剂。
答案:(1)D (2)SiO 2+2NaOH===Na 2SiO 3+H 2O 氢氟酸 (3)防火剂 D (4)C SiO 211.(2014·成都调研)晶体硅是信息科学和能源科学中的一种重要材料,可用于制芯片和太阳能电池等。
以下是工业上制取纯硅的一种方法。
请回答下列问题(各元素用相应的元素符号表示):(1)在上述生产过程中,属于置换反应的有________(填反应代号)。
(2)写出反应③的化学方程式_________________________________________________。
(3)化合物W 的用途很广,通常可用作建筑工业和造纸工业的黏合剂,可作肥皂的填充剂,是天然水的软化剂。
将石英砂和纯碱按一定比例混合加热至1 373~1 623 K 反应,生成化合物W ,其化学方程式是______________________________。
(4)A 、B 、C 三种气体在“节能减排”中作为减排目标的一种气体是________________(填化学式);分别通入W 溶液中能得到白色沉淀的气体是____________________(填化学式)。
(5)工业上合成氨的原料H 2的制法是先把焦炭与水蒸气反应生成水煤气,再提纯水煤气得到纯净的H 2,提纯水煤气得到纯净的H 2的化学方程式为________________________________________________________________________________________________。
解析:反应①为石英砂和焦炭生成粗硅和一氧化碳的反应:SiO 2+2C =====3 273 K Si +2CO↑,属于置换反应;反应②是Si +3HCl =====523~527 KSiHCl 3+H 2,属于置换反应;反应③是SiHCl 3+H 2=====1 357 K Si +3HCl ,属于置换反应;反应④为特定条件下的反应:CO +H 2O =====1 073 K 催化剂H 2+CO 2,不属于置换反应。
A 、B 、C 分别为CO 、CO 2、HCl ,其中CO 2是温室气体,是节能减排的目标气体,CO 2和HCl 通入W(硅酸钠)溶液中能够生成白色沉淀(硅酸)。
答案:(1)①②③(2)SiHCl 3+H 2=====1 357 K Si +3HCl(3)SiO 2+Na 2CO 3=====1 373~1 623 KNa 2SiO 3+CO 2↑ (4)CO 2 CO 2和HCl(5)CO 2+H 2O =====1 073 K 催化剂CO 2+H 2、CO 2+Ca(OH)2===CaCO 3↓+H 2O12.证明生石灰中既混有石英,又混有石灰石的正确方法是( )A .加入过量的盐酸,观察是否有气泡冒出B .加入过量的烧碱溶液,观察是否有固体溶解C .加热至高温,观察是否有气泡冒出,是否有硅酸钙生成D.先加过量的盐酸搅拌,观察是否有不溶物剩余及气泡出现;若有不溶物则滤出,投入到氢氧化钠溶液中看其是否溶解解析:选D SiO2不溶于除氢氟酸以外的酸;CaO、CaCO3均可溶于盐酸,且CaCO3溶于盐酸时会有气泡产生,SiO2能溶于NaOH溶液。
