12 羧酸
有机化学第12章 羧酸

四、α-H的卤代反应
羧酸的α-H可在光、碘、红磷、硫等催化剂存在下被溴 或氯取代生成卤代酸。
RCH2COOH
Br2 PΔ
RCHCOOH Br2
Br
PΔ
Br R-C-COOH
Br
控制条件,反应可停留在一取代阶段。
CH3CH2CH2CH2COOH + Br2
P Br2 70 ℃
实质上并非两者的简单组合
醛酮中 C O 键长 0.122nm
醇中
C OH 键长 0.143nm
O HC
OH
(甲酸)
0.1245nm 0.1312nm 电子衍射实验证明
O RC
O-H
P-π 共轭体系
RC sp2 杂化
O OH
O RC
OH O HC OH
O RC
O
O 0.127nm HC
O 0.127nm
O RC
O
O HC
O
羧酸的化学性质
H
脱羧反应
O
RCC
羟基断裂呈酸性
H
OH
α H 的反应
羟基被取代的反应
一、酸性
羧酸具有弱酸性,在水溶液中存在着如下平衡:
RCOOH
RCOO + H+
乙酸的离解常数Ka为1.75×10-5 , pKa =4.76 甲酸的Ka=2.1×10-4 , pKa =3.75 其他一元酸的Ka在1.1~1.8×10-5之间, pKa在4.7~5之间。 可见羧酸的酸性小于无机酸而大于碳酸(H2CO3 pKa1=6.73)。
oocoh形式上看羧基是由一个和一个组成coh实质上并非两者的简单组合醛酮中coo01245nm键长0122nmhc01312nmoh醇中coh甲酸电子衍射实验证明键长0143nmoorcohrc2ohp共轭体系sp杂化ooorcrcrcohoooo0127nmohchchcohoo0127nm羧酸的化学性质h脱羧反应orcc羟基断裂呈酸性ohhh的反应羟基被取代的反应一酸性?羧酸具有弱酸性在水溶液中存在着如下平衡
有机化学:12 羧酸及羧酸衍生物

C
+
O C O
H
(二)羧基上羟基的取代反应
O 酰卤 O 酸酐 O O 酯 O 酰胺 R C X R C O C R R C O R R C NH2(R)
1.成酯反应
O R C OH + H OR' H
+
O R C OR' + H2O
称酯化反应 反应特点:用酸做催化剂,反应可逆,速率慢
1.成酯反应
(1)诱导效应
HCOOH > CH3COOH > CH3CH2COOH
pKa 3.77 4.76 4.88
(一)酸性
如:卤素的位置——越靠近羧基影响越大
CH3CH2CHCOOH Cl
CH3CHCH2COOH CH2CH2CH2COOH Cl Cl
pKa
2.86
4.41
4.70
卤素的数目——越多,酸性越强
RCH2COOH + RCHCOX
X RCHCOOH
X X 该反应称为赫尔-佛尔哈德-泽林斯基(Hell-VolhardZelinsky)反应。 α-位如果还有H,可以进一步发生卤代反应,直至 所有α-H全部反应完。
问:
COOH CH3COOH 1 COOH 2 H2C COOH COOH 3
CH3COOH+SOCl2
pKa
4.20
3.83
4.09
4.10
2.电子效应的影响
邻位取代:
C和 I 都发挥作用,还有空间效应,情况复杂。
除氨基外,-X、-CH3、-OH、NO2酸性都比间 位或对位取代的强。邻位有取代时,羧基与 苯环不共平面,苯环电子云向羧基偏移少。
有机化学:第12章 羧酸

RCOONa + HCl RCOOH + NaCl
应用:用于羧酸的鉴别,分离,提纯。
另外,C12~18的RCOONa是肥皂的主要成份。
RCOOH > H2CO3 > C6H5OH > H2O >
pka: 4 ~ 5
6.38
10 15.74
RCH2OH > RNH2
16 ~ 19
~ 34
例如: 用化学方法鉴别(酸、酚、醇)
共轭效应的影响受到阻碍。
吸电子共轭效应
(-C )只能传递
到邻、对位。
• 卤素原子具有-I和+C效应,-I > +C。
COOH
COOH Cl
COOH
Cl
pKa: 4.2
2.92
3.82
• 羟基具有-I和+C效应,-I < +C。
COOH COOH OH
COOH OH
pKa: 4.2
2.98
4.08
COOH
O R C CH3
OH R CH CH3
X2 NaOH
RCOOH + CHX3
O CH3(CH2)4CCH3 I2/NaOH CH3(CH2)4COOH
4、由腈的水解制备:制备比原料多一个碳的羧酸
R CN
H
H2O,
OH
H
R COOH
H2O
CH3(CH2)4CN H2O/H+ CH3(CH2)4COOH
O CH2CH3
O
HOCCH2CHCH2CH2CHCH2COH
CH3
3–甲基–6–乙基辛二酸
(3-ethyl-6-methyloctanedioic acid)
第12章羧酸分解

第12章 羧酸§12.1 羧酸的分类、结构与命名12.1.1 结构和分类 1、定义分子中含有C OH O基团(羧基)的有机化合物称为羧酸。
2、羧酸的结构通式:R-COOH (-R=烷基或芳基) 3、羧酸(RCOOH)的分类方法☐ 按照羧基连的烃基构造: ☐ 按照分子中羧基的数目:脂肪族羧酸(饱和及不饱和) 一元羧酸 脂环族羧酸 二元羧酸 芳香族羧酸 多元羧酸其中链状的一元羧酸(包括饱和的及不饱和的)通称为脂肪酸12.1.2 命名 1、系统命名法A 、饱和脂肪酸的命名1)选择含有羧基的最长碳链为主链,并按主链碳数称“某酸”; 2)从羧基碳原子开始编号,用阿拉伯数字标明取代基的位置; 3)并将取代基的位次、数目、名称写于酸名前。
如:C H 3 C H 2 C H 2 CO O H丁酸 C H 3 C H C H 3 C H C H 3C H 2 C O O H 3 , 4 - 二甲基戊酸 β , γ - 二甲基戊酸12 3 4 5 α β γB 、不饱和脂肪酸的命名1)选择包括羧基碳原子和各C=C 键的碳原子都在内的最长碳链为主链,根据主链上碳原子的数目称“某酸”或“某烯(炔)酸”;2)从羧基碳原子开始编号;3)在“某烯(炔)酸”前并注明取代基情况及双键的位置。
如:CH 3CCHCH CH 3CH 3COOHC CCOOHHOOCH H2, 4–二甲基–3–戊烯酸 (E ) –丁烯二酸 3-苯基丙烯酸C 、脂环族羧酸的命名1)羧基直接连在脂环上时,可在脂环烃的名称后加上“羧酸或二羧酸”等词尾; 2)不论羧基直接连在脂环上还是在脂环侧链上,均可把脂环作为取代基来命名。
如:D 、芳香族羧酸的命名1)以芳甲酸为母体;2)若芳环上连有取代基,则从羧基所连的碳原子开始编号,并使取代基的位次最小。
如:E 、二元酸的命名选包括两个羧基碳原子在内的最长碳链作为主链,按主链的碳原子数称为“某二酸”。
第十二章 羧 酸
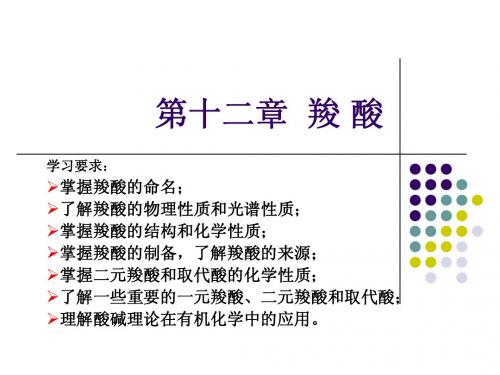
CH COOH 2 CH COOH CH CH COOH β -苯2 基 丙 烯酸 (肉 桂酸 )
丁二酸(琥珀酸)
CH3CH CHCOOH
CH3CHCH2COOH CH3 3-甲 基 丁酸
2-丁烯酸
书 P2 问题12-1
酰基: 羧酸分子中的羧基除去羟基后的基团;
酰氧基:羧酸分子中的羧基除去氢原子后的基团。
O
O18 CH3C-OC(CH3)3 + H2O
三、 脱羧反应
*1.强热脱羧 CH3COONa
*2.催化脱羧
2RCOOH
400—500℃
+
NaOH
CaO
强热
CH4
+
Na2CO3
ThO2
O
+
R
CO2
+
H2O
R
3.α-C原子连有吸电基的一元羧酸易脱羧
HOOCCH2COOH
O2N COOH NO2
H2O
O H3C C H3C O C O
乙 酰基
O PhCH2 C
乙 酰氧 基
O PhCH2 C O
苯 乙 酰基
O O
苯 乙 酰氧 基
O O
CH3CCH3CCH3 乙酰丙酮 CH3CCH3COCH2CH3 乙酰乙酸乙酯
第二节 羧酸的物理性质
1. 沸点:由于羧酸分子间及羧酸 分子与水分子间形成氢键,羧酸的 沸点高于分子量相近的醇。
5.比重:一元羧酸:甲酸、乙酸比重大于1; 其它羧酸的比重小于1。 二元羧酸、芳香羧酸的比重大于1。 6.状态: 十个碳原子以下的饱和一元酸是液体。 高级脂肪酸是蜡状固体。 二元脂肪酸和芳香酸都是结晶固体。
羧 烃 基 基
12 羧酸及其衍生物问题参考答案
12 羧酸及其衍生物问题参考答案问题1 以戊酸为实例,根据羧酸的分子结构分析解释羧酸类化合物可能具有的物理性质和化学性质。
讨论:戊酸的结构如下。
羧基可发生分子间的双缔合,沸点高。
化学性质为羟基易被取代,羧羰基的亲核加成反应比醛酮的羰基困难;可发生脱羧反应,α-H 受羧基的吸电子效应的影响表现出活泼性可被卤素原子取代。
C OOHH问题2 丙二酸HOOCCH 2COOH 的一级解离平衡常数K a1=1.49×10-2远大于二级解离平衡常数K a2=2.03×10-6。
请说明原因。
讨论:丙二酸一级解离后为HOOCCH 2COO -,因此由于同离子效应阻碍二级解离,羧基负离子的吸电子效应也较羧基明显减弱,二级解离困难得多。
问题3 芳香羧酸2, 4, 6-三硝基苯甲酸受热容易发生脱羧反应生成2, 4, 6-三硝基苯。
请从分子结构和电子效应方面进行解释。
讨论:由于三个强吸电基的作用使得羧基连接的苯环碳原子正电性大大增强,见下图。
有利于C —C 键的异裂而脱羧。
COOHNO 2N O 2NO O COOHNO 2N O 2NO O COOHNO 2N O 2NO O问题4 强氧化剂难氧化叔丁基苯成为苯甲酸,而强氧化剂却容易氧化仲丁基苯成为苯甲酸。
这是什么原因?讨论:仲丁基苯分子中与苯环直接相连的碳原子上连接有氢原子,C —H 键与苯环形成 -π超共轭体系,C —H 键更易断裂而发生氧化反应。
问题5 在盐酸存在和加热条件下,顺丁烯二酸可以转化为反丁烯二酸。
请提出该异构化反应较合理的机理。
讨论:如下为较合理的机理。
CO 2HCHHOOHHClCO 2HCHH OHOHClCO 2HC H HOH OHCl CO 2HC H ClO OHH H HClHCO 2H HHO 2C问题6 邻甲基苯甲酸(K a=12.4×10-5)的酸性较苯甲酸(K a=6.3×10-5)的酸性高,请从电子效应和分子的空间结构等方面进行解释。
12-羧酸衍生物药学专升本陆涛,7版-精品文档

二元羧酸可以生成酸性酯、中性酯;简单酯、 混合酯。
COOC2H5 COOH 酸性酯 简单酯 COOC2H5 COOC2H5 中性酯 混合酯 COOCH3 COOC2H5
O CH3—C—OCH3 乙酸甲酯 O (CH3)2CHCH2-C-OCH2异戊酸苄酯
O H-C—O—C2H5 甲酸乙酯
CH3COOCH=CH2 乙酸乙烯酯
O C H 3 3 C H C H C B r 对 甲 苯 基 丙 烯 酰 溴
O CH3—C—Br 酰卤键 乙酰溴
2. 酸酐:分为单酐和混酐. 单酐:羧酸名称+酐 命名:
混酐:简单羧酸名+复杂羧酸名+酐
O CH3-C
酐 键 O O CH3-C—O—C-CH3
酰基 酰氧基 酰氧基 酰基
混(合)酐 乙酸丙酸酐
COOC2H5 COOH 乙二酸氢乙酯 酸性酯
COOC2H5 COOC2H5 乙二酸二乙酯 中性酯,简单酯
COOCH3 COOC2H5 乙二酸甲乙酯 中性酯,混合酯
C O O C H 3 C O O C H H 2C 3
O
γ-丁内酯
O
邻苯二甲酸甲乙酯
CH2—O—C—C15H31 丙三醇三软脂酸酯
第十一章
羧酸衍生物
第十二章
羧酸衍生物
羧基中的-OH被其它原子或基团取代后所 生成的化合物,称为羧酸衍生物。
-X(-Cl,-Br) 酰卤
O R(Ar)—C—— L
羧酸衍生物
L=
-O-CR(Ar) O -O-R(Ar)
酸酐
酯
-NH2,-NHR,-NR2 酰胺
一、结构和命名
(一)结构 酰氯、酸酐、酯和酰胺分子中都含有酰基,可 O 用通式 表示。羰基碳为sp2杂化,未参 R C L 加杂化的 p 轨道与氧原子的 p 轨道交盖形成π键,
大学有机化学第12章羧酸

C O + H2O
C
O
邻苯二甲酸
邻苯二O 甲酸酐(100%)
羧酸的钠盐 酰氯 共热
O
O
OO
CH3 C O Na + CH3CH2 C Cl CH3 C O C CH2CH3 + NaCl
混合酸酐的生成
(3) 酯的生成和酯化反应机理 羧酸 醇 在强酸催化下 酯
酯化反应(esterification) O
+ H2O
(92%)
制备乙酸、苯甲酸的工业方法
(2) 由一氧化碳、甲醇或醛制备
CO与NaOH水溶液作用,生成HCOOH:
CO + NaOH
~210℃ ~0.8 MPa
HCOONa H2SO4
丙醛氧化法:
HCOOH
CH3CH2CHO +
1/2
O2
(CH3CH2COO)2 0.1 MPa,
Mn
甲醇法:
CH3 CN
H2O, H2SO4 ~85%
CH3 COOH
12.3.4 Grignard 试剂与CO2作用
Grignard 试剂的羧化作用 (carbonation)
(CH3)3C MgCl + O C O
O
C(CH3)3
H3O+
C O MgCl
(CH3)3CCOOH
反应特点:
• RX RCOOH
• 增长1个C的碳链
O C6H5 C 18OCH3 + H2O
羧酸
醇
酯化反应机理:
第一步 羰基质子化:
O R C OH H+
OH R C OH
酯
OH R C OH
第二步 醇分子对质子化羰基的亲核进攻:
第12章 羧酸

第12章 羧酸§12.1 羧酸的分类、结构与命名12.1.1 结构和分类 1、定义分子中含有C OH O基团(羧基)的有机化合物称为羧酸。
2、羧酸的结构通式:R-COOH (-R=烷基或芳基) 3、羧酸(RCOOH)的分类方法☐ 按照羧基连的烃基构造: ☐ 按照分子中羧基的数目:脂肪族羧酸(饱和及不饱和) 一元羧酸 脂环族羧酸 二元羧酸 芳香族羧酸 多元羧酸其中链状的一元羧酸(包括饱和的及不饱和的)通称为脂肪酸12.1.2 命名 1、系统命名法A 、饱和脂肪酸的命名1)选择含有羧基的最长碳链为主链,并按主链碳数称“某酸”; 2)从羧基碳原子开始编号,用阿拉伯数字标明取代基的位置; 3)并将取代基的位次、数目、名称写于酸名前。
如:C H 3 C H 2 C H 2 CO O H丁酸 C H 3 C H C H 3 C H C H 3C H 2 C O O H 3 , 4 - 二甲基戊酸 β , γ - 二甲基戊酸12 3 4 5 α β γB 、不饱和脂肪酸的命名1)选择包括羧基碳原子和各C=C 键的碳原子都在内的最长碳链为主链,根据主链上碳原子的数目称“某酸”或“某烯(炔)酸”;2)从羧基碳原子开始编号;3)在“某烯(炔)酸”前并注明取代基情况及双键的位置。
如:CH 3CCHCH CH 3CH 3COOHC CCOOHHOOCH H2, 4–二甲基–3–戊烯酸 (E ) –丁烯二酸 3-苯基丙烯酸C 、脂环族羧酸的命名1)羧基直接连在脂环上时,可在脂环烃的名称后加上“羧酸或二羧酸”等词尾; 2)不论羧基直接连在脂环上还是在脂环侧链上,均可把脂环作为取代基来命名。
如:D 、芳香族羧酸的命名1)以芳甲酸为母体;2)若芳环上连有取代基,则从羧基所连的碳原子开始编号,并使取代基的位次最小。
如:E 、二元酸的命名选包括两个羧基碳原子在内的最长碳链作为主链,按主链的碳原子数称为“某二酸”。
有机化学 第十二章 羧酸

王鹏
山东科技大学 化学与环境工程学院
12.3 羧酸的物理和波谱性质
二、1H-NMR:
-COOH: δ范围 10~14 邻近羧基的碳上的氢移向低场区, δ约2~2.6 O CH2 C O H
δ: 2~3
10~13
如p282 图13-2异丁酸的核磁图 羧酸核磁的另一特点是活性氢交换后低场区信号 减弱或消失
王鹏
12.4 羧酸的化学性质
酯化反应的亲核取代机理:
O R C OH + H
+
快
+OH
慢
OH R
快
R
快
C
OH
.. R'O H ..
C
+.. O R'
OH H O R C OR'
OH
快
+ OH OR'
H2O 快 慢
R
C
R
C
OR'
H
+
+ OH2
快
叔醇更倾向于酸碱中和机理,即酸失去H+,叔醇 失去OH-,剩余部分结合成酯
溶解性:
低级脂肪酸是极性分子,易溶于水(因为易与水成分子间 氢键)。随着碳原子数增加,水溶性逐渐降低
熔沸点:
羧酸的熔沸点比分子量相近的其他化合物高许多
王鹏
山东科技大学 化学与环境工程学院
12.3 羧酸的物理和波谱性质
一、IR:
O-H:3560~3500(单体)3000~2500(二聚) C=O:1720,C-O:1250 羧酸的红外特征是强而宽的羧基峰和羰基峰
王鹏
山东科技大学 化学与环境工程学院
12.2 羧酸的分类和命名
有机化学12羧酸衍生物

C H 3C O O C H 3>C H 3C O O C H 2C H 3> C H 3C O O C H (C H 3)2>C H 3C O O C (C H 3)3
2021/4/6
25
(一)水解
❖酰氯比酸酐活泼,在常温下立即发生反应,酸酐大多需 要加热才发生反应。
乙酰氯暴露在空气中即水解,放出HCl。
2021/4/6
22
❖反应的活性和离去基团的性质有关,羧酸衍生物的离去 基团L同时具有-I和+C效应。 第一步亲核加成,取决于羰基碳原子的亲电性。
电子效应:-I效应使羰基碳原子的电子密度减小,更容 易与亲核试剂起加成反应;
+C效应,使反应物的稳定性增加,羰基更不容易和亲 核试剂起加成反应。
R
2021/4/6
丙烯酸
2021/4/6
acryloic acid
O C Cl
苯甲酰氯 benzoyl chloride
O CH2 CHC Br
丙烯酰溴 acryloyl bromide
10
❖酰胺是羧酸分子中羟基被氨基取代后的生成物。 酰胺氮原子上的氢被烃基取代,称为取代酰胺。
O R C N H 2 酰胺
O R C NHR'
NCH3 O
❖酯的氨解,与氨反应不需加酸碱催化,氨本身就是碱。
2021/4/6
35
O
O
RCO R'+N H 3 RCN H 2+R'O H
酯的氨解反应比酸酐温和,与亲核性较弱的胺反应,常 在碱催化剂存在下进行。
O
CH3O
COC2H5+C6H5NH2
NaOH
DMSOCH3O
有机12-羧酸

2. 有机
R
试剂和CO 试剂和CO2的反应
CO2 RCOO H2O RCOOH
R
OLi R C R OLi
H2O
O R-C-R
格氏试剂。 )( (1)(2)(3) 格氏试剂。( )(
比 产物的
)
5
实
C2H5 CH3 C=C
例
I
n-C4H9Li/Et2O C H 2 5
CH3 C=C
Li CO2 H
-LiOH H2O
O R-C-R'
R'Li
RCOOMgX + R’H RH RCOOLi
R
R'Li
OLi R-C-OLi R'
H2O
R-C-OH R'
酯、酰氯、酸酐与有机锂试剂反应时生成的中间体不稳定,在反应过程中即 酰氯、酸酐与有机锂试剂反应时生成的中间体不稳定, 分解成酮、酮比酯活泼, ROH的混合物 的混合物。 分解成酮、酮比酯活泼,所以在反应体系中常得到酮与 3oROH的混合物。
机 理:
O O
1.
环 状 过 渡 态 机 理
H2 C C O H C O
RCCH2COH
≡
R
O
-CO2
R
t
C OH
CH2 互变异构
O RCCH3
碳与不饱和键相连时,一般都通过环状过渡态机理失羧。 当α-碳与不饱和键相连时,一般都通过环状过渡态机理失羧。
15
2. 羧酸负离子机理
Cl3CCOOH -H+ H2O
1H
NMR R2CHCOOH δH:10~12 HCR2COOH δH:2~2.6 : : 羧酸中的C=O: ~1710cm-1 CH2=CHCOOH ~1690cm-1 ArCOOH ~ 1690cm-1 : 羧酸中的 羧酸中的OH:3000 ~2500cm-1 羧酸中的 : 羧酸中的C-O ~ 1250 cm-1 羧酸中的
第十二章-羧酸

pka 2.98
pka 4.08
OH
pka 4.57
取代基对有机化合物酸性影响一般规律 1 脂肪族一元酸 吸电子基团增加酸性,供电子基团减弱酸性, 吸电子基团增加酸性,供电子基团减弱酸性, 且吸电子基团越多或吸电子基团离羧基越近酸性越强 2 芳香酸 芳香酸连有邻对位定位基时邻 > 间 > 对 芳香酸连有邻对位定位基时邻 芳香酸连有间位定位基时邻 芳香酸连有间位定位基时邻 > 对 > 间 间位定位基及Cl, Br, I 增加酸性 间位定位基及 邻对位致活定位基及F位于羧基对位时减弱酸性, 邻对位致活定位基及 位于羧基对位时减弱酸性, 位于羧基对位时减弱酸性 位于间位及邻位情况较复杂。 位于间位及邻位情况较复杂。
NO2 > CN > F > Cl > Br> I > C C >
OCH3>
C6 H 5 > C C >
H
2. 空间效应: 空间效应: 利于H 离解的空间结构酸性强,不利于H 利于H+离解的空间结构酸性强,不利于H+离解 的空间结构酸性弱. 的空间结构酸性弱. 场效应
COO COOH CH2
场效应的影响: 场效应的影响:
§12.4 羧酸的反应 一、 羧酸的结构和反应 二、 羧基中氢的反应 酰化反应 三 、 酰化反应 四、 脱羧反应 五、 还原反应 羧酸α-H的反应 六 、 羧酸 的反应
(赫尔 乌尔哈 泽林斯基反应) 赫尔-乌尔哈 泽林斯基反应) 赫尔 乌尔哈-泽林斯基反应
一 、 羧酸的结构和反应 酸性
R
C H
O C
硫酸、苯磺酸等 (常用的催化剂有盐酸 、硫酸、苯磺酸等), 常用的催化剂有盐酸 CH3COOH + C2H5OH 投料 1 1 : : 1 10
易错点12 羧酸衍生物的结构与性质(学生版)(人教版2019选择性必修3)

易错点12羧酸衍生物的结构与性质易错题【01】酯的化学性质 1.酯的水解反应原理酯化反应形成的键,即酯水解反应断裂的键。
请用化学方程式表示水解反应的原理:∆−−→。
2.酯在酸性或碱性条件下的水解反应①在酸性条件下,酯的水解是可逆反应。
乙酸乙酯在稀硫酸存在下水解的化学方程式为CH 3COOC 2H 5+H 2O浓硫酸Δ−−−−−→CH 3COOH +C 2H 5OH 。
②在碱性条件下,酯水解生成羧酸盐和醇,水解反应是不可逆反应。
乙酸乙酯在氢氧化钠存在下水解的化学方程式为CH 3COOC 2H 5+NaOH ∆−−→CH 3COONa +C 2H 5OH 。
③酯在碱性条件下的水解程度比在酸性条件下水解程度大。
3、酯化反应与酯的水解反应的比较酯化反应酯的水解反应反应关系 CH 3COOH +C 2H 5OH 浓硫酸ΔCH 3COOC 2H 5+H 2O_催化剂 浓硫酸稀硫酸或NaOH 溶液催化剂的其他作用 吸水、提高CH 3COOH 和C 2H 5OH 的转化率NaOH 中和酯水解生成的羧酸、提高酯的水解率 加热方式 酒精灯火焰加热 热水浴加热 反应类型 酯化反应、取代反应水解反应、取代反应易错题【02】油脂1、油脂的结构和分类 (1)概念油脂是由高级脂肪酸和甘油生成的酯,属于酯类化合物。
(2)结构①结构简式:。
②官能团:酯基,有的在其烃基中可能含有碳碳不饱和键。
(3)分类(4)常见高级脂肪酸2、油脂的性质1.物理性质①密度:比水的小。
②溶解性:难溶于水,易溶于有机溶剂。
③熔、沸点:天然油脂都是混合物,没有固定的熔、沸点。
2.化学性质①水解反应如:硬脂酸甘油酯在酸性条件下水解反应的化学方程式为+3H2O+H−−→3C17H35COOH+。
Δ如:硬脂酸甘油酯在NaOH溶液中水解的化学方程式为+3NaOH∆−−→3C17H35COONa+。
油脂在碱性溶液中的水解反应又称为皂化反应,工业上常用来制取肥皂。
12-羧酸衍生物

第十二章羧酸衍生物
概述
RCOX 酰卤(RCO)
O 酸酐
2 RCOOR’酯RCONH
酰胺
2
RCN 腈
水解均生成羧酸
§12.1 羧酸衍生物的结构、命名和物理性质
一、羧酸衍生物的结构
R -C -L =O
结构与羧酸类似:p-π共轭
H -C -NH 2 CH 3NH 2
=O
C -N 键长 0.1376nm 0.1474nm
H -C -OCH 3 CH 3OH
=O
C -O 键长0.1334nm 0.143nm
三、羧酸衍生物的物理性质
1. 气味
低级酰卤、酸酐:刺鼻气味低级酯:香味(香料)
乙酸异戊酯:香蕉味
戊酸异戊酯:苹果味
丁酸丁酯:菠萝味
2. 沸点
酰卤、酸酐、酯的沸点低于分子量相近的羧酸和酰胺(氢键)
CH 3CH 2CH 2CONH 2
CH 3CH 2CH 2CH 2COOH (CH 3CO)2O CH 3COOC 3H 7-n CH 3CH 2COCl b.p.(C)
216 186
140 102 80°
3. 溶解度
酰卤、酸酐不溶于水,低级酰卤、酸酐遇水分解
酯在水中溶解度小
低级酰胺溶于水
如:N,N-二甲基甲酰胺、
N,N-二甲基乙酰胺与水互溶
O
CH-
(CH CO)
CH23+ n-C4H7OH
Cd活性低于
OMgX。
第十二章 羧 酸

甲酸(蚁酸)的结构比较特殊,分子中的羧基和氢原子相连。 它既具有羧基的结构。同时又有醛基的结构,因而表现出与它的同 系物不同的一些特性。
因为甲酸分子中有醛基,故有还原性。甲酸能还原银氨溶液而 发生银镜反应,也能使高锰酸钾溶液退色,这些反应常用于甲酸的 定性鉴定。
47
2.乙二酸
乙二酸(草酸) 草酸以盐的形式存在于多种植物的细胞膜中,最 常见的是钙盐和钾盐,在人尿中也存在着少量的草酸钙。
草酸很容易被氧化成二氧化碳和水。在定量分析中常用草酸来 滴定高锰酸钾。
48
草酸可以与许多金属生成络离子,例如,草酸钾和草酸铁生成 如下的络离子。
这种络合物是溶于水的,因此草酸可用来除去铁锈或蓝墨水 的痕迹。
49
12.4羧酸的制法
12.4.1氧化法
1.烃氧化
上述两个反应分别是工业上生产乙酸和苯甲酸的方法之一。工 业上生产乙酸还可用轻油(C5~7的烷烃)为原料。
6
②羧基与侧链相连者,母体为脂肪酸,脂环或芳环作为取代基命名。 例如:
CH2CH2CH2COOH 4 环戊丁酸
CH CHCOOH
3 苯基丙烯酸
(肉桂酸)
7
12.2 羧酸的物理性质
状态:常温下,甲酸至壬酸的直链羧酸是液体,癸酸以上的羧
酸是固体。脂肪族二元羧酸和芳香族羧酸是晶状固体。
气味:甲酸、乙酸和丙酸有刺激性气味,丁酸至壬酸有腐败气
第十二章 羧 酸
12.1羧酸的分类和命名
羧酸的结构特征是分子中含有羧基(—COOH),羧基是羧酸的 官能团。除甲酸外,羧酸可以看作是烃的羧基衍生物。
1
1.分类
脂肪族羧酸
按羧基所连烃基碳架
脂环族羧酸 芳香族羧酸 杂环族羧酸
Ch.12 羧 酸

第12章羧酸含有羧基—COOH 的有机物称为羧酸,羧酸是很多有机物被氧化时的最后产物。
一、分类二、命名1.系统命名法2.俗名很多羧酸都有俗名。
如蚁酸、醋酸、草酸、安息香酸、水杨酸、酒石酸、柠檬酸、苹果酸第二节饱和一元羧酸的物理性质和光谱性质一、物理性质物态:C1—C3为具有强烈酸味和刺激性气味的液体。
C4—C9为具有腐臭气味的液体。
≥C10为挥发性很低、无气味的石蜡状固体体。
b.p:比分子量相当的醇的沸点还要高,这是因为羧酸分子间也是互相缔合的,象甲酸、乙酸即使是在气态时还能以二缔合体存在。
高级脂肪酸的润滑性:固体羧酸具有层状结构。
在同一层中羧酸的分子通过羧基互相缔合:层与层之间则通过烃基R以极弱的引力相结合。
水中的溶解度:<C4的一元饱和羧酸能与水混溶;≥C12的一元饱和羧酸则完全不溶于水。
二、光谱性质IR特征:νO-H(缔合)3200-2500cm-1(S)宽其中3200-2500cm-1的区域通常出现一系列连续的小峰,其它化合物很少在这个区域出现吸收,这一特征与νC=O峰联合考虑,特征性很强,可鉴定羧酸。
ν1725-1700cm-1(S)与醛、酮的C=O相同。
NMR特征:δCOOH= 10-13例见教材(下册)P. 4第三节羧酸的化学性质羧酸虽具有C=O和OH,但由于二者直接相连构成了p - π共轭体系,因此COOH化学性质不是醛、酮C=O 与醇OH简单的总和,而是另有特点。
一、酸性电子效应对羧酸酸性的影响诱导效应的影响见教材下册P.7表12-2。
思考题:下列物质酸性大小排列正确的是(A) 3>4>2>1 (B) 1>2>3>4(C) 1>3>2>4 (4) 3>2>4>1这道题说明了什么?诱导效应与共轭效应综合影响的例子分析:请解释为什么(1)的酸性比(2)弱,而(3)的酸性却比(2)强? 解释(1): HO-具有-I效应,使羧基酸性增强,但相距较远,影响甚微;HO-能与苯环构成p- 共轭体系,具有+C 效应,这个效应可传导到COOH使O-H键极性降低,酸性因而降低,同时HO-的+C效应也使离解后的羧酸根阴离子稳定性降低。
习题12羧酸习题答案

习题12羧酸习题答案习题12羧酸习题答案羧酸是有机化合物中含有羧基(-COOH)的一类化合物,是有机酸的一种重要类别。
在有机化学中,对羧酸的研究和应用非常广泛。
在习题12中,我们将探讨一些关于羧酸的习题,并给出相应的答案。
1. 请写出以下羧酸的结构式:a) 乙酸b) 苯甲酸c) 丙酸d) 乙烯二酸答案:a) 乙酸:CH3COOHb) 苯甲酸:C6H5COOHc) 丙酸:CH3CH2COOHd) 乙烯二酸:HOOCCH=CHCOOH2. 羧酸与碱反应会产生什么产物?请写出反应方程式。
答案:羧酸与碱反应会产生相应的盐和水。
反应方程式如下:RCOOH + NaOH → RCOONa + H2O3. 以下哪个化合物是羧酸的衍生物?a) 醇b) 醛c) 酮d) 酯答案:d) 酯是羧酸的衍生物。
酯是通过羧酸与醇反应生成的。
4. 请写出以下反应的产物:a) 乙酸与乙醇反应b) 丙酸与乙醇反应c) 甲酸与乙醇反应答案:a) 乙酸与乙醇反应会生成乙酸乙酯。
b) 丙酸与乙醇反应会生成丙酸乙酯。
c) 甲酸与乙醇反应会生成甲酸乙酯。
5. 请写出以下羧酸的IUPAC命名:a) CH3COOHb) CH3CH2COOHc) CH3CH2CH2COOH答案:a) CH3COOH:乙酸b) CH3CH2COOH:丙酸c) CH3CH2CH2COOH:丁酸6. 请写出以下羧酸的常用名称:a) CH3COOHb) C6H5COOHc) CH3CH2COOH答案:a) CH3COOH:乙酸b) C6H5COOH:苯甲酸c) CH3CH2COOH:丙酸7. 请写出以下羧酸的物理性质:a) 乙酸b) 苯甲酸c) 丙酸答案:a) 乙酸是无色液体,具有刺激性气味,密度为1.049 g/cm3,沸点为118.1°C。
b) 苯甲酸是白色结晶固体,具有辛辣的气味,熔点为122-124°C。
c) 丙酸是无色液体,具有刺激性气味,密度为0.99 g/cm3,沸点为141.1°C。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
O R C O H
p 、π共轭体系 共轭体系
上页 下页 返回 退出
甲酸的结构
动画 上页 下页 返回 退出
12.1
• (2)
羧酸的结构、分类和命名
羧酸的分类
乙酸 环戊基乙酸 苯甲酸 乙酸 丙烯酸 乙酸 乙二酸
• 1. 按羧酸所连烃基的不同可分为: –① 脂肪酸 与脂肪族烃基相连 –② 脂环酸 与脂环族烃基相连 –③ 芳香酸 烃基中含有芳环 –① 饱和酸 与饱和烃基相连 –② 不饱和酸 与不饱和烃基相连 • 2. 按分子中羧基的数目多少可分为: –① 一元羧酸 分子中含有一个羧基 分子中含有两个羧基 –② 二元羧酸 –③ 多元羧酸 分子中含两上以上羧基
传递距离 极性效果
练习:比较下列化合物的酸性
COOH
COOH
COOH
COOH
NO2 NO2 CH3
A
B
C
D
B>C>A>D > > >
上页 下页 返回 退出
(2)α-氢原子的卤代反应 羧酸的α-H和醛酮的α-H相似也有活性, 但活性比醛酮小,卤代反应需在红磷催化 下才能顺利发生。
例如: 例如:
赫尔-乌尔哈-泽林斯基 反应
有机化学
12 羧酸 (Carboxylic Acids and Derivatives) )
下页 返回 退出
12 羧 酸
12.1 羧酸的构造,分类和命名 12.2 羧酸的制备 12.3 羧酸的物理性质和化学性质 12.4 重要的羧酸 12.5 羟基酸的化学性质
上页 下页 返回 退出
12.1 羧酸的构造、分类和命名
上页 下页 退出
12.3 羧酸的物理性质
在室温下10个碳原子以下的饱和一元羧酸是液体。 10 个碳原子以上的羧酸为石蜡固体,挥发性很低,无气味。 4~9个碳原子的脂肪酸具有腐败恶臭、动物的汗液和 奶油发酸变坏的气味。 低级脂肪酸易溶于水(与水形成氢键),但随分子量 的增高而降低。10碳以上不溶于水。 饱和一元羧酸的沸点比相对分子质量相似的 醇还要高。 (分子间氢键形成二聚体) 饱和一元羧酸的熔点随分子中碳原子数目的增加呈锯 齿状的变化。
上页 下页
退出
12.1 羧酸的构造、分类和命名
(3)羧酸的命名 许多羧酸有俗名,主要是根据其来源 命名的。 例: HCOOH 蚁酸(甲酸) CH3COOH 醋酸(乙酸) 还有草酸、苹果酸和柠檬酸等。
上页 下页 返回 退出
(3)羧酸的命名
羧酸系统命名法是选择分子中含羧基的最长碳链为 主链,根据主链上碳原子数目称为某酸。 编号:从羧基的碳原子开始,用阿拉伯字表示(也可 以用希腊字母表示,即与羧基直接相连的碳原子为α, 其余依次为β、γ……等)。
上页 下页 退出
B. 酸酐的生成
• 羧酸在脱水剂(如:P2O5)的作用下,加热脱水生成酸 酐。 P 2O 5
RCOOH + RCOOH
(RCO)2O
这类反应也常用乙酸酐作脱水剂。 这类反应也常用乙酸酐作脱水剂。 乙酸酐作脱水剂 COOH (CH3CO)2O
脂环酸以脂环基为取代基命名
CH2COOH
环戊基乙酸
上页 下页 返回 退出
12.2
羧酸的制备方法
• 羧酸的制备方法有很多,其中以氧化法最为简便实施。 • 1. 氧化法 • 1) 高级脂肪烃氧化(工业制法) • 高级脂肪烃在MnO2的催化下,用空气氧化可制备高级脂 肪酸。
RCH2CH2R'
O2 , MnO2
pKa
pKa
2.86
2.84
4.05
4.06
4.50
4.52
FCH2COOH
ClCH2COOH BrCH2COOH
ICH2COOH
pKa pKa
2.66 2.66
2.82 2.86
2.86 2.86
3.12 3.12
上页 下页 返回 退出
诱导效应
• 由于原子的电负性不同,使电子云发生偏移,并且这种 影响沿着分子中的键进行传递,这种效应叫诱导效应。 • 特点:诱导效应沿分子链减弱,经过3个原子后,变得 很微弱。 • 诱导效应的强弱可通过测量偶极距得知 • • 衡量标准: • • 吸电子能力比氢强----吸电子基,负诱导(-I) 吸电子能力比氢弱----给电子基,正诱导(+I) 诱导效应是一个相对概念
上页 下页 退出
也可测量酸的离解常数来估算。
诱导效应一般规律如下:
• 1)同族从上向下吸电子诱导效应降低 • 同周期从左向右吸电子诱导效应增加 -CR3<-NR2<-OR<-F • 如:-F>-Cl>-Br>-I • 如:-C=C > -C=C
• 2)不饱和程度越大,吸电子能力越强 • 3)带正电荷的基团是吸电子基,带负电荷是给电子基 其他因素: 诱导效应常因基团所连母体的不同以及取代后原子间的 相互影响等复杂因素(共轭效应,场效应等)的存在而不同。
O
分子中的
R
C
称为酰基。
上页 下页 返回 退出
O PCl5
或PCl3或SOCl2
R O
C O
Cl
酰酰
R' O
C
OH
R
C O
酸酸
P2O5 ( H O ) 2 R C OH
R'
C O
O
R'OH -H2O H+ R C O NH3 加加 R C OR'
酯
NH2 酰酰
上页 下页 返回 退出
A. 酰氯的生成
上页 下页
退出
共轭效应与诱导效应比较表
诱导效应(I效应) 诱导效应 起源 存在 传递方式 传递路线 电负性 任何键上 诱导方式 沿共价键传递,或空 间(场效应)传递 短,一般不超过三个 共价键 极性变化是单一方向 共轭效应(C效应) 共轭效应 电负性, (共轭)电子对 共轭体系中 共轭方式 沿共轭链传递 远,从共轭链一端到 另一端 极性交替出现 上页 下页 退出
CH3 6 CH3 5 CH2 4 CH γ 3 CH2 β 2 CH2 α 1 COOH
4-甲基己酸 或( γ -甲基己酸) 甲基己酸 甲基己酸) 甲基己酸
上页 下页 返回 退出
(3)羧酸的命名 脂肪族二元羧酸的命名,是选择分子 中含有两个羧基的最长碳链为主链,称为 某二酸。 例如: HOOC-COOH HOOC-CH=CH-COOH
RCOOH + R'COOH
产物是以C12~C18的高级脂肪酸的混合物,多 产物是以C12~C18的高级脂肪酸的混合物,多 用于工业制皂。
上页 下页
退出
1
氧化法
KMnO4/H+
• 2). 烯烃、炔烃氧化
RCH CHR' RC CR'
RCOOH + R'COOH
1. O3 2. H2O
3). 芳烃侧链氧化 要求: 必须有α-H
碘仿反应
O
RCOOH
+
CHI3
此法主要用于制备其它方法难于制备的羧酸。 此法主要用于制备其它方法难于制备的羧酸。
上页 下页 退出
2
格氏试剂法
• 利用格氏试剂与CO2作用也可制备羧酸。
R MgX
+
1) . 干干
O C O
RCOOH
2) . H3O
+
格氏试剂与CO 格氏试剂与CO2进行亲核加成,然后水解,得到比原试剂 多一个碳原子的羧酸。 。 例: 由叔丁基氯制备 (CH3)3CCOOH
上页 下页 返回 退出
O H O H C OH H
H
O H O H
甲酸与水通 过氢键 氢键缔合 氢键
H
在固态和液态,羧酸主要以二聚体形式存在。低 级的羧酸,在气相时仍以双分子缔合状态存在。
O 2 RCOOH R C O
H H
O C O
上页 下页 返回 退出
R
12.3 羧酸的化学性质
羧酸的主要反应部位:
乙二酸(草酸) 丁烯二酸
上页 下页 返回 退出
(3)羧酸的命名 芳香族羧酸
A. 羧基连在芳环上,以芳甲酸为母体
例如:
COOH
COOH
NO2
COOH COOH 邻苯二甲酸
苯甲酸 (安息香酸)
邻硝基苯甲酸
上页 下页 返回 退出
B. 羧基在芳烃侧链上,以脂肪酸为母体。
CH
CH
C OOH
3-苯丙烯酸 (β-苯丙烯酸,肉桂酸)
α-H反应 反应
R
H α C H
O C O
羰基亲核反应 酸性
H
取代反应
还原反应
脱羧反应
p−π共轭降低了O-H中氧原子上的电子云密度,有利于质子的电 离而呈现明显的酸性。 p−π共轭同时增加了羰基氧上电子云密度,使其正电性降低, 不利于亲核反应。
上页 下页 返回 退出
(1) 酸性 羧酸根负离子的结构
CH2COOH H
Cl2 P
CH2COOH Cl
Cl2 P
Cl2CHCOOH
Cl2 P
Cl3CCOOH
上页 下页 返回 退出
卤代反应应用
• α−卤代羧酸经反应可转变为其它的α−取代羧酸或 α,β−不饱和羧酸。
R CH COOH NaCN X
H+ R CH COOH R CH COOH
CN
NaOH
R CH COONa H OH R CH COOH
• • 羧酸与PCl3、PCl5、SOCl2等试剂都可以发生羧 基中羟基被取代的反应,生成相应结构的酰氯。 酰氯是活泼的最常用的酰化试剂之一。
PCl3 PCl5 SOCl2
RCOOH
RCOOH RCOOH
