第九章有机化合物概述_图文.ppt
高一化学最新-有机化合物课件1 精品

2.苯的结构式可用 正确的是( )
来表示,下列关于苯的叙述不 .
A.苯主要是以石油为原料而获得的一种重要化工原料 B.苯中没有碳碳双键,所以苯不属于烯烃 C.苯分子中 6 个碳碳化学键完全相同 D.苯可以与溴水、高锰酸钾溶液反应而使它们褪色
• 解析:考查苯的结构和基本性质,苯分子 中没有双键,所以不与溴水、高锰酸钾溶 液反应。 • 答案:D
• 4.化学性质 • 烷烃的化学性质与甲烷相似,通常较稳定,不 与强酸、强碱及强氧化剂反应,但在一定条件 下可燃烧,可发生取代反应和分解反应。 • ①烷烃(CnH2n+2)的燃烧通式为: •
3n+1 点燃 CnH2n+2+ O2――→nCO2+(n+1)H2O 2
。
• ②乙烷与Cl2光照 发生取代反应生成一氯代物的化 CH3CH3+Cl2――→CH3CH2Cl+HCl 学方程式为:
• 4.下列关于常见的有机物的说法中不正确的 是( ) • A.甲烷与氯气发生反应,光照一段时间后黄 绿色气体消失 • B.苯和甲烷都不能使酸性高锰酸钾溶液褪色 • C.乙烯和甲烷不能用溴的四氯化碳溶液鉴别 • D.在相同条件下甲烷的密度小于空气 • 解析:乙烯与溴单质发生加成反应,能使溴的 四氯化碳溶液褪色,但是甲烷不能使溴的四氯 化碳溶液褪色,可以用溴的四氯化碳溶液鉴别,
考纲展示 核心要点 1.了解有机化合物 1.记住三种分子的结构:甲烷——正四面体;乙烯 中碳原子的成键特 ——六原子共平面;苯——平面正六边形。 征。了解有机化合 2.甲烷、乙烯、苯的化学性质: 物的同分异构现 光照 象。 (1)甲烷:CH4+Cl2――→CH3Cl+HCl(取代反应); 2.了解甲烷、乙烯、 (2)乙烯:CH2===CH2+Br2―→CH2Br-CH2Br(加 苯等有机化合物的 成反应); 主要性质。 (取代反应); 3.了解乙烯、氯乙 (3)苯: 烯、苯的衍生物等 (加成反应)。 在化工生产中的重 3.同分异构体的书写判断。 要作用。
有机化学课件第九章乙酰乙酸乙酯和丙二酸二乙酯

第一章 有机化合物概述 第二章 脂肪烃和脂环烃 第三章 芳香烃 第四章 对映异构体 第五章 卤代烃 第六章 醇、酚和醚 第七章 醛和酮 第八章 羧酸及其衍生物 第九章 乙酰乙酸乙酯和 丙二酸二乙酯 第十章 含氮有机化合物 第十一章 含杂原子有机化 合物 第十二章 生命有机化学 第十三章 有机化合物的波 谱知识简介 第十四章 有机化合物的分 离与纯化技术
化合物 CH3COCH3 H2O ROH EtO2CCH2CO2Et NCCH2CO2Et CH3COCH2CO2Et CH3COCH2COCH3 C6H5COCH2COCH3
O CHO
pKa 20 16 15 13.3 9 10.3 9
烯醇式含量 1.5×10-4(痕量)
7.7×10-3 2.5×10-1
乙酰乙酸乙酯实际上是酮式和烯醇式的混合物, 酮式和烯醇式混合物是互变异构体,两者处 于平衡状态,互相转换。在室温时,液态乙 酰乙酸乙酯是由约 7.5% 的烯醇式和 92.5% 的 酮式异构体组成的平衡混合物。这种能够互 相转变的两种异构体之间存在的动态平衡现 象就称为互变异构现象。
CH3COCH2COOC2H5
CH3CCH=COC2H5
O
O
OH
O
CH3 O
CH O H
OC2H5
CH3CCH2COC2H5
CH3C=CHCOC2H5
酮式(92.5%)
烯醇式(7.5%)
(三)乙酰乙酸乙酯在合成上的应用
得到的 -烃基取代的乙酰乙酸乙酯,再进行酸式或 酮式分解,可制得甲基酮、二酮、一元或二元羧酸。 还可用来合成酮酸及其他环状或杂环化合物 P163。
2、乙酰乙酸乙酯的酸式分解 乙酰乙酸乙酯与浓 的NaOH共热,则在α-和β-C原子之间发生断裂,生 成 两分子乙酸盐——故称为乙酰乙酸乙酯的酸式分 解。
第九章有机含氮化合物优秀课件

R N H 2
N2 H C3 H COO 4 NH N2 O
170℃
N2 O
N2 O
2. 腈和酰胺的还原
O
=
C3H
L
C 6 H 5NCC3H
i4 ,A 醚 lH C C 6 H 3 5H NC2 C H 3H
C15H 31CO O H
N H 3,△ H 2O
C15H 31CO NH 2
◆烃分子中的氢原子被一个或几个氨基取代后的 化合物统称为胺。
胺按氮原子连接的烃基数目不同, 可分为1°、 2°、3°胺。
RNH2 1°
R2NH 2°
R3N 3°
命名参见书P368
§9-2-1胺的制备方法 1. 氨或胺的烃基化
亲核试剂:NH3、RNH2(以1°胺为宜)。 烃基化试剂:卤代烃
R X + N H 3
OH N2O
◆Cl原子的邻、对位上的-NO2数目↑,其反应活性↑
Cl NO 2
Na2CO 3
130℃
O H NO 2
Cl NO2
NO2
10% Na2CO3 △, 煮沸
OH NO2
NO2
Cl O2N NO2
NO2
H2O 沸腾
OH O2N NO2
NO2
NO2 NaOH
Cl
Cl H2O
NO2
Cl
OH
§9-2 胺
P2O 5 ,△
H 2O C16H 31C
NH 2, N i
C15H 31CH 2NH 2
3. 酰胺的Hofmann降解
=O N a O C l,N a O H
N H 2
N H 2
第九章第一讲 甲烷乙烯苯

CH4+Cl2 → CH3Cl+HCl(第一步) →___________________________________________
→___________________________________________ CHCl3+Cl2→CCl4+HCl
光
考点突破 实验探究 高考演练 课时训练
考点一 甲烷
乙烯
苯
1.甲烷、乙烯、苯的比较 甲烷
物理性质 化 学 燃烧
乙烯
苯
无色液体
无色气体,难溶于水
性
溴
易燃、完全燃烧生成CO2和H2O 在Fe粉作用下发生 不反应 加成反应 取代反应 不反应 取代 氧化反应 加成、聚合
+) KMnO (H 4 质
不反应
加成、取代
主要反应类型
考点突破 实验探究 高考演练 课时训练
考点一 甲烷
乙烯
苯
烃的常见反应类型
(1)氧化反应 ①燃烧反应 ②KMnO4(H+)氧化
(2)取代反应 ①烷烃、苯及其同系物发生的卤代反应
考点一 甲烷
乙烯
苯
2.甲烷、乙烯、苯的特征反应 (1)取代反应:有机物分子里的某些原子或原子团被其他
原子或原子团 ____________________ 所替代的反应。
①完成甲烷与Cl2发生取代反应的化学方程式:
考点突破 实验探究 高考演练 课时训练
考点一 甲烷
乙烯
苯
2.甲烷、乙烯、苯的特征反应 (2)加成反应
考点一 甲烷
乙烯
苯
2.甲烷、乙烯、苯的特征反应 (1)取代反应:有机物分子里的某些原子或原子团被其他
原子或原子团 ____________________ 所替代的反应。
有机物概述

1 、有机物 — 碳氢化合物及其衍生物。( 但CO、 CO2 、碳酸、碳酸盐、金属碳化物 、CN-、SCN-、 等看作无机物。)
组成元素:碳、氢、氧、氮、硫、磷、卤素等
2 、有机化学 — 研究碳氢化合物及其衍生物的化学 科学.
(二)、有机化合物的特点
1、可燃性:绝大数有机化合物都可以燃烧,如棉花、汽油、 木材、酒精等。如大多数无机化合物,如酸、碱、盐、氧化 物等都不能燃烧。因而有时采用灼烧试验可以区别有机物和 无机物。 2、熔点低:在室温下,绝大多数无机化合物都是高熔点的固 体,而有机化合物通常为气体、液体或低熔点的固体。例如, 氯化钠和丙酮的相对分子质量相当,但二者的熔、沸点相差 很大。 大多数有机化合物的熔点一般在400oC以下,而且它们的 熔、沸点随着相对分子质量的增加而逐渐增加。一般地说, 纯粹的有机化合物都有固定的熔点和沸点。 3.难溶于水:水是一种强极性物质,所以以离子键结合的无 机化合物大多易溶于水,不易溶于有机溶剂。而有机化合物 一般都是共价键型化合物,极性很小或无极性,所以大多数 有机化合物在水中的溶解度都很小,但易溶于极性小的或非 极性的有机溶剂(如乙醚、苯、烃、丙酮等)中,这就是 “相似相溶”的经验规律。正因为如此,有机反应常在有机 溶剂中进行。
第三节
一、自由基反应
C
有机反应的类型
Y
:
均 裂
C
. + Y.
自由基
共价键的均裂:共价键断裂时共用电子对平均分给成键的两个原子,产 生(游离基)自由基.
例如:烷烃的卤化反应历程
由游离基引起的、连 续循环进行的反应称 游离基取代反应
二、离子型反应
C
:
Y
异 裂
第九章 有机化合物第三节 生活中两种常见的有机物

松油醇是一种调香香精,它是α、β、γ 三种同分异构体组成的混合物,可由松 节油分馏产品A(下式中的18是为区分两 个羟基而人为加上去的)经下列反应制得:
试回答:
(1)α-松油醇的分子式__________。
(2)α-松油醇所属的有机物类别是
________________。
a.醇
b.酚
编 ① 号
②
③
④
装 置
(3)实验时可观察到装置②中A瓶的石灰 水变浑浊。A瓶溶液的作用是________; B瓶溶液的作用是________;C瓶溶液 的作用是________。 (4)装置③的作用是________;装置① 中所盛的是________溶液,作用是 ________。 (5)装置④中所盛的固体药品是 ________,它可以确认的产物是 ________。 (6)尾气如何处理?
有机物A的结构简式如下图:
(1)A与过量NaOH溶液完全反应时,A与 参加反应的NaOH的物质的量之比为 __________。 (2)A与新制Cu(OH)2且悬浊液完全反应 时,A与参加反应的Cu(OH)2的物质的量 之比为__________,其中A与被还原 的Cu(OH)2的物质的量之比为 __________________。 (3)A与过量NaHCO3溶液完全反应时,A 与参加反应的NaHCO3的物质的量之比 为__________。
[解析] 醇若要能发生催化氧化,分子中 与—OH直接相连的碳原子上必须连有氢 原子,且当—OH连在碳链末端时其被氧 化成醛,当—OH连在碳链中间时,其被 催化氧化成酮。醇若要能发生消去反应, 分子中与—OH直接相连的碳原子的邻位 碳上必须有氢原子。 [答案] A、B、D、F E B、C、D、E
有机化学第九章要点全解

2598 含氮及杂环化合物内容提要本章主要讲述含C 、H 、O 、N 、X 等原子的化合物,着重阐述硝基化合物,胺类化合物以及胺的衍生物。
一些简单实用的杂环化合物也是本章学习的重点。
从结构上理解它们的性质,且掌握这些化合物的应用价值。
有机化合物除了含C 、H 外,还可含O 、N 、X 等杂原子。
前面讨论了含O ,X 的有机化合物,本章着重介绍有机含氮及杂环化合物。
前面章节中学过了腈、酰胺等含氮化合物,本章重点讨论硝基化合物、胺、季銨盐、重氮化合物、偶氮化合物和叠氮化合物。
它们的一般结构通式为:R-NO 2(Ar-NO 2) R-NH 2(Ar-NH 2) R 4N X ArN 2X(RN 2X) Ar-N=N-Ar(Ar')硝基化合物胺季銨盐类重氮化合物偶氮化合物由结构通式可知它们是不同氧化态的含氮有机物,因此,它们的性质和制备方法既有区别又有关联。
此外,本章还讨论C 与杂原子(如O 、N 、S)组成的环状化合物,即杂环化合物。
8.1 硝基化合物8.1.1 硝基化合物的命名和结构特征分子中含有硝基-NO 2的化合物称为硝基化合物,结构通式为:R-NO 2(Ar-NO 2)。
硝基化合物从结构上可看作烃的一个或多个氢原子被硝基取代的产物,可分为脂肪族硝基化合物和芳香族硝基化合物,脂肪族硝基化合物又可分为伯、仲、叔硝基化合物。
硝基化合物的命名类似于卤代烃,即以硝基为取代基命名,例如:CH 3NO 2CH 3CHCH 3NO 2CH 3O 2N硝基甲烷 2-硝基丙烷 对硝基甲苯在硝基化合物中,N 原子为sp 2杂化态,形成三个共平面的σ键,未参加杂化的具有一孤对电子的p 轨道与两个氧原子的p 轨道形成π43共轭体系。
两个N=O 键是等价的。
但习惯上写成R NO, 也有的写成R NO O 。
硝基甲烷分子的键长和键角为:H 3C N OC -N 147pm ,N -O 122pm ,∠ONO 为 127°两个N -O 键的键长相等,说明它们没有区别。
第九章 第一节 认识有机化合物
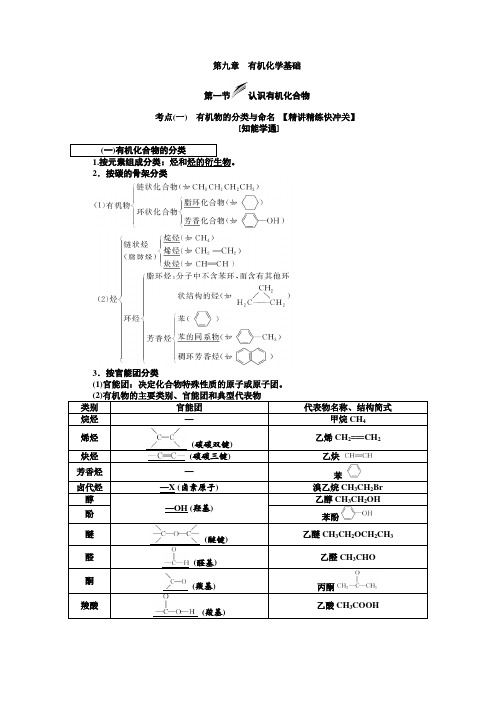
第九章有机化学基础第一节认识有机化合物考点(一)有机物的分类与命名【精讲精练快冲关】[知能学通]烃和烃的衍生物。
2.按碳的骨架分类3.按官能团分类(1)官能团:决定化合物特殊性质的原子或原子团。
CH CHCH COOH2.烷烃的系统命名法(1)几种常见烷基的结构简式甲基:—CH3;乙基:—CH2CH3;丙基:—CH2CH2CH3、。
(2)如命名为3-甲基己烷。
3.烯烃和炔烃的命名如命名为4-甲基-1-戊炔。
4.苯的同系物的命名(1)习惯命名法如称为甲苯,称为乙苯,二甲苯有三种同分异构体,分别为(邻二甲苯)、(间二甲苯)、(对二甲苯)。
(2)系统命名法将苯环上的6个碳原子编号,以某个甲基所在的碳原子的位置为1号,选取最小位次号给另一甲基编号。
如邻二甲苯也可叫作1,2-二甲苯,间二甲苯也叫作1,3-二甲苯,对二甲苯也叫作1,4-二甲苯。
5.烃的含氧衍生物的命名(1)醇、醛、羧酸的命名(2)酯的命名合成酯时需要羧酸和醇发生酯化反应,命名酯时“先读酸的名称,再读醇的名称,后将‘醇’改‘酯’即可”。
如甲酸与乙醇形成酯的名称为甲酸乙酯。
[题点练通]1.S-诱抗素制剂能保持鲜花盛开。
S-诱抗素的分子结构如图,下列关于该分子说法正确的是()A.含有碳碳双键、羟基、羰基、羧基B.含有苯环、羟基、羰基、羧基C.含有羟基、羰基、羧基、酯基D.含有碳碳双键、苯环、羟基、羰基解析:选A根据S-诱抗素的分子结构可知含有碳碳双键()、羟基(—OH)、羰基()、羧基(—COOH)。
2.对下列物质的类别与所含官能团的判断中不正确的是()A.醇类—OHB.CH3CH2COOH羧酸类—COOHC.酮类—CHOD.CH3CH2Br卤代烃类—Br解析:选C含有—OH,且—OH不与苯环直接相连,属于醇,故A正确;含有羧基,属于羧酸类,故B正确;含有醛基,属于醛类,故C错误;含有溴原子,属于卤代烃类,故D正确。
3.(1)中的官能团名称是_________________________。
有机化学第九章酚和醌PPT课件

酸性
部分醌类化合物具有酸性,能与碱反应生成盐 。
取代反应
在一定条件下,醌类化合物能发生取代反应,引入其他基团。
醌的加成反应
与烯烃的加成
在催化剂作用下,醌能与烯烃发生加成反应,生成相应的醇。
与炔烃的加成
醌也能与炔烃发生加成反应,生成相应的酮。
与氢气的加成
在催化剂存在下,醌能与氢气发生加成反应,生成相应的醇或酮。
醌的加成反应
醌可以与烯烃、炔烃等发生加成反应,生成环状的 化合物,这些化合物在有机合成中具有重要的应用 价值。
醌的取代反应
醌上的羰基可以被卤素、羟基等取代,生成 相应的取代产物,这些取代产物在有机合成 中具有重要的应用。
酚和醌在药物合成中的应用
酚类药物
许多药物分子中含有酚羟基结构,如阿司匹林、对乙酰氨基酚等,这些药物具 有解热镇痛、抗炎等作用。
酚的氧化反应
酚可以被氧化为醌或其他氧化产物,这些氧化产物在有机合成中具 有重要应用,如用于合成染料、药物等。
酚的缩合反应
酚可以与醛、酮等羰基化合物发生缩合反应,生成酚醛树脂等高分子 化合物,用于制备塑料、胶粘剂等。
醌在有机合成中的应用
醌的还原反应
醌可以被还原为酚或其他还原产物,这些还 原产物在有机合成中具有重要应用,如用于 合成香料、药物等。
醌的还原反应
化学还原
使用还原剂(如钠、锌等)可将醌还原为对应的酚。
催化氢化
在催化剂(如铂、钯等)存在下,通过氢气可将醌还 原为酚。
电化学还原
通过电解的方法,可将醌还原为酚或酮。
04
酚和醌的合成方法
酚的合成方法
芳香烃磺化碱熔法
芳香烃与浓硫酸反应生成磺酸,再与碱熔融 得到酚。
有机化学-第九章醛酮醌

3、低级醛酮的沸点比相对分子量相近的醇低。 (分子间无氢键)。
4、低级醛酮易溶于水,醛酮都能溶于水。丙酮能 溶解很多有机化合物,是很好的有机溶剂。
二、 醛酮的化学性质
1、 加成反应
• 烯烃的加成一般为亲电加成; • 醛酮的加成为亲核加成,易于HCN、NaHSO3、ROH、 RMgX等发生亲核加成反应。
(1)一般过酸 + 无机强酸(H2SO4) (2)强酸的过酸 :CF3COOOH (3)一般酸 + 一定浓度的过氧化氢(产生的过酸立即反应)。
反应机理
O
H+ +OH
R-C-R'
R-C-R'
OH
R-C-R'
+
-H+ O R"COO-H
OH R-C-R'
O-OCR" O
R
O
R' C
O O
H
O
C R"
R’重排 O-O键断裂 -R”COO- , -H+
(1)碳碳双键加成
2,3,5,6-四溴环己二酮
注意:两种方法的适用范围
• 克莱门森还原——适用对酸不敏感的化合物; 如:NH2-CH2-CH2-CO-CH3,就不能用此方法,
含有-NO2也被同时还原。 • 武尔夫-克日聂尔-黄鸣龙反应——适用对碱不敏感的
化合物; 如:含有羧基等就不行。
补充:
-CO,-NO2均 还原!
用HCl,可使 之变为酚!
• 由于醛基直接连在芳环上的芳醛都没有氢原子, 所以可以用坎尼扎罗反应来制备芳香族醇:
二、烃基的反应
1、α-氢原子的卤代反应
高中化学第九章 有机化合物知识点总结

第九章有机化合物第一讲认识有机化合物——主要的烃考点1主要烃的结构和性质一、有机化合物1.有机化合物:是指含碳元素的化合物,但含碳化合物CO、CO2、碳酸及碳酸盐属于无机物。
2.烃:仅含有碳、氢两种元素的有机物。
3.烷烃:碳原子与碳原子以单键构成链状,碳的其余价键全部被氢原子饱和,这种烃称为饱和链烃,也称为烷烃。
二、甲烷、乙烯和苯的结构与物理性质比较三、甲烷、乙烯和苯的化学性质比较下面从几种常见的有机反应类型角度认识三种主要烃:1.取代反应有机物分子里的某些原子或原子团被其他原子或原子团所替代的反应。
(1)甲烷与Cl2的取代反应(2)苯的取代反应(填化学方程式)2.加成反应有机物分子中的不饱和碳原子与其他原子或原子团直接结合生成新的化合物的反应。
(1)乙烯的加成反应(填化学方程式)(2)苯的加成反应苯与H2发生加成反应的化学方程式3.加聚反应乙烯合成聚乙烯塑料的化学方程式为四、烷烃1.烷烃的结构与性质2.烷烃的习惯命名法(1)当碳原子数n≤10时,用甲、乙、丙、丁、戊、己、庚、辛、壬、癸表示;当n>10时,用汉字数字表示。
(2)当碳原子数n相同时,用正、异、新来区别。
例如:CH3CH2CH2CH2CH3称为正戊烷,(CH3)2CHCH2CH3称为异戊烷,C(CH3)4称为新戊烷。
考点2同系物与同分异构体一、有机物中碳原子的成键特征1.碳原子的最外层有4个电子,可与其他原子形成4个共价键,而且碳碳原子之间也能相互形成共价键。
2.碳原子不仅可以形成单键,还可以形成双键或三键。
3.多个碳原子可以相互结合形成碳链,也可以形成碳环,碳链或碳环上还可以连有支链。
二、同系物1.定义:结构相似,在分子组成上相差一个或若干个CH2原子团的物质互称为同系物。
2.烷烃同系物:分子式都符合C n H2n+2(n≥1),如CH4、CH3CH3、互为同系物。
3.同系物的化学性质相似,物理性质呈现一定的递变规律。
三、同分异构体1.概念:具有相同的分子式,不同结构的化合物互称为同分异构体。
2015届高考化学总复习 第九章 第三节芳香烃精讲课件

【例1】 面的是(
(双选)下列化合物分子中的所有原子都处于同一平 )
A.溴苯C.氯ຫໍສະໝຸດ 烯B.对二甲苯D.丙烯
解析:B、D选项中均含有—CH3,依据甲烷的结构可知化合
物中所有的原子一定不在同一平面上;由苯的结构、乙烯的
结构可知A、C两项符合。 答案:AC
主要 产品
润滑油、 溶剂油、 凡士林、 汽油、煤 石蜡、 油、柴油、 沥青、煤 重油 焦油
抗震性能好 的汽油和甲 乙烯、丙烯、 烷、乙烷、 1,3-丁二烯 丙烷、丁烷、 等 乙烯、丙烯 等
主要化学成分 一般是C5~C11的 原油直接分馏, 直馏汽油 烷烃及少量的芳香 物理变化 烃等,性质稳定 含有C5~C11的烷 重油裂化,化学 裂化汽油 烃和烯烃,性质活 变化 泼
催化裂化
在催化剂存在 的条件下,把 相对分子质量 大、沸点高的 烃断裂为相对 分子质量小、 沸点低的烃
石油的裂解
在高温下,把 石油产品中具 有长链分子的 烃断裂为各种 短链的气态烃 或液态烃
原理
用蒸发冷凝的 方法把石油分 成不同沸点范 围的蒸馏产物
主要 原料
原油
重油
重油
含直链烷烃 的石油分馏 产品(含石油 气)
天然气
天然气田、油田
甲烷
燃料、化工原料
【例 2】
如何从石油中获得更多的轻质燃油一直是化学家
探索的课题,将石油分馏得到的重油进行裂化可以获得更多 的轻质燃油。
资料 1 :石蜡是含有 20 ~ 30 个碳原子的烷烃的混合物,常温
下呈固态。 资料2:石油催化裂化中通常使用Al2O3作催化剂。 某研究性学习小组在实验室中模拟石油的催化裂化,装置如 下图,实验过程中可观察到烧瓶Ⅰ中固体石蜡先熔化,试管 Ⅱ中有少量液体凝结,试管Ⅲ中酸性高锰酸钾溶液褪色,实 验后闻试管Ⅱ中液体气味,具有汽油的气味。
第九章 第1讲 认识有机化合物

第1讲认识有机化合物[考纲要求] 1.能根据有机化合物的元素含量、相对分子质量确定有机化合物的分子式。
2.了解常见有机化合物的结构;了解有机物分子中的官能团,能正确表示它们的结构。
3.了解确定有机化合物结构的化学方法和某些物理方法。
4.了解有机化合物存在同分异构现象,能判断简单有机化合物的同分异构体(不包括手性异构体)。
5.能根据有机化合物命名规则命名简单的有机化合物。
考点一有机化合物的组成、分类和性质特点1.有机物的组成和性质特点(1)组成特点含有碳元素的化合物称为有机化合物,简称有机物。
(但CO、CO2、碳酸及其盐、金属碳化物、金属氰化物等由于组成、性质与无机物相似,属于无机物)。
绝大多数有机化合物都含有氢元素。
C、H、O、N、S、P、卤素是有机物中的主要组成元素。
(2)性质特点(大多数有机物)①物理性质特点熔点低、易燃、不易导电,难溶于水,易溶于酒精、汽油、苯等有机溶剂。
同一系列有机物,随着相对分子质量的增大,分子间作用力增大,熔、沸点升高。
烃的衍生物的官能团大多数是极性基团,大大增强了分子间的作用力,故烃的衍生物的熔沸点比具有相近相对分子质量的烃的熔、沸点高。
极性较强的有机物能溶于水,随着碳原子数的增加,有机物在水中的溶解度逐渐减小。
②化学性质特点有机反应比较复杂,反应速率慢,一般需加热和使用催化剂,常伴有副反应,因而所得产品往往是混合物。
2.有机化合物的分类及官能团(1)按碳的骨架分类①有机化合物 ⎩⎨⎧链状化合物(如CH 3CH 2CH 3)环状化合物⎩⎪⎨⎪⎧脂环化合物(如OH )芳香化合物(如OH )②烃⎩⎪⎪⎨⎪⎪⎧脂肪烃⎩⎪⎨⎪⎧链状烃⎩⎪⎨⎪⎧烷烃(如CH 4)烯烃(如CH 2===CH 2)炔烃(如CH ≡CH )脂环烃:分子中不含苯环,而含有其他环状结构的烃(如CH 2H 2CCH 2)芳香烃⎩⎪⎨⎪⎧苯()苯的同系物(如CH 3)稠环芳香烃(如)(2)按官能团分类①官能团:决定化合物特殊性质的原子或原子团。
第九章 烃

基础化学
2、有机化学的概念
第九章
aliphatic 脂肪烃 hydrocarbons
有机化学(organic chemistry)是研究有机化合物 的组成、结构、性质及其变化规律的科学。
葛美林(Gmelin.L)凯库勒(KeKule .A)认为碳是有机 化合物的基本元素,把“碳化合物称为有机化合物”, “有机化学定义为碳化合物的化学”。 肖莱马(Schorlemmer,c.)把有机化学定义为研究烃及其 衍生物的化学。
基础化学
第九章
aliphatic 脂肪烃 hydrocarbons
1、有机化合物的概念
自从拉瓦锡(Lavoisier.A.L)和李比希(Von Liebig.J.F) 创造有机化合物的分析方法之后,发现有机化合物均含 有碳元素,绝大多数的含氢元素,此外,很多的有机化 合物还含氧、硫、氮等元素。
碳氢化合物及其衍生物称为有机化合物,简称有机物。 注意:简单的含碳化合物归属无机物。
基础化学
第九章
aliphatic 脂肪烃 hydrocarbons
1874年范特霍夫(Vant Hoff.J.H)和勒贝尔(Le Bel,J.A)分别 提出碳四面体构型学说,建立了分子的立体概念,说明 了旋光异构现象; 1885年拜尔(Von Baeyer.A)提出张力学说; 20世纪建立了现代有机结构理论; 1916年路易斯(Lewis,G.N)提出了共价键电子理论; 20世纪30年代量子力学原理和方法引入化学领域以后, 建立了量子化学; 20世纪60年代合成了维生素B12,发现了分子轨道守恒 原理; 20世纪90年代初合成了海葵毒素。
基础化学
第九章
aliphatic 脂肪烃 hydrocarbons
有机化学课件--醚和环氧化合物

3
第一节 醚的定义、分类、 结构特征和命名
一 醚的定义 H
R
醚?
O
O
H
R
二 醚的分类 (I)
醚的分类(II)
(取代基是否相同)
(取代基类型)
简单醚:ROR
混合醚:ROR’ 环醚
二烷基醚 二芳基醚 烷芳混合醚
乙烯醚 烯丙醚
2020/2/3
课件
4
三 醚的结构特征
1. 烷基醚分子中氧原子是sp3杂化, 整个分子成交叉构象。
(1)烯烃与过氧化物反应
O
C6H5C O OH
C6H5CH=CH2
CHCl3
O
C6H5CH
CH2
H
H
CH3CO3H, C6H6
H
O
CC
25℃
C6H5
C6H5
C6H5
H C6H5
2020/2/3
课件
33
注意:如果烯烃有顺反异构,用过氧酸氧化后,取 代基的相对位置不变,再如:
H C
C6H5
C6H5 C
CH3
141.0pm
O 111.7o
H H
H H
HH
H H
O
H H
H
O 105o
H
2. 芳基醚分子中氧原子采用sp2,氧原子中的一对 孤电子与苯环中的π电子存在p-π共轭。
136pm
CH3
H
O 108.9o
CH3
O
CH3
121o
2020/2/3
课件
5
四 醚的命名
R
1. 普通命名法:
O
写出两个烃基的名称,再加上“醚”字,
第九章第45讲认识有机化合物2025年高考化学一轮复习

(2)
中含氧官能团的名称是__(_酚__)羟__基__、__酯__基___。
(3)
— 22 —
中含有的官能团名称是__碳__碳__双__键__、__酯_基__、__羰__基____。
— 返回 —
脂环化合物与芳香族化合物的区别 芳香族化合物与脂环化合物的主要区别在于是否含有苯环等芳香环。芳香族化合物
类别
官能团
烷烃
代表物名称、结构简式 甲烷 CH4
烯烃
炔烃 芳香烃 卤代烃
醇 酚
□07 __________(碳碳双键)
—C≡C—(碳碳三键)
—X(碳卤键)
□08 __—__O__H____(羟基)
乙烯 CH2==CH2
乙炔 HC≡CH 苯
溴乙烷 C2H5Br 乙醇 C2H5OH 苯酚 C6H5OH
— 返回 —
— 19 —
— 返回 —
关键能力提升 一、有机化合物的分类和官能团的识别 1.下列有机化合物中:
— 返回 —
— 20 —
— 返回 —
(1)从官能团的角度看,可以看作醇类的是(填字母,下同)___B_D____;可以看作酚类的 是__A_B__C___;可以看作羧酸类的是__B_C__D___;可以看作酯类的是__E__。
— 返回 —
( □10
— 13 —
— 返回 —
②系统命名法 将苯环上的 6 个碳原子编号,以某个甲基所在的碳原子的位置为 1 号,选取最小位次 号给另一甲基编号。如邻二甲苯也可叫作 1,2-二甲苯,间二甲苯也叫作 1,3-二甲苯,对二 甲苯也叫作 1,4-二甲苯。
— 14 —
(3)含官能团有机物的命名
— 37 —
— 返回 —
基本有机化合物

三、有机化合物的分类
两种分类法: 链状 (一)按碳架分类 碳环
杂环
(二)按官能团分类
官能团——指有机物中能决定一类化合物 主要性质的原子或基团。见表9-1
第二节 链烃
分子中只含有C、H两种元素的化合物—— 碳氢化合物,简称烃。
链烃
饱和烃 ——烷烃 烯烃
不饱和烃 炔烃
环烃 脂环烃
芳香烃
一、链烃的结构(P111) (一) 碳原子的杂化
CH 2
CH 2
CH 2
4-甲基-6-乙基壬烷
CH 3
CH 3
(相*同注,:小C基H3先、写C。H2)CH3位次
CH 3 CH 2 CH CH 2 CH CH 3
CHCH 3
CH 3
2,5-二甲基-3-乙基己烷
CH 3
(*两条相同主链,选含取代基多的;如相同取 代基位次相同,则使第三取代基位次最பைடு நூலகம்。)
C3H CH C3H 2-溴 丙 烷 Br
主要产物
马氏规则——不对称加成时,氢加在含H多 的双键C上。
练习:
Br
HBr
CH 3 CH 2 C CH 2
CH3 CH2 C CH3
H 2C CC 3 H C3H
2-甲基-1-丙烯
碳原子的类型:伯碳 1º;仲碳 2º;叔碳 3º;季碳 4º。 (伯氢)(仲氢)(叔氢)
a
13
练习:
写出分子式为C9H20,含有8个2°氢原 子和12个1 °氢原子的烷烃结构式。
答案:
CH2 CH3
CH3 CH2
C CH2 CH3 1°
CH2 CH3
甲烷
H
键角109º28’,具有正四面体 构型。
有机化学

+ I (CH3CH2)4N
碘化四乙铵
(CH3CH2)3N OH CH3
氢氧化甲基三乙铵
+
练习题
NHCH3
[ (CH3)2N(C 2H5)2] I
+
N-甲基苯胺
NH2
碘化二甲基二乙基铵
CH3CHCHCH2CH3 CH3
3-甲基-2-氨基戊烷
二.胺的物理性质(自学)
三.胺的化学性质 胺的分子结构
●●
4.与亚硝酸反应 脂肪族伯胺
R NH2 NaNO2 HCl
0-5℃醇、烯、卤代烃
N2
放出的氮气是定量的,可用于氨基的定量分析 。
芳香族伯胺
Ar NH2
0
NaNO2 HCl
。 5C
[Ar
N N]Cl
H2O
NaCl
芳香胺重氮盐 低温稳定,室温分解成酚和氮气
仲胺与亚硝酸反应
R2NH NaNO2 HCl R2N N O (黄色油状)
重氮化反应应用
可以制备一些不能用直接方法制备的化合物
NO2 浓HNO3 浓 H2SO4 N2+ClNaNO2 HCl
0 5。 C
NH2 Fe HCl
NH2 Br2 H2O Br Br Br
Br Br
Br
H3PO2
Br Br
Br
(2)偶联反应
重氮盐与芳香叔胺类或酚类化合物在弱碱性、中性或弱 酸性溶液中发生反应,生成偶氮化合物,称为偶联(偶合) 反应。
CH3 N CH2CH3
N
CH2CH3
Cl
N-甲基-N-乙基环戊胺 H2NCH2CH2 CH2 CH2 NH2 1,4-丁二胺(腐胺)
N-甲基-N-乙基-4-氯苯胺 CH3CH2NHCH2CH2CH3 乙、丙胺
第九章 含硫、磷有机化合物

宁德职业技术学院
(二)命名 简单的含硫化合物的命名,只需在相应的含氧衍生物类 名前加上“硫”字即可.
宁德职业技术学院
含硫有机物, 有时也可将巯基作为取代基来命名.
亚砜、砜、磺酸及其衍生物的命名,也只需在类名前 加上相应的烃基的名称.
宁德职业技术学院
二.硫醇和硫酚 (一)物理性质 分子量较低的硫醇有毒,并有难闻的嗅味,煤气中加乙硫 醇作警示剂. 黄鼠狼发出的臭味, 主要含3-甲基-1-丁硫醇. 但C9以上硫醇有令人愉快的气味. 水溶性 、沸点比相应的醇低 得多,与分子量相应的硫醚相近. 硫酚也有恶臭味. (二)化学性质 1.酸性 硫醇和硫酚的酸性比对应的醇和酚强.
宁德职业技术学院
(二)代森锌
代森锌淡黄或灰色, 不溶于水, 有臭鸡蛋味. 代森锌是一种 保护性杀菌剂, 对病菌具有较强的触杀作用, 对人、畜毒性低, 对作物安全. 可用于防治麦类锈病, 白粉病, 苹果花腐病, 各种 蔬菜霜毒病, 炭疽病, 马铃薯晚疫病等多种真菌性病害.
宁德职业技术学院
(三)克菌丹
宁德职业技术学院
(二)敌百虫
敌百虫是无色晶体, 可溶于水. 它是一种高效低毒有机 磷杀虫剂, 对昆虫具有胃毒和触杀作用, 农业上可用于防治 多种害虫; 家庭中可用来杀灭蚊蝇等. 它对哺乳动物毒性很 低, 可用于防治家畜体内外的寄生虫.
宁德职业技术学院
(三)甲胺磷
甲胺磷为白色晶体, 易溶于水、甲醇及丙酮等极性 溶剂. 具有胃毒和触杀及内吸作用, 是一种高效的广谱 性杀虫、杀螨剂. 对抗药性蚜虫、螨类和稻飞虱及稻纵 卷叶螟的效果较好.
宁德职业技术学院
磺胺类药物能杀死的细菌有链球菌、肺炎球菌、脑膜炎 双球菌、琳球菌、葡萄球菌、大肠杆菌、痢疾杆菌、鼠疫杆 菌等, 主要用于医治血液中毒、上呼吸道感染(如咽喉炎、扁 桃腺炎、中耳炎、肺炎等 )、 泌尿道感染、肠道传染病、淋 病、脑膜炎、眼部感染(如结膜炎、沙眼)、疟疾以及许多其 他传染病. 长期服用磺胺药后,细菌会有抗药性.
