预防艾滋病、梅毒、乙肝母婴传播督导质控登记表(1)
(1.2)预防艾滋病梅毒乙肝母婴传播工作督导表

(附件1.2)预防艾滋病梅毒乙肝母婴传播工作督导表标准化文件发布号:(9312-EUATWW-MWUB-WUNN-INNUL-DDQTY-KII附件1预防艾滋病、梅毒和乙肝母婴传播专项督导表县(市、区)督导医院督导时间督导专家 .附件2预防艾滋病、梅毒和乙肝母婴传播项目调查表区:医院(盖章):填报日期:一、项目管理A1. 制定本院合理的预防艾滋病、梅毒和乙肝母婴传播服务流程:0 无 1有,请督导当天提供A2. 指定专人负责预防母婴传播工作:0 无 1有,姓名:联系方式:A3. 本院为孕期未进行HIV抗体检测的临产入院孕产妇提供两种试剂的快速检测的流程或方案:0 无 1有,请督导当天提供A4. 对相关工作人员进行预防母婴传播服务内容及服务流程培训:0 无 1有,请督导当天提供培训记录A5. 面向孕产妇的宣教资料包含艾滋病、梅毒和乙肝相关知识:0 无 1有,请督导当天提供相关宣教资料二、检测能力B1.艾滋病检测开展艾滋病抗体筛查:0 未开展(跳至B13)1 开展,标本外送至:检测(跳至B13)2 开展,本院初筛方法:已配备的筛查试剂:开展快速检测:0无 1 有,快速检测试剂1快速检测试剂2B2.梅毒检测开展非梅毒螺旋体抗原血清学实验:0 无 1 有,方法(可多选):1 RPR 2 TRUST 3 其他开展梅毒螺旋体抗原血清学实验:0 无 1 有,方法(可多选):1 TPPA 2 ELISA 3 其他开展梅毒螺旋体暗视野检查: 0 无 1 有开展梅毒螺旋体IgM 抗体检测:0 无 1 有三、期间服务情况C1.为艾滋病、梅毒感染孕产妇提供医学咨询和转介服务,并签署转介知情同意书:0 无 1有,请督导当天提供留存的知情同意书C2.本院分娩的产妇检测情况:分娩产妇数人,活产儿人孕期未接受HIV抗体检测的临产产妇共人,其中同时用两种不同的快速检测试剂进行HIV抗体筛查试验的有人,仅用一种快速检测试剂检测的有人,未进行快速检测的有人,未检测原因:仅产时(孕期未测)接受梅毒检测的产妇有人。
预防艾滋病、梅毒、乙肝母婴传播督导质控登记表

16分
4、管理人员对信息管理工作的熟练程度
对相关人员进行现场提问及操作考核
25分
工作人员完全不熟悉扣25分,一般熟悉扣5分,非常熟悉扣0分
管理人员对工作一般熟悉扣5分
20分
时间:
质控签名:
预防艾滋病、梅毒、乙肝母婴传播督导质控登记表
预防艾滋病、梅毒、乙肝母婴传播项目信息管理督导质控记录表
评价项目
评价方法
分数
扣分标准
扣分原因
实得分
1、有信息管理相关制度
查看制度相关资料,及落实制度相关资料
25分
无具体制度资料扣15分,无落实制度资料扣10分
未发现问题
25分
2、原始资料的管理
现场查看门诊、病房、检验等记录和报表、个案登记卡
25分
无门诊、病房、检验等记录和报表、个案登记卡各扣4分,记录、报表、登记卡信息记录不完整或记录不清楚扣5分
门诊、检验、病房记录不清扣5分
20分
3、信息管理的硬件设备
现场查看资料存放柜、计算机、网络设备及工作区域
25分
纸质资料无专门资料柜存放扣7分,无专用计算机、无网络上报系统、工作区域设置不合理各扣6分
预防梅毒乙肝母婴传播工作报表

仅 产 时 乙 肝 表 面 抗 原 阳 性 产 妇 数
乙 肝 表 面 抗 原 阳 性 产 妇 总 数
乙 肝 表 面 抗 原 阳 性 产 妇 所 生 活 产 数
其 中 : 注 射 乙 肝 免 疫 球 蛋 白 的 儿 童 数
接 受 梅 毒 检 测 产 妇 数
梅 毒 感 染 产 妇 总 数
梅 毒 感 染 产 妇 所 生 活 产 数
孕 期 接 受 梅 毒 检 测 产 妇 数
仅 产 时 接 受 梅 毒 检 测 产 妇 数
仅 产 时 诊 断 为 梅 毒 感 染 产 妇 数
梅 毒 感 染 产 妇 总 数
梅 毒 感 染 产 妇 所 生 活 产 数
孕 期 接 受 乙 肝 表 面 抗 原 检 测 产 妇 数
仅 产 时 接 受 乙 肝 表 面 抗 原 检 测 产 妇 数
填报 人:
说明: 县级妇幼机构收集各级医疗保健机构每季度的数据,按月分列,第二季度第一个月(即当年4、7、10月及次年1月)10日前汇总上报市级妇幼机构; 市级妇幼机构,按县分列,第二季度第一个月(即当年4、7、10月及次年1月)15日前汇总上报省级妇幼机构。
接 受 乙 肝 表 面 抗 原 检 测 产 妇 数
乙 肝 表 面 抗 原 阳 性 产 妇 总 数
乙 肝 表 面 抗 原 阳 性 产 妇 所 生 活 产 数
其 中 : 注 射 乙 肝 免 疫 球 蛋 白 的 儿 童 数
(甲) 1
2
3
4
5
6
7
8
9
10
11121314源自151617
18
19
20
21
22
23
填报 单位
预防梅毒乙肝母婴传播工作报表
预防艾滋病、梅毒和乙肝母婴传播项目督导表

%( / );先天梅毒治疗率: %( / );其他情况:
%( / );先天梅毒治疗率: %( / );其他情况:
%( / );先天梅毒治疗率: %( / );其他情况:
%( / %( /
%(
理 情 况 评 分
乙肝 免疫 球蛋 白注 射
对乙肝表面抗原阳性孕产妇所生新生儿,在12小时内尽早注 查阅1-5月报表、
查阅文件和相关资 料
1.有
2.无
所到机构的相关部门和科室原始登记、留存的报表个案和随
访登记及相关检测化验单保存完整、准确符合逻辑:及时上 查阅相关登记。
信息管 报审核数据;无漏报。
理
个案及时录入系统,并正确及时完成全部HIV、梅毒个案的县 级终审。
查看艾梅乙系统
原始登记:1.有 1.是 2.否
2.无
14、报表按时上报、个案及时录入(10分) (1-5月中,凡有一次报表未按时上报一次扣1分,个案未及时录入扣1分,扣完为止,特殊情况除外)
合计
分
督导组组长:
督导人员:
督导日期:
以上,并建立随访登记记录和阳性管理档案。
查阅1-5月HIV阳性 有 2.部分有 3.无
应用 全县HIV感染孕产妇所生儿童抗病毒用药率达到95%以上,并 抗病 建立随访登记记录。
产妇及所生婴儿的 抗病毒用药率为: 保健资料、病历、
%( / );随访登记:1.有 2.无
毒药
服药记录、个案卡 县级综合医院: %;民营医院: %;治疗记录:1.齐全(机构名称:
称:
) 、不掌握(机构名称:
)
务
主要问题
检 测 服 务
抽查机构入院分娩者中仅产时的检测率达到100%。医务人员 熟悉服务流程和干预要求;咨询登记、随访登记、上报留底 产房 报表、个案是否完整、及时,与检验科检测登记、上报县级 数据是否一致;保障隔离防护设施持续供应(隔离产房、防护 服等)
预防艾滋病、梅毒、乙肝随访登记卡

编号:□□□□□□—□□□—□□□□—□□□表 3–Ⅰ 、艾滋病病毒感染孕产妇/婚检妇女基本情况登记卡(保密)省(自治区、市) 县(市、区) 医院(妇幼保健院)一、基本情况 姓名: 身份证号: . 出生日期: 年 月 日(如出生日期不详,实足年龄: 岁) 民族: 汉、 壮、 满、 回、 苗、 维吾尔、 彝、 土家、 蒙古、 藏、 其他 文化程度: 文盲/半文盲、 小学、 初中、 高中(含中专、职业高中、技工学校等) 大专或大学、 硕士及以上、 不详 职业: 学生(研究生、大学、中学) 、 教师、 保育员及保姆、 餐饮食品业、 商业服务、 医务人员、 工人、 农民工、 农民、 牧民、 渔(船)民、 干部职员、 离退人员、 家务及待业、 其他 、 不详 婚姻状况: 未婚、 已婚( 初婚、 再婚) 、 同居、 离婚、 丧偶 孕产情况: 孕次、 产次、 现有子女数 现住址(详填) : 省 市 县(区) 乡(镇、街道) 村 (门牌号) 户口所在地: 省 市 县(区) 乡(镇、街道) 村 (门牌号) 工作单位: 联系电话(非必填) : 孕产妇/婚检妇女属于: 本县区、 本市其他县区、 本省其他地市 外省、 港澳台、 外籍 (国家) 二、艾滋病病毒感染相关情况 确认艾滋病病毒感染时期: 婚前检查、 人工流产、 引产、 孕期保健、 产时、 产后、 其他 确认艾滋病病毒感染时间: 年 月 日 本次妊娠前是否已知 HIV 感染(仅感染孕产妇填写) : 否、 是:本次是确认 HIV 感染后第 次妊娠 最可能的艾滋病病毒感染途径: 注射毒品、 性传播、 采血(浆) 、 输血/血制品、 母婴传播、 职业暴露、 不详、 其他 相关危险行为(多选) : 与 HIV 感染配偶或男友的性生活、 多性伴、 商业性行为、 注射吸毒、 有偿采供血、 输血或使用血制品、 纹身或穿耳等身体刺伤、 意外伤害、 职业暴露、 医源性感染、 不详、 其他 三、丈夫/性伴情况 姓名: 出生日期: 年 月 日(如出生日期不详,实足年龄: 岁) 民族: 汉、 壮、 满、 回、 苗、 维吾尔、 彝、 土家、 蒙古、 藏、 其他 文化程度: 文盲/半文盲、 小学、 初中、 高中(含中专、职业高中、技工学校等) 大专或大学、 硕士及以上、 不详 职业: 学生(研究生、大学、中学) 、 教师、 保育员及保姆、 餐饮食品业、 商业服务、 医务人员、 工人、 农民工、 农民、 牧民、 渔(船)民、 干部职员、 离退人员、 家务及待业、 其他 、 不详 HIV 检测情况: 不详、 未检测、 检测 HIV 检测结果: 不详、 阴性、 阳性,确认感染的时间: 年 月 日、 不详 最可能的艾滋病病毒感染途径: 注射毒品、 异性传播、 同性传播、 采血(浆) 输血/血制品、 母婴传播、 职业暴露、 不详、 其他 、 相关危险行为(多选) : 无危险行为、 多性伴、 嫖娼、 同性性行为、 注射吸毒、 有偿采供血、 输血或使用血制品、 纹身或穿耳等身体刺伤、 意外伤害、 职业暴露、 医源性感染、 不详、 其他 四、本次接受预防艾滋病母婴传播服务情况 本次接受预防艾滋病母婴传播服务的时期: 婚前检查、 人工流产、 引产、 孕前、 孕期、 艾滋病检测前咨询情况: 未咨询、 咨询; 艾滋病检测后咨询情况: 未咨询、 咨询 报告单位(盖章) : 联系电话: 备注(非必填) : 报告医生: 填报日期:产时、产后年月日编号:□□□□□□—□□□—□□□□—□□□1表 3–Ⅱ 、艾滋病病毒感染孕产妇妊娠及所生婴儿登记卡(保密)省(自治区、市) 县(市、区) 医院(妇幼保健院) 姓名: 身份证号: . 一、本次妊娠、孕产期保健及分娩情况 本次妊娠末次月经时间: 年 月 日,预产期: 年 月 日,初检孕周: 周 妊娠结局: 分娩、 自然流产、 人工终止妊娠,终止妊娠孕周: 周、 其他 是否失访: 未失访、 已失访,失访时期: 孕周或产后 周 孕产期异常情况(多选) : 未发生、 早产、 中重度贫血、 妊娠高血压疾病、 胎膜早破、 滞产、 产后出血、 妊娠合并糖尿病、 妊娠合并心脏病、 妊娠合并肝病、 妊娠梅毒、 其他 分娩方式: 阴道产、 择期剖宫产、 急诊剖宫产、 不详 分娩时间: 年 月 日 时 分, 孕周+ 天,总产程 小时 分 分娩地点: 市级以上助产机构、 县(区)级助产机构、 乡(街道)级助产机构、 家中、 其他 产科操作(多选) : 无、 侧切、 人工破膜、 胎吸、 产钳、 宫内头皮监测、 不详、 其他 会阴裂伤: 无、 Ⅰ 度裂伤、 Ⅱ 度裂伤、 Ⅲ 度裂伤及以上 分娩胎数: 单胎、 双胎、 三胎、 其他 (多胎请另附本表分别填写围产儿、新生儿有关内容) 孕产妇结局: 存活、 死亡,死亡原因 、 不详 围产儿转归: 活产、 死胎、 死产、 七天内死亡、 不详 围产儿异常情况(多选) : 无、 早产或低出生体重、 围产期肺炎、 新生儿窒息、 出生缺陷 、 其他 随访情况:孕期随访 次 二、孕产妇抗艾滋病病毒药物应用情况: 用药、 未用药(跳至“三、孕产妇复方新诺明用药情况”) 开始用药时间: 孕期, 孕周、 产时、 产后 孕期: 未用药、 用药,药物名称: + + ,漏服情况: 未漏服、 漏服 次 产时: 未用药、 用药,药物名称: + + ,漏服情况: 未漏服、 漏服 次 产后: 未用药、 用药,药物名称: + + ,漏服情况: 未漏服、 漏服 次 停止用药情况: 未停药、 已停药,停药时间: 孕期, 孕周、 产时、 产后 天 三、孕产妇复方新诺明用药情况: 用药、 未用药(跳至“四、孕产妇相关检测情况”) 开始用药时间: 孕期, 孕周、 产时、 产后 停止用药情况: 未停药、 已停药,停药时间: 孕期, 孕周、 产时、 产后 天 四、孕产妇相关检测情况: 进行过检测(检测填写结果,未检测用“/”表示) 、 未进行任何检测(跳至“四、新生婴儿情况”) 相关检测 检测结果 检测结果 检测结果 检测结果 检测孕周/时间 孕周 孕周 孕晚期 孕周/ 产时 产后 周 白细胞计数( 109/L) . . . . 总淋巴细胞计数( 109/L) . . . . 血小板计数( 109/L) 血红蛋白(g/L) 血糖(mmol/L) . . . . 谷丙转氨酶(ALT) (u/L) . . . . 谷草转氨酶(AST) (u/L) . . . . 总胆红素(T.BIL) (μmol/L) . . . . 血肌酐(μmol/L) . . . . 血尿素氮(mmol/L) . . . . CD4 细胞计数(个/mm3) CD8 细胞计数(个/mm3) 病毒载量(拷贝/ mL) 未检测、 检测,检测时间: 孕周 检测方法: 梅毒螺旋体抗原血清学试验(TPPA、TPHA 等) 非梅毒螺旋体抗原血清学试验(RPR、TRUST 等) 其他___________ 、 、 梅毒 梅毒螺旋体抗原血清学试验检测结果: 阴性、 阳性、 不确定、 不详 非梅毒螺旋体抗原血清学试验检测结果: 阴性、 阳性、 不确定、 不详 滴度: 未检测、 1:8 以下、 1:8~1:64、 1:64~1:128、 1:128~1:256、 1:256 以上 其他检测结果: 阴性、 阳性、 不确定、 不详 表面抗原(HBsAg) 未检测、 检测,检测时间: 孕周 检测结果: 阴性、 阳性、 不确定、 不详 乙肝 e 抗原(HBeAg) 未检测、 检测,检测时间: 孕周 检测结果: 阴性、 阳性、 不确定、 不详 HCV-IgG 未检测、 检测,检测时间: 孕周 检测结果: 阴性、 阳性、 不确定、 不详 丙肝 HCV-IgM 未检测、 检测,检测时间: 孕周 检测结果: 阴性、 阳性、 不确定、 不详 五、新生婴儿情况(如有多个活产婴儿,请分别填写婴儿基本情况及用药情况) 姓名: 性别: 男、 女 出生日期: 年 月 日 出生体重: 克 出生身长: . 厘米 随访情况: 随访中、 已失访 存活情况: 存活、 死亡,死亡原因 ,死亡时间: 年 月 日 预防接种情况: 未接种、 乙肝疫苗第一针、 卡介苗、 不详 六、新生婴儿抗艾滋病病毒药物应用情况: 用药、 未用药(跳至“报告单位(盖章)处”) 开始用药时间: 年 月 日,停止用药时间: 年 月 日 药物名称: + + ,漏服情况: 未漏服、 漏服 次 报告单位(盖章) : 报告医生: 联系电话: 填报日期: 年 月 日 备注(非必填) :; ; ; ; ; ; ; ; ; ; ; ; ; ; ; ; ; ; ; ; ; ; ; ; ; ; ; ; ; ; ; ; ; ; ; ; ; ; ; ; ; ; ; ; ; ; ; ; ; ; ; ;孕产妇编号:□□□□□□—□□□—□□□□—□□□2儿童编号:□□□□□□—□□□—□□□□—□□□—□表 3–Ⅲ 、艾滋病病毒感染产妇及所生儿童随访登记卡(保密)省(自治区、市)孕产妇姓名: 儿童姓名: 民族: 汉、 壮、 现住址(详填) : 随访日期: 一、感染妇女情况 (一)随访情况: (二)存活情况: (三)转介服务: (四)避孕情况: 身份证号: 性别: 男、 女 满、 回、 苗、 维吾尔、 乡(镇、街道) 村 年 月 日县(市、区)医院(妇幼保健院).出生日期: 年 月 彝、 土家、 蒙古、 藏、 其他 (门牌号) 联系电话(非必填) ; : 月 随访人姓名:日儿童月龄:随访、 未随访、 已失访,失访原因 存活、 死亡,死亡原因 、 不详 未提供、 提供,转介原因 ,转介机构 未避孕、 不详 避孕,避孕方法(可多选) : 安全套、 宫内节育器、 口服避孕药、 开始应用避孕方法时间: 年 月 随访、 存活、 未提供、不详、其他二、儿童情况 (一)随访情况: (二)存活情况: (三)转介服务:未随访、 已失访,失访原因 死亡,死亡原因 ,死亡时间: 年 提供,转介原因 1 ,转介机构 1 转介原因 2 ,转介机构 2 (四)生长发育:体重: 不详、 . 千克, 年龄别体重评价: 下 中 身长: 不详、 . 厘米, 年龄别身长评价: 下 中 身长别体重评价: 下 中 (五)喂养方式: 纯母乳喂养、 人工喂养、 混合喂养、 其他 (六)辅食添加: 未添加、 已添加, 月龄开始添加 (七)疾病情况(多选) : 未发现、 病理性黄疸、 上呼吸道感染、 病理性腹泻、 肺炎、 佝偻病、 中重度营养不良、 不详、 其他 (八)相关症状(多选) : 未发现、 间歇或持续性发热、 持续性咳嗽、 皮疹、 全身性淋巴结肿大、 口、咽部念珠菌感染、 肝脾肿大、 不详、 其他 (九)预防接种情况: 卡介苗: 未接种、 接种、 不详 乙肝疫苗: 未接种、 接种, (第 1/ 2/ 3 针) 、 不详 脊髓灰质炎疫苗: 未接种、 接种, (第 1/ 2/ 3 剂) 、 不详 麻疹疫苗: 未接种、 接种、 不详 百白破混合制剂: 未接种、 接种, (第 1/ 2/ 3 针) 、 不详 其他: 未接种、 接种, 、 不详 (十)HIV 检测: 未检测(跳至(十三)应用复方新诺明预防卡氏肺孢子虫肺炎处) 已检测,检测时间: 年 月 日 (十一)HIV 检测结果: 阴性、 阳性、 不确定、 不详、 其他 (十二)HIV 检测方法(多选) : DNA PCR 或其他早期诊断、 抗体筛查、 抗体确认试验、 其他 (十三)预防应用复方新诺明: 未应用、 应用,开始时间: 年 月 日 是否停药: 否、 是,停止时间: 年 月 停止原因________________________ (十四)备注(非必填) : 报告医生: 填报日期:月日上 上 上贫血、不详、日,报告单位(盖章) : 联系电话:年月日3编号:□□□□□□—□□□—□□□□—□□□表 4–Ⅰ 、梅毒感染孕产妇登记卡(保密)省(自治区、市) 一、基本情况 姓名: 出生日期: 民族: 职业: 汉、 壮、 文化程度: 年 满、 文盲/半文盲、 农民、 已婚( 回、 小学、 牧民、 初婚、 产次、 年 省 省 市 市 身份证号: 月 日(如出生日期不详,实足年龄: 苗、 维吾尔、 教师、 再婚) 、 月 彝、 土家、 蒙古、 初中、 岁) 藏、 其他 大专或大学、 其他 硕士及以上、 工人、 、 不详 不详 医务人员、 . 县(市、区) 医院(妇幼保健院)高中(含中专、职业高中、技工学校等) 、 保育员及保姆、 干部职员、 离婚、 同居、 餐饮食品业、 离退人员、 丧偶 年 乡(镇、街道) 乡(镇、街道) 月学生(研究生、大学、中学) 、 农民工、 未婚、商业服务、渔(船)民、 现有子女数家务及待业、婚姻状况: 孕产情况:孕次、本次妊娠末次月经时间: 现住址(详填) : 户口所在地: 工作单位: 二、梅毒感染相关情况 诊断梅毒感染时期: 诊断梅毒感染时间: 最可能的梅毒感染途径: 性传播、 血液传播、 婚前检查、 年日,预产期: 县(区) 县(区)日,初检孕周: 村 村 (门牌号) (门牌号)周联系电话(非必填) : 人工流产、 月 不详、 引产、 日 其他___________________ 商业性行为、 不详 不详 月 日、 不详 输血或使用血制品、 纹身或穿耳等身体刺伤 、 意外伤害、 孕期、 产时、 产后、 其他母婴传播、相关危险因素(多选) : 与梅毒感染配偶或男友的性生活、 职业暴露、 医源性感染、 丈夫/性伴梅毒检测情况: 丈夫/性伴梅毒检测结果: 丈夫/性伴梅毒检测时间: 三、孕产妇本次妊娠梅毒诊断检测情况 梅毒螺旋体抗原血清学试验: 未检测、 检测,检测方法及时间: 检测时间: 检测时间: 检测时间: 检测时间: 检测时间: 滴度结果: 1: 未检测、 滴度结果: 1: 滴度结果: 1: 滴度结果: 1: 滴度结果: 1: 检测,检测时间: 报告医生: 填报日期: 检测时间: ,检测时间: ,检测时间: ,检测时间: ,检测时间: 年 月 年 日 月 日 检测,检测方法及时间: 年 年 年 年 月 月 月 月 日 日 日 日 年 月 年 年 年 年 日 月 年 日 月 日 月 月 月 日 日 日 梅毒螺旋体颗粒凝集试验(简称 TPPA) 酶联免疫吸附试验(简称 ELISA) 梅毒螺旋体血凝试验(简称 TPHA) 梅毒螺旋体 IgM 抗体检测 梅毒快速检测 其他________________________ 非梅毒螺旋体抗原血清学试验定量检测: 快速血浆反应素环状卡片试验(简称 RPR) 甲苯胺红血清不需加热试验(简称 TRUST) 性病研究实验室玻片试验(简称 VDRL) 其他________________________ 暗视野显微镜梅毒螺旋体检测: 报告单位(盖章) : 联系电话: 备注(非必填) : 未检测、 检测、 阳性、 多性伴、 其他 未检测、 阴性、 年 不详、4孕产妇编号:□□□□□□—□□□—□□□□—□□□ 儿童编号:□□□□□□—□□□—□□□□—□□□—□表 4–II、梅毒感染产妇及所生儿童随访登记卡(保密)省(自治区、市) 县(市、区) 医院(妇幼保健院)梅毒感染孕产妇/母亲姓名: 身份证号: . 现住址(详填) : 市 乡(镇、街道) 村 (门牌号) 联系电话: ; 一、孕产妇本次妊娠及分娩情况 妊娠结局: 分娩、 自然流产, 孕周: 周、 人工终止妊娠,终止妊娠孕周: 周、 其他 是否失访: 未失访、 已失访,失访时期: 孕周或产后 周 分娩日期: 年 月 日 分娩方式: 阴道顺产、 阴道助产、 择期剖宫产、 急诊剖宫产、 不详 分娩胎数: 单胎、 双胎、 三胎、 其他 孕产妇结局: 存活、 死亡,死亡原因 、 不详 围产儿转归: 活产、 死胎、 死产、 七天内死亡、 不详 围产儿异常情况(多选) : 无、 早产或低出生体重、 围产期肺炎、 新生儿窒息、 出生缺陷、 其他 二、孕产妇梅毒药物应用情况: 用药、 未用药 治疗疗程: 个,首个治疗疗程与最后一个治疗疗程之间间隔: 周 治疗药物(多选) : 普鲁卡因青霉素 G、 苄星青霉素 G、 头孢曲松、 红霉素、 其他 用药时期(多选) : 孕早期、 孕中期、 孕晚期、 产时 是否规范治疗: 是、 否 用药详细信息: 第一个疗程 开始用药孕周: 孕周,药物名称: 普鲁卡因青霉素 G、 苄星青霉素 G 、 头孢曲松、 红霉素、 其他 持续用药次(天)数: 次(天) ,用药剂量 (万 U/次或 g/日) 第二个疗程 开始用药孕周: 孕周,药物名称: 普鲁卡因青霉素 G 、 苄星青霉素 G 、 头孢曲松、 红霉素、 其他 持续用药次(天)数: 次(天) ,用药剂量 (万 U/次或 g/日) 第三个疗程 开始用药孕周: 孕周,药物名称: 普鲁卡因青霉素 G、 苄星青霉素 G、 头孢曲松、 红霉素、 其他 持续用药次(天)数: 次(天) ,用药剂量 (万 U/次或 g/日) 三、梅毒检测情况: 孕产妇分娩前或孕晚期非梅毒螺旋体抗原血清学试验: 快速血浆反应素环状卡片试验(简称 RPR) 滴度结果: 1: ,检测时间: 年 月 日 甲苯胺红血清不需加热试验(简称 TRUST) 滴度结果: 1: ,检测时间: 年 月 日 性病研究实验室玻片试验(简称 VDRL) 滴度结果: 1: ,检测时间: 年 月 日 其他 滴度结果: 1: ,检测时间: 年 月 日 所生婴儿出生后非梅毒螺旋体抗原血清学试验: 快速血浆反应素环状卡片试验(简称 RPR) 滴度结果: 1: ,检测时间: 年 月 日 甲苯胺红血清不需加热试验(简称 TRUST) 滴度结果: 1: ,检测时间: 年 月 日 性病研究实验室玻片试验(简称 VDRL) 滴度结果: 1: ,检测时间: 年 月 日 其他 滴度结果: 1: ,检测时间: 年 月 日 四、梅毒感染孕产妇所生儿童情况 姓名: 性别: 男、 女 出生体重: 克 出生身长: . 厘米 (一)随访情况: 未失访、 失访,失访原因 (二)存活情况: 存活、 死亡,死亡原因 ,死亡时间: 年 月 日 (三)相关症状(多选) : 未发现、 水泡-大疱,红斑,丘疹,扁平湿疣、 鼻炎或喉炎、 全身性淋巴结肿大 骨髓炎,骨软骨炎及骨膜炎、 贫血、 肝脾肿大、 不详、 其他 (四)梅毒检测结果: 未检测、 阴性、 阳性、 不确定、 不详、 其他 (五)是否需要进行预防性治疗 是 否 (六)是否接受预防性治疗 是 否 (七)儿童梅毒感染状态: 诊断先天梅毒、 排除梅毒感染 (八)诊断为先天梅毒的依据(多选) 出生时非梅毒螺旋体抗原血清学试验滴度高于母亲分娩前滴度的 4 倍; 暗视野显微镜检查到梅毒螺旋体或梅毒螺旋体 IgM 抗体检测阳性; 随访过程中非梅毒螺旋体抗原血清学试验由阴转阳,或滴度上升且有临床症状; 随访至 18 月龄时梅毒螺旋体抗原血清学试验仍阳性。
(产科)预防艾滋病、梅毒、乙肝母婴传播工作产妇监测登记表
住 院 号
注 未 未 未 未 未 未 未 未 未 咨 阴 阳 咨 阴 阳 阴 阳 阴 阳 阴 阳 阴 阳 注 射 咨 检 咨 检 检 检 检 检 注 询 性 性 询 性 性 性 性 性 性 性 性 性 性 射 时 询 测 询 测 测 测 测 测 射 间
备注
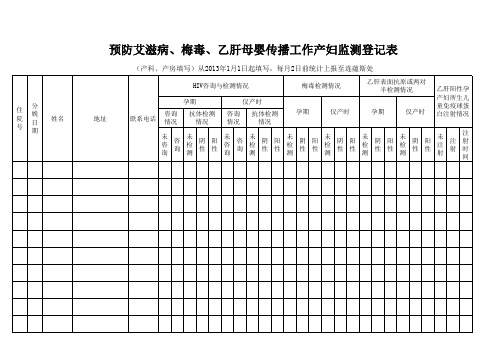
预防艾滋病、梅毒、乙肝母婴传播工作产妇监测登记表
(产科、产房填写)从2013年1月1日起填写,每月2日前统计上报至连藴斯处
HIV咨询与检测情况 分 娩 日 期 孕期 姓名 地址 联系电话 咨询 情 况 抗体检测 情况 咨询 情况 仅产时 抗体检测Байду номын сангаас情况 孕期 仅产时 孕期 仅产时 梅毒检测情况 乙肝表面抗原或两对 半检测情况 乙肝阳性孕 产妇所生儿 童免疫球蛋 白注射情况
预防艾滋病梅毒乙肝母婴传播工作产妇监测登记表姓名地址联系电话梅毒检测情况备注孕期咨询情况抗体检测情况抗体检测情况咨询阴性阳性咨询阴性阳性阴性阳性阴性阳性阴性阳性阴性阳性注射产科产房填写从2013年1月1日起填写每月2日前统计上报至连藴斯处住院分娩日期hiv咨询与检测情况乙肝表面抗原或两对半检测情况乙肝阳性孕产妇所生儿童免疫球蛋白注射情况咨询注射时间
6预防艾滋病、梅毒和乙肝母婴传播报表上报流程及要求

三、月报表
月报表上报时限
各级医疗保健机构信息统计员每月5日前上 报至市妇幼保健院 市妇幼保健院收集、整理每月12日前上报 至省妇幼保健院
月报表上报要求
Байду номын сангаас
月报表数据必须根据医疗机构门诊、病房、 产房孕妇监测登记表产生
月报表个案数与个案卡必须一致
个案卡上报时限
诊5日内填写上报:艾滋病、梅毒感染孕产妇/婚检妇女基本 况登记卡(表3-Ⅰ、表4-Ⅰ)
娠结局或产褥期后5日内填写上报:艾滋病、梅毒感染孕妇 娠及所生婴儿登记卡(表3-Ⅱ、表4-Ⅱ)
童满1、3、6、9、12、18个月后5日内填写上报:艾滋病 染产妇及所生儿童随访登记卡(表3-Ⅲ、表4-Ⅲ)
预防艾滋病、梅毒和乙肝母婴传 播报表上报流程及要求
东莞市妇幼保健院保健部
廖志妍
一、原始资料登记
预防艾滋病、梅毒和乙肝母婴传播工作孕妇监测登记表 (由医疗保健机构门诊填写)
预防艾滋病、梅毒和乙肝母婴传播工作产妇监测登记表 (由医疗保健机构产科病房、产房填写)
二、个案登记卡
上报流程
预防艾滋病、梅毒和乙肝母婴传播相关报表上报流程及要求(2020年版)
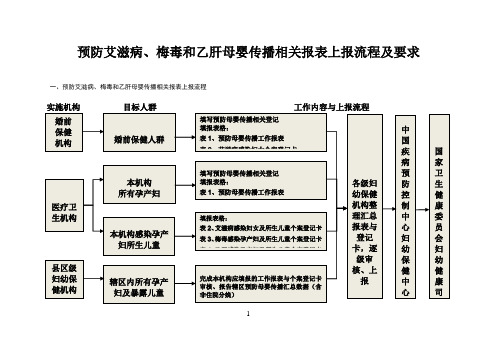
预防艾滋病、梅毒和乙肝母婴传播相关报表上报流程及要求一、预防艾滋病、梅毒和乙肝母婴传播相关报表上报流程实施机构目标人群工作内容与上报流程1二、预防艾滋病、梅毒和乙肝母婴传播报表上报时限及要求(一)预防艾滋病、梅毒和乙肝母婴传播工作报表(表1)。
1.报告对象:所有婚前保健人群及孕产妇人群2.报告时限及要求:各级医疗卫生机构应按时将预防艾滋病、梅毒和乙肝母婴传播工作报表(本机构填写部分)上报至本辖区的县(市、区)级妇幼保健机构。
县(市、区)级妇幼保健机构除完成本机构应填报内容外,还应负责收集、整理、汇总本地区工作汇总数据,审核后尽快完成网络报告。
地(市、州)级妇幼保健机构应负责收集、整理、汇总所辖各县(市、区)工作汇总数据,审核后尽快完成网络报告。
省级妇幼保健机构应于每月15日前完成本省(自治区、直辖市)工作月报表的审核、汇总与网络报告,并上报至中国疾病预防控制中心妇幼保健中心。
(二)预防艾滋病、梅毒和乙肝母婴传播个案卡(表2—表4)。
1.报告对象:所有诊断为艾滋病感染的婚检妇女、孕产妇及其所生的18月龄以内的儿童(表2)。
所有诊断为梅毒感染的孕产妇及其所生的18月龄以内的儿童(表3)。
所有乙肝病毒表面抗原阳性孕产妇及其新生婴儿(表4-I),以及其中血清HBV DNA>2×105IU/ml或HBeAg阳性产妇所生的12月龄内的儿童(表4-II)。
上述报告对象不包括以终止妊娠为直接目的而就医时发现的感染病例。
2.报告时限及要求:表2-I、3-I和4-I应于明确艾滋病、梅毒和乙肝感染状态后的5日内填写完成。
对既往已确诊感染者,也应在本次了解其感染状态后5日内填写完成。
表2-Ⅱ、3-Ⅱ和4-II应分别于艾滋病、梅毒或乙肝感染孕产妇分娩后及出院前填写完成,对发生自然流产、人工终止妊娠、死亡或失访等其他妊娠结局的艾滋病或梅毒感染孕产妇,应在获知其结局后的5日内填写完成。
表2-Ⅲ和3-Ⅲ应分别于艾滋病或梅毒感染产妇所生儿童按规定时限完成随访后5日内填写。
(产科)预防艾滋病、梅毒、乙肝母婴传播工作产妇监测登记表
咨询与检测
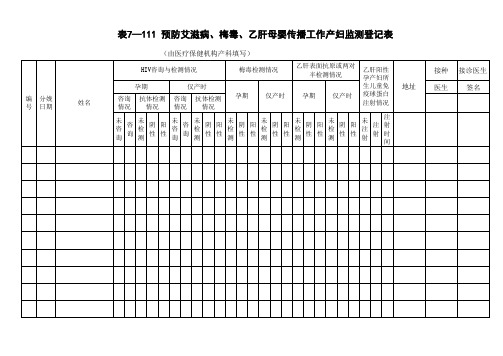
表7—111 预防艾滋病、梅毒、乙肝母婴传播工作产妇监测登记表
(由医疗保健机构产科填写)
HIV咨询与检测情况 孕期 编 号 分娩 日期 姓名 咨询 情况 抗体检测 情况 咨询 情况 仅产时 抗体检测 情况 孕期 仅产时 孕期 仅产时 梅毒检测情况 乙肝表面抗原或两对 半检测情况 乙肝阳性 孕产妇所 生儿童免 疫球蛋白 注射情况
接种 地址 医生
பைடு நூலகம்
接诊医生 签名
注 未 未 未 未 未 未 未 未 未 咨 阴 阳 咨 阴 阳 阴 阳 阴 阳 阴 阳 阴 阳 注 射 咨 检 咨 检 检 检 检 检 注 询 性 性 询 性 性 性 性 性 性 性 性 性 性 射 时 询 测 询 测 测 测 测 测 射 间
填表说明:1、表中内容可结合本机构原有登记,纳入常规分娩登记中;2、孕期“咨询”以该产妇提供孕期的艾滋病检测结果报告单及相关信息材料为依据;3、产时“咨询”指孕期未接受咨询与检测
预防艾滋病、梅毒、乙肝母婴传播工作采血情况登记

填报单位:医院编码:420684-002
填报单位:医院编码:420684-002
填报单位:医院编码:420684-002
填报单位:医院编码:420684-002
填报单位:医院编码:420684-002
填报单位:医院编码:420684-002
填报单位:医院编码:420684-002
填报单位:医院编码:420684-002
填报单位:医院编码:420684-002
填报单位:医院编码:420684-002
填报单位:医院编码:420684-002
填报单位:医院编码:420684-002
填报单位:医院编码:420684-002
填报单位:医院编码:420684-002
填报单位:医院编码:420684-002
填报单位:医院编码:420684-002
填报单位:医院编码:420684-002
填报单位:医院编码:420684-002
填报单位:医院编码:420684-002
填报单位:医院编码:420684-002
填报单位:医院编码:420684-002
填报单位:医院编码:420684-002
填报单位:医院编码:420684-002
预防艾滋病、梅毒、乙肝母婴传播工作采血情况登记
填报单位:医院编码:420684-002。
5 艾梅乙空表格

三、预防艾滋病、梅毒和乙肝母婴传播相关报表表1 预防艾滋病母婴传播工作月报(汇总)表(由妇幼保健机构汇总) 省(自治区、直辖市) 年 月 编 号1. 2. 3. 4. 5. 6. 7. 8. 9. 10. 11. 12. 13. 14. 15. 16. 17. 18. 19. 20. 21. 22. 23. 24. 25. 26. 27. 28. 29. 30. 31.市(县) 人数 指标说明项 接受婚前保健人数目 男 女 男 女 男 女 男 女婚 接受艾滋病咨询人数 前 保 接受 HIV 抗体检测人数 健 HIV 抗体阳性人数 接受初次产前保健的孕妇数 孕 接受艾滋病咨询孕妇数 期 接受 HIV 抗体检测孕妇数 HIV 抗体阳性孕妇数 住院分娩产妇数 孕期接受艾滋病咨询产妇数 孕期接受 HIV 抗体检测产妇数 住 仅产时接受艾滋病咨询产妇数 院 仅产时接受 HIV 抗体检测产妇数 分 仅产时 HIV 抗体检测阳性产妇数 娩 HIV 抗体阳性产妇总数 住院分娩活产数 HIV 抗体阳性产妇所娩活产数 非住院分娩产妇数 孕期接受艾滋病咨询产妇数 非 孕期接受 HIV 抗体检测产妇数 住 仅产时接受 HIV 抗体检测产妇数 院 仅产时 HIV 抗体检测阳性产妇数 分 HIV 抗体阳性产妇数 娩 非住院分娩活产数 HIV 抗体阳性产妇所娩活产数 地区产妇总数 地区活产总数由 表 1–Ⅰ 汇 总 获 得。
由 表 1–Ⅱ 汇 总 获 得。
由 表 1–Ⅲ 汇 总 获 得。
填报时间: 填报单位负责人:1填报人: 填报单位(盖章) :表 1–Ⅱ市(县)编 号 1. 项 目预防艾滋病母婴传播工作月报表(由助产机构填写) 医院(妇幼保健院)人 数 指标说明年月指初次接受孕期保健服务的孕妇人 数。
以艾滋病检测相关告知登记或咨询登 2. 孕 接受艾滋病咨询孕妇数 记或其他记录资料为依据。
孕期初次接受 HIV 抗体检测的孕妇 3. 接受 HIV 抗体检测孕妇数 人数,以艾滋病抗体检测结果报告单 期 为依据。
预防艾滋病梅毒与乙肝母婴传播工作报表填表说明

2020/11/14
11
2020/11/14
12
2020/11/14
13
预防艾滋病母婴传播工作月报表 的上报时限
辖区内的所有助产机构应于每月5日前将上月工作月报 中本机构填写的部分,上报至辖区的县(区)妇幼保 健机构。
县(区)妇幼保健机构于每月8日前将上月工作月报的 数据收集、整理、汇总后,及时完成网上录入和审核 工作。形成“预防艾滋病母婴传播工作月报(汇总) 表”(表1)。
2020/11/14
31
2020/11/14
32
2020/11/14
33
婴儿用药
提供2种抗HIV病毒婴儿用药 ,齐多夫定 (AZT)口服液、奈韦拉平(NVP)口服液,无 论选择哪种药物,都应在婴儿出生后尽早 (6-12小时)开始服用,至出生后4-6周。
2020/11/14
34
2020/11/14
辖区的县(区)妇幼保健机构在接到个案登记卡后 的2日内完成网络直报和审核工作。并负责将原始资料 留存备案,同时上报至省级妇幼保健机构。
2020/11/14
67
几点要求
数据质量要求 真实性、准确性、完整 性
上报时间 及时性 审核报表 逻辑性 表、卡上报要一致
2020/11/14
68
2020/11/14
统一编制。
第三部分,4位,填报年度编码,填写填报所属年份。 第四部分,3位,个人顺序编码,按每个助产机构填报
顺序依次编码。
每个婚检妇女、每个孕产妇的每一次妊娠需对应一个 唯一的编号。
编号的第一、二部分应与填报的助产机构名称一致。
2020/11/14
21
身份证号不详的填写要求
前6位填写上报县(市、区)的行政区划代码。 7-10位填写年份,可根据实足年龄推算。 11-14位填写月份和日期,不详时填写07月01日。 15-18位填写9999依次逆序编写,如9999、9998、9997
预防艾滋病、梅毒、乙肝母婴传播项目随访情况登记册

艾滋病阳性孕产妇艾滋病阳性
孕产妇所生
儿童
梅毒感染孕
产妇
梅毒感染孕
产妇所生儿
童
乙肝阳性孕
产妇
预防艾滋病、梅毒、乙肝母婴传播项目孕产妇、儿童序号姓名性别年龄
接受干预、随访原因
乙肝阳性孕产妇所生儿
童指导、服用
药物(具体
药物名称、
剂量,包括
抗病毒药物
、复方新诺
明、长效青
霉素等)
实验室相关
检查(详细
注明检验名
称及结果,
包括早期诊
断等)
使用乙肝高
效免疫球蛋
白
、儿童提供干预、随访情况登记表
接受干预、随访时间预约下次随
访时间
本次干预、随访情况。
预防艾滋病、梅毒、乙肝母婴传播工作督导评分表

6
建立快速、便捷、合理的检测流程
1
7
建立严格保密制度,制定保密程序和措施
3
(三)信息管理
9
8
专人负责信息管理并对工作熟悉
2
9
资料管理档案化,资料齐全、归档有序,查找便利
1.5
10
原始登记完整,记录保存完好
1.5
11
各类报表完整,上报及时
2
12
上报数据准确,符合逻辑
2
(四)物品、经费管理
6
13
物品登记清楚、发放及时
检测任务要求完成50%
总分
100
2
14
设专账、专人管理,经费到位及时,合理使用
4
二、能力建设
20
(一)人员培训
8
15
参加国家或者省级培训班
2
16
本地区开展逐级培训,培训覆盖率达85%
4
17
检测人员培训覆盖率达85%
2
(二)检测能力
6
18
实验室建设
2
19
实验室管理
2
20
检测操作能力
2
(三)服务环境与预防职业暴露
6
21
良好保密的咨询环境
3
(三)自愿咨询检测-检测服务
8
29
为孕产妇免费提供HIV、乙肝、梅毒抗体筛查检测
4
30
为孕产妇免费提供HIV确诊检测
4
(四)应用药物干预
4
31
及时为HIV阳性孕产妇及所生婴儿提供抗病毒药物婴儿提供预防性治疗;为乙肝表面抗原阳性产妇所生婴儿注射乙肝免疫球蛋白
1
22
人工流产手术室、产科病房及产房布局合理、设施齐全、安全
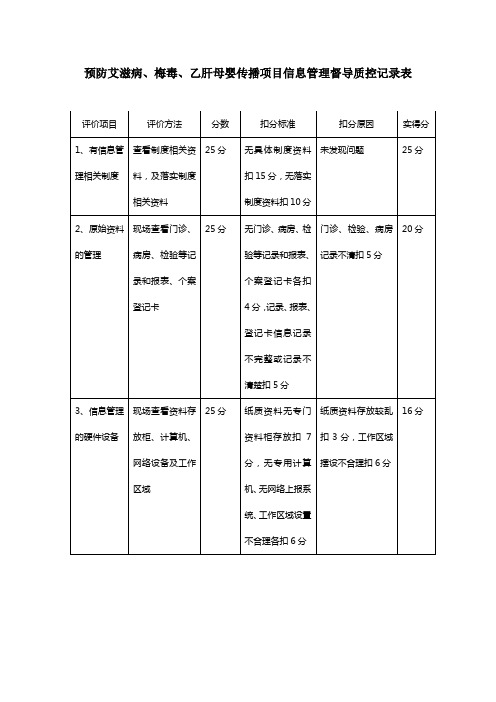
预防艾滋病、梅毒、乙肝母婴传播督导质控登记表
20分
3、信息管理的硬件设备
现场查看资料存放柜、计算机、网络设备及工作区域
25分
纸质资料无专门资料柜存放扣7分,无专用计算机、无网络上报系统、工作区域设置不合理各扣6分
纸质资料存放较乱扣3分,工作区域摆设不合理扣6分
16分
4、管理人员对信息管理工作的熟练程度
对相关人员进行现场提问及操作考核
预防艾滋病、梅毒、乙肝母婴传播项目信息管理督导质控记录表
评价项目
评价方法
分数
扣分标准
扣分原因
实得分
1、有信息管理相关制度
查看制度相关资料,及落实制度相关资料
25分
无具体制度资料扣15分,无落实制度资料扣10分
未发现问题
25分
2、原始资料的管理
现场查看门诊、病房、检验等记录和报表、个案、个案登记卡各扣4分,记录、报表、登记卡信息记录不完整或记录不清楚扣5分
25分
工作人员完全不熟悉扣25分,一般熟悉扣5分,非常熟悉扣0分
管理人员对工作一般熟悉扣5分
20分
时间:
质控签名:
预防艾梅乙母婴传播工作表

单位: 编号 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 孕期 婚 前 检 查 年 月 指标说明
项目 接受婚前保健人数 接受艾滋病咨询人数 接受HIV抗体检测人数 HIV抗体阳性人数 接受初次产前保健的孕妇数 接受艾滋病咨询孕妇数 接受HIV抗体检测孕妇数 HIV抗体阳性孕妇数 住院分娩产妇数 孕期接受艾滋病咨询产妇数 孕期接受HIV抗体检测产妇数 仅产时接受艾滋病咨询产妇数 男 女 男 女 男 女 男 女
填报时间: 填报单位负责人:
人数
由 表 1-I 汇 总 获 得 。来自由表 1- Ⅱ汇总获得 。
住院分娩 仅产时接受HIV抗体检测产妇数 仅产时HIV抗体检测阳性产妇数 HIV抗体阳性产妇总数 住院分娩活产数 HIV抗体阳性产妇所娩活产数 非住院分娩产妇数 孕期接受艾滋病咨询产妇数 孕期接受HIV抗体检测产妇数 非住院分 仅产时接受HIV抗体检测产妇数 娩 仅产时HIV抗体检测阳性产妇数 HIV抗体阳性产妇数 非住院分娩活产数 HIV抗体阳性产妇所娩活产数 地区产妇总数 地区活产总数 填报人: 填报单位(盖章): 由表 1- Ⅲ汇总获得 。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
20分
3、信息管理的硬件设备
现场查看资料存放柜、计算机、网络设备及工作区域
25分
纸质资料无专门资料柜存放扣7分,无专用计算机、无网络上报系统、工作区域设置不合理各扣6分
纸质资料存放较乱扣3分,工作区域摆设不合理扣6分
16分
4、管理人员对信息管理工作的熟练程度
对相关人员进行现场提问及操作考核
25分
工作人员完全不熟悉扣ቤተ መጻሕፍቲ ባይዱ5分,一般熟悉扣5分,非常熟悉扣0分
管理人员对工作一般熟悉扣5分
20分
时间:
质控签名:
预防艾滋病、梅毒、乙肝母婴传播项目信息管理督导质控记录表
评价项目
评价方法
分数
扣分标准
扣分原因
实得分
1、有信息管理相关制度
查看制度相关资料,及落实制度相关资料
25分
无具体制度资料扣15分,无落实制度资料扣10分
未发现问题
25分
2、原始资料的管理
现场查看门诊、病房、检验等记录和报表、个案登记卡
25分
无门诊、病房、检验等记录和报表、个案登记卡各扣4分,记录、报表、登记卡信息记录不完整或记录不清楚扣5分
