初中化学酸碱盐推断题.doc
酸碱盐推断题

③A和D两溶液混合,产生白色沉淀;
④D与F混合产生气泡。C也能与F发生化学反应。
(1)分析上述实验现象,推出各物质中的溶质(填化学式)。
A
,B
,E
。
(2)A与D反应的化学方程式:
;
C与F的化学反应应方程式:
;
D与F的化学反应应方程式:
。
例3
下图是初中化学所学的常见化合物之间的相互转化关系 (反应条件和生成产物中的水已略去)。其中A是一种常见的 建筑材料,B是一种常见的气体,H是一种含钠的化合物。
(2)写出B与盐酸反应的化学方程式: ______________________________________。
(3)D中含有的溶质可能有哪几种情况?①
;
②
;③
。
例6
若下图中A、B、C、D等物质间所发生的反 应均能完全反应,试根据图中变化关系和反应 现象推断:
(1)D是______________;C是____________。 (2)若B是水,则A是__________________。 (3)若B为酸溶液,则A是_____或_______。
例4
物质X和A~F都是初中化学中的常见物质, 且有如图所示的转化关系。已知A、D为碱溶液, 回答下列问题:
(1)写出下列物质的化学式:X 、E 。
(2)写出下列反应方程式:
X+A:
;
D+CuCl2→E+F:
。
例5
A是一种白色难溶于水的钙盐,由三种元素组成, 其相对分子质量为100。
(1)用化学式表示:A ______,B ______。
例7
有一包白色粉末,可能是碳酸钠、氢氧化 镁、氯化钡、硫酸钠、硝酸钠中的一种或几种 的混合物,现做如下实验:
中考化学专题五酸碱盐推断题 A4

专题五酸碱盐推断题一、文字推断题1.有一包白色粉末,可能含有CuSO4、NaCl、AgCl、Na2SO4、Na2CO3中的一种或几种,现进行如下的实验:(1)将白色粉末放入足量的水中,得到无色澄清溶液。
(2)向无色澄清溶液中加入氯化钡溶液,有白色沉淀生成。
(3)向白色沉淀中加入足量的稀硝酸,有部分沉淀溶解,并生成能使澄清石灰水变浑浊的气体。
根据以上事实,该白色粉末中一定含有_________ _______,可能含有_________ ______,一定没有________ __________。
2.某混合物中,可能含有碳酸钠、氯化钙、硫酸铜、硫酸钠、氯化钡中的几种物质,根据下表所列的事实,推3.实验室现有一包白色粉末,可能由氯化钠、硫酸钠、碳酸钠、氯化钡、硫酸铜中的一种或几种组成,其中到底含有那些物质呢?实验探究:Ⅰ.取少量粉末样品于试管中,加水溶解得无色溶液;Ⅱ.取少量粉末样品于另一试管中,滴加稀盐酸,有气泡产生。
请回答下列问题(写化学式):(1)原粉末中一定含有的物质是;(2)原粉末中一定不含有的物质是。
(3)原粉末中可能含有的物质是。
4.某实验室的废液中,可能含有氯化铁、硫酸、硫酸钠、氯化钠、氢氧化钠、碳酸钠和硝酸钡中的一种或多种。
初三化学课外活动小组的同学对废液进行了如下试验:(1)取废液观察,为无色溶液;(2)取废液,向其中滴加氯化钡溶液,有白色沉淀产生,继续加入稀硝酸,无明显现象;(3)另取废液,向其中加入铁粉后,产生大量气泡。
根据以上试验现象可推断,废液中肯定含有_____ ____,肯定不含有_____ ___,不能确定是否含有______ __ 。
5.实验室现有四种失去标签的白色固体,分别为无水硫酸铜、硝酸钡、氯化钡、氢氧化钠中的一种。
为区分它们进行了下列实验:步骤一:将四种固体分别编号为A、B、C、D步骤二:取少量上述白色固体样品分别放入四支试管中,加入足量蒸馏水,振荡,固体全部溶解,且C溶液呈蓝色,则C是(化学式,下同)步骤三:取少量A、B、D的溶液分别放入三支试管中,向三种溶液各加入适量C溶液,装有B溶液的试管中产生蓝色沉淀,则B是,该反应的化学方程式是___________________ _ 装有A溶液和D溶液的试管中均有白色沉淀。
初三化学酸碱盐推断题专题复习一(精析)

初三化学酸碱盐推断题专题复习一(精析)1、有一包白色固体样品,可能由硫酸钠、氢氧化钠、碳酸钙、氯化钡、氯化镁中的一种或几种物质组成,为探究该样品的组成,某小组取适量样品按下列流程进行试验。
请回答下列问题:(查阅资料)CO2不能直接与BaCl2和MgCl2发生反应。
(1)、过滤操作中用到的玻璃仪器有烧杯、漏斗、玻璃棒。
(2)、滤渣a的成分是CaCO3、Mg(OH)2;白色沉淀b的成分是BaCO3。
(3)、滤渣a中加入足量稀盐酸的目的:排除硫酸钡沉淀的干扰,证明样品中无硫酸钠。
(4)、若现象①“滤渣全部溶解”变为“滤渣部分溶解”,其他现象不变,则原样品一定存在的物质是CaCO3、BaCl2、Na2SO4、NaOH。
分析:CaCO3难溶,不和碱、盐反应;Ba2++ SO42- = Ba SO4↓(BaCl2、Na2SO4只能含有一种);MgCl2+ 2NaOH= Mg(OH)2↓+ 2NaCl;设产生0.44g的CO2需要CaCO3的质量为xCaCO3 + 2HCl = CaCl2 + H2O + CO2↑100 44(1g)0.44g1g<1.5g,因此沉淀中还有Mg(OH)2;“滤渣中加入足量的稀HCl,完全溶解,有气泡产生”,因此样品中一定含有CaCO3;“滤液中通入二氧化碳,有白色沉淀生成”,因此样品中一定含有氢氧化钠、氯化钡;白色沉淀b的成分是BaCO3。
2、A~G都是初中化学中常见物质,其中B、D是无色气体,C为白色沉淀,A、E是黑色固体,G为红色固体,C为白色沉淀。
这些物质之间的转化关系如图所示(部分反应物和生成物略去)。
(1)、写出A、E、G的化学式:A、 C、E、 Fe、G、Cu。
(2)、写出C的一种用途:用作建筑材料。
(3)、写出①、②、③的化学方程式:①、Ca(OH)2 + CO2 = CaCO3↓+ H2O;②、Fe3O4 +4CO高温3Fe+4CO2;③、Fe + CuSO4 = FeSO4 + Cu。
酸碱盐的常见化学方程式及推断题练习(1)

酸碱盐的常见化学方程式及推断题练习跟盐酸有关的化学方程式:NaOH(也可为KOH)+HCl==NaCl+H2O 现象:不明显HCl+AgNO3==AgCl↓+HNO3现象:有白色沉淀生成,这个反应用于检验氯离子CaCO3+2HCl==CaCl2+H2O+CO2↑现象:百色固体溶解,生成能使纯净石灰水变浑浊的气体Na2CO3+2HCl==2NaCl+H2O+CO2↑现象:生成能使纯净石灰水变浑浊的气体NaHCO3+HCl==NaCl+H2O+CO2↑现象:生成能使纯净石灰水变浑浊的气体Fe2O3+6HCl==2FeCl3+3H2O 现象:红色固体逐渐溶解,形成黄色的溶液Fe(OH)3+3HCl==FeCl3+3H2O 现象:红棕色絮状沉淀溶解,形成了黄色的溶液Cu(OH)2+2HCl==CuCl2+2H2O 现象:蓝色沉淀溶解,形成黄绿色的溶液CuO+2HCl==CuCl2+H2O 现象:黑色固体溶解,生成黄绿色的溶液Zn+2HCl==ZnCl2+H2↑现象:同上Mg+2HCl==MgCl2+H2↑现象:同上Fe+2HCl==FeCl2+H2↑现象:溶液变成浅绿色,同时放出气体2Al+6HCl==2AlCl3+3H2↑现象:有气体生成以上四个反应,盐酸、硫酸都相似,后面两类就不赘述了,只需写出配平即可;硝酸一般具有氧化性,所以产物一般不为H2跟硫酸有关的化学方程式:2NaOH(或KOH)+H2SO4==Na2SO4+2H2O 现象:不明显Fe2O3+3H2SO4==Fe2(SO4)3+3H2O 现象:红色固体溶解,生成黄色溶液CuO+H2SO4==CuSO4+H2O 现象:黑色固体溶解,生成蓝色溶液Cu(OH)2+H2SO4==CuSO4+2H2O 现象:蓝色沉淀溶解,生成蓝色溶液H2SO4+BaCl2==BaSO4↓+2HCl 现象:生成不溶于强酸的白色沉淀,用于检验硫酸根离子CaCO3+H2SO4==CaSO4+H2O+CO2↑Na2CO3+H2SO4==Na2SO4+H2O+CO2↑2NaHCO3+H2SO4==Na2SO4+2H2O+2CO2↑现象:这三个反应现象同与盐酸反应现象一致跟硝酸有关的化学方程式:Fe2O3+6HNO3==2Fe(NO3)3+3H2O 现象:红色固体溶解,生成黄色溶液CuO+2HNO3==Cu(NO3)2 +H2O 现象:黑色固体溶解,生成蓝色溶液Cu(OH)2+2HNO3==Cu(NO3)2+2H2O 现象:蓝色沉淀溶解,生成蓝色溶液NaOH(或KOH)+HNO3==NaNO3+H2O 现象:不明显Mg(OH)2+2HNO3==Mg(NO3)2+2H2O 现象:白色沉淀溶解CaCO3+2HNO3==Ca(NO3)2+H2O+CO2↑Na2CO3+2HNO3==2NaNO3+H2O+CO2↑NaHCO3+HNO3==NaNO3+H2O+CO2↑现象:以上三个反应现象同与盐酸反应现象一致跟碱有关的化学方程式:NaOH+HCl(或HNO3、H2SO4)==NaCl+H2O 现象:酸碱中和反应,现象不明显CaO+H2O==Ca(OH)2现象:放出大量的热3NaOH(KOH)+FeCl3(Fe(NO3)3、Fe2(SO4)3)==Fe(OH)3↓+3NaCl现象:生成红棕色絮状沉淀,括号里面的反应过程相似,产物相对应就行了2NaOH(KOH)+FeCl2(Fe(NO3)2、FeSO4)==Fe(OH)2↓+2NaCl现象:生成白色絮状沉淀,括号里面的反映过程相似,产物相对应就行了2NaOH(KOH)+CuCl2(Cu(NO3)2、CuSO4)==Cu(OH)2↓+2NaCl现象:生成蓝色絮状沉淀,括号里面的反应过程相似,产物相对应就行了NH4Cl(NH4NO3、(NH4)2SO4)+NaOH(KOH)==NH3↑+H2O+NaCl现象:有可以使石蕊试纸变蓝的气体生成MgCl2(Mg(NO3)2、MgSO4)+2NaOH(KOH)==Mg(OH)2↓+2NaCl现象:生成白色沉淀,括号里面的反应过程相似,产物相对应就行了NaHCO 3+NaOH==Na 2CO 3+H 2O 现象:不明显 此反应的Na 换成K 是一样的 Ca(HCO 3)2+2NaOH==CaCO 3↓+Na 2CO 3+2H 2O现象:生成白色沉淀,此反应把Na 换成K 是一样的2NaOH+CO 2==Na 2CO 3+H 2O 现象:无明显现象 此反应的Na 换成K 是一样的 Ca(OH)2+CO 2==CaCO 3↓+H 2O 现象:产生白色沉淀,此反应用于检验二氧化碳 NaHSO 4+NaOH==Na 2SO 4+H 2O 现象:无明显现象 2NaOH+SO 2==Na 2SO 3+H 2O 现象:无明显现象 跟钡盐有关的化学方程式:BaCl 2+Na 2SO 4==BaSO 4↓+2NaCl 现象:有白色的不溶于强酸的沉淀生成 BaCl 2+Na 2CO 3==BaCO 3↓+2NaCl现象:有白色沉淀生成但可溶于盐酸和硝酸,其实也溶于硫酸,但生成硫酸钡沉淀,不容易看出来 跟钙盐有关的化学方程式:CaCl 2+Na 2CO 3==CaCO 3↓+2NaCl 现象:生成白色沉淀 CaCO 3+CO 2+H 2O==Ca(HCO 3)2 现象:固体逐渐溶解 Ca(HCO 3)2+Ca(OH)2==2CaCO 3↓+2H 2O 现象:生成白色沉淀 跟几种金属及其盐有关的化学方程式:铜:CuSO 4•5H 2O △====CuSO 4+5H 2O ↑ 现象:固体由蓝色变为白色 高温CuO+CO====Cu+CO 2现象:固体由黑色逐渐变成红色,同时有能使纯净的石灰水变浑浊的气体生成H 2+CuO △====Cu+H 2O 现象:固体由黑色逐渐变成红色,同时有水珠生成 Cu+2AgNO 3==Cu (NO 3)2+2Ag 现象:铜表面慢慢生成了银白色金属 CuCl 2+2NaOH==Cu (OH) 2↓+2NaCl 现象:生成了蓝色絮状沉淀CuO+H 2SO 4==CuSO 4+H 2O 现象:黑色固体溶解,生成蓝色溶液 Cu (OH) 2+H 2SO 4==CuSO 4+2H 2O 现象:蓝色沉淀溶解,生成蓝色溶液 Fe(Zn)+CuSO 4==FeSO 4+Cu 现象:有红色金属生成Cu 2(OH)2CO 3△====2CuO+H 2O+CO 2↑现象:固体由绿色逐渐变成黑色,同时有能使纯净石灰水变浑浊的气体生成 铁:Fe+2HCl==FeCl 2+H 2 现象:铁粉慢慢减少,同时有气体生成,溶液呈浅绿色 FeCl 2+2NaOH==Fe(OH)2↓+NaCl 现象:有白色絮状沉淀生成4Fe(OH)2+O 2+2H 2O==4Fe(OH)3 现象:氢氧化铁在空气中放置一段时间后,会变成红棕色 Fe (OH)3+3HCl==FeCl 3+3H 2O 现象:红棕色絮状沉淀溶解,溶液呈黄色 Fe (OH)2+2HCl==FeCl 2+2H 2O 现象:白色絮状沉淀溶解,溶液呈浅绿色 Fe+CuSO 4==FeSO 4+Cu 现象:铁溶解生成红色金属Fe+AgNO 3==Fe(NO 3)2+Ag 现象:铁溶解生成银白色的金属Fe 2O 3+6HCl==2FeCl 3+3H 2O 现象:红色固体溶解,生成黄色的溶液 23432F e O F e O点燃= 现象:铁剧烈燃烧,火星四射,生成黑色的固体Zn+FeCl 2==ZnCl 2+Fe 现象:锌粉慢慢溶解,生成铁 银:AgNO 3+HCl==AgCl ↓+HNO 3 现象:有白色沉淀生成,且不溶于强酸 AgNO 3+NaCl==AgCl ↓+NaNO 3 现象:有白色沉淀生成,且不溶于强酸Cu+2AgNO 3==Cu(NO 3)2+2Ag 现象:红色的铜逐渐溶解,同时有银白色的金属生成 2AgNO 3+Na 2SO 4==Ag 2SO 4↓+2NaNO 3 现象:有白色沉淀生成 补充化学方程式:3Ag+4HNO 3(稀)==3AgNO 3+NO ↑+2H 2O 现象:银逐渐溶解,生成气体遇空气变棕色 Ag+2HNO 3(浓)==AgNO 3+NO 2↑+H 2O 现象:银逐渐溶解,生成棕色气体Cu+2H 2SO 4(浓)==CuSO 4+SO 2↑+2H 2O 现象:铜逐渐溶解,生成有刺激性气味的气体 2FeCl 3+Fe==3FeCl 2 现象:铁粉逐渐溶解,溶液由黄色变成浅绿色2Na2O2(过氧化钠)+2H2O=4NaOH+O2现象:有能使带火星的木条复燃的气体生成1、基本反应类型:化合反应:多变一分解反应:一变多置换反应:一单换一单复分解反应:互换离子2、常见元素的化合价(正价):一价钾钠氢与银,二价钙镁钡与锌,三价金属元素铝;一五七变价氯,二四五氮,硫四六,三五有磷,二四碳;一二铜,二三铁,二四六七锰特别。
初中化学酸碱盐推断练习题

一、文字叙述型推断题1, 某固体混合物可能含有氯化镁、碳酸钙、硫酸铜、碳酸钾和硝酸钠中的一种或几种。
现进行以下实验:(1)将该混合物放入足量水中,得无色透明溶液;(2)向(1)的溶液中加入氢氧化钠溶液无明显现象;(3)在上述(1)的溶液中加入盐酸,有气泡产生。
据上可推断原混合物中肯定有,肯定没有,可能有。
用化学方程式表示上述实验中肯定发生的反应。
2、某固体混合物可能含有氯化钾、碳酸钠、硫酸铜、硫酸钾和硝酸钡。
现进行以下实验:(1)将该混合物放入足量水中,产生白色沉淀,得无色透明溶液;(2)再加入足量的稀硝酸,沉淀全部溶解,逸出无色气体,所得溶液澄清透明;(3)最后加入稀硫酸,又立刻出现白色沉淀。
据上可推断原混合物中肯定有,肯定没有,可能有。
用化学方程式表示上述实验中肯定发生的反应。
3有一包白色混合物,可能含有硫酸铜、硫酸钡、碳酸钠、氯化钙、硝酸钠、氯化钾中的一种或几种,现做如下实验:①将混合物放入足量水中,得到无色透明液体②在上述溶液中加入盐酸,有气泡产生③在完全反应后的②中滴入硝酸银溶液,有白色沉淀生成。
则原混合物中一定有:混合物中一定没有,可能含有。
肯定发生的化学方程式是:(1)(2)4,有一混合气体由HCl、CO、H2、H2O、CO2组成,将其依次通过①足量氢氧化钠溶液,②浓硫酸,③灼热氧化铜后,剩余气体是()A、没有气体剩余B、只有CO2剩余C、只有H2O 剩余D、H2O和CO25,甲乙两车间的废水中含有Na+、Ag+、Cu2+、CO32-、OH-、NO3-六种离子:(1)乙车间的废水呈蓝色,其中的阴离子为_______,如果加入足量的铁可以回收的金属有______;(2)甲车间的废水含有的三种离子是_________;(3)如果将甲乙两车间的废水混合,可以使废水的某些离子转化为沉淀,经过滤后的废水中含有_______;(4)写出检验其中一车间废水中含有OH-的方法。
二、方程式叙述型推断题1:已知A、B、C、D、E、F6种物质的转化关系如下:(1)A+B→C+H2O (2)C+KOH→D↓(蓝色)+E (3)B+D→C+H2O (4)E+BaCl2→F↓(白色,不溶于稀硝酸)+KCl根据上述变化关系,推断有关物质的化学式:A ________;B _______;C _______;D________ ;E __________;F _________。
中考酸碱盐——推断题 偏难

一.填空题(共5小题)1.要鉴别Na2CO3、NaOH、Ba(NO3)2三种无色溶液,可分别滴进一种试液,该试剂可以是_________(写化学式);要鉴别KCl、KOH、BaCl2三种无色溶液,可分别滴进一种试液,该试剂可以是_________(写化学式).2.某澄清溶液由HNO3、K2CO3、H2SO4、CuCl2四种中的两种混合而成.向该溶液中逐滴滴加Ba(OH)2溶液,产生沉淀的质量和加入Ba(OH)2溶液的体积如图.(1)滴加Ba(OH)2溶液开始时无沉淀产生,说明溶液中一定不含_________.(2)该溶液所含溶质是_________和_________.(3)不含另外一种物质的原因是_________.3.有一包固体粉末,可能含有碳酸钠、硫酸钠、硝酸钡、氯化钾和氯化铜中的一种或几种.未确定其组成,进行如下实验:(1)取该固体粉末少量,加足量水,搅拌,静置,得到白色沉淀,上层为无色溶液;(2)过滤,在白色沉淀中加入足量稀硝酸,白色沉淀有一部分溶解,且有无色气体产生.依据上述实验对原固体粉末的判断正确的是_________A.一定含有碳酸钠、硫酸钠、硝酸钡、氯化钾,可能含有氯化铜B.一定含有碳酸钠、硫酸钠、硝酸钡,一定不含氯化铜,可能含有氯化钾C.一定含有碳酸钠、硫酸钠、硝酸钡,可能含有氯化铜;氯化钾D.一定含有碳酸钠、硝酸钡,一定不含硫酸钠、氯化铜,可能含有氯化钾.4.有一包固体,可能由硫酸铜、硝酸钡、碳酸钾、硫酸钾、氯化钠中的一种或几种组成,依次进行如下实验:(1)把该固体溶于水,得白色沉淀,静置后上层溶液呈无色,过滤;(2)向(1)所得沉淀中加入稀硝酸,沉淀不溶解;(3)向(1)所得滤液中加入氯化钡溶液,产生白色沉淀,再加入足量稀硝酸,沉淀不溶解.以上实验,可确定混合物中一定含有_________,一定没有_________,不能确定混合物中是否含有_________;若要检验不能确定的物质是否存在,应向(1)所得滤液中加入的试剂依次是_________、_________、稀硝酸.(4)如果将(2)中的沉淀不溶解改为全部溶解,则混合物中一定含有_________,一定没有_________.5.(2009•广州)A、B、C、D、E五瓶无色透明溶液,分别是HCl溶液、Na2CO3溶液、MgCl2溶液、NaNO3溶液、NaOH溶液中的一种.分别进行下列实验:Ⅰ.将A分别滴入B、C、D、E中,均没有明显现象.Ⅱ.将B分别滴入A、C、D、E中,C、E中均产生白色沉淀,其余没有明显现象.Ⅲ.将C分别滴入A、B、D、E中,B中产生白色沉淀,D中有气泡冒出,其余没有明显现象.(1)A是_________,B是_________,C是_________;(2)B加入E中的化学方程式是_________;(3)C加入D中的化学方程式是_________.二.解答题(共9小题)6.实验室现有四种失去标签的白色固体,分别为无水硫酸铜、硝酸钡、氯化钡、氢氧化纳中的一种.为区分它们进行了下列实验:步骤Ⅰ:将这四种白色固体分别编号为A、B、C、D;步骤Ⅱ:取少量上述四种白色固体样品分别放入四支试管中,加入足量蒸馏水,振荡,固体全部溶解,且C溶液呈蓝色,则C是_________(写化学式,下同);步骤Ⅲ:取少量A、B、D的溶液分别放入三支试管中,向三种溶液中各加入适量C溶液,装有B溶液的试管中产生蓝色沉淀,则B是_________,该反应的化学方程式为_________;装有A溶液和D溶液的试管中均有白色沉淀产生;步骤Ⅳ:为进一步区分A和D,另用两支试管分别取少量A溶液和D溶液,加入适量_________溶液,若装有A溶液的试管中产生白色沉淀,则A是_________.7.现有一种固体混合物,其中可能含有Fe2O3、Fe(OH)3、CaCO3、BaCl2、Cu五种物质中的两种或多种.按下图所示进行实验(设过程中所有可能发生的反应均恰好完全反应).试根据实验过程和发生的现象判断:(1)白色沉淀C是_________(写化学式,下同),产生的气体E是_________.(2)原固体混合物中,一定存在的物质是(写化学式)_________,一定没有的物质是_________.(3)滤液F中,一定存在的溶质有_________.(4)写出过程③中一定或可能发生的化学反应中的一个化学方程式(只能写1个,多写该空不得分):_________.8.有A~F六种无色的液体,已知液体E有咸味,其溶质可作为调味品,其余分别是稀盐酸、碳酸钠溶液、氢氧化钠溶液、氢氧化钙溶液、水中的某一种,请根据下面实验现象回答问题.Ⅰ.将少量A分别滴入适量的B、C、D、F中,均没有明显现象;Ⅱ.将少量B分别滴入适量的A、C、D、F中,C中有气泡出现,其余均没有明显现象;Ⅲ.将少量D分别滴入适量的A、B、C、F中,均没有明显现象.(1)液体E中的溶质是_________.(2)写出B滴入C中发生反应的化学方程式_________.(3)根据实验现象能判断出的液体是_________.(4)将少量C分别滴入适量的A、B、D、F中,写出观察到的现象_________.(5)对还没有确定的液体,下列几种鉴别方法中,正确的是_________(填序号).A.分别滴加稀盐酸B.分别滴加澄清石灰水C.分别滴加紫色石蕊溶液D.分别滴加无色酚酞溶液.9.有一包白色固体粉末,是由碳酸钠、碳酸钙、硝酸钾、硫酸铜、氯化钡中的一种或几种组成.为确定其组成,某化学小组同学进行了如下探究活动:提出假设:白色粉末由上述五种物质组成实验探究:步骤1:取少量粉末放入烧杯中,加足量的水搅拌,得到无色透明溶液步骤2:另取少量粉末放入试管中,滴加足量稀盐酸,观察不到明显现象步骤3:取少量步骤1得到的溶液,加入适量K2SO4溶液和稀HNO3,产生了白色沉淀获得结论:(1)原白色粉末中一定没有_________(填化学式,下同),说明假设不成立.(2)步骤3得到的沉淀是_________.(3)原白色粉末的组成可能是_________.10.有一包白色固体,可能由氯化钠、硫酸铜、氯化钡、硝酸钠、碳酸钠、硫酸钠中的一种或几种组成,进行如下实验:①将粉末溶于水,得到白色沉淀和无色滤液;②过滤,在白色沉淀中加入足量稀硝酸,沉淀一部分消失,并生成气泡;③在滤液中加入硝酸银溶液,生成白色沉淀,加稀硝酸,沉淀不消失.(1)则原固体中一定有_________.(2)一定没有_________.(3)可能有的为_________.(4)②中的反应方程式为_________.11.实验室有一包白色固体,可能含有无水硫酸铜、硫酸钠、碳酸钙、氯化钡、氯化钾中的一种或几种.现做如下实验:a.取少量白色固体加足量的水溶解,过滤得沉淀和无色溶液.b.向所得的沉淀中加入足量的稀硝酸,沉淀有部分溶解,并有气体产生,再过滤,滤液无色.回答下列问题:(1)仅根据第一步实验现象的描述,你认为白色固体中无水硫酸铜_________.(选填“存在”、“不存在”或“不能确定”).(2)根据两步实验的现象,你认为该白色固体中一定不含有的物质是_________,不能确定是否含有的物质是_________,沉淀有部分溶解的化学反应方程式是_________.12.某实验室的废液中,可能含有FeCl3、NaCl、Na2SO4、Ba(NO3)2中的一种或多种.某同学取该废液样品观察为无色溶液,向其中滴加BaCl2溶液产生白色沉淀,继续加稀硝酸无明显现象.根据以上实验现象分析、推断:(1)根据溶液的物理性质就能判断出废液中一定不存在的物质是_________.(2)滴加BaCl2溶液后产生白色沉淀,写出该反应的化学方程式_________.(3)根据你的推理,可知溶液中可能存在的物质是_________.13.(2007•天津)A、B、C、D分别是NaNO3、NaOH、HNO3和Ba(NO3)2四种物质的溶液中的一种.现利用另一种物质X的溶液,用下图所示的方法,即可将它们逐一确定.则A是_________B是_________C是_________D是_________X是_________.14.(2007•青岛)有一包固体粉末,可能含有碳酸钙、硫酸铜、硝酸钾、硫酸钠、氯化钡中的一种或几种.为确定其组成,进行如下实验:(1)取该固体粉末少量加足量水,搅拌,静置,得到白色沉淀,上层为无色溶液;(2)过滤,在白色沉淀中加入足量稀硝酸,白色沉淀不溶解.根据以上实验可推断原固体粉末中不能确定的物质是_________;为确定这包固体粉末的组成,小华取原固体粉末7.00g加足量水充分溶解后过滤,将沉淀洗涤、干燥.称得起质量为4.66g.通过计算后,确定这包固体粉末的组成是_________.。
初三化学酸碱盐推断题训练甄选.

初三化学酸碱盐推断题训练#.酸碱盐推断题训练1.一包固体,可能含有镁粉、碳粉、氧化铜、氢氧化钠、氯化钾中的一种或几种.为探究固体的组成,某化学兴趣小组进行了如图所示实验:请回答下列问题:(1)该实验中生成白色沉淀滤渣乙的化学方程式为;(2)原固体中一定不含有的物质是(写名称或化学式均可,下同),证据是(3)原固体中一定含有的物质是;(4)实验结束后,该兴趣小组将滤液C和滤液D都倒入废液缸,有白色沉淀生成,上层清液E为蓝色,经检验,E中不含氯离子,则E中一定含有的溶质是;2.(7分)有一包白色固体可能含碳酸钠、硫酸钠、氯化钾、硝酸钡、氢氧化钠中的一种或几种。
某化学兴趣小组为探究其成分做了以下实验:Ⅰ.取少量固体于烧杯中,逐渐加水并不断搅拌,烧杯内固体的质量随加入水的质量的变化如图1所示;Ⅱ.取少量B点时的清液于试管中,滴加酚酞溶液,酚酞溶液不变色;Ⅲ.继续向烧杯中滴加稀硝酸并不断搅拌,烧杯内固体的质量随加入稀硝酸的质量的变化如图2所示。
请回答下列问题:(1)BC段可观察到的现象是,从C到D液体的pH (填“增大”、“减小”或“不变”);(2)原白色固体中一定含有,可能含有;(3)D点时,溶液中一定含有的溶质是;(4)为进一步探究该白色固体的成分,该组同学取少量原固体样品于试管中,加足量水溶解,加,过滤;再向滤液中加,观察现象。
3.(6分)某无色溶液可能含有氢氧化钠、氢氧化钙、硫酸钠、氯化钠、碳酸钠中的一种或几种物质。
为探究其组成,某化学兴趣小组的同学进行了如下探究活动。
请根据实验填空。
探究活动一:取适量原无色溶液放入试管中,滴加1—2滴无色酚酞溶液后,将所得溶液分成两份。
(1)向第一份溶液中加入一种物质后,观察现象,得出结论:原溶液中一定含有碳酸钠。
由此可推出:原溶液中一定不含____________________.(写化学式、物质名称皆可,下同)。
(2)向第二份溶液中加入足量另一种物质后,观察现象,得出结论:原溶液中一定含有氢氧化钠。
“酸、碱、盐”性推断题例析.
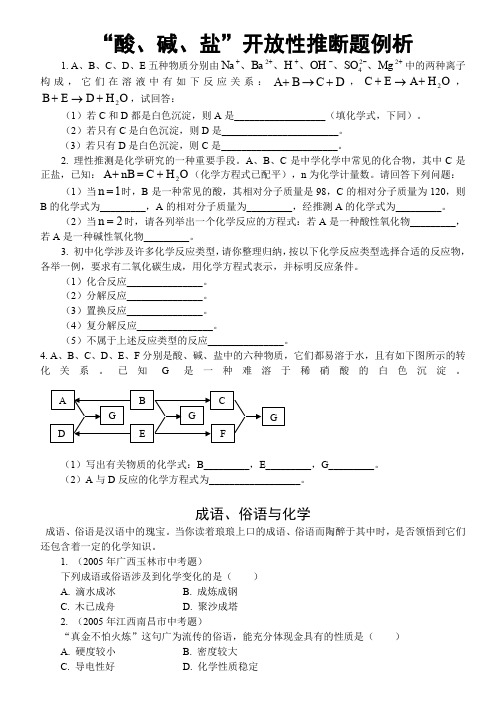
“酸、碱、盐”开放性推断题例析1. A 、B 、C 、D 、E 五种物质分别由+--+++2242Mg SO OH H Ba Na 、、、、、中的两种离子构成,它们在溶液中有如下反应关系:D C B A +→+,O H A E C 2+→+,O H D E B 2+→+,试回答:(1)若C 和D 都是白色沉淀,则A 是__________________(填化学式,下同)。
(2)若只有C 是白色沉淀,则D 是_______________________。
(3)若只有D 是白色沉淀,则C 是_______________________。
2. 理性推测是化学研究的一种重要手段。
A 、B 、C 是中学化学中常见的化合物,其中C 是正盐,已知:O H C nB A 2+=+(化学方程式已配平),n 为化学计量数。
请回答下列问题:(1)当1=n 时,B 是一种常见的酸,其相对分子质量是98,C 的相对分子质量为120,则B 的化学式为_________,A 的相对分子质量为_________,经推测A 的化学式为_________。
(2)当2=n 时,请各列举出一个化学反应的方程式:若A 是一种酸性氧化物_________,若A 是一种碱性氧化物_________。
3. 初中化学涉及许多化学反应类型,请你整理归纳,按以下化学反应类型选择合适的反应物,各举一例,要求有二氧化碳生成,用化学方程式表示,并标明反应条件。
(1)化合反应_______________。
(2)分解反应_______________。
(3)置换反应_______________。
(4)复分解反应_______________。
(5)不属于上述反应类型的反应_______________。
4. A 、B 、C 、D 、E 、F 分别是酸、碱、盐中的六种物质,它们都易溶于水,且有如下图所示的转化关系。
已知G 是一种难溶于稀硝酸的白色沉淀。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
1. A 、 B 、C 、 D 、 E 、F 、 G 为常见的物质,其中 B 、 E 、 G 属于单质,反应②是炼铁工业中的主要反应,下图是它们之间的相互转化关系。
请回答:CY 高温D过量稀盐酸②X 溶液BA①③O 2 加热④ EFG红色固体 浅绿色溶液 无色气体( 1)A 物质的化学式 。
( 2)写出反应②的化学方程式, C 物质固态时的名称 ,该固体物质在实际生活中的一种用途是。
( 3)写出反应③中生成红色固体的化学方程式 。
( 4)上图转化中产生无色气体 G 的原因是,写出物质 G 和 A 在加热条件下反应的化学方程式2.现有初中化学中常见的易溶于水的三种钠盐组成的混合物,将其溶于水后得无色溶液A ,进行如下实验并得到相应结果:试回答下列问题:( 1)无色气体 D 的化学式为,白色沉淀 E 的化学式为,钡盐 B 的化学式为( 2)原混合物中含有的三种易溶于水的钠盐的化学式分别为、、 。
3.为了除去食盐(主要成分为NaCl )样品中含有少量的氯化镁和硫酸钠杂质,某学生根据氯碱工业中精制。
食盐水的基本原理,运用所学知识设计了如下图所示的①至⑤步除杂方案:甲沉①② 淀乙A 过量沉样 水 NaOH 溶液③ 淀 丙溶品过滤沉溶解液B 过量④BaCl 2 溶液淀滤过量过滤C液Na 2 CO 3溶液⑤滤过滤过量液 D 固盐酸滤 体加热蒸发液丁请根据上述除杂方案,回答下列问题:( 1)沉淀甲是 ;滤液 C 中的溶质名称是 ;操作⑤中加入过量盐酸的作用是。
( 2)假设整个操作过程中物质转化无损失, 则固体丁中 NaCl 的质量比原样品中 NaCl 的质量 (填 增大、不变或减小) ;若在操作②中改为加过量的 KOH 溶液,固体丁中可能含有的杂质是 。
4.已知 A 、 B 、C 、 D 四种物质都含有同一种元素,其中 A 是单质, B 是黑色固体, C 是红色固体。
它们之间 存在着如下转化关系: ( 1) A 在不同条件下能够转化成 B 或 C ;( 2) A 和稀硫酸反应有 D 生成;(3)在高温 条件下, B 、 C 分别和无色气体 E 反应,都能生成 A 和另一种无色气体。
根据上述信息,写出下列物质的化学式:A; B;C;D;E。
5.有一种白色固体可能含有:BaCl2、NaCl 、Na2CO3、Na2SO4和 CuSO4中的一种或几种。
对该固体进行如下实验。
①取样,加足量的水,充分搅拌,过滤。
得到白色沉淀 A 和无色溶液B。
②在白色沉淀 A 中加入稀盐酸,沉淀全部溶解,放出能使石灰水变浑浊的无色气体。
③在无色溶液 B 中加入 AgNO3溶液,得到白色沉淀,再加入稀盐酸,白色沉淀不溶解。
请回答下列问题。
(1)原白色固体中一定不含有 _________________ ;一定含有 ______________ 。
...(2)实验①得到的无色溶液 B 中一定含有的溶质是 _______________________ 。
....(3)原白色固体中可能含有 ________________________________________6.某固体可能由Na2SO4、 NaCl 、Na2CO3、 KNO3中的一种或几种组成,现实验如下:试回答:( 1)白色沉淀 A 的化学式为,无色气体 D 的化学式为。
( 2)原固体中一定含有,一定不含有,可能含有。
(3)为检验上述可能含有的物质是否一定存在,某同学又设计了如下实验方案:①取少量固体溶于水,加入足量的Ba(NO3) 2溶液,充分反应后,过滤;②取滤液加入 AgNO3溶液,观察有无白色沉淀生成,由此得出结论。
在上述某同学的实验方案①中,加入足量的Ba(NO3) 2溶液的目的是。
7.某化学试剂厂 A、 B、 C、 D 四个车间排放的废水中,分别含有氢氧化钠、氯化铁、碳酸钠、盐酸中的一种。
在不加试剂的情况下,若控制流量,将它们排放到反应池中,使其恰好完全反应,最后可形成不污染环境的废液排入河流。
已知 B 车间排放的污水显碱性,C车间排放的污水有颜色,反应池 1 中有气泡产生,则 A 车间排放的废水中含有____________, D 车间排放的废水中含有_____________。
反应池 2 中可观察到的现象是 _________________________________________ ,反应的化学方程式为________________ ,最后排入河流的废液中含有的主要物质是______________。
A反应池 1B河C流反应池 2D8.有一包白色固体 A,可能含有FeCl3、CaCO3、NaOH、Ba (OH )2、BaCl2、Na2SO4中的几种,取少量 A 做如下实验,主要现象如图所示。
试用化学式填空:白色B +HNO 3全部溶解沉淀白色+H2 O固体 A无色+CO 2白色沉淀 D溶液 C(1)白色沉淀 B 是 ________________ , D是 ________________________ ;( 2)白色固体 A 中一定不存在的物质是_________________________________ ;( 3)若白色固体 A 中只含两种物质,它们是_________________________________ ;(4)白色固体 A 还有哪些可能的组成:①______________________________②______________________________③______________________________④______________________________9.某化工厂排出的废液中含有AgNO3、Cu(NO3)2和Zn (NO3)2。
为了减少废液对环境的污染,并回收银和铜,某化学小组同学设计了如下方案进行实验:滤液 1:Fe(NO 3) 2废液:Zn(NO 3)2AgNO 3 过量固体 a Cu(NO 3)2 固体乙过滤Zn(NO 3 )2过量溶液 b固体甲过滤滤液 2 过量固体 aFeSO4溶液过滤根据实验推断:(1)固体甲是 ______________________ ;(2)滤液 2 中的溶质是 ________________( 写化学式 ) ;(3) 滤液 2 跟固体 a 反应的化学方程式是_____________________ 。
10.研究小组为了解北京西山的地质情况,从实地选取两块样品D和J,进行如下所示的实验(其中部分反应产物被略去):( 1)样品 D 和 J 的主要成分分别是(用化学式表示)_________、 _________。
( 2)实验室用固体J 制取气体G的化学方程式为___________________________ 。
( 3)上述实验中部分反应的化学方程式J→H: ______________________________________________________ ;F+X→: ______________________________________________________ ;D+E→: ______________________________________________________ ;B+C→: ______________________________________________________ 。
11.有一包固体物质,可能是由H2SO4、CaCO3、Fe(NO3) 3、 Ba(OH)2、NaCl、MgCl2中的一种或几种组成。
为确定其成分,进行如下实验:①取样品放入小烧杯中,加水充分溶解,静置,有白色沉淀。
②再向小烧杯中逐滴加入稀硝酸,开始无现象,后沉淀逐渐溶解,最后沉淀不再减少。
试推断:( 1)这包固体中一定不存在的物质是___________,可能存在的物质是___________ 。
( 2)写出①中发生的反应方程式:______________________________________________________________________________________________________________12.有四家相邻的小化工厂排放的废水中溶质的主要成分如下表:厂名 A 厂 B 厂 C 厂 D 厂废水中溶质的主要成分H 2SO4 Na 2CO3 Ba(OH) 2 CuCl 2为保持环境、防止污染,四厂决定联合处理废水,其处理方案如下:( 1)排气池中发生反应的化学方程式为:____________________________(2)沉淀池中出现的现象是 ______________,化学方程式为 _______________( 3 )若进入混合池中的物质恰好完全反应,经检测合格后排入江河的溶液中的溶质是____________________ (填化学式);( 4)若排气池中 B 厂废水过量,则混合池中发生反应的化学方程式为:_____________________________________________________________13.“三酸两碱”是几种重要的无机化工原料,下图是它们与其他物质间相互转化的关系。
已知:① A、 A1、 A2是工业上常见的三大强酸,B、 B1、 B2是正盐, C、 C1、 C2是碱。
② B2是食盐的主要成分,且 B、 B1、 B2、 C1中含有相同的金属离子。
③ A B CO2, B C 白色沉淀A2 沉淀完全溶解并放出二氧化碳, A C 白色沉淀A2 沉淀不溶解。
请回答:(1)有关物质的化学式:B2 ____________ ,C1 ____________。
(2)有关反应的化学方程式:A B :____________________________________________________________,B C :____________________________________________________________。
( 3)C2可能的化学式(写三个): ____________________________________ 。
14.有 A、B、C、D 四种化合物, A 是硝酸盐, B 是酸, C是碱, D 是含 +3 价元素的氯化物。
以上物质间发生下列反应:①A、 B 的溶液相混,产生不溶于稀硝酸的白色沉淀。
②B、 C 的溶液完全反应后,得到食盐溶液。
③C、 D 的溶液相混,出现红褐色沉淀。
试推断写出A、B、 C、 D的化学式:A : ______________; B: ______________;C : ____________ _ ; D: ______________。
