天然气化工工艺学 第04章 甲醇和二甲醚合成
年产10万吨甲醇合成二甲醚工艺设计

年产10万吨甲醇合成二甲醚工艺设计1. 引言甲醇是一种重要的化工原料,在许多工业领域都有广泛的应用,比如作为燃料、溶剂和合成其他化学品的中间体。
而二甲醚(DME)是一种重要的替代燃料和清洁能源,在汽车和家庭用品等方面具有潜在应用价值。
为了满足市场需求,在本文中,我们将设计一种工艺,以每年产出10万吨的甲醇,并利用甲醇合成二甲醚。
2. 工艺图下图展示了年产10万吨甲醇合成二甲醚的工艺图:工艺图工艺图3. 工艺步骤3.1 甲醇生产首先,我们需要生产甲醇。
这可以通过对天然气进行蒸汽重整反应来实现。
该反应将天然气中的甲烷转化为一氧化碳和氢气。
然后,将一氧化碳和氢气在催化剂的存在下进行合成反应,生成甲醇。
3.2 甲醇净化生产的甲醇需要经过净化步骤,以去除杂质。
这包括使用吸附剂和分离技术,如蒸馏和结晶,将甲醇中的杂质去除,提高甲醇的纯度。
3.3 甲醇合成二甲醚在甲醇净化后,我们将进行甲醇合成二甲醚的反应。
该反应将甲醇与催化剂一起加热,生成二甲醚。
这是一个可逆反应,所以我们需要对反应条件进行控制,以提高二甲醚的产率。
3.4 二甲醚净化生产的二甲醚需要经过净化步骤。
这包括使用分离技术,如蒸馏和结晶,将二甲醚中的杂质去除,提高二甲醚的纯度。
4. 工艺参数为了实现年产10万吨甲醇合成二甲醚的目标,我们需要考虑以下工艺参数:•甲醇生产装置的产能•甲醇净化装置的效率•甲醇合成二甲醚反应的温度和压力•甲醇合成二甲醚反应的催化剂选择和用量•二甲醚净化装置的效率这些参数将直接影响到工艺的效果和产量。
5. 结论通过设计合理的工艺步骤和参数,我们可以实现每年产10万吨甲醇合成二甲醚的目标。
这有望满足市场需求,并为清洁能源领域做出贡献。
然而,需要注意的是,实际生产中可能会受到许多因素的影响,包括原材料供应、设备故障等等。
因此,需要进行全面的工艺设计和风险评估,以确保工艺的可行性和稳定性。
参考文献•Smith, J. M., Van Ness, H. C., & Abbott, M. M. (2005). Introduction to Chemical Engineering Thermodynamics (7th ed.). McGraw-Hill.。
二甲醚生产工艺

二甲醚生产工艺二甲醚是一种无色、无味的液体,化学式为 CH3OCH3,是一种重要的有机化学品。
它具有很高的燃烧热值,被广泛应用于化工领域。
下面我们来介绍一下二甲醚的生产工艺。
目前,二甲醚的主要生产工艺是通过甲醇脱水制备而成。
其具体的生产过程如下:首先,将甲醇加入至醇解器中,然后加入一定量的硫酸作为酸催化剂。
醇解器采用浸没式加热,在适宜的温度下进行反应。
甲醇与硫酸反应生成甲基甲醚,反应方程式为:CH3OH + H2SO4 → CH3OCH3 + H2O其中,甲醇为脱水剂,而硫酸则起催化剂的作用,加快反应速率。
随着反应的进行,甲基甲醚会沉淀形成液相和固相两个分离层。
液相中的甲基甲醚通过分离装置进行分离,然后经过净化处理,去除其中的杂质和有害物质。
固相中的硫酸则需要进行再生利用。
接下来,对液相中的甲基甲醚进行精馏操作,将其中含有的杂质分离出来,以提高二甲醚的纯度。
精馏塔通常采用连续操作,通过控制温度和压力来实现分馏。
分馏过程中,高纯度的二甲醚会在顶部的冷凝器中凝结成液体,然后被收集起来,而杂质则会在底部的渣油中积聚。
最后,经过精馏处理后得到的二甲醚为产品,可以通过灌装或其他方式包装出厂。
产生的废气和废水通过处理设备进行处理,以减少对环境的影响。
二甲醚的生产工艺需要一定的设备和化学药剂的投入,同时也需要进行精确的操作和控制。
在生产过程中,要注意安全生产,避免发生事故和意外,确保工作人员的人身安全。
总结起来,二甲醚的生产工艺主要包括甲醇脱水反应、分离和净化处理、精馏操作等步骤。
通过这些步骤,可以得到高纯度的二甲醚产品。
生产过程中需要考虑资源利用和环境保护等因素,以实现可持续发展。
二甲醚的生产方法有一步法和二步法
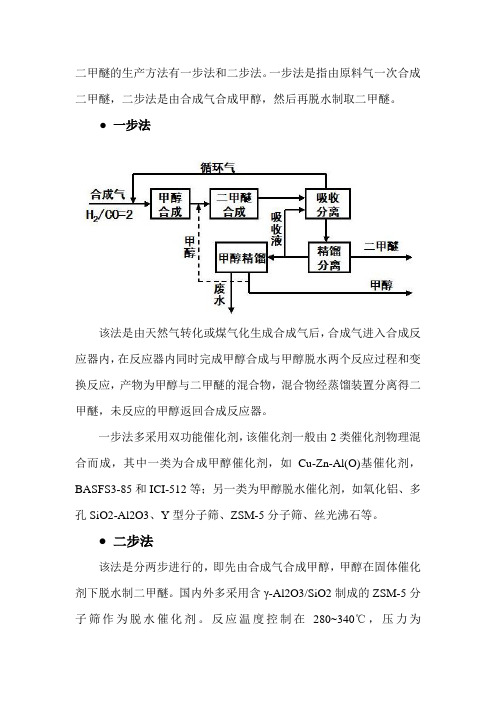
二甲醚的生产方法有一步法和二步法。
一步法是指由原料气一次合成二甲醚,二步法是由合成气合成甲醇,然后再脱水制取二甲醚。
● 一步法该法是由天然气转化或煤气化生成合成气后,合成气进入合成反应器内,在反应器内同时完成甲醇合成与甲醇脱水两个反应过程和变换反应,产物为甲醇与二甲醚的混合物,混合物经蒸馏装置分离得二甲醚,未反应的甲醇返回合成反应器。
一步法多采用双功能催化剂,该催化剂一般由2类催化剂物理混合而成,其中一类为合成甲醇催化剂,如Cu-Zn-Al(O)基催化剂,BASFS3-85和ICI-512等;另一类为甲醇脱水催化剂,如氧化铝、多孔SiO2-Al2O3、Y型分子筛、ZSM-5分子筛、丝光沸石等。
● 二步法该法是分两步进行的,即先由合成气合成甲醇,甲醇在固体催化剂下脱水制二甲醚。
国内外多采用含γ-Al2O3/SiO2制成的ZSM-5分子筛作为脱水催化剂。
反应温度控制在280~340℃,压力为0.5-0.8MPa。
甲醇的单程转化率在70-85%之间,二甲醚的选择性大于98%。
一步法合成二甲醚没有甲醇合成的中间过程,与两步法相比,其工艺流程简单、设备少、投资小、操作费用低,从而使二甲醚生产成本得到降低,经济效益得到提高。
因此,一步法合成二甲醚是国内外开发的热点。
国外开发的有代表性的一步法工艺有:丹麦Topsφe工艺、美国Air Products工艺和日本NKK工艺。
二步法合成二甲醚是目前国内外二甲醚生产的主要工艺,该法以精甲醇为原料,脱水反应副产物少,二甲醚纯度达99.9%,工艺成熟,装置适应性广,后处理简单,可直接建在甲醇生产厂,也可建在其它公用设施好的非甲醇生产厂。
但该法要经过甲醇合成、甲醇精馏、甲醇脱水和二甲醚精馏等工艺,流程较长,因而设备投资较大。
但目前国外公布的大型二甲醚建设项目绝大多数采用两步法工艺技术,说明两步法有较强的综合竞争力。
甲醇制造二甲醚(DME)

甲醇制二甲醚(DME)摘要:综述了二甲醚的性质、用途、生产方法及使用二甲醚时候的注意事项。
关键词:二甲醚化工产品合成气一步法甲醇液相法甲醇气相法一、产品说明1、二甲醚的基本概况二甲醚别名:甲醚英文名称:methyl ether;dimethyl ether;DMECAS编号:115-10-6分子式:C2H6O结构式:CH3—O—CH3二甲醚又称甲醚,简称DME。
二甲醚在常压下是一种无色气体或压缩液体,具有轻微醚香味。
相对密度(20℃)0.666,熔点-141.5℃,沸点-24.9℃,室温下蒸气压约为0.5MPa,与石油液化气(LPG)相似。
溶于水及醇、乙醚、丙酮、氯仿等多种有机溶剂。
易燃,在燃烧时火焰略带光亮,燃烧热(气态)为1455kJ/mol。
常温下DME具有惰性,不易自动氧化,无腐蚀、无致癌性,但在辐射或加热条件下可分解成甲烷、乙烷、甲醛等。
二甲醚是醚的同系物,但与用作麻醉剂的乙醚不一样,毒性极低;能溶解各种化学物质;由于其具有易压缩、冷凝、气化及与许多极性或非极性溶剂互溶特性,广泛用于气雾制品喷射剂、氟利昂替代制冷剂、溶剂等,另外也可用于化学品合成,用途比较广泛。
2 生产原理2.1 生产方法简介目前国内外二甲醚生产方法主要有合成气一步法和甲醇法。
甲醇法又分为甲醇气相法和甲醇液相法。
合成气一步法的工业化技术尚未成熟,理由是: ①现有的技术未经装置检验;②即使按现有技术,其生产成本也高于甲醇气相法2.2 反应方程式甲醇液相法:甲醇脱水反应在液相、常压或微正压、130 ~130 ℃下进行。
其化学反应式如下:2CH3OH =H3COCH3 +H2O甲醇气相法:催化剂为ZSM分子筛、磷酸铝或γ2Al2O3。
甲醇脱水反应的化学反应式如下。
主反应:2CH3OH =H3COCH3 +H2O主要副反应:CH3OH =CO + 2H2H3 COCH3 =CH4 +H2 +COCO +H2O =CO2 +H23 工艺过程及流程图3.1工艺过程甲醇液相法甲醇液相法由硫酸法发展而来,而硫酸法生产二甲醚工艺是硫酸法生产硫酸二甲酯生产流程中的前半段生产工艺。
甲醇气相脱水制二甲醚的基本原理实用PPT文档
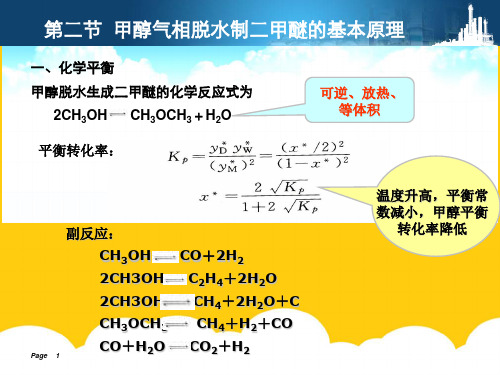
温度升高,平衡常 数减小,甲醇平衡
转化率降低
甲单醇击气此相处脱编水辑制母二版甲标醚题的样基式本原理 二、反应速率
本征动力学
rM=5.50× 1010× e122867RT yM2(1-yD yw/Kp yM2 )
宏观动力学
rM=1.59322× 105× e/RTP23y(1-yD yw/ Kp yM2 )
Page 2
甲醇单气击相此处脱编水辑制母二版甲标醚题样的式基本原理
三、影响甲醇转化率的因素
C2CHH3O31OC.HH3质C量CHH4空+4+2速HH22与O++C甲OC 醇转化率的关系
甲醇脱水生成二甲醚的化学反应式为
2.反应温度与甲醇转化率的关系 2甲2C温2甲二5甲二C甲 5第第甲233C12甲e甲二/CCCC00. . . .HHO醇度醇、醇、醇二二醇醇醇、××HHHH33+R质反反反气 升 气 反 气 反 气节 节 气 气 气 反333OO311TH应应应量OOOO00CCP相高相应相应相 相相相应2112HHHHHH温压压空甲甲O脱,脱速脱速脱 脱脱脱速00333度力力速××醇醇y水平水率水率水 水水水率(ee与与与与气气1衡制制制制 制制制CC11CCC-甲甲甲甲相相2222常二二二二 二二二CCHHOHH22y醇醇醇醇脱脱HH442数甲甲甲甲 甲甲甲88D44+ +44+66转转转转水水++醚减醚醚醚 醚醚醚y++7722H化化化化制制w22RR的小的的的 的的的HHHH2HH/TT率率率率二二2222基,基基基 基基基22OO++K的的的的甲甲OO本甲本本本 本本本p+ +CC关关关关醚醚原醇原原原 原原原yOOCC系系系系的的M理平理理理 理理理2基基衡)本本转原原化理理率降低
单第击二此处节编甲辑母醇版气标相题脱样水式制二甲醚的基本原理
甲醇制二甲醚

甲醇制二甲醚的生产工艺及催化剂的研究摘要:二甲醚应用广泛,主要用于气雾剂、溶剂和燃料。
作为氟里昂的替代产品,对大气臭氧层没有破坏,还可作为冷冻剂、萃取剂等。
可作为民用燃料代替天然气、液化石油气、人工煤气。
作为车用燃料可以解决我国石油紧张和汽车尾气排放带来的环境污染问题。
二甲醚碳烟排放和微粒排放几乎为零,没有加速烟尘,一氧化碳和醛类有害物质排放都低于世界上最严格的美国加州排放标准。
以至于甲醇制二甲醚的生产工艺及催化剂的研究成为了工业发展的要求。
关键词:甲醇二甲醚气相脱水法催化剂目前,世界上主要有4个致力于研究二甲醚特性及应用的组织,分别是国际二甲醚协会(IDA)、日本二甲醚论坛(JDF)、韩国二甲醚论坛(KDF)、中国二甲醚协会(CDA)。
2006年,日本二甲醚论坛首度发行了二甲醚使用手册,详细介绍了二甲醚的相关知识和发展历程。
2010年9月2日,国家质量监督检验检疫总局、国家标准化管理委员会联合批准发布国家标准GB 25035—2010《城镇燃气用二甲醚》,并自2011年7月1日起实施。
该标准严格规定了二甲醚的质量,使得二甲醚的应用有章可循。
国家标准《液化二甲醚气瓶》、国家标准《液化二甲醚气瓶阀》、国家标准《家用二甲醚燃气灶具》、行业标准《耐二甲醚密封材料》、行业标准《瓶装液化二甲醚调压器》等也正在编制中。
相关标准规范的不断完善,对推广二甲醚作为城镇燃气发挥了重要作用。
[1]1 生产工艺研究甲醇气相脱水法,是目前国内外使用最多的生产二甲醚工业方法,化学反应如下:主要副反应:2CH3OH=H3COCH3+H2OCH3OH=CO+2H2H 3COCH3=CH4+H2+COCO+H2O=CO2+H22CH3OH=C2H6+2H2O主要生产工艺过程为:甲醇经气化与反应器出来的反应产物换热后,进入二甲醚反应器进行气相催化脱水反应,反应产物经换热后,用循环水冷却冷凝。
反应条件为 0.5~1.8MPa、230℃~400℃,催化剂为 ZSM分子筛、磷酸铝或γ-Al2O3,冷却冷凝后的物料进行气液分离,气相送洗涤塔用甲醇或甲醇-水溶液吸收回收二甲醚,液相的粗二甲醚送精馏系统分离。
1.《天然气化工工艺学》习题、指导与训练2016.10.09讲解

1. 《天然气化工工艺学》习题、指导与训练要求:① 考核范围:系统掌握利用教材、讲义核心内容;② 注重训练:独立完成和理解本作业与训练-1,注重理解,提高解决实际问题的能力; ③ 公平竞争:考核结果取决于你自己的努力; ④ 教师关注:考核质量和及格率两大问题! ⑤ F = A*30% + B*70% + C* 0%)总结与训练-1 §1.0 天然气的组成与性质1. 天然气是由多种可燃和不可燃的气体组成的混合气体, 其中烃类气体主要成分为CH 4,其次为C 2H 6、C 3H 8等;非烃类气体通常为CO 2、CO 、N 2、H 2、H 2S 、H 2O 及微量惰性气体He 、Ar 等。
2. 1m 3(mol )天然气完全燃烧所放出的热量称为天然气的体积(摩尔)热值,可燃气热值分类:高热值(水蒸气冷却为冷凝水状态)和低热值(水蒸气为蒸汽状态) 。
3. 可燃物摩尔高热值与摩尔低热值的关系为蒸发焓)(22OH O H Hn LHV HHV ∆⋅+= 4. 甲烷、乙烷、丙烷的低热值(LHV) LHV(CH 4) > LHV (C 2H 6) > LHV(C 3H 8)。
5. 计算天然气的爆炸极限为5-15 v%。
其含义为若低于5 v%或者高于15 v%,则会因为天然气在空气中的含量不足或者过剩而不会发生爆炸。
6. CH 3OH 的爆炸极限为5.5% ~ 44 v% (6% ~ 36.5%)。
7. C 3+烃小于100mL(l)/m 3 (g)的天然气俗称贫气;而C 3+烃大于100mL(l)/m 3 (g)天然气俗称富气。
8. C 5+烃小于10mL(l)/m 3 (g)的天然气俗称干气;而C 5+烃小于10mL(l)/m 3 (g)的天然气俗称湿气。
§2 天然气净化1. 天然气中的硫化物主要是以H 2S 的形式存在,同时还可能有一些有机硫化物,如硫醇和硫醚等。
2.天然气脱硫工艺主要采用是醇胺法和砜胺法,其中醇胺法属于化学溶剂法,而砜胺法为主的化学-物理溶剂法。
天然气化工工艺学 第04章 甲醇和二甲醚合成

《天然气化工工艺学》第4章
甲醇的性质
③ 甲醇与硝酸作用生成硝酸甲酯
CH3OH HNO3 CH3 NO3 H2O
(4.1.10)
(5) 甲醇氯化
CH3OH Cl2 H2 CH3Cl HCl H2O
《天然气化工工艺学》第4章
4.1.3 甲醇合成反应热力学
表4.1 不同温度压力下CO合成甲醇的平衡常数值
温度 /℃ 200 250 300 350 400 450 500 压 力 /atm 50 3.780×10-2 3.075×10-3 3.938×10-4 6.759×10-5 1.482×10-5 4.003×10-6 1.282×10-6 100 6.043×10-2 4.516×10-3 5.235×10-4 8.342×10-5 1.758×10-5 4.657×10-6 1.470×10-6 150 9.293×10-2 6.416×10-3 6.907×10-4 1.013×10-4 2.019×10-5 5.205×10-6 1.593×10-6 200 1.230×10-1 8.578×10-3 8.778×10-4 1.202×10-4 2.324×10-5 5.655×10-6 1.742×10-6 250 1.617×10-1 1.072×10-2 1.026×10-3 1.387×10-4 2.539×10-5 6.630×10-6 1.952×10-6 300 2.023×10-1 1.297×10-2 1.211×10-3 1.586×10-4 2.905×10-5 7.025×10-6 2.072×10-6
y CO y H2O y CO2 y H2
气相催化法甲醇脱水合成二甲醚的工艺和催化剂研究

第36卷第1期四川大学学报(工程科学版)V ol.36N o.1 2004年1月JOURNA L OF SICH UAN UNIVERSITY(E NG INEERING SCIE NCE E DITION)Jan.2004文章编号:100923087(2004)0120028204气相催化法甲醇脱水合成二甲醚的工艺和催化剂研究慈志敏1,储 伟13,戴晓雁1,谢在库2,陈庆龄2(1.四川大学化学工程学院,四川成都610065;2.中石化上海石油化工研究院,上海201208)摘 要:采用气相催化法以甲醇为原料合成二甲醚,为了筛选并制备高活性催化剂以使二甲醚具有高收率,研究了硅钛、硅铝和改性氧化铝系列固体酸催化剂的制备条件、反应温度、液体空速和反应时间等因素对甲醇转化率和二甲醚选择性的影响。
结果表明,以改性氧化铝作催化剂为最佳,并在常压、300℃、甲醇液体空速为8ml/(g.h)时,转化率和选择性分别可达92.5%和98.0%。
该气相催化法工艺比液相法具有明显的优势。
关键词:二甲醚合成;甲醇脱水;气相催化法;催化剂中图分类号:T Q203.2文献标识码:AC atalysts and Process for the G as2phase Synthesis of DMEby the Dehydration of MethanolCI Zhi2min1,CHU Wei13,DAI Xiao2yan1,XIE Zai2ku2,CHEN Qing2ling2(1.School of Chem.Eng.,S ichuan Univ.,Chengdu610065,China;2.Shanghai Research Inst.of Petrochemical T echnology,Shanghai201208,China)Abstract:DME was synthesized by the gas2phase catalytic dehydration of methanol.In order to select or prepare the cata2 lysts with high activity for getting a high yield rate of DME,three kinds of catalysts,SiO2-T iO2/S O42-,SiO2-T iO2/ Fe3+and SiO2-Al2O3,were investigated,including their preparation conditions,reaction tem peratures and times,and liquid space2velocities.The results show that with the m odified alumina as catalyst and under the conditions of normal pressure,tem perature of300℃and the methanol liquid space2velocity of8ml/(g・h),the methanol conversion and DME selectivity were92.5%and98.0%,respectively,indicating that the gas2phase catalytic process is obviously supe2 rior to the liquid2phase process.K ey w ords:DME synthesis;methanol dehydration;gas2phase catalysis;catalyst 二甲醚(DME)在常温下是一种无色、无味、低毒、化学稳定、水溶性良好的气体。
CO2加氢制备甲醇、二甲醚的研究

CO2加氢制备甲醇、二甲醚的研究摘要:CO2催化加氢合成甲醇、二甲醚是解决CO2减排的有效途径之一,具有环保、经济等意义.本文从新的视角综述了CO2催化加?浜铣杉状肌⒍?甲醚催化剂的研究进展和研究特点,并从催化剂的制备方法、沉淀剂的选择、焙烧时间、催化剂载体、助剂等方面进行了系统综述.关键词:CO2;甲醇;二甲醚;催化剂;前言:现代工业的发展使CO2排放量急骤增加,由此引发的环境问题也日益得到人们的重视,因此研究CO2的利用具有重要意义。
利用CO2加氢合成二甲醚是一项很有意义的工作。
二甲醚是重要的有机中间体[1],在有机合成、制药、轻工等行业有着广泛用途。
同时二甲醚也可以作为代替汽油的清洁燃料[2]。
所以说CO2催化加氢转化为二甲醚的研究具有重大的工业价值并兼有化工、能源、环保等多重意义。
二氧化碳是主要的温室气体之一,对温室效应有着重要的影响。
随着工业的不断发展,化石燃料的消费猛增,空气中的二氧化碳含量日益增加,严重破坏了人类的生存环境,二氧化碳的综合利用已成为迫切需要进行的研究。
二甲醚是重要的有机化工品,既是许多化工产品的重要原料,也是化石燃料的理想替代品。
不论从经济还是从环境的角度出发,通过二氧化碳加氢合成二甲醚都是对二氧化碳回收利用的有效途径。
目前制备二甲醚主要采用甲醇催化脱水法或混合气直接合成法。
一:合成催化剂的研究对CO2直接加氢合成二甲醚催化剂的研究,目前国内主要集中于南京工业大学、天津大学、华东理工大学、四川大学、江苏石油化工学院和长岭炼化有限责任公司催化剂厂等。
其研究主要内容在于催化剂中各组分含量的配比、催化剂的改性、助剂的添加、脱水催化剂的选择及不同催化剂制备方法对催化剂活性的影响。
二、原理分析二氧化碳加氢合成二甲醚经过近十多年的发展,虽在催化剂材料选择和合成条件方面取得一定的成果,但未达到工业化程度,需进行进一步研究。
按溴丙烷和三正丙胺摩尔比1∶1,采用冷凝回流法制备溴化四正丙基胺(TPAB),考察了反应温度、反应时间以及溶剂对产率和干燥温度对TPAB变质的影响。
三相浆态床中合成甲醇与二甲醚

二、气液固三相浆态床中甲醇合成
在70年代,美国化学系统公司提出液相法甲醇合 成的概念,开发了三相床甲醇合成工艺。研究工作 主要在实验室进行,包括液相介质选择、催化剂评 价、合成气在液相介质中的溶解度以及合成气组成 对过程的影响等。 80年代,美国能源部资助,由美国空气产品和化 学品公司主持,在该公司的德克萨斯州拉波特 (Laporte)联合企业建立了日产5吨甲醇的浆态床中试 系统。此后,便投入了大量的人力、物力、财力开 展了操作运转、经济评价、概念设计等方面的工作, 将此研究命名为LPMEOH。
C、三相床中甲醇合成宏观动力学
研究了三相床中适用于富 CO 合成气的宏观动力 学模型;三相床甲醇合成过程因液相的存在所产生 的传递阻力影响;获得了 C302 催化剂合成动力学 方程;为合成条件的确定、三相床甲醇合成过程的 数学模拟和工程分析,以及热模试验方案的确定, 提供了依据。
(3相合成气制甲醇和二甲醚的三相床反应器原 料气适应性强,反应物主要组分CO可在大范围内变化, 可用副产蒸汽量的大小来调节,床层仍可维持恒温在 设定的较佳温度。而这对于气-固相催化法是不可能 的。
2.4 操作的可塑性 ●优良的传热性能与合理的产汽配置 ●极低的床层压降
操作气速 ( 或质量空速 ) 可在较大范围内变化而反 应器内仍能正常稳定操作。这是气-固相催化法不可 能的; 主要取决于起始流化速度与床层节涌速度; 与分布器的类型、设计参数和反应器的结构设计 有关。
含氧燃料指用煤与天然气制得合成气 (CO+H2),再以合 成气为原料,在较低温度压力下,催化合成烃类燃料油、甲
醇、二甲醚和其他含氧化合物的过程,整个过程中从外界引
入了氧。 由合成气合成烃类燃料油,只是部分的利用了煤中的C和 H ,另一部分 C 和 H 被氧转化成了 CO2 和 H2O ;而合成含氧燃 料,充分利用了合成气中的氧,为原子经济型反应。
二甲醚生产工艺概述毕业设计甲醇合成

二甲醚生产工艺概述来源:中国化工信息网 2008年7月23日二甲醚,又称甲醚、氧二甲,是一种无色可燃气体,可压缩液化。
它在传统上用途可作为气雾剂的推进剂,也可广泛用作化工原料,在精细化学晶的合成、制药、燃料、农药化学工业中有许多独特的用途,但这些领域的用量均非常有限,使二甲醚在一个较长的时期内没有大规模的工业化生产。
随着国际石油价格的不断攀升,以及大规模低成本二甲醚生产工艺的日趋成熟,二甲醚作为新型能源的替代优势日趋明显,其在民用燃料和替代柴油方面的优势使其有越来越广阔的发展空间,许多企业看好二甲醚巨大的市场潜力和良好的发展前景,纷纷投资建设二甲醚生产装置。
依托国内丰富的煤炭资源和众多的甲醇生产企业,目前已经有数十家二甲醚生产企业,而且规划和在建的企业也很多,二甲醚的生产工艺主要有一步法、两步法以及联产法。
1 一步法一步法也称直接合成法,它以H2、CO和CO2为原料,直接在反应器里生成二甲醚,其主要反应过程如下:CO+222=CH3OH2CH3OH=CH3OCH3+H2OCO+H2O=H3+CO2将上述反应过程合并,则总反应方程式为:3H2+3CO=CH3OCH3+CO2根据反应移热方式不同,一步法生产技术又可分为气相法和液相法。
1.1 气相法气相一步法合成二甲醚在固定床反应器中进行,国内外均有相关单位从事过这一工艺的研发,有代表型性的技术有丹麦托普索公司的TI-GAS法、日本三菱重工业公司与COSMO石油公司联合开发的ASMTG法、浙江大学以及大连化学物理所等。
不同工艺主要技术特点见表1。
进行时,反应热不易移出,因此存在传热性能差、温度控制难、时空产率低等缺点,并在低转化率和高空速的情况下操作,未反应的合成气大量循环,因而无法解决工程放大问题,目前还没有工业化装置投产。
1.2 液相法针对气相一步法合成二甲醚的固定床反应器传热能力差,无法将反应热及时移出,温度控制困难等问题,国内外相关研究单位都开发了浆态床一步法合成二甲醚的工艺,使用的是甲醇合成和甲醇脱水复合催化剂。
甲醇及二甲醚的生产
且会导致羰基有铁利聚于集移在走催反化应剂热上,,防引止起催催化化剂剂过失热
活。故一般采。用但氢空过速量太。高.转化率降低,循环气
量增加,作费用增加。空速过小,则
空气速度及气体的循环 不能满足生产任务要求。
2021/3/1
11
联醇生产是在10.O~13.OMPa压力下,采用铜基 催化剂,串联在合成氨工艺中,用合成原料气中的CO 、C02、H2合成甲醇。
2021/3/1
15
《煤炭气化工艺》
第二节 甲醇合成及其应用
联醇生产工艺流程
2021/3/1
16
《煤炭气化工艺》
第二节 甲醇合成及其应用
联醇生产工艺条件
反应压力:综合考虑工艺和设备要求,一般中、 小型氮肥厂都采用3MPa压力。
副反应:
CH3CH2OH CO CH3CH2COOH CO H2O CO2 H2
2021/3/1
23
《煤炭气化工艺》
第四节 醋酸的生产
高压羰基和成法制醋酸工艺流程
2021/3/1
24
《煤炭气化工艺》
第四节 醋酸的生产
Monsanto低压法羰基2)精制工段, (3)轻组分回收工段
《煤炭气化工艺》
第二节 甲醇合成及其应用
三、甲醇生产方法
高压法
高压法是在压力为30MPa,温度为300~ 400℃下使用锌铬催化剂合成甲醇
浆态床工艺
低压法
液相法
液相络合催化法
气相法
中压法
中压法是在低压法基础上开发的在5~ 10MPa压力下合成甲醇的方法,其工艺流程 如图8-5所示
2021/3/1
年产20万吨甲醇合成二甲醚的工艺设计

年产20万吨甲醇合成二甲醚的工艺设计The Process Design of 200000t/a Dimethyl Ether Preparedby Methanol目录摘要 (I)Abstract (II)引言 (1)第1章文献综述 (2)1.1 二甲醚概况 (2)1.1.1 二甲醚的发展状况 (2)1.1.2 二甲醚的传统领域的应用及其拓展 (2)1.2 国内二甲醚市场简况 (4)1.2.1 现状 (4)1.2.2 国内市场预测 (6)1.3 国外二甲醚市场简况 (7)1.3.1 现状 (7)1.3.2 国外市场预测 (9)1.4 原料说明 (10)1.4.1 物理性质 (10)1.4.2 化学性质 (11)1.5 二甲醚的性质 (11)1.5.1 化学性质 (11)1.5.2 物理性质 (12)1.5.3 DME的毒性 (12)第2章工艺流程介绍 (13)2.1生产方法简述 (13)2.1.1 甲醇脱水制二甲醚 (13)2.1.2 合成气直接合成二甲醚 (14)2.2 工艺流程说明 (15)2.2.1 原料甲醇 (16)2.2.2 反应 (16)2.2.3 合成气冷却 (16)2.2.4 二甲醚精馏 (16)2.2.5 甲醇塔和二甲醚精馏塔 (17)2.3生产工艺特点 (17)2.4主要工艺指标 (18)2.4.1 二甲醚产品指标 (18)2.4.2 催化剂的使用 (18)第3章塔设备计算及选型 (19)3.1 汽化塔及其附属设备的计算选型 (19)3.1.1 物料衡算 (19)3.1.2 热量衡算 (21)3.1.3 理论板数、塔径、填料选择及填料层高度的计算 (25)3.1.4 汽化塔附属设备的选型计算 (31)3.2 合成塔物料衡算 (32)3.3 精馏塔及其附属设备的计算选型 (32)3.3.1 物料衡算 (33)3.3.2 热量衡算 (34)3.3.3 附属设备的选型计算 (36)3.3.4 理论塔板数的计算 (37)3.3.5 精馏塔主要尺寸的设计计算 (37)3.3.6 塔径设计计算 (39)3.3.7 填料层高度的计算 (41)3.3.8 填料塔液体分布装置 (42)3.3.9填料塔壁厚的计算 (42)结论 (44)致谢 ....................................................................................... 错误!未定义书签。
二甲醚生产工艺流程

合成气制二甲醚工艺目前合成气合成二甲醚的生产工艺主要有两步法和一步法两种,两步法是经过甲醇合成和甲醇脱水两步过程得到DME,一步法是合成气直接生产DME,新开发的工艺有二氧化碳加氢合成二甲醚和生物质间接液化制取二甲醚。
1、两步法制二甲醚两步法制二甲醚是以合成气为原料由低压法制得甲醇后,甲醇再经脱水制得DME,其主要过程如图1所示:图1两步法合成二甲醚流程简图其中甲醇脱水制二甲醚的方法又包括液相甲醇脱水法和气相甲醇脱水法液相甲醇脱水是将甲醇与浓硫酸混合加热使甲醇脱水得到二甲醚,浓硫酸起到催化剂的作用该工艺具有反应温度低,原料转化率和二甲醚的选择性高的优点,但是产品后处理比较困难,而且浓硫酸的存在使设备腐蚀严重,并且产生大量的废液,带来很大的环境污染,限制了此工艺的发展"目前国内仅有武汉硫酸厂和山东久泰化工科技有限公司开发此工艺。
在液相脱水制DME基础上,为了避免液体酸作为甲醇脱水剂时产生的设备腐蚀问题,美孚公司和意大利的ESSO公司开发了以固体酸为催化剂的甲醇气相脱水技术,气相甲醇脱水法的基本原理是将甲醇蒸汽通过固体酸催化剂脱水生成二甲醚,目前常用的催化剂主要有沸石、氧化铝、二氧化硅/氧化铝、阳离子交换树脂等,由于甲醇脱水反应是放热反应,因此维持适宜的反应温浙江大学博士学位论文合成气合成二甲醚和乙二醇研究综述度是气相甲醇脱水法的关键,两步法制二甲醚的反应条件温和,副反应少,二甲醚的选择性和产品的纯度高,但是由于需要从合成气开始生产甲醇,导致合成气的转化率低,生产流程长,并且需要经过甲醇分离精制过程,使得整个工艺的成本增加,即使购买成品甲醇直接脱水制得二甲醚,也容易受到甲醇价格的影响,而使成本难以控制。
2、一步法制二甲醚合成气直接制二甲醚被称为“一步法”,一步法合成二甲醚由甲醇合成和甲醇脱水两个过程组成,同时还存在水汽变换反应,由于受到热力学的限制,甲醇合成反应的单程转化率一般较低,而由合成气一步法合成二甲醚,采用具有合成甲醇和甲醇脱水两种功能的复合催化剂,由于催化剂的协同效应,反应系统内各个反应相互祸合,生成的甲醇不断转化为二甲醚,合成甲醇不再受热力学的限制,与传统的经甲醇合成和甲醇脱水两步得到DME两步法,相比,一步法具有流程短、操作压力低、设备规模小、单程转化率高等优点,经济上更加合理,但缺点在于二甲醚的选择性低,产物的纯度不高。
液相甲醇合成二甲醚工艺流程

液相甲醇合成二甲醚工艺流程作者/来源:日期:2008-4-181、甲醇罐区原料甲醇由甲醇罐区用泵经管道送至生产区甲醇储槽贮存,然后由甲醇输送泵经流量计计量后送往二甲醚反应工序作为反应物料。
2、二甲醚反应由甲醇计量泵计量后经反应预热器加热至60℃左右后,由二甲醚反应釜底部进入温度为150℃左右的液相催化剂中,在催化剂的作用下脱水生成二甲醚。
该反应为微放热反应,为保证反应的连续进行,需用加热泵循环打酸,混酸在釜外的反应加热器中与低压蒸汽间接换热获得热量。
从反应釜顶部出来的气体为二甲醚、水蒸汽和少部分甲醇混合气,温度150℃左右,气体经过甲醇冷凝器降温至55℃,气液混合物进入净化槽中进行气液分离。
气相二甲醚经过甲醇冷凝器进一步冷凝,其中含有甲醇,进入分离槽再进行气液分离,净化槽中的甲醇、二甲醚水溶液(二甲醚为溶解其中)同时也溢流至分离槽。
在分离槽中气相二甲醚送往二甲醚压缩工段,液相的甲醇水溶液则由塔前甲醇泵送往精馏塔,并经塔前预热器预热到60℃左右。
在精馏塔塔底重沸器中,甲醇、二甲醚水溶液在低压蒸汽的加热下变为气相进入精馏塔中,经过逐段分离,甲醇、二甲醚气体由塔顶进入塔顶冷凝器中,甲醇冷凝为液体进入液封槽,二甲醚气体则由液封槽顶部并入二甲醚管道送往二甲醚压缩工段。
甲醇液体由回流泵加压后一部分经计量后送到塔顶作回流液,其余部分由甲醇冷却器冷却至38℃左右循环送至甲醇中间槽进一步反应。
塔底的残液通过液位调节排至废水槽,经废水泵排入污水系统。
反应式为:CH3OH+H2SO4—→CH3HSO4+H2OCH3OH+H3PO4—→CH3H2PO4+H2OCH3OH+ CH3HSO4—→CH3OCH3+H2SO4CH3OH +CH3H2PO4—→CH3OCH3+H3PO4反应温度控制在135-155℃左右,甲醇单程转化率约88%左右。
其具体工艺流程见附图。
3、二甲醚压缩工段从二甲醚反应工段来的二甲醚气体先进入二甲醚冷却器降温至-10℃左右,然后进入二甲醚气液分离器分离出少量的甲醇残液,残液溢流至甲醇回流槽,由回流泵送至二甲醚反应工段的分离槽中进行精馏回收。
ASPEN化工设计课程作业甲醇生产二甲醚

目录1绪论 (3)2综述 (4)2.1设计条件 (4)2.2设计产品发展现状、性能及用途 (5)2.3两步法二甲醚合成工艺 (5)3工艺流程模拟设计 (7)3.1工艺方案选择及论证 (7)3.2模拟流程图 (8)3.3模块模拟说明 (9)3.4工艺物料流程图 (21)3.5带控制点的工艺流程图 (21)4物料衡算 (22)4.1人工计算 (22)4.2与ASPEN软件计算比较 (23)5能量衡算 (25)5.1已知条件 (25)5.2计算公式 (25)5.3入塔热量计算 (25)5.4塔内反应热的计算 (25)5.5出塔气各气体组分焓 (26)5.6全塔热损失 (26)5.7沸腾水吸收热量 (27)5.8热量衡算表 (27)6气体和液体输送设备的设计与选型 (28)6.1概况 (28)6.2选型参数确定 (28)6.3泵性能的核算 (29)7换热器的设计 (31)7.1换热器的选择原则 (31)7.2介质流程 (31)7.3温度 (31)7.4传热面积的估算 (32)7.5换热器结构尺寸计算 (33)7.6初选换热器 (35)7.7热流量核算 (35)7.8压力损失核算 (37)8塔设备的设计与选型 (39)8.1塔设备的选择原则 (39)8.2精馏塔的选择 (39)8.3部分衡算 (40)8.4塔主要工艺尺寸计算 (42)8.5塔板主要工艺尺寸的计算 (44)8.6塔板布置 (45)8.7塔板的流体力学核算 (46)8.8辅助设备计算 (49)8.9其他塔设备计算 (51)9反应器的设计与选型 (53)9.1反应器设计要求 (53)9.2反应器的选择 (53)9.3二甲醚生产物料平衡计算 (54)9.4热量衡算 (55)9.5反应器体积 (56)9.7反应器参数设计 (61)10二甲醚分离工段设备布置图 (61)11二甲醚分离工段管道布置图 (62)11.1管道设计的一般原则 (62)11.2常用设备管路布置 (62)11.3管道布置图的绘制 (64)12工艺成本估算及经济分析报告 (65)12.1固定资本 (65)12.2产品生产成本估算 (67)13工厂选址及总布置设计 (70)13.1厂址选择 (70)13.2总平面布置图 (72)13.3总平面布置说明 (72)参考文献 (73)二甲醚又称甲醚、木醚氧、二甲,是最简单的脂肪醚重要的甲醇下游产品之一。
甲醇制造二甲醚(DME)

甲醇制二甲醚(DME)摘要:综述了二甲醚的性质、用途、生产方法及使用二甲醚时候的注意事项。
关键词:二甲醚化工产品合成气一步法甲醇液相法甲醇气相法一、产品说明1、二甲醚的基本概况二甲醚别名:甲醚英文名称:methyl ether;dimethyl ether;DMECAS编号:115-10-6分子式:C2H6O结构式:CH3—O—CH3二甲醚又称甲醚,简称DME。
二甲醚在常压下是一种无色气体或压缩液体,具有轻微醚香味。
相对密度(20℃)0.666,熔点-141.5℃,沸点-24.9℃,室温下蒸气压约为0.5MPa,与石油液化气(LPG)相似。
溶于水及醇、乙醚、丙酮、氯仿等多种有机溶剂。
易燃,在燃烧时火焰略带光亮,燃烧热(气态)为1455kJ/mol。
常温下DME具有惰性,不易自动氧化,无腐蚀、无致癌性,但在辐射或加热条件下可分解成甲烷、乙烷、甲醛等。
二甲醚是醚的同系物,但与用作麻醉剂的乙醚不一样,毒性极低;能溶解各种化学物质;由于其具有易压缩、冷凝、气化及与许多极性或非极性溶剂互溶特性,广泛用于气雾制品喷射剂、氟利昂替代制冷剂、溶剂等,另外也可用于化学品合成,用途比较广泛。
2 生产原理2.1 生产方法简介目前国内外二甲醚生产方法主要有合成气一步法和甲醇法。
甲醇法又分为甲醇气相法和甲醇液相法。
合成气一步法的工业化技术尚未成熟,理由是: ①现有的技术未经装置检验;②即使按现有技术,其生产成本也高于甲醇气相法2.2 反应方程式甲醇液相法:甲醇脱水反应在液相、常压或微正压、130 ~130 ℃下进行。
其化学反应式如下:2CH3OH =H3COCH3 +H2O甲醇气相法:催化剂为ZSM分子筛、磷酸铝或γ2Al2O3。
甲醇脱水反应的化学反应式如下。
主反应:2CH3OH =H3COCH3 +H2O主要副反应:CH3OH =CO + 2H2H3 COCH3 =CH4 +H2 +COCO +H2O =CO2 +H23 工艺过程及流程图3.1工艺过程甲醇液相法甲醇液相法由硫酸法发展而来,而硫酸法生产二甲醚工艺是硫酸法生产硫酸二甲酯生产流程中的前半段生产工艺。
天然气转化合成甲醇的工艺完整版

天然气转化合成甲醇的工艺HEN system office room 【HEN16H-HENS2AHENS8Q8-HENH1688】天然气转化合成甲醇的工艺综述2015-6-24专业:化工12-3班学号:学生姓名:**指导教师:**天然气转化合成甲醇的工艺一.前言20世纪60年代,石油和天然气作为一次能源与煤炭一起成为主要能源。
与此同时,以石油和天然气为原料的化学工业也迅猛发展起来。
与石油不同的是,天然气的成分主要是低分子量的烷烃。
因此,天然气化工在发展中逐步成为一个体系。
天然气是储量十分丰富的资源和能源,同时也是主要的温室气体之一,合理地利用天然气不仅关系到未来的资源配置和能源利用,而且也是可持续发展的重要战略发展方向之一。
天然气可以合成多种化工原料产品,比如生产合成氨还有甲醇,其中甲醇是最重要的。
甲醇是一种重要的基础化工产品和化工原料,主要用于生产甲醛。
醋酸、甲苯胺、氯甲烷、乙二醇及各种酸的酯类和维尼纶等,并在很多工业部门中广泛用作溶剂。
甲醇在气田开发中用作防冻剂,添在汽油中可提高汽油的辛烷值,甲醇还可直接用作燃料用于发动机。
目前工业上几乎都是采用一氧化碳、二氧化碳加压催化氢化法合成甲醇。
典型的流程包括原料气制造、原料气净化、甲醇合成、粗甲醇精馏等工序。
天然气、石脑油、重油、煤及其加工产品(焦炭、焦炉煤气)、乙炔尾气等均可作为生产甲醇合成气的原料。
天然气与石脑油的蒸气转化需在结构复杂造价很高的转化炉中进行。
由天然气制合成气进而合成甲醇是制甲醇产品一条重要的工艺路线。
二.主体部分1.天然气合成甲醇的原理天然气转化合成气中的CO 或2CO 与2H 在一定温度、压力和催化剂作用下反应生成甲醇。
其主反应为:OH CH H CO 322⇔+ (1)O H OH CH H CO 23223+⇔+ (2)主要副反应有:O H OCH CH H CO 233242+⇔+ (3)O H CH H CO 2423+⇔+ (4)O H OH H C H CO 2942384+⇔+ (5)O H CO H CO 222+⇔+ (8)甲醇的合成反应是减分子放热反应,由化学热力学原理可知,增加压力、降低温度、减少反应气流中的惰性气体浓度均有利于甲醇的生成。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
(4.1.6)
① 甲醇与甲酸反应生成甲酸甲酯
CH 3OH HCOOH HCOOCH 3 H2O
(4.1.7)
② 甲醇与硫酸作用生成硫酸氢甲酯、硫酸二甲酯
CH 3OH H2SO4 CH 3HSO 4 H2O
(4.1.8)
2CH 3OH H2SO4 (CH 3 )2SO 4 2H2O
(4.1.9)
表4.1 不同温度压力下CO合成甲醇的平衡常数值
温度
压 力 /atm
/℃
50
100
150
200
250
300
200 3.780×10-2 6.043×10-2 9.293×10-2 1.230×10-1 1.617×10-1 2.023×10-1 250 3.075×10-3 4.516×10-3 6.416×10-3 8.578×10-3 1.072×10-2 1.297×10-2 300 3.938×10-4 5.235×10-4 6.907×10-4 8.778×10-4 1.026×10-3 1.211×10-3 350 6.759×10-5 8.342×10-5 1.013×10-4 1.202×10-4 1.387×10-4 1.586×10-4 400 1.482×10-5 1.758×10-5 2.019×10-5 2.324×10-5 2.539×10-5 2.905×10-5 450 4.003×10-6 4.657×10-6 5.205×10-6 5.655×10-6 6.630×10-6 7.025×10-6 500 1.282×10-6 1.470×10-6 1.593×10-6 1.742×10-6 1.952×10-6 2.072×10-6
(4.1.23)
(2) CO2 3H2 CH3OH (g) H2O(g) r H (2) 49.5kJ mol (4.1.24)
(3) CO2 H2 CO H2O(g) r H (3) 41.2kJ mol
(4.1.25)
r H (1) r H (2) r H (3)
合成甲醇属于体积减小的放热反应,从反应平衡角度, 低温和高压均有利于甲醇生成。副产物有烃、醇、醛、醚、 酸和酯等化合物。
《天然气化工工艺学》第4章
4.1.3 甲醇合成反应热力学
这三个反应中,只有两个是独立的,上述三个反应的平
衡常数KP
p2 H2
1 p2
yCH 3OH
yCO
y2 H2
(4.1.33)
Kp2
pCH3OH pH2O pCO2 p3H2
1 p2
yCH3OH yH2o
具有醇类的典型反应;因含有甲基,所以又能进行甲基 化反应。
《天然气化工工艺学》第4章
4.1.1 甲醇的性质
(1)甲醇氧化制甲醛,进一步氧化制甲酸。制甲醛条件, 温度600~700℃,催化剂:沸石银、铜、五氧化二钒
CH 3OH 0.5O2 HCHO H2O
(4.1.1)
HCHO 1/ 2O2 HCOOH
(4.1.5)
《天然气化工工艺学》第4章
甲醇的性质
(3) 甲醇羰基化。甲醇与一氧化碳250℃、50~70MPa 条件下,通过碘化钴催化剂,或者在180℃、3~4MPa件 下,通过铑的羰基化合物催化剂,以碘甲烷为助催化剂,
合成醋酸。
CH 3OH CO CH 3COOH
(4) 甲醇酯化,生成各种酯类化合物。
(4.1.2)
(2)甲醇氨化,制甲胺。甲醇与氨混合,在370~420℃、 5.0~20.0MPa条件下,以活性氧化铝为催化剂
CH 3OH NH3 CH 3NH 2 H2O
(4.1.3)
2CH 3OH NH3 (CH 3)2 NH 2H2O
(4.1.4)
3CH 3OH NH 3 (CH 3 )3 N 3H2O
《天然气化工工艺学》第4章
甲醇的性质
③ 甲醇与硝酸作用生成硝酸甲酯
CH 3OH HNO 3 CH 3NO3 H2O
(4.1.10)
(5) 甲醇氯化
CH 3OH Cl 2 H2 CH 3Cl HCl H2O CH 3Cl Cl 2 CH 2Cl 2 HCl
CH 3Cl 2 Cl 2 CHCl 3 HCl
4 甲醇/DME及其衍生物
4.1 甲醇合成 4.2 醋酸 4.3 碳酸二甲酯 4.4 二甲醚合成
• 甲醇制二甲醚 • 合成气直接制二甲醚
《天然气化工工艺学》第4章
4.1 甲 醇
分子式CH3OH,相对分子质量32.04,常压沸点64.7℃, 常温常压下是无色透明、略带乙醇香味的挥发性液体。甲醇 与水互溶,在汽油中有较大溶解度。甲醇有毒,易燃烧,爆 炸极限为6.0~36.5% (体积分数)。
(4.1.16)
(4.1.17) (4.1.18) (4.1.19)
(4.1.20) (4.1.21)
《天然气化工工艺学》第4章
4.1.2 甲醇合成反应原理
在一定温度、压力下,CO、CO2和H2在固相铜催化剂 上进行反应可合成甲醇,主要化学反应为:
(1) CO 2H2 CH3OH (g) r H (1) 90.8kJ mol
(8) 甲醇与苯反应生成甲苯
CH 3OH C6H6 C6H5CH 3 H2O
(9) 与光气反应
CH 3OH COCl 2 CH 3OCOCl HCl
CH 3OH CH 3OCOCl (CH 3O)2 CO HCl
(10) 甲醇与二硫化碳反应 ,再与硝酸反应
4CH 3OH CS2 2(CH 3)2S CO 2 2H2O 3(CH3)2 S 2HNO3 3(CH3)2 SO 2NO H2O
yCO 2
y3 H2
(4.1.34)
K p3
pCO pH2O pCO2 pH2
yCO yH2O yCO2 yH2
(4.1.35)
K p1 K p2 K p3
(4.1.36)
式中,pi为i组分的分压,atm;yi为i组分的体积分率;p
为反应体系的总压,atm。
《天然气化工工艺学》第4章
4.1.3 甲醇合成反应热力学
CH 3Cl 3 Cl 2 CCl 4 HCl
(6) 甲醇与氢氧化钠反应
CH 3OH NaOH CH 3ONa H2O
(4.1.11) (4.1.12) (4.1.13) (4.1.14)
(4.1.15)
《天然气化工工艺学》第4章
甲醇的性质
(7) 甲醇的脱水
2CH 3OH (CH 3)2 O H2O
