苯_乙醇_水混合液的分离提纯.
苯甲酸的分离提纯方法

苯甲酸的分离提纯方法苯甲酸是一种常用的有机酸,广泛应用于医药、染料、香料等领域。
然而,在实际应用中,苯甲酸的纯度往往不够高,需要进行分离提纯。
下面将介绍两种常用的分离提纯方法:结晶法和萃取法。
1. 结晶法结晶法是一种常用的分离提纯方法,适用于苯甲酸的固体样品。
其基本原理是利用物质在溶液中的溶解度随温度的变化而产生的结晶现象,将杂质与苯甲酸分离。
将苯甲酸样品加入适量的溶剂中,通常选择水或乙醇作为溶剂。
然后加热溶液,使苯甲酸完全溶解。
接着,慢慢降低溶液温度,使其逐渐冷却。
在适当的温度下,苯甲酸会开始结晶,杂质会留在溶液中。
最后,通过过滤或离心,将结晶的苯甲酸分离出来,并用冷溶剂洗涤,以去除残留的杂质。
最终,将苯甲酸在低温下干燥,得到纯净的苯甲酸晶体。
2. 萃取法萃取法是一种常用的液相分离提纯方法,适用于苯甲酸的液体样品。
其基本原理是利用不同溶剂对苯甲酸和杂质的不同溶解度,实现分离提纯。
将苯甲酸样品与适当的溶剂混合,搅拌均匀。
通常选择具有较高溶解度的有机溶剂,如乙酸乙酯或二氯甲烷。
然后,将混合溶液放置一段时间,使苯甲酸和杂质在两种溶剂中分配达到平衡。
接着,将两相分离,并收集有机相。
为了提高分离效果,可以进行多次萃取。
每次萃取后,将有机相收集起来,并与新鲜的溶剂进行下一轮的萃取。
通过多次萃取,可以逐渐提高苯甲酸的纯度。
将收集到的有机相进行蒸发,去除溶剂,得到纯净的苯甲酸。
以上就是苯甲酸的两种常用分离提纯方法:结晶法和萃取法。
根据实际情况,选择合适的方法进行分离提纯,可以得到高纯度的苯甲酸,满足不同领域的需求。
广东实验中学2022-2023学年高二下学期期中考试化学试题含答案

广东实验中学2022—2023学年高二下学期期中考试化学本试卷分选择题和非选择题两部分,共8页,满分100分,考试用时75分钟。
注意事项:1.答卷前,考生务必用黑色字迹的钢笔或签字笔将自己的姓名、考号填写在答题卷上。
2.选择题每小题选出答案后,用2B铅笔把答题卷上对应题目的答案标号涂黑;如需改动,用橡皮擦干净后,再选涂其它答案;不能答在试卷上。
3.非选择题必须用黑色字迹的钢笔或签字笔作答,答案必须写在答题卷各题目指定区域内的相应位置上;如需改动,先划掉原来的答案,然后再写上新的答案;不准使用铅笔和涂改液.不按以上要求作答的答案无效。
4.考生必须保持答题卡的整洁,考试结束后,将答题卷收回。
可能用到的相对原子质量H 1 C 12 N 14 O 16 Na 23 Mg 24 Al 27 Si 28 S 32 Cl 35.5 Fe 56 Cu 64 Ni 59第Ⅰ卷(选择题共44分)一、选择题:本题共16小题,共44分。
第1~10小题每小题2分,第11~16题每小题4分。
在每小题给出的四个选项中,只有一项符合题目要求。
1.下列化学用语或图示表达不正确的是( )A.基态氮原子的轨道表示式:B.顺式聚异戊二烯的结构简式:C.CaC2的电子式:D.基态24Cr的简化电子排布式:[Ar]3d44s22.下列有机物的系统命名正确的一组是( )A.CH2Br﹣CH2Br二溴乙烷B.1,3,4﹣三甲苯C.2,2,3−三甲基戊烷D.2﹣甲基﹣1,3﹣二丁烯3.下列有关芳香烃的叙述中,错误的是( )A.苯与浓硝酸、浓硫酸共热可反应生成硝基苯B.苯乙烯在合适条件下催化加氢可生成C.乙苯可被酸性高锰酸钾溶液氧化为(苯甲酸)D.甲苯与氯气在光照下发生一元取代反应,主要生成4.设N A为阿伏加德罗常数的值,下列说法不正确的是( )A.lmol SiO2晶体含有共价键数目为4N AB.12g金刚石中含有的晶胞数目为N A/8C.标准状况下,22.4LCH2Cl2中C—Cl键的数目为2N AD.28g乙烯和环己烷(C6H12)的混合物中含有碳原子数为2N A5.下列各项比较中前者高于(或大于或强于)后者的是( )A.戊醇和乙醇在水中的溶解度B.CH3CH2CH2COOH的酸性和CH3COOH的酸性C.SO2Cl2分子中的Cl﹣S﹣Cl键角和SO2F2分子中的F﹣S﹣F键角D.邻羟基苯甲醛()的沸点和对羟基苯甲醛()的沸点6.用下列装置进行实验,能达到实验目的的是( )证明乙炔可使溴水褪色制备溴苯并验证有HBr产生萃取振荡时放气7.下列关于有机化合物的说法错误的是( )A.正己烷和2,2﹣二甲基丁烷互为同系物B.中共平面的原子数目最多为15个C.正丁烷的沸点比异丁烷的高,乙醇的沸点比二甲醚的高D.甲苯能使酸性高锰酸钾溶液褪色,而烷烃则不能,说明苯环活化了甲基8. 下列由实验得出的结论正确的是( ) 9. 下列关于有机物的说法不正确的是( ) A .2-丁烯分子存在顺反异构B .有机物()的一氯代物有4种C .抗坏血酸分子()中有2个手性碳原子D .有机物()与氢气1∶1加成后的产物只有一种10. 溴苯可用于生产镇痛解热药和止咳药,其制备、纯化流程如图。
分离提纯方法

分离提纯方法分离提纯方法是化学领域中非常重要的一个环节,它涉及到从混合物中提取出纯净的物质,以便进行进一步的分析和应用。
在实际操作中,我们常常会遇到各种各样的混合物,而要想得到我们需要的单一物质,就需要借助于各种分离提纯方法。
本文将介绍几种常见的分离提纯方法,希望对大家有所帮助。
首先,最常见的分离提纯方法之一就是蒸馏。
蒸馏是利用混合物中各成分的沸点差异来进行分离的方法。
在蒸馏过程中,混合物被加热至其中一个成分的沸点,这个成分会转化为气体,然后通过冷凝器冷却成液体,从而分离出目标物质。
蒸馏方法适用于液体混合物的分离提纯,常用于酒精、水等液体的提纯过程。
其次,结晶是另一种常见的分离提纯方法。
结晶是通过溶解度的差异来分离混合物中的成分。
当溶解度较大的成分溶解在溶剂中,而溶解度较小的成分无法完全溶解时,就可以通过结晶的方式将溶解度较小的成分从溶液中分离出来。
结晶方法适用于固体混合物的分离提纯,常用于盐类、糖类等固体物质的提纯过程。
另外,萃取也是一种常用的分离提纯方法。
萃取是利用溶剂对混合物中成分的选择性溶解性来进行分离的方法。
通过与混合物中的目标成分有较高的亲和力,从而将目标成分从混合物中提取出来。
萃取方法适用于液-液或固-液混合物的分离提纯,常用于天然产物的提取和化学反应物的分离过程。
最后,色谱技术也是一种非常重要的分离提纯方法。
色谱技术是利用不同成分在固定相和移动相之间的分配系数差异来进行分离的方法。
通过在固定相上的吸附和移动相的流动,不同成分会以不同的速度通过色谱柱,从而实现分离。
色谱技术适用于各种复杂混合物的分离提纯,常用于化学分析和药物研发领域。
总之,分离提纯方法在化学领域中具有非常重要的意义,它们为我们提供了丰富的手段来从复杂的混合物中分离出纯净的物质。
不同的分离提纯方法各具特点,可以根据具体情况选择合适的方法来进行操作。
希望本文介绍的几种常见的分离提纯方法对大家有所帮助,也希望大家在实际操作中能够根据需要灵活运用,取得理想的分离提纯效果。
液体有机化合物的分离和提纯
2-5 液体有机化合物的分离和提纯在生产和实验中,经常会遇到两种以上组分的均相分离问题。
例如某物料经过化学反应以后,产生一个既有生成物又有反应物及副产物的液体混合物。
为了得到纯的生成物,若反应后的混合物是均相的,时常采用蒸馏(或精馏)的方法将它们分离。
一、简单蒸馏通过简单蒸馏可以将两种或两种以上挥发度不同的液体分离,这两种液体的沸点应相差30℃以上。
1. 简单蒸馏原理液体混合物之所以能用蒸馏的方法加以分离,是因为组成混合液的各组分具有不同的挥发度。
例如,在常压下苯的沸点为80.1℃,而甲苯的沸点为110.6℃。
若将苯和甲苯的混合液在蒸馏瓶内加热至沸腾,溶液部分被汽化。
此时,溶液上方蒸气的组成与液相的组成不同,沸点低的苯在蒸气相中的含量增多,而在液相中的含量减少。
因而,若部分汽化的蒸气全部冷凝,就得到易挥发组分含量比蒸馏瓶内残留溶液中所含易挥发组分含量高的冷凝液,从而达到分离的目的。
同样,若将混合蒸气部分冷凝,正如部分汽化一样,则蒸气中易挥发组分增多。
这里强调的是部分汽化和部分冷凝,若将混合液或混合蒸气全部冷凝或全部汽化,则不言而喻,所得到的混合蒸气或混合液的组成不变。
综上所述,蒸馏就是将液体混合物加热至沸腾,使液体汽化,然后,蒸气通过冷凝变为液体,使液体混合物分离的过程,从而达到提纯的目的。
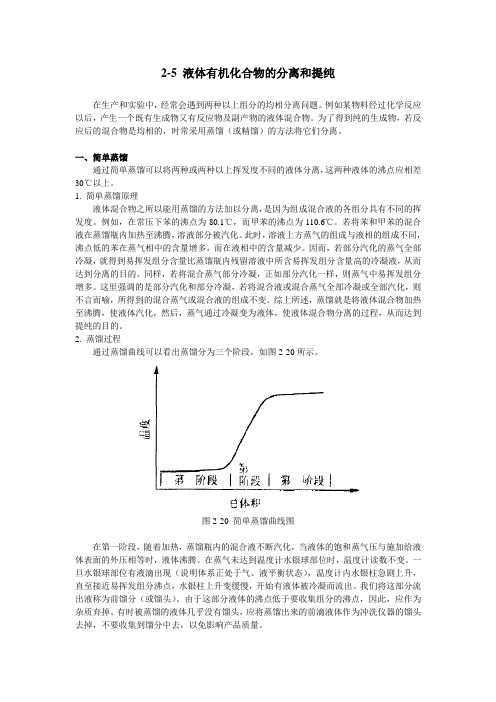
2. 蒸馏过程通过蒸馏曲线可以看出蒸馏分为三个阶段,如图2-20所示。
图2-20 简单蒸馏曲线图在第一阶段,随着加热,蒸馏瓶内的混合液不断汽化,当液体的饱和蒸气压与施加给液体表面的外压相等时,液体沸腾。
在蒸气未达到温度计水银球部位时,温度计读数不变。
一旦水银球部位有液滴出现(说明体系正处于气、液平衡状态),温度计内水银柱急剧上升,直至接近易挥发组分沸点,水银柱上升变缓慢,开始有液体被冷凝而流出。
我们将这部分流出液称为前馏分(或馏头)。
由于这部分液体的沸点低于要收集组分的沸点,因此,应作为杂质弃掉。
有时被蒸馏的液体几乎没有馏头,应将蒸馏出来的前滴液体作为冲洗仪器的馏头去掉,不要收集到馏分中去,以免影响产品质量。
苯甲酸的分离提纯方法

苯甲酸的分离提纯方法苯甲酸是一种常见的有机化合物,广泛应用于医药、染料、香料等领域。
在实验室中,对苯甲酸进行分离和提纯是常见的操作。
本文将介绍苯甲酸的分离提纯方法。
我们可以通过普通的提纯方法,如结晶法、萃取法等,对苯甲酸进行初步的分离。
其中,结晶法是一种常用且简便的方法。
首先将苯甲酸溶解在适量的溶剂中,如水或有机溶剂,然后加热溶液至溶解温度,使苯甲酸完全溶解。
随后,慢慢冷却溶液,苯甲酸会逐渐结晶出来。
最后,将生成的苯甲酸晶体用冷溶剂洗涤并过滤,即可得到相对纯净的苯甲酸。
除了结晶法,萃取法也是一种常用的分离提纯方法。
在萃取法中,我们可以选择适当的溶剂来萃取苯甲酸。
通常,苯甲酸具有较好的溶解性,可以选择无水乙醇、乙醚等有机溶剂进行萃取。
首先将苯甲酸与溶剂充分混合,然后分层,将有机相收集。
接着,用饱和氯化钠溶液洗涤有机相,去除杂质。
最后,用旋转蒸发仪将溶剂蒸发,得到纯净的苯甲酸。
我们还可以利用色谱技术进行苯甲酸的分离和提纯。
色谱是一种基于物质在固定相和流动相中分配系数差异而进行分离的方法。
对于苯甲酸的分离,可以选择合适的固定相和流动相,如硅胶、活性炭等固定相,甲醇、水等流动相。
将混合物溶解在流动相中,通过色谱柱,利用分配差异使苯甲酸与其他组分分离开来。
最后,用旋转蒸发仪将流动相蒸发,得到纯净的苯甲酸。
还可以通过亚氨基钼酸法对苯甲酸进行分离和提纯。
亚氨基钼酸法是一种常用的重金属离子分离的方法,也适用于苯甲酸的提纯。
首先将苯甲酸溶解于水中,加入亚氨基钼酸钠溶液,生成沉淀。
然后,通过过滤或离心的方式将沉淀收集。
最后,用水洗涤沉淀,去除杂质,即可得到纯净的苯甲酸。
苯甲酸的分离提纯方法有结晶法、萃取法、色谱技术和亚氨基钼酸法等。
在实际操作中,我们可以根据具体情况选择合适的方法进行分离提纯,以获得纯净的苯甲酸。
这些方法不仅可以应用于实验室中,也可以在工业生产中得到推广和应用。
简述水提醇沉法的操作要点

简述水提醇沉法的操作要点
水提醇沉法是一种常用的分离和提纯化合物的方法,它基于醇类物质在水中溶解度较高的特点。
在操作过程中,需要注意以下几个要点。
要选择合适的溶剂。
水提醇沉法主要利用水和醇的亲和性差异进行分离,因此需要选用适合的醇类溶剂。
常用的溶剂有乙醇、丙醇、异丙醇等,根据不同的化合物特性选择合适的醇类溶剂。
需要控制溶剂的浓度。
在水提醇沉法中,溶剂的浓度对分离效果有很大影响。
一般情况下,溶剂的浓度越高,分离效果越好。
但是过高的浓度会增加操作难度,因此需要根据实际情况选择适当的浓度。
接下来是溶剂的加入和混合。
在操作过程中,需要将溶剂逐渐加入待分离的混合物中,并进行充分的混合。
混合的方式可以是搅拌、摇晃或超声波处理等,目的是使混合物中的化合物充分溶解。
然后是等待分离。
在混合物中加入溶剂后,需要给予足够的时间让不同化合物在溶剂中分离。
这个过程一般需要一定的时间,可以通过观察溶液的透明度变化或者使用离心机加速分离。
最后是分离产物的收集。
分离完成后,需要将溶液中的上层液体(富含醇类溶剂)和下层液体(含有较少醇类溶剂)分别收集。
可以使用分液漏斗或离心机等工具进行分离,注意保持收集容器的清洁和干燥。
总结一下,水提醇沉法的操作要点包括选择合适的溶剂、控制溶剂的浓度、充分混合混合物、等待分离、分离产物的收集。
这些要点能够帮助我们有效地进行水提醇沉法的操作,实现对化合物的分离和提纯。
有机物分离和提纯的常用方法

有机物分离和提纯的常用方法分离和提纯有机物的一般原则是:根据混合物中各成分的化学性质和物理性质的差异进行化学和物理处理,以达到处理和提纯的目的,其中化学处理往往是为物理处理作准备,最后均要用物理方法进行分离和提纯.下面将有机物分离和提纯的常用方法总结如下:分离、提纯的方法目的主要仪器实例分液分离、提纯互不相溶的液体混合物分液漏斗分离硝基苯与水蒸馏分离、提纯沸点相差较大的混合溶液蒸馏烧瓶、冷凝管、接收器分离乙醛与乙醇洗气分离、提纯气体混合物洗气装置除去甲烷中的乙烯过滤分离不溶性的固体和液体过滤器分离硬脂酸与氯化钠渗析除去胶体中的小分子、离子半透膜、烧杯除去淀粉中的氯化钠、葡萄糖盐析胶体的分离��分离硬脂酸钠和甘油上述方法中,最常用的是分液(萃取)、蒸馏和洗气。
最常用的仪器是分液漏斗、蒸馏烧瓶和洗气瓶。
其方法和操作简述如下:1. 分液法��常用于两种均不溶于水或一种溶于水,而另一种不溶于水的有机物的分离和提纯。
步骤如下:分液前所加试剂必须与其中一种有机物反应生成溶于水的物质或溶解其中一种有机物,使其分层。
如分离溴乙烷与乙醇(一种溶于水,另一种不溶于水):又如分离苯和苯酚:2. 蒸馏法��适用于均溶于水或均不溶于水的几种液态有机混合物的分离和提纯.步骤为:蒸馏前所加化学试剂必须与其中部分有机物反应生成难挥发的化合物,且本身也难挥发。
如分离乙酸和乙醇(均溶于水):3。
洗气法�;�适用于气体混合物的分离提纯.步骤为:例如:此外,蛋白质的提纯和分离,用渗析法;肥皂与甘油的分离,用盐析法。
有机物分离和提纯的常用方法 1,洗气 2,萃取分液溴苯(Br2),硝基苯(NO2),苯(苯酚),乙酸乙酯(乙酸) 3, a,制无水酒精:加新制生石灰蒸馏 b,酒精(羧酸)加新制生石灰(或NaOH固体)蒸馏 c,乙醚中混有乙醇:加Na,蒸馏 d,液态烃:分馏 4,渗析 a,蛋白质中含有Na2SO4 b,淀粉中KI 5,升华奈(NaCl)鉴别有机物的常用试剂所谓鉴别,就是根据给定的两种或两种以上的被检物质的性质,用物理方法或化学方法,通过必要的化学实验,根据产生的不同现象,把它们一一区别开来.有机物的鉴别主要是利用官能团的特征反应进行鉴别.鉴别有机物常用的试剂及特征反应有以下几种:1. 水适用于不溶于水,且密度不同的有机物的鉴别.例如:苯与硝基苯.2。
乙醇和水的分离实验报告

乙醇-水精馏实验报告实验名称:共沸精馏实验人员:同组人:实验地点:实验时间:班级/学号:指导教师:实验成绩:共沸精馏一、实验目的1. 通过实验加深对共沸精馏过程的理解2. 熟悉精馏设备的构造掌握精馏操作方法3. 能够对精馏过程做全塔物料衡算4. 学会使用气相色谱分析气、液两相组成。
二、实验原理精馏是利用不同组份在气-液两相间的分配,通过多次气液两相间的传质和传热来达到分离的目的。
对于不同的分离对象,精馏方法也会有所差异。
例如分离乙醇和水的二元物系。
由于乙醇和水可以形成共沸物而且常压下的共沸温度和乙醇的沸点温度极为相近。
所以采用普通精馏方法只能得到乙醇和水的混合物。
而无法得到无水乙醇。
为此,在乙醇-水系统中加入第三种物质,该物质被称为共沸剂。
共沸剂具有能和被分离系统中的一种或几种物质形成最低共沸物的特性。
在精馏过程中共沸剂将以共沸物的形式从塔顶蒸出,塔釜则得到无水乙醇。
这种方法就称作共沸精馏。
乙醇-水系统加入共沸剂苯以后可以形成四种共沸物。
现将它们在常压下的共沸温度、共沸组成列于表1。
为了便于比较再将乙醇、水、苯三种纯物质常压下的沸点列于表2。
从表1和表2列出沸点看除乙醇-水二元共沸物的共沸物与乙醇沸点相近之外其余三种共沸物的沸点与乙醇沸点均有10℃左右的温度差。
因此,可以设法使水和苯以共沸物的方式从塔顶分离出来,塔釜则得到无水乙醇。
整个精馏过程可以用图1来说明。
图中A、B、W分别为乙醇、苯和水的英文字头,ABZ,AWZ,BWZ代表三个二元共沸物,T表示三元共沸物。
图中的曲线为25℃下的乙醇、水、苯三元共沸物的溶解度曲线。
该曲线的下方为两相区上方为均相区。
图中标出的三元共沸组成点T是处在两相区内。
以T为中心连接三种纯物质A、B、W及三个二元共沸点组成点ABZ、AWZ、BWZ将该图分为六个小三角形。
如果原料液的组成点落在某个小三角形内。
当塔顶采用混相回流时精馏的最终结果只能得到这个小三角形三个顶点所代表的物质。
分离提纯方法归纳.

【方法突破1】
获得溶解度随温度变化不大的单一热稳定性好的溶质
(如从NaCl溶液中获得NaCl)——操作方法:蒸发结晶 (蒸发至大部分晶体析出即停止加热)。 蒸发结晶
NaCl溶液
NaCl固体
二、蒸发浓缩、冷却(降温)结晶
如下图所示,是氯化钠和硝酸钾固体的溶解度曲线, 硝酸钾符合大多数物质溶解度变化的普遍规律,随温度 升高,溶解度显著增大(也有个别反常的,溶解度随温 度升高而减小的如:Ca(OH)2、Li2CO3等),也即是一 条陡峭的曲线。 现在如果只有KNO3水溶液,如何可以得到KNO3晶体? 是否也是和NaCl的处理方法相同呢? 结合溶解度曲线可知,操作方法不相同,因 为其溶解度随温度升高而增大,温度较高温 下情况下析出晶体少,因而KNO3只需要蒸 发浓缩(使其在较高温度下达到饱和——此 时会出现结晶膜),再冷却(降温)结晶就 会析出大量的晶体(曲线越陡峭,晶体的析 出率越高,KNO3通过降温结晶析出率高达 90%以上),而不必蒸发结晶(那样会加热 时间更久,浪费更多燃料和时间)。这种考 查方式比较常见。
考点分析
近5年广东高考化学试题在化工流程题中有关 物质的分离提纯考查结晶、过滤问题有4年考过。
分别是:
2009年第22题制备氯酸镁考查蒸发浓缩、趁热过滤、 冷却结晶、过滤; 2010年第32题制备Li2CO3考查蒸发浓缩、趁热过滤; 2012年第32题由“呆矿”制备K2SO4考查蒸发浓缩、 冷却结晶、第33题苯甲酸提纯考查重结晶; 2013年第32题CuSO4溶液制备胆矾考查蒸发浓缩、 冷却结晶),
考情分析
本内容是学生错误率较高考点,归结其原因 是不少同学初中溶解度这一块的知识就没学好, 碰到一些具体问题就缺乏分析能力 。
本节课我们就从各地高考模拟题中进行了相关总结, 对蒸发结晶,蒸发浓缩、冷却结晶,蒸发浓缩(结晶)、 趁热过滤等做系统的分析和比较,以期能够顺利突破这 一高频考点和难点内容。
2019-2020学年高一化学新人教版必修第二册单元练习卷:第七章有机化合物.

第七章有机化合物1.下列反应属于取代反应的组合是()A.①②B.③④C.①③D.②④解析:选D①是加成反应,②是酯化反应,属于取代反应,③是氧化反应,④是取代反应,②、④符合题意。
2.下列关于①苯、②乙醇、③乙酸、④葡萄糖等有机物的叙述中,不正确的是() A.可以用新制氢氧化铜鉴别③与④B.只有③能与金属钠反应C.①、②、③均能发生取代反应D.一定条件下,④可以转化为②解析:选B A项,乙酸与Cu(OH)2发生中和反应,葡萄糖与新制Cu(OH)2悬浊液在加热条件下生成砖红色沉淀;B项,2Na+2CH3COOH―→2CH3COONa+H2↑,2CH3CH2OH +2Na―→2CH3CH2ONa+H2↑,葡萄糖分子中含—OH,也能和金属钠发生反应;C项,苯的硝化、乙醇和乙酸的酯化均属于取代反应;D项,葡萄糖发酵生成乙醇。
3.下列有机物中,既能发生酯化反应,又能被新制Cu(OH)2悬浊液氧化的物质是() A.CH2CH—CHOB.CH3CH2COOHC.CH2CH—COOCH3D.CH2OH(CHOH)4CHO解析:选D A项中没有羟基或羧基,不能发生酯化反应;B项中只有羧基,只能发生酯化反应;C项中没有羟基或羧基,所以不能发生酯化反应,也不能与新制氢氧化铜悬浊液反应;D项为葡萄糖,既能被新制氢氧化铜悬浊液氧化,又能发生酯化反应。
4.下列表示物质结构的化学用语或模型正确的是()A.丙烯的结构简式:CH2CHCH3B.甲烷分子的空间充填模型:C.羟基的电子式:D.葡萄糖的最简式:C6H12O6解析:选B丙烯的结构简式为CH2CHCH3,A项错误;羟基的电子式为,C 项错误;葡萄糖的最简式为CH2O,D项错误。
5.下列生活用品中主要由合成纤维制造的是()A.尼龙绳B.宣纸C.羊绒衫D.棉衬衣解析:选A尼龙绳是由尼龙切片制成的纤维丝经一系列加工制成的,它属于合成纤维,A项符合题意;宣纸的主要成分是于天然纤维,B项不符合题意;羊绒衫的主要原料是羊毛,属于蛋白质,C项不符合题意;棉衬衣的主要原料是棉花,棉花属于天然纤维,D项不符合题意。
化工原理课程设计-乙醇-水混合液精馏塔设计

化工原理课程设计-乙醇-水混合液精馏塔设计全套论文化工原理课程设计题目:乙醇-水混合液精馏塔设计学院:化学与材料工程学院专业:高分子材料与工程*名:***学号:*********指导教师:***河南城建学院2012年12月25日《化工原理》课程设计工艺条件一、设计目的和要求课程设计是化工原理课程教学中综合性和实践性较强的教学环节,是理论系实际的桥梁。
通过课程设计,培养学生查阅资料、选用公式和搜索数据的能力;熟悉工程设计基本内容,掌握化工单元操作设计的主要程序及方法;锻炼和提高学生综合运用理论知识和技能的能力、独立工作和创新能力;培养学生能用简洁的文字清晰的图表来表达自己设计思想的能力。
二、设计任务完成精馏塔工艺设计,运用最优化方法确定最佳操作条件;精馏设备设计, 有关附属设备的设计和选用;绘制带控制点工艺流程图,塔板结构简图和塔板负荷性能图,编制设计说明书;等。
三、设计题目题目二:乙醇-水混合液精馏塔设计四、设计条件年处理量:8000吨/年料液浓度(质量%):40% 料液初温:30 C塔顶产品浓度:94% (质量分率)塔底乙醇含量不高于0.3% (以质量计)精馏塔塔顶压强:4kPa(表压)进料状态:泡点进料回流比:自选单板压降w 0. 7 k pa冷却水温度:30 E 设备形式:筛板塔饱和水蒸汽压力:2.5kgf/cm2(表压)(1kgf/=98.066kPa)每年实际生产天数:330天,每天24小时连续运转设计方案简介 (4)二物料流程说明 (4)三设计说明书 (5)3.1.气液相平衡数据 (5)3.2全塔物料衡算 (6)3.3工艺条件及物性数据计算..................................... .63.3.1操作温度: (7)3.3.2操作压强 (7)3.3.3平均分子量的计算 (8)3.3.4平均密度 (9)3.3.5混合液体表面张力 (10)3.3.6液体粘度 (11)3.3.7塔的物性数据列表 (12)3.4实际塔板数的计算 (12)3.4.1计算最小回流比错误!未定义书签。
实验二 共 沸 精 馏

实验二共沸精馏一、实验目的:1.通过实验加深对共沸精馏过程的理解。
2.熟悉精馏设备的构造,掌握精馏操作方法。
3.能够对精馏过程做全塔物料衡算。
4.学会使用气相色谱分析气、液两相组成。
二、实验原理:精馏是利用不同组份在气一液两相间的分配,通过多次气液两相间的传质和传热来达到分离的目的。
对于不同的分离对象,精馏方法也会有所差异。
例如,分离乙醇和水的二元物系。
由于乙醇和水可以形成共沸物,而且常压下的共沸温度和乙醇的沸点温度极为相近,所以采用普通精馏方法只能得到乙醇和水的混合物,而无法得到无水乙醇。
为此,在乙醇一水系统中加入第三种物质,该物质被称为共沸剂。
共沸剂具有能和被分离系统中的一种或几种物质形成最低共沸物的特性。
在精馏过程中共沸剂将以共沸物的形式从塔顶蒸出,塔釜则得到无水乙醇。
这种方法就称作共沸精馏。
乙醇—水系统加入共沸剂苯以后可以形成四种共沸物。
现将它们在常压下的共沸温度、共沸组成列于表1。
为了便于比较,再将乙醇、水、苯三种纯物质常压下的沸点列于表2。
表1 乙醇—水—苯三元共沸物性质从表1和表2列出沸点看,除乙醇一水二元共沸物的共沸点与乙醇沸点相近之外,其余三种共沸物的沸点与乙醇沸点均有10℃左右的温度差。
因此,可以设法使水和苯以共沸物的方式从塔顶分离出来,塔釜则得到无水乙醇。
整个精馏过程可以用图1 来说明。
图中A、B、W分别为乙醇、苯和水的英文字头;AB Z、AW Z、BW Z代表三个二元共沸物,T表示三元共沸物。
图中的曲线为25℃下乙醇、水、苯三元混合物的溶解度曲线。
该曲线下方为两相区,上方为均相区。
图中标出的三元共沸组成点T是处在两相区内。
以T为中心,连接三种纯物质A、B、w及三个二元共沸点组成点AB Z、AW Z、BW Z,将该图分为六个小三角形。
如果原料液的组成点落在某个小三角形内。
当塔顶采用混相回流时精馏的最终结果只能得到这个小三角形三个顶点所代表的物质。
故要想得到无水乙醇,就应该保证原料液的组成落在包含顶点A的小三角形内,即在ΔATABz或ΔATAWz内。
分离苯 乙酸 乙醇 苯酚的方法

分离苯、乙酸、乙醇和苯酚的方法有很多种,以下是其中一种常用的方法:
首先,将混合物加入分液漏斗中,加入适量的蒸馏水,充分搅拌混合。
然后静置分液漏斗,使液体分层。
由于乙酸和乙醇都溶于水,所以它们会与水形成一层。
而苯和苯酚则不溶于水,会形成另一层。
接下来,将分液漏斗中的上层液体(含有乙酸和乙醇的水溶液)倒入另一个容器中。
再次向分液漏斗中加入适量的蒸馏水,重复上述步骤,直到分液漏斗中的下层液体(含有苯和苯酚的有机溶剂)变得足够清澈为止。
最后,将分液漏斗中的下层液体倒入一个干净的容器中。
此时,我们已经成功地将苯、乙酸、乙醇和苯酚分离开来了。
需要注意的是,在操作过程中要避免产生任何火花或高温,因为苯和苯酚都是易燃物质。
此外,还需要注意保护眼睛和皮肤,避免接触这些化学物质。
综上所述,通过分液漏斗可以将苯、乙酸、乙醇和苯酚分离开来。
这种方法简单易行,适用于实验室或工业生产中的小规模分离操作。
2021年高中化学选修三第三章《烃的衍生物》经典练习题(答案解析)(2)
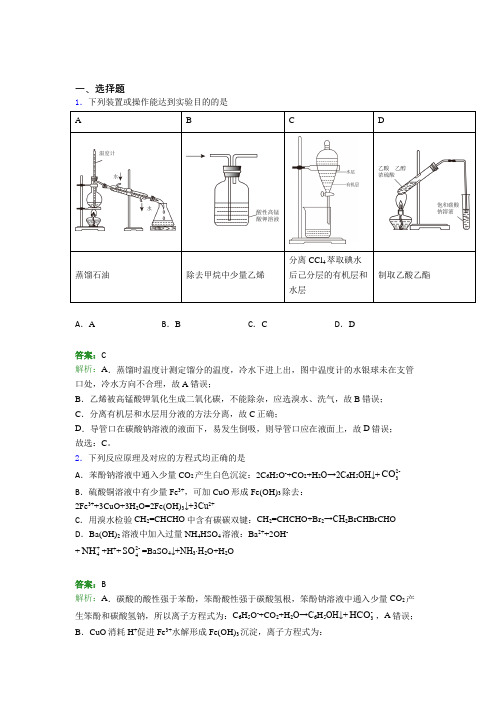
一、选择题1.下列装置或操作能达到实验目的的是 ABCD蒸馏石油除去甲烷中少量乙烯分离 CCl 4萃取碘水后己分层的有机层和水层制取乙酸乙酯A .AB .BC .CD .D答案:C解析:A .蒸馏时温度计测定馏分的温度,冷水下进上出,图中温度计的水银球未在支管口处,冷水方向不合理,故A 错误;B .乙烯被高锰酸钾氧化生成二氧化碳,不能除杂,应选溴水、洗气,故B 错误;C .分离有机层和水层用分液的方法分离,故C 正确;D .导管口在碳酸钠溶液的液面下,易发生倒吸,则导管口应在液面上,故D 错误; 故选:C 。
2.下列反应原理及对应的方程式均正确的是A .苯酚钠溶液中通入少量CO 2产生白色沉淀:2C 6H 5O -+CO 2+H 2O→2C 6H 5OH↓+2-3CO B .硫酸铜溶液中有少量Fe 3+,可加CuO 形成Fe(OH)3除去:2Fe 3++3CuO+3H 2O=2Fe(OH)3↓+3Cu 2+C .用溴水检验CH 2=CHCHO 中含有碳碳双键:CH 2=CHCHO+Br 2→CH 2BrCHBrCHOD .Ba(OH)2溶液中加入过量NH 4HSO 4溶液:Ba 2++2OH -++4NH +H ++2-4SO =BaSO 4↓+NH 3∙H 2O+H 2O答案:B解析:A .碳酸的酸性强于苯酚,笨酚酸性强于碳酸氢根,笨酚钠溶液中通入少量CO 2产生笨酚和碳酸氢钠,所以离子方程式为:C 6H 5O -+CO 2+H 2O→C 6H 5OH↓+-3HCO ,A 错误; B .CuO 消耗H +促进Fe 3+水解形成Fe(OH)3沉淀,离子方程式为:2Fe 3++3CuO+3H 2O=2Fe(OH)3↓+3Cu 2+,B 正确;C .溴水具有强氧化性,可以氧化具有还原性的醛基,所以除了加成反应之外还有氧化反应,醛基被氧化,C 错误;D .Ba(OH)2与过量NH 4HSO 4反应:24444242Ba(OH)2NH HSO BaSO (NH )SO 2H O +=↓++,所以离子方程式为:Ba 2++2OH -+2H ++2-4SO =BaSO 4↓+2H 2O ,D 错误; 所以答案选B 。
溶剂提纯

在有机化学实验中,经常使用各类溶剂作为反应介质或用来分离提纯粗产物。
由于反应的特点和物质的性质不同,对溶剂规格的要求也不相同。
有些反应(如格氏试剂的制备反应)对溶剂的要求较高,即使微量杂质或水分的存在,也会影响实验的正常进行。
这种情况下,就需对溶剂进行纯化处理,以满足实验的正常要求。
这里介绍几种实验室中常用的有机溶剂的纯化方法。
1.无水乙醚市售乙醚中常含有微量水、乙醇和其他杂质,不能满足无水实验的要求。
可用下述方法进行处理,制得无水乙醚。
在250mL干燥的圆底烧瓶中,加入100mL乙醚和几粒沸石,装上回流冷凝管。
将盛有10mL浓硫酸的滴液漏斗通过带有侧口的橡胶塞安装在冷凝管上端接通冷凝水后,将浓硫酸缓慢滴入乙醚中,由于吸水作用产生热,乙醚会自行沸腾。
当乙醚停止沸腾后,拆除回流冷凝管,补加沸石后,改成蒸馏装置,用干燥的锥形瓶作接收器。
在接液管的支管上安装一支盛有无水氯化钙的干燥管,干燥管的另一端连接橡胶管,将逸出的乙醚蒸气导入水槽中。
用事先准备好的热水浴加热蒸馏,收集34.5℃馏分70~80mL,停止蒸馏。
烧瓶内所剩残液倒入指定的回收瓶中(切不可向残液中加水!)。
向盛有乙醚的锥形瓶中加入1g钠丝,然后用带有氯化钙干燥管的塞子塞上,以防止潮气侵入并可使产生的气体逸出。
放置24h,使乙醚中残存的痕量水和乙醇转化为氢氧化钠和乙醇钠。
如发现金属钠表面已全部发生作用,则需补加少量钠丝,放置至无气泡产生,金属钠表面完好,即可满足使用要求。
2.绝对乙醇市售的无水乙醇一般只能达到99.5%的纯度,而许多反应中需要使用纯度更高的绝对乙醇,可按下法制取。
在250mL干燥的圆底烧瓶中,加入0.6g干燥纯净的镁丝和10mL99.5%的乙醇,安装回流冷凝管,冷凝管上口附加一支无水氯化钙干燥管。
在沸水浴上加热至微沸,移去热源,立刻加入几粒碘(注意此时不要振荡),可见随即在碘粒附近发生反应,若反应较慢,可稍加热,若不见反应发生,可补加几粒碘。
乙醇和水的分离实验报告

乙醇-水精馏实验报告实验名称:共沸精馏实验人员:同组人:实验地点:实验时间:班级/学号:指导教师:实验成绩:共沸精馏一、实验目的1. 通过实验加深对共沸精馏过程的理解2. 熟悉精馏设备的构造掌握精馏操作方法3. 能够对精馏过程做全塔物料衡算4. 学会使用气相色谱分析气、液两相组成。
二、实验原理精馏是利用不同组份在气-液两相间的分配,通过多次气液两相间的传质和传热来达到分离的目的。
对于不同的分离对象,精馏方法也会有所差异。
例如分离乙醇和水的二元物系。
由于乙醇和水可以形成共沸物而且常压下的共沸温度和乙醇的沸点温度极为相近。
所以采用普通精馏方法只能得到乙醇和水的混合物。
而无法得到无水乙醇。
为此,在乙醇-水系统中加入第三种物质,该物质被称为共沸剂。
共沸剂具有能和被分离系统中的一种或几种物质形成最低共沸物的特性。
在精馏过程中共沸剂将以共沸物的形式从塔顶蒸出,塔釜则得到无水乙醇。
这种方法就称作共沸精馏。
乙醇-水系统加入共沸剂苯以后可以形成四种共沸物。
现将它们在常压下的共沸温度、共沸组成列于表1。
为了便于比较再将乙醇、水、苯三种纯物质常压下的沸点列于表2。
从表1和表2列出沸点看除乙醇-水二元共沸物的共沸物与乙醇沸点相近之外其余三种共沸物的沸点与乙醇沸点均有10℃左右的温度差。
因此,可以设法使水和苯以共沸物的方式从塔顶分离出来,塔釜则得到无水乙醇。
整个精馏过程可以用图1来说明。
图中A、B、W分别为乙醇、苯和水的英文字头,ABZ,AWZ,BWZ代表三个二元共沸物,T表示三元共沸物。
图中的曲线为25℃下的乙醇、水、苯三元共沸物的溶解度曲线。
该曲线的下方为两相区上方为均相区。
图中标出的三元共沸组成点T是处在两相区内。
以T为中心连接三种纯物质A、B、W及三个二元共沸点组成点ABZ、AWZ、BWZ将该图分为六个小三角形。
如果原料液的组成点落在某个小三角形内。
当塔顶采用混相回流时精馏的最终结果只能得到这个小三角形三个顶点所代表的物质。
分离提纯的方法总结(通用4篇)

分离提纯的方法总结第1篇萃取是利用溶质在互不相溶的溶剂里溶解度的不同,用一种溶剂把溶质从另一溶剂所组成的溶液里提取出来的操作方法。
萃取分离物质时,必须用分液漏斗。
萃取的关键是找到一个合适的萃取剂,被萃取的物质在两个溶剂中的溶解度差距越大,则萃取的效果就越好。
萃取法在化工制药等领域属于常用手段,但高中阶段常见的是利用有机溶剂萃取水溶液中的物质,比如利用CCl4萃取碘水中的碘。
萃取完得到的CCl4-I2混合体系,可以采用蒸馏的方法进行分离,从而得到较纯的碘单质。
分离提纯的方法总结第2篇溶质从溶液中析出的过程(即晶体在溶液中形成的过程)称为结晶。
而重结晶是指将晶体溶于溶剂(或熔融)以后,又重新从溶液(或熔体)中结晶的过程,又称再结晶。
重结晶主要针对固态晶体物质的分离提纯,效果与溶剂选择大有关系。
溶剂最好满足以下任一条件:(1)、对主要化合物是可溶性的,对杂质是微溶或不溶的溶剂。
滤去杂质后,将溶液浓缩、冷却结晶,即得较纯的物质。
(2)、物质的溶解度在该溶剂中受温度影响较为显著。
中学阶段最常见的实例是KNO3和NaCl的混合物。
对于该混合物的分离,主要是利用它们在同一种溶剂中的溶解度随温度的变化差别很大。
则可在较高温度下将混合物溶液蒸发、浓缩,首先析出的是溶解度升高不大的NaCl晶体,除去NaCl以后的母液再浓缩和冷却后,可得较纯KNO3。
另一个实际例子就是选修5第一章提到的苯甲酸的重结晶实验。
重结晶往往需要进行多次,才能获得较好的纯化效果。
分离提纯的方法总结第3篇蒸馏是利用混合液体或液-固体系中各组分沸点不同,使低沸点组分蒸发,再冷凝以分离整个组分的`操作过程,是蒸发和冷凝两种单元操作的联合。
与其它的分离手段,它的优点在于不需使用系统组分以外的其它溶剂,从而保证不会引入新的杂质。
蒸馏是分离和提纯液态化合物常用的方法之一,是重要的基本操作。
但蒸馏主要针对组分沸点相差大于30℃以上时,才有理想的分离效果。
对于组分沸点相差不大的混合体系则采用分馏。
化工原理课程设计--乙醇——水混合液常压连续精馏

化工原理课程设计--乙醇——水混合液常压连续精馏课程设计任务书一、设计题目:乙醇——水混合液常压连续精馏二、设计原始数据:原料液处理量28000吨/年原料液初温20℃原料液含乙醇45%(质量)馏出液含乙醇93%(质量)乙醇回收率99.9%(质量)三、设计任务:完成精馏工艺设计,精馏塔设备设计和有关附属设备的设计、选用;编写设计说明书;绘制工艺流程图和塔板结构简图。
四、设计完成日期: 2013年01月18日五、设计者:王尧尧设计指导教师:张鸿发目录:1.…………………………………………………………………绪论2.………………………………………………………………工艺计算3.…………………………………………………………塔设备的计算4.………………………………………………………泵的选择及计算5.……………………………………………………………主凝器选型6.…………………………………再沸器加热釜中水蒸汽的用量计算7.………………………………………………………计算结果汇总表8.…………………………………………………………工艺流传简图绪论精馏塔是进行精馏的一种塔式汽液接触装置,又称为蒸馏塔。
有板式塔与填料塔两种主要类型。
根据操作方式又可分为连续精馏塔与间歇精馏塔。
蒸气由塔底进入,与下降液进行逆流接触,两相接触中,下降液中的易挥发(低沸点)组分不断地向蒸气中转移,蒸气中的难挥发(高沸点)组分不断地向下降液中转移,蒸气愈接近塔顶,其易挥发组分浓度愈高,而下降液愈接近塔底,其难挥发组分则愈富集,达到组分分离的目的。
由塔顶上升的蒸气进入冷凝器,冷凝的液体的一部分作为回流液返回塔顶进入精馏塔中,其余的部分则作为馏出液取出。
塔底流出的液体,其中的一部分送入再沸器,热蒸发后,蒸气返回塔中,另一部分液体作为釜残液取出。
精馏塔的工作原理是根据各混合气体的汽化点(或沸点)的不同,控制塔各节的不同温度,达到分离提纯的目的。
化工生产常需进行液体混合物的分离以达到提纯或回收有用组分的目的,精馏操作在化工、石油化工、轻工等工业生产中中占有重要的地位。
乙醇-水精馏实验报告

竭诚为您提供优质文档/双击可除乙醇-水精馏实验报告篇一:精馏法分离乙醇—水报告化工基础实验报告精馏法分离乙醇—水体系姓名:李伟峰学号:系别:_____化学工程系______专业:石油加工生产技术年级:20XX级同组人:_赖仪凤,周春丹,陈茂飞,李伟勇指导教师:_____陈少峰,梁燕,________20XX年11月13一、实验目的(1)熟悉板式塔的结构及精馏流程;(2)理论联系实际,掌握精馏塔的操作;(3)学会精馏塔塔效率的测定方法。
(4)了解填料精馏塔的基本结构,熟悉精馏的工艺流程。
(5)掌握精馏过程的基本操作及调节方法。
(6)掌握测定塔顶、塔釜溶液浓度的实验方法。
(7)掌握精馏塔性能参数的测定方法,并掌握其影响因素。
(8)掌握用图解法求取理论板数的方法。
二.实验方法本实验采用精馏法对乙醇—水混合液进行分离提纯,通过对全回流和部分回流条件下各参数的测定,进而由图解法求取其理论塔板数,确定出最适宜的精馏分离操作条件,并采用等板高度(heTp)来表示其分离能力。
1.实验装置与流程本实验装置的主体设备是填料精馏塔,配套的有加料系统、回流系统、产品出料管路、残液出料管路、进料泵和一些测量、控制仪表。
精馏装置由板式精馏塔主体(包括塔釜、塔身和塔顶冷凝器)、加料系统,产品贮槽及测量仪表所组成。
本精馏装置所采用的精馏塔为筛板塔,塔内径为50mm,塔板15块,板间距为100mm,开孔率4-6%、降液管管径φ14*2;塔釜以2支1kw的电加热棒进行加热,其中一支是常加热,而另一支通过自耦变压器可在0~1kw范围内调节;塔顶为盘管式冷凝器,上升蒸汽在盘管外冷凝,冷凝液流至分配器储槽,一部分回流至塔内,一部分作为产品输出。
料液由泵输送,经转子流量计计量后加入塔内。
本实验料液为乙醇溶液,由进料泵打入塔内,釜内液体由电加热器加热汽化,经填料层内填料完成传质传热过程,进入盘管式换热器管程,壳层的冷却水全部冷凝成液体,再从集液器流出,一部分作为回流液从塔顶流入塔内,另一部分作为产品馏出,进入产品贮罐;残液经釜液转子流量计流入釜液贮罐。
乙醇蒸馏实验报告

一、实验目的1. 了解乙醇蒸馏的原理和操作方法。
2. 掌握蒸馏装置的安装和操作技巧。
3. 通过实验测定乙醇的沸点。
4. 分析蒸馏过程中可能出现的现象和解决方法。
二、实验原理蒸馏是利用液体混合物中各组分沸点不同,通过加热使低沸点组分先汽化,然后冷凝回收,从而实现分离和提纯的方法。
乙醇的沸点为78.5℃,低于水的沸点,因此可以利用蒸馏法将乙醇从水中分离出来。
三、实验仪器与试剂1. 实验仪器:蒸馏烧瓶、温度计、冷凝管、接收瓶、铁架台、石棉网、酒精灯、蒸馏头、接引管、量筒、沸石等。
2. 实验试剂:乙醇、水、苯酚(或硫酸)。
四、实验步骤1. 将乙醇和水按一定比例混合,加入苯酚或硫酸作为助剂。
2. 将混合液倒入蒸馏烧瓶中,加入沸石。
3. 将蒸馏烧瓶放在铁架台上,安装好冷凝管、接收瓶等。
4. 将冷凝管插入接收瓶中,确保冷凝管底部接触接收瓶底部。
5. 用酒精灯加热蒸馏烧瓶,开始蒸馏。
6. 观察温度计,当温度达到78.5℃时,停止加热。
7. 收集蒸馏出的液体,记录体积。
8. 重复步骤5-7,进行多次蒸馏,以提高乙醇的纯度。
五、实验现象1. 加热过程中,烧瓶内液体逐渐沸腾,产生气泡。
2. 温度达到78.5℃时,蒸馏烧瓶内液体开始汽化,蒸汽通过冷凝管冷凝成液体,流入接收瓶中。
3. 随着蒸馏的进行,接收瓶中的液体体积逐渐增加,颜色逐渐变浅。
六、实验结果与分析1. 通过多次蒸馏,乙醇的纯度逐渐提高,颜色逐渐变浅。
2. 实验测得的乙醇沸点为78.5℃,与理论值相符。
3. 实验过程中,可能出现的现象有:烧瓶内液体沸腾剧烈、冷凝管堵塞、接收瓶内液体浑浊等。
解决方法如下:- 调整火焰大小,控制烧瓶内液体沸腾程度。
- 清理冷凝管,确保蒸汽畅通。
- 用滤纸过滤接收瓶内的液体,去除杂质。
七、实验结论1. 通过乙醇蒸馏实验,掌握了乙醇蒸馏的原理和操作方法。
2. 实验结果表明,蒸馏法可以有效地将乙醇从水中分离出来,提高乙醇的纯度。
3. 在实验过程中,要注意安全操作,防止烫伤、火灾等事故的发生。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第30卷第2期2010年3月云南师范大学学报Journa l o fYunnan Nor m alUn i v ersity*V o. l 30No . 2M ar . 2010苯-乙醇-水混合液的分离提纯苏永庆, 胡红艳, 段爱红(云南师范大学化学化工学院, 云南昆明650092摘要: 在大学物理化学实验教学中, 苯-乙醇-水三组分体系相图的绘制实验将产生大量的苯-乙醇-水混合废液, 并分层为上层苯液(含有少量水和乙醇, 下层乙醇-水溶液(含有大量乙醇和水, 以及少量苯. 文章根据苯、乙醇在水中的溶解度不同, 对上层苯液进行多次水萃取乙醇, 最后用无水CaC l 2干燥处理得到纯苯(98. 9%. 对于下层乙醇-水溶液, 由于苯与乙醇、水形成三元恒沸物, 通过蒸馏除去苯, 继续蒸馏得到乙醇-水的二元恒沸物(乙醇95. 6%, 水4. 4% 和纯乙醇(99. 7w t %. 将乙醇-水的二元恒沸物通过CaC l 2脱水处理, 得到99. 4w t %以上的乙醇. 关键词: 苯; 乙醇; 分离; 提纯; 萃取; 蒸馏中图分类号: O 622 文献标识码: A 文章编号: 1007-9793(2010 02-0059-04在大学的物理化学实验教学中[1], 作为经典混溶, 且苯、乙醇、水三组分混合后不会发生化学反应, 用水作溶剂, 通过少量水多次萃取, 就可以除去溶液里的乙醇. 萃取分离乙醇后的苯液含有少量的水(20 时水在苯中的含量为0. 050%, 通过干燥剂处理便可以除去里面的水. 通过密度测量来检测它的纯度.对于下层含有少量苯的乙醇-水溶液, 由于乙醇和水可以任意比例混溶, 用萃取的方法不能将它们分开, 但可借鉴工业提纯乙醇的方法. 工业上制得的酒精一般是乙醇(含量95%左右和水的混合液, 为了得到更纯的乙醇, 工业上常用苯法除去乙醇中所含的水分, 即把少量的苯加入到乙醇溶液中, 然后把含苯的乙醇-水混合液投入精溜塔中, 在64. 6 时蒸出苯、乙醇和水的三元恒沸物(苯74. 1%, 乙醇18. 5%, 水7. 4%. 如果苯过量, 则在69. 4 时蒸出苯和水的二元恒沸物(苯91. 1%, 水8. 9%, 继续加热, 则可以在78. 2 时蒸出乙醇和水的二元恒沸物(乙醇95. 6%, 水4. 4%, 当温度达到78. 5 时蒸出纯的乙醇, 通过这种方法得到的乙醇的含量可达到99%以上. 由于云南地处高原, 大气压力为605-608mmH g , 蒸馏温度与上述温度有所偏差. 对于[3, 4]实验之一的苯-乙醇-水三组分体系相图的绘制将产生大量的苯-乙醇-水的混合废液. 苯是有毒有机物, 如果不处理就把它随意倒掉, 将造成环境污染, 并且苯、乙醇是广泛使用的重要化工原料, 所以本文设计一种简单有效的方法来分离提纯这种混合废液, 使苯, 乙醇可以重复利用, 节约资源, 减少环境污染.1 实验原理图1是常温下苯-乙醇-水三组分体系的相图, 帽形图以内的为部分互溶区域, 帽形图以外的是完全互溶区域. 可以看到, 苯-乙醇-水的混合液, 由于两两组分溶解度不同, 在帽形区域内出现分层. 混合液的上层为含有少量乙醇和水的苯液, 下层为含有少量苯的乙醇-水溶液. 用分液漏斗分离上下两层溶液, 使各自都回到帽行区域外.上层苯液中主要含有苯、少量乙醇和水, 只要除去里面的少量乙醇和水就可以得到纯度较高的苯. 由于苯在水中的溶解度为0. 175g , 乙醇含有一个亲水性基团 -OH , 可以与水任意比例* 收稿日期:2009-08-28[2]基金项目:云南师范大学综合性、设计性实验研究项目(2007:(, 男, , 博士.60云南师范大学学报(自然科学版第30卷乙醇和水的二元恒沸物, 可以用工业生产无水乙醇的方法或直接加入干燥剂来制取纯度较高的乙醇.除去水的苯液中只含有苯和少量的乙醇, 在知道纯苯、纯乙醇的密度后, 可以根据下列公式计算得到苯的纯度.= 1a 1+ 2a 2= 1a 1+ 2(1-a 1 a 1=( - 2 /( 1- 2 式中: 溶液的密度; 1 纯苯的密度; 2 纯乙醇的密度; a 1 苯的质量分数; a 2 乙醇的质量分数.分别取50mL 纯乙醇和50mL 纯苯, 用比重天平测它们的密度, 重复三次, 取平均值, 结果见表1.表1 纯苯和纯乙醇的密度T ab . 1 The density of pure a lcohol and benzene 测量次数苯(分析纯 g /L乙醇(分析纯 g /L一次875786二次874787三次874786平均值8747862 实验材料与仪器设备2. 1 实验材料与试剂苯-乙醇-水混合废液(由物化实验室收集提供, 苯(A.R . , 乙醇(A. R. , 无水C a C l 2(A. R . , CuSO 4(A. R . , 蒸馏水等2. 2 仪器及设备阿贝(Abbe 折光仪(QG230 1998, 上海精密科学仪器有限公司, 比重天平(天津仪器厂, 恒温震荡器(TB 2000, 天津仪器厂, 梨形分液漏斗等.3. 3苯的提纯取100mL 苯液加入到梨形分液漏斗中, 加入20m L 蒸馏水. 轻轻振摇分液漏斗, 每隔几秒钟将漏斗倒置, 打开活塞放气, 重复操作2~3次. 然后将漏斗放到震荡器上, 振荡15m i n , 取下置于铁圈上, 静止分层. 当溶液分为两层后, 小心旋开活塞, 放出下层水液, 重复上述萃取过程. 最后将萃取后[4]的苯液倒入锥形瓶, 加入无水C a C l 2干燥. CaC l 2价格便宜, 吸水能力强, 但平衡速度慢, 所以用Ca C l 2干燥时, 需放置一段时间, 并间歇振摇. 干燥后的苯液用白色的无水CuSO 4检验, 若苯液中无水, CuSO 4不变色, 仍为白色; 若还含有水, CuSO 4会与水反应生成CuSO 4 5H 2O 而显蓝色.除尽水后的苯液, 用比重天平测量它的密度, 计算纯度. 实验数据及计算结果见表2.表2 水萃取次数对苯液密度的影响T ab . 2 E ffect o f the wa ter ex tracti ng ti m eson t he density o f benzene 萃取次数苯液的密度g /L苯的质量分数%二次86792. 0三次87297. 7四次87398. 9五次87398. 93 实验过程与结果讨论3. 1原料的预处理把从物化实验室收集的苯-乙醇-水混合废液放置分层, 用梨形分液漏斗分离上层苯液(含有少量乙醇和水和下层乙醇-水溶液(含有少量苯, 备用. 3. 2纯苯, 纯乙醇的密度测定纯苯, 纯乙醇的密度是确定后面萃取所得到的苯的纯度的依据, 尽管它们的密度在商品标签上已经给出, 但因为所处环境和所用仪器不同, 测.3. 4乙醇的提纯1第2期苏永庆, 等:苯-乙醇-水混合液的分离提纯61绘制物质的折光率不但与它的分子结构和光线波长有关, 而且也受温度, 压强等因素的影响. 通常, 温度升高一度, 液体有机物的折光率就减小3 5 10-4[5]3. 4. 2乙醇-水溶液中苯的分离取3. 1分离得到的下层乙醇-水溶液(含有少量苯 160mL , 倒入250mL 圆底烧瓶中, 加入2~3粒沸石, 安装好蒸馏的装置. 下层溶液蒸馏时, 在59 时开始沸腾, 59. 5 时出现第一滴馏分, 为苯、乙醇和水的三元恒沸物, 控制加热温度, 以每秒钟产生1~2滴馏分为益, 沸腾持续了一段时间后有所减弱. 到65. 9 又开始第二次激烈沸腾, 产生苯和水的二元恒沸物, 大约20s 后沸腾有所减弱. 温度升到74. 2 时, 开始第三次激烈沸腾, 到78. 6 时温度回落, 在此温度期间蒸出乙醇和水的二元恒沸物. 在第三次激烈沸腾, 滴出馏分3~4滴后, 收集馏分供后续的脱水处理. 在表3 乙醇水标准溶液的折光率(温度:30 水=998g /L, 乙醇=786g /L~5. 5 10. 在实际工作中, 一般都是-4固定某个温度, 所有的物质的折光率都在这个温度下测量, 本实验中固定温度为30 .将阿贝折光仪配套的恒温水浴调整运行到30 , 按照下表用移液管精确配置好乙醇溶液, 浓度由低到高测出不同浓度乙醇的折光率, 绘制乙醇标准溶液的组成折光率特性曲线. 数据计算见表3, 标准曲线见图2.78. 6 后继续加热, 得到含量99. 7w %t 的纯乙醇馏分.3. 4. 3乙醇的脱水处理上述收集到的乙醇-水的二元恒沸物, 乙醇的质量分数为95. 6%, 水的质量分数为4. 4%.要进一步除去水分, 可重复使用3. 4. 2的方法, 或者[6]采用氧化钙法制备无水乙醇(实验室法, 本实验采用后者, 即取250m L 短颈圆底烧瓶, 放入100mL 上步蒸馏得到的乙醇和水的溶液, 慢慢加入小快的生石灰40g 和氢氧化钠0. 5g . 装上回流装置, 封好瓶塞, 在水浴上煮沸回流约1h . 回流完毕, 拆下冷凝管, 改装为蒸馏装置, 用干燥的锥形瓶收集无水乙醇馏分.3. 4. 4乙醇纯度的检验对收集到的无水乙醇馏分进行折光率测定, 并对照图2的乙醇-水标准溶液的组成折光率曲线, 找到对应的点, 得到它的纯度, 见表4.表4 馏分在30 时的折光率T ab . 4The refractive i ndex of t he d i still ation a t 30 测量次数馏分的折光率(n 乙醇的质量分数%一次二次三次平均值 99. 4Tab . 3 Refracti ve i ndex of nor mati ve sol uti on of alcohol-water (T e m perature :30 , =998g /L, a lcoho l =786g /L w a te r乙醇体积/mL10. 009. 509. 008. 508. 007. 006. 005. 003. 00水体积/mL0. 000. 501. 001. 502. 003. 004. 005. 007. 00乙醇的质量分数%10093. 787. 681. 775. 964. 754. 144. 025. 2折光率(n 1.1. 1. 1. 1. 1. 1. 1. 1.3546352035073487347234433416339233561. 35441. 35451. 354599. 2 99. 599. 54 结论(1 对于苯-乙醇-水的混合液, 通过分液(62醇-水溶液(含有少量苯分离.云南师范大学学报(自然科学版第30卷[1] 云南师范大学化学化工学院物理化学教研室, 物理化学实验[M].昆明:云南民族出版社, 2003. [2] 化学工程手册编委会. 化学工程手册(第8篇[M].北京:化学工业出版社, 1989.[3] 刑存, 于跃芹. 有机化学(上册 [M ].济南:山东大学出版社, 2000.[4] 陆国元. 有机化学[M ].南京:南京大学出版社, 1999.[5] 苏联 , B . A 拉宾诺维奇, 哈文著. 尹承烈译. 简明化学手册[M].北京:化学工业出版社, 1983. [6] F i eser , L . F . , O rg an i c Exper i m ents , R ay theon Educa ti on Co . , L ex ing t on , M ass , . 1968.(2 对于上层苯液, 用蒸馏水萃取4~5次就可以除去苯液中的乙醇, 使苯的纯度达到98.9w %t 以上.(3 对于下层乙醇-水溶液, 通过蒸馏得到乙醇-水的二元恒沸物(乙醇95. 6%, 水4. 4% 和纯乙醇(99. 7w %t . 将乙醇-水的二元恒沸物通过Ca C l 2脱水处理, 可以得99. 4w %t 以上的乙醇.参考文献:Separation and purificati on of benzene -ethano l -waterwaste li qui dSu Yong qing , Hu Hong yan , Duan ai -hong(F acu lty of Che m istry &Che m i ca l Eng i neer i ng , Y unnan N orma lU n i ve rsity , 650092K un m i ng C ity , P . R. Chi naAbst ract :: A lot of benzene-ethanol-w ater w aste m i x ed liquid w as produced in physi c al-che m ical ex peri m ent course Phase dra w o f benzene-ethano l-w ater . The w aste liqu i d d i v ided into t w o layers . The up per layer w as benzene so l u ti o n w ith a little ofw ater and ethano. l The do w n layerw as ethano l solution w ith l o ts of ethano, l w ater and a little o f benzene . The upper benzene so lution w as ex tracted repetiti o usly by w ater accord i n g to the difference of so lubility o f benzene and ethano l i n w ater separate l y . Then itw as treated by desic cant and the pure benzene (98. 9% w as go tten . For the down ethano l solution , the benzene w as w i p ed o ff by distilli n g because benzene , ethanol and w ater can for m three do llars azeotrope . The t w o do llars azeotrope o f ethano l-w ater(ethano l 95. 6w %t , w ater 4. 4w %t and pure ethano l (99. 7w %t w ere gotten by Further dis tilling . The t w o do llar azeotrope o f et h ano l-w ater w as treated C a C l 2by desiccan t to get the pure alcoho l (99. 4%. K ey w ords :benzene ; et h ano; l separation ; purificati o n ; ex traction; distillation。
