讲胶体的稳定性PPT课件
第五章胶体的稳定性
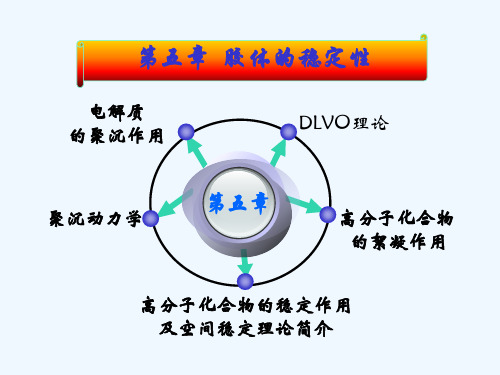
64 n KT 2 0 2 k) d 0exp( k
式5-10
exp( Ze KT ) 1 0/2 0 exp( Ze KT ) 1 0/2
R 表示两平板质点的双电层在单位面积上的相互排斥能(斥力位能)。
当 0 很高时,Ze 0 >>1,则 0 →1, R 与 0 无关
§5-1 电解质的聚沉作用
一、聚沉与老化
聚沉:胶粒聚集变大而沉淀的过程,与沉淀反应不同, 因聚沉电解质的量远少于沉淀量,其间不存在当量关系。
老化:由于小颗粒具有大的溶解度,静止时,溶液中的 小颗粒溶解,大颗粒长大,直到形成分散度较单一的大颗粒 ,这一过程称为老化。
二、聚沉值及其测定方法
聚沉值:在指定条件下,使溶胶聚沉所需电解质的最 低浓度,以mol/L表示。
一、胶粒间的范德华吸引能
a、永久偶极之间 1、分子间的范德华吸引能
对于同种分子
b、色散吸引能 c、诱导偶极与永久偶极之间
6 x 分
式5-1 (六次律)
式中: 分 :分子间总的范德华引力
2 2 3 2 2 hv 3 KT 4
式5-2
x:分子间距离 α :分子的极化度
对斥能峰的高低有较大影响。 ② s 的影响 , A与 0无关,而 0 随 A 上升而增加,所以 R 2 0 与A相同时,势垒能 s 增加而上升。 泥浆不抗盐是因为电解质对双电层的压缩,使 s下降 ,势垒下降。
R 2 ,所以A与 不变时, ③ 的影响 A与 无关, 0 越小,双电层越厚,势垒越高。
1 1 1 ∶ ∶ 1 2 3
6
6
6
聚沉值与离子价数的6次方成反比,即schulze-hardy 规则。除了反离子外,同号离子的性质、大小均对聚沉值 有影响。
讲-第章-胶体的稳定性

(ii) 脱水效应—高聚物分子由于亲水,其水化作用较胶粒 水化作用强(憎水),从而高聚物的加入夺去胶粒的水化外壳 的保护作用。
(iii) 电中和效应—离子型高聚物的加入吸附在带电的胶 粒上而中和胶粒表面电荷。
2. 空间稳定理论( steric stabilization)
向溶胶中加入高聚物或非离子表面活性剂,虽降低了电势, 但却显著地提高了溶胶系统的稳定性,这是用DLVO理论所解 释不了的。这种结果可用空间稳定理论加以解释。空间稳定理 论认为这是由于溶胶粒子表面吸附了高聚物,吸附的高聚物层 引起系统的G >0.
可见,聚沉能力是聚沉值的倒数,即聚沉值愈小,该电解 质的聚沉能力就愈大;反之,聚沉值越小的电解质,其聚沉能 力越强。
(1)电解质中与胶粒所带电荷相反的离子是其主要聚沉作用 的离子,并且离子价数越高,电解质的聚沉能力越大。
对某一给定溶胶,一、二、三价反离子聚沉值的比例大约是:
100 :1.6 : 0.14
当x缩小,先出现一 极小值F,则发生粒子的
Born排斥 {U}
聚集称为絮凝(可逆的)。
UR ∝exp{-x} —德拜参量
Umax
当x再缩小,则出现 极大值Umax。只有两胶 粒通过热运动积聚的动 能超过15kT时才有可能
超过此能量值,进而出 现极小值C,在此处发
生粒子间的聚沉(不可 逆)。
势垒
exp( Ze0 ) 1
2kT
exp( Ze0 ) 1
2kT
B:常数; :介电常数;Z:分散离子价数 ; :复合比 (complex ration) ; kB :波尔滋曼常数
9.6胶体稳定性
带相反电荷的溶胶互相混合发生聚沉
二、 溶胶的聚沉
3.大分子化合物的作用 (1) 保护作用:有足量的大分子化合物 停靠基团
原因:高分子覆盖溶胶表面可起保护作用
应用:如墨汁,油漆,照相乳剂 (2) 絮凝作用:少量大分子化合物 絮凝:疏松的棉絮状沉淀 原因:大分子的搭桥效应、脱水效应、电中和效应 稳定基团
二、 溶胶的聚沉
聚沉:溶胶聚结沉降现象
1.电解质对溶胶稳定性的影响
电解质影响溶胶电性,溶胶对其十分敏感
• 适量电解质是溶胶稳定必要条件
适量定位离子使溶胶荷电而稳定(制备时不可净化过度) 聚沉原因:反离子压缩双电层,使 d,,= 0时最不稳定 • 过多电解质使溶胶发生聚沉 聚沉值:使溶胶聚沉所加的电解质的最低浓度 不同电解质聚沉能力(聚沉值)不同,其规律
V
Vr= e –kH
Vb
第六节 溶胶的稳定性和聚沉作用 H
1 Va H
一、胶体稳定性
热力学因素:高分散度,比表面能大,有自发聚集倾向
稳定溶胶的因素 : 1. 动力稳定性(扩散力):扩散,Brown运动,有利稳定 粒径越小、介质粘度越大,越使溶胶稳定 2. 表面带电(静电斥力): 带电后的电性斥力,是溶胶稳定的主要原因 3. 溶剂化(水化膜斥力 ):降低表面能,有利稳定 4. 添加高分子保护
二、 溶胶的聚沉
1.电解质对溶胶稳定性的影响 聚沉值: 使溶胶聚沉所加的电解质的最低浓度 不同电解质聚沉能力不同,可用聚沉值来衡量,其规律有 (1) 反离子:价数: 1价: 2价: 3价 = 1 :
1 1 : 2 3
6
6
同价:水化半径越小,越易靠近质点,聚沉能力越强 (2) 同号离子:对溶胶有稳定作用,价数越高作用越强 (3) 有机化合物的离子:通常有强吸附能力,有很强的聚沉能力 (4) 不规则聚沉:溶胶对高价反离子强烈吸附的结果 2.溶胶的相互聚沉作用
胶体的稳定性
聚沉值
使溶胶发生明显聚沉时外加电解质的最小 浓度称为该电解质对该溶胶的聚沉值 浓度称为该电解质对该溶胶的聚沉值
聚沉能力
聚沉能力=1/聚沉值 聚沉能力=1/聚沉值
解释: 解释:
ci ↑ I ↑
κ↑
VR ↓↓ V ↓↓
斥力不足以克服引力——聚沉 聚沉 斥力不足以克服引力 聚沉值: 聚沉值:
∂V
V = V A + VR = 0
(3)法扬斯(Fajans)规则 法扬斯(Fajans)规则 能与晶体的组成离子形成不溶物或难电离化合物的 异电离子优先被吸附,具有强的聚沉能力。 异电离子优先被吸附,具有强的聚沉能力。
(4)不规则聚沉 有时,少量电解质使溶胶聚沉,电解质浓度高时, 有时,少量电解质使溶胶聚沉,电解质浓度高时, 又重新分散,浓度再高又聚沉,此为不规则聚沉, 又重新分散,浓度再高又聚沉,此为不规则聚沉,多发 不规则聚沉 生在以大离子或高价离子为聚沉剂的情况——大离子或 生在以大离子或高价离子为聚沉剂的情况 大离子或 高价离子引起电动电势反号。 高价离子引起电动电势反号。 (5)有机离子一般具有较强聚沉能力——特殊吸附力 有机离子一般具有较强聚沉能力 特殊吸附力 (6)同号离子的影响 大的同号有机离子因与质点强烈的van 大的同号有机离子因与质点强烈的van der Waals 引力而被吸附,从而改变质点的表面性质。一般说来, 引力而被吸附,从而改变质点的表面性质。一般说来, 大的或高价的负离子对于负溶胶有一定稳定作用, 大的或高价的负离子对于负溶胶有一定稳定作用,大的 或高价正离子对于正溶胶有一定稳定作用。 或高价正离子对于正溶胶有一定稳定作用。
-
- + + ++ + + + ++
胶体化学第5章-胶体的稳定性

电解质
负电溶胶的聚沉值(mmol/L)
As2S3溶胶
Au溶胶
AgI溶胶
实验 平 均 实验 平 均 实 验 平均
值
值
值
值
值
值
LiCl
58
LiNO3
—
NaCl
51
Na NO3
—
KCl
49.5
K NO3
50
55
1/2K 2SO4
65.5
Rb NO3
—
CH 3COOK 110
HCl
31
Ag NO3
—
— — 24 — — 25 24 23 — — 5.5 —
—
165
—
140
—
136
142
—
126
—
—
0.01
电解质
MgCl 2 Mg(NO3 )2 Mg SO4 CaCl 2 Ca(NO3 )2 SrCl2 Sr(NO3 )2 BaCl2 Ba(NO3 )2 ZnCl2 Zn(NO3 )2 UO2(NO3 )2 CuSO4 Pb(NO3 )2
As2S3溶胶
⑸Burton-Bishop规则:溶胶的浓度也影响电解质的聚沉值。通常对一 价反离子,溶胶稀释时聚沉值增加;对二价反离子,不变;对三价反离 子,降低。这就是Burton-Bishop规则。
4.2 DLVO理论
前 苏 联 学 者 Derjaguin 和 Landau ( 1941 ) 与 荷 兰 学 者 Verwey 和 Overbeek(1948)分别独立提出胶粒之间存在范德华吸引势能和双电层 排斥势能,据此对溶胶稳定性进行定量处理,形成了比较完善地解释胶
分子对之间相互作用的加和。由此推导出不同形状粒子间的范德华引
第8章 胶体分散体系稳定性(共46张PPT)

8.2.2 慢聚沉:
• 当质点之间有势垒存在时,势垒的作用相当于质点 之间存在一斥力,在其作用下,质点向彼此远离的 方向扩散。
• 于是,慢聚沉的聚沉速度常数 Ks 比快聚沉小〔应加 一阻力校正项〕:
U
K K exp( m )
s
r
kT
〔Ks 即 Kslow 〕
B
• 式中 Kr 相当于碰撞频率,Vm 势垒相当于慢聚沉过
14
8.1.3 总的势能曲线
系统的总势能为斥力势能和引力势能的加和。
UUAUR
以总势能对距离作图, 即得总势能曲线
Umax为势垒
当粒子的动能大于势垒时方能聚沉
势垒的上下决定了胶体的稳定性
15
当颗粒动能较小时,不能越过能垒而相互靠近; 只有当动能很高时,方能越过能垒而聚沉。这就很好 地说明了溶胶是一种亚稳的系统。
M 1 :M 2:M 3 (1 )6:(1 )6:(1 )6 1 :6:7 429 1 ccccccccc 2 3
CCC:临界絮凝浓度〔临界聚沉值〕
19
临界聚沉浓度
胶体的稳定性取决于总势能曲线上的势垒的大小。那 么就可以定性地把是否存在势垒作为判断胶体稳定与否的 标准。
势垒的高度随溶液中电解质浓度的增大而降低,
ψ0为正值,随距离增大呈指数衰减。 (4) 参加电解质对引力势能影响不大,但对斥力势能的影响却十分显著
从电解质对胶体粒子势能的影响看, 当电解质的浓度或价数增加使溶胶发生聚沉时, 所必须克服的势垒高度和位置皆发生变化。
(b) 聚沉值与分散介质介电常数的立方成正比
22
DLVO理论总结〔1〕
胶粒既存在斥力势能,也存在引力势能。前者是带电胶粒靠
4
胶体的稳定性

胶体的稳定性
答案:
胶体(Colloid)又称胶状分散体,是一种分散质粒子直径介于粗分散体系和溶液之间的一类分散体系[1]。
胶体不一定都是胶状物,也不一定是液体,常见的胶体有有色玻璃、果冻、鸡蛋清、血液等。
介稳性:
胶体的稳定性介于溶液和浊液之间,在一定条件下能稳定存在,属于介稳体系。
胶体具有介稳性的两个原因:
原因一:胶体粒子可以通过吸附而带有电荷,同种胶粒带同种电荷,而同种电荷会相互排斥(要使胶体聚沉,就要克服排斥力,消除胶粒所带电荷)。
原因二:胶体粒子在不停地做布朗运动,与重力作用相同时便形成沉降平衡的状态。
结构:
根据法扬斯规则(能与晶体的组成离子形成不溶物的离子将优先被吸附.优先吸附具有相同成分的离子),胶体粒子是胶粒,胶粒与扩散层在一起组成了胶团,而胶粒又包括胶核与吸附层。
高一化学胶体课件

胶体制备与提纯的注意事项
注意安全
在制备和提纯过程中,应避免使用有 毒有害的试剂,并确保操作安全。
控制条件
制备和提纯过程中,应控制好温度、 压力、浓度等条件,以保证实验结果 的准确性和可靠性。
实验操作规范
在实验过程中,应遵循实验操作规范 ,避免污染和交叉污染。
实验后处理
实验结束后,应对废液进行妥善处理 ,避免对环境和人体造成危害。
胶体在医学中的应用
胶体在医学中也有着重要的应 用,如医用胶、血液透析等。
医用胶是一种常用的外科手术 材料,具有快速止血、促进伤 口愈合等作用,广泛应用于手 术和创伤治疗中。
血液透析则是利用胶体的渗透 作用,将血液中的毒素和多余 水分滤出,以治疗肾功能衰竭 等疾病。
胶体在其他领域的应用
除了化学工业和医学领域,胶体 在其他领域也有着广泛的应用。
如胶体在环保领域中可以用于污 水处理、土壤修复等;在农业领 域中可以用于农药和肥料的缓释
剂等。
此外,胶体还在化妆品、食品、 墨水等领域中有着广泛的应用, 如隐形眼镜护理液、墨水等产品
中都含有胶体成分。
05
胶体的实验研究
胶体实验的目的与原理
目的
通过实验了解胶体的性质和特点,加深对胶体概念的理解。
原理
胶体是一种分散质粒子直径在1nm-100nm之间的分散系,具有介稳性、丁达 尔效应等特点。实验通过观察胶体的电泳、聚沉等性质,探究胶体的本质。
实验步骤与操作方法
步骤一
制备胶体。将一定量的Fe(OH)3固体溶解在沸水中,得到Fe(OH)3胶体。
步骤二
进行电泳实验。将胶体置于电场中,观察胶体粒子在电场中的移动情况。
氧化铝等。
胶体化学第5章胶体的稳定性

体的移动速度来计算电渗和电动现象,从而判断胶体的稳定性。
02 03
沉降法
沉降法是通过测量胶体在重力场中的沉降速度来判断其稳定性。如果沉 降速度很快,说明胶体的稳定性较差;如果沉降速度很慢,说明胶体的 稳定性较好。
光学法
光学法是通过观察胶体在光学显微镜下的形态来判断其稳定性。如果观 察到明显的聚沉现象,说明胶体的稳定性较差;如果没有观察到明显的 聚沉现象,说明胶体的稳定性较好。
反絮凝
是指通过某些措施使已经 絮凝的胶体重新分散成小 聚集体的过程。
04 胶体的应用
胶体在化学工业中的应用
胶体在化学工业中有着广泛的应用, 如涂料、颜料、粘合剂、印染等。胶 体作为分散相,能够提高产品的性能 和稳定性,改善产品的外观和手感。
胶体在化学工业中还可以用于制备功 能性材料,如光敏材料、电绝缘材料 ห้องสมุดไป่ตู้磁性材料等,以满足不同领域的需 求。
A
B
C
D
电子信息领域
利用胶体化学制备高性能的电子材料和器 件,推动电子信息技术的进步和发展。
能源与催化领域
利用胶体化学制备高效催化剂和燃料添加 剂,提高能源利用效率和减少环境污染。
感谢您的观看
THANKS
分散剂的作用
分散剂可以降低胶体粒子 之间的相互作用力,使胶 体粒子在介质中均匀分散。
分散剂的种类
常用的分散剂包括表面活 性剂、高分子物质等。
胶体的絮凝与反絮凝
胶体的絮凝
是指在某些条件下,胶体 粒子通过相互作用形成较 大聚集体的现象。
絮凝的条件
电解质、高分子物质、温 度变化等都可能引起胶体 的絮凝。
根据分散相粒子的大小,胶体可 分为粗分散体系、溶胶、高分子 溶液和缔合胶体等。
第五章胶体的稳定性分解

第五章胶体的稳定性分解胶体是由固体颗粒或液滴分散在连续相中而形成的混合物。
在胶体中,颗粒或液滴的尺寸通常在1纳米至1微米之间,介于溶液和悬浮液之间。
在自然界和工业中,我们经常可以观察到各种胶体,如乳液、凝胶和泡沫等。
胶体的稳定性是指胶体系统维持稳定状态的能力,即颗粒或液滴分散均匀,并且不易聚集和沉降。
胶体的分解是指胶体系统中颗粒或液滴发生聚集而失去稳定性的过程。
胶体分解的原因有很多,最常见的原因是颗粒之间的吸引力增强,导致聚集现象的发生。
颗粒之间的吸引力可以通过静电作用、范德华力、亲水性或疏水性相互作用等来实现。
当这些吸引力超过分散力时,胶体就会发生分解。
胶体的分解会导致胶体体系不均匀,颗粒或液滴会聚集成大块或沉降到容器底部。
为了维持胶体的稳定性,我们可以采用一些方法来防止胶体的分解。
常见的方法包括添加稳定剂、控制环境条件和调节胶体粒径。
添加稳定剂是最常用的方法之一、稳定剂可以降低颗粒或液滴之间的吸引力,从而有效地抑制聚集的发生。
常见的稳定剂包括表面活性剂、胶体保护剂和电解质等。
表面活性剂是一类能够吸附在颗粒或液滴表面的物质,通过形成电荷屏障或分散剂层来降低吸引力,从而使颗粒或液滴保持分散状态。
胶体保护剂是一类能够与颗粒或液滴表面发生化学反应的物质,形成一层稳定的保护膜来防止聚集的发生。
电解质可以通过改变胶体系统中的离子浓度,从而改变颗粒或液滴表面的电荷性质,进而影响吸引力的大小。
控制环境条件也是维持胶体稳定性的重要方法之一、环境条件的改变可以直接影响颗粒间的吸引力和分散力之间的平衡。
例如,温度的变化会改变胶体中颗粒或液滴的热运动速度,从而影响颗粒之间的碰撞频率和能量大小。
pH值的变化则会改变胶体中颗粒或液滴的表面电荷,进而影响吸引力的大小。
通过控制环境条件,我们可以调节各种力的平衡,从而更好地维持胶体的稳定性。
此外,调节胶体粒径也是维持胶体稳定性的一种方法。
胶体粒径的大小直接影响胶体中颗粒或液滴之间的相互作用力。
第五章胶体和胶体的稳定性

胶原纤维截面也是纳米级别的
这些物质含有巨大的表面积,具有双电层结构,在性质上有何胶体类似的性质。
1.4 溶胶的制备
(1)分散法 研磨法 是用胶体磨把大颗粒固体磨细,在
研磨的同时加入丹宁或明胶做稳定剂。工业用 的胶体石墨、颜料、医用硫溶胶等都是用胶体 磨磨制成的。
胶溶法 是一种使暂时凝集起来的分散相又 重新分散的方法。把新生成的沉淀洗涤后,加 入稳定剂,经过搅拌,沉淀就重新分散而形成 溶胶。
胶体及胶体的稳定性
? 胶体定义和分类 ? 胶体特性 ? 胶体稳定性的影响因素
1.1胶体
悬浊液、乳浊液 (分散质粒子大于 100nm) 分散系 溶液(分散质粒子小于 1nm)
胶体(分散质粒子在 1nm--100nm 之间)
1.2 胶体的分类
1、胶体的外观:类似于溶液,多数均一、透明 2、胶体分散质的构成:
1)胶团之间既存在斥力势能,也存在引力势能。 其来源可从其结构得到解释。
胶核
B
扩散层边界
左图中是两个带正电荷 的胶团。在胶团外之任一 点A处,则不受正电荷影 响;在扩散层内任一点B, 因正电荷作用未被完全抵 消,仍表现出正电性。但 当两个胶团扩散层未重叠B
扩散层边界
当两个胶团扩散层发生重叠 时,重叠区内负离子浓度增加。 两个胶团扩散层对称性都受到 破坏。使重叠区内过剩负离子 向未重叠区扩散。导致渗透性 斥力的产生。由于双电层的静 电平衡破坏,导致两个胶团间 产生静电斥力。随着重叠区的 加大,这两种斥力势能都增加。
例如,对于给定的溶胶,异电性离子分别为一、 二、三价,则聚沉值的比例为:
100 ? 1.6 ? 0.14
即为:
?1 ??1
6
? ??
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
2019/11/21
7
3 溶胶相互作用聚沉
两种相反电荷的胶体混合会发生聚沉,但这种聚沉必需在 混合数量达到一定比例才能发生,否则不发生或聚沉不完 全。如明矾净化水、医院用血液能否相互凝结来判断血型 等。
当x缩小,先出现一 极小值F,则发生粒子的
Born排斥 {U}
聚集称为絮凝(可逆的)。
UR ∝exp{-x} —德拜参量
Umax
当x再缩小,则出 现极大值Umax。只有两
胶粒通过热运动积聚的
动能超过15kT时才有可
能超此能量值,进而
出现极小值C,在此处
势垒
U
0
F
{x}
C
第一极小
UA∝
1 x
第二极小
2019/11/21
8
§5.2 溶胶稳定理论
1. DLVO理论
20 世 纪 40 年 代 初 , 由 德 查 金 (Darjaguin) 、 朗 道 (Landau) 和 维 韦 (Verwey) 、 奥 弗 比 可 (Overbeek)提出的理论,要点如下:
在胶粒之间,存在着两种相反作用力所产生的势能。
2e2Lcz 2 1/2
(
)
kT
CCCC
9.75B2 3kB5T 5 4
可见,聚沉能力是聚沉值的倒数,即聚沉值愈小,该电解质 的聚沉能力就愈大;反之,聚沉值越小的电解质,其聚沉能力 越强。
2019/11/21
4
(1)电解质中与胶粒所带电荷相反的离子是其主要聚沉作用 的离子,并且离子价数越高,电解质的聚沉能力越大。
对某一给定溶胶,一、二、三价反离子聚沉值的比例大约是:
100 :1.6 : 0.14
12 H
0
dU dH
U R
UA H
0
即 H U A 1
UR
因此:
BkB2T 2a 2
z2
exp[ 1]
Aa
12
0
2019/11/21
4.415 BkB2T 2 2
14
Az 2
对胶粒而言, 0 ,相当于Debye Huckel离子氛厚度为:
下顺序:
F- > IO3- > BrO3- > Cl- > Br- > NO3-> I- > 这种次C序N称S为- 感胶离子序(lyotropic series)。反离子的水
化半径越大,越不易被质点吸附,聚沉能力也就越弱,因此这 类顺序与离子水化半径由小到大的次序大致相同。
2019/11/21
6
(3)有机化合物的离子都有很强的聚沉能力,这是由于有 机离子具有较强的van der Waals力来吸引胶粒,致使发 生聚沉,特别是一些高分子絮凝剂的表面活性物质及聚酰 胺类化合物。
斥力势能UR —— 由扩散双电层相互重叠时而产生。
吸力势能UA —— 另一是由分子存在的远程v·d·W力而产生。
2019/11/21
9
UA
Aa 12x
A:为 Hameaker常 a: 为粒子半
径
A
( A111/ 2
A1/ 2 22
)2
A11、A22分别为粒子和介质的Hameaker
表明:介质的存在减小了颗粒间的引力,且介质
2019/11/21
1
1 电解质影响溶胶稳定性的本质
电解质对溶胶的稳定性影响很大,这是由于随着电解质 的加入,可以使更多的反离子进入双电层的紧密层内,导 致 电势降低,并使扩散层变薄,因此少量的电解质加入, 就可引起溶胶的聚沉。
有时,胶粒表面可以对外加电解质的反离子产生强烈
吸附,导致紧密层中含有过剩的反离子,迫使 电势变
发生粒子间的聚沉(不
可逆)。
图 胶粒间斥力势能、吸力
2019/11/21
12
势能及总势能曲线
2019/11/21
13
2. DLVO对CCCC ∝ 1 / Z6 解释:
根据以上讨论可以知道,当电解质在溶胶中达到临 界聚沉浓度时:
U
UR
UA
BkB2T 2a 2
z2
exp[ H ] Aa
亦即
1 :1 :1 16 26 36
这一聚沉值与起聚沉作用的离子价数的六次方成反比的 规律被称之为Schulze-Hardy规则。
2019/11/21
5
(2)具有价数相同的离子,它们的聚沉能力也不相同。
相同价数的阳离子聚沉带负电荷的溶胶时,聚沉能力有如 下顺序:
相同价数H>的+阴L>i离+ C子s聚+ 沉>带R正b+电>荷N的H溶4胶+时>,K+聚>沉N能a力+有如
2kT
exp( Ze0 ) 1
2kT
B:常数; :介电常数;Z:分散离子价数 ; :复合比
20(1c9/o11/m21 plex ration) ; kB :波尔滋曼常数
11
U=UR+ UA即系统的总势能,U的变化决定着系统的稳 定性。UR, UA及U均是胶粒之间的距离x的函数,如图所示。
性质与颗粒性质越接近,颗粒将引力越弱,胶体
越稳定
2019/11/21
10
重叠区离子浓度较大,破坏了原来电荷平衡分布的对 称性,引起重新分布,即向未重叠区扩散,使带正电的 胶粒受到斥力而相互脱离。
UR:按双电层理论,重叠程度越大,斥力越大
UR
BkB2Ta
Z2
2
exp[ kx]
exp( Ze0 ) 1
§5.1 电解质聚沉作用(coagulation)
溶胶粒子有着剧烈的Brown运动,这使它能保持相当长 时间的相对稳定,因此溶胶具有动力稳定性。
胶体分散体系是热力学的不稳定体系,其中的溶胶粒 子能自动合并变大而自发地下沉,这种过程称为聚沉,所 以说溶胶又具有聚结不稳定性。
实验表明:在溶胶加入电解质、使带不同电性的胶体相 互混合、加热、辐射、光照射等都能引起聚沉。这里主要 讨论电解质对溶胶的聚沉作用。
号,在这种情况下,溶胶反而不能聚沉,但胶粒的电性
与原来的相反。
2019/11/21
2
+
A
=0时称为等
点状态
电 势
ζ2 0
ζ1 ζ 3 表面距离
B -
电解质对电位的影响曲线
2019/11/21
3
2. 聚沉值
利用聚沉值可以比较各种电解质对某一溶胶的聚沉能力。聚 沉值是指在一定条件下,刚刚引起某溶胶明显开始聚沉时所需 电解质的最小浓度(以mmol•dm-3表示)。 聚沉值又称临界凝集浓度(缩写成CCC,critical coagulation concentration)。
