电极电势和电池的电动势
化学反应中的电极电势与电池电动势实例

化学反应中的电极电势与电池电动势实例在化学反应中,电极电势和电池电动势是两个重要的概念。
电极电势指的是在电化学反应中,电极与溶液中某种溶质之间建立的电势差。
而电池电动势则是指整个电池中两个电极之间的电势差。
本文将结合实例介绍化学反应中的电极电势与电池电动势的概念与相关原理。
实例一:铜与铁电池在铜与铁电池中,铜离子是从铜电极溶解产生的,这个反应可以表示为:Cu(s) → Cu²⁺(aq) + 2e⁻而在铁电极上,则是铁离子发生还原反应:Fe²⁺(aq) + 2e⁻ → Fe(s)根据这两个半反应的标准电极电势可以计算出它们之间的电势差。
在标准状态下,铜电极的标准电极电势为+0.34V,而铁电极的标准电极电势为-0.44V。
所以,在这个铜与铁电池中,电池电动势可以计算为:Ecell = E(铜) - E(铁) = +(0.34V) - (-0.44V) = +0.78V这个正值表示铜与铁电池是一个可行的电池反应,并且产生正向的电势差。
这意味着当铜与铁电池连接成电路时,电子会从铁电极流向铜电极,而离子则会在溶液中迁移,从而产生电流。
实例二:锌与铜电池在锌与铜电池中,锌离子会溶解,并且金属锌会被氧化为锌离子,这个反应可以表示为:Zn(s) → Zn²⁺(aq) + 2e⁻与之相对应的是铜电极上的还原反应:Cu²⁺(aq) + 2e⁻ → Cu(s)通过比较这两个半反应的标准电极电势,可以计算出锌与铜电池的电动势。
在标准状态下,锌电极的标准电极电势为-0.76V,而铜电极的标准电极电势为+0.34V。
因此,锌与铜电池的电动势可以计算为:Ecell = E(锌) - E(铜) = (-0.76V) - (+0.34V) = -1.1V这个负值表示锌与铜电池是一个不可行的电池反应,不能产生正向的电势差。
因此,在锌与铜电池中,电子从铜电极流向锌电极,但离子却会在溶液中迁移,从而产生反向的电流。
电极势与电池电动势之间的关系

电极势与电池电动势之间的关系电极势是指在电池中两个电极上的电势差,即正极与负极之间的电位差。
而电池电动势则是指电池在无负载情况下产生的电压。
电极势和电池电动势之间存在着密切的关系。
首先,我们来了解一下电极势。
电极势是由电池内部的化学反应引起的,在电池内完成氧化还原反应的正极和负极上会形成电势差。
对于一般的电池,正极电势相对于负极电势更高,从而形成了电势差。
这个差值正好等于电池电动势。
电池电动势是指在没有负载时,电池正负极之间产生的电压。
正常情况下,正极的势高于负极,形成了一个电势差。
这种电势差是电池内部化学反应所产生的,能够推动电荷在电池中自由流动,从而产生电流。
电池电动势通常以伏特(V)为单位。
电极势和电池电动势之间的关系可以用下式来表示:电池电动势 = 正极电势 - 负极电势根据这个关系,我们可以看出电池电动势的大小取决于正极和负极电势的差值。
如果正极电势和负极电势之间的差值越大,那么电池电动势就会越大。
相反,如果差值较小,电池电动势也会相应地减小。
正常情况下,电池的电动势是一个恒定的值。
然而,在实际应用中,电池的电动势往往会随着使用时间的增加而降低。
这是因为电池内部的化学反应会导致电极材料的消耗和损耗,从而使得正极和负极之间的电势差减小。
最后,还需要注意的是,电极势和电池电动势是两个不同的概念。
电极势是针对单个电极来讨论的,而电池电动势是针对整个电池来讨论的。
在一个完整的电池中,正极和负极之间形成的电势差就是电池电动势。
总结起来,电极势和电池电动势之间有着密切的关系。
电池电动势是由正极和负极之间的电势差引起的,而这个差值可以被称为电极势。
电极势和电池电动势的大小取决于正极和负极之间的电势差。
通过研究和了解这个关系,我们能够更好地理解电池的工作原理,并有效地应用于各种电子设备和能源系统中。
化学反应中的电极电势与电池电动势

化学反应中的电极电势与电池电动势化学反应是一种涉及原子和分子之间重组的过程,而电池则是利用化学反应产生电能的装置。
电极电势和电池电动势是描述电化学反应中电子转移能力的重要参数。
本文将介绍电极电势和电池电动势的概念、影响因素以及它们之间的关系。
一、电极电势的概念与测量电极电势是指电极与溶液或气体之间的电势差。
在电化学反应中,电极上电子的转移产生电势差,进而影响反应的进行。
电极电势能够反映电子在电极上的活动程度,是判断电极是氧化还是还原的参数。
电极电势通常用标准电极电势(E°)来表示,单位为伏特(V)。
测量电极电势的方法有很多种,其中最常用的方法是通过比较电池。
比较电池由两个半电池组成,可以产生一个已知电势差的电池。
通过将待测电极与比较电池相连,测量它们之间的电势差,从而确定待测电极的电势差。
二、电极电势的影响因素1. 温度:电极电势随温度的变化而变化。
温度升高会导致电极电势升高或降低,具体取决于反应的热力学性质。
2. 浓度:电极电势与参与反应的物质浓度有关。
当参与反应的物质浓度发生改变时,电极电势也会发生变化。
3. 压力:对于气体电极,电极电势随气体的分压变化而变化。
增大气体分压会导致电极电势升高。
4. pH 值:对于溶液电极,电极电势会受到 pH 值的影响。
改变溶液pH 值能够改变电极电势。
三、电池电动势的概念与计算电池电动势是指电池两个电极之间的电势差,表征了电化学反应产生的电能。
电池电动势通常用电池电动势(Ecell)来表示,单位为伏特(V)。
计算电池电动势的方法是通过测量两个电极的电极电势,并利用Nernst 方程进行计算。
Nernst 方程是描述电极电势与反应物浓度之间关系的数学方程。
Ecell = E°cell - (RT/nF)ln(Q)其中,E°cell 是标准电动势,R 是气体常数,T 是温度,n 是电子转移的摩尔数,F 是法拉第常数,Q 是反应物的活度积。
电动势和电极电势的关系

电动势和电极电势的关系
电动势和电极电势是电学中两个重要的概念,它们之间存在着密切的
关系。
电动势是指单位正电荷在电路中沿闭合回路移动时所获得的能量,通常用符号ε表示,单位是伏特(V)。
而电极电势则是指电池两极之间的电势差,通常用符号E表示,单位也是伏特(V)。
在电学中,电动势和电极电势的关系可以用基尔霍夫第二定律来描述。
基尔霍夫第二定律指出,在任意一个闭合回路中,电动势之和等于电
势降之和。
也就是说,电动势是电路中各个电池的电极电势之和。
具体来说,假设一个电路中有n个电池,它们的电极电势分别为E1、
E2、E3……En,那么电路中的电动势ε就可以表示为:
ε = E1 + E2 + E3 + …… + En
这个公式表明,电动势是由电路中各个电池的电极电势共同作用而产
生的。
因此,如果我们想要提高电路中的电动势,就需要增加电池的
数量或者提高每个电池的电极电势。
另外,电动势和电极电势还有一个重要的区别。
电动势是一个电源的
特性,它代表了电源的输出能力。
而电极电势则是一个电池的特性,
它代表了电池内部化学反应的能力。
因此,电动势和电极电势在物理意义上是不同的,不能混淆使用。
总之,电动势和电极电势是电学中两个重要的概念,它们之间存在着密切的关系。
电动势是由电路中各个电池的电极电势共同作用而产生的,它代表了电源的输出能力。
而电极电势则是一个电池的特性,它代表了电池内部化学反应的能力。
了解它们之间的关系,可以帮助我们更好地理解电路中的电学现象,为电路的设计和优化提供指导。
平衡电极电势和电池电动势解读课件

比较不同电极的氧化还原能力
不同电极的平衡电极电势不同,可以根据其相对 大小比较不同电极的氧化还原能力。
04
电池电动势
定义和计算
电池电动势是指电池正负极之间的电势 差,通常用符号E表示。
电池电动势可以通过测量电池在不同状 态下的开路电压来确定。
通过比较不同电极材料和不同溶液浓 度下的平衡电极电势,可以评估电池 在不同条件下的性能。
存在的问题和改进方向
平衡电极电势和电池电动势的 测量结果容易受到实验条件和 环境因素的影响,需要严格控 制实验条件以获得准确结果。
对于某些电极材料和电池体系 ,平衡电极电势和电池电动势 的测量可能需要更复杂的实验
最后将两个电极反应式合并,得到电池总反应式。
06
实验方法和数据分析
实验方法
01
02
03
04
选择合适的电解质和电 极材料。
组装电池并确保良好的 电气连接。
记录电流、电压等实验 数据。
电池在不同温度下的测 试。
数据处理和分析
01
02
03
04
电流和电压的测量与记录。
计算电极电势和电池电动势。
分析实验数据,如绘制极化曲 线等。
平衡电极电势和电池电 动势的关系
Nernst方程
Nernst方程是一种描述电池电动势和各物质浓度的关系式。
它可以将电池反应的化学能转化为电能,从而直观地反映电池的工作原 理。
Nernst方程通常表示为E=E0-(RT/nF)ln(Redox),其中E为电池电动势, E0为标准电极电势,R为气体常数,T为绝对温度,n为电荷转移数,F为 法拉第常数,ln为自然对数,Redox为氧化还原反应的浓度。
电极电势与电池电动势

第3章 电极电势与电池电动势
8
3.1.2 胶体双电层
❖ 当给胶体溶液通直流电时,可以看到胶粒 向某一电极移动,这种现象就叫电泳。说 明胶体粒子是带电的,其原因如下:
a. 因吸附其它离子而带电。胶核优先吸附与 其有相同化学元素的离子;
b. 因电离作用而使胶粒带电。有些胶粒与分 散介质接触时,会发生电离,使一种离子 进入液相,而本身带电。
散分布在吸附层外围。
2020/5/13
第3章 电极电势与电池电动势
10
❖ 胶核和吸附层构成胶粒;
❖ 胶粒和扩散层形成的整体为胶团。
❖ 胶团是电中性的,而胶粒是带电的。
❖ 胶团分散于液体中便是
溶胶。
❖ 在外电场(如通直流电)
作用下,胶团会从吸附
层与扩散层之间分离,
形成带电荷的胶粒而发
生电泳现象。
2020/5/13
20
3.2.2 电池电动势的组成
❖ 电池电动势E 电池正、负极之间的电势差称为电池 电势,在开路下测得的电池电势称为电池电动势。
2020/5/13
第3章 电极电势与电池电动势
12
3.1.4 液体接界电势及其消除
❖ 液体接界电势 又称扩散电势,表示在两种不同的 溶液(电解质不同,或电解质相同而浓度不同)的界 面上存在的电势差。
2020/5/13
第3章 电极电势与电池电动势
13
❖ 液体接界电势是由溶液中离子扩散速度不同引起 的,它的电势一般较小,不超过40mV。
❖ 盐桥可降低液接电势,但不能完全消除,一般在
2020/5/113~2mV.
第3章 电极电势与电池电动势
15
❖ 盐桥消除液接电势的原理如下图所示
2020/5/13
电池电动势与电极电势

电极电势的计算方法
Nernst方程
电极电势可以通过Nernst方程计算,该方程描述了电极电势与溶液中离子浓度 的关系。
线性关系
电极电势与反应物和产物的浓度之间存在线性关系,可以利用这一关系求出电 极电势。
影响电极电势的因素
物质性质
电极电势与参与反应的物质性质有关,如氧化还原能力、离子迁 移率等。
温度
温度对电极电势产生影响,温度升高会导致电极电势降低。
物质浓度
参与反应的物质浓度也会影响电极电势,浓度变化会导致电极电 势相应发生变化。
03 电池电动势与电极电势的 关系
电动势与电极电势的差异
定义不同
电池电动势是指电池在开路状态 下正负极之间的电位差,而电极 电势是指电极与其周围溶液之间
的电位差。
决定电池性能
电池电动势和电极电势共同决定了电池的性能,如能量密度、功率 密度、充放电效率等。
平衡状态
在一定条件下,电池电动势和电极电势可以达到平衡状态,此时电 池性能达到最优。
电动势与电极电势在实际应用中的重要性
1 2
能源存储
电池电动势和电极电势是决定电池能量存储和释 放的关键因素,对于电动汽车、移动设备等领域 具有重要意义。
电池电动势与电极电势
目录
• 电池电动势 • 电极电势 • 电池电动势与电极电势的关系 • 电化学反应与电极过程 • 电池性能的优化与改进
01 电池电动势
定义与性质
定义
电池电动势是指在标准温度和压 力下,电池正负极之间的电势差 。
性质
电池电动势是衡量电池能量转换 效率的重要参数,具有方向性, 即电流从正极流向负极。
电极反应的可逆性
可逆电极反应在正向和逆向反应中均能进行, 且正向和逆向反应速率相等。
平衡电极电势和电池电动势

= (待测)
例:H2(g,p0)│H+(aq, a+=1)‖Cu2+(aq, aCu)│Cu
(C u 2 /C u ) EIfE > 0 , (C u 2 /C u )> 0 E < 0 , (C u 2 /C u )< 0
饱和甘汞电极示意图
E= (待测)- 0 (H+/H2) = (待测)-0
RT 1 RT 1 ⑴第一类电极(这类电极一般只有一个相界面o )
( 2F ln a ) ( 2F ln a ) 金⑵镀属第铂与 二 黑其类的阳电铂离极片子浸(存组入在成a两H的+个=电1相的极界溶面液)中并以pH2C=u1p2的纯氢气不断冲击到CuPt2电 (极a2上)。
⑵第二类电极(存在两个相界面)
电池电动势等于两个电极电势的差值。
电
池:Zn(s)|Zn2+||Cu2+|Cu(s)
⑵第二类电极(存在两个相界面)
以标准氢电极作氧化极,即负极;
⑴第一类电极(这类电极一般只有一个相界面)
以标准氢电极作氧化极,即负极;
实验只能测得两个电极构成的电池的电动势E,而无法测得单独电极的电极电势 。
§4 平衡电极电势和电池电动势
• 电池电动势等于两个电极电势的差值。
• 实验只能测得两个电极构成的电池的电动势 E,而无法测得单独电极的电极电势。
• 若选定一个电极作为标准,使其与任意其它 电极组成电池,测其电动势,就可得出各电
极的相对电极电势。
• 利用两电极的相对电极电势,可以方便的求
得由它们组成的电池的电动势,E= +--。
标准氢电极
镀铂黑的铂片浸入 aH+=1的溶液中并以 pH2=1p o 的纯氢气不断 冲击到Pt电极上。
无机化学-电池电动势和电极电势
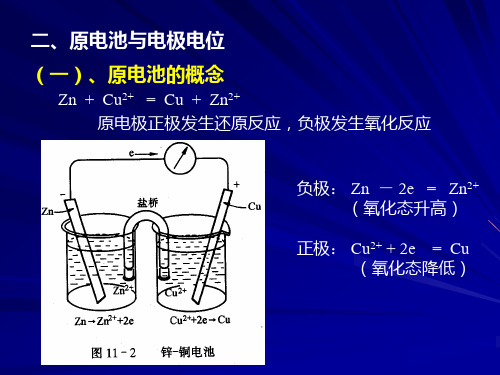
标准甘汞电极(NCE) 1.0 mol / L +0.2828
饱和甘汞电极(SCE) 饱和溶液 +0.2438
温度校正,对于SCE,t ℃时的电极电势为:
t= 0.2438- 7.6×10-4(t-25) (V)
电池符号: (-) Hg,Hg2Cl2(s)︱KCl (1 mol·dm-3) Mn+ (1 mol·dm-3 ) M (+)
氧化半反应: H2 - 2e = 2H+ 还原半反应: Cl2 + 2 e = 2Cl– 总反应: H2 + Cl2 = 2H+ + 2Cl–
2. 题中给出总反应方程式,要能够写出电池符号和半反应
例题:试以中和反应 H+ (aq) + OH–(aq) = H2O(l)为电池反应, 设计成一种原电池反应(用电池符号表示),分别写出电极半 反应,并求出它在25℃时的标准电动势。
二、原电池与电极电位 (一)、原电池的概念
Zn + Cu2+ = Cu + Zn2+ 原电极正极发生还原反应,负极发生氧化反应
负极: Zn - 2e = Zn2+ (氧化态升高)
正极: Cu2+ + 2e = Cu (氧化态降低)
盐桥(Salt bridge)
通常内盛饱和 KCl 溶液或 NH4NO3 溶液(以琼胶 作成冻胶)。
作用: ● 让溶液始终保持电中性 ,使电极反应得以继续进行 ● 消除原电池中的液接电势(或扩散电势)
(二)、原电池的表达式
(-) Zn|Zn2+ (C1) ‖ Cu2+ (C2)|Cu (+)
1、负极写在左边,正极写在右边 2、用∣表示电极与离子溶液之间的物相界面 3、不存在相界面,用,分开。 4、用表示盐桥 5、在有气体参加的电池中还要表明气的压力,溶液要表 明浓度。
电极电势和电池的电动势

E Ox|Red (R ) Ox|Red (L)
电池电动势的计算
Zn(s)|Zn 2 (aZn 2 )||Cu 2 (aCu 2 )|Cu(s)
( ) Zn(s) Zn 2 (a Zn 2 ) 2e
( ) Cu 2 (aCu 2 ) 2e Cu(s)
Ox|Red
RT zF
ln a
B
这是计算电极还原电极电势的 Nernst 方程
电极电势计算通式
例如有电极
Cl ( aCl )|AgCl(s)|Ag(s)
电极的还原反应为
AgCl(s) e Ag(s)+Cl ( aCl )
电极电势的计算式为
Cl |AgCl|Ag Cl |AgCl|Ag
10月31日交第八章和第九章作业
第九周(10月31日)期中考试
• • • • 方式:随堂闭卷笔试 时间:60min 范围:第八章和第九章 题型:单选(15题,30分),判断(10题, 20分),简答(3题,30分),计算(1题 20分) • 难度:单选和判断难度中等;简答和计算题 难度低于教材的思考题和习题。全卷以教材 的基本概念和理论为主。
电池电动势的计算
r Gm (1) 2 E1 F r Gm (2) 2 E2 F E1 Cu 2|Cu(s ) E2 Zn 2|Zn(s )
r Gm (3) 2 E1 F ( 2 E2 F ) 2 E3 F
E3 E1 E 2 Cu 2|Cu(s ) Zn 2|Zn(s )
标准氢电极 || 给定电极
K | K(s) Ca 2 | Ca(s) Al 3 | Al(s) Zn 2 | Zn(s) Pb
普通化学课件4.2电极电势与电池电动势32页PPT

斯特方程:
nF
25℃时,
EE 0.059l2gQ n
Eθ—原电池标准电动势,即两电极 各物质处于标准态时电极电势差值。
Eθ= Eθ(+)- Eθ(-)
(2)影响电极电势的因素——能斯特方程
对于电极电势来说,也有能斯特方程,只不过两者区别在于
E与E(Ox/Red) ,前者为原电池电动势,后者为电极电势。
(Ag
/
Ag)
0.0592V
lg
Ksp c(Cl ) /
c
1.61010
0.80V 0.0592V lg
0.22V
1.0
E(AgCl/ Ag)
由于氧化型(Ag+)浓度大大减小,E降低。氧化能力降低
比较下列电极电势的高低
(1) E(AgCl/Ag), E(AgBr/Ag) E(AgI/Ag) (2) E(Cu2+/CuI), E(Cu2+/CuBr), E(Cu2+/CuCl)
将原电池反应改为电极反应,但不管正负极均按得电子的还 原反应来写:
对于电极反应:
还原反应
a Ox + ne → bRed E (Ox/Red)
有: E (Ox) /E R (O ex d ) /2 .R 3 nR 0 e F l3 T d g [[c c ((R O ))//e c c x ]]a d b
(2)E+
E( HgO
/ Hg)
0.0592 V 2
lg
1 (OH -)2
E-
E( ZnO
/
Zn)
0.0592 V 2
lg
1 (OH - )2
E=E+-E E( HgO / Hg)-E( ZnO / Zn) E 对于固定的电极在一定 条件下为定值,
电极电势与电池电动势

Zn2+ Cd
+ Zn2++Cd
+ + ④ 氧化还原电极 Pt │Fe 3+,Fe 2+
用金属Pt作惰性电极,电极可表示为: 用金属 作惰性电极,电极可表示为: 作惰性电极
+ + Pt │ Fe 3+,Fe 2+、Pt,H2 │ H+、 ,
Pt,Cl2 │ Cl-等,金属及其难溶盐。 , 金属及其难溶盐。 例如AgCl/Ag,其电极组成为, 例如 ,其电极组成为, Ag │ AgCl,Cl,
盐桥两边分别为2个半电池( 盐桥两边分别为 个半电池(即两 个半电池 个电极), ),每个电极反应包括两类物 个电极),每个电极反应包括两类物 一类是可作还原剂(处于低价态) 质,一类是可作还原剂(处于低价态) 的物质,叫做还原态(或还原型)物 的物质,叫做还原态(或还原型) 另一类是可作氧化剂( 质;另一类是可作氧化剂(处于高价 的物质,叫做氧化态(或氧化型) 态)的物质,叫做氧化态(或氧化型) 物质。两者关系可表示如下: 物质。两者关系可表示如下: 氧化态+ 氧化态+ne ⇌还原型
(2)表中所列标准电极电势的数值和符 ) 不因电极反应的书写方式而改变。 号,不因电极反应的书写方式而改变。 例如, 例如,不管电极反应是按
+ Zn2++2e
Zn还是 -2e 还是Zn- 还是
+ Zn2+
进行,该电对的标准电极电势都是- 进行,该电对的标准电极电势都是- 0.7628V
(3)电极的标准电极电势是强度性质, )电极的标准电极电势是强度性质, 没有加合性, 没有加合性,其数值与反应系数 +为例, 无关。以电对Fe + 无关。以电对 3+/Fe2+为例, 不管是Fe + 不管是 3++e
在极板上
溶解 沉积
Mn+(aq)+ne在溶液中 留于极板上
电极电势与电池电动势的计算

电极电势与电池电动势的计算电极电势(Electrode Potential)和电池电动势(Cell EMF)是研究电化学中极其重要的概念。
本文将对这两个概念进行详细的解释,并介绍相关的计算方法。
一、电极电势电极电势是指一个半电池电极与标准氢电极之间的电势差。
标准氢电极的电极电势被定义为0V。
电极电势通过协调氧化还原反应中的电子转移来衡量化学反应的方向和程度。
确定电极电势的方法有两种:1.标准电极电势法:以标准氢电极为参考,通过将待测电极与标准氢电极连接,通过电桥测得两个电极之间的电势差,就可以计算出待测电极的电极电势。
标准电极电势的计算公式如下:E°(待测电极)=E°(标准氢电极)-ΔE°(待测电极)其中,ΔE°(待测电极)为待测电极中的氧化还原反应的标准电极电势。
2.直接电位法:直接电位法通过将待测电极与参比电极连在一起,由两个电势计测得不同电极之间的电势差,从而计算出待测电极的电极电势。
二、电池电动势电池电动势是指一个完整电池的两个电极之间的电势差。
它是衡量一个电池输出电能的能力。
电池电动势等于正极电极电势减去负极电极电势。
计算电池电动势的方法也有两种:1.离子数法:这种方法通过计算反应中再配位离子的数目来确定电池电动势。
计算公式如下:E°(电池)=E°(正极)-E°(负极)其中,E°(正极)和E°(负极)分别为电池阳极和阴极的标准电极电势。
2.直接电动势法:直接电动势法通过直接测量电池两个电极之间的电势差来确定电池电动势。
三、实例计算下面以铜/银电池(Copper/Silver Battery)为例来进行具体计算:铜电极的标准电极电势为0.34V,银电极的标准电极电势为0.80V。
根据离子数法,铜/银电池的电动势可以通过计算两个电极的电势差来得到:E°(电池)=E°(铜)-E°(银)=0.34V-0.80V=-0.46V根据直接电动势法,可以直接测量铜/银电池的电动势,从而得到电池电动势的准确数值。
电动势和电极电势的关系

电动势和电极电势的关系引言电动势和电极电势是电学领域中重要的概念,它们与电路中的电流、电压息息相关。
理解电动势和电极电势的关系对于理解电学原理和解决实际电路问题至关重要。
本文将深入探讨电动势和电极电势的概念、性质以及它们的关系。
电动势电动势是指电源向电路提供能量的能力。
它是电压源的重要性质,通常表示为E。
单位是伏特(V)。
在闭合电路中,电源通过内部的化学、物理过程将其他形式的能量转化为电能,并将电荷推动从低电位端流向高电位端。
这个推动电荷的能力就是电动势。
电动势的大小不取决于电路中物质的特性,而是取决于电源本身。
例如,相同电源电动势的电流大小可以在不同电路中有所不同。
而电源的电动势则是一个恒定的量,与电流的大小无关。
电动势可以理解为电路中电能来源的一种度量。
它提供了流动电流所需的推动力,就像水从高处流向低处一样。
电动势的方向从正极指向负极。
电极电势电极电势指的是电池电势两极之间的差异。
它是电池内化学反应所提供的电势差,用于推动电流流动。
电池的电极电势由化学反应产生,并通过电池的两个极端形成电势差。
电池的正极具有较高的电极电势,而负极具有较低的电极电势。
这种电势差使得正极产生多余的电子,而负极则缺少电子。
当电路闭合,电子将从负极流向正极,以平衡电子的不平衡分布,从而形成电流。
电动势与电极电势的关系电动势和电极电势之间存在密切的关系,可以通过以下方程来描述:电动势E = 电极电势V1 - 电极电势V2其中,V1为电池的正极电势,V2为电池的负极电势。
这个方程表明,电动势是由电池的两个极端的电极电势之差所决定的。
也就是说,电动势是电池提供给电路的能量大小的度量。
当电池的两个极端的电势一致时,电动势为零,电流不会流动。
只有当两个极端的电势差存在时,才会产生电动势,电流才能流经电路。
应用实例1. 串联电池考虑一个由两个电池串联而成的电路。
第一个电池的电动势为E1,电极电势分别为V1+和V1-;第二个电池的电动势为E2,电极电势分别为V2+和V2-。
4.2 电极电势与电池电动势解读
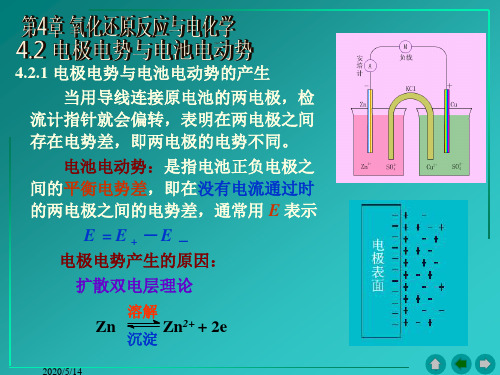
(2)浓 差电池
下一节
浓度对电池电动势的影响 Au(s) 与 Cl2(g) 在水溶液中的反应方程 式为:2Au + 3Cl2 2Au3+ + 6Cl-
试问: 1) 标准态条件下正向反应能否发生?
2) 若与纯金相接触的 AuCl3 浓度为 1.0×10-3mol· dm-3,Cl2的分压是 1×105 Pa, 正向反应能否发生?
4.2.1 电极电势与电池电动势的产生 当用导线连接原电池的两电极,检 流计指针就会偏转,表明在两电极之间 存在电势差,即两电极的电势不同。 电池电动势:是指电池正负电极之 间的平衡电势差,即在没有电流通过时 的两电极之间的电势差,通常用 E 表示 E = E +- E - 电极电势产生的原因: 扩散双电层理论 Zn
解:
ClO 6H 6e 3
Cl 3H2O
E (ClO 3 / Cl)
6 c ( ClO ) c (H ) 0.0592V θ 3 EA (ClO 3 / Cl) lg 6 c(Cl )
0.0592V 1.45V lg10.06 1.51V 6
0.0592 [c(Ox ) / c ] E (Ox/Red) E (Ox/Red) lg n [c( Red) / c ]b
注意:反应体系中是固体或纯液体时,其浓度视为1。对于气 体组分,用分压代替浓度,并要将分压作标准化处理
(1)电极电动势的影响因素 A、浓度对电极电动势的影响 B、溶液 pH 对电极电动势的影响 C、沉淀的生成对电极电势的影响 D、配合物的生成对电极电势的影响 E、弱电解质的生成对电极电势的影响
例: 已知 E ( Ag / Ag) 0.799V,若在Ag 和Ag 组成的半 电池中 加入NaCl 会产产AgCl (s) ,
电极电势与电池电动势的计算解读

电极电势与电池电动势的计算解读电极电势和电池电动势是电化学中重要的概念,用于描述电化学反应中的电势变化和电能的转化。
它们的计算和解读对于理解电化学反应的机理和性质具有重要意义。
首先,我们来解释电极电势的概念。
电势是一种能量形式,可以理解为单位电荷在电场中所具有的能量。
在电化学反应中,电极是通过将电子转移给或从溶液或电解质中的离子来参与反应的地方。
电极电势是指电极上电子的能量与电荷相对位置的差异,即电荷从电极内部到电极外部或反之所需的能量。
计算电极电势需要使用标准氢电极(SHE)作为参考电极。
标准氢电极的电势被定义为0V。
其他电极的电势可以通过与标准氢电极进行电位差测量来确定。
根据电极电势的正负差异,可以判断电极是否是氧化还是还原,以及其与参考电极之间的电势差,进而推断电化学反应的方向和性质。
电极电势的计算基于如下公式:E = E° - (RT/nF)lnQ其中,E是电极电势,E°是标准电堆电动势,R是气体常量,T是温度,n是反应物的电子数,F是法拉第常数,Q是反应物的反应物的活度。
通过这个公式,我们可以计算电极电势,并了解电极上电子转移的驱动力。
正值的电极电势表示自发反应,即电子从电极内部向外部移动,这种反应称为还原反应。
负值的电极电势表示非自发反应,电子从外部移动到电极内部,这种反应称为氧化反应。
与电极电势相对应的是电池电动势。
电池电动势是指电化学反应在电池中转化为电能的能力,可以通过连接两个电极并测量它们之间的电势差来测量。
电池电动势的正负差异也可以判断电化学反应的方向和性质。
在电池中,正极(或称为阳极)是发生氧化反应的地方,负极(或称为阴极)是发生还原反应的地方。
电池电动势可以通过将正极电势减去负极电势来计算。
相对于电极电势,电池电动势更加稳定,因为它不受电池中各种电化学反应的影响。
电池电动势的计算基于如下公式:Ecell = Ered - Eox其中,Ecell是电池电动势,Ered是还原反应的电极电势, Eox是氧化反应的电极电势。
电极电势与电池电动势的计算

1 电极电势与电池电动势
Emf E右 E左
EmOf E右O E左O
2 根据Nernst 公式计算
0 BB
B
Emf
EmOf
RT zF
ln(
aB B
)
B
E( OOx
ze-
RRed)
EO
RT zF
ln
[Re d] R [Ox] O
2019/8/15
这种类型浓差电池电动势的大小,决定于两个电解质
活度的比值。只有当正极电解质溶液的活度(a2)大于负极 电解质溶液(a1)时,Emf才为正值。放电的效果相当于活度 a2的银离子自发地由高化学势区向低化学势区(活度a1) 转移。
2019/8/15
三 浓差电池电动势的计算(3复合)
3 复合型浓差电池
Na(Hg)(a)|NaCl(a1)|AgCl(s)|Ag(s)—Ag(s)|AgCl(s)|NaCl(a2)|Na(Hg)(a)
0
V
2019/8/15
标准氢电极
标准氢电极
Pt | H2 (p$ ) | H (aH 1)
规定
E$ (H |H2 ) 0
用镀铂黑的金属铂导电
2019/8/15
一 电极电势
(1)铜电极 Cu | Cu2 (a )
Pt | H2( pO ) | H (a 1) || Cu2 (a ) | Cu
Na(Hg) (a1)|Na+ (a)|Na(Hg) (a2)
(a1 > a2)
2019/8/15
三 浓差电池电动势的计算(2双液)
2 双液浓差电池 Ag (s)|AgNO3(a1)‖AgNO3(a2)|Ag (s) a2 >a1
电极电势与电池电动势

电极电势与电池电动势电极电势和电池电动势是电化学中重要的概念,它们贯穿于电学和化学的交叉领域,对于理解电化学反应和电池工作原理具有重要意义。
一、电极电势电极电势是指在电化学反应中,电极与电解质溶液之间的电位差。
电极电势的大小取决于反应物质在电极上的活性和电解质溶液中的离子浓度。
按照惯例,电极电势被定义为标准氢电极与待测电极之间的电位差。
在电池中,一个电极受到氧化反应,被称为氧化电极(或阳极),而另一个电极则进行还原反应,被称为还原电极(或阴极)。
这两个电极之间的电位差即为电极电势。
二、电池电动势电池电动势是指电池在开路状态下的电位差,也可以理解为电池输出电能的能力。
电池中的电荷通过化学反应在电池内部产生电势差,从而驱动电流的流动。
常见的两种电池类型是原电池和电解池。
原电池是一种能将化学能转化为电能的电池,如干电池。
电解池是一种利用外加电源提供能量让非自发反应发生的电池,在这种情况下电动势可以是负值。
三、关系与计算电极电势与电池电动势存在一定的关系。
对于任意一个电池来说,电池电动势等于正极电极电势减去负极电极电势。
也就是说,一个电池的电动势等于其正极电极的电势减去负极电极的电势。
对于某些单质或者物种在标准状态下的电极电势,可以利用标准电极电势表来查找。
标准电极电势表列出了各种物质在标准状态下相对于标准氢电极的电势差。
通过查表,我们可以计算出两个电极的电势差,从而得到电池的电动势。
四、结论与应用电极电势和电池电动势是研究电化学反应和电池性能的重要工具。
了解电极电势和电池电动势可以帮助我们理解电化学反应速率、电流的产生和电池的工作原理。
在实际应用中,电极电势和电池电动势的概念广泛应用于能源领域、锂电池、燃料电池等电化学系统的设计和优化。
通过调节电极材料、电解质浓度等因素,可以改变电极电势和电池电动势,从而提高电池性能和能量转化效率。
综上所述,电极电势和电池电动势是电化学中的重要概念,它们相互关联并共同决定着电池的性能。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
五、电势滴定
基本原理: 随着滴定剂的加入,由于发生化学反应,被测离子的浓度 不断发生变化,指示电极的电位相应发生变化,在 化学计 量点,电位发生突跃.
终点确定: 不受视觉影响,适用于有色溶液、浑浊液的滴定,并可滴 定混合物。
第八节 浓差电池
一、化学电池
凡是电池中物质的总变化涉及的是一化学反应,称 之为化学电池。 1. 无液接的化学电池
Pt|H2(p )|HCl(a=1)|Cl2(p )|Pt 电池反应:H2(p )+ Cl2(p ) HCl(a=1)
2. 用盐桥消除液接界的化学电池 Zn(s)| Zn2+(a1)‖Fe3+(a2),Fe2+(a3)| Pt
电池反应: Zn(s)+ 2Fe3+(a2) Zn2+(a1)+ Fe2+(a3)
二、浓差电池
凡是电池中物质变化的净作用仅仅是由高浓度向低浓 度的扩散,则称之为浓差电池。
浓差电池的标准电动势E =0
组成电池的两个电极液种类或活度相同,而两个电 极的活度或逸度不同(如汞齐电极、气体电极)而组成 的电池,称为单液浓差电池;电极相同,电极反应相同, 只是电极液的浓度(或活度)不同,称为双液浓差电池。
设计电池 Ag (s)|AgNO3 (a1)‖KCl (a2)|AgCl (s)|Ag (s)
,
φAg/Ag 0.7991V
φCl-/AgCl/Ag 0.2224V
E φAgCl/Ag φAg/Ag 0.2224 0.7991 0.5767V
zFE 1 96500 (0.576) ln Ksp RT 8.314 298
二、浓差电池
(一)单液浓差电池
例如,气体电极组成的浓差电池:
Pt|H2(p1)|HCl(m)|H2(p2)|Pt 电极反应
负极反应
H2(p1) 2H+(m)+ 2e
正极反应 总变化
2H(m)+ 2e H2(p2) H2(p1) H2(p2)
E RT ln p2 /p RT ln p1 /p 2F p1 /p 2F p2 /p
Ksp=1.78×1010
四、测定溶液的pH值
参比电极:甘汞电极,银电极 方法:
氢离子可逆的指示电极:玻璃 电极,氢电极,锟-氢锟电极
电池
玻璃电极|待测溶液(aH)‖甘汞电极
两次测量 1.用已知pH值的标准缓冲溶液标定玻璃电极的玻璃 2. 测定未知溶液的pH
pH x
pH s
(Ex Es )F 2.303RT
E左
( AgCl/Ag
H /H2
)
RT F
ln a1
Ag(s) + HCl(a2) H2(p )+ AgCl(s)
E右
( H /H2
) AgCl/Ag
RT F
ln a2
总反应
HCl(a2) HCl(a1)
E总
E左
E右
RT F
ln
a2 a1
第九节 电极电势和电动势的应用
一、判断化学反应方向
Fe3/Fe2 0.771V
Ce4/Ce3 1.61V
ln Ka
zFE RT
1 96500 (1.61 0.771) 8.314 298
Ka 1.561014
三、求难溶盐的活度积
方法:设计电池,查表得两电极的 ,计算出E ,求得Ksp
例 计算难溶盐AgCl在298 K时的活度积。
解:AgCl溶解过程:AgCl(s) Ag+ + Cl
gt;0 正向
E<0 逆向
例 Fe能否将Fe3+还原为Fe2+ ?
反应 电池
Fe + 2Fe3+ 3Fe2+
负 Fe –2e Fe2+ 正 2Fe3+ +2e 2Fe2+
–= –0.4402 V +=0.7710 V
E =1.2112 V
因E >0,正向进行
二、浓差电池
(三)双联浓差电池
两个相同的电池串接在一起,构成双联浓差电池,可
消除液接电势。例如: Pt∣H2(p )∣HCl(a1)∣AgCl(s)∣Ag(s)——Ag (s)∣AgCl(s)∣HCl(a2)∣H2(p )∣Pt
左电池反应 右电池反应
H2(p )+ AgCl(s) Ag(s) + HCl(a1)
二、浓差电池
(二)双液浓差电池 例如,硝酸银浓差电池:
Ag(s)|AgNO3(a1)‖AgNO3(a2)|Ag(s)
电极反应
负极反应 Ag(s) Ag+(a1)+ e
正极反应 Ag+(a2)+ e Ag(s)
总变化
Ag+(a2) Ag+(a1)
E RT ln a1 RT ln a2 F a2 F a1
二、求化学反应的平衡常数
方法:将反应设计为电池,根据电池电动势E 与电池反应
的关系求Ka。用此法还可求出难溶盐的活度积。
RT
ΔrGm zE F RTlnKa
E zF lnKa
例 计算298 K时,反应:Ce4++ Fe2+ Fe3+ + Ce3+的 标准平衡常数。
解: 设计电池
Pt|Fe2+ (a=1), Fe3+ (a=1)‖Ce4+ (a=1), Ce3+ (a=1)|Pt
