j第十章 醇和酚
有机化学课件-醇和酚

醇在清洁用品中的应用
醇是常见的清洁剂成分,用于 去除污垢和杀菌消毒。
比较醇和酚的性质和反应
分子结构 性质 化学性质 应用
醇 含有羟基的碳链 有酒精味 加成、消除、氧化、磺化 清洁剂、溶剂
酚 苯环上有羟基 有特殊香味 亲电取代、缩合、酯化 药物、化妆品
缩合反应类型 酚的烷基化反应 酚的羧酸化反应 酚的醚化反应
反应条件 酚与醇在酸催化下缩合 酚与羧酸在酸催化下缩合 酚与醇在酸催化下缩合
酚的酯化反应
1 定义
酚与酸反应生成酯。
2 反应条件
酚和酸在酸催化下反应。
醇和酚在生活中的应用
醇在化妆品中的应用
醇常用作保湿剂和溶剂,广泛 应用于各种化妆品中。
酚在药物中的应用
有机化学课件-醇和酚
本课件介绍醇和酚的基本概念,包括分子结构、物理性质、化学性质以及在 生活中的应用。我们将深入探讨各种反应,并提供考试中可能出现的相关题 目及解析。
醇与酚的分子结构与化学式
醇
CnH2n+1OH
酚
C6H6O
醇和酚的物理性质
1醇
一般为无色液体或固体,具有特有的酒精味。
2酚
常为无色结晶固体,具有特殊香味。和氧化反应。
2酚
具有芳香性,可进行亲电取代、缩合和酯化反应。
醇和酚的加成反应
1
醇的酸碱反应
与强碱反应生成盐和水。
2
酚的氧化反应
与氧气反应生成酚醛或酚酮。
3
醇和酚的磺化反应
与磺酰氯反应生成磺酸酯。
醇和酚的消除反应
1
酚的缩合反应
2
通过缩合反应,酚可以形成醚。
3
醇和酚

醇酚知识点1 醇和酚的定义(1)醇:是羟基与烃基或苯环侧链上的碳原子相连形成的化合物,或者说醇是烃分子中饱和碳原子上的氢原子被羟基取代后形成的化合物。
(2)酚:羟基与苯环直接相连而形成的化合物称为酚,最简单的酚是苯酚。
易错点津:醇类的羟基必须要烃基或苯环侧链上的碳原子直接相连;酚类的羟基必须是直接与苯环相连。
例1下列物质中,不属于醇类的是A.C3H7OH B.C5H5CH2OH C.C6H5OH D.CH2—CH—OHOH CH3例2 下列物质与互为同系物的是知识点2 醇类概述1.,醇的分类(1)根据分子里的羟基数目分:①一元醇:②二元醇:如:CH2—CH2OH OH③多元醇: 如:CH2—CH—CH2OH OH OH(2)根据醇分子里羟基是否饱和,醇可分为:①饱和醇:②不饱和醇:如:CH2==CH—CH2OH(3)根据醇分子里是否含有苯环,醇可以分为:①脂肪醇②芳香醇:2.常见的醇(1)甲醇(CH3OH)甲醇是一种常见的纯,最初来源于木材的干馏,俗称木精或木醇,是无色透明的液体,甲醇有剧毒,误饮少量可致眼睛失明,多量则可以致人死亡。
甲醇是一种重要的有机化工原料,在能源、工业领域应用广泛。
(2)乙二醇CH2OHCH2OH乙二醇是一种无色、粘稠、有甜味的液体,其水溶液的凝固点很低,可作汽车发动机的抗冻剂,乙二醇主要用于生产聚酯纤维。
(3)丙三醇丙三醇俗称甘油,是无色、粘稠、有甜味的液体,吸湿性强,有护肤作用,是重要的化工原料。
丙三醇与HNO3酯化形成的三硝酸甘油酯,俗称硝酸甘油,是一种烈性炸药。
例3(双选)下列说法中,正确的是A.甲醇、乙二醇、丙三醇互为同系物B.甲醇、乙二醇、丙三醇都易溶于水C.甲醇、乙二醇、丙三醇都有剧毒D.相同质量的甲醇、乙二醇、丙三醇完全燃烧时甲醇耗氧量最大。
例4 (双选)只用水就能鉴别的一组物质是A.苯乙醇四氯化碳B.乙醇乙酸乙烷C.乙二醇甘油溴乙烷D.碳化钙碳酸钙氯化钠知识点3 乙醇的性质(重点)1.乙醇的结构分子式:;结构式:结构简式:。
西北农林科技大学理学院朱玮教授 有机化学教案 第十章 醇和酚

有机合成设计的基本内容是由目标分子经 骨架和官能团的转化得到合成元或中间体。转 化是依据已知或可靠的反应而进行的,由此可 倒推至目标分子所需的起始原料,此过程正好 与合成相反,因此也称为反合成。 同一目标分子可以进行多途径的反合成分 析,因此可推导出不同的合成路线和起始原料 ,形成所谓合成树。再进一步的合成设计工作 是将此合成树进行裁剪,从经济性、有效性以 及灵活性等多方面进行综合考察,然后选定在 实验室中付诸实施的合成计划。
2,4,5-三甲基-3-氯-1-庚醇
OH
Cl
H
(2)饱和脂环醇
H CH3
(1R,2R)-2-甲基环己醇
(3)不饱和醇
CH3C CHCH2CHCH3 CH3 OH
OH
2-环己烯醇
C6H5 H H C C H OH CH3
5-甲基-4-己烯-2-醇 (4)芳香醇
CH2OH
苯甲醇
(1R,2Z)-1-苯基-2-丁烯-1-醇
(1)反应活性 与卤代烷E1反应类似,醇发 生分子内脱水反应的活性次序为: 3°>2°>1°ROH
CH3 CH3 C OH CH2 H 20%H2SO4 85~90℃
(CH3)2C CH2
(2)区域选择性 合Sayrzeff规则。
如果分子中存在2 ~ 3
种可消除的不同β-氢原子,其脱去方式符
66%H2SO4 CH3CH2CHCH3 100℃
δδδ+ δ+ δ+ δ+ δ+ δ+ δδ+ δδδ+ δ δ+ δ- δδ δ+
δ-
RO δ+ δδ+
H3O+ δ- + δ δ+
第十章 醇、酚、醚(alcohols、phenols、ether)

第九章醇和酚(alcohols and phenols)第一节醇的分类和命名R-OH 醇,烃分子中一个(或几个)氢原子被羟基取代后所生成的化合物。
那么是否有含羟基的烃类衍生物都叫醇呢?实际上并非如此。
在芳香化合物中,假如羟基连在支链烷基上,也叫做醇(芳香醇 Aromatic alcohol)如:苯甲醇C6H5CH2OH。
但如果羟基直接连在苯环上就叫做酚(phenol)而不叫做醇。
一.醇的分类二.醇的命名简单的一元醇,根据和羟基相连的烃基名称来命名。
在“醇”字前面加上烃基的名称。
分子较对称的醇常以甲醇衍生物命名。
结构比较复杂的醇,采用系统命名法:即选择含有羟基的最长碳链作为主链,把支链看作取代基,从离羟基最近的一端开始编号,按照主链所含的碳原子数目称为“某醇”,羟基在1位的醇,可省去羟基的位次。
多元醇的命名方法,要选取含有尽可能多的带羟基的碳链作为主链,羟基的数目写在醇字的前面。
用二、三、四等数字表明。
如果分子中除羟基外尚有其他官能团时,需按规定的官能团次序选择最前面的一个官能团作为这个化合物的类名。
其他官能团则作为取代基。
IUPAC规定的次序大体上为:正离子(如铵盐)、羧酸、磺酸、酸的衍生物(酯、酰卤、酰胺等)、腈、醛、醇、酚、硫醇、胺、醚、过氧化物第二节醇的物理性质从前面烃和卤代烃的结构和性质来看,一个有机化合物的性质是取决于它的结构。
1.状态:C1-C4是低级一元醇,是无色流动液体,比水轻。
C5-C11为油状液体,C12以上高级一元醇是无色的蜡状固体。
甲醇、乙醇、丙醇都带有酒味,丁醇开始到十一醇有不愉快的气味,二元醇和多元醇都具有甜味,故乙二醇有时称为甘醇(Glycol)。
甲醇有毒,饮用10毫升就能使眼睛失明,再多用就有使人死亡的危险,故需注意。
2.沸点:醇的沸点比含同数碳原子的烷烃、卤代烷高。
CH3CH2OH 78.5℃, CH3CH2Cl 12℃.这是因为液态时水分子和醇分子一样,在它们的分子间有缔合现象存在。
有机化学第10章 醇、酚、醚

①醇可依分子中所含羟基数目分为一元醇、二元醇及三元醇等,二
元及二元以上的醇称为多元醇。例如:
CH3CH2OH CH2CH2 OH OH
乙醇(一元醇) 乙二醇(二元醇)
CH2CH CH2 OH OH OH
丙三醇(三元醇)
3
②醇也可依分子中烃基的不同而分为脂肪醇(包括饱和醇及不饱和 醇)、脂环醇和芳香醇。 例如:
C(CH3)2或 C(CH3)3
23
在醇的核磁共振谱图中,羟基质子(O—H)由于受
分子间氢键的影响,其化学位移(δ)出现在1~5.5范围 内,在核磁共振谱中产生一个单峰。由于氧的电负性 较大,羟基所连碳原子上的质子的化学位移一般在 3.4~4.0。
24
10.1.4 醇的化学性质
羟基是醇的官能团,作为反应中心羟基决定了醇的化学性质。
2,3-二甲基-3-戊醇
12
不饱和醇的命名,除应选择同时连有羟基和不饱和键的最长碳 链作为主链外,其它原则与饱和醇相同。
CH3CH2CH2CHCH2CH2CH2OH CH CH2
5 6
4
3
2
1
4-丙基-5-己烯-1-醇
CH CHCH3 CH3CH2CHCHCH2CHCH3 CH3 OH
4-甲基-5-乙基-6-辛烯-2-醇
32
醇和氢卤酸反应的速率与醇的结构的关系: 醇的活性顺序是:烯丙型醇、苄基型醇>叔醇>仲醇>伯醇。 例如:
33
利用不同醇与盐酸反应速率的不同,可以区分伯、仲、叔醇。无
水氯化锌与浓盐酸配制的溶液,叫做Lucas试剂。因为水溶性较好的
醇与Lucas试剂反应后,生成与水不互溶的氯代烃,形成乳状的混浊 溶液或分层,所以可利用Lucas试剂鉴别低碳(C6以下)一元伯、仲、叔 醇(C6以上的一元醇水溶性较差,难于用Lucas试剂鉴别)。例如:
有机化学 10

3o, 氢重排
(CH3)2CCH2CH3 100%
(CH3)3CCH2OH + HBr
Br
1o
3o, 碳重排
3oROH 、大多数2oROH和空阻大 的 1oROH按SN1机理进行反应。
(2) 醇与卤化磷的反应 (i)常用的卤化试剂
PCl5 、PCl3 、 PBr3 、 P + I2
(ii)反应方程式 3ROH + PBr3 5ROH + PX5 (iii)适用范围 3RBr + H3PO4 RX
5. 醇的物理性质 (1) 物理性质
a. 存在形式:固态,缔合较为牢固。
液态,形成氢键和氢键的解离均存在。 气态或在非极性溶剂的稀溶液中,醇分子可以单独存在。 b. 沸点:由于醇分子之间能形成氢键,沸点较相应分子量的 其它有 机物为高。 c. 溶解度:由于醇分子与水分子之间能形成氢键,三个碳以 内的醇和叔丁醇能与水混溶。 d. 密度:烷醇密度小于1,芳香醇密度大于1。
用于氧化还原
醇的酸性强弱的分析
液相测定酸性强弱 H2O > CH3OH > RCH2OH > R2CHOH > R3COH > HCCH > NH3 > RH
在液相中,溶剂化 作用会对醇的酸性 强弱产生影响。
溶剂化作用使负电 荷分散,而使RO稳定。
2022年高考一轮复习 第10章 有机化学基础 第3节 第1课时 卤代烃醇和酚

引入—OH,生成含—OH 消去HX,生成含碳碳双键或
特征
的化合物
碳碳三键的不饱和化合物
(2)卤代烃消去反应的规律 ①卤代烃不能发生消去反应的两种情况 a.只含一个碳原子的卤代烃不能发生消去反应。如:CH3Br、 CH2Cl2。
b.
和
不能消
去,因其分子中与连有卤素原子的碳原子相邻的碳原子上无氢原子。
______________________________。
(2)苯环上氢原子的取代反应 苯酚与饱和溴水反应,产生白色沉淀,反应的化学方程式为
______________________________。 利用这一反应可检验苯酚的存在及定量测定苯酚。 (3)显色反应 苯酚跟FeCl3溶液作用显_紫___色,利用这一反应可检验苯酚的存 在。
C.
互为同分异构
体 D.乙醇、苯甲醇、苯酚都既能与钠反应,又能与NaOH反应
AC 解析:苯甲醇、苯酚的结构不相似,故不互为同系物,B 错;酚与分子式相同的芳香醇、芳香醚互为同分异构体,C正确;乙 醇、苯甲醇的羟基都不显酸性,都不能与NaOH反应,D错。
练后梳理] 1.醇、酚的概念 (1)醇是羟基与饱和碳原子相连的化合物,饱和一元醇的分子通 式为__C_n_H_2_n_+_1_O__H_(_n_≥_1_)___。 (2)酚是羟基与苯环_直__接__相连而形成的化合物,最简单的酚为苯
[自主解答] __________________________________________________________________________________________ __________________________________________________________________________________________
第十章 醇、酚、醚

伯醇氧化生成醛
仲醇氧化生成酮
叔醇只有在强烈氧化条件下才被氧化-----发生键的断裂
选择性氧化-异丙醇铝-----选择性氧化羟基而保留双键
+|
Cl
伯醇主要按SN2反应机制进行,
快+
RCH2—OH +HX————→RCH2—OH2+ X一
+
RCH2—OH2+ X一———→X…CH2…OH2———→RCH2X + H2O
|
R
不同的醇在与相同的氢卤酸反应时的活性为:烯丙型醇、叔醇>仲醇>伯醇。
无水氯化锌与氯化氢的混合试剂称为卢卡斯(Lucas)试剂。其中无水氯化锌是强的路易斯酸。
3.与无机酸的反应
A.与HX反应得到卤代烃和水ROH+HX——→RX+H2O
大多数的仲醇和叔醇与氢卤酸的反应是按SN1反应机制进行的。仲醇反应时,由于仲碳正离子不如叔碳正离子稳定,某些特殊结构的醇可能容易发生重排。
活性:HX:HI>HBr>HCl;
醇:烯丙醇>3°>2°>1°
烯丙醇、三级醇、二级醇在酸催化下可通过SN1历程进行:
三、光谱性质
IR:醇的C—O吸收峰出现在1000—1200cm-1,其中伯醇约在1060—1030cm-1区域;仲醇约在1100cm-1附近;叔醇约在1140cm-1附近;酚的C—O吸收峰出现在1230cm-1。醇的—OH有两个吸收峰,未缔合的自由—OH在3600—3610cm-1有一外形较锐的吸收带;缔合—OH在3600—3210cm-1有一外形较宽的吸收带
胡宏纹《有机化学》课后习题及详解(醇和酚)【圣才出品】
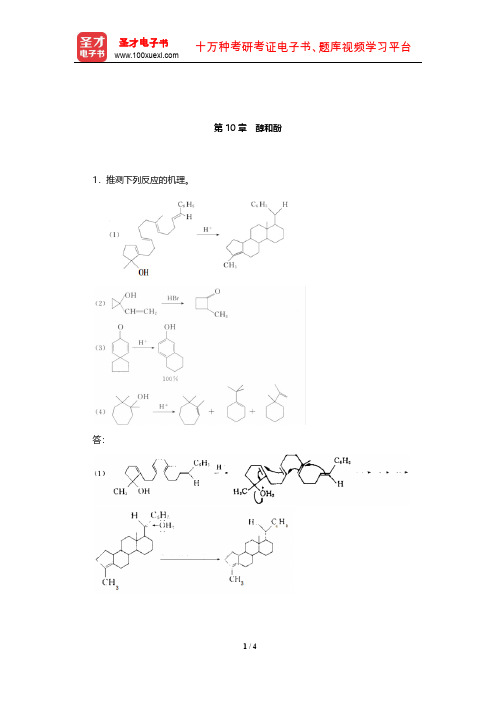
3.2,4,6-三叔丁基苯酚在醋酸溶液中与溴反应,生产化合物
,产率
差不多是定量的。A 的红外光谱图中在 1630 cm-1 和 1650 cm-1 处有吸收峰,1H NMR 谱
图中有三个单峰,δH=1.19,1.26 和 6.90,其面积比为 9:18:2。试推测 A 的结构。
答:A 的结构为:
4.推测下列化合物的结构。
3/4
圣才电子书 十万种考研考证电子书、题库视频学习平台
答:
4/4
ቤተ መጻሕፍቲ ባይዱ
解:
不饱和度为 4,提示可能有苯环;IR,3350 cm-1 峰提示可能
有羟基,3070,1600,1490 cm-1 提示可能有苯环,830 cm-1 提示可能为对位二取代;1H
NMR 中δH:6.8(q,4H)与对位二取代苯相符合,其他的峰说明侧链为 CH2CH2CH3,δ
H:5.5 为羟基上的质子。
圣才电子书 十万种考研考证电子书、题库视频学习平台
第 10 章 醇和酚 1.推测下列反应的机理。
答:
1/4
圣才电子书 十万种考研考证电子书、题库视频学习平台
2.如何完成下列转变?
2/4
圣才电子书
答:
十万种考研考证电子书、题库视频学习平台
有机化学(第五版)第十章 醇、酚、醚

2) 根据分子中烃基的类别分为:脂肪醇、脂环醇、 和芳香醇(芳环侧链有羟基的化合物,羟基直接连在 芳环上的不是醇而是酚)。
3) 根据分子中所含羟基的数目分为:一元醇、二元 醇和多元醇。 两个羟基连在同一碳上的化合物不稳定,这种结 构会自发失水,故同碳二醇不存在。另外,烯醇是不 稳定的,容易互变成为比较稳定的醛和酮。 井冈山大学化学化工学院
井冈山大学化学化工学院
关于频哪醇重排需要注意的问题
3.某些环状结构的频哪醇,重排后可得环扩大产物
井冈山大学化学化工学院
五、Preparation of Alcohols
1.由烯烃制备 1) 烯烃的水合 2) 硼氢化-氧化反应
硼氢化反应操作简单,产率高,是制备伯醇的好办法。
井冈山大学化学化工学院
3)羟汞化-脱汞反应
井冈山大学化学化工学院
乙醇液膜
乙醇(CCl4)
四、Chemical Properties of Alcohols
醇的化学性质主要由羟基官能团所决定,同时也受到烃 基的一定影响,从化学键来看,反应的部位有 C—OH、 O—H、和C—H。
分子中的C—O键和O—H键都是极性键,因而醇分子中有 两个反应中心。 又由于受C—O键极性的影响,使得α—H具 有一定的活性,所以醇的反应都发生在这三个部位上。 井冈山大学化学化工学院
(2)双分子消除反应(E2)
一步反应:
E2反应的特点: 1)一步反应,与SN2的不同在于B:进攻β-H。 E2与SN2是互相竟争的反应。 2)反应要在浓的强碱条件下进行。 3)通过过渡态形成产物,无重排产物。 井冈山大学化学化工学院
2. 消除反应的取向
A. Saytzeff规则:优先生成具有较多烷基取代的(也是较稳定的)烯烃。
胡宏纹《有机化学》章节题库(醇和酚)【圣才出品】

6.(多选)下列化合物与 Lucas 试剂作用,最快的为( ),最慢的为( )。 A.2-丁醇
2 / 27
圣才电子书
B.2-甲基-2-丁醇
十万种考研考证电子书、题库视频学习平台
C.2-甲基-1-丙醇
(2)由苯为主要原料制备三苯甲醇还有其他路线: ①经三苯甲基氯合成三苯甲醇 在无水三氯化铝存在下,苯与四氯化碳作用,生成三苯 甲基氯。三苯甲基氯在碱性条件下水解,生成三苯甲醇。 ②经二苯甲酮合成三苯甲醇 在无水三氯化铝存在下,苯与光气作用生成二苯甲酮。
在无水三氯化铝存在下,苯与四氯化碳作用生成二苯基二氯甲烷,然后水解生成二苯甲 酮。
圣才电子书 十万种考研考证电子书、题库视频学习平台
第 10 章 醇和酚
一、选择题 1.下列化合物在水中溶解度最大的是( )。 A.1-丁醇 B.1,3-丙二醇 C.乙醚 【答案】B 【解析】亲水基团越多,水中溶解度越大。
2.下列化合物中沸点最高的是( )。 A.2-甲基丙醇 B.正丁醇 C.1-氯丙烷 【答案】B 【解析】能形成分子内氢键的沸点较高,故醇比氯代烃高,且同数碳的醇支链越多,沸 点越低。
7 / 27
圣才电子书 十万种考研考证电子书、题库视频学习平台
苯溴代生成溴苯: 溴苯与镁作用,生成溴化苯基镁,溴化苯基镁与二苯甲酮作用,生成溴化三苯甲醇镁, 溴化三苯甲醇镁水解,生成三苯甲醇。 (3)溴苯与金属镁是放热反应,反应有诱导期,一旦反应开始,一般无需再加热。但 如果滴加溴苯的速度太慢,反应放出的热小于反应体系散失的热,导致反应温度下降,从而 造成反应速率下降,直至反应几乎停止。随着溴苯的滴加,体系中溴苯的浓度增加,如加热 反应体系,重新启动反应,将产生爆发式反应(即开始不反应,当加热到一定温度时,突然 反应,温度快速上升,反应很快结束),副反应增多。如果滴加溴苯的速度太快,局部溴苯 浓度增加,反应热增加,反应激烈,溴苯与金属镁作用生成的溴化苯基镁会与溴苯作用,生 成联苯。
第十章醇酚醚

3. 相对密度 一元醇的相对密度大于烷烃,但小于1,多元醇、芳香 醇的相对密度大于1。 4. 与某些无机盐形成结晶醇化合物 MgCl2· 6CH3OH CaCl2· 2H5OH 4C
① 有机物中有少量醇时,可加无机盐提纯。 如:工业乙醚常杂有少量乙醇,加入CaCl2可使醇从
乙醚中沉淀下来。
②不能用无水MgCl2、CaCl2、CuSO4 等无机盐干燥醇。
R Cl
反应生成的卤代烃不溶于Lucas试剂,溶液出现混浊或分层。 ①叔醇在室温下很快出现浑浊,并分层; ②仲醇要5~10分钟后出现浑浊; ③伯醇在室温下不发生反应,加热才出现浑浊。 适用范围:六个碳以下的醇。大于6个碳的醇(苄醇除外) 不溶于卢卡斯试剂,易混淆实验现象。
烯丙式醇、叔醇、大多数仲醇,反应是按SN1历程进行的。
§10-1 醇
一、分类、命名和结构
1. 分类 (1)根据和羟基相连的碳原子的类型:
CH3
CH3CH2CH2OH
伯醇 一级醇(1º 醇)
CH3CH2CHCH3 OH
仲醇 二级醇(2º 醇)
CH3
C OH
叔醇
CH 3
三级醇(3º 醇)
(2)根据分子中烃基的类别:
CH3CH2OH
脂肪醇 脂环醇
OH
芳香醇
C6H5 C6H5 C OH C 6 H5
三苯甲醇
triphenyl carbinol
主官能团的优先次序为:羧酸、磺酸、酯、酰卤、酰
胺、腈、醛、酮、醇、酚、胺、醚。
OH
CH3CHCH2CHO OH
3-羟基丁醛 3-hydroxylbutanal
CH2OH
邻羟基苯甲醇 o-hydroxyl benzyl alcohol
醇和酚

(F) 芳醇的命名:以芳环为取代基,按脂肪醇命名。
CH3
OH
CH3C=CHCH2CHCH3
6 54 3 2 1
5-甲基-4-己烯-2-醇
OH HOCH2CH2CHCH3
1,3-丁二醇
CH3CH=CHCH2CH2OH
3-戊烯醇
9.1 醇和酚的分类、构造和命名
酚的系统命名 • 以芳环名称加“酚”为母体,在母体前按“次序规则”冠 以
9.1.2 醇和酚的构造异构
Байду номын сангаас
醇 碳链异构 CH3-CH2-CH2-CH2-CH2-OH 的 异 构 羟基位置的异构 CH3CH2CH2CH2-OH
OH
CH3-CH2-CH2-OH CH3
CH3CH2CHCH3 OH
烃基异构
酚
的
OH
异
构
烃基与羟基在芳
环上的相对位次
OH
OH CH3
OH
OH
OH
OH
CH3
将硫原子代替氧原子,即得对应的硫醇、硫酚。
饱和一元醇最常见,通式:CnH2n+1OH 苯酚及烷基衍生物最常见,通式:CnH2n-6OH
9.1 醇和酚的分类、构造和命名
9.1.1 醇和酚的分类
按羟基数目分:一元醇、二元醇,三元醇,多元醇等.
例: CH3CH2CH2OH
CH2-CH2
CH2-CH-CH2
• 和三卤化磷,五氯化磷,亚硫酰氯作用,不发生重排
ROH + SOCl2
RCl + SO2 + HCl
9.6 醇和酚的化学性质
(4)脱水反应 低温脱水生成醚,高温脱水生成烯
(A)分子间脱水生成醚
j第十章 醇酚醚

( 俗称: 甘油 )
(俗名: 季戊四醇)
顺-1,2-环戊二醇
二、醇的物理性质
低级醇为具有酒味的无色透明液体。 C12以上的直链醇为固体。 低级直链饱和一元醇的沸点比相对分子质量相近的 烷烃的沸点高得多(Why?) 。
R O H O R H O
R H H O R
(醇分子间氢键缔合)
直链伯醇的沸点最高,带支链的醇的沸点要低些, 支链越多,沸点越低。
CH2R + O
O S O
好的离去基团
R’
5. 醇的脱水反应
<100℃ CH3CH2OH
H2SO4 140℃ 170℃
CH3CH2OSO3H 硫酸氢乙酯 (CH3CH2)2O CH2 = CH2 乙 醚
乙 烯
醇的脱水有两种方式,即分子内脱水和分子间脱水。 至于是成酯、成醚还是生成烯烃,取决于醇的结构 和反应条件。
多元醇分子中含有两个以上的羟基,可以形 成更多的氢键,所以分子中所含羟基越多,沸 点越高,在水中的溶解度也越大。 例: 乙二醇沸点:197℃ 甘油(丙三醇)沸点:290℃。
三、醇的光谱性质
乙醇的红外吸收光谱(液膜法)
乙醇的红外光谱(1%乙醇的CCl4溶液)
3650cm-1:O—H伸缩振动,游离羟基:其它同上图
例4:
合成尼龙-66的原料 (与乙二胺)
(2)脱氢→生成醛、酮 例5:
例6:
7. 多元醇的反应
-H2O
O ROPOH OH
烷基磷酸酯 ROH -H2O
O ROPOH ROH
-H2O
O ROPOR OR
三烷基磷酸酯
OR
二烷基磷酸酯
与有机酸及酰 卤反应成酯
第十章醇酚醚习题答案(第五版)

第十章醇、酚、醚(P306-310)1.写出戊醇C5H11OH的异构体的构造式,用系统命名法命名。
解:(1) (2)1-戊醇 3-戊醇(3)(4)2-戊醇 3-甲基-1-丁醇(5)(6)2-甲基-1-丁醇 2-甲基-2-丁醇(7)(8)3-甲基-2-丁醇 2,2-二甲基-1-丙醇2.写出下列结构式的系统命名:(1) 3-甲基-2-戊醇 (2)反-4-己烯-2-醇或 (E)-4-己烯-2-醇(3) 2-对氯苯基乙醇 (4)(顺)-2-甲基-1-乙基环己醇(1-己醇中的1可以省)(5) 2-甲基-1-乙氧基丙烷或乙基异丁基醚(6) 5- 硝基-3-氯-1,2-苯二酚 (7) 对溴乙氧基苯或对溴苯基乙醚(8) 2,6-二溴-4-异丙基苯酚(9) 1,2,3- 三甲氧基丙烷或丙三醇三甲醚 (10) 1,2-环氧丁烷(11)反-1-甲基-2-乙氧基环己烷或反乙基-2-甲基环己基醚 (12)1-甲氧基-1,2-环氧丁烷 3.写出下列化合物的构造式:(1)(2)OCH 3OCH3(4)(9)(10)OOOO4 .写出下列化合物的构造式5.写出异丙醇与下列试剂作用的反应式: (1) Na(2) Al(3) 冷浓H2SO4(4) H2SO4 > 1600C(5) H2SO4 < 1400C(6) NaBr+H2SO4(7) 红P + I2(8) SOCl2(9) CH3C6H4SO2Cl(10) (1) 的产物+C2H5Br(11) (1)的产物+ 叔丁基氯(12) (5)的产物+HI(过量)6.7 .有试剂氘代醇和HBr,H2SO4共热制备,的具有正确的沸点,但经对光谱性质的仔细考察,发现该产物是CH3CHDCHBrCH3和CH3CH2CDBrCH3的混合物,试问反应过程中发了什么变化?用反应式表明。
解:第一个实验是亲核反应,第二个实验以消除反应为主,生成烯烃气体放出,过量的乙醇没参加反应而留下。
8.完成下列反应式注:MCPBA:间氯过氧苯甲酸9、写出下各题中括弧中的构造式:10.用反应式表示下列反应解:11.化合物A为反-2-甲基环己醇,将A与对甲苯磺酰氯反应的产物以叔丁醇钠处理获得的唯一烯烃是3-甲基环己烯:(1)写出以上各步反应式(2)指出最后一步的立体化学(3)若将A用硫酸脱水,能否得到上述烯烃。
化学课件《醇和酚》优秀ppt10 鲁科版

为什么苯酚显弱酸性,而乙醇不显弱酸性呢 ?
Байду номын сангаас
(1)苯酚的弱酸性
OH O- +H+
①苯酚与NaOH溶液的反应
OH +NaOH ONa +H2O
(苯酚钠,易溶于水)
苯酚俗称石炭酸
ONa +H2O +CO2
OH +NaHCO3 ONa +NaHCO3
OH + Na2CO3
通过上面的实验,你是怎样认识苯酚的酸性的 ? OH 结论:酸性:H2CO3
暴露在 空气中
结论:苯酚暴露在空气中,被氧化 而呈粉红色,说明苯酚可以发生氧 化反应,具有还原性
电 木 化 妆 品 医
苯 药 酚 的 用 合 途
成 纤 维
农 药
小结
1、苯酚分子组成和结构
2、苯酚的物理性质 苯酚
①弱酸性
3、苯酚的化学性质 ②取代反应
③显色反应
4、苯酚的用途
④氧化反应
练习
: 1、下列物质久置于空气中, 颜色会发生变化的
它不具有的性质是(
C)
①易溶于水 ②可以燃烧 ③能使酸性高锰 酸钾溶液褪色 ④能跟KOH溶液反应 ⑤能跟NaHCO3溶液反应 ⑥能与溴水发生取代反应 ⑦能与钠反应 ⑧能发生加聚反应 A.①④ B.①②⑥ C.①⑤ D.③⑤⑥
18
85.每一年,我都更加相信生命的浪费是在于:我们没有献出爱,我们没有使用力量,我们表现出自私的谨慎,不去冒险,避开痛苦,也失去了快乐。――[约翰· B· 塔布] 86.微笑,昂首阔步,作深呼吸,嘴里哼着歌儿。倘使你不会唱歌,吹吹口哨或用鼻子哼一哼也可。如此一来,你想让自己烦恼都不可能。――[戴尔· 卡内基] 87.当一切毫无希望时,我看着切石工人在他的石头上,敲击了上百次,而不见任何裂痕出现。但在第一百零一次时,石头被劈成两半。我体会到,并非那一击,而是前面的敲打使它裂开。――[贾柯· 瑞斯] 88.每个意念都是一场祈祷。――[詹姆士· 雷德非] 89.虚荣心很难说是一种恶行,然而一切恶行都围绕虚荣心而生,都不过是满足虚荣心的手段。――[柏格森] 90.习惯正一天天地把我们的生命变成某种定型的化石,我们的心灵正在失去自由,成为平静而没有激情的时间之流的奴隶。――[托尔斯泰] 91.要及时把握梦想,因为梦想一死,生命就如一只羽翼受创的小鸟,无法飞翔。――[兰斯顿· 休斯] 92.生活的艺术较像角力的艺术,而较不像跳舞的艺术;最重要的是:站稳脚步,为无法预见的攻击做准备。――[玛科斯· 奥雷利阿斯] 93.在安详静谧的大自然里,确实还有些使人烦恼.怀疑.感到压迫的事。请你看看蔚蓝的天空和闪烁的星星吧!你的心将会平静下来。[约翰· 纳森· 爱德瓦兹] 94.对一个适度工作的人而言,快乐来自于工作,有如花朵结果前拥有彩色的花瓣。――[约翰· 拉斯金] 95.没有比时间更容易浪费的,同时没有比时间更珍贵的了,因为没有时间我们几乎无法做任何事。――[威廉· 班] 96.人生真正的欢欣,就是在于你自认正在为一个伟大目标运用自己;而不是源于独自发光.自私渺小的忧烦躯壳,只知抱怨世界无法带给你快乐。――[萧伯纳] 97.有三个人是我的朋友爱我的人.恨我的人.以及对我冷漠的人。 爱我的人教我温柔;恨我的人教我谨慎;对我冷漠的人教我自立。――[J·E·丁格] 98.过去的事已经一去不复返。聪明的人是考虑现在和未来,根本无暇去想过去的事。――[英国哲学家培根] 99.真正的发现之旅不只是为了寻找全新的景色,也为了拥有全新的眼光。――[马塞尔· 普劳斯特] 100.这个世界总是充满美好的事物,然而能看到这些美好事物的人,事实上是少之又少。――[罗丹] 101.称赞不但对人的感情,而且对人的理智也发生巨大的作用,在这种令人愉快的影响之下,我觉得更加聪明了,各种想法,以异常的速度接连涌入我的脑际。――[托尔斯泰] 102.人生过程的景观一直在变化,向前跨进,就看到与初始不同的景观,再上前去,又是另一番新的气候――。[叔本华] 103.为何我们如此汲汲于名利,如果一个人和他的同伴保持不一样的速度,或许他耳中听到的是不同的旋律,让他随他所听到的旋律走,无论快慢或远近。――[梭罗] 104.我们最容易不吝惜的是时间,而我们应该最担心的也是时间;因为没有时间的话,我们在世界上什么也不能做。――[威廉· 彭] 105.人类的悲剧,就是想延长自己的寿命。我们往往只憧憬地平线那端的神奇【违禁词,被屏蔽】,而忘了去欣赏今天窗外正在盛开的玫瑰花。――[戴尔· 卡内基] 106.休息并非无所事事,夏日炎炎时躺在树底下的草地,听着潺潺的水声,看着飘过的白云,亦非浪费时间。――[约翰· 罗伯克] 107.没有人会只因年龄而衰老,我们是因放弃我们的理想而衰老。年龄会使皮肤老化,而放弃热情却会使灵魂老化。――[撒母耳· 厄尔曼] 108.快乐和智能的区别在于:自认最快乐的人实际上就是最快乐的,但自认为最明智的人一般而言却是最愚蠢的。――[卡雷贝· C· 科尔顿] 109.每个人皆有连自己都不清楚的潜在能力。无论是谁,在千钧一发之际,往往能轻易解决从前认为极不可能解决的事。――[戴尔· 卡内基] 110.每天安静地坐十五分钟· 倾听你的气息,感觉它,感觉你自己,并且试着什么都不想。――[艾瑞克· 佛洛姆] 111.你知道何谓沮丧---就是你用一辈子工夫,在公司或任何领域里往上攀爬,却在抵达最高处的同时,发现自己爬错了墙头。--[坎伯] 112.「伟大」这个名词未必非出现在规模很大的事情不可;生活中微小之处,照样可以伟大。――[布鲁克斯] 113.人生的目的有二:先是获得你想要的;然后是享受你所获得的。只有最明智的人类做到第二点。――[罗根· 皮沙尔· 史密斯] 114.要经常听.时常想.时时学习,才是真正的生活方式。对任何事既不抱希望,也不肯学习的人,没有生存的资格。 ――[阿萨· 赫尔帕斯爵士] 115.旅行的精神在于其自由,完全能够随心所欲地去思考.去感觉.去行动的自由。――[威廉· 海兹利特] 116.昨天是张退票的支票,明天是张信用卡,只有今天才是现金;要善加利用。――[凯· 里昂] 117.所有的财富都是建立在健康之上。浪费金钱是愚蠢的事,浪费健康则是二级的谋杀罪。――[B·C·福比斯] 118.明知不可而为之的干劲可能会加速走向油尽灯枯的境地,努力挑战自己的极限固然是令人激奋的经验,但适度的休息绝不可少,否则迟早会崩溃。――[迈可· 汉默] 119.进步不是一条笔直的过程,而是螺旋形的路径,时而前进,时而折回,停滞后又前进,有失有得,有付出也有收获。――[奥古斯汀] 120.无论那个时代,能量之所以能够带来奇迹,主要源于一股活力,而活力的核心元素乃是意志。无论何处,活力皆是所谓“人格力量”的原动力,也是让一切伟大行动得以持续的力量。――[史迈尔斯] 121.有两种人是没有什么价值可言的:一种人无法做被吩咐去做的事,另一种人只能做被吩咐去做的事。――[C·H·K·寇蒂斯] 122.对于不会利用机会的人而言,机会就像波浪般奔向茫茫的大海,或是成为不会孵化的蛋。――[乔治桑] 123.未来不是固定在那里等你趋近的,而是要靠你创造。未来的路不会静待被发现,而是需要开拓,开路的过程,便同时改变了你和未来。――[约翰· 夏尔] 124.一个人的年纪就像他的鞋子的大小那样不重要。如果他对生活的兴趣不受到伤害,如果他很慈悲,如果时间使他成熟而没有了偏见。――[道格拉斯· 米尔多] 125.大凡宇宙万物,都存在着正、反两面,所以要养成由后面.里面,甚至是由相反的一面,来观看事物的态度――。[老子] 126.在寒冷中颤抖过的人倍觉太阳的温暖,经历过各种人生烦恼的人,才懂得生命的珍贵。――[怀特曼] 127.一般的伟人总是让身边的人感到渺小;但真正的伟人却能让身边的人认为自己很伟大。――[G.K.Chesteron] 128.医生知道的事如此的少,他们的收费却是如此的高。――[马克吐温] 129.问题不在于:一个人能够轻蔑、藐视或批评什么,而是在于:他能够喜爱、看重以及欣赏什么。――[约翰· 鲁斯金]
第10章醇和酚

10.1 醇和酚的结构和分类
10.1.1 醇的结构
醇和水有相似的结构,可将醇看成是水分子中的 一个氢原子被烃基取代后的生成物。由于醇分子中氧 原子的电负性比碳原子大,使氧原子上的电子云密度 较高,所以醇分子具有较强的极性。
➢酚的构造
➢ 构造:-OH直接连在芳环上的化合物称为酚。 通式为 Ar-OH。
第10章 醇和酚 (Alcohols and Phenols)
10.1 醇和酚的结构和分类 10.1.1 醇的结构 10.1.2 醇和酚的分类
10.2 醇和酚的命名 10.2.1 醇的命名 10.2.2 酚的命名
10.3 醇和酚的物理性质与光谱性质 10.3.1 醇的物理性质与光谱性质 10.3.2 酚的物理性质与光谱性质
phenols101醇和酚的结构和分类1011醇的结构1012醇和酚的分类102醇和酚的命名1021醇的命名1022酚的命名103醇和酚的物理性质与光谱性质1031醇的物理性质与光谱性质1032酚的物理性质与光谱性质104醇和酚的酸性1041醇的酸性1042酚的酸性105醇的反应1051醇的氧化10521053醇与氯化亚砜的反应1054醇与卤化磷的反应1055醇的脱水反应1056酸催化醇脱水反应的反应机理1057醇的酯化反应1058二醇的特殊反应106醇和制备1061卤代烃的水解及羰基还原1062由烯烃制备醇1063从格氏试剂制备醇107硫醇1071硫醇的物理性质及制备方法1072硫醇的化学性质108酚的制备109酚的反应1091酚氧负离子亲核取代1092酚氧化还原反应1093芳环上的亲电取代反应1010周环反应ii迁移反应1011011醇的结构醇和水有相似的结构可将醇看成是水分子中的一个氢原子被烃基取代后的生成物
注意:①由伯醇制备相应的卤烷时,一般用卤化钠和浓
教案-第十章--醇酚

第十章醇和酚授课对象:化学师范;化学类.学时安排:9学时教材:<<有机化学>> (第3版),胡宏纹主编,普通高等教育“十五”国家级规划教材一、教学目的与要求1、掌握醇的命名、分类、结构。
2、掌握醇的化学性质:与金属钠反应,与无机含氧酸成酯,脱水成烯,醇的氧化。
3、掌握邻二醇类的特性反应:与氢氧化铜反应、与过碘酸反应。
烯醇与FeCl3显色。
4、掌握酚的结构,化学性质:酸性、氧化、亲电取代。
5、了解醇、酚的物理性质,重要的醇、酚。
二、教学重点1、醇的中、英文命名法。
2、醇的化学性质:与金属钠反应,与无机含氧酸成酯,分子内脱水成烯,醇的氧化。
邻二醇类的特性:与氢氧化铜反应、与过碘酸反应。
3、酚的亲电取代反应、氧化反应。
三、教学难点1、醇钠的碱性2、醇分子内脱水过程中,中间体正碳离子的重排。
四、教学方法采用讲授法。
1、醇和酚的一般性质在中学学过,以复习的形式进行。
2、醇分子内脱水成烯,伴有重排的反应是本章的难点,只介绍1,2迁移和1,3-迁移重排。
并通过多媒体课件中设置活动画面来加深印象,帮助理解。
3、邻多醇的特性反应多举实例,并结合实验课来讲解。
五、教具电脑、幻灯投影仪、powerpoint课件、教鞭。
六、教学步骤及时间分配导言:1、阐述醇和酚在结构上的异同点。
2、引导学生回顾醇的通式、来源或制备方法,生活中有哪些常见的醇?3、已经学过了的醇和酚有哪些主要的性质?4、从日常生活中的实例引入醇和酚化合物的重要性,引入本章内容。
1 醇一、醇的结构、分类和命名1、结构以甲醇为例,说明醇分子中氧原子采取sp3杂化参与成键, COH为108.90。
结合路易斯电子结构式和球棍模型讲述。
2、分类(1)按羟基所在碳原子的类型分:伯、仲、叔醇(2)按羟基的数目分:一元醇、二元醇、三元醇、多元醇(3)按烃基的不同分:饱和醇、不饱和醇、脂环醇、芳香醇每种类型的醇给出通式并各举一例,由投影仪一一列出。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
2012-3-22
有机化学
CH3OH + HO SO3H 2 CH3 O SO3H C12H25OSO3Na CH2ONO2 CHONO2 CH2ONO2 蒸馏
CH3SO4H 硫酸氢甲酯 CH3 O SO3H + H2O 甲 基化试 剂 (CH3)2SO4 硫酸二甲酯 CH3 O SO2 O CH3 + H2SO4 阳离子 表面 活性 剂
CH3CH2OH
浓 硫酸 170℃ ℃ 浓 硫酸 140℃ ℃
CH2 CH2 + H2O CH3CH2OCH2CH+ H2O 3
AI2O3 350~400℃ ℃ 硫酸
2 CH3CH2OH
CH3CH2CH2CH2OH
CH2 CHCH2CH3 CH CH CH2CH3
CH2CHCH2CH3 OH
课堂习题:教材206页问题10-11、10-12。 课堂习题:教材206页问题10-11、10-12。 206页问题10
CH CH CH2OH
2012-3-22
有机化学
2)醇的构造异构 具有相同碳原子的饱和一元醇,因碳架不同和羟基位次 不同而产生的异构体。 3)醇的命名 ① 普通命名法-简单的醇
OHOH OH H2C CH CH2 丙三醇
CH2OH HOH2C C CH2OH 季戊四醇 CH2OH
② 衍生命名法-以甲醇为母体
CH3 CH3 CH CH3 CH3 CH CH3 CH3
2012-3-22
ZnCI2 H C CH3 + HCI OH H C CH3 + H OH 重排 H C CH3
CH3 CH3 C CH2 CH3 CI CH3 -H2O H CH C CH3 OH2 CH3
CH3
C H
CH3
C
CH2CH3
OMgX
OMgX H3C C H R 干醚
H3O 水解
OMgX H3C C CH3 R
H3O 水解
2012-3-22
有机化学
选用那一种羰基化合物与格利雅试剂反应制备所需 醇,可以从连接醇羟基碳原子上的三个基团的结构来考 虑,其中一个烃基来自于格利雅试剂,另两个基团来自 于羰基化合物,然后考虑其中那些原料比较易得。
c
2012-3-22
δ
O
SP
3
δ
H
H H
C
O
H
有机化学
H
10.1.1 醇的分类、构造异构和命名 醇的分类、 1)醇的分类 根据分子中羟基所连碳原子不同分伯醇、仲醇和叔醇; 根据分子中烃基不同分饱和醇、不饱和醇和芳醇; 根据分子中含羟基的数目不同分一元醇、二元醇和多元醇。
OH CH3 CH CH3 OH CH3 CH CH2 CH3 OH CH3 C CH3 CH3 OHOH OH H2C CH CH2 CH2OH HOH2C C CH2OH CH2OH CH2 CH CH2OH OH CH2CHCH3
第十章 醇和酚
醇和酚的基础知识 醇和酚的制法 醇和酚的物理性质 醇和酚的化学性质 几种重要的醇和酚制品
2012-3-22
有机化学
学习要求
掌握醇和酚的分类、命名和同分异构等知识。 1.掌握醇和酚的分类、命名和同分异构等知识。 掌握醇和酚的制法。 2.掌握醇和酚的制法。
3.了解醇和酚的物理性质。 了解醇和酚的物理性质。
OH CI
OH OH
2012-3-22
有机化学
10.1.7 硫醇 “-SH”称为巯基,它是硫醇的官能团。命名与醇相似, 只要把“醇”改为相应的“硫醇”即可。 低级硫醇有恶臭,可用来检查管道泄漏。
CH3CH2SH + NaOH 2 CH3CH2SH + HgO CH3CH2SNa + H2O (CH3CH2S)2Hg 白色
有机化学
5)卤代烃水解 一般卤代烃水解有许多副产物,且醇比相应的卤代烃 容易得到,故只有相应的卤代烃易得时才用此法。
CH2
CH
CH2CI + H2O
NaCO3
CH2
CH
CH2OH
CH2CI + H2O
NaOH
CH2OH
课堂习题:教材199页问题10课堂习题:教材199页问题10-3、10-4。 199页问题10 102012-3-22
CH CH CH2OH
2012-3-22
有机化学
4)由格利雅试剂制备-常用于合成构造较复杂、且难用 其他方法合成的醇
δ δ R MgX + Oδ C δ O R MgX + H C H O R MgX + H3C C H O R MgX + H3C C CH3 OMgX 干醚 C R 干醚 H C H R 干醚 H3O 水解 H3O 水解 OH C R R CH2OH 伯醇 OH R CHCH3 仲醇 OH R C CH3 叔 醇 CH3
SO3H NaOH SO3Na 300~320℃ NaOH, 碱融
2012-3-22
ONa H
OH
有机化学
10.2.3 酚的物理性质 10.2.4 酚的化学性质 1)酚羟基的反应 ① 弱酸性
OH O +H 一对SP2 杂化,P电子与芳环发生共轭 R O +H O2 N OH H3 C O2 N OH O2 N OH
2-甲基-2-丙醇
CH2 CH CH2OH
课堂习题:教材198页问题10课堂习题:教材198页问题10-1、10-2。 198页问题10 102012-3-22
有机化学
10.1.2 醇的制法 1)烯烃水合-遵循马氏规则,可能有重排发生。
CH3 H+ C CH2 + H2O H OH CH3 C CH3 H
重点掌握醇和酚的化学性质。 4.重点掌握醇和酚的化学性质。 了解几种重要的醇和酚制品的相关知识。 5.了解几种重要的醇和酚制品的相关知识。
Hale Waihona Puke 2012-3-22有机化学
10.1 醇
定义: 定义:烃分子中饱和碳原子上的氢原子被羟基(-OH) 取代的化合物。 结构: 结构:由于氧原子电负性比碳原子大,造成α碳原子带有 部分正电荷;同样的道理,羟基中的氢原子在适当的条 件下能以质子的形式解离出来;氧原子上的两对孤对电 子也会对醇的性质产生轻微影响。
2012-3-22
有机化学
命名下列化合物:
OH OH CH3 OH HO COOH OH SO3H HO NO2
OH
NO2 CH3
OH
NO2 OH
HO
OH SO3H
2012-3-22
有机化学
10.2.2 酚的制法 1)由异丙苯制备-工业生产苯酚的主要方法
CH(CH3)2 + CH3CH CH2 H2SO4 O2
CH CH C H
2012-3-22
有机化学
③ 用氢化铝锂(LiAIH4)还原
O LiAIH4 R CH2OH R C H OH O LiAIH4 R CH CH3 R C CH3 O LiAIH4 CH CH C H O LiAIH4 R C OH R CH2OH O LiAIH4 R CH2OH R C OR'
课堂习题:教材207-208页问题10-13。 课堂习题:教材207-208页问题10-13。 207 页问题10
2012-3-22
有机化学
10.1.5 乙二醇 俗名甘醇,是最简单最重要的二元醇。 10.1.6 丙三醇 俗名甘油,是最简单最重要的三元醇。 制备方法有:
CH2 CH CH3 CI2 高温 CH2 CH CH2 CI Ca(OH)2 60℃ ℃ CH2 O CH CH2 CI 10% NaOH 150℃ ℃ CH2 HO CH CI2 + H2O CH2 CI CH2 CH CH2
2012-3-22
有机化学
2)卤代烃的生成 ① 浓盐酸和无水氯化锌所配置的溶液称为卢卡斯试剂。 醇与卢卡斯试剂的反应可用来鉴别不同类型的醇。
各种醇在卢卡斯试剂存在下的反应活性顺序如下: CH2OH > CH2 CH CH2OH > 叔醇 > 仲醇 > 伯醇 > 甲醇
② 由伯醇制备相应的卤烷,由于反应按SN2进行,故无 重排现象发生。
有机化学
④ 醇与三卤化磷、五氯化磷或亚硫酰氯反应生成相应的 醇时,不发生重排。 课堂习题:教材204页问题10-10。 课堂习题:教材204页问题10-10。 204页问题10 3)酯的生成 醇与无机含氧酸和有机酸作用,发生分子间脱水生成酯。 常用的无机酸有硫酸、硝酸、磷酸等;常用的有机酸有羧 酸等。
2012-3-22
有机化学
HI CH3CH2CH2CH2OH + HBr
∆ H2SO4
CH3CH2CH2CH2I + H2O CH3CH2CH2CH2Br + H2O CH3CH2CH2CH2CI + H2O
∆ ZnCI2 HCI ∆
③ 由仲、叔醇制备相应的卤烷,由于反应按SN1进行, 故有重排现象发生。
OH H3C CH2 CH CH3
2012-3-22
甲基乙基甲醇
有机化学
③ 系统命名法 选主链:含有羟基的最长碳链; 编号:从靠近羟基的一端开始; 命名:根据主链所含碳原子数叫做“某醇”,前面依次列出 取代基的位次和名称。
OH CH3 CH CH3 CH3 OH C CH3 CH3 OH CH CH CH2OH 3-苯基-2-丙烯醇 CH2CHCH3 2-苯丙醇 2-丙醇 CH3 OH CH CH2 CH3 2-丁醇 2-丙烯醇
有机化学
10.1.3 醇的物理性质 醇是极性分子,醇分子间能形成氢键,醇的物理性 质大多与此有关。 10.1.4 醇的化学性质 1)与金属的反应
