2018中考化学习题集-原子的结构
2018年中考化学知识分类汇编练习卷: 原子结构及元素(含答案)

原子结构及元素一、选择题1.【2018年山东省德州市】近日,中国在四川某地发现了一个超大规模的锂矿,储量高达52万吨,被称之为“中国锂谷”。
锂矿是重要的国家战略资源,有着21世纪改变世界格局的“白色石油”和“绿色能源金属”之称。
下图是锂原子结构示意图和锂元素在元素周期表中的相关信息。
下列说法正确的是( )A.锂元素属于非金属元素 B.锂原子在化学反应中易得电子C.锂原子的相对原子质最是6.94lg D.锂原子核内有3个质子【答案】D2.【2018年湖北省随州市】下图是元素周期表中提供的碘元素部分信息及碘原子结构示意图。
下列说法错误的是A.碘单质(I2)是由碘原子直接构成的 B.碘的相对原子质量为127,原子核内质子数为53C.碘原子核外共有53个电子,最外层有7个电子D.碘元素属于非金属元素,碘原子在化学反应中容易得到电子【答案】A3.【2018年湖南省岳阳市】硒是人体必需的一种微量元素,严重缺硒可能诱发皮肤病和癌症。
硒的原子结构示意图及其在元素周期表中的某些信息如图所示,下列分析正确的是()A.硒属于金属元素 B.硒的相对原子质量为78.96gC.硒原子的核电荷数为34 D.硒原子的核外有6个电子【答案】C4.【2018年湖北省咸宁市】1869年发现了元素周期律并编制出元素周期表的科学家是A.道尔顿 B.阿伏加德罗 C.门捷列夫 D.侯德榜【答案】C5.【2018年湖北省咸宁市】稀土是一种重要的战略资源。
铈是一种常见的稀土元素,下列有关铈的说法正确的是A.铈属于非金属元素 B.铈原子的中子数是58C.铈原子的核外电子数是58 D.铈原子的相对原子质量是140.1g【答案】C6.【2018年安徽省】硼是作物生长必需的微量营养元素,硼元素的相关信息如图所示。
下列有关硼的说法正确的是A.相对原子质量为10.81g B.属于金属元素C.原子的核电荷数为5 D.原子核外有6个电子【答案】C7.【2018年广州市】下图为某粒子的结构示意图,下列说法正确的是A.该粒子有12个质子 B.该粒子有2个电子层C.该粒子属于非金属元素 D.该粒子已达到相对稳定结构【答案】A8.【2018年安徽省】归纳法是学习化学的重要方法之一,下列图示正确的是【答案】A9.【2018年湖南省岳阳市】地壳中含量最多的元素是()A.Si B.Al C.O D.Fe【答案】C10.【2018年江苏省南京市】北京大学生命科学学院蒋争凡教授研究组发现,锰离子是细胞内天然免疫激活剂和警报素。
2018年中考化学重要考点 原子的结构练习卷

原子的结构练习卷1.下列说法错误的是A. 原子不显电性B. 在化学变化中能否再分是原子和分子的本质区别C. 原子的质量主要集中在原子核上D. 所有原子的原子核都含有中子和质子【答案】D2.钠原子的原子结构示意图是【答案】B3.冰箱所用的材料中含稀土元素钆(Gd),钆元素的一种原子的相对原子质量为157,核电荷数为64,则其原子的中子数为A. 64B. 57C. 93D. 128【答案】C4.已知一个碳原子(质子数为6,中子数也是6)的质量为a kg,A原子的质量为b kg,则A原子的相对原子质量为A. b/12B. a/12C. 12a/bD. 12b/a【答案】D5.核电荷数相同的粒子是A. 同一种原子B. 同一种离子C. 同一种元素D. 无法确定【答案】D6.据报道,上海某医院正研究用放射性碘治疗肿瘤,这种碘原子的核电荷数是53,相对原子质量是125,下列关于这种原子的说法错误的是A. 质子数是53B. 中子数是53C. 核外电子数是53D. 质子数与中子数之和是125【答案】B7.相对原子质量的说法有:①相对原子质量是一个原子的质量;②相对原子质量是一个原子质量的1/12;③相对原子质量是原子的相对质量,是一个比值;④相对原子质量的近似值为中子数和质子数之和;⑤相对原子质量是以碳的相对原子质量为标准的比值;⑥一般化学计算时采用相对原子质量的近似值。
其中正确的是A. ③④⑤B. ③④⑥C. ②③④D. ①③⑤【答案】B8.决定元素种类和元素化学性质的分别是原子的A. 质子数和最外层电子数B. 质子数和核外电子数C. 质子数和中子数D. 中子数和核外电子层数【答案】A9.下列各种原子各l g。
所含原子个数最多的是(括号内是该原子的相对原子质量)A. 氧原子(32)B. 铁原子(56)C. 氢原子(1)D. 碳原子(12)【答案】C10.某原子的原子核内有161个中子,其相对原子质量为272,则下列说法错误的是A. 该原子的质子数是111B. 该原子的核电荷数为161C. 该原子的核外电子数是111D. 该原子的质量是一个碳12原子质量的272 12倍【答案】B11.A原子与B原子的质量之比为a∶b,而B原子与作为相对原子质量标准的碳原子的质量之比为m∶n,则A原子的相对原子质量为A. B. C. D.【答案】A12.在分子、原子、原子核、质子、中子、电子等粒子中,找出符合下列条件的粒子填在相应的横线上:(1)能直接构成纯净物的有_______;(2)化学反应中种类一定变化的是_______;(3)一定能保持物质化学性质的粒子是________;(4)化学变化中的最小粒子是________;(5)带正电荷的粒子是________;(6)不显电性的粒子是________;(7)质量最小的粒子是________;(8)在同一原子中数目相等的粒子是________;(9)决定原子质量大小的粒子主要是________。
经典初中化学原子结构(练习题)

经典初中化学原子结构(练习题)
下面是一些关于经典初中化学原子结构的练题,希望能帮助您巩固和提高对这一知识领域的理解。
1. 原子是物质的最小单位,它由什么组成?
答案:原子由质子、中子和电子组成。
2. 请问原子核中质子和中子的区别是什么?
答案:质子带有正电荷,中子不带电荷。
3. 原子核的质量是由质子和中子的质量之和决定的,请问原子核外的电子贡献了什么?
答案:原子核外的电子贡献了负电荷,使得原子整体处于电中性状态。
4. 请问在原子模型中,电子是如何排布的?
答案:根据原子模型,电子是按能级分布在原子的不同轨道上。
5. 在氢原子中,质子数和电子数相等吗?
答案:是的,氢原子中质子数和电子数相等,都是1。
6. 原子团和化合物中的原子是如何结合的?
答案:原子团和化合物中的原子通过化学键结合在一起。
7. 请问原子的核外电子是如何参与化学反应的?
答案:原子的核外电子通过与其他原子的核外电子进行共享、
转移或接受电子等方式参与化学反应。
这些练习题旨在帮助您回顾和巩固对经典初中化学原子结构的
理解,希望对您有所帮助。
如果您还有其他问题,请随时提问。
初中化学 原子的结构 练习题(含答案)

初中化学原子的结构练习题(含答案)一、选择题1. 原子的结构是()A. 细胞B. 粒子C. 分子D. 质子答案:C2. 原子中组成原子核的粒子是()A. 电子B. 质子C. 中子D. 什么都不是答案:B3. 下列说法正确的是()A. 电子在原子核外绕行B. 质子和中子分别带正电和负电C. 原子核中的粒子数目不固定D. 原子核内质子质量大于中子答案:A4. 原子的结构是由()构成的。
A. 原子核和电子云B. 原子核和质子C. 原子核和中子D. 电子云和质子答案:A5. 原子核中所含的质子数决定了()。
A. 元素的化学性质B. 元素的物理性质C. 元素的放射性D. 元素的熔点答案:A6. 下列关于原子核的说法,正确的是()A. 原子核的直径是电子云的数千倍B. 原子核内质子和中子的质量几乎相等C. 原子核内质子和中子的数量相等D. 原子核是由正电质子组成的答案:B二、判断题1. 原子核由质子和电子组成。
答案:错2. 原子核的直径大约是原子的直径的万分之一。
答案:对3. 原子核的电子云中没含有电子。
答案:错4. 原子核中的质子数目决定了元素的原子序数。
答案:对5. 原子核内质子的质量大于中子。
答案:错三、填空题1. 原子核由________和________组成。
答案:质子,中子2. 原子核的直径约为________。
答案:10^-15米3. 原子核内质子与中子的数量差异称为________。
答案:中子过剩4. 原子的质子数称为________,用符号____表示。
答案:原子序数,Z5. 电子绕行的区域称为________。
答案:电子云四、简答题1. 请简要描述原子核的构成和性质。
答案:原子核是由质子和中子组成的,在原子中占据着非常小的体积空间,约占整个原子体积的10^-15倍。
原子核带有正电荷,质子和中子的质量几乎相等,质子的质量略大于中子。
此外,原子核还具有放射性。
2. 原子的质子数如何影响元素的性质?答案:元素的质子数,即原子核内质子的数量,决定了元素的原子序数。
2018届初三中考化学复习 原子的结构 专题复习练习 含答案

2019届初三中考化学复习原子的结构专题复习练习1.下列原子中的粒子,带负电荷的是( )A. 原子核B. 电子C. 质子D. 中子2. 钛和钛合金被认为是21世纪的重要金属材料,它们具有熔点高、密度小、抗腐蚀性强等优良性能,因此被广泛用于火箭、航天飞机、船舶和化工等。
已知钛原子的质子数为22,中子数为26,则钛原子的核外电子数为( )A. 48 B. 26 C. 4 D. 223. 原子核中一定含有的粒子是( )A. 中子B. 质子C. 电子D. 质子和中子4. 已知一种碳原子可用于测定文物的年代,该原子的原子核内含有6个质子和8个中子,则该原子内的粒子总数为( )A. 20B. 6C. 8D.145. 2019年10月,中国科研团队首次证实了天然铀单质的存在。
用于核电工业的一种铀原子中含有92个质子和143个中子。
下列有关该原子的说法不正确的是( ) A. 该原子的中子数为143 B.该原子的电子数为92C. 该原子的核电荷数为92D. 该原子的相对原子质量为1436.在原子中,电子数等于( )A. 质子数与中子数之和B. 质子数与中子数之差C. 中子数D. 质子数7. 铈(Ce)是一种常见的稀土元素,已知铈原子的原子核内有58个质子和82个中子,该原子的核外电子数为( )A.24B. 58C. 82D. 1408.根据钠原子结构示意图,不能确定的是( )A. 质子数B. 电子层数C. 相对原子质量D. 原子种类9. 下列说法正确的是( )A. 原子由原子核和核外电子构成B. 物质都由原子直接构成C. +2Mg表示两个镁离子 D. 2H表示两个氢分子10. 某原子的结构示意图为,下列说法正确的是( )A. 该原子中所含的质子数为16B. 该原子属于金属元素的原子C. 该原子属于非金属元素的原子D. 该原子的核外电子数为611. 下列说法正确的是( )A. 氢、碳、氧的原子核都由质子和中子构成B. 某粒子的核电荷数为17,核外电子数为18,该粒子一定是阳离子C. 质子和中子的相对质量都约等于1,每个质子、中子都带1个单位正电荷D. 氯原子的结构示意图为,在化学反应中若得到一个电子即变成氯离子(-Cl) 12. 物质是由原子、分子、离子等粒子构成。
初中化学 原子的结构 练习题(含答案)

——原子的构成【知识点回顾】一、原子结构:原子是由居于原子中心的带的,和核外做高速运动的带的构成。
是由带的和不带电的构成。
1.每个带一个单位的正电荷2. 不带电3.每个带一个单位的负电荷4.核电荷数(原子核所带的电荷数)= 数= 数5.整个原子不带电的原因是二、核外电子的排布规律1.原子核外电子是排布的。
按照离核由到,由到把原子核外空间依次分为电子层。
离核最近的最低的是第层。
2.用可以简明方便地表示原子核外电子的排布情况。
三、离子1.钠在氯气中的燃烧实验:①现象:。
②钠+氯气→点燃氯化钠,2.离子:①叫离子②分类:离子分为带电的离子和带电的离子。
③形成:离子是形成的四、相对原子质量1. 叫相对原子质量2.相对原子质量= ,相对原子质量=【真题演练】1.(2019百色)下列粒子结构示意图中,表示阴离子的是()2.(2019聊城)下列关于微观粒子说法不正确的是()A.分子的质量一定比原子的质量大B.同种原子可以构成不同种分子C.所有原子都由原子核和核外电子构成D.原子得到或失去电子变成离子3.(2019常州)已知某氧原子的实际质量为mg,其相对原子质量为16。
有一种铕(Eu)原子的相对原子质量为152,铕(Eu)原子的质量为A.152mg16B.152m16C.152mg12D.152m124.(2019临沂)与元素的化学性质关系最密切的是()A.元素的相对原子质量B.原子的核外电子数C.元素的核电荷数D.原子的最外层电子数5.(2019岳阳)如图是两种粒子结构示意图,从图中获得的信息不正确的是()A.①和②的核外电子层数不同B.②易得到6个电子形成稳定结构C.②表示原子D.①表示阴离子6.(2019自贡)下列说法正确的是A.水变成水蒸气说明分子可以再分B.八月丹桂飘香,说明分子在不停的运动C.保持水的化学性质的最小粒子是氢原子和氧原子D.400L氧气能压缩在40L的钢瓶中,说明分子的体积变小7.(2019济宁)关于分子、原子、离子的下列说法中,错误的是()A.分子、原子、离子都是在不断运动的粒子B.分子是由原子构成的一种粒子C.分子、原子、离子都是不显电性的粒子D.分子、原子、离子都是构成物质的基本粒子8.(2019南京)下列原子结构示意图中,表示相对稳定结构的是9.(2019娄底)下列符号能表示两个氢原子的是A.2HB.2H2C.H2D.2H2O210.(2019江西)考古学家通过测定碳14的含量等方法将人类生活在黄土高原的历史推前至距今212万年。
初三化学上册《原子的结构》初三练习题 含答案

课题2 原子的结构一、选择题(每小题只有一个选项符合题意)1.下列关于原子的叙述正确的是( )A.原子由原子核和核外电子构成B.原子由原子核和中子构成C.原子由质子和电子构成D.原子由质子和中子构成2.核能已经成为一种重要的能源,氘和氚都是未来生产核能的燃料。
氚是氢元素的一种原子,氚原子的核电荷数是( )A.1B.2C.3D.43.下列原子各1×1021个,总质量最大的是( )A.氧原子B.氯原子C.氢原子D.铁原子4.下列关于原子的叙述中,错误的是( )A.原子呈电中性B.原子是实心球体C.原子由原子核与核外电子构成D.原子可以构成分子5.最近科学家发现了一种与天体中的中子星构成类似的,只由四个中子构成的粒子,这种粒子称为“四中子”,也称为“零号元素”。
有关这种粒子的说法正确的是( )A.易失去电子B.相当于一个氢分子的质量C.不显电性D.在周期表中可与氢元素占同一位6.2010年2月19日德国重粒子研究中心宣布第112号元素的符号位Cn,它的中文名称为鎶。
已知Cn的相对原子质量为277,其质子数是112,则这种原子的核外电子数为( )A.112B.165C.277D.3897.从下列图片中不能..获取的信息是( )A.分子之间有间隔B.硅原子是由原子核和电子构成的C.受热水分子运动速率加快D.构成物质的粒子有分子、原子和离子8.中科院的全超导的“人造太阳”——托克马克核聚变试验装置的调试运行成功,使我国在该领域的研究处于世界前列。
氘和氚是核聚变的原料(氘、氚原子核内都只有1个质子,但含不同数目的中子),聚变发生后,氘、氚原子核转变为氦原子核。
根据以上叙述,下列说法正确的是( )A.核聚变是化学变化B.氘原子和氚原子属于不同元素C.氘原子和氚原子是氢元素的两种不同原子D.氘原子和氚原子的相对原子质量相同9.英国科学家道尔顿最先确立了原子学说,他的中心论点主要有:①原子是不能再分的粒子;②原子是微小的实心球;③同种元素的原子,其性质和质量都相同。
初中化学 原子的结构 练习题(含答案)

初中化学原子的结构练习题(含答案)一、选择题1. 下列不属于原子的基本组成部分的是()。
A. 质子B. 中子C. 电子D. 胶子答案:D2. 原子的电子构型是()。
A. 1B. 2C. 3D. 4答案:B3. 下列不属于物质的基本性质的是()。
A. 原子数B. 元素符号C. 原子量D. 原子序数答案:B4. 原子的最外层电子数目决定了()。
A. 元素的化学性质B. 元素的物理性质C. 元素的原子量D. 元素的原子序数答案:A5. 下列元素中,原子结构相同的是()。
A. 氧、硫、硒B. 氮、氧、氟C. 硅、磷、硫D. 氢、碳、氮答案:C二、判断题1. 原子的质子数等于元素的原子序数。
答案:正确2. 电子是带正电荷的,质子是带负电荷的。
答案:错误3. 一个原子的质子数和中子数之和等于它的原子量。
答案:正确4. 在原子核外围能容纳的最多电子数目等于2n^2(n为层数)。
答案:错误5. 原子的质子和中子都存在于原子核中。
答案:正确三、填空题1. 一个氧原子包含()个质子。
答案:82. 原子的质量数等于()。
答案:质子数+中子数3. 具有相同质子数,但质量数不同的原子叫做()。
答案:同位素4. 正电荷的质子和负电荷的电子的数量是()。
答案:相等5. 原子核的直径是原子直径的()倍。
答案:约1/10四、简答题1. 什么是同位素?请举例说明。
答案:同位素是指具有相同的质子数,但质量数不同的原子。
例如,氢的三种同位素分别是氘(质子数为1,中子数为1),氢(质子数为1,中子数为0),氚(质子数为1,中子数为2)。
2. 原子的结构由哪些基本组成部分构成?各有何作用?答案:原子由质子、中子和电子构成。
质子和中子集中成核,在原子核中,质子带正电荷,中子是中性的;电子绕核而行,带负电荷。
质子和中子决定了原子的质量和核的稳定性,电子决定了原子的化学性质。
3. 为什么说原子是宇宙中最微小的物质单位?答案:原子是宇宙中最微小的物质单位,因为原子是由基本粒子构成的,而基本粒子是所有物质的最基本单位,无法再分解为更小的单位。
2018-2019学年人教版九年级化学上册 3.2原子的结构 同步练习

2018-2019学年人教版九年级上册3.2原子的结构同步练习一、单选题1.有两种原子,一种原子核内有17个质子和18个中子,另一种原子核内有17个质子和19个中子,则它们不相等的是()A. 核电荷数B. 核外电子数C. 原子质量D. 原子的带电荷量2.世界十大科技进展新闻之一是合成118号超重元素,全球学生所熟悉的元素周期表将需要作出更新.已知该元素原子的相对原子质量为293,核电荷数为118,其核内中子数和核外电子数分别为()A. 118 175B. 118 118C. 193 118D. 175 1183.如图是四种粒子的结构示意图,说法正确的是()A. ①和③属于同种元素B. ①和③表示的元素是金属元素C. ①和③化学性质相似D. ②和④表示的是阳离子4.国际化学联合会于2月19日宣布,第112号化学元素已获正式名称“Copernicium”,相应元素符号为“Cn”.化学元素周期表中又添新成员.新元素的质量约是氢原子质量的277倍,是目前获得正式承认的最重的元素,则该元素原子核内的中子数为()A. 112B. 277C. 165D. 3895.下列叙述正确的是①原子由质子和中子构成②原子不显电性③原子不能再分④原子的质子数决定元素种类⑤原子可以构成分子,也可直接构成物质()A. ①②④B. ②④⑤C. ③④D. ①②③⑤6.保持氢气化学性质的粒子是( )A. H2OB. H2C. H2SO4D. 2H7.相同数目的下列粒子中,所含电子数相等的是()A. O2﹣和Cl﹣B. OH﹣和H2OC. NH 和S2﹣D. Na+和Al8.下列关于四种粒子结构示意图的说法中正确的是()A. ①④属于同种元素B. ①属于离子,离子符号为Cl(Cl正上方写﹣1)C. ②表示的原子在化学反应中容易失去1个电子D. ①③的化学性质相似9.下列原子中的粒子,带负电荷的是()A. 电子B. 中子C. 质子D. 原子核10.如图是三种微粒的结构示意图,有关它们的说法正确的是()A. 它们都是原子B. 它们的核外都有两个电子层C. 它们是属于同种元素的微粒D. 它们的最外层电子数不同11.我国“嫦娥工程”探月计划的一个重要目标是开发月球新能源——“氦—3”(3是质量数,质量数=质子数+中子数),10吨氦—3就能满足我国一年所有的能源需求。
江苏省南京市2018届中考化学天天练 原子结构示意图(5.22,pdf)
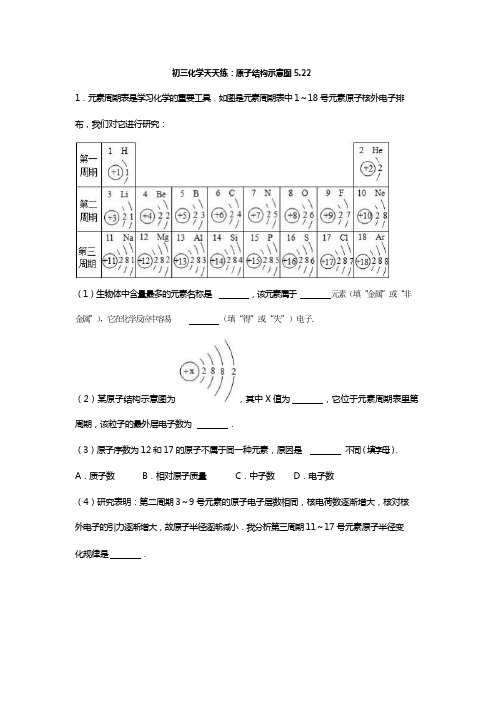
初三化学天天练:原子结构示意图 5.22
1.元素周期表是学习化学的重要工具.如图是元素周期表中 1~18 号元素原子核外电子排
布,我们对它进行研究:
(1)生物体中含量最多的元素名称是
金属”),它在化学反应中容易 ,该元素属于 (填“得”或“失”)电子. 元素(填“金属”或“非
(2)某原子结构示意图为
,其中 X 值为 ,它位于元素周期表里第
周期,该粒子的最外层电子数为
.
(3)原子序数为 12 和 17 的原子不属于同一种元素,原因是
不同(填字母).
A .质子数
B .相对原子质量
C .中子数
D .电子数
(4)研究表明:第二周期 3~9 号元素的原子电子层数相同,核电荷数逐渐增大,核对核
外电子的引力逐渐增大,故原子半径逐渐减小.我分析第三周期 11~17 号元素原子半径变
化规律是 .
答案
【解答】解:(1)生物体中含量最多的元素是氧元素,它属于非金属元素;该原子的最外层电子数是6,在化学反应中容易得电子;
(2)该原子的核外电子数是20,根据核内质子数=核外电子数,X=20;该原子有四个电子层,故位于第四周期,最外层电子数是2;
(3)原子序数为12和17的原子不属于同一种元素,原因是质子数不同;
(4)研究表明:第二周期从3号~9号元素的原子电子层数相同,核电荷数逐渐增大,核对核外电子的引力逐渐增大,故原子半径逐渐减小;利用知识迁移,则可分析第三周期从11号~17号元素原子半径变化规律是原子半径逐渐减小;
故答案为:
(1)氧;非金属;得;
(2)20;四;2;
(3)A;
(4)原子半径逐渐减小.。
2018年中考化学专题复习 原子的结构练习卷

原子的结构1.铈(Ce)是一种常见的稀土元素,已知铈原子的原子核内有58个质子和82个中子,该原子的核外电子数为A.24 B.58 C.82 D.1402.核电荷数多于核外电子数的粒子一定是A.分子B.原子C.阴离子D.阳离子3.某粒子的结构示意图如图所示,该粒子是A.Al B.Al3+C.Mg D.Mg2+4.学习完“原子的构成”之后,萍萍同学形成了以下认识,其中错误的是A.原子由居于中心的原子核和核外电子构成B.核外电子在离核远近不同的区域中运动C.原子核的质量和电子的质量相差不大D.原子核的体积与整个原子的体积相比要小很多5.图为钠的原子结构示意图。
下列说法不正确的是A.钠原子的质子数为11B.图中 n的值为10C.钠在反应中易失去电子D.钠元素位于第三周期6. 1897年,英国科学家汤姆生发现了原子内有带负电的电子,而原子是电中性的,由此推测,原子内还有带正电的物质。
在此基础上,经过卢瑟福、玻尔等科学家的不断完善和修正,建立了现代原子结构模型。
如图是小柯整理的物质微观构成网络图,则汤姆生当年推测的“带正电的物质”相当于图中的A.甲B.乙C.丙D.丁7.下列说法正确的是A.由分子构成的物质在发生化学变化时,分子种类改变,原子种类不变B.离子是带电的原子或原子团,所以带电的微粒一定是离子C.构成固体物质的微粒都是静止不动的D.与元素化学性质关系最密切的是原子的核外电子数8.下列关于四种粒子的结构示意图说法正确的是A.①、②的化学性质相似B.②所示的粒子符号为NaC.③在化学反应中易失去电子D.④中X可能为89.下列物质由离子构成的是A.Al B.H2OC.CO2D.NaCl10.2016年12月,中国在核聚变领域取得了重大突破,自然界中最容易实现的聚变反应是氢的同位素——氘与氚的聚变,氚原子的原子核内有1个质子和2个中子,该原子的核外电子数为A.0 B.1 C.2 D.311.与铝元素的化学性质关系最密切的是A.铝原子的核外电子数B.铝原子最外层电子数C.铝元素的相对原子质量D.铝元素的核电荷数12.下列关于Mg、Mg2+两种粒子的判断中不正确的是A.核电荷数相同B.质量几乎相等C.Mg2+比Mg稳定D.电子层数相同13.某元素原子A的质子数为a,已知B3+和A2﹣具有相同的核外电子数,则B元素的质子数为A.a﹣2+3 B.a﹣2﹣3C.a+2+3 D.a+2﹣314.某粒子最外层有8个电子,下列对该粒子的判断中正确的是A.一定是阳离子B.一定是阴离子C.一定是稀有气体原子D.无法确定15.如图是氯原子的结构示意图,下列说法不正确的是A.氯原子的原子核内质子数为17B.氯原子的原子核内中子数为17C.氯原子的核外有三个电子层D.氯原子的最外层电子数目影响氯元素的化学性质16.某粒子的结构示意图为,下列说法正确的是A.该粒子核外电子数为19B.该粒子带1个单位正电荷C.该粒子最外层电子数为2D.该粒子是阴离子17.2014年1月26日报道,美国正在催日本归还超过300公斤的放射物质钚。
2018年秋九年级化学上册 第三单元 课题2 原子的结构 3.2.2 原子的结构课后作业 (新版)新人教版

原子的构成课后作业1.与元素的化学性质关系最密切的是( )。
A.中子数 B.电子数C.最外层电子数 D.核外电子层数2.某原子结构示意图如图所示.下列有关该原子的说法不正确的是( )A .该原子为钠原子B .质子数和中子数总和为11C .最外层电子数为1D .核外有3个电子层3.某原子结构示意图为,则该原子核电荷数为______,核外有______个电子,第二层上有______个电子,最外层有______个电子,在化学反应中易______电子。
4.说出下列符号中数值“2”的含义。
(1)H2:________________________________。
(2)2H:________________________________。
5. 原子的结构示意图如下,下列叙述正确的是( )。
22A .原子是实心球体B .原子、中子、电子均匀分布在原子中C .质子与电子质量相等D .整个原子的质量主要集中在原子核上6.如下图是某元素的原子结构示意图,下列说法正确的是( )。
A .该原子的核外电子数是16B .该原子在化学反应中容易失去6个电子,该元素的化合价为+6价C .该元素属于非金属元素,不能与氧元素形成化合物D .该原子的最外层达到了稳定结构7.已知一种碳原子可用于测定文物的年代,该原子的原子核内含有6个质子和8个中子,则该碳原子的相对原子质量为( )。
A .2B .6C .8D .148.下列物质由离子构成的是( )。
A .汞B .氧气C .金刚石D .硫酸铜9.下列有关微观粒子的说法中正确的是 ( )。
A .分子由原子构成B .分子是保持物质化学性质的唯一粒子C .原子中的粒子都不带电D .物质都是由离子构成原子的构成课后作业参考答案1.C2.B 3.16 16 8 6 得到4.(1)表示每个氢分子由2个氢原子构成(2)表示2个氢原子5.D 6.A 7.D 8.D 9.A3。
【人教版】2018-2019学年九年级化学上册3.2原子的结构练习2含答案

课题2 原子的结构一、选择题(每小题只有一个选项符合题意)1.与元素化学性质密切相关的是( )A.质子数B.核外电子数C.电子层数D.最外层电子数2.物质是由原子、分子、离子等粒子构成。
今有一粒子,其原子核内有16个质子、16个中子,原子核外有18个电子,该粒子是( )A.原子B.阳离子C.阴离子D.分子3.下列有关分子、原子和离子的说法正确的是( )A.分子是保持物质性质的一种粒子B.分子、原子、离子都可以直接构成物质C.物体有热胀冷缩现象,主要是因为物体中的粒子大小随温度的改变而改变D.在化学反应中,任何离子都不能再分4.是某原子的结构示意图,以下说法正确的是( )A.该原子的元素符号为XB.该原子核外电子总数为4C.金刚石中含有该原子D.该种元素属于金属元素5.对于钠原子和钠离子两种粒子的比较,下列说法不正确的是( )A.它们的电子数相同B.它们的化学性质不相同C.它们的质子数相同D.它们都是构成物质的粒子6.右图是钠元素的原子结构示意图,下列叙述不正确...的是( )A.钠原子的质子数为11B.钠原子的最外层电子数为1C.钠原子易失去电子形成阳离子D.钠元素为非金属元素7.下列粒子结构示意图中,表示原子的是( )8.綦江发展将有六大特色,其中之一是“打造主城休闲避暑养生区和主城近郊最大的负氧离子库”。
空气中氧分子得到电子就能形成负氧离子(如O22-),O22-与O2不相同的是( )A.质子数B.电子数C.含氧原子个数D.相对原子质量之和9.下列说法正确的是( )A.因核外电子质量小,运动速度快,所以核外电子运动状态和宏观物体不同,没有固定的轨道,只有经常出现的区域B.在多电子的原子里,电子的能量各不相同,能量高的在离核较近的区域里运动C.最外层只有达到8个电子的结构才是稳定结构D.金属元素的最外层电子数一定少于4个,非金属元素的最外层电子数一定多于或等于4个,稀有气体元素的最外层电子数一定为8个10.右图是人体不可缺少的钙元素的原子结构示意图,则有关钙原子的下列说法中正确的是( )A.核外共有2个电子层B.在化学反应中易得电子C.核外电子总数为40D.在化学反应中易失电子二、填空题(每空2分,共30分)11.A、B、C三种元素的粒子结构示意图如下图所示(1)当A、B为原子时,x= ;y= ;(2)C表示的粒子符号是,该元素与B元素形成的化合物是由(填“分子”、“原子”、“离子”)构成的。
2018年秋九年级化学第三单元课题2原子的结构3.2.2原子的结构课后作业新版新人教版

原子的构成课后作业1.与元素的化学性质关系最密切的是( )。
A.中子数 B.电子数C.最外层电子数 D.核外电子层数2.某原子结构示意图如图所示.下列有关该原子的说法不正确的是( )A .该原子为钠原子B .质子数和中子数总和为11C .最外层电子数为1D .核外有3个电子层3.某原子结构示意图为,则该原子核电荷数为______,核外有______个电子,第二层上有______个电子,最外层有______个电子,在化学反应中易______电子。
4.说出下列符号中数值“2”的含义。
(1)H2:________________________________。
(2)2H:________________________________。
5. 原子的结构示意图如下,下列叙述正确的是( )。
A.原子是实心球体B.原子、中子、电子均匀分布在原子中C.质子与电子质量相等D.整个原子的质量主要集中在原子核上6.如下图是某元素的原子结构示意图,下列说法正确的是( )。
A.该原子的核外电子数是16B.该原子在化学反应中容易失去6个电子,该元素的化合价为+6价C.该元素属于非金属元素,不能与氧元素形成化合物D.该原子的最外层达到了稳定结构7.已知一种碳原子可用于测定文物的年代,该原子的原子核内含有6个质子和8个中子,则该碳原子的相对原子质量为( )。
A.2 B.6 C.8 D.148.下列物质由离子构成的是( )。
A.汞 B.氧气 C.金刚石 D.硫酸铜9.下列有关微观粒子的说法中正确的是 ( )。
A.分子由原子构成B.分子是保持物质化学性质的唯一粒子C.原子中的粒子都不带电D.物质都是由离子构成原子的构成课后作业参考答案1.C2.B 3.16 16 8 6 得到4.(1)表示每个氢分子由2个氢原子构成(2)表示2个氢原子5.D 6.A 7.D 8.D 9.A。
2018学年度九年级化学上册《原子的结构》习题导练(含解析)(新版)新人教版

原子的结构【巩固练习】一、选择题 (每小题只有一个选项符合题意)1.绝大多数原子的原子核中含有()A.质子、中子、电子 B.质子、电子C.中子、电子D.质子、中子2.碳的相对原子质量是()A.12g B.12 C.1.66×10-27 Kg D.1/12g3.在一个原子的原子核内必定含有的微粒是()A.质子和中子 B.质子 C.中子 D.质子和电子4.已知一个原子的核电荷数,可以推断它的()A.质子数 B.质子数和中子数之和C.中子数 D.元素的种类5.据报道,上海某医院正在研究用放射性碘治疗肿瘤.这种碘原子的核电荷数为53,相对原子质量为125.下列关于这种原子的说法中,错误的是()A.中子数为72 B.质子数为72C.电子数为53 D.质子数和中子数之和为1256.已知铯-137的质子数为55,中子数为82。
下列有关铯-137的说法正确的是()A.铯-137原子的核外电子数为82 B.铯-137的相对原子质量为137gC.铯-137原子的核电荷数为55 D.铯-137属于非金属元素7.下列叙述错误的是()A.分子和原子都能直接构成物质B.原子中原子核与核外电子的电量相等,电性相反,所以整个原子不显电性C.决定原子质量大小的主要是质子和电子D.原子核体积很小,原子内部有很大空间8.科学家在古城考古时,曾通过测定古生物遗骸中的碳14含量来推断古城年代。
碳14原子的核电荷数为6,相对原子质量为14。
下列关于碳14原子的说法中,错误的是()A.中子数为6 B.质子数为6 C.电子数为6 D.质子数和中子数之和为14二、填空题9.19世纪与20世纪之交,物理学中的放射现象和电子的先后发现,不仅将人们的视线引入了原子的内部,而且更进一步地驱使人类积极探索原子核的内部构成。
某学习小组的同学在关于原子和原子核的讨论中,下列说法正确的是。
①原子是由位于原子中心的原子核和核外电子构成的;②带负电的电子在原子核外空间里绕核运动;③原子的全部正电荷和全部质量都集中在原子核里;④原子核是由质子和中子构成的,质子的个数一定不等于中子的个数。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
课题2 原子的结构 第1课时 原子的构成01 知识管理 1.原子的构成结 构:原子⎩⎪⎨⎪⎧原子核⎩⎪⎨⎪⎧质子(每个质子带 ) (不带电)电子(每个电子带 )关 系:在原子中,核电荷数=________=________,故整个原子不显电性。
注 意:原子核内的质子数不一定等于中子数;并不是所有的原子中都有中子,如普通氢原子中没有中子。
2.原子核外电子的排布分层运动:能量低的电子在离核________的区域运动,能量高的电子在离核________的区域运动,这种现象又叫核外电子的分层排布。
电 子 层:一共分为七层,离核最近的电子层为________,最多容纳________个电子,离核最远的电子层又叫________,电子数不超过________个。
表示方法:原子结构示意图(以钠原子为例):302 1.下列粒子不属于构成原子的粒子的是 ()A .质子B .中子C .分子D .电子 2.(荆州中考)原子核中一定含有的粒子是()A .中子B .质子C .电子D .质子和中子3.(永州中考)铈(Ce)是一种常见的稀土元素,已知铈原子的原子核内有58个质子和82个中子,该原子的核外电子数为()A .24B .58C .82D .140 4.(杭州中考)如图为某原子的结构示意图,该原子的原子核中有()A .6个质子和8个中子B .8个质子和6个中子C .6个质子和8个电子D .8个质子和6个电子5.(广州中考)是某原子的结构示意图,下列关于该原子的描述正确的是 ()A .容易得到电子B .属于非金属原子C .核电荷数为11D .最外层电子数为11 6分析表中信息,下列说法正确的是()A.原子核内质子数等于中子数B.原子核都由质子和中子构成C.原子只由质子和电子构成D.原子中质子数等于核外电子数7.在分子、原子、原子核、质子、中子、电子等粒子中,找出符合下列条件的粒子填在相应横线上:(1)能直接构成纯净物的是________;(2)能保持物质化学性质的是________;(3)化学变化中最小的粒子是________;(4)带正电荷的是________;(5)带负电荷的是________;(6)不显电性的是________;(7)在同一原子中数目相等的是________。
8.氮元素的原子结构示意图为。
(1)“+7”表示________________________________________________________________________。
(2)弧线表示___________________________。
(3)弧线上的数字表示________________________。
03中档题9.(重庆A卷)同一原子中,下列说法错误的是()A.质子和电子的数目相同B.原子和中子的电性不同C.原子核和电子的质量不同D.原子核和原子的体积不同10.(百色中考)下列结构示意图所表示的粒子在化学反应中容易得到电子的是()11.(云南中考)如图是某原子的结构示意图。
下列说法不正确的是()A.该原子的质子数为12 B.该原子的核外有三个电子层C.该原子的核外电子数为12 D.该原子在化学反应中容易得到2个电子12.如图为小明制作的原子模型,外圈上小球为电子,内圈为原子核,下列说法正确的是()A.该模型表示一种碳原子B.该原子的核电荷数为4C.该原子的原子核占的体积较大D.该原子核由2个质子和2个中子构成13.(株洲中考)下图中A、B、C、D是四种粒子的结构示意图,请回答下列问题。
(1)以上四种粒子的结构示意图中,具有相同质子数的粒子是________(填字母代号)。
(2)以上四种粒子中,能得到电子的是________(填字母代号)。
(3)D粒子的名称是________;D中x=________。
14.(龙东中考)如图为原子构成示意图,请你仔细观察此图片,你从中能获得哪些信息?(答出三条信息)(1)_______________________________________________________________________________;(2)_______________________________________________________________________________;(3)_______________________________________________________________________________。
15.有A、B、C、D四种原子,它们的核电荷数依次增加且为4个连续的数。
B和D的原子核里质子数和中子数相等,A和C的原子核里质子数比中子数少1,已知B原子核外有10个电子。
(1)(2)分析表中的数据,你发现了哪些规律?①________________________________________________________________________;②________________________________________________________________________。
化学用语请画出下列原子的原子结构示意图:氢H:____________,氦He:____________,锂Li:____________,铍Be:____________,硼B:____________,碳C:____________,氮N:____________,氧O:____________,氟F:____________,氖Ne:____________,钠Na:____________,镁Mg:____________,铝Al:____________,硅Si:____________,磷P:____________。
第2课时离子和相对原子质量01知识管理1.离子定义:________的原子。
分类:________的原子是阳离子;________的原子是阴离子。
意义:(以镁离子为例)注意:原子形成离子只是核外电子的得失,核内质子数不变;失电子时电子层数减少一层,得电子时电子层数不变。
2.相对原子质量定义:以________________________为标准,其他原子的________跟它相比较所得到的比。
符号为A r。
表达式:某原子的相对原子质量(A r)=某种原子的质量一种碳原子质量×1/12关系:与构成原子的粒子之间的关系相对原子质量≈________数+________数注意:相对原子质量是原子的质量与一种碳原子质量的1/12比较得到的比值,没有质量单位,其单位是“1”,一般省略不写。
02基础题1.(曲靖中考)下列粒子结构示意图中,表示阳离子的是()2.关于相对原子质量的叙述正确的是()A.相对原子质量是一个比值,它的国际单位制单位为“1”B.相对原子质量只是一个比值,它没有单位C.相对原子质量就是原子的质量D.碳的相对原子质量是12 g3.(广州中考)如图是X的一种粒子结构示意图,下列说法正确的是()A.X是金属原子B.该粒子最外电子层已达到稳定结构C.该粒子的核电荷数为18 D.该粒子可表示为X+4.(成都中考)两种微粒的结构示意图是和其中相同的是()A.电子数B.质子数C.电子层数D.所带电荷数5.(湘西中考)某原子的结构示意图为。
(1)x=________;(2)该原子核外有________个电子层,在化学反应中易________(填“得到”或“失去”)电子。
6.下列示意图表示的粒子中,属于原子的有________(填序号,下同),属于阴离子的有________,属于阳离子的有________。
通过上图可以总结出,原子和离子的区别在于:(1)________________________________________________________________________;(2)________________________________________________________________________。
03中档题7.(鄂州中考)下列关于Mg、Mg2+两种粒子的判断中不正确的是()A.核电荷数相同B.质量几乎相等C.Mg2+比Mg稳定D.电子层数相同8.下图中微粒均是由核外电子有三层的原子形成的,依照此示意图,下列描述正确的是()A.示意图①、②、③、④表示的全部是原子结构B.示意图②中的核电荷数x=12C.示意图④若表示的是离子结构,则它的最外层电子数y=7D.示意图①的最外层电子数为8,所以它是稀有气体的原子9.(郴州中考)阳离子R2+中含有18个电子,R的相对原子质量为40,则一个R原子中所含中子数为() A.40 B.22 C.20 D.1810.(广州中考)原子的构成示意图如图,下列叙述正确的是()A.原子是实心球体B.质子、中子、电子均匀分布在原子中C.质子与电子质量相等D.整个原子的质量主要集中在原子核上11.(六盘水中考)认真分析测定相对原子质量的示意图,推断A原子的相对原子质量约为()A.12 B.16 C.5 D.1012.如图形象地表示了氯化钠的形成过程。
下列叙述中不正确的是()A.钠原子在化学反应中容易失去电子B.钠原子与钠离子都不显电性C.氯原子得到1个电子形成氯离子D.氯化钠由钠离子和氯离子构成13.(长春改编)下图是钠与氯气反应生成氯化钠的微观示意图。
请根据图示回答相关问题:(1)由图可知,原子在化学反应中的表现主要是由原子的________(填序号)决定的。
A.最外层电子数B.核外电子数C.电子层数D.质子数(2)原子得到或失去电子后转变成的离子也是构成物质的一种基本粒子,原子得失电子后电子层________(填“一定”或“不一定”)改变。
(3)生成物NaCl是由________和________(填符号)构成的。
14.(1)已知一个碳12原子的质量为m kg,另一个A原子的质量为n kg,且其中有a个质子。
则A原子中的中子数是________。
(2)已知一个碳12原子的质量为5.4 m kg,R原子的相对原子质量是n/3,则一个R原子的质量是________ kg。
(3)现以一种氧原子质量的1/16为标准,其他原子的质量跟它相比所得的比值作为这种原子的相对原子质量。
一个氧原子的质量为2.657×10-26 kg,一个铁原子的质量是9.288×10-26 kg,则铁原子的相对原子质量为________。
15.下图是核电荷数分别为1~18的原子最外层电子数与原子核电荷数的关系图。
试完成下列问题:(1)一个水分子共有________个原子核、________个质子。
