昆明理工大学植物纤维化学2007--2014,2016,2017,2019年考研真题
昆明理工大学管理学2007--2010,2012--2014年考博真题

昆明理工大学2007年秋季入学博士生招生考试试题
考试科目代码:366考试科目名称:管理学
试题适用招生专业:管理科学与工程
考生答题须知
1.所有题目(包括填空、选择、图表等类型题目)答题答案必须做在考点发给的答题纸上,做在本试题册上无效。
请考生务必在答题纸上写清题号。
2.评卷时不评阅本试题册,答题如有做在本试题册上而影响成绩的,后果由考生自己负责。
3.答题时一律使用蓝、黑色墨水笔或圆珠笔作答(画图可用铅笔),用其它笔答题不给分。
4.答题时不准使用涂改液等具有明显标记的涂改用品。
昆明理工大学2008年秋季入学博士研究生招生入学考试试
第 1 页共11 页。
昆明理工大学考研试题矿物加工工程学(2012-2016年)

昆明理工大学2012年硕士研究生招生入学考试试题(A卷)考试科目代码:806 考试科目名称:矿物加工工程学(综合)试题适用招生专业:081902 矿物加工工程、085218 矿业工程考生答题须知1.所有题目(包括填空、选择、图表等类型题目)答题答案必须做在考点发给的答题纸上,做在本试题册上无效。
请考生务必在答题纸上写清题号。
2.评卷时不评阅本试题册,答题如有做在本试题册上而影响成绩的,后果由考生自己负责。
3.答题时一律使用蓝、黑色墨水笔或圆珠笔作答(画图可用铅笔),用其它笔答题不给分。
4.答题时不准使用涂改液等具有明显标记的涂改用品。
一、名词解释(共30分,每题3分)1、品位2、选矿比3、磨矿机利用系数4、球形系数5、磁系偏角6、零电点7、浮选8、抑制剂9、疏水性矿物10、还原焙烧二、简答题(共36分,每题6分)1、矿石的选矿处理过程三个最基本的工艺过程是什么?各包括哪些内容?2、棒磨机的应用范围有哪些?3、水力旋流器的优缺点是什么?4、什么是化学选矿?其分选过程包括哪些步骤?5、起泡剂的作用有哪些?对起泡剂有哪些特殊要求?6、矿浆浓度对浮选有何影响?昆明理工大学2011年硕士研究生招生入学考试试题三、计算题(共24分,每题12分)1、某选厂采用3.2×3.1米格子型球磨机磨矿,衬板厚度100mm,问:⑴如果磨机实际工作转速为19转/分,试计算磨机转速率为多少?⑵如果磨机转速率达88%,试计算磨机实际工作转速为多少?2、某铁矿石磨至-200目74%时用磁选管选别,原矿100g,品位35%,测得磁精矿重量52g,品位60%,试计算尾矿产率和尾矿品位各是多少?四、综合题(共60分,每题30分)1、某铅锌矿矿石中主要金属矿物为方铅矿、闪锌矿、黄铜矿,并含极少量白铅矿、白红银矿、辉银矿。
脉石矿物为石英,其次为方解石、白云石等。
方铅矿呈他形晶粒或细脉状嵌布在黄铁矿、闪锌矿的间隙和裂隙中,粒度大部分在0.01~0.5mm之间。
2019年度云南省科学技术奖(科技进步奖)提名项目公示
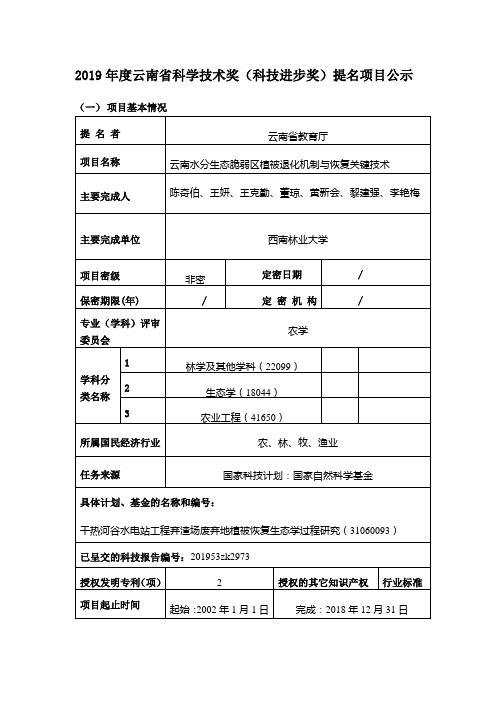
2019年度云南省科学技术奖(科技进步奖)提名项目公示(一)项目基本情况提名者云南省教育厅项目名称云南水分生态脆弱区植被退化机制与恢复关键技术主要完成人陈奇伯、王妍、王克勤、董琼、黄新会、黎建强、李艳梅主要完成单位西南林业大学项目密级非密定密日期/保密期限(年) / 定密机构/专业(学科)评审委员会农学学科分类名称1 林学及其他学科(22099)代2 生态学(18044)代3 农业工程(41650)代所属国民经济行业农、林、牧、渔业任务来源国家科技计划:国家自然科学基金具体计划、基金的名称和编号:干热河谷水电站工程弃渣场废弃地植被恢复生态学过程研究(31060093)已呈交的科技报告编号:201953zk2973授权发明专利(项)2授权的其它知识产权行业标准项目起止时间起始:2002年1月1日完成:2018年12月31日(二)项目简介为了全面改善云南干热河谷和岩溶石漠化等水分脆弱区的整体生态环境质量,落实长江经济带建设中“共抓大保护、不搞大开发”的国家战略,助推社会经济全面发展,发挥云南省在我国“两屏三带”生态安全战略格局中的作用,依托5项国家自然科学基金和1项国家林业局林业科技推广项目的研究成果及推广应用实践成果,以云南省干热河谷、岩溶石漠化为代表的水分生态脆弱区为研究对象,探明了生态退化区植被水分适宜性、水分生态承载力、土壤水分入渗和产流产沙特征、集水系统的水文生态过程,揭示了植被退化成因和生态恢复的约束条件;在自然坡面产流率、集水系统的水分生产力研究基础上,提出了集水组合、导流组合和土地整理整装的集水造林技术;通过适应性综合研究,筛选构建了以本地种为主体的乔灌结合的植被重建技术和相应模式;在人为干扰植被退化区和工程建设废弃地立地条件以及周边土壤种子库特征基础上,提出了通过封育和土壤种子库恢复以及利用客土促进废弃地植被恢复的技术。
具体技术指标如下:(1)径流小区和集水区尺度的微整地、林地及管护封禁坡面比人为干扰荒草地、坡耕地的产流量和产沙量分别减少39%和50%以上,土壤入渗性能明显改善,土壤水分含量增加,土壤水分消退时间延长。
非异氰酸酯聚氨酯合成原理及应用研究进展

林业工程学报,2023,8(4):19-26JournalofForestryEngineeringDOI:10.13360/j.issn.2096-1359.202206004收稿日期:2022-06-09㊀㊀㊀㊀修回日期:2023-03-24基金项目:云南省基础研究专项-面上项目(202201AT070045);植物纤维功能材料国家林业和草原局重点实验室开放基金(2020KFJJ12);云南省教育厅基金(2022J0490)㊂作者简介:席雪冬,男,博士,讲师,研究方向为木材胶黏剂及生物质复合材料㊂通信作者:雷洪,女,教授㊂E⁃mail:lfxgirl@163.com非异氰酸酯聚氨酯合成原理及应用研究进展席雪冬1,2,张倩玉1,3,陈实1,3,曹龙1,3,杜官本1,3,雷洪4∗(1.西南林业大学材料科学与工程学院,云南省木材胶黏剂及胶制品重点实验室,昆明650224;2.福建农林大学植物纤维功能材料国家林业和草原局重点实验室,福州350108;3.国家生物国际联合研究中心,昆明650224;4.浙江农林大学化学与材料工程学院,杭州311300)摘㊀要:传统聚氨酯(PU)是由多异氰酸酯与多元醇化合物反应制得的高分子物质,因结构可控㊁性能优良,在诸多领域中有广泛应用㊂但由于异氰酸酯的毒性及湿敏性问题,在很大程度上限制了PU的进一步发展,寻求传统PU替代物成为大势所趋,非异氰酸酯聚氨酯(NIPU)由此应运而生㊂NIPU是一种不使用异氰酸酯为原料而合成的具有氨基甲酸酯结构的新型聚氨酯化合物,其具有与传统聚氨酯相似的优良性能,且由于分子链中重复结构单元可形成分子内六元环氢键结构,使得NIPU具有较优于传统聚氨酯的化学稳定性㊁耐水解性㊁耐化学性及抗渗透性等,可作为传统聚氨酯的理想替代物之一㊂此外,NIPU合成过程中不使用高毒害物质为原料,因而成为当前聚氨酯工业领域的重点研究内容㊂笔者综述了非异氰酸酯聚氨酯的合成方法㊁反应机理及其主要应用领域的研究现状,重点阐述了其在胶黏剂,尤其是木材胶黏剂领域中的应用研究进展㊂并结合木材工业产业发展状态,及当前有关生物质原料在木材胶黏剂领域的应用研究热潮,对非异氰酸酯聚氨酯胶黏剂的发展前景做出展望㊂关键词:非异氰酸酯聚氨酯;合成方法;反应机理;胶黏剂;新型聚氨酯化合物中图分类号:TQ32㊀㊀㊀㊀㊀文献标志码:A㊀㊀㊀㊀㊀文章编号:2096-1359(2023)04-0019-08Areviewonthenon⁃isocyanatepolyurethaneanditsresearchprogressinthefieldofadhesivesXIXuedong1,2,ZHANGQianyu1,3,CHENShi1,3,CAOLong1,3,DUGuanben1,3,LEIHong4∗(1.YunnanKeyLaboratoryofWoodAdhesivesandGlueProducts,CollegeofMaterialScienceandEngineering,SouthwestForestryUniversity,Kunming650224,China;2.KeyLaboratoryofStateForestryandGrasslandAdministrationofPlantFiberFunctionalMaterials,FujianAgricultureandForestryUniversity,Fuzhou350108,China;3.InternationalJointResearchCenterforBiomassMaterials,Kunming650224,China;4.CollegeofChemistryandMaterialsEngineering,ZhejiangA&FUniversity,Hangzhou311300,China)Abstract:Traditionalpolyurethane(PU)isapolymericmaterialpreparedbythereactionofisocyanatesandpolyolcompounds.Fortheadvantagesofitscontrollablestructures,easypreparationandexcellentperformance,PUhasbeenwidelyusedinpreparingmanytypesofmaterialsandadhesivesforbondingrubber,plastic,wood,leather,fabric,paperandmanyothermaterialsinvariousfieldsnowadays.However,duetothetoxicityandhumidsensitivityofthenecessaryisocyanaterawmaterialcurrentlyusedduringthePUpreparationprocess,aswellastheissuesaboutenvi⁃ronmentalprotection,thehealthandsafetyofhumanbeingshavebeenmoreconcernedbypeopleallovertheworld,thefurtherdevelopmentofPUisnowseverelimited.IthasbecomeanirresistibletrendforseekingthereplacementofthetraditionalPUwithmoregreenproducts.Therefore,non⁃isocyanatepolyurethane(NIPU)hasbeensuccessfullysynthesizedanddeveloped.Non⁃isocyanatepolyurethaneisacompoundthatwithalsourethanestructureandsynthe⁃sizedwithoutusinghighlytoxicisocyanateasarawmaterial.Themainpreparationmethodofthenon⁃isocyanatepoly⁃urethaneisbythereactionofcycliccarbonatewithpolyaminecompounds,whichisaneasyprocesstobecarriedoutandalsoenvironmentallyfriendly.Furthermore,becausetherepeatedstructuralunitsinthemolecularchainofthesyn⁃thesizednon⁃isocyanatepolyurethanecanformtheintramolecularsix⁃memberedcyclichydrogenbondstructures,whichcausedthenon⁃isocyanatepolyurethanetobebetterchemicalstability,hydrolysisresistance,chemicalresist⁃林业工程学报第8卷ance,andpermeabilityresistancethanthetraditionalpolyurethane,itcanbeusedasanidealalternativetothetradi⁃tionalPU.Inaddition,becausethesynthesisprocessonnon⁃isocyanatepolyurethanedoesnotusehighlytoxicsub⁃stancesasrawmaterials,ithasbecomethefocusofresearchinthefieldofpolyurethaneindustry,alargenumberofstudieshavereportedthesynthesis,reactionmechanism,modificationmethodsandapplicationonnon⁃isocyanatepol⁃yurethaneresins.Tonow,non⁃isocyanatepolyurethaneresinshavebeenalreadysuccessfullyappliedinthefieldsoffoams,coating,plastic,etc.Henceinthispaper,theresearchstatusofsynthesisreactionmechanismofnon⁃isocya⁃natepolyurethaneanditsmainapplicationfieldsarereviewed.Theresearchprogressofitsapplicationinthefieldofadhesives,especiallywoodbondingadhesives,isgenerallyintroduced.ThemainproblemsandsolutionsofNIPUusedaswoodadhesivesarediscussedadditionally.Combinedwiththedevelopmentstatusofthewoodindustry,andthetrendofbiomassmaterialsappliedinpreparingwoodadhesives,thedevelopmentofnon⁃isocyanatepolyurethaneresinadhesivesisalsoprospectedinthisstudy.Keywords:non⁃isocyanatepolyurethane;syntheticmethod;reactionmechanism;adhesive;newpolyurethanecom⁃pound㊀㊀聚氨酯(PU)是分子链中含有重复氨基甲酸酯( NH COO )结构单元的一类化合物统称,通常由异氰酸酯单体与多元醇反应而成,由于性能优异且结构可调控,PU被广泛用于涂料㊁弹性体㊁泡沫材料以及胶黏剂等行业[1-2]㊂PU作为胶黏剂时,由于结构中氨基甲酸酯基㊁异氰酸酯基等极性或高反应性基团的存在,使得其能够与绝大多数含有活泼氢结构的材料以化学共价键或氢键形式结合,因此可用于橡胶㊁塑料㊁木材㊁皮革㊁织物㊁纸张等诸多材料的粘接,且胶合性能良好[3-4]㊂在木材工业领域中,由于生产加工过程中不存在甲醛释放问题,且具有施胶量少㊁胶接强度高㊁固化温度低等诸多优点而备受关注,PU胶黏剂的使用量逐年增加㊂但由于聚氨酯制备过程中使用具有高毒性㊁湿敏性且价格高昂的异氰酸酯为原料,加之异氰酸酯在合成过程中需使用毒性较大的光气等会给人类身体健康㊁自然环境造成较大危害,导致聚氨酯胶黏剂的应用推广受到一定制约[5]㊂因此,寻求更加绿色环保的聚氨酯替代物势在必行,非异氰酸酯聚氨酯(NIPU)也应运而生㊂1㊀NIPU合成反应机理NIPU是不以异氰酸酯为原料制备的含有氨基甲酸酯重复单元结构的聚氨酯㊂目前,NIPU主要的制备方法是通过环碳酸酯与多元胺类化合物反应得到,由于五元环碳酸酯的合成较六元环和七元环相对容易,所以在非异氰酸酯聚氨酯的合成研究中多采用五元环碳酸酯与脂肪胺制备,其反应机理如图1所示[6]㊂通过伯氨基对环碳酸酯中羰基的亲核进攻,得到一种四面体中间体;所形成的四面体物质继续被伯氨基进攻而除去一个H+,并使得氮原子上形成高密度电子云从而导致五元环上碳氧键断裂而开环;同时,碳上氧负离子快速与H+结合成羟基,最终形成重复单元中含氨基甲酸酯结构及β位碳原子上含有羟基的聚氨酯化合物㊂由于重复单元结构的氨基甲酸酯键中羰基氧原子可与β位碳原子上羟基通过氢键作用力形成分子内六元环结构的相对稳定状态,从而可弥补传统聚氨酯中的弱键结构特点,使得NIPU在某些性能方面优于传统聚氨酯,如耐化学性㊁耐水解性及抗渗透性等㊂图1㊀环碳酸酯与脂肪族伯胺制备NIPU反应机理[6]Fig.1㊀ReactionmechanismofNIPUfromcycliccarbonateswithaliphaticprimaryamines㊀㊀Zabalov等[7]采用量子化学计算方法研究了五元环碳酸酯与胺化合物之间的反应,揭示了反应过程中存在2种可能的过渡态㊂对比2种过渡态反应能垒的高低,从理论上证明五元环碳酸酯与胺之02㊀第4期席雪冬,等:非异氰酸酯聚氨酯合成原理及应用研究进展间的反应容易进行,且该反应总体为放热过程,反应条件简单㊂鉴于此,有关NIPU的合成研究工作大多集中在五元环碳酸酯的制备之上㊂环碳酸酯制备方法有多种,如环氧化合物CO2插入法㊁邻二醇法和邻氯醇法等(图2)㊂其中最为常用的合成方法有2种:一是以环氧化合物与CO2为原料,通过加压催化反应得到环碳酸酯;另一合成路线是采用临羟基化合物与绿色化工原料碳酸二甲酯催化反应得到㊂大量的研究工作探索了合成路径㊁反应原料㊁溶剂体系㊁催化剂㊁反应条件等因素对环碳酸酯化合物的合成影响[8-14]㊂针对环氧化合物 CO2插入法,目前可用的催化剂有多种,大体可分为均相催化体系和多相催化体系两类㊂均相催化体系主要为碱金属盐㊁铵盐等盐类化合物,金属离子配合物以及离子液体等,多相催化体系主要包括金属氧化物㊁硅酸盐类以及高分子负载型催化剂等[14]㊂同时,为有效提高环碳酸酯得率,该合成反应多在高压环境下进行,这使得该工艺方法对设备要求较高,一定程度上制约了其应用发展㊂因此,寻求新的高效催化剂并降低反应体系压力仍是该合成方法的研究重点㊂而采用邻二醇与碳酸二甲酯在金属氧化物㊁碱催化剂㊁三乙胺等催化剂作用下反应制备环碳酸酯的合成路径则相对更具优势,该反应体系对压力要求不高,加之碳酸二甲酯作为一种绿色化工原料,使得该合成工艺更为绿色环保㊂图2㊀环碳酸酯主要合成路径Fig.2㊀Mainsyntheticroutesofcycliccarbonates2㊀NIPU应用研究进展由于NIPU具有相较于传统PU的环保优势和相似性能特点,因而关于NIPU的应用研发备受人们关注㊂目前,大量研究工作围绕NIPU替代传统聚氨酯材料在泡沫材料㊁塑料㊁胶黏剂㊁涂料等领域而开展,并取得较大进展[14-16]㊂2.1㊀NIPU泡沫塑料NIPU泡沫具有与常规聚氨酯泡沫相同甚至更优的性能,因而具有巨大的市场潜力㊂Cornille等[17]通过将聚(环氧丙烷)二碳酸酯或三羟甲基丙烷三碳酸酯和脂肪胺化合物在1,5,7⁃三叠氮双环(4,4,0)癸⁃5⁃烯(TDB)催化条件下反应得到基体聚合物后,再利用聚⁃甲基氢硅氧烷为发泡剂,制备得到NIPU软质湿泡沫㊂该湿泡沫在80ħ下烘干12h㊁120ħ下后固化4h,得到表观密度在0.19 0.29g/cm3的非异氰酸酯高密度泡沫,其具有良好的抗压强度和减震性能,可用于家具或汽车行业,以及用作包装运输行业中的填充物等㊂Figovsky等[18]采用芳香族环氧树脂㊁脂肪族环碳酸酯和多胺化合物为原料,合成了具有密度低㊁抗压和抗拉伸强度大等优点的新型NIPU硬质泡沫材料㊂美国Eurotech公司在NIPU的应用研发方面处于世界领先地位,其所研制的非异氰酸酯聚氨酯泡沫已实现工业化生产[19]㊂随着 绿色化学 理念的兴起以及人们环境保护的意识不断加强,使得以生物质材料为原料进行相关应用研发在科研领域受到广泛重视,有关生物质基非异氰酸酯聚氨酯泡沫材料制备研究也随即备受关注㊂以生物质原料,如植物油[20]㊁单宁[21]㊁葡萄糖[22]㊁山梨醇[23]等合成非异氰酸酯聚氨酯并用于硬质泡沫的应用研究已有报道,但此类工作还处于实验室研究阶段,距离工业化生产还存在诸多有待攻克的难题,例如生物质基NIPU反应产物得率低㊁发泡均匀性差㊁固化温度高等㊂2.2㊀NIPU塑料塑料材料是聚氨酯物质作为泡沫之外的另一种重要应用形式,为开发PU替代物非异氰酸酯聚氨酯在塑料材料领域的应用,研究者们开展了系列研究工作㊂Ke等[24]以丙二醇二缩水甘油醚和双酚A二缩水甘油醚为原料,与CO2经加压催化反应合成环碳酸脂后,再与胺类化合物聚合,制备了一系列结构可控且机械强度及热稳定优良的杂化NIPU塑料材料㊂Kébir等[25]使用1,5,7⁃三叠氮双环(4,4,0)癸⁃5⁃烯(TDB)催化聚乙二醇和碳酸二甲酯反应得到环碳酸脂后,与二胺聚合制备得到具有良好热稳定性的NIPU弹性塑料体㊂王芳等[26]在高温高压环境下,使用四丁基溴化铵催化环氧树脂E⁃44与CO2反应合成环碳酸酯聚合物,该物质在室温条件下经三乙胺催化与己二胺反应,得到具有线性结构的NIPU热塑性材料㊂随着人们对环境保护问题的日趋重视,在科研12林业工程学报第8卷界也兴起了一场 生物质 热潮,探究以可再生生物质原料制备NIPU塑料成为非异氰酸酯聚氨酯研究领域的重点话题㊂Poussard等[27]以环氧大豆油(ESBO)与CO2为原料,经高温加压催化制备环碳酸酯(CSBO)化合物,再将其与二胺化合物通过熔融共混反应制备得到生物基NIPU塑料材料,结果表明CSBO与二胺化合物的比例直接决定所得NIPU材料的热力学性能,并且二胺分子链长与NIPU的拉伸强度和热性能有关,短的二胺分子链所形成的NIPU具有较差拉伸强度和热性能㊂冯月兰等[28]以ESBO和CO2为原料合成CSBO,详细探究了CSBO化合物的制备条件,并进一步将CSBO与二胺反应制备NIPU,探究CSBO与二胺物料配比对NIPU材料性能的影响,结果表明当两者质量比为1ʒ1时,所制生物质大豆油基NIPU材料具有最佳热学和力学性能㊂Doley等[29]以葵花籽油为原料,经氧化处理后得到环氧葵花籽油,再与CO2加压高温催化反应制备了含五元环碳酸酯结构的碳酸葵花籽油(CSFO),并将此碳酸葵花籽油与异佛尔酮二胺和环氧树脂(环氧值170 180g/eq)混合制备改性非异氰酸酯聚氨酯(HNIPU)塑料,研究显示当CSFO使用量为30%(质量分数)时所制HNIPU具有最佳力学性能;进一步使用氧化石墨烯为添加剂,制备了HNIPU纳米复合材料,该材料具有优良的力学性能㊁热稳定性以及化学稳定性,是一种优良的高性能材料㊂此外,基于NIPU塑料材料的制备合成,也有研究将NIPU或其改性材料用于静电纺丝及3D打印[30-31],这有效拓展了NIPU的应用领域,为NIPU材料的多元化应用发展奠定了基础㊂2.3㊀NIPU涂料由于PU在涂料领域具有重要应用,因此作为PU替代物的NIPU在涂料领域的应用研发也受到人们的重视㊂早在21世纪初,Figovsky等[32]即使用含有环碳酸酯基和环氧基的化合物与多元胺反应,制备了具有良好硬度和耐化学腐蚀性能的NIPU涂料,但该涂料抗紫外线效果有限㊂为解决这一问题,Figovsky等[33]以丙烯酸㊁硅氧烷环碳酸酯以及多官能度支化氨基硅氧烷化合物为原料,制备了可室温固化,黏附性能良好,且具有优异抗紫外线性能的改性NIPU涂料㊂为提升NIPU树脂涂料硬度,有研究者采用双酚A型环氧树脂E⁃51对多官能度环碳酸酯与多元胺制备的非异氰酸酯聚氨酯进行改性,制备得到环氧树脂杂化改性NIPU涂料,研究表明随着环氧树脂用量的增加,该改性NIPU涂料固化后漆膜硬度及耐溶剂性都得到了显著提高[34]㊂刘波等[35]将过甲氧基聚丙二醇环碳酸酯和环氧树脂混合后再与二乙烯三胺反应制备得到杂化NIPU⁃环氧树脂涂料,该涂料固化后形成涂膜耐冲击性能良好,且在水㊁汽油㊁盐雾浸泡数百小时后仍不起泡㊁不变色㊁不脱落,表现出优异的耐腐蚀性能和附着力㊂经过近几十年的研究,有关NIPU涂料应用研究工作取得巨大进展,已经开发了NIPU涂料作为无孔整体涂层㊁表面覆盖层等应用于混凝土㊁金属或木材等表面的抗腐蚀保护和抗磨损保护材料㊂美国Esterman㊁Lyondell㊁Eurotech等公司皆在NIPU涂料产业化应用推广方面开展了大量工作,制备了系列耐溶剂性㊁光泽性好,且硬度高的NIPU涂料产品[36-37]㊂近年来,石化资源短缺和环境保护问题的日益突出,使得可再生生物质资源材料的应用受到国内外各研究领域的重视㊂随着NIPU合成历程的不断深入发展,研究以可再生天然资源为原料制备NIPU也成为近年来非异氰酸酯聚氨酯研究领域的重点㊂在NIPU作为涂料应用领域也涌现了大量以生物质材料制备NIPU涂料的研究报道㊂其中,研究最多的是使用环氧植物油(如大豆油㊁葵花油㊁蓖麻油㊁麻风树籽油等)为原料,经CO2催化加压反应形成环碳酸酯,进而与多胺类化合物反应得到生物油基NIPU树脂,再通过添加纳米材料㊁环氧树脂㊁丙烯酸㊁硅氧烷等改性材料以提升该类NIPU涂料相关性能[38-41]㊂此外,也有研究者使用木质素㊁单宁㊁糖类㊁植物萜烯类物质为原料以制备相应NIPU树脂,并用作金属㊁木材等材料的涂饰保护,但此类NIPU涂料存在颜色深㊁固化温度较高等问题[42-44]㊂因此,尽管有关生物质基NIPU涂料应用研究已取得长足进展,相关材料性能也得到不断提升,但距离成熟的工业化产品还存在许多有待解决的技术问题㊂2.4㊀NIPU胶黏剂由于NIPU分子结构中存在氨基甲酸酯基团㊁羟基㊁氨基等极性活泼官能团,这也使得NIPU对许多材料具有良好的粘接性能,可作为胶黏剂使用㊂有关NIPU树脂在胶黏剂领域的应用研究主要集中于微电子㊁光电子器件及木材等材料的粘接㊂Figovsky[45]使用含端环碳酸酯化合物和端氨基化合物为原料,制备合成了具有良好耐水解性能的NIPU树脂微电子器件粘接用胶黏剂,通过对树脂结构分析表明,所合成NIPU分子中重复结构单元氨基甲酸酯键中羰基与相邻β位碳原子上羟基22㊀第4期席雪冬,等:非异氰酸酯聚氨酯合成原理及应用研究进展可形成氢键作用力(见图1中NIPU结构),形成分子内六元环结构,从而有效降低NIPU胶黏剂出现传统PU树脂中存在的弱键结构特点,使得NIPU胶黏剂具有更好的耐水解性㊁耐化学性以及抗渗透性等㊂Cornille等[46]分别以几种不同二元或三元环碳酸酯与二元胺反应,制备得到多种NIPU树脂胶黏剂,该胶黏剂用以粘接木材㊁铝和玻璃等材料时均表现出良好的粘接性能㊂在木材胶黏剂领域,有关NIPU胶黏剂的应用研究起步较晚,相关研究报道也较少,而以生物质材料为原料制备NIPU木材胶黏剂的报道则更少㊂为了制备更为绿色环保的NIPU木材胶黏剂,并充分利用天然生物质原材料,Xi等[47]报道了以葡萄糖为原料与碳酸二甲酯和己二胺反应制备得到葡萄糖基NIPU树脂胶黏剂,并用作胶合板的黏合,所制备的板材表现出优异的胶合强度和耐水性能,其干状剪切强度㊁24h冷水浸泡湿强度㊁63ħ温水3h浸泡湿强度以及2h沸水湿强度分别达3.15,3.62,3.34和3.38MPa,满足GB/T9846 2015‘普通胶合板“标准中相关性能要求(ȡ0.7MPa)㊂通过相关结构分析,阐明该葡萄糖基NIPU树脂制备反应机理,如图3所示㊂图3㊀葡萄糖基非异氰酸酯聚氨酯树脂反应原理[47]Fig.3㊀Preparationmechanismofglucose⁃basednon⁃isocyanatepolyurethaneresin㊀㊀基于葡萄糖制备生物质NIPU树脂胶黏剂的研究结果,Xi等[48]以来源更为广泛,价格低廉且易于获得的蔗糖为原料,与碳酸二甲酯和己二胺反应,合成了蔗糖基非异氰酸酯聚氨酯(S⁃NIPU)并用于刨花板制备,同时使用硅烷偶联剂KH560为交联剂以降低S⁃NIPU胶黏剂的固化温度㊂研究结果表明,S⁃NIPU具有优异的粘接性能和耐热性,但所需固化温度较高,当热压温度为200ħ时,所制备刨花板(ρ=0.7g/cm3)的内结合强度(IB)高达1.06MPa;通过相关热性能分析表明,添加硅烷偶联剂KH560后可以显著降低S⁃NIPU树脂的固化温度,这可确保该S⁃NIPU树脂胶黏剂能够在较低的热压温度下实现完全固化,从而实现优良的胶合性能㊂也有研究者以缩合单宁㊁碳酸二甲酯㊁己二胺为原料,通过图4中的反应流程制备了单宁基NIPU胶合板用胶黏剂㊂受限于单宁大分子结构导致的反应活性低㊁空间位阻大的原因,该单宁基NIPU胶黏剂胶合性能并不理想㊂为了提升该胶黏剂的胶合性㊁耐水性能并降低其固化温度,研究中使用二缩水甘油醚作为交联改性剂,从而制备得到具有较低固化温度,且胶合性能满足GB/T9846 2015‘普通胶合板“要求的改性单宁基NIPU木材胶黏剂[49]㊂最近亦有研究报道使用木质素㊁碳酸二甲酯㊁己二胺为原料,制备了一种同时具有支链和直链结构的木质素基非异氰酸酯聚氨酯树脂预聚物㊂该树脂被用作刨花板制备用胶黏剂,在热压温度为230ħ时显示出良好的胶接效果,但在较低固化温度时所制备的木质素基NIPU树脂固化效果不佳,板材内结合强度较差,而通过添加硅烷偶联剂可有效提高该NIPU树脂的反应性,进而实现在低于200ħ的热压温度条件下制备刨花板性能可达到相关标准要求[50]㊂32林业工程学报第8卷图4㊀单宁基非异氰酸酯聚氨酯合成机理Fig.4㊀Synthesismechanismoftannin⁃basednon⁃isocyanatepolyurethanes3㊀结㊀语随着对环保问题的日益重视,传统聚氨酯原料毒性大的问题将成为限制PU材料进一步发展的重大因素㊂非异氰酸酯聚氨酯由于合成过程中不使用高毒害物质,加之与传统PU相比具有更好的加工性能㊁水解稳定性㊁抗渗透性及耐化学品腐蚀性能等,将会作为传统PU的有效替代物而得到巨大广泛适用㊂此外,由于当今石油资源供应日趋紧张,充分开发利用可再生生物质材料将成为大势所趋㊂因此,研究以相关生物质原料,如单宁㊁木质素㊁糖类㊁植物油等制备合成性能优良的NIPU材料将成为聚氨酯工业领域的重点研究课题,尤其是如何有效提高生物质基NIPU产物得率㊁降低固化反应温度㊁优化合成工艺㊁改善其综合性能等问题将是现阶段主要研究工作㊂而随着研究的不断深入,有关生物质基NIPU的合成工艺㊁材料制备方法等定将不断趋于成熟,多元化NIPU材料产品也将会不断涌现,并替代现有传统PU材料而应用于众多行业中㊂参考文献(References):[1]王乔逸,展雄威,陆少锋,等.聚氨酯发展及改性研究现状[J].纺织科技进展,2021(4):1-10.DOI:10.19507/j.cnki.1673-0356.2021.04.001.WANGQY,ZHANXW,LUSF,etal.Researchstatusofde⁃velopmentandmodificationofpolyurethane[J].ProgressinTextileScience&Technology,2021(4):1-10.[2]马萍萍.聚氨酯材料的应用研究进展[J].化工设计通讯,2021,47(1):36-37.DOI:103969/j.issn.1003-6490.2021.01.019.MAPP.Applicationandresearchprogressofpolyurethanemate⁃rials[J].ChemicalEngineeringDesignCommunications,2021,47(1):36-37.[3]徐海翔.聚氨酯胶黏剂综述[J].橡塑资源利用,2018(3):25-33.DOI:CNKI:SUN:TJXJ.0.2018-03-006.XUHX.Reviewofpolyurethaneadhesives[J].Rubber&PlasticsResourcesUtilization,2018(3):25-33.[4]朱俊.聚氨酯胶粘剂主要应用领域现状及发展趋势[J].化学工业,2013,31(11):34-38.DOI:10.3969/j.issn.1673-9647.2013.11.008.ZHUJ.Thepresentsituationofmainapplicationfieldsofpolyure⁃thaneadhesivesanditsdevelopmenttrend[J].ChemicalIndustry,2013,31(11):34-38.[5]ARISTRIMA,LUBISMAR,YADAVSM,etal.Recentde⁃velopmentsinlignin⁃andtannin⁃basednon⁃isocyanatepolyurethaneresinsforwoodadhesives areview[J].AppliedSciences,2021,11(9):4242.DOI:10.3390/app11094242.[6]杨玉姿,徐丹,雍奇文,等.非异氰酸酯聚氨酯研究综述[J].聚氨酯工业,2020,35(5):5-8.DOI:10.3969/j.issn.1005-1902.2020.05.002.YANGYZ,XUD,YONGQW,etal.Areviewofresearchonnon⁃isocyanatepolyurethane[J].PolyurethaneIndustry,2020,35(5):5-8.[7]ZABALOVMV,LEVINAMA,TIGERRP.Polyurethaneswithoutisocyanatesandisocyanateswithoutphosgeneasanewfieldofgreenchemistry:mechanism,catalysis,andcontrolofre⁃activity[J].RussianJournalofPhysicalChemistryB,2019,13(5):778-788.DOI:10.1134/S1990793119050129.[8]KIHARAN,ENDOT.Synthesisandpropertiesofpoly(hydroxyurethane)S[J].JournalofPolymerSciencePartA:PolymerChemistry,1993,31(11):2765-2773.DOI:10.1002/pola.1993.080311113.[9]TOMITAH,SANDAF,ENDOT.Structuralanalysisofpoly⁃hydroxyurethaneobtainedbypolyadditionofbifunctionalfive⁃memberedcycliccarbonateanddiaminebasedonthemodelreac⁃tion[J].JournalofPolymerSciencePartA:PolymerChemistry,2001,39(6):851-859.DOI:10.1002/1099-051842㊀第4期席雪冬,等:非异氰酸酯聚氨酯合成原理及应用研究进展(20010315)39:6<851:AID-POLA1058>3.0.CO;2-3.[10]BIRUKOVAO,POTASHNIKOVAR,LEYKINA,etal.Advan⁃tagesinchemistryandtechnologyofnon⁃isocyanatepolyurethane[J].Journal ScientificIsrael⁃TechnologicalAdvantages ,2014,16(3):92-99.[11]CAMARAF,BENYAHYAS,BESSEV,etal.Reactivityofsec⁃ondaryaminesforthesynthesisofnonisocyanatepolyurethanes[J].EuropeanPolymerJournal,2014,55:17-26.DOI:10.1016/j.eurpolymj.2014.03.011.[12]BLATTMANNH,FLEISCHERM,BÄHRM,etal.Isocyanate⁃andphosgene⁃freeroutestopolyfunctionalcycliccarbonatesandgreenpolyurethanesbyfixationofcarbondioxide[J].Macromo⁃lecularRapidCommunications,2014,35(14):1238-1254.DOI:10.1002/marc.201400209.[13]BOYERA,CLOUTETE,TASSAINGT,etal.SolubilityinCO2andcarbonationstudiesofepoxidizedfattyaciddiesters:towardsnovelprecursorsforpolyurethanesynthesis[J].GreenChemistry,2010,12(12):2205-2213.DOI:10.1039/C0GC00371A.[14]KATHALEWARMS,JOSHIPB,SABNISAS,etal.Non⁃iso⁃cyanatepolyurethanes:fromchemistrytoapplications[J].RSCAdvances,2013,3(13):4110-4129.DOI:10.1039/C2RA21938G.[15]袁野,王强,欧阳春发,等.非异氰酸酯聚氨酯的最新研究进展[J].聚氨酯工业,2015,30(1):5-8.DOI:10.3969/j.issn.1005-1902.2015.01.002.YUANY,WANGQ,OUYANGCF,etal.Thenewresearchprogressofnonisocyanatepolyurethane[J].PolyurethaneIndustry,2015,30(1):5-8.[16]HALIMAK,SAJIDI,MOHDI,etal.Areviewontheproduc⁃tion,propertiesandapplicationsofnon⁃isocyanatepolyurethane:agreenerperspective[J].ProgressinOrganicCoatings,2021,154:106124.DOI:10.1016/j.porgcoat.2020.106124.[17]CORNILLEA,DWORAKOWSKAS,BOGDALD,etal.Anewwayofcreatingcellularpolyurethanematerials:NIPUfoams[J].EuropeanPolymerJournal,2015,66:129-138.DOI:10.1016/j.eurpolymj.2015.01.034.[18]FIGOVSKYO,SHAPOVALOVL,LEYKINA,etal.Recentad⁃vancesinthedevelopmentofnon⁃isocyanatepolyurethanesbasedoncycliccarbonates[J].InternationalLettersofChemistryPhysics&Astronomy,2012,30(4):256-263.[19]贺文媛,顾尧.非异氰酸酯聚氨酯的研究进展及应用[J].聚氨酯工业,2011,26(1):1-4.DOI:10.3969/j.issn.1005-1902.2011.01.001.HEWY,GUY.Researchprogressandapplicationofnonisocya⁃natepolyurethaneapplication[J].PolyurethaneIndustry,2011,26(1):1-4.[20]MALIKM,KAURR.SynthesisofNIPUbythecarbonationofcanolaoilusinghighlyefficient5,10,15⁃tris(pentafluorophenyl)corrolato⁃Manganese(Ⅲ)complexasnovelcatalyst[J].PolymersforAdvancedTechnologies,2018,29(3):1078-1085.DOI:10.1002/pat.4219.[21]CHENXY,XIXD,PIZZIA,etal.Preparationandcharacter⁃izationofcondensedtanninnon⁃isocyanatepolyurethane(NIPU)rigidfoamsbyambienttemperatureblowing[J].Polymers,2020,12(4):750.DOI:10.3390/polym12040750.[22]XIXD,PIZZIA,GERARDINC,etal.Glucose⁃biobasednon⁃i⁃socyanatepolyurethanerigidfoams[J].JournalofRenewableMa⁃terials,2019,7(3):301-312.DOI:10.32604/jrm.2019.04174.[23]JAMESHC,THOMASJF,IANDVI,etal.Renewableself⁃blowingnon⁃isocyanatepolyurethanefoamsfromlysineandsorbitol[J].EuropeanJournalofOrganicChemistry,2018,2018(31):4265-4271.DOI:10.1002/ejoc.201800665.[24]KEJX,LIXY,WANGF,etal.Non⁃isocyanatepolyurethane/epoxyhybridmaterialswithdifferentandcontrolledarchitecturespreparedfromaCO2⁃sourcedmonomerandepoxyviaanenviron⁃mentally⁃friendlyroute[J].RSCAdvances,2017,7(46):28841-28852.DOI:10.1039/C7RA04215A.[25]KÉBIRN,NOUIGUESS,MORANNEP,etal.Nonisocyanatethermoplasticpolyurethaneelastomersbasedonpoly(ethylenegly⁃col)preparedthroughthetransurethanizationapproach[J].JournalofAppliedPolymerScience,2017,134(45):44991-44999.DOI:10.1002/app.44991.[26]王芳,阮家声,张宏元,等.一种非异氰酸酯聚氨酯的合成与表征[J].粘接,2008,29(6):6-10.DOI:10.3969/j.issn.1001-5922.2008.06.002.WANGF,RUANJS,ZHANGHY,etal.Synthesisandcharac⁃terizationofakindofnonisocyanatepolyurethane[J].AdhesioninChina,2008,29(6):6-10.[27]POUSSARDL,MARIAGEJ,GRIGNARDB,etal.Non⁃isocya⁃natepolyurethanesfromcarbonatedsoybeanoilusingmonomericoroligomericdiaminestoachievethermosetsorthermoplastics[J].Macromolecules,2016,49(6):2162-2171.DOI:10.1021/acs.macromol.5b02467.[28]冯月兰,王军威,亢茂青,等.环氧大豆油和CO2合成环状碳酸酯及NIPU的研究[J].聚氨酯工业,2017,32(1):12-15.DOI:10.3969/j.issn.1005-1902.2017.01.006.FENGYL,WANGJW,KANGMQ,etal.Thesynthesisofcy⁃cliccarbonateandnon⁃isocyanatepolyurethanefromESBOandCO2[J].PolyurethaneIndustry,2017,32(1):12-15.[29]DOLEYS,SARMAHA,SARKARC,etal.Insitudevelopmentofbio⁃basedpolyurethane⁃blend⁃epoxyhybridmaterialsandtheirnanocompositeswithmodifiedgrapheneoxidevianon⁃isocyanateroute[J].PolymerInternational,2018,67(8):1062-1069.DOI:10.1002/pi.5612.[30]ROKICKIG,PARZUCHOWSKIPG,MAZUREKM.Non⁃isocy⁃anatepolyurethanes:synthesis,properties,andapplications[J].PolymersforAdvancedTechnologies,2015,26(7):707-761.DOI:10.1002/pat.3522.[31]STACHAKP,ŁUKASZEWSKAI,HEBDAE,etal.Recentad⁃vancesinfabricationofnon⁃isocyanatepolyurethane⁃basedcom⁃positematerials[J].Materials(Basel,Switzerland),2021,14(13):3497.DOI:10.3390/ma14133497.[32]FIGOVSKYOL,SHAPOVALOVLD.Featuresofreactionamino⁃cyclocarbonateforproductionofnewtypenonisocyanatepolyurethanecoatings[J].MacromolecularSymposia,2002,187(1):325-332.DOI:10.1002/1521-3900(200209)187:1<325:AID-MASY325>3.0.CO;2-L.[33]FIGOVSKYO,SHAPOVALOVL,BUSLOVF.Ultravioletandthermostablenon⁃isocyanatepolyurethanecoatings[J].SurfaceCoatingsInternationalPartB:CoatingsTransactions,2005,88(1):67-71.DOI:10.1007/BF02699710.[34]WANGC,WUZ,TANGL,etal.Synthesisandpropertiesofcy⁃cliccarbonatesandnon⁃isocyanatepolyurethanesunderatmosphericpressure[J].ProgressinOrganicCoatings,2019,127:359-365.DOI:10.1016/j.porgcoat.2018.11.040.52林业工程学报第8卷[35]刘波,周莉,赵彦芝,等.非异氰酸酯聚氨酯⁃环氧树脂涂膜的制备及性能研究[J].精细化工,2010,27(7):639-641.DOI:10.13550/j.jxhg.2010.07.016.LIUB,ZHOUL,ZHAOYZ,etal.PreparationandpropertiesresearchofNIPU⁃epoxyresins[J].FineChemicals,2010,27(7):639-641.[36]GOMEZ⁃LOPEZA,ELIZALDEF,CALVOI,etal.Trendsinnon⁃isocyanatepolyurethane(NIPU)development[J].ChemicalCommunications(Cambridge,England),2021,57(92):12254-12265.DOI:10.1039/d1cc05009e.[37]陈云龙.非异氰酸酯聚氨酯泡沫的应用及进展[J].科技创新导报,2018,15(27):108,110.DOI:10.16660/j.cnki.1674-098X.2018.27.108.CHENYL.Applicationandprogressofnon⁃isocyanatepolyure⁃thanefoam[J].ScienceandTechnologyInnovationHerald,2018,15(27):108,110.[38]TAMAMIB,SOHNS,WILKESGL.Incorporationofcarbondi⁃oxideintosoybeanoilandsubsequentpreparationandstudiesofnonisocyanatepolyurethanenetworks[J].JournalofAppliedPol⁃ymerScience,2004,92(2):883-891.DOI:10.1002/app.20049.[39]马超,李国荣.以可再生资源为原料的环氧⁃非异氰酸酯聚氨酯杂化涂料的制备[J].涂料工业,2013,43(7):47-51.DOI:10.3969/j.issn.0253-4312.2013.07.011.MAC,LIGR.Thepreparationofepoxy⁃NIPUhybridcoatingbyusingrenewableresources[J].Paint&CoatingsIndustry,2013,43(7):47-51.[40]YANGXX,WANGSB,LIUXX,etal.Preparationofnon⁃isocyanatepolyurethanesfromepoxysoybeanoil:dualdynamicnetworkstorealizeself⁃healingandreprocessingundermildcon⁃ditions[J].GreenChemistry,2021,23(17):6349-6355.DOI:10.1039/D1GC01936H.[41]HANIFFAMACM,CHINGYC,CHUAHCH,etal.Synthe⁃sis,characterizationandthesolventeffectsoninterfacialphenom⁃enaofJatrophacurcasoilbasednon⁃isocyanatepolyurethane[J].Polymers,2017,9(5):162.DOI:10.3390/polym9050162.[42]YUAZ,SETIENRA,SAHOUANIJM,etal.Catalyzednon⁃isocyanatepolyurethane(NIPU)coatingsfrombio⁃basedpoly(cycliccarbonates)[J].JournalofCoatingsTechnologyandRe⁃search,2019,16(1):41-57.DOI:10.1007/s11998-018-0135-7.[43]LEEA,DENGYL.Greenpolyurethanefromligninandsoybeanoilthroughnon⁃isocyanatereactions[J].EuropeanPolymerJour⁃nal,2015,63:67-73.DOI:10.1016/j.eurpolymj.2014.11.023.[44]THÉBAULTM,PIZZIA,ESSAWYHA,etal.Isocyanatefreecondensedtannin⁃basedpolyurethanes[J].EuropeanPolymerJournal,2015,67:513-526.DOI:10.1016/j.eurpolymj.2014.10.022.[45]FIGOVSKYOL.Hybridnonisocyanatepolyurethanenetworkpol⁃ymersandcompositesformedtherefrom[P].US:US6120905,2000-09-19.[46]CORNILLEA,MICHAUDG,SIMONF,etal.Promisingme⁃chanicalandadhesivepropertiesofisocyanate⁃freepoly(hydroxyurethane)[J].EuropeanPolymerJournal,2016,84:404-420.DOI:10.1016/j.eurpolymj.2016.09.048.[47]XIXD,PIZZIA,DELMOTTEL.Isocyanate⁃freepolyurethanecoatingsandadhesivesfrommono⁃anddi⁃saccharides[J].Poly⁃mers,2018,10(4):402.DOI:10.3390/polym10040402.[48]XIXD,WUZG,PIZZIA,etal.Non⁃isocyanatepolyurethaneadhesivefromsucroseusedforparticleboard[J].WoodScienceandTechnology,2019,53(2):393-405.DOI:10.1007/s00226-019-01083-2.[49]CHENXY,PIZZIAP,FREDONE,etal.Lowcuringtempera⁃turetannin⁃basednon⁃isocyanatepolyurethane(NIPU)woodad⁃hesives:preparationandpropertiesevaluation[J].InternationalJournalofAdhesionandAdhesives,2021,112:103001.DOI:10.1016/j.ijadhadh.2021.103001.[50]SARAŽINJ,PIZZIA,AMIROUS,etal.Organosolvligninfornon⁃isocyanatebasedpolyurethanes(NIPU)aswoodadhesive[J].JournalofRenewableMaterials,2021,9(5):881-907.DOI:10.32604/jrm.2021.015047.(责任编辑㊀李琦)62。
昆明理工大学考研历年真题之工程力学2007--2014年考研真题

昆明理工大学2007年硕士研究生招生入学考试试题(A卷)
考试科目代码:845 考试科目名称:工程力学
试题适用招生专业:农业机械化工程、农业生物环境与能源工程、农业电气化与自动化
考生答题须知
1.所有题目(包括填空、选择、图表等类型题目)答题答案必须做在考点发给的答题纸上,做在本试题册上无效。
请考生务必在答题纸上写清题号。
2.评卷时不评阅本试题册,答题如有做在本试题册上而影响成绩的,后果由考生自己负责。
3.答题时一律使用蓝、黑色墨水笔或圆珠笔作答(画图可用铅笔),用其它笔答题不给分。
4.答题时不准使用涂改液等具有明显标记的涂改用品。
年硕士研究生招生入学考试试题
第 1 页共68 页。
《十种鼠尾草属植物萜类化学成分与生物活性》项目信息

《十种鼠尾草属植物萜类化学成分与生物活性》项目信息1、项目名称:十种鼠尾草属植物萜类化学成分与生物活性2、完成单位:中国科学院昆明植物研究所、昆明理工大学主要完成人员:赵勤实(中国科学院昆明植物研究所),许刚(中国科学院昆明植物研究所),潘争红(中国科学院昆明植物研究所),李蓉涛(昆明理工大学),蒋永俊(昆明理工大学)3、提名意见:鼠尾草属植物是重要的植物类群,具有重要的药用、食用和观赏价值。
我国鼠尾草属资源丰富,云南是该属植物最多的省份,研究该属植物化学成分与生物活性具有重要的科学价值。
该项目系统地研究了十种鼠尾草属植物萜类化学成分与生物活性,项目重要科学发现包括:(1)研究发现7种中国原产鼠尾草属植物萜类成分主要是松香烷二萜和倍半萜,3种外来植物萜类重要特征成分是克罗烷型二萜,这为分类学提供了重要的化学依据,同时为开发利用提供了物质基础科学依据;(2)发现65个新化合物,并报道122已知化合物,其中7个新化合物为骨架新颖的化合物。
其中przewalskin A和B引起有机合成家的关注和合成,为这两个化合物开发利用提供了重要基础;(3)发现活性化合物物17个,涉及抗病毒、细胞毒活性和神经保护活性,为进一步研究提供了重要基础。
项目发表的20篇核心论文均为SCI收录的论文,8篇代表性论文均发表在本领域知名国际期刊,其中3篇发表在Nature index 期刊Organic Letter和Chemical communication。
20篇核心论文他引246次。
培养6名博士研究生和1名硕士研究生,其中2名博士研究生已经晋升为研究员。
该项目完成为我国鼠尾草属化学成分与生物活性研究做出了重要贡献,该成果拟提名云南省科学技术奖(自然科学)二等奖。
4、项目简介:鼠尾草属(Salvia Linn.)是唇形科(Labiatae)最大的一属植物类群,主要分布在温带和热带地区。
全球约有1000种左右,主要分布在中南美洲、其次是西亚、欧洲、东亚和北美。
第二章_植物纤维

初生层:约束和保护作用
纤维的初生细胞壁,由 网状原纤组成。对棉纤维 整体起约束机械性质 (1)棉纤维在加厚期淀积而成的部 分,几乎都是纤维素。
(2)纤维素逐日淀积一层形成了棉 纤维的日轮。
(3)与棉纤维的成熟度、天然转曲 有关。(纤维素以束状小纤维的形态
与纤维轴倾斜呈螺旋形,在纤维长度方 向上有左有右,使得棉纤维有天然转 曲。)
日轮
中腔:影响颜色、保暖性等 (1)纤维停止生长后,胞壁内遗留下来的空隙。
同一品种的棉纤维,外周长大致相等,次生层 厚时中腔就小,次生层薄时中腔就大。 (2)含有少量原生质和细胞核残余,对棉纤维的 颜色有影响。
(2)加厚期:细胞壁由外向里逐日螺旋淀积纤维素,最 后留有中腔,与成熟度有关。(35-55天)
(3)转曲期:棉纤维干涸后,胞壁产生扭转,形成不规 则的螺旋形,称为天然转曲。
一定条件下形成“短绒”、“不孕籽”。 影响棉纤维长度的因素:品种、生长条件、后加工。
9
2.棉纤维的形状特征 (1) 纵向形态:
截面接近圆形时,常用这些指标,单位(μm)。 非圆形的面纤维,可用理论直径来表示。
DC
D:理论直径;C-周长;
测量方法:显微镜切片法。
38
(2) 间接指标
①特克斯(定长制 ):1000米长的纤维所具有的质量克数
公式:
G Ntex L 1000
长绒棉:0.12-0.14tex;细绒棉:0.15-0.2tex
1. 长度 2. 细度 3. 成熟度 4. 强度 5. 天然转曲 6. 原棉的水分、杂质与疵点 7. 综合检验
连续化肥减量配施有机肥提升植烟土壤肥力质量的综合评价

70 中国土壤与肥料 2024 (1)doi:10.11838/sfsc.1673-6257.22786连续化肥减量配施有机肥提升植烟土壤肥力质量的综合评价余顺平1,熊于斌1,廖 涛1,张诗卿1,汤 利1,2*,李少明1*(1.云南农业大学资源与环境学院,云南 昆明 650201; 2.农业农村部云南耕地保育科学观测实验站,云南 昆明 650201)摘 要:为准确评价连续多年化肥减量配施有机肥料对烤烟产量及植烟土壤综合肥力质量的影响,探究植烟土壤质量提升与烤烟绿色优质协同的化肥减量有机替代技术。
以长期定位试验的第7年数据为基础,运用因子分析法、相关系数法、内梅罗指数法,对不施肥(CK)、当地推荐常规施肥(100%化肥,CF)、化肥减量20%配施有机肥(OF)和配施生物有机肥(BIO)4个处理的土壤肥力质量进行综合评价,并采用随机森林回归分析,探讨各土壤单项肥力指标对烤烟产量的解释度。
结果表明,在连续7年化肥减量20%条件下,配施有机肥和生物有机肥均能降低烤烟青枯病和黑胫病的发病率和病情指数,提高烤烟经济性状、产量可持续性与稳定性,提高植烟土壤养分含量和土壤肥力综合质量。
随机森林分析表明,植烟土壤有效磷、碱解氮、全氮是影响烤烟产量的决定因素,其解释率分别为19.66%、15.38%、12.07%。
在3种评价方法下,植烟土壤综合肥力指数IFI 值均表现为BIO>OF>CF>CK,BIO 和OF 处理较CF 处理分别提高23.03%~31.75%和4.92%~7.94%。
3种评价方法的IFI 值与烤烟相对产量均呈显著或极显著正相关关系,相关系数大小依次为内梅罗指数法(0.884)>因子分析法(0.867)>相关系数法(0.747)。
因此,连续多年化肥减量配施不同有机肥具有提高植烟土壤综合肥力质量和烤烟产量及质量的持续效应,且以化肥减量20%配施生物有机肥的效果最优。
关键词:化肥减量;植烟土壤综合肥力质量评价;内梅罗指数法;因子分析法;相关系数法收稿日期:2022-12-15;录用日期:2023-04-07基金项目:云南省重大科技专项计划(202102AE090030,202202AE 090025)。
某理工大学《食品化学》考试试卷(906)

某理工大学《食品化学》课程试卷(含答案)__________学年第___学期考试类型:(闭卷)考试考试时间:90 分钟年级专业_____________学号_____________ 姓名_____________1、判断题(75分,每题5分)1. 叶绿素是水溶性的,有a、b两种结构,其结构中存在一个大的共轭体系。
()答案:错误解析:2. 柠檬酸和EDTA可用来降低pH和络合金属离子。
当用量适当时既可抑制酶促褐变,又可抑制非酶褐变。
()[昆明理工大学2018研]答案:正确解析:柠檬酸属于有机酸,能够降低体系pH。
在酶促褐变当中,既能够抑制酚酶的活性,又能够与酚酶辅基的铜离子络合而抑制其活性。
在非酶褐变当中,美拉德反应在低pH中反应不明显。
EDTA作为金属螯合剂,在酶促褐变与非酶褐变中都能够螯合参与反应的金属离子从而达到抑制褐变的效果。
3. 蛋白质溶胶是一种胶体溶液,不连续相为带水胶体。
()答案:正确解析:蛋白质溶胶是指蛋白质在水中形成的一种比较稳定的亲水胶体,属于胶体系统。
4. 抗氧化剂应尽早加入。
()答案:正确解析:5. 氧化剂的存在会使二硫键形成,有利于面团的弹性和韧性。
()[沈阳农业大学2017研]答案:正确解析:添加氧化剂如溴酸盐可使蛋白质形成分子间二硫键,面团的韧性和弹性会增强。
6. 通常蛋白质的起泡能力好,则稳定泡沫的能力也好。
()答案:错误解析:7. 小分子糖的增塑作用,对防止焙烤食品老化、减轻食品蛋白质的变性是十分有益的。
()[昆明理工大学2018研]答案:错误解析:防止淀粉老化可以选用小分子糖作为增塑剂,但小分子增塑剂与淀粉之间相互作用的稳定性较差,制备的热塑性淀粉易重结晶,导致材料老化变脆,而失去其实际应用的价值。
而增塑剂对于蛋白质的变性是没有减轻的作用的。
8. 乳化剂的亲水亲油能力,用亲水亲油平衡(HLB)表示,混合乳化剂的HLB是可加和的。
()[沈阳农业大学2017研]答案:正确解析:亲水亲油平衡(HLB)是用来表征亲水亲油能力的指标,HLB 值越小,亲油性越强;反之,亲水性越强。
某理工大学《食品化学》考试试卷(109)

某理工大学《食品化学》课程试卷(含答案)__________学年第___学期考试类型:(闭卷)考试考试时间:90 分钟年级专业_____________学号_____________ 姓名_____________1、判断题(75分,每题5分)1. 植物中(尤其谷类、豆类)的P主要以植酸的形式存在。
()答案:错误解析:植物中的P主要以植酸盐的形式存在。
2. 维生素B2和维生素C共存时,维生素B2可抑制维生素C的分解。
()答案:错误解析:3. 糖溶液冰点下降的程度与浓度呈正相关,与分子量呈负相关。
()[昆明理工大学2018研]答案:正确解析:将糖加入到水中会引起冰点的降低,且糖溶液冰点下降的程度与浓度呈正相关,与分子量呈负相关。
4. 温度范围10~40℃最能刺激味觉,30℃最为敏感,50℃感觉迟钝。
()答案:正确解析:5. 细胞外起作用的维生素E与细胞内起作用的维生素C都有较强的抗氧化能力。
()答案:正确解析:6. 酸奶的制作是因为pH降低引起蛋白质变性引起的。
()[浙江大学2018、2019研]答案:正确解析:酸奶的制作原理是:乳酸菌发酵产生大量乳酸,乳酸使奶中酪蛋白胶粒中的胶体磷酸钙转变成可溶性磷酸钙,从而使酪蛋白胶粒的稳定性下降,并在pH4.6~4.7时,酪蛋白变性凝固,形成酸奶。
因此,酸奶的制作是因为pH降低引起蛋白质变性引起的。
7. 直链淀粉在水溶液中是线性分子。
()解析:8. 加入食盐能提高大豆蛋白的起泡能力和泡沫稳定性。
()答案:错误解析:加入食盐能提高大豆蛋白的起泡能力,降低其泡沫稳定性。
9. 单糖都具有旋光性。
()[沈阳农业大学2017研]答案:错误解析:单糖中的二羟丙酮没有旋光性。
10. 就溶解性而言,胡萝卜素不溶于水,叶黄素类溶于水。
()答案:错误解析:11. 所有的类胡萝卜素都是脂溶性色素。
()答案:错误解析:类胡萝卜素多数不溶于水,溶于脂溶剂,不稳定,易氧化。
但也存在稀有的水溶性类胡萝卜素,如北虫草黄素。
高等植物中一碳化合物代谢研究进展

西北植物学报,2009,29(6):1284-1289Acta Bot.Boreal.-Occident.Sin.文章编号:1000-4025(2009)06-1284-06高等植物中一碳化合物代谢研究进展徐 迪,陈丽梅*,年洪娟,梅 岩(昆明理工大学生命科学与技术学院生物工程技术研究中心,昆明650224)摘 要:高等植物中一碳(C1)化合物的代谢主要包括甲醇代谢、甲醛代谢和甲酸代谢等,它们是高等植物一碳单位代谢的重要组成部分.由于C1化合物的代谢机制复杂、代谢规模非常小、参与代谢反应的酶和中间产物的含量低且不稳定等特点,相关研究报道很有限.现代生化和分子遗传学方法的综合使用使得人们对参与植物中C1化合物代谢的酶和基因有了一定程度的了解,该文主要综述了近年来有关高等植物中内源和外源C1化合物甲醇、甲醛和甲酸的来源和代谢途径方面的研究进展,并提出了该研究领域目前存在的问题和今后的研究方向.关键词:高等植物;一碳化合物;甲醇代谢;甲醛代谢;甲酸代谢中图分类号:Q945.18文献标识码:AResearch Progresses on One-carbon CompoundMetabolism in Higher PlantsXU Di,CH EN L-i m ei*,N IAN H ong-juan,M EI Yan(Biotechnology Research C enter,College of Life Science and Technology,Kunming U nivers ity of Science and T echnology,Kun-min g650224,Chin a)Abstract:T he metabolism of one-car bon compounds(C1co mpo unds)in hig her plants m ainly includes methanol m etabolism,fo rmaldehyde metabolism and fo rmic acid metabolism,w hich is an im po rtant part in C1unit metabolism s.H ow ever,because o f their com plex metabolic mechanisms,the very sm al-l scale me-tabolism,and their enzy mes and intermediates tending to be labile and low in abundance,the studies o n C1 com po unds m etabo lism in plants are very po or.Fortunately,the integ ration o f molecular and genetic ap-proaches w ith biochem ical ones allow ed certain understanding of enzy mes and g enes involv ed in C1com-pound m etabolism s in hig her plants.T his paper review ed the recent research prog ress on the endo geno us and ex ogenous C1compound metabolic pathw ays in higher plants,as w ell as the various enzy mes and meta-bolic interm ediates invo lved in these m etabo lic pathw ays.Key words:hig her plants;C1com pounds;m ethanol m etabolism;form aldehy de metabolism;for mic acid me-tabolism高等植物中的一碳(C1)化合物主要包括甲醇、甲醛和甲酸.在正常的生长发育过程中,植物体内会产生甲醇,除了部分从气孔中释放外,植物还能通过自身的甲醇代谢反应将剩余甲醇消耗掉,防止甲醇过度积累而影响正常的代谢活动.甲醇在植物中可以代谢为丝氨酸、甲硫氨酸、卵磷脂,进而同化成为细胞组分,因而植物能充分利用自身产生的甲醇,减少浪费.甲醛是植物甲醇代谢中一个重要的中间产物.因甲醛能与蛋白质、核酸和脂类产生非特异性的反应,因此甲醛对植物体具有很强的毒性.植物的甲*收稿日期:2008-11-26;修改稿收到日期:2009-05-31基金项目:国家自然科学基金(30670163);云南省中青年学术与技术带头人培养费和昆明理工大学人才培养费(2004PY01-5)作者简介:徐 迪(1982-),男(汉族),在读硕士研究生,主要从事植物代谢基因工程研究.E-mail:justinxu@m *通讯作者:陈丽梅,教授,博士生导师,主要从事植物代谢基因工程研究.E-mail:ch enlim eikm@醛代谢可以消耗掉自身产生的甲醛,消除其对植物的毒性,从而保证植物新陈代谢的正常进行.另外,有报道称,拟南芥甲酸脱氢酶基因(FDH )的表达是由甲醛诱导的而不是甲酸[1].这意味着甲醛还是甲酸代谢的信号分子,在某种程度上决定着一碳代谢的方向.甲酸是植物一碳代谢中另一个重要的中间代谢产物.它可能既是一碳代谢的起点,又是终点.作为起点,甲酸在依赖于AT P 的10-甲酰-四氢叶酸合成酶的作用下进入叶酸介导的C1代谢途径,最终同化为细胞的组分;作为终点,无论是甲醇或者甲醛还是C1-T H F(带有一碳单位的四氢叶酸),都可以通过甲酸在甲酸脱氢酶的作用下氧化为CO 2,或者直接释放到大气中.由此可见,植物的C1化合物代谢是植物一碳代谢中的几个重要环节.植物C1单位的代谢由4个部分组成:叶酸介导的反应(Folate -mediated reactions)、一系列不依赖叶酸的反应(Fo late -independent reactions)、甲基化循环(Activ ated methy l cycle)和S -甲基甲硫氨酸循环(SMM cycle)[2].C1化合物代谢可以为植物细胞合成提供反应C1单位、清除代谢所产生的有毒中间产物并维持正常代谢,因而它对植物来说就显得至关重要.近年来,由于生化和分子遗传学方法的综合使用使得人们对高等植物中甲醇、甲醛和甲酸代谢有了一定程度的了解,比如:植物体内甲醇的代谢一般是通过甲醛和甲酸这些中间产物进行同化和异化代谢;甲醛的代谢则主要通过两种途径进行:依赖谷胱甘肽途径和依赖叶酸途径;甲酸的代谢主要通过异化作用分解为CO 2,另外还会有部分转化为乙醛酸或者由叶酸介导转化为细胞组分,如图1所示[2].本文主要对近年来这方面的研究进展进行综述.1 植物中内源一碳化合物的来源和代谢1.1 植物中内源甲醇的来源和代谢植物中甲醇的主要来源是果胶和木质素的脱甲基作用[3].另外,在马铃薯块茎组织中,通过甲醛歧化作用或者还原作用也可以形成甲醇[4].Nem ecek -M arshall 等研究表明,植物叶片中含有小的甲醇库(大约1 mol g -1FW),甲醇库中的部分甲醇可能被释放到大气中[5].虽然在植物中循环的甲醇比例还不清楚,但是植物组织确实能够代谢甲醇.图1 高等植物中一碳化合物代谢的基本途径CAT.过氧化氢酶;FALDH.依赖于谷胱甘肽的甲醛脱氢酶;FGH.S -甲酰谷胱甘肽水解酶;FDH.甲酸脱氢酶;SYN.10-甲酰-四氢叶酸合成酶;FTD.10-甲酰-四氢叶酸脱甲基酶;M TD/M TC.5,10-亚甲基-四氢叶酸脱氢酶/5,10-甲川-四氢叶酸环水解酶;S HM T.丝氨酸羟甲基转移酶;GDC.甘氨酸脱羧酶复合体;GXS.乙醛酸合成酶;GXDC.乙醛酸脱羧酶;H M -GSH.S -羟甲基谷胱甘肽;Form-l GS H.甲酰谷胱甘肽;SM M cycle.S -甲硫氨酸循环F ig.1 T he basic pathway of C1metabolisms in higher plantsCAT.Catalase;FAL DH.GS H -dependent formaldeh yde dehydr ogenase;FGH.S -formylglutathion e hydrolase;FDH.Formate dehydrogenase;FTS.10-Formy-l TH F synthetase;FTD.10-Formy-l T H F deformylase;M T D/M T C.5,10-M ethylene -T H F deh ydrogenase/5,10-M ethen y-lT H F cyclohydrolase;SH M T.S erine hydroxymeth yltran sferase;GDC.Gly decarboxylase com plex;GXS.Glyoxylate synthetase;GXDC.Glyoxylate decarboxylase;H M -GSH.S -hydroxymeth ylglutathione;Form-l GSH.S -meth ylmeth ion ine cycle12856期 徐 迪,等:高等植物中一碳化合物代谢研究进展14C放射性示踪剂和13C-NMR[6]研究显示,甲醇库中的甲醇可以通过甲醇 甲醛 甲酸 CO2路径进行代谢.从甲醇到甲醛的反应机理目前还不清楚,其中一种可能是由过氧化氢酶(CAT)介导并需要有H2O2参与的氧化作用[7].一个典型的CAT 相对分子质量大约为200~340kDa,它是由4个亚基构成的聚合体,每个亚基各含有1个亚铁血红素分子,保守序列存在于催化位点和亚铁血红素的结合位点中[8].有研究发现,干旱、寒冷、高盐、臭氧等胁迫能显著诱导植物表达CAT,并调节CAT的活性来提高植物对逆境的忍耐力[9-11].该反应步骤在甲基营养型酵母中是由甲醇氧化酶催化的,在甲基营养菌中是由甲醇脱氢酶催化的,但是至今还没有生化或者DNA序列方面的证据证明植物中存在这两种酶.此外,有研究发现,甲醇 甲醛 甲酸 CO2路径所形成的甲醛或者甲酸有部分进入了C1叶酸库中[5,6].1.2 植物中内源甲醛的来源和代谢有人使用稳定的甲醛加合物试剂证明植物体内存在甲醛库(0.1~10 mol g-1FW).用这种方法探测到的甲醛大部分在植物体内不以自由态存在,而是与谷胱甘肽、精氨酸、天冬酰氨和四氢叶酸等内源性亲核试剂可逆结合,并且它们在植物中的水平不超过1nmo l g-1[12,13].由于这些天然辅助因子和甲醛的结合具有热力学优势,因此反应能自发地进行,甲醛与谷胱甘肽和四氢叶酸形成加合物的平衡常数分别是670L mol-1和32000L mo l-1[12,13].然而,植物中甲醛的具体来源还不清楚,其中的一部分可能来自甲醇的氧化作用,还有一部分可能来自于光呼吸形成的C1-TH F的分解作用.如同其他生物一样,植物也有依赖于谷胱甘肽的甲醛脱氢酶,它催化S-羟甲基谷胱甘肽生成S-甲酰谷胱甘肽的反应,此酶在植物中有高水平的表达并对S-羟甲基谷胱甘肽具有高亲和力(K m为1.4~ 13 m ol L-1)[14].S-甲酰谷胱甘肽水解酶也已经在植物中检测到,它可作用于S-甲酰谷胱甘肽使之水解产生甲酸[15].上述两种酶可能组成了将甲醛氧化到甲酸的不依赖于叶酸的代谢途径(谷胱甘肽依赖途径)[2].由于甲醛也能与TH F反应生成5,10-亚甲基四氢叶酸,此反应不需要酶的参与,因而植物中又存在着依赖叶酸的甲醛代谢途径.1.2.1 依赖谷胱甘肽的甲醛代谢途径 依赖谷胱甘肽的甲醛代谢途径主要步骤为:甲醛(H CH O) S-羟甲基谷胱甘肽 S-甲酰谷胱甘肽 甲酸(H COOH) CO2+H2O,除了H COOH CO2+ H2O是在线粒体或叶绿体中进行外,其他反应主要是在细胞质中进行的,这个途径的关键酶是依赖于谷胱甘肽的甲醛脱氢酶(g lutathio ne-dependent form aldehy de dehydrog enase,FALDH).Achkor等的研究表明,在拟南芥中过量表达FALDH可以增强转基因拟南芥植株吸收甲醛的能力和对甲醛的耐性[16].此外,催化H COOH CO2+H2O反应的甲酸脱氢酶也已经从拟南芥和马铃薯块茎中分离到,推测它可能存在于线粒体或叶绿体中[17,18].1.2.2 依赖叶酸的甲醛代谢途径 依赖叶酸的甲醛代谢途径可能是叶酸介导的甲醛氧化途径,主要步骤可能是:H CH D 5,10-亚甲基四氢叶酸(5,10-CH2-TH F) 5,10-甲川四氢叶酸(5,10=CH-T H F) 10-甲酰四氢叶酸(10-H CO-TH F) 甲酸 CO2+H2O[1],这个途径由细胞质和线粒体中的酶共同完成,此途径可能是植物甲醛代谢的主要途径,这和微生物的甲醛异化代谢途径非常相似[19].另外在线粒体中有甘氨酸存在情况下,5,10-CH2-THF在丝氨酸羟甲基转移酶(Serine hydrox ym-ethy-l transferase,SH MT)的催化作用下能生成丝氨酸,从而将C1单位整合入其他胞质成分.通过研究拟南芥的shm缺陷突变体发现它的shm1主要在叶子中表达,而其shm2主要是在根和茎尖分生组织中表达[20].植物光呼吸作用提供的甘氨酸在甘氨酸脱羧酶复合体(Gly decar box ylase co mplex,GDC)的作用下也能生成5,10-CH2-T H F[2].5,10-CH2-T H F还能在5,10-亚甲基-四氢叶酸还原酶的作用下生成5-甲基四氢叶酸(5-CH3-TH F),C1单位通过5-CH3-TH F进入SMM循环和甲基化循环最后也能整合入胞质成分中[21].1.3 植物中内源甲酸的来源和代谢有研究证明植物拥有一个具有代谢活性的小型甲酸库(一般为0.1到1 mo l g-1FW)[22].同甲醇一样,甲酸可从叶片释放到大气中,但释放速率比甲醇低[23].在光照下的C3植物叶片中,甲酸通常被认为是来自光呼吸中形成的乙醛酸,经由依赖H2O2的乙醛酸脱羧基作用的介导或过氧化氢酶的过氧化活性介导而生成[24].然而,因为大部分证据需要依靠突变体或者抑制剂来获得,这是否是正常情况下的一个最重要的途径还不清楚.在暗环境中,非光合作用组织和C4植物中甲酸的形成机制也不清楚,形成过程可能包括甲醛氧化和10-甲酰-四氢叶酸裂解,后者可能是真核生物线粒体甲酸的主要来1286西 北 植 物 学 报 29卷源[25].也有证据表明在马铃薯块茎叶绿体中可将CO2直接还原为甲酸[26].Oliv er和H o urto n-Cabassa[27]的研究结果说明菠菜线粒体能很快氧化甲酸.Gout等在研究铜叶槭(A cer p seud op latanus L.)对甲酸的代谢时也得出了同样的结论.他们发现完整铜叶槭细胞氧化甲酸比代谢甲醇的速度更快(大约1 mo l h-1 g-1FW 对比0.21 mo l h-1 g-1FW)[6].植物中甲酸代谢途径主要有3条:线粒体型依赖NAD甲酸脱氢酶途径、四氢叶酸介导的同化途径和乙醛酸合成酶途径.1.3.1 线粒体型依赖NAD甲酸脱氢酶途径 线粒体型依赖NAD甲酸脱氢酶途径的主要步骤是通过线粒体依赖NAD的甲酸脱氢酶催化将甲酸氧化成CO2,然而在植物叶绿体中,甲酸脱氢酶也能催化其逆反应,即将CO2还原为甲酸[28,29].线粒体型甲酸脱氢酶是植物线粒体基质酶,纯化的酶是一个42 kDa的二聚体,然而在细胞器中它可能是一个包含其他蛋白的200kDa复合物[29].尽管甲酸脱氢酶是非绿色组织线粒体中最丰富的可溶性蛋白之一,但在光照或没有环境胁迫的条件下叶片细胞线粒体中甲酸脱氢酶的含量却很低[27].近年来有报道证明在拟南芥叶绿体中也含有甲酸脱氢酶[18].叶片中甲酸脱氢酶被黑暗、C1相关化合物或环境胁迫强烈诱导,在根部施用甲酸、缺氧或缺铁的情况下也能诱导其表达[30].1.3.2 四氢叶酸介导的同化途径 有研究表明在拟南芥中存在着由四氢叶酸介导的从甲酸到丝氨酸的代谢流[31].甲酸可能是C1单位的重要来源,它是通过依赖于AT P的活化作用进入叶酸介导的C1代谢途径,这个活化作用是由10-甲酰-四氢叶酸合成酶介导的,该酶存在于胞质、线粒体和叶绿体中.此反应的逆反应,同样也是由10-甲酰-四氢叶酸合成酶介导的,可能也是甲酸离开叶酸介导的C1代谢的门户[31].这说明植物中确实存在四氢叶酸介导的甲酸同化途径.然而,DNA序列证据表明,植物中还存在10-甲酰-四氢叶酸脱甲酰基酶,此酶介导10-甲酰-四氢叶酸不可逆的水解反应,有人还证明该酶是植物在正常环境下进行光呼吸作用的必需酶[32].因此,尽管从甲酸能生成C1叶酸,但是更多的甲酸是由甲酸脱氢酶氧化为CO2[33].1.3.3 乙醛酸合成酶途径 依赖乙醛酸合成酶途径最初发现于青皮马铃薯块茎中[32],而放射性同位素示踪数据表明此途径可能也存在于马铃薯的叶片中[34].催化该途径的酶是乙醛酸合成酶,目前已经从马铃薯块茎的叶绿体中纯化到该酶并鉴定了其分子特征[35,36].在乙醛酸合成酶催化作用下,由两分子的甲酸或两分子甲酸结合的四氢叶酸合成乙醛酸.此酶是否也介导逆反应,还没有相关报道.2 植物中外源一碳化合物的代谢2.1 植物中外源甲醇的代谢用13C-NM R的研究表明,植物对人为添加在培养基中的外源甲醇同样具有代谢能力.有研究者用13C甲醇培养铜叶槭细胞,结果发现13C甲醇进入铜叶槭细胞中后可以缓慢代谢为 -13C丝氨酸、13 CH3甲硫氨酸和13CH3卵磷脂等化合物[6].他们推断铜叶槭细胞对13C甲醇的同化可能是通过将其转化为13CH2-TH F和S-腺苷甲硫氨酸来进行的[6].令人感兴趣的是,在铜叶槭细胞中有部分13C甲醇还能同化为一种新的细胞代谢产物 13CH3- -D-吡喃葡萄糖苷,而且同化到甲基- -D-吡喃葡萄糖苷中的甲基不需要形成CH2-TH F[6].由于该化合物中富积的13C接近100%,说明甲基- -D-吡喃葡萄糖苷的甲基完全来自于甲醇.另外,在玫瑰花瓣和很多蔷薇科水杨梅属植物中也发现有甲基- -D-吡喃葡萄糖苷存在[9].初步研究认为,甲基- -D-吡喃葡萄糖苷在植物液泡中积累,并且一旦合成就很稳定[6].然而,甲基- -D-吡喃葡萄糖苷的富集对植物的影响及其最后的去向还没有相关的报道.最近,Dow nie等通过生物芯片研究用外源甲醇处理拟南芥植株的转录谱时发现,外源甲醇在植物体内的代谢分为3个时期.其中 时期反应主要由细胞色素P450超家族催化的, 时期是I时期反应产生的亲水性物质连接到亲电化合质如谷胱甘肽和含有活泼羟基的化合物如葡萄糖或丙二醛分子上的反应,在 时期时, 时期反应产物转运到亚细胞器(如液泡)中[37].2.2 植物中外源甲醛的代谢为了研究植物对外源甲醛的代谢,Giese等将吊兰的枝条暴露于7.1 L L-1(8.5mg m-3)14C 甲醛的气体中24h,发现植物获得了大约88%放射性,这些放射性物质已掺入到有机酸、氨基酸、游离糖类和脂类以及细胞壁成分中.利用含有14C甲醛溶液培养的无菌大豆细胞悬浮培养物的研究也得到了相似的结果,即丝氨酸和卵磷脂是14C甲醛的主要代谢产物[38].我们在用14C标记的甲醛处理拟南芥时也发12876期 徐 迪,等:高等植物中一碳化合物代谢研究进展现,即使在很短的标记时间(20m in)内,在拟南芥中也有大量14C标记的丝氨酸和少量的有机酸出现[39].这些实验结果说明植物对添加的外源甲醛也有一定的代谢能力.2.3 植物中外源甲酸的代谢Prabhu等用13C甲酸溶液处理拟南芥植株,然后用13C-NM R检测发现13C甲酸会活化植物内源的TH F,并会使其与13C甲酸在C1-TH F合成酶的作用下形成5,10-13CH2-T H F.然后5,10-13CH2-T H F 在SH M T的催化作用下与Gly反应生成13C Ser;同时用NM R检测拟南芥植株中13C甲酸的含量,结果发现几乎检测不到游离的13C甲酸存在,因此认为植物中外源甲酸的代谢速度非常快,植物中游离甲酸的水平只能维持在极低水平[30].3 结论和展望在高等植物中除了甲醇代谢可能有一个特殊的反应(甲醇可能被转糖基化作用催化产生甲基- -D-吡喃葡萄糖苷并稳定地积累在液泡中)外,甲醇、甲醛、甲酸代谢其实是交叉重叠在一起的,互为代谢中间产物,在各种酶的协助下组成了一系列彼此相关的反应(图1)[2].因而它们都能互相影响,互相调控.这种调控关系和植物内部的一碳流紧密联系[40],在外界环境的作用下显得更加纷繁复杂.为了了解这些调控关系,需要利用转基因技术和分子生物学方法结合定量测定反应流量等手段进行更深入的研究.除此以外,现阶段该研究领域还存在许多实际问题亟待解决,如植物体内甲醛、甲酸库的起源;有些酶(催化甲醇 甲醛的氧化酶及其逆反应的还原酶等)在植物中是否存在?有些酶(乙醛酸合成酶等)是否普遍存在于植物中?一碳化合物对C1途径的贡献量是多少?某一代谢反应的增强对植物的表型影响等.今后对上述问题的深入探讨将是植物一碳代谢研究的一个重要方向,这方面的研究成果将会为植物C1化合物代谢相关基因工程和全球环境污染物的评估及治理提供重要的理论依据.参考文献:[1] FU KU SAKI E,IKEDA T,S HIRAIS HI T,NISH IKAWA T,KOBAYAS HI A.Formate d ehydrogenas e gene of Ar abidop sis th aliana is in-duced by formaldehyde and n ot by formic acid[J].J.Biosci.Bioe ng.,2000,90(6):691-693.[2] H ANSON A D,ROJE S.One-carb on m etab olism in higher plants[J].A nnu.Re v.Plant P hysiol.P lant M ol.Biol.,2001,52:119-137.[3] FALL R,BE NS ON A A.Leaf methan ol the sim ples t natural pr odu ct from plan ts[J].T re nds in Plant S cience,1996,1(9):296-301.[4] M ASON R P,S ANDERS JERE M Y K M,GIDLEY M J.NM R visualization of free asparagine in potato tissue us ing adduct formation with[13C]formaldeh yd e[J].P hytochemistr y,1986,25(7):1567-1571.[5] NE M ECEK-M ARS HALL M,M ACDONALD R C,et al.M ethanol emis sion from leaves(enzymatic detection of gas-phase m ethanol an dr elation of m ethanol fluxes to stomatal conductance and leaf developm ent)[J].Plant P hysiol.,1995,108(4):1359-1368.[6] GOUT E,AUBERT S,BLIGNY R,REBEILLE F,NONOM URA A R,BENSON A A,DOUCE R.M etab olism of m ethanol in plant cells.Carbon-13nuclear magnetic resonance studies[J].P lant Ph ysiol.,2000,123(1):287-296.[7] H AVIR E A,M CH ALE N A.Purification and characterization of an isozyme of catalase w ith enhanced-peroxidatic activity from leaves ofN icotiana sylv estr is[J].A rch Bioch em.Biop hy s.,1990,283(2):491-5.[8] KWON S I,LEE H S,C HU NG S A.Differential ex pres sion of three catalas e genes in th e s mall radish(Rhap hanus sativ us L.var.sativ us)[J].M ol.Ce lls,2007,24(1):37-44.[9] CH EN J F(陈金峰),WANG G N(王宫南),CH ENG S M(程素满).Progr ess about catalas e function in plan t stres s reactions[J].A ctaBot.B or eal.-Occiden t.S in.(西北植物学报),2008,28(1):188-193(in Chin es e).[10] LU M H(逯明辉),SONG H(宋 慧),L I X M(李晓明),CH EN J F(陈劲枫).Chan ges of SOD,CAT and POD activities in cucu mberleaves during cold damage[J].A cta Bot.B or eal.-Oc cident.S in.(西北植物学报),2005,25(8):1570-1573(in Ch ines e).[11] GOULAS E,SC HU BE RT M,KIES ELBACH T,et al.Th e ch loroplast lumen and stromal proteom es of A r abidop sis thaliana show dif-ferential s ens itivity to s hort2and long2term ex posure to low tem perature[J].P lant J.,2006,47(5):720-734.[12] BOURGIS F,ROJ E S,NUCCIO M L,FISH ER D B,T ARCZYNS KI M C,et al.S-methylmeth ionine plays a major role in phloem sulfu rtransp ort an d is syn thesized by a novel type of methyltransferase[J].P lant Cell,1999,11(8):1485-1498.[13] CHE N L,CH AN S Y,COSS INS E A.Distribution of folate derivatives and enzymes for synth esis of10-formyltetrahydrofolate in cytosol-ic and m itochondrial fractions of pea leaves[J].Plant P hysiol.,1997,115(1):299-309.[14] U OT ILA L,KOIVUS ALO M.Purification of formaldehyde an d formate d ehydrogenas es from pea s eeds by affinity ch romatography an dS-formylglu tathione as the intermediate of formaldehyde m etabolism[J].Ar ch B iochem.B iop hys.,1979,196(1):33-45.[15] H ANSON,A D,GAGE D A,e t al.Plant one-carbon metabolism and its engineerin g[J].T rend s Plant S ci.,2000,5(5):206-213. 1288西 北 植 物 学 报 29卷[16] ACH KOR H ,DIAZ M ,FERNANDEZ M R,BIOSC A J A,PARE S X,M ARTINEZ M C.Enh an ced form aldehyde detoxification b y over -expression of glutathione -dependent formaldehyde deh yd rog enase from Ar abidop sis [J].Plant P hy siol.,2003,132(4):2248-2255.[17] BYKOVA N V,ST ENSBALLE A,EGSGAARD H ,JE NSEN O N,M OL LER I M.Phosph orylation of formate dehydrogenase in potatotub er mitochondria[J].J.B iol.Chem.,2003,278(28):26021-26030.[18] OLSON B J,SKAVDAHL M ,RAM BERG H,OST ERM AN J C,M ARKWELL J.Formate dehydrogen as e in A rabid opsis thaliana :char -acterization an d pos sible targeting to the chloroplast[J].P lant S ci.,2000,159(2):205-212.[19] C ROWT H ER G J ,KOS ALY G,LIDS TROM M E.Formate as th e main b ranch point for methylotrophic m etabolism in M eth ylobacteriumextorquen s AM 1[J].J.Bac ter iol ,2008,190(14):5057-5062.[20] VOLL L M ,JAM AI A,RENNE P,VOLL H ,M CCLU NG C R,W EBER A P.Th e ph otorespiratory A rabid op sis shm 1mutant is deficientin SH M 1[J ].P lant Phy siol.,2006,140:59-66.[21] J AE K K,T AKES HI B,KAZU O H ,EIICH IRO F,AKIO K.Tim e -course metabolic profiling in A rabid opsis thaliana cell cultures afters alt stress treatmen t[J ].J.Ex p.B ot .,2007,58(3):415-424.[22] W INGLE R A,LEA P J,LEEGOOD R C.Photor espiratory metabolism of glyoxylate and formate in glycin e -accumulating mutan ts of bar -ley and A maranthus ed ulis [J].P lanta ,1999,207(4):518-526.[23] GABRIEL R,SCH ER L,GERLACH C,RAUSCH T,KESSE LM EIER J.Factor s contr olling th e emiss ions of volatile organ ic acidsfrom leaves of Quer cus ile x L.(Holm oak)[J].A tmosp her ic E nv ir onmen t ,1999,33(9):1347-1355.[24] W INGLE R A,LEA P J,LEEGOOD R C.Photor espiration:metabolic pathw ays and th eir role in stress protection[J].P hilos T r ans R S ocL ond B Biol .S ci.,2000,355(1402):1517-1529.[25] GIRGIS S,SU H J R,J OLIVET J,ST OVER P J.5-Formyltetrahydr ofolate regulates homocysteine rem ethylation in human neu rob lasto -ma[J].J.B iol.Chem.,1997,272(8):4729-4734.[26] S ANGE ETA A,KRIS HNAN R N,M ADH USU DANAN N P.Partial purification an d some properties of a latent CO 2r eductase fr omgr een potato tuber chloroplasts[J ].Eur op ean J our nal of Biochemistr y ,1985,153(3):509-514.[27] H OU RT ON -CABASS A C,AM BARD -BRETT EVILLE F,M OREAU F,DAVY DE VIRVILLE J,REM Y R,FRANCS -S M ALL C C.S tress indu ction of mitochondrial form ate dehydrogenase in potato leaves[J].P lant P hysiol .,1998,116(2):627-635.[28] VL ADIM IR I T ,VLADIM IR O P.Protein engineering of formate dehydrogenase[J ].Biomol E ng.,2006,23:89-110.[29] VL ADIM IR I T ,VLADIM IR O P.Catalytic m ech anism and application of formate dehydrogen as e[J].Bioch emistry ,2004,69(11):1252-1267.[30] S HIRAISH I T ,FU KUSAKI E,KOBAYASH I A.Form ate deh ydrogenase in rice plant:grow th stim ulation effect of formate in rice plant[J ].J.Biosci .Bioeng.,2000,89(3):241-246.[31] PRABHU V,CH AT SON K B,et al .13C nuclear magnetic res on an ce detection of interactions of serine hydroxymethyltran sferase withC1-tetrahydrofolate s ynthase an d glycine decarb oxylase complex activities in Ar abid op sis [J ].P lant P hy siol.,1996,112(1):207-216.[32] COLLAKOVA E,GOYER A,NAPONE LLI V,KRAS SOVSKAYA I,GREGORY J F,H ANSON A D,SH ACH AR -H ILL Y.Ar abid op-sis 10-formyl tetrahydrofolate deform ylas es are es sen tial for ph otorespiration[J].P lant Cell ,2008,20(7):1818-1832.[33] M CNEIL S D,NUCCIO M L,RH ODES D,SH ACH AR -HILL Y,H ANSON A D.Radiotracer and com pu ter m odeling evidence that phos -ph o -base m ethylation is the m ain route of choline s ynthes is in tobacco[J ].P lant Phy siol.,2000,123:371-380.[34] J ANAVE M T ,RAM ASW AM Y N K,NAIR P M.Glyoxylate synthetase isolated from green potato tu ber chloroplasts catalys ing theconversion of formate to glyoxylate[J ].P lant S ci .L ett ,1983,32:213-220.[35] ZEM LYANUKHIN A A,M AKEE V A M ,RAIKH INSH TEIN M V.M etabolism of formic acid an d related compounds in maize seedlings[J ].P lant Phy siol.,1972,19:473-479.[36] J ANAVE M T ,RAM ASWAM Y N K,NAIR P M.Studies on determination of active site amino acid residues in glyoxylate s ynthetasefrom potato tub er chloroplasts[J].P lant P hysiology and Bioche mistry ,1999,37(2):121-129.[37] DOWNIE A,M IYAZAKI S ,BOH NERT H ,J OH N P,COLEM AN J ,PARRY M ,H ASLAM R.Ex pres sion profiling of the respons e ofA ra bidop sis thaliana to methanol stimulation[J].Plant Ce ll ,2004,65(16):2305-2316.[38] GIESE M ,BAUE R -DORA NTH U ,et al .Detox ification of formaldehyde by the spider plant (Chlor op hy tum comosum L.)and by S oy -bean (G ly cine max L.)cel-l su spen sion cultures[J].Plant P hysiol.,1994,104(4):1301-1309.[39] M A L(马 莉),CH EN L M (陈丽梅).The research advances on s erine hydr oxym ethyltransferas e gene in plants [J].B iote chnology B ul -letin (生物技术通报),2008,2:15-19(in Ch ines e).[40] LOIZEAU K,GAM BONNET B,ZHANG G F,e t al .Regu lation of one -carbon m etabolism in A r abidop sis :the N -termin al regu latory do -main of cys tathionine gamma -synthase is cleaved in res pon se to folate starvation[J].P lant Ph ysiol.,2007,145(2):491-503.12896期 徐 迪,等:高等植物中一碳化合物代谢研究进展。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
昆明理工大学2019年硕士研究生招生入学考试试题(A卷) 考试科目代码:832 考试科目名称:植物纤维化学
考生答题须知
1.所有题目(包括填空、选择、图表等类型题目)答题答案必须做在考点发给的答题纸上,做在本试题册上无效。
请考生务必在答题纸上写清题号。
2.评卷时不评阅本试题册,答题如有做在本试题册上而影响成绩的,后果由考生自己负责。
3.答题时一律使用蓝、黑色墨水笔或圆珠笔作答(画图可用铅笔),用其它笔答题不给分。
4.答题时不准使用涂改液等具有明显标记的涂改用品。
第 1 页共30 页。
