醚的分类与命名
醚

CH3CH2CH2CHCH3 OC2H5
COOH
2-乙氧基戊烷
4-甲氧基苯甲酸 对甲氧基苯甲酸
OCH3
二、醚的化学性质 1. 盐的形成 . 醚中的氧原子上具有孤电子对 能接受质子, 氧原子上具有孤电子对, 醚中的氧原子上具有孤电子对,能接受质子,但接受质 子的能力较弱,只有与浓强酸中的质子, 子的能力较弱,只有与浓强酸中的质子,才能形成一种不稳 定的盐, 定的盐,称 盐 。
酚是离去基
例 (CH3)3COCH3 + HI
(CH3)3CI + CH3OH
历程 SN1
+ (CH3)3COCH3 H + I(CH3)3C + (CH3)3C + (CH3)3CI CH3OH
3.过氧化物的生成 3.过氧化物的生成
CH3CH2OCH2CH3+ O2 CH3CH2 O CHCH3 OOH
二苯醚不发生此反应。 注:⑴ 二苯醚不发生此反应。 过量, ⑵若HI过量,生成的醇还可以继续反应 过量 生成的醇还可以继续反应。 CH3CH2OH
HI △
CH3CH2I + H2O
SN2
δ+ H δ+ CH3CH2 O CH3 + I -
进攻进攻- C H 3位阻小
δ+
乙醇是离去基 SN2
δ+ H .. O δ+ p- 共轭使 C2H5 + I - , π 共轭 使 O 键加强
KCNS
[Fe(CNS)6]3- 变红
除去方法:加入还原剂 除去方法:加入还原剂Na2SO3 或FeSO4。
4.环氧乙烷 4.环氧乙烷
C
H2O
C
CH2 OH
醚的命名规则及举例

醚的命名规则及举例一、介绍醚是一类有机化合物,由氧原子连接两个烷基基团而组成。
它们广泛存在于自然界和化工领域,并具有多种应用。
在化学领域中,命名规则是非常重要的,它能准确地描述化合物的结构和性质。
本文将详细介绍醚的命名规则,并提供一些举例来帮助读者更好地理解。
二、命名规则醚的命名规则主要涉及到以下三个方面:命名前缀、主体命名和醚的分类。
2.1 命名前缀命名前缀用于描述连接在氧原子上的烷基基团,通常是通过字母“R”表示的。
如果只有一个烷基基团连接在氧原子上,那么命名前缀就是这个烷基基团的名称;如果有两个以上的烷基基团连接在氧原子上,那么需要使用特定的前缀来表示不同的基团数目。
以下是常见的命名前缀及其含义:•单基团:methyl、ethyl、propyl等•两个基团:dimethyl、diethyl、diisopropyl等•三个基团:trimethyl、triethyl、triisopropyl等•四个基团:tetramethyl、tetraethyl、tetraisopropyl等2.2 主体命名主体命名是描述醚分子中氧原子连接的两个烷基基团的主要规则。
根据主体命名的规则,首先列出较大的烷基基团的名称,然后在其前面加上“oxy”作为连接氧原子的表示符,最后再加上较小的烷基基团的名称。
举例来说,如果有一个乙基基团连接在氧原子上,另一个甲基基团连接在氧原子的另一端,那么这个醚的名字就是“methoxyethane”。
2.3 醚的分类根据不同的性质和结构特点,醚可以分为以下几类:1.烷基醚(Alkyl ether):含有烷基基团的醚,是最常见的醚类化合物。
根据烷基基团的数目,可以分为二甲醚(dimethyl ether)、乙基甲醚(ethyl methyl ether)等。
2.芳基醚(Aryl ether):含有芳基基团的醚。
根据芳基基团的结构不同,可以分为苯醚(phenyl ether)、萘醚(naphthyl ether)等。
9.9 醚的分类与命名
9.9 醚的分类与命名
9.9.1 分类
简单醚:R= R’ ,如: 混合醚:R≠ R’,如:
O C2H5 C2H5
环醚:R, R’ 相连即亚烃基与O相连,如:
根据烃基类型: 饱和醚:R, R’ 为饱和烃,如: 不饱和醚:R, R’ 至少一个为不饱和烃,如:
O OBiblioteka 芳香醚:R, R’ 至少一个为芳基,如:
多元醚:含有多个C-O-C醚官能团的化合物,如:
冠醚:以乙二醇为结构单元的环状多醚,含有多个 醚官能团的化合物。由于这类醚的构象外形与西方的王 冠相似,因此,把这类大环多醚称为冠醚。如:
O O O
O O
O
9.9.2 醚的命名 (1)无环单醚:
普通命名法: 两个烃基名称后面+“醚”词尾。 IUPAC命名法:烃为母体,较小的烷氧基为取代基。
1,4,7,10,13,16-六氧杂环十八烷
(2)环醚(环氧化物):
环醚用“环氧某烃”命名,并用数字标明环氧的位置; 环醚也可以用“氧杂环某烃”命名,氧杂表明环上碳原子被 氧原子所取代,如环上有取代基,以氧原子开始沿着环编号。 如:
1,3O 1,4O O 1,4 1,4 O (THF)
(3)冠醚:
命名方法为m-冠-n,m: 环的总原子数,n: 环中的氧原子数。 如:
有机化学基础知识点醚的命名与结构

有机化学基础知识点醚的命名与结构醚是一类重要的有机化合物,广泛应用于化工、医药和日用化学品等领域。
在有机化学中,了解醚的命名和结构是非常基础且重要的知识点。
本文将重点介绍醚的命名规则和结构特点,帮助读者更好地掌握有机化学的基础知识。
一、醚的命名规则醚根据官能团的不同位置和碳链的长度,可以分为两类:对称醚和不对称醚。
对称醚指的是两个有机基团相同的醚,而不对称醚则是两个有机基团不同的醚。
1. 对称醚的命名规则对称醚的命名非常简单,只需要按照以下步骤进行:步骤一:确定有机基团的名称。
步骤二:将有机基团的名称按字母顺序排列。
步骤三:在有机基团的名称两侧分别加上前缀"氧"。
例如,对称醚乙醚(Ethyl ether)的结构式为:OCH2CH3,命名时只需将乙基的名称按字母顺序排列,即为乙氧基乙氧。
2. 不对称醚的命名规则不对称醚的命名相对复杂一些,主要分为三个步骤:步骤一:确定较长的有机基团。
步骤二:确定较短的有机基团。
步骤三:在较长的有机基团的名称前加上较短的有机基团名称,并在两个有机基团的名称之间加上前缀"氧"。
例如,甲基乙醚(Methyl ethyl ether)的结构式为:CH3OCH2CH3,命名时将甲基和乙基按照字母顺序排列,即为甲氧基乙氧。
二、醚的结构特点醚的结构特点主要体现在两个方面:1)官能团的特点;2)分子的空间构型。
1. 官能团的特点醚的官能团为一个氧原子连接两个碳链,氧原子与碳原子通过一个共价键连接。
这个特殊的结构赋予醚许多独特的性质,例如较低的沸点和溶解度,以及较弱的酸碱性等。
2. 分子的空间构型醚的空间构型可以分为简单的线性构型和复杂的环状构型两种。
简单的线性构型是指醚分子中两个碳链呈线性排列,如乙醚。
这种构型的醚分子通常比较活泼,易于与其他分子进行反应。
复杂的环状构型是指醚分子中两个碳链形成环状结构,如环氧乙烷。
环状结构使得醚分子在化学反应中更为稳定,同时也赋予了醚分子更多的反应可能性。
有机化学第九章醚

四氢呋喃 tetrahydrofuran
四氢吡喃 tetrahydropyran
二噁烷(1,4-二氧六环) 1,4-dioxane
1,2-环氧丙烷(氧化丙烯) 1,2-epoxypropane
四氢吡喃的 椅式构象
有机化学 (第9版)
一、环氧化合物
(一)结构和命名
系统命名:三元环氧化合物以“氧杂环丙烷”(oxirane)为母体,四元环 氧化合物以“氧杂环丁烷”(oxetane)为母体。
第九章
醚
第一节 醚 第二节 环醚
重点难点
掌握 掌握醚的命名、结构和化学性质;掌握环氧化合物 的命名、结构和化学性质
熟悉 冠醚的结构和命名
了解 冠醚的性质
第一节
醚
有机化学 (第9版)
一、结构和命名
1.醚的结构
甲醚分子的结构
醚键中的氧原子为sp3杂化,其中两个sp3杂化轨道分别与两个烃基碳原子 形成σ键,键角约112°,未成键的两个sp3杂化轨道含两对孤对电子。
有机化学 (第9版)
二、冠醚
含有多个氧原子的大环多醚。通常分子中具有—OCH2CH2—重复单元。立体结构 状似王冠,故称冠醚。冠醚命名时称“m-冠-n”,m代表构成环的碳原子和氧原 子的总数,n代表环中氧原子数。 冠醚的结构特点是随环的大小不同而与不同金属离子形成络合物,从而可以选择
性地识别金属离子。如18-冠-6的空穴直径和K+的直径相近,所以它能与K+离子
(二)开环反应
1. 酸催化开环反应 酸性条件下为具有SN1性质的SN2反应,亲核试剂进攻取代基较多的环碳原 子,这个碳由于取代基的供电效应使正电荷分散而稳定。
更稳定
有机化学 (第9版)
一、环氧化合物
有机化学第8章第三节醚2013
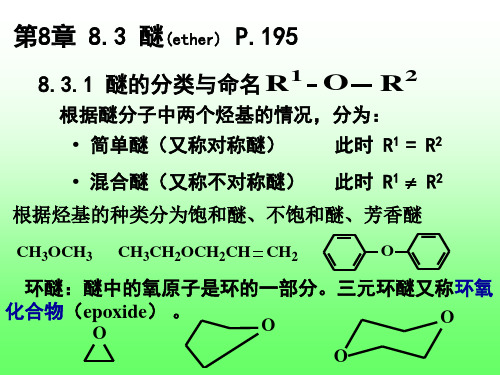
二巯基丙醇(BAL)
CH2 CH CH2 SH SH SO3Na
二巯基丙磺酸钠
HS HC CO2Na HS HC CO2Na
二巯基丁二酸钠
上述解毒剂与金属离子的亲和力较强,它们不仅能 与进入体内的重金属离子结合成不易解离的无毒配合物 由尿排出体外,以保护酶系统,而且还能夺取已经与酶 结合的重金属离子,使酶的活性恢复,从而达到解毒的 目的。但若酶的巯基与重金属离子结合过久,酶的活性 则难以恢复,故重金属中毒需尽早用药抢救。
第8章 8.3 醚(ether) P.195
1 O R 8.3.1 醚的分类与命名
R2
根据醚分子中两个烃基的情况,分为:
• 简单醚(又称对称醚) 此时 R1 = R2
• 混合醚(又称不对称醚)
此时 R1 R2
根据烃基的种类分为饱和醚、不饱和醚、芳香醚
CH3OCH3 CH3CH2OCH2CH CH2 O
CH3CH2OCH2CH3 + O2
CH3CHOCH2CH3 O OH
形成的过氧化物遇热容易爆炸,所以储存时间长的醚在 使用前必须进行检查,若会使湿的KI-淀粉试纸变蓝或使 FeSO4-KCNS 混合液变红,则表明醚中含有过氧化物。 加铁粉或用FeSO4水溶液洗涤,可破坏其中的过氧化物。
8.3.3 醚的制备
1)酸性
RSH + NaOH
RSNa + H2O
C2H5SH > H2O >C2H5OH pKa 10.5 15.7 15.9
2).与重金属作用
与无机硫化物类似,硫醇可与 Pb、 Hg 、Cd、 Ag 、Cu 等重金属盐或氧化物作用生成不溶于水 的硫醇盐。
醚的分类和命名
CH
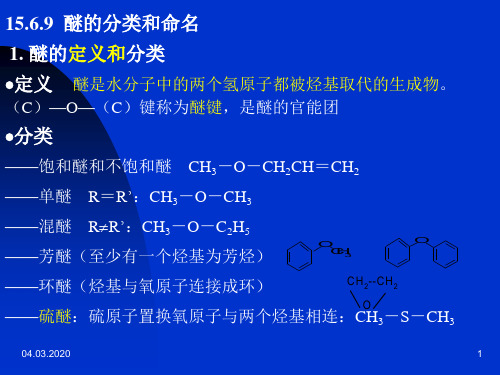
O CH 3C+OOC(H 2C H 13H C 0℃ O2O Z~n2) 5C0℃ H 2=CH O3( C醋 CH酸乙烯
乙基乙烯基醚和醋酸乙烯酯都是重要的化工原料,广泛用来制造粘
合剂、涂料、增塑剂等。
04.03.2020
8
15.6.11 醚的物理性质
•状态 除甲醚和甲乙醚为气体外,多为挥发性高、易燃、易流
•消除过氧化物方法
——用还原剂(如FeSO4/稀H2SO4)后摇荡,以破坏它 ——贮藏醚类化合物时,加入少量金属钠或铁屑或抗氧化剂(例: 对苯二酚),避免过氧化物生成
04.03.2020
15
15.6.13 环醚和冠醚
• 定义
脂环烃的环上碳原子被一个或多个氧原子取代后生成的化合物
例
C H2 C H2
04.03.2020
22
4、乙醚 •制法 乙醇脱水 •性质
无色液体,比水轻,可溶于水,易燃,爆炸极限1.85%36.5% 极性小,较稳定,可溶解很多有机物质,是常用的良好的有机 溶剂和萃取剂 乙醚有麻醉作用,医药上用作麻醉剂
04.03.2020
23
5、环氧树脂
•定义和制法
双酚A的制备 苯酚与丙酮在硫酸存在下于40℃缩合生成2,2
RORˊ + NaX
•注意 制备具有叔烃基的混醚时,应使叔醇钠与伯卤代烷作用。
原因:叔卤代烃在醇钠的作用下,主要发生消除反应
(C3)3 H CONa3C2H B +rSN 2C(H C3)3 H CO2C C3H H+ NaBr (C3)3 H CBr 3C +2H ON CE 2 aHC2H =C3 ()2CH + 3C2 C H OH H +
有机化学醚

3oROH不能制得醚,而只能得到烯烃。
二、 Williamson 合成法(混醚)
RONa ArONa
+ +
R'X RX
SN2
ROR' Ar-O-R
+ +
NaX NaX
12
SN2
例:
CH3CH2CH2CH2O—Na + I—CH2CH3 CH3CH2CH2CH2OC2H5 71%
(CH3)2CHO—Na + Cl—CH2-C6H5
(CH3)2CH—O—CH2-C6H5 84%
(CH3)2SO4 ONa +
或
O—CH3
CH3—I
13
由于该反应是SN2反应,为尽量减少E2消除,卤代 烷部分尽可能避免采用仲卤代烷和叔卤代烷。例:
CH3 CH3—C—ONa + BrCH2CH3 SN2 CH3 CH3 CH3—C—O—C2H5 CH3
R R O + BF3
气态 bp:-1010C
R O + RMgX R X
R R O BF3
溶液
R R O Mg O R
R 2 R
如:格氏试剂在金属镁的表面生成,与醚形成络合物 后脱离金属镁的表面进入溶液,使得格氏试剂的制备 得以进行。
16
二、醚键断裂的反应
醚与浓的HCl、HBr、HI作用,醚键可发生断裂。 HX的反应活性:HI > HBr > HCl 醚键断裂的顺序:30烷基>20烷基>10烷基>芳烃基 1、 若两个是10烷基则发生SN2,小烃基生成碘代烷, 大烃基生成醇。若氢碘酸过量则均生成碘代烷。
OCH2CH3
间乙氧基苯酚
4
醚的命名和化性及制备

二、醚的结构特点
..O..
R
R'
1、折线型,可视为水分子中两个氢被烃基取代;
2、氧上具孤对 e,可接受质子,由于烃基的位阻,醚只能与浓酸形成形成 钅羊 盐 ;
3、醚键为极性键,可断裂而发生裂解反应(亲核取代); 4、α-H 较活泼,可发生过氧化。
三、醚的化学性质 1、 钅羊盐的生成
‥ C2H5 O C2H5 + 浓 HCl
‥
H ‥
+_
C2H5
O ‥
C2H5
Cl
注:(1)醚中的氧周围有烃基包围,孤对 e 不够裸露,需浓酸,用水稀释可析出原来的醚; (2)醚可溶于浓酸,籍此可用浓酸区别醚与烷烃、卤代烃;也可用于分离。此法不可用于 鉴别醚与醇(醇更易溶于酸)。
2、醚键的断裂反应 ‥
C2H5 ‥O C2H5 + 浓 HI O
I-
(2)烃、芳基混醚:烃基形成 RI,芳基形成酚(p-π使苯基碳与氧的键强↑) (3)二苯醚同样条件下则不能进行该反应。
3、生成过氧化物
OOH
CH3CH2OCH2CH3 + O2
CH3CHOCH2CH3
注:(1)醚中常混有过氧化物®易爆;
(2)蒸馏乙醚前必须检查过氧化物;
(3)检查方法:FeSO4-KCNS 试纸变红则有过氧化物存在;
注:(1)类似 SN1 机制(涉及 C+重排) (2)得到双官能团产物 (3)常见:Nu-—H2O,EtOH,PhOH,HBr,HCN 等
2、碱催化开环
OH-
O
+ NH3 O
HOCH2CH2NH2 乙醇胺
OH-
HOCH2CH2NHCH2CH2OH 乙醇胺
第三节 醚

第 三 节 醚
本节要求
1、掌握醚的结构、分类和命名。 2、了解醚性质。
3、了解常见的醚。
醚的概念:
醚:两个烃基通过氧原子相连而成的化合物是醚。 通式: R—O—R/、R—O—Ar、Ar—O—Ar/ 官能团:—O— 称为醚键,是醚的官能团。
一、醚的分类和命名 (一)分类 与氧相连的两个烃基相同,称作单醚 如 C2H5-O-C2H5 与氧相连的两个烃基不同,称作混醚 如 CH3-O-C2H5
乙醚在空气的作用下能氧化成过氧化物、醛和 乙酸,暴露于光线下能促进其氧化。当乙醚中含有 过氧化物时,在蒸发后所分离残留的过氧化物加热 到100℃以上时能引起强烈爆炸; 这些过氧化物可 加5%硫酸亚铁水溶液振摇除去。与无水硝酸、浓硫 酸和浓硝酸的混合物反应也会发生猛烈爆炸。 乙醚对人的麻醉浓度为109.08~196.95g/m3, 当浓度为212.1~303g/m3时可致呼吸停止,当浓度 超过10%时通常可以致命。 乙醚是低毒物质,对皮肤及呼吸道粘膜有轻微 的刺激作用。长期接触低浓度乙醚蒸气时可出现头 痛、头晕、易激动或淡漠、嗜睡、忧郁、体重减轻、 食欲减退、恶心、呕吐、便秘等症状。吸人较高浓 度乙醚蒸气时可出现头晕、癔病样发作、精神错乱、 嗜睡、面色苍白、恶心、呕吐、呼吸不规则等短时 间大量接触后发生的中毒症状,一经脱离现场,稍 待休息,经对症处理后就可恢复。
2-甲氧基-5-氯-3-己醇
二、常见的醚 —— 乙醚
乙醚是最常见的和最重要的醚。它是易挥发的无色透明 液体,有特殊气味,沸点34.5℃。 非常易燃,乙醚蒸气与空气混合达到一定比例时,遇火 可引起爆炸,因此在制备和使用时,周围要避免明火,并采 取必要的安全措施。 乙醚比水轻,微溶于水。其蒸汽比空气重2.5倍。能溶 解多种有机物,是一种良好的有机溶剂,常用于提取中草药 的有效成分。 乙醚有麻醉作用,医用乙醚是高效麻醉药品,只要5到 10秒钟就让人昏迷,曾用作吸入式全身麻醉剂,由于可引起 恶心、呕吐等副作用,现已被更高效、安全的麻醉剂所代替。
醚的分类和命名

醚的分类和命名
《醚的分类和命名》
嘿,今天咱就来聊聊醚的那些事儿哈!醚呢,其实有好多不同的种类哦。
就说有一种醚叫脂肪醚,它们就像是一群调皮的小家伙,有着自己独特的性格。
还有芳香醚,那感觉就像是带着点神秘香气的小精灵。
咱就拿我有一次在实验室里的经历来说吧。
那时候我正在研究一种醚,我小心翼翼地拿着那些瓶瓶罐罐,就像捧着宝贝似的。
我仔细地观察着它们,心里想着:“嘿,你们这些小家伙到底有啥特别的呀。
”我轻轻地摇晃着瓶子,看着里面的液体晃动,就好像它们在跟我打招呼呢。
然后我对照着资料,一点点去分辨它们是哪种醚,给它们取合适的名字,那过程可真是有趣极了呀!
还有环醚呢,它们就像是一个个小小的圆环,有着别样的魅力。
哎呀呀,醚的世界真的是丰富多彩呀!
总之呢,醚的分类和命名虽然听起来有点复杂,但只要咱慢慢去了解,就会发现它们也是很有意思的哟!就像我在实验室里和那些醚打交道的那次经历,让我对它们有了更深刻的认识呢!以后再看到醚,我肯定能一下子就认出它们来啦!哈哈!。
醚的命名规则

醚的命名规则
醚是一类有机化合物,其命名规则是由国际纯粹与应用化学联合会(IUPAC)制定的。
醚的命名规则可以分为两部分,分别是主链的命名和取代基的命名。
主链的命名规则是根据碳原子数来确定的。
首先,根据主链的碳原子数,确定主链的名称。
如果主链中有一个羟基(-OH)官能团,那么主链的名称以“-ol”结尾。
例如,含有一个羟基的醚的命名为“醇醚”。
在主链的命名确定之后,接下来需要确定取代基的位置和名称。
取代基的位置是通过编号来表示的,编号是从主链的一个端点开始,按照离羟基最近的碳原子的顺序进行。
取代基的名称则是根据其化学结构来确定的。
常见的取代基有甲基(-CH3)、乙基(-C2H5)等。
下面以一个例子来说明醚的命名规则。
假设有一个主链上有5个碳原子,并且有一个羟基官能团,同时还有一个甲基取代基。
首先,根据主链的碳原子数,确定主链的名称为戊醇。
然后,确定取代基的位置为2号碳原子,取代基的名称为甲基。
因此,这个化合物的名称为2-甲基戊醚。
需要注意的是,当主链上有两个羟基官能团时,其命名规则稍有不同。
此时,主链的名称以“-diol”结尾,并且取代基的位置和名称需要分别用数字和字母来表示。
总结一下,醚的命名规则包括确定主链的名称和取代基的位置和名称。
主链的名称是根据碳原子数来确定的,取代基的位置是通过编号来表示的,取代基的名称是根据其化学结构来确定的。
遵守这些命名规则,可以准确命名各种类型的醚化合物。
醚的分类和命名.
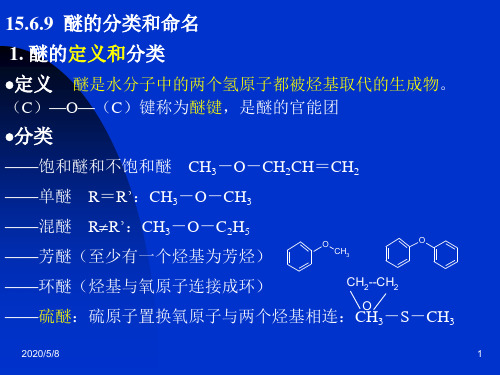
CH 2=CH OCH 2CH 3 (乙基乙烯基醚) O (CH3 COO) Zn 2 CH 2=CH OCCH 3 (醋酸乙烯酯) 210 ℃~250 ℃
乙基乙烯基醚和醋酸乙烯酯都是重要的化工原料,广泛用来制造粘 合剂、涂料、增塑剂等。
2018/9/13
8
15.6.11 醚的物理性质
除甲醚和甲乙醚为气体外,多为挥发性高、易燃、易流 动的无色液体,有特殊气味,相对密度小于1
O
2
HOCH 2CH 2CH 2CH 2OCHCH 3 CH 3 4-异丙氧基-1-丁醇
CHO OCH 3 4-羟基-2-甲氧基苯甲醛 HO
苯氧基苯
CH3OCH2CH2OCH2CH2OCH3 CH2=CH-CH2-O- (CH3)2CH-O- (CH3)2CH-CH2-O- CH3CH2CH(CH3)-O- (CH3)3C-O-
剂的醚有:乙醚、四氢呋喃、1,4-二氧六环、乙二醇二甲醚
2018/9/13
9
15.6.12 醚的化学性质 概况
——醚键很稳定(小环醚除外)。一般与碱、氧化剂、还原剂都不 作用。故有机反应常用醚作溶剂 ——常温下醚与金属钠也不起反应,因而可用钠干燥醚 ——醚有碱性,遇酸可形成钅羊 盐,甚至醚键断裂 ——简单的环醚性质活泼
C2H5OCH(CH 3)2 CH 3OCH 2CH=CH 2 C6H5OC2H5 乙基异丙基醚 甲基烯丙基醚 苯乙醚 C2H5OC2H5 (二)乙(基)醚 C6H5OC6H5 二苯醚
2018/9/13
2
复杂的醚 系统命名法:取碳链最长的烃基作为母体,以烃氧基
(RO﹣)作为取代基:
CH 3CH 2CH 2CHCH=பைடு நூலகம்H OCH 3 3-甲氧基-1-己烯
醚的命名和化性及制备

4、 CH3OPh
5、 H3C
OCH3
6、 O
7、 O
8、 O
OO
9、
H2C
10、 H2C
O C2H5 O C2H5
H2C HC
11、 H2C
O C2H5 OH OH
CH3CH2CHOCH3
12、
OCH3
CH3CHCHCH3
13、 H3C OC2H5
14、 C6H5 O C6H5
15、 CH2 CHCH2 O CH3
醚的命名和化学性质及制备
一、命名
1、单醚——“某烃基”醚 2、混醚——“小烃基(芳基)+大烃基”醚 3、多元醚——“多元醇+烃基”醚,醚键位号要标注 4、环醚——(1)环氧(标位置)+烃基名
(2)杂环命名法(略) 5、结构复杂的醚将烃氧基作取代基 例题:
1、 CH3OCH3
2、 C2H5OC2H5
3、 CH3OC2H5
‥
H ‥
+_
C2H5
O ‥
C2H5
Cl
注:(1)醚中的氧周围有烃基包围,孤对 e 不够裸露,需浓酸,用水稀释可析出原来的醚; (2)醚可溶于浓酸,籍此可用浓酸区别醚与烷烃、卤代烃;也可用于分离。此法不可用于 鉴别醚与醇(醇更易溶于酸)。
2、醚键的断裂反应 ‥
C2H5 ‥O C2H5 + 浓 HI O
CH2ClCH2OH + HCl
CH2ClCH2OH + Ca(OH)2
O + CaCl2 + H2O
2、氧化法(1937 年美国联合碳化物公司开发)
Ag
CH2=CH2 + O2 200~300 oC
O
醚
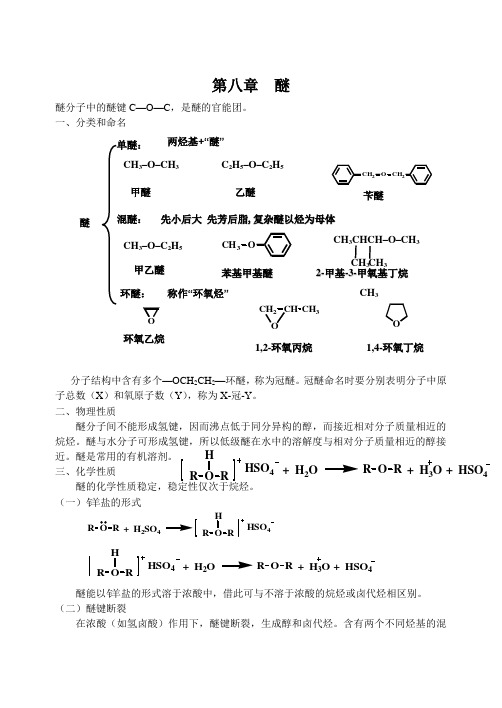
第八章 醚醚分子中的醚键C —O —C ,是醚的官能团。
一、分类和命名分子结构中含有多个—OCH 2CH 2—环醚,称为冠醚。
冠醚命名时要分别表明分子中原子总数(X )和氧原子数(Y ),称为X-冠-Y 。
二、物理性质醚分子间不能形成氢键,因而沸点低于同分异构的醇,而接近相对分子质量相近的烷烃。
醚与水分子可形成氢键,所以低级醚在水中的溶解度与相对分子质量相近的醇接近。
醚是常用的有机溶剂。
三、化学性质醚的化学性质稳定,稳定性仅次于烷烃。
(一)钅羊 盐的形式R O R + H 2SO 4R O RHHSO 4R O R + HSO 4R O RH HSO 4+ H 2O+ H 3O醚能以钅羊 盐的形式溶于浓酸中,借此可与不溶于浓酸的烷烃或卤代烃相区别。
(二)醚键断裂在浓酸(如氢卤酸)作用下,醚键断裂,生成醇和卤代烃。
含有两个不同烃基的混2O CH C H 32CH CH 3混醚:单醚:环醚:C 2H 5–O –C 2H 5两烃基+“醚”先小后大 先芳后脂,复杂醚以烃为母体称作“环氧烃”CH 3–O –CH 3 甲醚乙醚苄醚CH 3–O –C 2H 5甲乙醚 苯基甲基醚1,2-环氧丙烷 环氧乙烷1,4-环氧丁烷醚CH 3CHCH –O –CH 3 CH 32-甲基-3-甲氧基丁烷CH 3 CH 3R O + HSO 4R O RH HSO 4+ H 2O + H 3O醚,通常是较小的烃基生成卤代烃,较大的烃基生成醇。
如果氢卤酸过量并加热,生成的醇可进一步反应生成卤代烃。
含有苯基的混醚,总是生成酚和卤代烃,二苯基的混醚则不发生醚键断裂.。
醚键断裂的机理为亲核取代。
CH 3OCH 2CH(CH 3)2+HI CH 3I +(CH 3)2CHCH 2OH32OCH 3+2HI 2CH 3I +OH CH 2OH(三)环氧化合物环氧化合物是特指含有三元环的醚及其衍生物。
环氧化合物的普通命名法称为氧化某烯,环氧化合物的衍生物有两种命名法: (1) 将环氧化合物的母体命名为环氧乙烷,三元环中的氧原子编号为1,两个碳原子依次编号; (2) 环氧化合物命名为环氧某烷,并标明与氧原子成环后的碳原子的位置。
醚

醚的命名
• 1. 习惯法
• 结构简单的醚一般采用习惯法命名,方法是将 “烃基名”写在“醚”字前,单醚在烃基名前加 “二”(但除芳醚和不饱和醚外,一般可省略)。 如 • CH3CH2OCH2CH3 (二)乙醚 • 若是混醚,则按次序规则中,较大基团在后书写。 如:CH3OCH2CH3 甲乙醚 • CH3OCH2CH=CH2 甲基烯丙基醚 • 芳醚书写时,原则是先写芳基,后写烷基。如: OCH2CH3 OCH3 苯甲醚 茴香醚 苯乙醚
(2)混合醚反应时,碳氧键断裂的顺序:
3o烷基> 2o烷基> 1o烷基>甲基>芳基。
四 1,2环氧化合物的开环反应
1. 环氧化合物在酸性条件下的开环反应
H H O CH 3 CH 2CH 3
H+
H H O+ H
CH3 CH2CH3
H H O + H
H H
+
CH3 CH2CH3
H2O18
H
H
18 +
OH2
-H+
OH
18
CH 3 CH 2CH 3
OH
OH
CH 3 CH 2CH 3
环氧化合物与硼烷的反应
CH 3
H O
H
H
+ B2H6
Hale Waihona Puke CH 3 H B HH
H O H
H
2
H CH 3 O
H
H
(CH3CH2CH2O)3B
H2O
CH3CH2CH2OH
2. 1,2环氧化合物的碱性开环反应
H CH3 O
H
• 措 施 : ① 久 贮 的 醚 在 使 用 前 , 用 FeSO4 或 Na2SO3等还原剂处理后方可蒸馏。 • ② 贮存醚时,可在醚中加入少量的金属 钠或还原铁粉以防止过氧化物的生成。
有机化学醚

O (1)位阻较大
-
Nu
CH3CH CH2
O (2)
N u-:RO-、PhO-、RMgX
OH CH3CH
CH2 H2O Nu
反应特点:碱作为Nu-从氧环背后进攻,断键与成键同时进行, 为SN2反应。对于不对称环氧化合物,试剂选择进攻取代基较 少(即位阻较小)的环碳原子。
H 3C H 5C 2
( 主)
C CH 2 + -OCH3
O
CH3OH
H 3C H 5C 2
C CH 2OCH 3 OH
*立体化学:若被亲核试剂进攻的碳原子为手性碳原子,则构型 转化。
CH3
eg. H
R
R
O
H3C H
NH3.H2O
H3C H
OH H2N
SH
CH3
O
C2H5OH
OH H
-OC2H5
H OC2H5
H2C
CH2
O
H2O/H+ ROH/H+ HX HCN
CH3
CH3 C CH3 Br
C2H5ONa C H 3
CH3 C CH2
➢三 醇与烯烃的加成
1. 烯烃与醇反应制备叔烷基醚
R
HCl
C CH2 + HO R
R'
•合成上的应用:保护醇羟基
R R' C O R
CH3
例:完成转变 HO
Br
HO
合成路线
HO
Br
H3C
CH3 CO CH3
H2C
CH3 CH3
SO 3 H
ONa
Br2 Fe
Mg Br 乙醚
MgBr
H2C
第三节 醚

单醚:
CH3-O-CH3 CH3-CH2-O-CH2-CH3
(二)甲醚 (二)乙醚
CH2=CH-O-CH=CH2
O
二乙烯醚
二苯醚
混醚: 混醚:
CH3-O-CH2-CH3
H3C -O-CH2-CH3
甲乙醚
对-甲苯乙醚
二、乙醚 乙醚是最重要的醚。 乙醚是最重要的醚 。 是无色透明的 液体,沸点34. 有特殊的气味, 液体,沸点34.5℃,有特殊的气味, 极易挥发及着火。 极易挥发及着火 。 乙醚在水中溶解度 又比水轻。 乙醚化学性质稳定, 小 , 又比水轻 。 乙醚化学性质稳定 , 又能溶解许多有机物, 又能溶解许多有机物 , 是常用的有机 溶剂。 溶剂。
2. 盐的形成 乙醚不溶于水,但能溶于浓强酸, 乙醚不溶于水,但能溶于浓强酸, 如浓硫酸、浓盐酸等。 如浓硫酸、浓盐酸等。
CH3-CH2-O-CH2-CH3 + HCl H ¨ ]+ Cl[ CH3-CH2-O-CH-CH3
盐(溶于酸) 溶于酸)
第三节 醚 一、醚的分类和命名 (一)分类 醚结构中与氧相连的两个烃基 相同的称为单醚 单醚, 相同的称为单醚,两个烃基不 同的则称为混醚 混醚。 同的则称为混醚。
(二)命名
单醚的命名是在烃基名称后面加“ 单醚的命名是在烃基名称后面加 “ 醚 ” 字 ; 混醚命名时,两个烃基的名称都要写出来, 混醚命名时 , 两个烃基的名称都要写出来 , 较小的烃基的名称放在前面, 较小的烃基的名称放在前面 , 较大的烃基 的名称放在后面, 的名称放在后面 , 但芳香烃基的名称放在 脂肪烃基的前面, 然后再加上“ 脂肪烃基的前面 , 然后再加上 “ 醚 ” 字 。 单醚分子中烃基为烷基时, 往往把“ 单醚分子中烃基为烷基时 , 往往把 “ 二 ” 字省去,例如: 字省去,CH3 + O2
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
ONa + (CH3)2 SO4 NaOH
+ +
OCH3 + CH3OSO3Na
10.9 醚的化学性质
醚的结构与醇相似,脂肪醚中, 为 杂化, - - 键角接 醚的结构与醇相似,脂肪醚中,O为SP3杂化,C-O-C键角接 近109.5°。 °
O CH3 110° CH3 O CH3
在芳香醚中,O为SP2杂化,C-O-C键角为 在芳香醚中, 为 杂化, - - 键角为120°。 ° 键角为 在醚分子中,与氧相连的都是烃基,分子极性较小, 在醚分子中,与氧相连的都是烃基,分子极性较小,化学活性较 它的稳定性稍次于烷烃。醚键一般对碱、氧化剂、 低,它的稳定性稍次于烷烃。醚键一般对碱、氧化剂、还原剂都 非常稳定,也不与金属钠作用。但是,醚键对酸不稳定, 非常稳定,也不与金属钠作用。但是,醚键对酸不稳定,能与酸 作用。因为醚键中,氧上具有未共用的电子对,相当于路易斯碱。 作用。因为醚键中,氧上具有未共用的电子对,相当于路易斯碱。 所以可与酸作用形成洋盐 可与酸作用形成洋盐。 所以可与酸作用形成洋盐。
第十章 (二)醚(Ethers)
10.7 醚的分类与命名 10.8 醚的制备 10.9 醚的性质 1、羊盐的形成 、 钅 2、醚键的断裂 、 3、过氧化合物的形成 、 10.10 重要的醚 乙醚、环醚、冠醚 乙醚、环醚、
10.7 醚的分类与命名
醚可看作是醇分子中羟基被烃基取代后的产物。 →ROR’ 醚可看作是醇分子中羟基被烃基取代后的产物。ROH→ → 醚和同碳醇是同分异构体,在醚分子中,氧基- -叫作“ 醚和同碳醇是同分异构体,在醚分子中,氧基-O-叫作“醚 键”。 饱和 CH3 OCH3 醚
CH3CHCH2CH2CH3 CH3 O CH CHCH2CH3 HO OCH2CH3 OCH3 2-甲氧基戊烷 1-甲氧基-1-丁烯 对乙氧基苯酚
10.8 醚的制备
1)醇脱水法 )
2 ROH
H2SO4
R O R + H 2O
这里除了生成醚外,如果温度过高,还有烯烃生成。 这里除了生成醚外,如果温度过高,还有烯烃生成。工业上是将 醇蒸汽通过加热的Al 催化剂制得醚。 醇蒸汽通过加热的 2O3催化剂制得醚。 Al2O3 CH3CH2OCH2CH3 + H2O 2 CH3CH2OH 300℃ 醇脱水法制醚只适用于制备单醚,如果用不同的醇脱水制醚, 醇脱水法制醚只适用于制备单醚,如果用不同的醇脱水制醚,得 到的是混合物,不好分离,无制备意义。 到的是混合物,不好分离,无制备意义。 2)威廉姆森(Williamson)合成法 )威廉姆森( ) 即用醇钠与卤代烃发生亲核取代反应
+ +
3、过氧化物的生成
醚对氧化剂比较稳定,但是,遇空气长期接触, 醚对氧化剂比较稳定,但是,遇空气长期接触,却能被空气中的 氧逐渐氧化生成过氧化物。一般认为氧化是首先发生在α 氧逐渐氧化生成过氧化物。一般认为氧化是首先发生在α-C-H - 键上,然后再转变成结构更为复杂的过氧化物。 键上,然后再转变成结构更为复杂的过氧化物。
RCH2OCH2R'
O2 (空气)
RCH2OCHR' (过氧化物) OOH
过氧化物是易发生爆炸的物质,由于它沸点较高,不易被蒸出, 过氧化物是易发生爆炸的物质,由于它沸点较高,不易被蒸出, 所以在蒸馏含有过氧化物的乙醚时,过氧化物就残留在容器内, 所以在蒸馏含有过氧化物的乙醚时,过氧化物就残留在容器内, 如果继续加热,就会发生爆炸。 如果继续加热,就会发生爆炸。 为了避免爆炸事故的发生,一般在蒸馏放置较久的乙醚前, 为了避免爆炸事故的发生,一般在蒸馏放置较久的乙醚前,可采 用KI-淀粉试纸来检验,如果有过氧化物存在,会使试纸显蓝 -淀粉试纸来检验,如果有过氧化物存在, 色。 要破坏过氧化物,可加入还原剂( 要破坏过氧化物,可加入还原剂(如Na2SO3、FeSO4等)搅拌 反应除去。 反应除去。
10.10 重要的醚
另外,在蒸馏乙醚时,不要蒸干,以免残留的过氧化物爆炸。 另外,在蒸馏乙醚时,不要蒸干,以免残留的过氧化物爆炸。 在贮藏乙醚时,为防止过氧化物的生成,可加入少量的金属钠、 在贮藏乙醚时,为防止过氧化物的生成,可加入少量的金属钠、 或铁粉,以避免过氧化物的生成。 或铁粉,以避免过氧化物的生成。
环氧乙烷的性质
环氧乙烷在酸催化下进行的是亲电开环反应。 环氧乙烷在酸催化下进行的是亲电开环反应。
H2O CH2 CH2 OH OH2 CH2 CH2 O H CH2 CH2 O H H CH2 CH2 OH OH CH2 CH2 OH OCH3
CH3OH CH2 CH2 H OH HOCH3 HCl HO CH2CH2 Cl
+
威廉姆森合成法制醚
另外,在制备芳香醚时,也不能用醇钠进攻卤代苯,只能用酚钠 另外,在制备芳香醚时,也不能用醇钠进攻卤代苯, 进攻卤代烃。 进攻卤代烃。
ONa + CH3Cl Cl + CH3ONa OCH3 + NaCl
这是因为卤代苯为乙烯型卤代烃,卤素最不活泼, 这是因为卤代苯为乙烯型卤代烃,卤素最不活泼,最不易被取代 乙烯型卤代烃 但如果卤素的邻、对位上有硝基时,则可进行反应。 掉。但如果卤素的邻、对位上有硝基时,则可进行反应。 此外,制备芳香醚还可用硫酸二甲酯、硫酸二乙酯作烷基化试剂。 此外,制备芳香醚还可用硫酸二甲酯、硫酸二乙酯作烷基化试剂。
不饱 醚 CH3 OCH CH2 和 芳醚 Ar O CH3 ArOAr 醚 据 根 所边 基 构 烃 结 的不 可 为 同 分 CH2 CH2 O O O 环醚 OOO O 硫醚 CH3 S CH3 单 C2 H5OC2H5 ArOAr 醚 根 醚 两 所 烃 的 同 据 键 端 连 基 异 分 混 CH3OCH2 CH3 ArOCH3 醚
醚的命名
醚的命名有习惯命名法和系统命名法。 醚的命名有习惯命名法和系统命名法。简单的醚常用习惯命名法 习惯命名法 1)单醚,叫“二某基醚”,有时“二”和“基”可以省略。 二某基醚” 有时“ 可以省略。 )单醚,
CH3CH2 OCH2CH3 O CH2
二乙基醚(乙醚)
二苯基醚(二苯醚) CH O CH CH2 二乙烯基醚
10.10 重要的醚 1)乙醚(自学) )乙醚(自学) 2)环氧乙烷 )
环氧乙烷是最简单的环醚,由于三元环的张力较大, 环氧乙烷是最简单的环醚,由于三元环的张力较大,再加上氧的 电负性也较大,所以环氧乙烷的化学性质非常活泼, 电负性也较大,所以环氧乙烷的化学性质非常活泼,在酸或碱催 化下能与许多物质作用,生成重要的化工产品。所以, 化下能与许多物质作用,生成重要的化工产品。所以,环氧乙烷 是重要的有机合成原料。 是重要醚是一个路易斯碱,在常温下,能与强酸作用而形成洋盐。 由于醚是一个路易斯碱,在常温下,能与强酸作用而形成洋盐。
R R
O + H2SO4
R R
OH HSO4
H 2O
ROR + H2SO4
利用这个性质,可把醚从其它不溶于酸的物质(如烷烃、卤代烃) 利用这个性质,可把醚从其它不溶于酸的物质(如烷烃、卤代烃) 除去。当然,也可用于醚的定性鉴别 定性鉴别。 中除去。当然,也可用于醚的定性鉴别。 上述形成的醚盐是一个弱碱强酸盐,遇水就很快水解出原来的醚。 上述形成的醚盐是一个弱碱强酸盐,遇水就很快水解出原来的醚。 可利用这个性质将醚从其它物质中分离出来。 分离出来 可利用这个性质将醚从其它物质中分离出来。 醚除了能与质子酸形成洋盐外,还可以与其它路易斯酸( 醚除了能与质子酸形成洋盐外,还可以与其它路易斯酸(如BF3、 R AlCl3、RMgX)等生成盐。 R )等生成盐。 F R O O B F R Mg X R F O R R
醚的命名
3)硫醚的命名就是把相应的“醚”换成“硫醚”。 )硫醚的命名就是把相应的“ 换成“硫醚” 如: CH3SCH2CH3 甲乙硫醚 4)多元醇形成的醚 CH3OCH2CH2 OCH3 CH3OCH2 CH2OH )
乙二醇二甲醚
乙二醇单甲醚
5)对于结构复杂的醚可用系统命名法,系统命名法是以烃作母 )对于结构复杂的醚可用系统命名法, 烷氧基为取代基。 体,烷氧基为取代基。
CH3CH2 O CH3 HI CH3CH2OH + CH3I HI CH3CH2I + CH3I
醚键的断裂
对于苯甲醚,同样是先从甲基一端断裂。 对于苯甲醚,同样是先从甲基一端断裂。
O CH3
HI
OH + CH3 I HI I
过量, 但,即使HI过量,生成的苯酚也不会发生 -O键断裂生成碘代 即使 过量 生成的苯酚也不会发生C- 键断裂生成碘代 苯。因为在O与苯环之间存在着 -π共轭,键能较强,不易断裂。 因为在 与苯环之间存在着P- 共轭,键能较强,不易断裂。 与苯环之间存在着 所以二苯醚是不与HI发生醚的断裂反应 发生醚的断裂反应。 所以二苯醚是不与 发生醚的断裂反应。 在上述反应中,生成的CH 沸点 沸点(42.4℃ )较低,一加热就可被 较低, 在上述反应中,生成的 3I沸点 ℃ 较低 蒸出,将蒸出的CH 通入 通入AgNO3的醇溶液中,由于生成 的醇溶液中,由于生成AgI的 蒸出,将蒸出的 3I通入 的 量来计算原来醚分子中甲氧基的含量,这种方法叫蔡塞尔 量来计算原来醚分子中甲氧基的含量,这种方法叫蔡塞尔 (Zeisel)甲氧基定量分析法。 甲氧基定量分析法。 甲氧基定量分析法
2)混醚命名时,将两个烃基按先简单后复杂的顺序排在“醚” )混醚命名时,将两个烃基按先简单后复杂的顺序排在“ 先简单后复杂的顺序排在 之前, 芳基应放在烃基之间。 之前,但芳基应放在烃基之间。
CH3OCH2CH3 CH3CH2 O CH CH2 OCH3 甲基乙基醚 乙基乙烯基醚 苯基甲基醚 (甲乙醚) (苯甲醚)
CH3CH2ONa + CH3 I
CH3CH2OCH3 + NaI
