十五硝基化合物和胺课后参考答案
【免费下载】高教第二版徐寿昌有机化学课后习题答案第15章
对全部高中资料试卷电气设备,在安装过程中以及安装结束后进行高中资料试卷调整试验;通电检查所有设备高中资料电试力卷保相护互装作置用调与试相技互术关,系电,力根通保据过护生管高产线中工敷资艺设料高技试中术卷资,配料不置试仅技卷可术要以是求解指,决机对吊组电顶在气层进设配行备置继进不电行规保空范护载高与中带资负料荷试下卷高问总中题体资,配料而置试且时卷可,调保需控障要试各在验类最;管大对路限设习度备题内进到来行位确调。保整在机使管组其路高在敷中正设资常过料工程试况中卷下,安与要全过加,度强并工看且作护尽下关可都于能可管地以路缩正高小常中故工资障作料高;试中对卷资于连料继接试电管卷保口破护处坏进理范行高围整中,核资或对料者定试对值卷某,弯些审扁异核度常与固高校定中对盒资图位料纸置试,.卷保编工护写况层复进防杂行腐设自跨备动接与处地装理线置,弯高尤曲中其半资要径料避标试免高卷错等调误,试高要方中求案资技,料术编试交写5、卷底重电保。要气护管设设装线备备置敷4高、调动设中电试作技资气高,术料课中并3中试、件资且包卷管中料拒含试路调试绝线验敷试卷动槽方设技作、案技术,管以术来架及避等系免多统不项启必方动要式方高,案中为;资解对料决整试高套卷中启突语动然文过停电程机气中。课高因件中此中资,管料电壁试力薄卷高、电中接气资口设料不备试严进卷等行保问调护题试装,工置合作调理并试利且技用进术管行,线过要敷关求设运电技行力术高保。中护线资装缆料置敷试做设卷到原技准则术确:指灵在导活分。。线对对盒于于处调差,试动当过保不程护同中装电高置压中高回资中路料资交试料叉卷试时技卷,术调应问试采题技用,术金作是属为指隔调发板试电进人机行员一隔,变开需压处要器理在组;事在同前发一掌生线握内槽图部内 纸故,资障强料时电、,回设需路备要须制进同造行时厂外切家部断出电习具源题高高电中中源资资,料料线试试缆卷卷敷试切设验除完报从毕告而,与采要相用进关高行技中检术资查资料和料试检,卷测并主处且要理了保。解护现装场置设。备高中资料试卷布置情况与有关高中资料试卷电气系统接线等情况,然后根据规范与规程规定,制定设备调试高中资料试卷方案。
第15章 硝基化合物和胺-1

叔硝基化合物与亚硝酸不起反应。 叔硝基化合物与亚硝酸不起反应。
此性质可用于鉴别三类硝基化合物。 此性质可用于鉴别三类硝基化合物。
2. 硝基的还原 Fe、Sn、Zn + HCl还原 、 、 还原
NH2 NH2 Sn + HCl
NO2 Fe + HCl
NH2
NO2
NH2
Ni、Pt、Pd催化加氢 、 、 催化加氢
15.4 硝基化合物的化学性质
1. 与碱作用
O CH3 N O
O CH2 N O CH2 N O
NaOH
O CH2 N O
O CH2 N O O
Na
+ H2O
α RCH2
O N O RCH N
OH O
NaOH H
O RCH N O Na
硝基式
酸式
可以借此分离低级的伯仲硝基化合物与叔硝基基化合物
NaOH R CH2 NO2 + HONO R CH NO2 R C NO2 Na NO 蓝色 结晶 R2 CH NO2 + HONO R2 C NO 蓝色 结晶 NO2 NaOH 不溶于 NaOH 蓝色不变 NO 溶于 NaOH 呈红色溶液
胺的结构
N:1s22s22p3 :
N R
1
R R2
3
15.6 胺的制法
芳香族硝基化合物的还原
Ni or Pt or Pd NH2
NO2
+ 3 H2
NO2 Fe + HCl
NH2
铵的烷基化 脂肪族的卤代烷与氨作用
RX + NH3 RNH2 + RX R2NH + RX R3N + RX RNH3 X R2NH2 X R3NH X R4NH2 X NH3 NH3 NH3 RNH2 + NH4 X R2NH + NH4 X R3N + NH4 X
23第十五章硝基化合物和胺

芳香叔胺发生芳环的亲电取代反应,生成有色固体。
CH3 N CH3 ON NaNO2/HCl ON CH3 N CH3
分类
脂肪胺与亚硝酸的反应
NaNO2, HCl 0-5oC -N2
芳香胺与亚硝酸的反应
ArNH2
NaNO2, HCl 0-5oC + [Ar-NN]Cl-
5、酰胺的 Hofmann 降解( Hofmann重排)
O R C NH2
Br2 / NaOH R NH2 + CO2
6、Gabriel 伯胺合成法:在强碱条件下,邻 苯二甲酰亚胺转化为邻苯二甲酰亚胺负离子, 该负离子与卤代烃进行烷基化,再进行水解 (或肼解)而得到伯胺。
O
KOH
O R N or K2CO3 O K 或 R OTs X
气味并有毒。硝基化合物比重大于一,硝基越
多比重越大;不溶于水,溶于有机溶剂;分子
的极性较大,沸点较高。多硝基化合物受热时 以分解爆炸。
15.3.硝基化合物的物理性质
Physical of Nitration compouds
硝基乙烷红外光谱:
15.3.硝基化合物的物理性质
Physical of Nitration compouds
structural and Nomenclature of Nitration compouds
烃分子中的氢原子被硝基取代后的衍生 物称为硝基化合物。 根据硝基的数目可分为一硝基化合物和 多硝基化合物。 根据硝基连接的碳原子又可分为伯、仲、 叔硝基化合物。
硝基化合物的命名 ——将硝基作为取代基
1,4-戊二胺
第十五章 硝基化合物和胺

5
··
O R CH2 N O
OH RCH N O
酮式(硝基式)
烯醇式(假酸式)
烯醇式中连在氧原子上的氢相当活泼,反映了分子的酸性,称假酸式,其能与强碱成盐,
所以含有α-氢硝基化合物可溶于氢氧化钠溶液中,无 α-氢硝基化合物则不溶于氢氧化钠
溶液。利用这个性质,可鉴定是否含有α-氢的伯、仲硝基化合物和叔硝基化合物。
对映异构体之间,相互转化是不可能的。事实上,它能分离出右旋和左旋异构体。
§15.6 胺的制法
CH3
+
N C2H5
= CH2 CHCH2 C6H5
1. 氨或胺的烃基化
CH3
+N C6H5
轭效应,使卤原子与苯环碳原子结合得更加紧密,因此卤原子很不活泼。在一般条件下,
卤代苯不能发生亲核取代反应。例如在一般条件下氯苯很难和氢氧化钠作用,发生碱性水
解。但如果在氯苯C l 分子中氯原子的邻、对位引入硝O H 基,由于硝基的吸电子诱导效应和吸电
370℃
子共轭效应,硝基邻位或对位的电水子云密度降低,从而使 C-Cl 键极性增强,因此氯原子活
氮原子的电子结构为:
1 s2 ,
2 s2 ,
2
p1
x
,
2 py1 ,
2 pz1
其中三个 2p 轨道都没有完全填满,可以成键。氮原子应为三价,且键角似乎应互为 90°。
但实际上 N 原子和 H 原子或烷基形成的单键的键角为 109 °。这就是说,N 原子在成键时,
10
··
发生了轨道的杂化,形成四个 sp3 杂化轨道,其中三个轨道分别与氢或碳原子形成三个σ键, 未共用电子对占据另一个 sp3 杂化轨道,呈棱锥形结构。
第十五章 硝基化合物和胺(习题解答)

解答:
解答:与HNO2 反应能放出气体的为乙胺;或:加入 CHCl3的强碱醇溶液,有恶臭的为为乙胺。另外一种 化合物为乙酰胺。
5、比较下列各组化合物的碱性,试按碱性强弱排列
解答:
解答:
解答: 甲胺 N-甲基苯胺 苯胺 三苯胺
解答:
6、完成下列各反应式:
解答:
解答:
霍夫曼规 则P382
1、命名下列化合物 解答: N-苯基对苯二胺
对氨基二苯胺
三甲基异丙基氢氧化铵
氢氧化异丙基三甲铵 N-甲基苯磺酰胺
氯化对溴苯三甲铵
三甲基对溴苯基氯化铵
对 亚 硝 基 -N,N- 二 甲 基 苯 胺 (P379) N,N-二甲基对亚硝基苯胺 丙烯腈
2、写出下列化合物的构造式
解答:
3、用化学方法区别下列各组化合物
有机化学 Organic Chemistry
教材:徐寿昌 主编 高等教育出版社
第十五章
硝基化合物和胺
(习题解答)
主讲教师:王启宝 教授
wqb@
中国矿业大学(北京)化学与环境工程学院
第十五章
作业(P387)
硝基化合物和胺
1(5、6、7、8、9、10) 2(3、4、5、6、7) 3(1、3) 5(1、2、3、4) 6、 7(4、6、7) 8(2、3、4、6、8、10*)提示:第10小题由于硝基 苯不发生傅克反应,故要求选择合适的酰卤化合物与 苯发生傅克反应。 11。
+ (CH3)3N
解答:
-氨基酸的制 备P372
7、完成下列转化:
解答:
解答:
解答:
降解!减少 一个碳!
8、以苯、甲苯及三个碳以下的有机物为原料合成下 列化合物:
有机化学_第二版答案(全)

《有机化学》第二版习题参考答案第二章烷烃1、用系统命名法命名下列化合物(1)2,3,3,4-四甲基戊烷(2)3-甲基-4-异丙基庚烷(3)3,3,-二甲基戊烷(4)2,6-二甲基-3,6-二乙基辛烷(5)2,5-二甲基庚烷(6)2-甲基-3-乙基己烷(7)2,2,4-三甲基戊烷(8)2-甲基-3-乙基庚烷2、试写出下列化合物的结构式(1) (CH3)3CC(CH2)2CH2CH3(2) (CH3)2CHCH(CH3)CH2CH2CH2CH3(3) (CH3)3CCH2CH(CH3)2(4) (CH3)2CHCH2C(CH3)(C2H5)CH2CH2CH3(5)(CH3)2CHCH(C2H5)CH2CH2CH3(6)CH3CH2CH(C2H5)2(7) (CH3)2CHCH(CH3)CH2CH3(8)CH3CH(CH3)CH2CH(C2H5)C(CH3)33、略4、下列各化合物的系统命名对吗?如有错,指出错在哪里?试正确命名之。
均有错,正确命名如下:(1)3-甲基戊烷(2)2,4-二甲基己烷(3)3-甲基十一烷(4)4-异丙基辛烷(5)4,4-二甲基辛烷(6)2,2,4-三甲基己烷5、(3)>(2)>(5)>(1) >(4)6、略7、用纽曼投影式写出1,2-二溴乙烷最稳定及最不稳定的构象,并写出该构象的名称。
H交叉式最稳定重叠式最不稳定8、构象异构(1),(3)构造异构(4),(5)等同)2),(6)9、分子量为72的烷烃是戊烷及其异构体(1) C(CH3)4(2) CH3CH2CH2CH2CH3 (3) CH3CH(CH3)CH2CH3(4) 同(1)10、分子量为86的烷烃是己烷及其异构体(1)(CH3)2CHCH(CH3)CH3(2) CH3CH2CH2CH2CH2CH3 , (CH3)3CCH2CH3 (3)CH3CH2CH(CH3)CH2CH3(4)CH3CH2CH2CH(CH3)214、(4)>(2)>(3)>(1)第三章 烯烃1、略2、(1)CH 2=CH — (2)CH 3CH=CH — (3)CH 2=CHCH 2— CH 2CH CH 3M eH H i-P rE t M en-P rM e M e E t i-P rn-P r (4)(5)(6)(7)3、(1)2-乙基-1-戊烯 (2) 反-3,4-二甲基-3-庚烯 (或(E)-3,4-二甲基-3-庚烯 (3) (E)-2,4-二甲基-3-氯-3-己烯 (4) (Z)-1-氟-2-氯-2-溴-1-碘乙烯(5) 反-5-甲基-2-庚烯 或 (E)-5-甲基-2-庚烯 (6) 反-3,4-二甲基-5-乙基-3-庚烯 (7) (E) -3-甲基-4-异丙基-3-庚烯 (8) 反-3,4-二甲基-3-辛烯 4、略 5、略 6、CH 3CH 2CHC H 2CH 3CH 3CH 2CCHC H 3CH 3OH BrCH 3CH 2CCHC H3CH 3Cl ClCH 3CH 2C CHC H3CH 3OH OHCH 3CH 2CHCHC H 3CH 3OHCH 3CH 2COCH3CH 3CHOCH 3CH 2CHCHC H 3CH 3Br(1)(2)(3)(4)(5)(6)(7)7、活性中间体分别为:CH 3CH 2+ CH 3CH +CH 3 (CH 3)3C + 稳定性: CH 3CH 2+ > CH 3CH +CH 3 > (CH 3)3C + 反应速度: 异丁烯 > 丙烯 > 乙烯8、略9、(1)CH 3CH 2CH=CH 2 (2)CH 3CH 2C(CH 3)=CHCH 3 (有顺、反两种) (3)CH 3CH=CHCH 2CH=C(CH 3)2 (有、反两种)用KMnO 4氧化的产物: (1) CH 3CH 2COOH+CO 2+H 2O (2)CH 3CH 2COCH 3+CH 3COOH (3) CH 3COOH+HOOCCH 2COOH+CH 3COCH 310、(1)HBr ,无过氧化物 (2)HBr ,有过氧化物 (3)①H 2SO 4 ,②H 2O (4)B 2H 6/NaOH-H 2O 2 (5)① Cl 2,500℃ ② Cl 2,AlCl 3(6)① NH 3,O 2 ② 聚合,引发剂 (7)① Cl 2,500℃,② Cl 2,H 2O ③ NaOH 11、烯烃的结构式为:(CH 3)2C=CHCH 3 。
第十五章 硝基化合物和胺

(一) 硝基化合物15.1硝基化合物的分类、结构和命名硝基化合物是指分子中含有硝基(-NO2)的化合物,可以看作是烃分子中的氢原子被硝基取代后得到的化合物,常用RNO2或ArNO2表示。
1..分类⑴根据烃基不同可分为:脂肪族硝基化合物R—NO2和芳香族硝基化合物ArNO2⑵根据硝基的数目可分为:一硝基化合物和多硝基化合物。
⑶根据C原子不同可分为:可分为伯、仲、叔硝基化合物。
2.结构通式:R—NO2 或ArNO2硝基是一个强吸电子基团,因此硝基化合物都有较高的偶极矩。
通过键长的测定发现,硝基中的氮原子和两个氧原子之间的距离相同。
根据杂化轨道理论,硝基中的氮原子是sp2杂化的,它以三个sp2杂化轨道与两个氧原子和一个碳原子形成三个共平面的σ键,未参于杂化的一对p电子所在的p轨道与每个氧原子的一个p轨道形成一个共轭π键体系。
CH3NO2:偶极矩为3.4D;键长均为0.121nm3.命名卤代烃相似,通常硝基作为取代基。
CH3NO硝基甲烷 2-硝基丙烷对硝基苯甲酸2,4,6-三硝基苯酚(苦味酸) 2,4,6-三硝基甲苯(T N T) 1,3,5-三硝基苯(T N B)15.2制备R-R-+或R NO-+R NOO -+CH3CHCH3NO2HOOC NO2OHO2NNO2NO2CH3O2NNO2NO2O2NNO2NO21.烃类直接硝化 ①芳烃硝化②脂肪族硝基化合物2.卤代烷硝基取代15.3物理性质1..硝基是一个强极性基,硝基化合物的偶极矩较大。
2..沸点比相应的卤代烃高。
3.多硝基化合物具有爆炸性。
4.液体硝基化合物是良好的有机溶剂。
5.有毒。
6.比重大于1。
15.4化学性质15.4.1酸性脂肪族硝基化合物中,硝基的α碳原子上有氢原子时,能产生互变异构现象。
CH 2N OH R R O硝基式 酸式酸式含量较低,平衡主要偏向硝基式一方。
加碱可使平衡向右移动,使全部转变为酸式的盐而溶解。
例如:CH 3CH 2CH 3CH 3CH 2CH 2NO 23CH 2NO 23NO 2CH 3CHCH 3NO 2R —X AgNO 2R-NO 2+R-ONO 或 NaNO 2硝基化合物亚硝酸酯O - O —X 尿素DMF N O - OR +X -H 2O N —N O OR +X -在不同的溶剂中可得到不同的主产物N O 2H 2SO 4HNOCH 2NO 2OHNaOHHClCH = NO Na +-15.4.2还原反应硝基容易被还原,尤其是直接连在芳环上的硝基,还原产物随还原介质的不同而有所不同。
有机化学第15章 硝基化合物和胺

CH3OH
NH3 ,Al2O3 380~450℃
CH3NH2
CH3OH,Al2O3 380~450℃
(CH3)2NH
CH3OH,Al2O3 380~450℃
(CH3)3N
5MPa
5MPa
5MPa
Cl
+ NO2
2 NH3
CH3COONH4
170℃
NH2
+ NO2
NH4Cl
NO2
NO2
2、醛、酮的还原氨化
NO2 Fe + HCl
NH2
注意: SnCl2 + HCl 是一个选择性还原剂,当苯环上同 时连有羰基和硝基时,只还原硝基。
NO2
NH2
SnCl2+HCl
CHO
CHO
(2)碱性介质中一般还原历程
NO2 N N+ ONN
NN HH
NH2
氧化偶氮苯 偶氮苯 氢化偶氮苯
注意: 多硝基化合物在钠或铵的硫化物、硫氢化物、多
33%
+ + CH3CH2NO2
CH3NO2
26%
9%
+ CH3CH2Cl NaNO2
+ CH3CH2NO2 NaCl
2、芳香族硝基化合物的制备
+ HNO3
H2SO4
50℃
+ NO2
H2O
四、硝基化合物的物理性质
1、 物质状态 脂肪族硝基化合物为无色有香味的液体; 芳香族硝基化合物为有苦杏仁味的淡黄色固体或液体。
1、物质状态 甲胺、二甲胺、三甲胺和乙胺为气体,其它胺为
液体或固体。
许多胺类有难闻的气味,如三甲胺有鱼腥味、1,4丁二胺俗称“腐肉胺”、1,5-戊二胺俗称“尸胺”。
15-第十五章 硝基化合物及胺

第十五章 硝基化合物及胺学习要求1.握硝基化合物及胺的分类、命名法和结构。
2.掌握胺的化学性质:碱性(结构和溶剂化效应),胺的鉴别,季铵盐的性质及霍夫曼规则。
3.掌握硝基化合物的性质。
4.理解三种分子重排反应的实例。
5. 了解腈和异腈的性质。
6.了解硝基化合物的性质、制法以及重要代表物。
7.了解硝基化合物及胺的制法。
8.了解相转移原理作为有机合成新方法的原因。
9. 了解表面活性剂。
计划课时数 4课时重点:胺的化学性质:碱性(结构和溶剂化效应),胺的鉴别,季铵盐的性质及霍夫曼规则。
难点:分子重排反应教学方法 采用多媒体课件、模型和板书相结合的课堂讲授方法。
引言:分子中含有C-N 键的有机化合物称为含氮有机化合物。
含氮有机化合物种类很多,本章简单讨论硝基化合物,重点讨论胺、重氮盐和分子重排反应。
硝基化合物硝基化合物一般写为R-NO 2 ,Ar-NO 2 ,不能写成R-ONO (R-ONO 表示硝酸酯)。
§15.1 硝基化合物分类、命名、结构1. 分类 (略)2. 命名 (与卤代烃相次似)硝基乙烷对硝基甲苯3. 硝基的结构 一般表示为(由一个N=O 和一个N →O 配位键组成)物理测试表明,两个N —O 键键长相等,这说明硝基为一P-π共轭体系(N 原子是以sp2杂化成键的,其结构表示如下:共振结构式:NOOR氮带一个正电荷,每个氧各带½负电荷,这与硝基化合物高的偶极矩相联系。
根据R的不同,偶极矩在3.5D和4.0D之间,由于硝基化合物的偶极特征,结果比相同分子量的酮沸点高(挥发慢)。
如硝基甲烷(MW61)沸点101℃,丙酮(MW58)沸点56℃。
意外地,在水中溶解度低,在水中硝基甲烷的饱和溶液,以重量计少于10%,而丙酮完全溶于水。
§15.2硝基化合物的制备1.烷烃的硝化:烷烃可与硝酸进行气相或液相硝化,生成硝基烷烃。
其中以气相硝化更具有工业生产价值.烷烃的硝化是以游离基历程进行的:烷烃的碳骼对硝化速度具有一定的影响,活性次序为:叔C-H > 仲C-H > 伯C-H 。
第15章 硝基化合物和胺

波谱性质
① 红外光谱(IR) NH 仲缩振动 NH 伸缩振动 CN 伸缩振动 3500~3400 cm1 RNH2 R2NH R3N (二峰) (一峰) (无峰)
1580~1650 ㎝1 650~900 ㎝1 (宽峰) 1000~1350 ㎝1
脂肪胺:1230~1030 ㎝1 芳香胺:1340~1250 ㎝1
例如: 甲胺、二甲胺和三甲胺的工业制备:
• 得到的是混合物,以二甲胺、三甲胺为主。
3. 酰胺及腈等含碳氮重键化合物的还原
RCN
腈 H2 / Ni 或LiAlH4 H2 / Ni 或LiAlH4 LiAlH4
RCH2NH2 RCH2NH2
RCH=NOH
肟
O RCNH2
酰胺
RCH2NH2
Pka: 10
OH
Pka: 7.15
8.0
OH NO2 NO2
7.21
OH O2N NO2
NO2
NO2
4
0.38
(二) 胺
15.5 胺的分类、命名和结构 15.6 胺的制法 15.7 胺的物理性质 15.8 15.9 胺的化学性质 季铵盐和季铵碱
15.5 胺的分类、命名和结构
N N
氧化偶氮苯(黄色) Fe /OH
NO2
电解还原 Fe OH Zn/HCl Zn OH
N N
偶氮苯(桔红 )
NO
亚硝基苯
Zn H 2O
NH NH
氢化偶氮苯(无色) H+
NH2
Zn或Sn, HCl
Zn或Sn, HCl
第十五章 硝基化合物和胺 课后答案

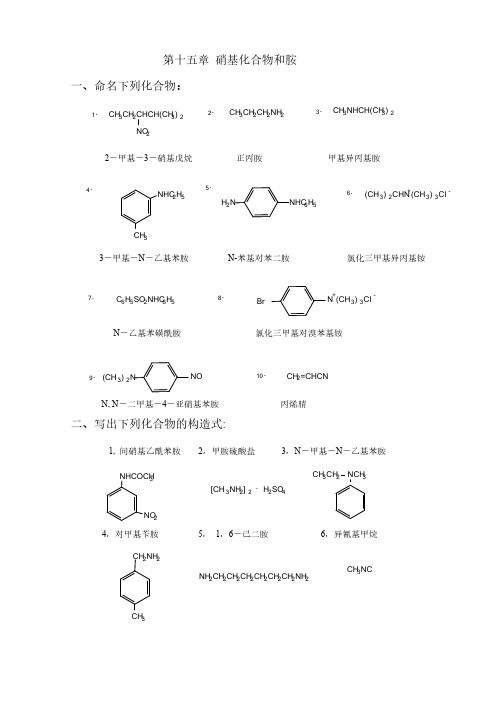
第十五章 硝基化合物和胺一、命名下列化合物:1.CH 3CH 2CHCH(CH 3)2NO 22.CH 3CH 2CH 2NH 23.CH 3NHCH(CH 3)24.NHC 2H 5CH 3H 2N NHC 6H 56.7.C 6H 5SO 2NHC 6H 58.BrN +(CH 3)3Cl -(CH 3)2CHN +(CH 3)3Cl -9.(CH 3)2NNO10.CH 2=CHCNN.N -二甲基-4-亚硝基苯胺 丙烯腈 二、写出下列化合物的构造式:1, 间硝基乙酰苯胺 2,甲胺硫酸盐 3,N -甲基-N -乙基苯胺NO 2NHCOCH 3[CH 3NH 2]2.H 2SO 4NCH 3CH 3CH 24,对甲基苄胺 5, 1,6-己二胺 6,异氰基甲烷CH 2NH 2CH 3NH 2CH 2CH 2CH 2CH 2CH 2CH 2NH 2CH 3NC7,β-萘胺 8,异氰酸苯酯NH 2NCO三、用化学方法区别下列各组化合物: 12、邻甲苯胺 N -甲基苯胺 N,N -二甲基苯胺解:分别与亚硝酸钠+盐酸在低温反应,邻甲苯胺 反应产物溶解, N -甲基苯胺生成黄色油状物,N,N -二甲基苯胺生成绿色固体。
3,乙胺和乙酰胺解:乙胺溶于盐酸,乙酰胺不溶。
4,环己烷与苯胺。
解:苯胺溶于盐酸,环己烷不溶。
四、试用化学方法分离下列化合物:1.CH 3(CH 2)3NO 2(CH 3)3CNO 2CH 3CH 2CH 2NH 2NaOHaq CH 3(CH 2)3NO 2(CH 3)3CNO 2CH 3CH 2CH 2HClCH 3CH 2CH 2NH 2.HClNaOHaqCH 3CH 2CH 2NH 22,苯酚,苯胺和对氨基苯甲酸解:用氢氧化钠水溶液处理,苯酚和对氨基苯甲酸溶于碱溶液,分出有机相。
有机相为含苯胺。
向水相通入二氧化碳,游离出苯酚,对氨基苯甲酸在水相中,酸化得到对氨基苯甲酸。
3,正己醇,2-己酮,三乙胺和正己胺解:加入亚硫酸氢钠饱和水溶液,2-己酮生成晶体分出,然后用稀酸处理这个晶体又得到2-己酮。
徐寿昌有机化学答案13-15章

第十三章 羧酸及其衍生物1、(1) 己酸 (2) 2,2,3-三甲基丁酸 (3) 2-氯丙酸 (4) β-萘甲酸 (5) 3-丁烯酸(6) 环己烷羧酸 (7) 对甲基苯甲酸甲酯 (8) 对苯二甲酸 (9) α-萘乙酸 (10) 乙酸酐 (11) 甲基丁烯二酸酐 (12) N,N-二甲基甲酰胺 (13) 3,5-二硝基苯甲酰氯(14) 邻苯二甲酰亚胺 (15) 2-甲基-3-羟基丁酸 (16) 1-羟基环戊烷羧酸 2、 COOH COOHC C COOH COOHH H CH=CHCOOHCH 3(CH 2)16COOH(1)(2)(3)(4)O OONHCOCH 3C OOCOO C H 2C COOCH 3CH 3(5)(6)(7)(8)H 2C CH 2COH 2CCH 2CH 2NHH 2NCOOC 2H 5CO NH CH 2CO CONH (9)(10 )(11)CH 2N H 2NH 2HC CH O O OCH 2CHOCOCH 3(13 )(14)(12)nn3、略4、(1)草酸 > 丙二酸 > 甲酸 > 乙酸 > 苯酚(2)F 3CCOOH > ClCH 2COOH > CH 3COOH > C 6H 5OH > C 2H 5OH (3)对硝基苯甲酸 > 间硝基苯甲酸 > 苯甲酸 > 苯酚 > 环己醇 5、(1)① Ag(NH 3)2OH ② I 2 + NaOH (或NaHCO 3)(2)① Ag(NH 3)2OH ② △ (3)① Br 2 ② KMnO 4 (4)① FeCl 3/H 2O ② NaHCO 3(5)① AgNO 3 (乙酰氯有AgCl 生成) ② AgNO 3/C 2H 5OH6、(1) CH 3CBr(CH 3)COOH (2) (CH 3)2CHCH 2OH (3) (CH 3)2CHCOCl (4) (CH 3CH(CH 3)CO)2O (5) (CH 3)2CHCOBr (6) (CH 3)2CHCOOC 2H 5 (7) (CH 3)2CHCONH 27、CH 3CH 2CH 2CHO CH 3CH 2COCH 2CH3CH 3CH 2CH 2COOH CH3CH 2CH 2CH 2OHNaHSO 3 (饱和溶液)白色结晶O H 3+△2,4-二硝基苯肼黄色NaOH/H 2O溶于水不溶于水油水分离水层油层H+×××××CH 3CH 2CH 2CHOO H 3+△CH 3CH 2COCH 2CH 3CH 3CH 2CH 2COOHO CO CO O CH 3C H 3CH 3CH 3CH 2CH 2H 2CCOCH 2OCOO H 2CCHCH CH 3C H 3CH 3CH=CHCOOHCO 2 H 2O+(1)(2)(3)(4)(5)8、9、(1)A : H 3O + B :PCl 3、PCl 5(或SOCl 2) C :NH 3 D :P 2O 5,△ E :NH 3 ,△ F :NaOBr + NaOH G :H 2/Pd-BaSO 4(2)C O O HC 2H 5①②C 2H 5M g B r H 3O +,PB r3;(3)2NH 3 ,H 2NCONHCONH 2 (4);OH CNOH COOHO COCO O;10、CH 3CH 2CH 2COOHCH 3CH 2CH 2OHCH 3CH 2CH 2BrCH 3CH 2COOHLiAlH 4PBr 3NaCNO H 3+△(1)CH 3CH 2CH 2COOHCH 3CH 2COOHCH 2CH 2CH(OH)COOH△Cl 2POH -KMnO 4H+(2)CH 2CH 2BrCH 2COOHNaCNO H 3+△过氧化物HBr(3)CH 3COCH 2CH 2CBr(CH 3)2HOCH 2CH 2OHOC CH 2O CH 2CH 2CH 2CBr(CH 3)2C H 3CH 3COCH 2CH 2C(CH 3)2COOHOH 3+干HClMg 干醚CO 2(4)(1)(2)(3)CH 2CH 2CH 2CH 2COO CO COOC 2H 5COOC 2H 5CH 2COOH CH 2COOH11、(4)COOHCOOH C OCH 3O(5)(6)CH 3C COC C 2H 5Br HO CH 3HCH 3NH 2CNOCH 3CH 2CO CH 3CH 2CH 2COCH 2COOC 2H 5CH 2COOC 2H 5(7)(8)(9)(10)12、(1) HCOOCH 3 > CH 3COOCH 3 > CH 3COOC 2H 5 > CH 3COOCH(CH 3)2 > CH 3COOC(CH 3)3(2)CH 3OCO 2CH 3CO 2CH 3ClCO 2CH 3O 2NCO 2CH 3∨∨∨△(1)HC≡CHCH 2=CHCNCH 2=CHCOOCH3HCN CH 3OH , H 2OH 2SO 4CuCl 213、NaCNO H 3+△HBrMg 干醚CO 2(2)CH 3CH(OH)CH 3CH 3CH(Br)CH 3CH 3CH(CH 3)COOHCH 3CH(CH 3)COOHOH 3+NaCNO H 3+△Mg 干醚CO 2(3)OH 3+C 6H 5CH 3C 6H 5CH 2ClC 6H 5CH 2COOHC 6H 5CH 2COOHCl 2光NaCNO H 3+△P(4)Cl 2CH 3CH 2CH 2COOHCH 3CH 2CH(COOH)2NaCNO H 3+△(5)CH 2=CH 2HOBrHOCH 2CH 2BrOHCH 2CH 2COOH(6)CH 3OCHOCH 3OCH(OH)CNO 2NCH(OH)COOHHCNOH 3+NaCNO H 3+△PH+HBr干醚(7)CH 3CH 2BrCH 3CH(Br)COOHCH 3CH(Br)COOC 2H 5CH 3CH(ZnBr)COOC 2H 5CH 3CH 2COOHBr 2C 2H 5OH Zn O H 2CH 2=CH 2CH 3CH 2CHOClHCH 3CH(OH)CH(CH 3)COOH OH 2CH 3CH 2COOH CH 3CH 2COClH 2PCl 5Pd/BaSO 4CH 3CH 2CHO△PH+干醚(8)Br 2C 2H 5OH ZnO H 2ClH OCH 3COCH 3OCH 3CH 3C CH 2COOC 2H 5OZnBrCH 3CH 3C CH 2COOC 2H 5OHBrZnCH 2COOC 2H 5CH 3CH 2OH CH 3COOH BrCH 2COOHBrCH 2COOC 2H 5BrZnCH 2COOC 2H 5[O](9)OH 2OH 2ClH BrZnCH 2COOC 2H5O OZnBr CH 2COOC 2H 5OH CH 2COOH14、从氯到两个羧基的距离不同,诱导效应也不同来解释。
第十五章 硝基化合物和胺

命名: 命名:
和卤烃相似,硝基化合物的命名是以烃作为母体, 硝基作为取代基。例如:
CH3NO2
硝基甲烷
(CH3)2CHNO2
2-硝基丙烷
O2N(CH2)5NO2
1,51,5-二硝基戊烷
CH3 NO2 CH(CH3)2 2-硝基-4-异丙基甲苯 O2 N
CH3 NO2 NO2 2,4,6-三硝基甲苯 (TNT) 2-硝基萘
注意:伯、 注意:伯、仲、叔胺与伯、仲、叔醇的涵义不同。例: 叔胺与伯、 叔醇的涵义不同。 (CH3)3C-OH 叔醇;(CH3)3C-NH2 伯胺; 叔醇;(CH
19
③根据氨基的数目不同: RNH2 一元胺, H2NRNH2 二元胺 等。
命名:
① 习惯命名法:适用于简单胺。 在“胺”字前加烃基的名称。 习惯命名法:适用于简单胺。 字前加烃基的名称。
17
胺的分类、命名和结构
NH3(氨)分子中的氢原子被R-或Ar-取代后的衍生物叫做胺。 胺类广泛存在于生物界,如许多生物碱具有生理或药理作用。 例如:
N CHOHCHCH3 NHCH3
CH3
H OOCCH CH2OH
阿托品
麻黄碱
18
分类: 分类:
① 根据烃基的不同:RNH2 脂肪胺;ArNH2 芳香胺; 根据烃基的不同:RNH 脂肪胺;ArNH ②氨分子中一个、两个、三个氢原子被烃基取代后的生成物,分别 氨分子中一个、两个、三个氢原子被烃基取代后的生成物, 称为伯胺、 称为伯胺、仲胺和叔胺: RNH2 伯胺、1°胺; R2NH 仲胺、2°胺; 伯胺、 仲胺、 R3N 叔胺、3°胺; 叔胺、 相应于氢氧化铵和铵盐的四烃基取代物: R4N+X- 季铵盐, 季铵盐, R4N+OH- 季铵碱。 季铵碱。
15硝基化合物和胺

2、异腈酸酯(R-N=C=O 略)
有机合成
(1)乙醇→甲胺、乙胺、 (1)乙醇→甲胺、乙胺、丙胺 乙醇 (2)乙烯 乙烯→ (2)乙烯→丙腈 (3)乙烯 1,4乙烯→ (3)乙烯→1,4-丁二胺 (4)丙烯 丙烯→ (4)丙烯→甲基丁二酸
(1) C2H5OH C2H5OH C2H5OH (2) H2C (3) H C
+
HCl
NH2
. HCl
苯胺盐酸盐或盐酸苯胺
可利用此性质分离提纯胺类化合物
2、烷基化反应
C2H5-Br
NH3
+ C2H5NH3 Br
NH3
C2H5-NH2 +NH4Br
C2H5Br C2H5-NH2 (C2H5)2NH2Br
NH3 (C2H5)2NH +NH4Br
(C2H5)2NH
C2H5Br
NH3 (C2H5)3N +NH4Br (C2H5)4N+Br
第十五章 硝基化合物和胺
HO
CH3
HO OH N H
H3C N CH2CH2OH OHCH3
+
含氮有机物与生命体的关系极为密 切,本章仅讨论硝基化合物及胺类。 本章仅讨论硝基化合物及胺类。 许多含氮有机物可看成是无机氮 化物的衍生物: 化物的衍生物:
NH3 NH4OH NH4Cl HO-NO2 R-NH2 R4NOH R4NCl R-NO2 Ar-NO2 Ar-NH2
δ-
O R + N
δ-
O
15.2
硝基化合物的制法
脂肪族硝基化合物: 脂肪族硝基化合物:
烷烃和硝酸的混合蒸气在400-500℃气相条件下反 烷烃和硝酸的混合蒸气在400-500℃气相条件下反 400 烷烃分子中的氢可被硝基取代。 应,烷烃分子中的氢可被硝基取代。
15第十五章 硝基化合物和胺

34
用途:
(1). 用于胺类的鉴定 N-取代酰胺均为结晶固体,具有固定的熔点,根据所 测熔点,可推断出原来胺的结构。 (2). 从胺的混合物中分离出叔胺 由于酰胺容易水解,而叔胺又不发生酰基化,利 用这一性质可将叔胺从混合胺中分离出来。
RCONHR' +
H
+
or O H
H 2O
R'NH
2
+ RCOOH
NH2
8
(3)硝基对邻、对位取代基的影响 A . 对卤原子活性的影响
Cl 10% N aO H 400 ℃ 32M Pa Cl NO
2
OH
ONa NaHCO
3
OH NO
2
溶液
H
NO
2
130 ℃
Cl NO
2
ONa NaHCO
3
OH NO
2
溶液
H
NO
2
100 ℃ NO
2
NO
2
NO
2
B. 对酚类酸性的影响(略)
O R C NH2 + Br2 OH
-
R
NH2
O C NH2 N a O H ,B r 2 ~90% NH2
21
5. Gabriel合成法 邻苯二甲酰亚胺与卤代烷反应,生成N- 烃基邻苯二甲基酰亚胺,水解得到纯伯胺。
O
KOH
O R N or K2CO3 K X
O
NH
N
R
O 邻苯二甲酰亚胺
O
O
NaOH,水解
物理测试表明,两个N—O键键长相等:0.121nm 硝基为P-π共轭体系,N原子是sp2杂化的。
3
有机化学第十五章 硝基化合物和胺

4.掌握区别伯、仲、叔胺的方法及氨基保护在有 机合成中的应用。
硝基化合物和胺
3
(一) 硝基化合物
烃分子中的氢原子被硝基取代后生成的化合物 称硝基化合物。
15.1
硝基化合物的分类、命名和结构
脂肪族硝基化合物,如: CH 3 NO
2 2
按烃基不同 芳香族硝基化合物,如:
NO
硝基化合物可用通式 RNO2 或 ArNO2 表示。
+
R
CH
N
=
O
+
O R CH N R O CH
=N
O
+
O
=
O
具有α-H的伯或仲硝基化合物都存在上述互变异构现 象,所以它们都呈酸性. 例如: CH3NO2、CH3CH2NO2、(CH3)2CHNO2 pKa 10.2、 8.5、 7.8 叔硝基烷如 (CH3)3CNO2 无α - H,不溶于碱
硝基化合物和胺 14
催化氢化
CN CN
雷尼镍, H
2
NH2 NH2
C H 2N H 2 CH3
130℃,13.6MPa
LiAlH
4 还原
C N L iA lH 4 C H 3 乙醚
L iA lH 4 乙醚
88%
88%
O C N (C H 3 ) 2
C H2 N (C H 3 ) 2
含氮有机物中有硝基化合物、胺、腈、重氮化合物和偶 氮化合物以及氨基酸和蛋白质等。
本章主要讨论硝基化合物和胺类化合物。
硝基化合物和胺 2
学习要求
1. 掌握硝基化合物的制法、性质。理解硝基对 苯环邻对位取代基(X、OH)性质的影响。
2.掌握胺的分类、命名和制法。 3.掌握胺的性质及胺的碱性强弱次序,理解影响 胺的碱性强弱的因素。
第十五章 硝基化合物和胺 课后答案

第十五章硝基化合物和胺课后答案第十五章硝基化合物和胺课后答案第十五章硝基化合物和胺一、命名以下化合物:1.ch3ch2chch(ch3)2no22.ch3ch2ch2nh23.ch3nhch(ch3)22-甲基-3-硝基戊烷正丙胺甲基异丙基胺4.5.6.nhc2h5h2nnhc6h5(ch3)2chn+(ch3)3cl-ch33-甲基-n-乙基苯胺n-苯基对苯二胺氯化三甲基异丙基‘铵7.c6h5so2nhc6h58.brn+(ch3)3cl-n-乙基苯磺酰胺氯化三甲基对溴苯基铵9.(ch3)2nno10.ch2=chcnn.n-二甲基-4-亚硝基苯胺丙烯腈二、写下以下化合物的结构式:1,间硝基乙酰苯胺2,甲胺硫酸盐3,n-甲基-n-乙基苯胺nhcoch3[ch3nh2]2.h2so4ch3ch2nch34,对甲基苄胺5,1,6-己二胺6,异氰基甲烷ch2nh2nh2ch2ch2ch2ch2ch2ch2nh2ch3ncno2ch37,β-萘胺8,异氰酸苯酯nh2nco三、用化学方法区别下列各组化合物:1,乙醇,乙醛,乙酸和乙胺碳酸钠水溶液托伦试剂碘,氢氧化钠水溶液乙醇乙醛乙酸放出二氧化碳―乙胺不变不变不变不变银镜不变碘仿――不变2、邻甲苯胺n-甲基苯胺n,n-二甲基苯胺解:分别与亚硝酸钠+盐酸在低温反应,邻甲苯胺反应产物溶解,n-甲基苯胺生成黄色油状物,n,n-二甲基苯胺生成绿色固体。
3,乙胺和乙酰胺求解:乙胺溶盐酸,乙酰胺不水溶性。
4,环己烷与苯胺。
解:苯胺溶于盐酸,环己烷不溶。
四、试用化学方法分离下列化合物:1.ch3(ch2)3no2熔化,划出酸化(ch3)3cno2naohaq(ch3)3cno2hclch3ch2ch2nh2hcl 熔化,划出,然后碱ch3ch2ch2nh2溶液中和ch3(ch2)3no2ch3ch2ch2nh2.hclnaohaqch3ch2ch2nh22,苯酚,苯胺和对氨基苯甲酸求解:用氢氧化钠水溶液处置,苯酚和对氨基苯甲酸溶碱溶液,划出有机二者。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第十五章 硝基化合物和胺一、命名下列化合物:1.CH 3CH 2CHCH(CH 3)2NO 22.CH 3CH 2CH 2NH 23.CH 3NHCH(CH 3)24.NHC 2H 5CH 3H 2N NHC 6H 56.7.C 6H 5SO 2NHC 6H 58.BrN +(CH 3)3Cl -(CH 3)2CHN +(CH 3)3Cl -9.(CH 3)2NNO10.CH 2=CHCNN.N -二甲基-4-亚硝基苯胺 丙烯腈 二、写出下列化合物的构造式:1, 间硝基乙酰苯胺 2,甲胺硫酸盐 3,N -甲基-N -乙基苯胺NO 2NHCOCH 3[CH 3NH 2]2.H 2SO 4NCH 3CH 3CH 24,对甲基苄胺 5, 1,6-己二胺 6,异氰基甲烷CH 2NH 2CH 3NH 2CH 2CH 2CH 2CH 2CH 2CH 2NH 2CH 3NC7,β-萘胺 8,异氰酸苯酯NH 2NCO三、用化学方法区别下列各组化合物: 12、邻甲苯胺 N -甲基苯胺 N,N -二甲基苯胺解:分别与亚硝酸钠+盐酸在低温反应,邻甲苯胺 反应产物溶解, N -甲基苯胺生成黄色油状物,N,N -二甲基苯胺生成绿色固体。
3,乙胺和乙酰胺解:乙胺溶于盐酸,乙酰胺不溶。
4,环己烷与苯胺。
解:苯胺溶于盐酸,环己烷不溶。
四、试用化学方法分离下列化合物:1.CH 3(CH 2)3NO 2(CH 3)3CNO 2CH 3CH 2CH 2NH 2NaOHaq CH 3(CH 2)3NO 2(CH 3)3CNO 2CH 3CH 2CH 2HClCH 3CH 2CH 2NH 2.HClNaOHaqCH 3CH 2CH 2NH 22,苯酚,苯胺和对氨基苯甲酸解:用氢氧化钠水溶液处理,苯酚和对氨基苯甲酸溶于碱溶液,分出有机相。
有机相为含苯胺。
向水相通入二氧化碳,游离出苯酚,对氨基苯甲酸在水相中,酸化得到对氨基苯甲酸。
3,正己醇,2-己酮,三乙胺和正己胺解:加入亚硫酸氢钠饱和水溶液,2-己酮生成晶体分出,然后用稀酸处理这个晶体又得到2-己酮。
分理处2-己酮。
向正己醇,三乙胺和正己胺混合物中加入稀盐酸,正己醇不溶,分出。
三乙胺和正己胺溶在稀盐酸中,再用氢氧化钠水溶液中和,分出三乙胺,正己胺。
然后与乙酰氯反应,,正己胺发生酰基化反应,为固体,分出三乙胺。
然后水解酰基化产物,得到正己胺。
五、比较下列各组化合物的碱性,试按碱性强弱排列顺序:>NH2NH2NH2NO2CH2NH2>>>CH3NH2NHCH3NH2()3N>>>4.NH2NHCOCH3NH2NH2NHCOCH3NH2>> 5.NNHH六、完成下列反应式:1.CH 3CH 2CNH O +CH 3CH 2COOHSOCl CH 3CH 2COCl (CH CH CH )NHCH 3CH 2CON(CH 2CH 2CH 3)LiAlH (CH 3CH 2CH 2)3N2.N CH 3NCH 3CH 3H2CH 3I1,2,Ag 2O,H 2OCH 3+OH-CH 3NCH 3CH 31,CH 3I2,Ag 2O,H 2OCH 3NCH 3CH 3CH 3+-OHCH 2=CHC=CH 2CH 3+(CH 3)3N3,C N COO C N CON COK BrCH(COOC H )2CH(COOC 2H 5)21,NaOC 2H 52652CCOOC 2H 5COOC 2H 5CH 2C 6H 51,H 2O,-OH 2,HCOOHCOOH+H 2NC COOH CH 2C 6H 5HOOCCHCH 2C 6H 5NH 2七、完成下列转化:1.3CH 3CHCH 2NH 2CH 3CH 3CHCH 2CH 2OH 3CH 3CHCH 2CH 2[O]CH 3CHCH 2COOH CH 3SOCl CH 3CHCH 2COCl 3NH CH 3CHCH 2CONH 232NaOHCH 3CHCH 2NH 232.3CH 3CHCH 2CH 2OHCH 3CHCH 2CH 2NH 2CH 3CH 3CH 3CHCH 2CH 2OH NH 3CH 3CHCH 2CH 2NH 2CH 33.CH 3CHCH 2CH 2OHCH 3CHCH 2CH 2CH 2NH 233SOCl 2CH 3CHCH 2CH 2Cl CH 33CH 3CHCH 2CH 2OH SOCl 2CH 3CHCH 2CH 2Cl 3NaCNCH 3CHCH 2CH 2CN CH 32CH 3CHCH 2CH 2CH 2NH 2CH 34.CH 2=CH 2H 2NCH 2CH 2CH 2CH 2NH 2CH 2=CH 22BrCH 2CH 2Br 2NaCNNCCH 2CH 22H 2NCH 2CH 2CH 2CH 2NH 25.CH 2=CH 2CH 3CH 2CNCH 2=CH 2CH 3CH 2BrCH 3CH 2CN6.CH 3CH=CH 2CH 3CH COOH CH 2COOH CH 3CH=CH 2Br 2CH 3CHCH 2Br 2NaCNCH 3CHCH 2CN CN2+CH 3CH COOH CH 2COOH7.CH 3NO 2NH 2NO 2CH 3NO 2[O]NO 2COOHSOCl NO 2COClNO 22NH 3CONH八、以苯,甲苯以及三个碳原子以下的有机化合物为原料,合成下列化合物:1.COOHCH 3CH 3NO 2COOHNO 2NH 22HNO3H 2SO 4[O]2.NH 2NO 23H 2SO 4NO 2NO 2Na 2S NH2NO 23.NH 2NH 2HNO 3H 2SO 4NO 2NH 2Fe/HClH 2SO 4NH 2SO 3HNHCOCH 33HCH COClHNO H 2SO 4NHCOCH 3SO 3HNO 2HCl,H 2ONH 2NO2NH 2NH 2Fe/HCl4.NH 2NO 2O 2NCH3CH 332NH 4HSNH2NO 2O 2NCH 35.SO 2NHNO 2HNO H 2SO 4NO 22HSO 3ClSO 2ClNO 2NH2SO 2NHNO 2NO 2Fe/HClNH 26.NHNHNO 22Zn,NaOH/C 2H 5OHNHNH7.CH 3NHCH 2CH 3NH 2CH 3ClCH 2CH 3NHCH 2Cl 2,hvCH 2Cl8.2CH 2NH 2OCH 3CH 2CH 2NH 2CH 3OH332Cl ,hvOCH 3CH 2ClNaCNOCH 32CNNaBH OCH 39.CH 2N(CH 3)3+[]Br -CH 3NBSCH 2BrN(CH )CH 2N(CH 3)3+[10.CH 3CONH O NO2CH 33H 2SO 4CH 3NO2HOOC[O]3H 2SO 4NO 2NH 2CH 3COClNHCOCH 3NO 2HOOCSOCl2NO 2ClOC NHCOCH 3CH 3CONH O NO 2九、由对氯甲苯合成对氯间硝基苯甲酸,有三种可能的合成路线:1, 先硝化,再还原,然后氧化, 2, 先硝,再氧化,然后还原, 3, 先氧化,再硝化,再还原。
其中那种最好,为什么? 解:第三种路线最好。
CH 3COOHClHNO H 2SO 4COOHClNO 2Fe/HCl COOHNH 2另外两种合成路线得不到要求的产物。
十、写出下面反应历程:COOCH 3OCH 232ON C OCH 3COOCH 3OCH 23C N CH 2CH 3OH+O-CN CH 2CH 3O HOON C O 3十一、某碱性化合物A(C 4H 9N)经臭氧化分解,得到的产物中有一种是甲醛。
A 经催化加氢得到B(C 4H 11N),B 也可由戊酰胺和溴的氢氧化钠溶液反应得到。
A 和过量的碘甲烷作用,能生成盐C(C 7H 16IN)。
该盐和湿氧化銀反应,并加热分解得到D(C 4H 6)。
D 和丁炔二酸二甲酯加热反应得到E(C 10H 12O 4),E 在钯存在下,脱氢生成邻苯二甲酸二甲酯,试推测A,B,C,D,E 的结构,并写出各步反应式。
解: A,B,C,D,E 的结构及各步反应式如下:A:CH 2=CHCH 2CH 2NH 2B:CH 3CH 2CH 2CH 2NH 2CH 2=CHCH 2CH 2NH 21.32.Zn,H 2OCH 2O+OHCCH 2CH 2NH 2CH 2=CHCH 2CH 2NH 2H 2/Cat CH 3CH 2CH 2CH 2NH 2B:C 4H 11NCH 3CH 2CH 2CH 2CNH 2OBr ,NaOHCH 3CH 2CH 2CH 2NH 2CH 2=CHCH 2CH 2NH 2CH 3I3CH 2=CHCH 2CH 2N(CH 3)3I -C:C 7H 16NICH 2=CHCH 2CH 2N(CH 3)3I -CH 2=CHCH=CH 2D:C 4H 6CH 2=CHCH=CH 2+CH 3OOCC CCOOCH 3COOCH 3COOCH 3E:C 10H 12O 4COOCH 3COOCH 3H 2COOCH 3COOCH 3(完)。
