化学反应的热效应-习题及答案
化学反应的热力学与热效应练习题

化学反应的热力学与热效应练习题热力学是研究能量转化规律以及能量转化过程中所伴随的其他物理和化学性质变化的学科。
在化学反应中,热力学起着非常重要的作用,它可以帮助我们理解反应的方向、速率以及能量转化的方式。
本文为大家提供几道关于化学反应热力学与热效应的练习题,帮助大家巩固所学知识。
1. 根据下面的反应方程式写出反应的反热。
2. 计算下面反应的焓变值:2H2(g) + O2(g) → 2H2O(l)3. 结合下面的数据计算反应的焓变值:反应1: C(graphite) + 2H2(g) → CH4(g) ΔH1 = ?反应2: C(graphite) + 2H2(g) + O2(g) → CH3OH(l) ΔH2 = -726 kJ反应3: CO(g) + 2H2(g) → CH3OH(l) ΔH3 = -91 kJ反应4: CO2(g) + 2H2(g) → CH3OH(l) ΔH4 = -195 kJ反应5: CO2(g) + 4H2(g) → CH4(g) + 2H2O(l) ΔH5 = ?反应6: CH3OH(l) → CH4(g) + 1/2O2(g) ΔH6 = ?4. 结合下面的反应焓变值计算反应的焓变值:反应1: 2H2(g) + O2(g) → 2H2O(g) ΔH1 = -572 kJ反应2: H2(g) → H2(g) + 1/2O2(g) ΔH2 = -286 kJ反应3: 2H2(g) → 2H2(g) + O2(g) ΔH3 = ?5. 如下为反应方程式和各反应物和产物的焓变值,请根据热力学定律判断该反应是放热还是吸热反应。
反应:2H2(g) + O2(g) → 2H2O(g) ΔH = -484 kJ答案与解析:1. 例如:2H2(g) + O2(g) → 2H2O(l) 反热为 -483.6 kJ2. 反应的焓变值为ΔH = -484 kJ解析:根据化学方程式,反应物的摩尔数系数为2,产物的摩尔数系数为2,所以焓变值也是反应方程式右边各物质的摩尔数系数与它们的焓变之和。
化学反应的热效应 经典习题(含详解)

化学反应的热效应经典习题1.下列说法不正确的是()A.化学能可以转变成为热能、电能等B.化学反应必然伴随发生能量变化C.化学反应中的能量变化主要是由化学键的变化引起的D.化学反应中能量变化的多少与反应物的质量无关答案D解析化学反应的实质是旧化学键断裂、新化学键形成,一定伴随能量变化;化学变化过程中产生的能量可以转化为热能、电能等,且化学反应中,反应物的质量(或物质的量)的多少及物质的聚集状态,影响着反应中能量变化的多少。
2.根据如图所示的反应,判断下列说法中错误的是()A.CO2(g)和CaO(s)的总能量大于CaCO3(s)的总能量B.该反应的焓变大于零C.该反应中既有离子键断裂也有共价键断裂,化学键断裂吸收能量,化学键生成放出能量D.由该反应可推出凡是需要加热才发生的反应均为吸热反应答案D解析因为碳酸钙受热分解是吸热反应,所以CO2(g)和CaO(s)的总能量大于CaCO3(s)的总能量,焓变大于零,A、B两项均正确;在CaCO3中,Ca2+和CO2-3之间存在离子键,CO2-3中C 与O之间存在共价键,故反应中既有离子键断裂也有共价键断裂,断键吸收能量,成键放出能量,C项正确;需要加热才发生的反应不一定为吸热反应,如碳的燃烧反应就是放热反应,D项错误。
3.已知2H2(g)+CO(g)CH3OH(g)为放热反应,对该反应的下列说法正确的是() A.因该反应为放热反应,故不加热就可发生B.相同条件下,2 mol H2的能量或1 mol CO的能量一定高于1 mol CH3OH的能量C.相同条件下,反应物2 mol H2和1 mol CO的总能量一定高于生成物1 mol CH3OH的总能量D.达到平衡时,CO的浓度与CH3OH的浓度一定相等答案C解析A项,放热反应与反应条件无关,可能需要加热才发生,错误;B项,物质的能量与状态有关,由放热反应可知,相同条件下,2 mol H2(g)的能量与1 mol CO(g)的能量和一定高于1 mol CH3OH(g)的能量,错误;C项,反应物总能量大于生成物总能量时,为放热反应,则相同条件下,反应物2 mol H2和1 mol CO的总能量一定高于生成物1 mol CH3OH的总能量,正确;D项,平衡时,各物质的浓度不变,浓度是否相等与起始量、转化率有关,错误。
化学反应的热效应试题含解析

化学反应的热效应1.下列说法错误的是()A.化学反应中的能量变化都表现为热量变化B.需要加热才能发生的反应不一定是吸热反应C.向醋酸钠溶液中滴入酚酞试液,加热后若溶液红色加深,则说明盐类水解是吸热的D.反应物和生成物所具有的总能量决定了反应是放热还是吸热解析化学反应中的能量变化除了表现为热量变化外,还可以表现为电能和光能等。
答案 A2.已知化学反应A2(g)+B2(g)===2AB(g)的能量变化如图所示,判断下列叙述中正确的是()A.每生成2分子AB吸收b kJ热量B.该反应热ΔH=+(a-b)kJ·mol-1C.该反应中反应物的总能量高于生成物的总能量D.断裂1 mol A—A和1 mol B—B键,放出a kJ能量解析由图示可知生成物总能量高于反应物总能量,C错;1 molA2(g)与1 mol B2(g)反应生成2 mol AB(g)吸收(a-b)kJ热量,A错,B正确;化学键断裂吸收能量,D 错。
答案 B3.已知下列热化学方程式:①H2(g)+1/2O2(g)===H2O(g)ΔH1=a kJ·mol-1 ②2H2(g)+O2(g)===2H2O(g)ΔH2=b kJ·mol-1③H2(g)+1/2O2(g)===H2O(l)ΔH3=c kJ·mol-1 ④2H2(g)+O2(g)===2H2O(l)ΔH4=d kJ·mol-1下列关系式中正确的是()A.a<c<0B.b>d>0 C.2a=b<0 D.2c=d>0解析H2的燃烧反应都是放热反应,ΔH<0,a、b、c、d都小于0,B、D错;反应③与反应①相比较,产物的状态不同,H2O(g)转化为H2O(l)为放热反应,所以a>c,A错;反应②的化学计量数是①的2倍,反应热②也是①的2倍,b=2a<0,C对。
答案 C4.已知热化学方程式:2SO2(g)+O23(g)ΔH=-Q kJ·mol-1(Q>0)。
高考化学复习 化学反应中的热效应含答案及解析

化学反应中的热效应(时间:45分钟满分:100分)一、选择题(本题包括10小题,每小题6分,共60分,每小题只有一个选项符合题目要求)1.下列说法正确的是( ).A.需要加热才能发生的反应一定是吸热反应B.放热反应在常温下一定很容易发生C.吸热反应只有在加热条件下才能发生D.反应是吸热还是放热必须看反应物和生成物所具有的总能量的相对大小答案D解析反应在加热条件下进行,不一定是吸热反应,例如:Fe+S FeS属于加热条件下进行的放热反应,A错误;放热反应常温下不一定容易发生,如铝热反应,B错误;有些吸热反应不加热也能反应,如氢氧化钡晶体与氯化铵晶体常温下就能反应,C错误。
2.(2018·宁波十校第一次联考)已知:2H2(g)+O2(g)2H2O(g)ΔH1=-483.6 kJ·mol-12H2(g)+O2(g)2H2O(l) ΔH 2=-571.6 kJ·mol-1;据此判断,下列说法正确的是( )A.2H2O(l)2H2(g)+O2(g) ΔH3=+X kJ·mol-1,X小于571.6B.2 mol氢气和1 mol氧气的总能量大于2 mol液态水的能量C.1 mol H2O(l)转变成 1 mol H2O(g)放出 44.0 kJ 热量D.1 mol H2O(g)转变成 1 mol H2O(l)放出 88.0 kJ 热量答案B解析热化学反应方程式的正过程热效应的绝对值等于逆过程热效应的绝对值,即X为571.6,故A错误;氢气的燃烧是放热反应,反应物的总能量大于生成物的总能量,即2mol氢气和1mol氧气的总能量大于2mol液态水的能量,故B正确;给已知热化学方程式依次编号为①②,即①2H2(g)+O2(g)2H2O(g),②2H2(g)+O2(g)2H2O(l),由盖斯定律可知,(①-②)×得H2O(l)H2O(g)ΔH=×(571.6-483.6)kJ·mol-1=+44.0kJ·mol-1,即1molH2O(l)转变成1molH2O(g)吸收44.0kJ的热量,C错误;根据C选项的分析可知,1mol水蒸气转化成1mol液态水,放出的热量为44kJ,故D错误。
高考化学考点规范练15 化学反应的热效应(含答案)

考点规范练化学反应的热效应一、选择题1.下列说法正确的是()。
A.需要加热才能发生的反应一定是吸热反应B.任何放热反应在常温条件下一定能发生C.反应物和生成物所具有的总能量的相对大小决定了反应是放热还是吸热D.吸热反应只能在加热的条件下才能进行2.甲烷燃烧时的能量变化如图所示,下列有关说法正确的是()。
图1图2A.图1中反应为CH4(g)+2O2(g)CO2(g)+2H2O(l)ΔH=+890.3 kJ·mol-1B.图2中反应为CH4(g)+3O2(g)CO(g)+2H2O(g)ΔH=-607.3 kJ·mol-12O2(g)CO2(g)ΔH=-283 kJ·mol-1C.由图可以推得:CO(g)+12D.由图可以推知:等物质的量的CO2和CO,CO2具有的能量高3.(双选)工业上常利用CO2和NH3合成尿素[CO(NH2)2],该可逆反应分两步进行,整个过程中的能量变化如图所示。
下列说法错误的是()。
A.NH2COONH4为合成尿素反应的中间产物B.反应Ⅰ逆反应的活化能>反应Ⅱ正反应的活化能C.反应Ⅱ在热力学上进行趋势很大D.2NH3(g)+CO2(g)CO(NH2)2(l)+H2O(l)的焓变ΔH=E1-E24.(2021浙江衢州高三检测)下列关于ΔH的判断不正确的是()。
Si(s)+2Cl2(g)SiCl4(g)ΔH1Si(s)+2Br2(g)SiBr4(g)ΔH2Cu(OH)2(s)+2H+(aq)Cu2+(aq)+2H2O(l)ΔH32H2O(l)+Cu2+(aq)Cu(OH)2(s)+2H+(aq)ΔH4A.ΔH1<0,ΔH2<0B.ΔH1<ΔH2C.ΔH3<0,ΔH4>0D.ΔH3>ΔH45.肼(N2H4)在不同条件下的分解产物不同,200 ℃时在Cu表面分解的机理如图1所示。
已知200 ℃时,反应Ⅰ:3N2H4(g)N2(g)+4NH3(g)ΔH1=-32.9 kJ·mol-1,反应Ⅱ:N2H4(g)+H2(g)2NH3(g)ΔH2=-41.8 kJ·mol-1,下列说法不正确的是()。
1.1 化学反应中的热效应练习题及答案解析3套

1.1 化学反应中的热效应 第1课时 每课一练(苏教版选修4)基础达标1.在25 ℃、101 kPa 下,1 g 甲醇燃烧生成CO 2和液态水时放热22.68 kJ ,下列热化学方程式正确的是( )A.CH 3OH(l)+3/2O 2(g) ====CO 2(g)+2H 2O(l)ΔH=+725.8 kJ·mol -1B.2CH 3OH(l)+3O 2(g) ====2CO 2(g)+4H 2O(l)ΔH=-1 452 kJ·mol -1C.2CH 3OH (l )+3O 2(g )====2CO 2(g )+4H 2O (l )ΔH=-725.8 kJ·mol -1D.2CH 3OH(l)+3O 2(g) ====2CO 2(g)+4H 2O(l)ΔH=+1 452 kJ·mol -1解析:本题考查热化学方程式的计算及含义。
由1 g CH 3OH 放出热量为22.68 kJ 可知,1 molCH 3OH 即32 g 放出的热量为gmol g kJ 13268.221-∙⨯≈725.8 kJ·mol -1,因CH 3OH 燃烧为放热过程,故ΔH <0,A 、D 错误;又因热化学方程式中热量应与反应方程式中物质的计量系数相匹配,故B 中2 mol CH 3OH 放出热量为725.8×2 kJ,B 正确,C 错误。
答案:B2.航天飞机用铝粉与高氯酸铵(NH 4ClO 4)的混合物为固体燃料,点燃时铝粉氧化放热引发高氯酸铵反应,其方程式可表示为:2NH 4ClO 4△ N 2↑+4H 2O+Cl 2↑+2O 2↑ΔH <0。
下列对此反应的叙述中错误的是( )A.上述反应属于分解反应B.上述反应瞬间产生大量高温气体推动航天飞机飞行C.反应从能量变化上说,主要是化学能转变为热能和动能D.在反应中高氯酸铵只起氧化剂作用解析:在2NH 4ClO 4△ N 2↑+4H 2O+Cl 2↑+2O 2↑ ΔH <0中,高氯酸铵既是氧化剂又是还原剂。
人教版(2019)化学选择性必修1《化学反应的热效应》测试题(含答案)

7.下列说法中,错误的是 ( )
A.化学变化中的能量变化主要是由化学键变化引起的
B.化学反应中能量变化的大小与反应物的质量多少无关
C.化学反应必然伴随发生能量变化
D.能量变化是化学反应的基本特征之一
8.信使分子NO对人体生命活动有重要意义,在一定温度时可以发生反应2NO+O2 2NO2,如图是在其他条件相同时,分别在有、无催化剂时反应过程的能量变化。下列说法正确的是( )
12.下列关于反应能量的说法正确的是
A.若反应A=B△H<0,说明A物质比B物质稳定,分子内共价键键能A比B大
B.Zn(s)+CuSO4(aq)==ZnSO4(aq) +Cu(s);△H=-216kJ·mol-1。则反应物总能量>生成物总能量
C.101kPa时,2H2(g)+O2(g)==2H2O(g);△H=-QkJ·mol-1,则H2的燃烧热为1/2QkJ·mol-l
A.反应Ⅰ中各物质的化学计量数既可表示物质的量,又可表示分子个数
B.反应Ⅱ中S(s)和O2(g)的总能量低于SO2(g)的总能量
C.ΔH3的数值为-254
D.ΔH的数值大小与物质的状态无关
11.一定条件下,在水溶液中1molCl-、ClOx-(x=1,2,3,4)的能量(kJ)相对大小如图所示。下列有关说法正确的是()
B.需要加热的反应不一定是吸热反应
C.热化学方程式中化学计量数表示分子个数
D.1mol甲烷燃烧生成水和二氧化碳所放出的热量就是甲烷的燃烧热
4.物质A在一定条件下可发生一系列转化,由图判断下列关系错误的是()
A.A→F,ΔH=-ΔH6
B.ΔH1+ΔH2+ΔH3+ΔH4+ΔH5+ΔH6=1
高中化学选修一第一章《化学反应的热效应》测试卷(含答案解析)(19)

一、选择题1.(0分)[ID :138099]键能是化学键断开需吸收的能量或形成所放出的能量。
N 4在21世纪才被发现,跟你们的年龄差不多。
N 4是正四面体结构,有六个N-N 单键,N-N 键能为193kJ/mol ,而N 2有一个N N 键,键能为946kJ/mol 。
下列叙述正确的是A .2molN 2变成1molN 4需要吸收能量734kJB .2molN 2的总能量高于1molN 4的总能量C .N 4比N 2更稳定,因为N 4的键能更小D .如图所示,A 为N 4,B 为2N 22.(0分)[ID :138000]已知断裂1 mol 化学键所需的能量(kJ ):N≡N 为942、O=O 为500、N -N 为154,O -H 为452.5,则断裂1 mol N -H 所需的能量(kJ )是A .194B .316C .391D .658 3.(0分)[ID :138093]已知:反应2CuO/CuCl 20℃22404HCl+O 2Cl +2H O 中,4 mol HCl 被氧化,放出115.6 kJ 的热量。
则断开1 mol H-O 键与断开1 mol H-Cl 键所需能量相差A .31. 9 kJB .63.8 kJC .95.7 kJD .127.6 kJ4.(0分)[ID :138074]已知:2CO(g)+O 2(g)=2CO 2(g) ΔH=-566 kJ/molNa 2O 2(s)+CO 2(g)=Na 2CO 3(s)+12O 2(g) ΔH=-226 kJ/mol 根据以上热化学方程式判断,下列说法不正确的是A .CO 的燃烧热为283 kJ/molB .如图可表示由CO 生成CO 2的反应过程和能量关系C .2Na 2O 2(s)+2CO 2(s)=2Na 2CO 2(s)+O 2(g ) ΔH>-452 kJ/molD .CO(g)与Na 2O 2(s)反应放出509 kJ 热量时,电子转移数为2×6.02×1023 5.(0分)[ID :138066]工业上,在一定条件下利用乙烯和水蒸气反应制备乙醇。
高考化学专题复习-专题九化学反应的热效应-综合篇-模拟练习题(附答案)
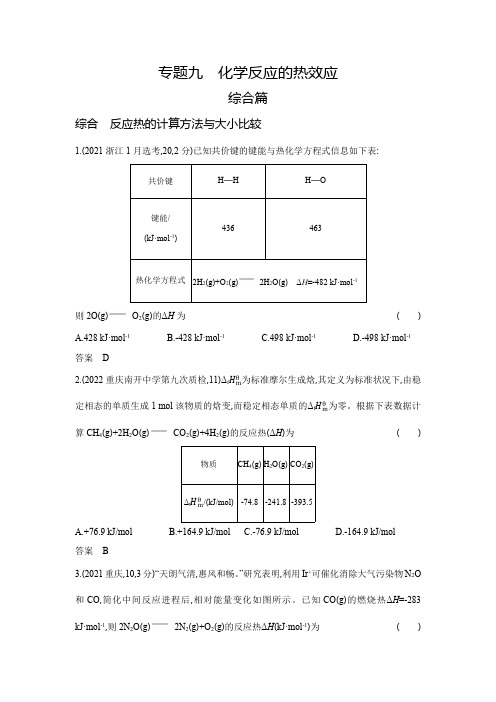
专题九化学反应的热效应综合篇综合反应热的计算方法与大小比较1.(2021浙江1月选考,20,2分)已知共价键的键能与热化学方程式信息如下表:共价键H—H H—O键能/436463(kJ·mol-1)热化学方程式2H2(g)+O2(g)2H2O(g)ΔH=-482kJ·mol-1则2O(g)O2(g)的ΔH为() A.428kJ·mol-1 B.-428kJ·mol-1 C.498kJ·mol-1 D.-498kJ·mol-1答案D2.(2022重庆南开中学第九次质检,11)Δf mθ为标准摩尔生成焓,其定义为标准状况下,由稳定相态的单质生成1mol该物质的焓变,而稳定相态单质的Δf mθ为零。
根据下表数据计算CH4(g)+2H2O(g)CO2(g)+4H2(g)的反应热(ΔH)为()物质CH4(g)H2O(g)CO2(g)Δf mθ/(kJ/mol)-74.8-241.8-393.5A.+76.9kJ/molB.+164.9kJ/molC.-76.9kJ/molD.-164.9kJ/mol答案B3.(2021重庆,10,3分)“天朗气清,惠风和畅。
”研究表明,利用Ir+可催化消除大气污染物N2O 和CO,简化中间反应进程后,相对能量变化如图所示。
已知CO(g)的燃烧热ΔH=-283 kJ·mol-1,则2N2O(g)2N2(g)+O2(g)的反应热ΔH(kJ·mol-1)为()A.-152B.-76C.+76D.+152答案A4.(2023届安徽江淮十校联考一,9)下列关于反应热的说法正确的是()A.a.A(g)+B(g)C(g)ΔH1;b.A(s)+B(g)C(g)ΔH2,若a、b反应均放热,则ΔH1<ΔH2B.已知2CH4(g)+4O2(g)2CO2(g)+4H2O(g)ΔH=-1780.6kJ·mol-1,则甲烷的燃烧热为890.3kJ·mol-1C.A4(s)4A(s)ΔH=-29.2kJ·mol-1,则常温下A4(s)比A(s)更稳定D.2X(g)+Y(g)3Z(g)ΔH>0,恒温恒压下达平衡后加入X,上述反应ΔH增大答案A5.(2019江苏单科,11,4分)氢气与氧气生成水的反应是氢能源应用的重要途径。
(常考题)人教版高中化学选修一第一章《化学反应的热效应》测试题(有答案解析)

一、选择题1.(0分)[ID:138013]下列热化学方程式正确的是(注:△H的绝对值均正确)A.C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(g)△H=-1367.0kJ/mol(燃烧热)B.NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)△H=-57.3kJ(中和热)C.S(s)+O2(g)=SO2(g)△H=-269.8kJ/mol(反应热)D.2NO2=O2+2NO△H=+116.2kJ/mol(反应热)2.(0分)[ID:138003]下列化学用语的表述正确的是()A.H+(aq)+OH-(aq)===H2O(l)ΔH=-a kJ·mol-1,故1 mol NaOH固体与足量的稀盐酸反应,放出热量大于a kJB.因CuSO4·5H2O(s)===CuSO4(s)+5H2O(l)ΔH=+b kJ·mol-1,故1 mol CuSO4(s)溶于水放出热量b kJC.氢气的燃烧热为c kJ·mol-1,电解水的热化学方程式为2H2O(l)===2H2(g)+O2(g)ΔH=+c kJ·mol-1D.因N2(g)+3H2(g)2NH3(g)ΔH=-d kJ·mol-1,故在某容器中通入1 mol N2与3 mol H2充分反应后,放出热量等于于d kJ3.(0分)[ID:138000]已知断裂1 mol化学键所需的能量(kJ):N≡N为942、O=O为500、N-N为154,O-H为452.5,则断裂1 mol N-H所需的能量(kJ)是A.194B.316C.391D.6584.(0分)[ID:138086]下列说法正确的是A.滴瓶中的滴管在加完药品后应将滴管洗净后再放回原瓶B.硝酸钾晶体的制备中,趁热过滤后加入2mL水的目的是避免NaCl冷却结晶,提高KNO3的纯度C.在中和热的测定实验中,为准确测得反应前后的温差,应将氢氧化钠溶液与盐酸在隔热的容器中混合测量混合液初始温度,然后迅速搅拌测量混合液的最高温度D.冬季时的乙酸常结成冰状固体,取用时可先将试剂瓶置于石棉网上用小火加热使乙酸熔化,再倾倒或用胶头滴管吸取5.(0分)[ID:138082]肼(H2NNH2)是一种高能燃料,有关化学反应的能量变化如图所示,已知断裂1mol化学键所需的能量(kJ):N≡N为942、N-H为391、O=O为500,则断裂1molN—N键所需的能量是 kJA.1327B.391C.516D.154 6.(0分)[ID:138079]氨气还原法可用于消除NO对环境的污染。
化学反应的热效应(习题)

化学反应的热效应(习题)1.下列有关化学反应与能量变化的说法中正确的是()A.物质发生化学反应都伴随着能量变化B.伴有能量变化的物质变化都是化学变化C.所有的化合反应都是放热反应D.所有的分解反应都是吸热反应2.下列关于焓变△H的说法正确的是()A.当反应放热时,△H>0;当反应吸热时,△H<0B.在一个化学反应中,当反应物总能量大于生成物总能量时,反应放热,△H<0C.同温同压下,H2(g)+Cl2(g)2HCl(g)在光照和点燃条件下的△H不同D.反应焓变是指1 mol物质参加反应时的能量变化3.已知:H2(g)+12O2(g)H2O(g) △H= -242.0 kJ•mol-1,氧气中1 mol O=O键完全断裂时吸收热量496 kJ,水蒸气中1 mol H-O键形成时放出热量463 kJ,则氢气中1 mol H-H键断裂时吸收热量()A.920 kJ B.188 kJ C.436 kJ D.922 kJ4.已知2SO2(g)+O2(g)2SO3(g)不正确的是()A.a代表旧化学键断裂时吸收的能量B.b代表反应热C.该反应为放热反应D.该反应△H>05.已知:C(s)+H2O(g)CO(g)+H2(g) △H= +131.3 kJ•mol-1,表示,在298K时()A.碳和水反应吸收131.3 kJ热量B.1 mol固态碳和1 mol液态水反应生成一氧化碳气体和氢气吸收131.3 kJ热量C.1 mol固态碳和1 mol水蒸气反应生成一氧化碳气体和氢气吸收131.3 kJ热量D.1个固态碳原子和1分子水蒸气反应吸收131.3 kJ热量6.下列热化学方程式书写正确的是()A.2NO2O2+2NO △H= +116.2 kJ•mol-1B.2H2(g)+O2(g)2H2O(l) △H= -571.6 kJ•mol-1C.S(s)+O2(g)SO2(g) △H= +269.8 kJ•mol-1D.3NO2(g)+H2O(l)2HNO3(aq)+NO(g) △H= -138 kJ7.写出298 K时,下列反应的热化学方程式。
第一章:化学反应的热效应强基习题-高二化学人教版(2019)选择性必修1

第一章:化学反应的热效应强基习题一、单选题(共12小题)1.氢气和氧气发生反应的过程用如下模型表示“-”表示化学键),下列说法正确的是A .过程I 是放热过程B .过程III 一定是吸热过程C .a 的总能量大于d 的总能量D .该反应的能量转化形式只能以热能的形式进行2.人体内葡萄糖的消耗可用下列热化学方程式表示:C 6H 12O 6(s)+6O 2(g)=6CO 2(g)+6H 2O(l) ΔH=-2800.6 kJ·mol -1;如果某人每天消耗12540 kJ 热量,则他每天至少要摄入葡萄糖的质量为 A .806 gB .1000 gC .1250 gD .1500 g3.肼(H 2NNH 2)是一种高能燃料,有关化学反应的能量变化如图所示。
已知断裂1 mol 化学键所需的能量(kJ):N≡N 为942、O=O 为500、N -H 为391,则形成1 mol N -N 所需的能量(kJ) 是A .194B .391C .154D .6584.相同温度和压强下,关于反应的ΔH ,下列判断正确的是(g)+H 2(g)→(g) 1ΔH (g)+2H 2(g)→(g) 2ΔH (g)+3H 2(g)→(g) 3ΔH(g)+ H 2(g)→(g) 4ΔHA .ΔH 1>0,ΔH 2>0B .ΔH 3=ΔH 1+ΔH 2C .ΔH 1>ΔH 2,ΔH 3>ΔH 2D .ΔH 2=ΔH 3+ΔH 45.下列热化学方程式或离子方程式中,正确的是A .0.01mol•L -1KAl(SO 4)2溶液与0.02mol•L -1Ba(OH)2溶液等体积混合Al 3++2SO 24-+2Ba 2++3OH -=2BaSO 4↓+Al(OH)3↓B .一定条件下,将0.5mol N 2(g)和1.5molH 2(g)置于密闭的容器中充分反应生成NH 3(g),放热19.3kJ ,热化学方程式为:N 2(g)+3H 2(g)⇌2NH 3(g) ∆H=-38.6kJ/molC .2H 2(g)+O 2(g)=2H 2O(g) ∆H=-571.6 kJ•mol -1,则H 2的燃烧热为285.8 kJ/molD .CO(g)的燃烧热是283.0 kJ•mol -1,则CO 2分解的热化学方程式为:2CO 2(g)=2CO(g)+O 2(g) ∆H=+566.0 kJ/mol 6.叔丁基溴在稀的碱性水溶液中水解生成叔丁醇的反应分三步进行,反应中每一步的能量变化曲线如图所示,下列有关说法不正确的是A .叔丁基溴在稀的碱性水溶液中生成叔丁醇的反应是放热反应B .()+33CH C 和()+323C C O H -H 为反应活性中间体C .决定叔丁基溴水解生成叔丁醇反应的速率的是第二步反应D .第三步反应为()()+-32333CH C-H +Br CH C-OH+HBr O → 7.依据图示关系,下列说法不正确...的是A .54ΔH >ΔHB .石墨的稳定性比金刚石高C .C(石墨,s)2+CO (g)=2CO(g) 32ΔH=ΔH -ΔHD .1mol 石墨或1molCO 分别完全燃烧,石墨放出热量多8.我们把能够发生化学反应的碰撞叫做有效碰撞;发生有效碰撞的分子必须具有足够的能量,这种分子叫做活化分子;活化分子具有的平均能量与反应物分子具有的平均能量之差,叫做反应的活化能。
化学反应中的热效应经典习题(含解析)

7、(2014•九江二模)有关热化学方程式书写与对应表述均正确的是( )
A.稀硫酸与0.1 mol/LNaOH溶液反应:H+(aq)+OH-(aq)=H2O(l)△H=-57.3 kJ•mol-1
B.在101KPa下氢气的燃烧热△H=-285.5 kJ•mol-1,则水分解的热化学方程式:2H2O(l)=2H2(g)+O2(g)△H=+285.5 kJ•mol-1
(5)PCl5+4H2O=H3PO4+5HCl
D.寻找特殊化学物质,用于开发廉价能源,以分解水制取氢气
2、综合题
1、用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题:
(1)从实验装置上看,图中尚缺少的一种玻璃仪器是。
(2)烧杯间填满碎纸条的作用是。
2、红磷P(s)和Cl2(g)发生反应生成PCl3(g)和PCl5(g)。反应过程和能量关系如图所示(图中的△H表示生成1mol产物的数据)。
根据右图回答下列问题:
(1)P和Cl2反应生成PCl3的热化学方程式__________________________________。
(2)PCl5分解成PCl3和Cl2的热化学方程式_________________________________,上述分解反应是一个可逆反应,温度T1时,在密闭容器中加入0.80molPCl5,反应达到平衡时PCl5还剩0.60mol,其分解率α1等于___________;若反应温度由T1升高到T2,平衡时PCl5的分解率为α2,α2_____α1(填“大于”、“小于”或“等于”)。
高考化学总复习《化学反应的热效应》专项练习题及答案解析

高考化学总复习《化学反应的热效应》专项练习题及答案解析学校:___________班级:___________姓名:___________考号:___________一、单选题1.(2023春·辽宁沈阳·高三沈阳市第八十三中学校联考期中)下列说法正确的是 A .反应()()()34NH g HCl g NH Cl s +=在低温下能自发进行,说明该反应的Δ<0HB .2H 的热值(单位质量的燃料完全燃烧时所放出的热量,叫做燃料的热值)为1142.9kJ g -⋅,则氢气燃烧的热化学方程式可表示为:()()()2222H g O g 2H O l += 1Δ=285.8kJ mol H --⋅C .能自发进行的反应一定能迅速发生D .增大反应物浓度,可增大活化分子百分数,从而增加有效碰撞的次数2.(2023春·河南新乡·高三延津县第一高级中学校考期中)下列反应既属于氧化还原反应又属于吸热反应的是A .3NaHCO 与盐酸反应B .Na 与水反应C .22Ba(OH)8H O ⋅与4NH Cl 反应D .C 与2CO 反应3.(2023春·四川南充·高三校考期中)已知H 2O 2(aq)分解为H 2O(l)和O 2(g)的能量变化如图曲线A 所示,若在H 2O 2溶液中加入少量KI ,则H 2O 2的分解过程可表示为:①H 2O 2+I -=H 2O+IO -,①H 2O 2+IO -=H 2O+O 2+I -,其能量变化如图曲线B 所示。
下列有关说法不正确...的是A .上述反应①为吸热反应,反应①为放热反应B .2molH 2O 2(aq)具有的能量大于2molH 2O(l)和1molO 2(g)具有的总能量C .I -在H 2O 2分解过程中起到催化剂作用D .催化剂不参与化学反应,反应前后性质、质量不变4.(2023春·福建宁德·高三校联考期中)反应NO 2(g) +CO(g)NO(g) +CO 2 (g)的能量变化如图所示,下A .H(g)和O(g)形成H 2O(g)的过程要吸收能量B .等质量的H 2O(1)与H 2O(g)具有相同的能量C .2H 2(g)+O 2(g)=2H 2O(g)的能量关系可用上图表示D .在H 2(g)和O 2(g)的反应过程中,断开化学键吸收的总能量大于形成化学键释放的总能量7.(2023·全国·高三统考专题练习)工业上可以利用水煤气(2H 、CO )合成二甲醚(33CH OCH ),同时生成2CO 。
人教版初中高中化学选修一第一章《化学反应的热效应》经典练习题(含答案解析)

一、选择题1.下图为N2分子在催化剂作用下发生一系列转化的示意图,下列叙述正确的是()A.若N≡N键能是a kJ·mol-1,H—H键能是b kJ·mol-1,H—N键能是c kJ·mol-1,则每生成2 mol NH3,放出(6c-a-3b)kJ热量B.NH3分子和H2O分子的中心原子杂化类型不同C.催化剂a、b表面均发生了极性共价键的断裂D.在催化剂b作用下发生转化得到的两种生成物,均为直线形分子答案:A【详解】A.反应热就是断键吸收的能量和形成化学键所放出的能量的差值,则根据键能数据可知,该反应的反应热△H=akJ/mol+3bkJ/mol-2×3ckJ/mol,则每生成2 mol NH3,放出(6c-a-3b)kJ热量,选项A正确;B.水分子中价电子数=2+12(6-2×1)=4,水分子中含有2个孤电子对,所以氧原子采取sp3杂化,氨气中价层电子对个数=3+12(5-3×1)=4且含有1个孤电子对,所以N原子采用sp3杂化,杂化方式相同,选项B错误;C.催化剂a表面是氢气氮气反应生成氨气,催化剂a表面发生了非极性键(氢氢键和氮氮键)的断裂,催化剂b表面发生了非极性共价键(氧氧双键)的断裂,选项C错误;D.在催化剂b作用下发生转化得到的两种生成物H2O和NO,NO为直线形分子,H2O为V形分子,选项D错误;答案选A。
2.断裂1mol化学键所需的能量如表,火箭燃料肼(H2N—NH2)的有关化学反应的能量变化如图所示,则下列说法错误的是化学键N—N O=O N≡N N—H键能(kJ)154500942aA.N2(g)比O2(g)稳定B.N2H4(g)+O2(g)=N2(g)+2H2O(g)ΔH1=-534kJ·mol-1C.图中的ΔH3=+2218kJ·mol-1D.表中的a=194答案:D【详解】A.化学键的断裂要吸收能量,N≡N键能942kJ,O=O键能500kJ,所以N≡N键能大,破坏需吸收更多的能量,相对于破坏氧气中O=O难,N2(g)比O2(g)稳定,故A正确;B.根据图中内容,可以看出N2H4(g)+O2(g)=N2(g)+2H2O(g)ΔH1=-534kJ·mol-1,故B正确;C.根据图中内容,可以看出N2H4(g)+O2(g)=2N(g)+4H(g)+2O(g),△H3=△H1−△H2=−534kJ/mol-(-2752kJ/mol)=+2218kJ/mol,故C正确;D.根据图中内容,可以看出N2H4(g)+O2(g)=2N(g)+4H(g)+2O(g),△H3=−534kJ/mol-(-2752kJ/mol)=2218kJ/mol,化学反应的焓变等于产物的能量与反应物能量的差值,旧键断裂吸收能量,新键生成释放能量,设断裂1molN−H键所需的能量为akJ/mol,旧键断裂吸收的能量:154kJ/mol+4akJ/mol+500kJ/mol=2218kJ/mol,解得a=391,故D错误;答案选:D。
高中化学:化学反应的热效应测试题(含答案)

19.(1)运动会中的火炬一般采用丙烷(C3H8)为燃料。丙烷热值较高,污染较小,是一种优良的燃料。丙烷(C3H8)的燃烧热ΔH1=-2215kJ/mol;二甲醚(CH3OCH3)是一种新型燃料,应用前景广阔。1mol二甲醚完全燃烧生成CO2和液态水放出1455kJ热量。若mol丙烷和二甲醚的混合气体完全燃烧生成CO2和液态水共放出1645kJ热量,则混合气体中,丙烷和二甲醚的物质的量之比为________。
D.图l所示过程①是放热反应
10.为探究NaHCO3、Na2CO3与1 mol/L盐酸反应(设两反应分别是反应Ⅰ、反应Ⅱ)过程中的热效应,进行实验并测得如下数据:
序号
液体
固体
混合前温度
混合后最高温度
①
35mL水
2.5g NaHCO3
20℃
18.5℃
②
35mL水
3.2g Na2CO3
20℃
24.3℃
③
5.含有8gNaOH的稀溶液与1L0.1mol·L−1的H2SO4溶液反应,放出 的热量。下列说法正确的是
A.弱酸与弱碱反应也可以准确测出中和热
B.有水生成的反应都为放热反应
C.用8g固体NaOH与1L0.1mol·L−1的H2SO4溶液反应,放出的热量一样
D.中和热的热化学方程式为 kJ·mol−1
A.反应HCO (aq)+H+(aq)=CO2(g)+H2O(l)为放热反应
B.CO (aq)+2H+(aq)=CO2(g)+H2O(l)∆H=(∆H1+∆H2+∆H3)
完整版反应热练习题及答案

化学反应与热效应练习题1个正确答案)一、选择题(每题只有)(1、今有如下三个热化学方程式:a kJ/mol (g)+1/2O(g)=HO(g);△H=H222b kJ/mol =(g)+1/2O(g)=HO(l);△HH222c kJ/mol (g)(g)+O=2HO(l);△H=2H222关于它们的下列表述,正确的是B. a、b和c均为正值 A. 它们都是吸热反应cD. 反应热的关系:2b= C. 反应热的关系:a=b,下列说法正确的是F2、已知:H(g)+(g)错误!未找到引用源。
2HF(g)+270kJ22 ) (热量的氟气吸收270kJ氟化氢气体分解成1L的氢气和1LA.2L270kJ 2mol液态氟化氢放出的热量小于1mol氢气与1mol氟气反应生成B.氟化氢气体氟气的能量总和大于2mol.在相同条件下,1mol氢气与1molC 的能量270kJ2个氟化氢分子放出1个氢气分子与1个氟气分子反应生成D.。
已知断裂下列化学键需要吸收的OP3、白磷与氧可发生如下反应:+5O=P102441——1—1 O=O 、P —O bkJ·mol akJ·molmol、、P=O ckJ·能量分别为:P—P1—mol。
dkJ·△)根据图示的分子结构和有关数据估算该反应的H,其中正确的是(1——1 mol B(4c+12b-6a-5d)A.(6a+5d-4c-12b)kJ·molkJ·1—1 —4cD.(4a+5d--12b)kJ·mol.(C4c+12b-4a-5d)kJ·mol-1、mol、CH(g)和CHOH(1)的燃烧热分别是-285.8kJ·4、已知H(g)52242-1-1OH(l)H,则由CH(g)和HO(l)-1411.0kJ·mol反应生成和-1366.8kJ·molC54222)( 的△H为-1-1 mloB.+44.2kJA.-44.2kJ·mol·-1-1mloD.+330kJC.-330kJ·mol·图所示,该反应的热化学方程式13+3H=2NH的能量变化如题5、化学反应N322 ( ) 是-1 mol△H=2(a-b-c)kJ·(g)=2NHA.N(g)+3H(1); 322-1 mol·(g)+3HB.N(g)=2NH(g); △H=2(b-a)kJ32231-1 mol△(1); H=(b+c-a)kJ.·N(g)+H(g)=NHC3222213-1 mol=(a+b)kJ·H(g)+NH(g)=NH(g); △D.32222) ( 、下列关于热化学反应的描述中正确的是6.反和Ca(OH)57.3kJ/mol,则HSOA.HCl和NaOH反映的中和热△H=-22457.3)kJ/mol(-H=2×映的中和热△2CO(g)!未找到引用源。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
.
第一节 化学反应的热效应训练案
班级: 姓名:
1、下列说法正确的是 ( ) A .物质发生化学变化都伴随着能量变化 B .任何反应中的能量变化都表现为热量变化 C .伴有能量变化的物质变化都是化学变化 D .没有物质的变化,不可能有能量的变化
2、下列反应中生成物总能量高于反应物总能量的是 ( )
A .碳酸钙受热分解
B .乙醇燃烧
C .铝粉与氧化铁粉末反
D .氧化钙溶于水
3、下列反应是放热反应,但不是氧化还原反应的是 ( )
A 、铝片与稀硫酸的反应
B 、氢氧化钡与硫酸的反应
C 、灼热的炭与二氧化碳的反应
D 、甲烷在氧气中燃烧 4、下列各组热化学方程式中,△H 1>△H 2的是 ( )
①、C(s)+O 2(g)===CO 2(g) △H 1 C(s)+1
2
O 2(g)===CO(g) △H 2
②、S(s)+O 2(g)===SO 2(g) △H 1 S(g)+O 2(g)===SO 2(g) △H 2 ③、H 2(g)+1
2
O 2(g)===H 2O(l) △H 1
2H 2(g)+O 2(g)===2H 2O(l) △H 2 ④、CaCO 3(s)===CaO(s)+CO 2(g) △H 1 CaO(s)+H 2O(l)===Ca(OH)2(s) △H 2 A .① B .④ C .②③④ D .①②③ 5、已知H 2(g)+Cl 2(g)=2HCl(g) △H=―184.6kJ·mol -1,则反应HCl(g)=1/2H 2(g)+1/2Cl 2(g)的△H 为( ) A .+184.6kJ·mol -1 B. ―92.3kJ·mol -1 C. ―369.2kJ·mol -1 D. +92.3kJ·mol -1 6、根据以下3个热化学方程式: 2H 2S(g)+3O 2(g)=2SO 2(g)+2H 2O(l) △H =―Q 1 kJ/mol 2H 2S(g)+O 2(g)=2S (s)+2H 2O(l) △H =―Q 2 kJ/mol 2H 2S(g)+O 2(g)=2S (s)+2H 2O(g) △H =―Q 3 kJ/mol 判断Q 1、Q 2、Q 3三者关系正确的是 ( ) A. Q 1>Q 2>Q 3 B. Q 1>Q 3>Q 2 C. Q 3>Q 2>Q 1 D. Q 2>Q 1>Q 3 7、沼气是一种能源,它的主要成分是CH 4,0.5mol CH 4完全燃烧生成CO 2和液态水时放出445kJ 的热量,则下列热化学方程式中正确的是 ( ) A 、CH 4(g)+2O 2(g) CO 2(g)+2H 2O(g); △H=—890kJ ·mol -1 B 、CH 4(g)+2O 2(g) CO 2(g)+2H 2O(l); △H=—890kJ ·mol -1 C 、CH 4(g)+2O 2(g) CO 2(g)+2H 2O(l) △H=890kJ ·mol -1 D 、1/2CH 4(g)+O 2(g) 1/2CO 2(g)+H 2O(l) △H=890kJ ·mol -1 8、已知25℃、101kPa 下,石墨、金刚石燃烧的热化学方程式分别为
C(石墨)+O 2(g)=CO 2(g) △H =-393.51kJ ·mol -1 C(金刚石)+O 2(g)=CO 2(g) △H =-395.41kJ ·mol -1
据此判断,下列说法中正确的是 ( ) A 、由石墨制备金刚石是放热反应;石墨比金刚石稳定 B 、由石墨制备金刚石是吸热反应;金刚石比石墨稳定 C 、由石墨制备金刚石是吸热反应;石墨比金刚石稳定 D 、由石墨制备金刚石是放热反应;金刚石比石墨稳定 9、火箭推进器中盛有强还原剂液态肼(N 2H 4)和强氧化剂液态双氧水。
当把0.4mol 液态肼和0.8mol H 2O 2
混合反应,生成氮气和水蒸气,放出256.7kJ 的热量(相当于25℃、101 kPa 下测得的热量)。
(1)、反应的热化学方程式为 。
(2)、又已知H 2O(l) = H 2O(g) ΔH= +44kJ/mol 。
则16g 液态肼与液态双氧水反应生成液态水时放
出的热量是 kJ 。
(3)、此反应用于火箭推进,除释放大量热和快速产生大量气体外,还有一个很大的优点是 。
10、中和热测定实验的关键是要比较准确地配制一定的物质的量浓度的溶液,量热器要尽量做到绝热,
在量热的过程中要尽量避免热量的散失,要求比较准确地测量出反应前后溶液温度的变化。
(1)、中学化学实验中的中和热的测定所需的玻璃仪器有 (2)、该实验常用0.50mol ·L -1 HCl 和0.55mol ·L -1的NaOH 溶液各50mL 。
NaOH 的浓度大于HCl 的
浓度作用是 。
11、已知:Zn (s )+S (斜方)=ZnS (s );△H 1=-206.0kJ/mol ZnS (s )+2 O 2=ZnS O 4(s);△H 2=-776.8kJ/mol 试求由单质反应生成ZnS O 4(s)的反应热,即 Zn (s )+S (斜方)+2 O 2=ZnS O 4(s)的△H= 。
12、已知 Sn (s ) + Cl 2 (g ) = SnCl 2 (s ) △H = -349.8 kJ.mol-1
SnCl 2(s) + Cl 2(g) = SnCl 4 (l ) △H = -195.4 kJ.mol-1 Sn(s )+ 2Cl 2(g ) = SnCl 4(l ) 的反应热△H 为 13、如图所示,把试管放入盛有25℃时饱和石灰水的烧杯中,试管中开始放入几小块镁片,再滴入5mL 盐酸,试回答下列问题。
(1)实验中观察到的现象是 (2)产生上述现象的原因是 (3)写出有关反应的离子方程式
.
(4)由实验推知,2MgCl 溶液和2H 的总能量___________ (填“大于”、“小于”或“等于”)镁片和盐酸的总能量。
第一节 化学反应的热效应训练案 答 案
1、A 2 A 3 B 4 C 5 D 6 A 7 B 8 C
9 (1)、N 2H 4(l )+ 2H 2O 2(l ) == N 2(g )+ 4H 2O (g )
△H 2 = — 641.75kJ•mol —1 (2)、 408.9 (3)、无污染 10、(1) 烧杯 温度计 量筒 (2)使反应进行的充分 11、— 982.8 kJ•mol —1 12、 — 545.2 kJ•mol —1 13、(1)、试管中有气泡产生 烧杯中石灰水变浑浊 (2)、Mg +2 HCl == Mg Cl 2 + H 2 ↑, 反应放热
Ca(OH)2 的溶解度随温度升高而降低 (3)、Mg +2 H + == Mg 2+ + H 2 ↑ (4)、小于
如有侵权请联系告知删除,感谢你们的配合!。
