生物化学王镜岩第三版ppt课件
合集下载
生物化学王镜岩三磷酸戊糖途径课件完整版

又称2-酮-3C-脱H氧2-O6-磷P酸O葡3糖H酸2(KDPG)裂C解H途O径。
3-phosphate
H
C
OH
5-磷酸核酮糖 与植物光合作用有关-C3,C4
(有氧时经过呼吸链) (无氧时H进行细菌C乙醇发酵O)H 利ri用b脂u肪lo合s成e糖5(-油p料h植os物p种h子at萌e发)。
2)、是谷胱甘肽还原酶的辅酶 H
CH2OH CO HO C H
磷酸戊糖途径的非氧化阶段之三
(3-磷酸甘油醛异构、缩合与水解)
3-磷酸甘油醛
异 构 酶
醛缩酶
H2O Pi 二磷酸果糖酯酶
1,6-二 磷酸果糖
6-磷酸葡萄糖的生成
6-磷酸果糖
P
P
P
磷酸戊糖途径的非氧化分子重排阶段
阶
6 5-磷酸核酮糖
段
之
异构酶
一
2 5-磷酸木酮糖
2 5-磷酸核糖
5-磷酸核糖作用
各种核苷酸辅酶
核苷酸
(1)NAD(P)+合
(2)FAD (3)HSCoA
成 原 料
} (1) NTP
(2)dNTP DNA、RNA合成原料 (3)cAMP/cGMP
第二信使
NADPH的主要功能
1)、作为供氢体 ---参与体内多种生物合成反应
2)、是谷胱甘肽还原酶的辅酶 ---对维持细胞中还原型谷胱甘肽的正常含量
ROH+NADP++
H2O
羟化酶
蚕豆病 :
蚕豆病,俗称蚕豆黄
蚕豆病的症状是: 吃蚕豆几小时或1~2天后,突 然感到精神疲倦、头晕、恶心、畏寒发热、全身酸痛、 萎靡不振,并伴有黄疸、肝脾肿大、呼吸困难、肾功 能衰竭,甚至死亡。
3-phosphate
H
C
OH
5-磷酸核酮糖 与植物光合作用有关-C3,C4
(有氧时经过呼吸链) (无氧时H进行细菌C乙醇发酵O)H 利ri用b脂u肪lo合s成e糖5(-油p料h植os物p种h子at萌e发)。
2)、是谷胱甘肽还原酶的辅酶 H
CH2OH CO HO C H
磷酸戊糖途径的非氧化阶段之三
(3-磷酸甘油醛异构、缩合与水解)
3-磷酸甘油醛
异 构 酶
醛缩酶
H2O Pi 二磷酸果糖酯酶
1,6-二 磷酸果糖
6-磷酸葡萄糖的生成
6-磷酸果糖
P
P
P
磷酸戊糖途径的非氧化分子重排阶段
阶
6 5-磷酸核酮糖
段
之
异构酶
一
2 5-磷酸木酮糖
2 5-磷酸核糖
5-磷酸核糖作用
各种核苷酸辅酶
核苷酸
(1)NAD(P)+合
(2)FAD (3)HSCoA
成 原 料
} (1) NTP
(2)dNTP DNA、RNA合成原料 (3)cAMP/cGMP
第二信使
NADPH的主要功能
1)、作为供氢体 ---参与体内多种生物合成反应
2)、是谷胱甘肽还原酶的辅酶 ---对维持细胞中还原型谷胱甘肽的正常含量
ROH+NADP++
H2O
羟化酶
蚕豆病 :
蚕豆病,俗称蚕豆黄
蚕豆病的症状是: 吃蚕豆几小时或1~2天后,突 然感到精神疲倦、头晕、恶心、畏寒发热、全身酸痛、 萎靡不振,并伴有黄疸、肝脾肿大、呼吸困难、肾功 能衰竭,甚至死亡。
王镜岩生化第三版课件 糖代谢共104页文档

1、最灵繁的人也看不见自己的背脊。——非洲 2、最困难的事情就是认识自己。——希腊 3、有勇气承担命运这才是英雄好汉。——黑塞 4、与肝胆人共事,无字句处读书。——周恩来 5、阅读使人充实,会谈使人敏捷,写作使人精确。——培根
王镜岩生化第三版课件 糖代谢
21、没有人陪你走一辈子,所以你要 适应孤 独,没 有人会 帮你一 辈子, 所以你 要奋斗 一生。 22、当眼泪流尽的时候,留下的应该 是坚强 。 23、要改变命运,首先改变自己。
24、勇气很有理由被当作人类德性之 首,因 为这种 德性保 证了所 有其余 的德性 。--温 斯顿. 丘吉尔 。 25、子的梯阶从来不是用来搁脚的 ,它只 是让人 们的脚 放上一 段时间 ,以便 让别一 只脚能 够再往 上登。
生物化学王镜岩第三第六章蛋白质的高级结构 课件(共54张PPT)

弹性蛋白:存在于结缔组织
纤维状蛋白质
不溶性〔硬 蛋白〕
角蛋白
α角蛋白:主要存在于毛发中
β角蛋白:天然存在于丝中,丝 心蛋白
胶原蛋白:结缔组织中〔骨、皮肤等〕大量存 在
可溶性蛋 白
肌球蛋白
血纤蛋白原
其它
说明: α角蛋白经充分伸展后可转变成β角蛋白,即β折叠片结构。
(4) 无规那么卷曲〔nonregular coil〕 蛋白质的空间结构:二级结构单元〔 -螺旋、 -折叠、 -转角、自由回转〕、三级与四级结构〔超二级结构、结构域、亚基〕及结构与功 能的关系 特征:两条或多条伸展的多肽链〔或一条多肽链的假设干肽段〕侧向集聚,通过相邻肽链主链上的N-H与C=O之间有规那么的氢键,形成锯齿 状片层结构,即β-折叠片。 70年代,提倡Vitamin C治百病 2 、 螺旋体中所有氨基酸残基R侧链都伸向外侧,链中的全部>C=0 和>N-H几乎都平行于螺旋轴;
4. 蛋白质的超二级结构
(1)超二级结构〔 supersecondary structure 〕 蛋白质中相邻的二级结构单位〔即单个α-螺
旋或β-折叠或β-转角〕组合在一起,形成有规 那么的、在空间上能辩认的二级结构组合体称为蛋 白质的超二级结构
根本组合方式:αα;β×β;βββ
超二级结构类型
αα
Β-链
β×β
βαβ
1 2ββ--迂迂回3 回4 5
βββ
回形拓扑结构
5 2回形3 拓扑4 结1构
丙糖磷酸异构酶
乳酸脱氢酶结构域1
黄素蛋白
丙酮酸激酶结构域4
羧肽酶
腺苷酸激酶
(a)
()
平行 -折叠的结构比较〔a〕 -园桶形排布,〔b〕马蹄形排布
生物化学王镜岩第三版第31章--氨基酸的生物合成PPT课件
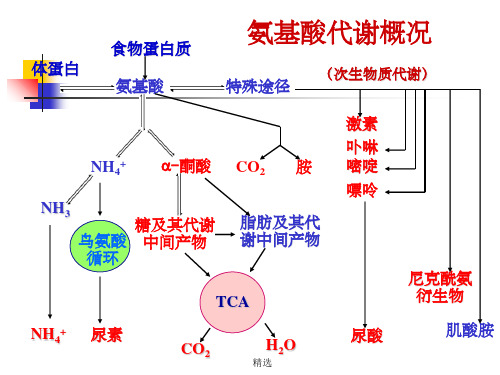
氨
NAD(P)H+H+ NAD(P)+
谷氨酸脱氢酶
α-酮戊二酸
精选
COO│ H3N— C—H │ CH2 │ CH2 │ COO-
谷氨酸
谷氨酸脱氢酶途径
COOH
CH2 CH2 + NH3
L-谷氨酸脱氢酶
C=O COOH
NAD(P)H+H+ NAD(P)+
α-酮戊二酸
(TCA循环产生的)
COOH
CH2
谷氨酸族
精选
柠檬酸循环
氨基酸的分族
α-酮戊二酸 谷氨酸
草酰乙酸 天冬氨酸
谷氨酰胺 脯氨酸 精氨酸
(谷氨酸族)
天冬酰胺 甲硫氨酸 赖氨酸 苏氨酸
(天冬氨酸族)
精选
糖酵解
甘油酸-3-磷酸
丝氨酸
半胱氨酸
甘氨酸
(丝氨酸族)
丙酮酸
丙氨酸 缬氨酸 亮氨酸
(丙酮酸族)
精选
糖酵解
戊糖磷酸途径
磷酸烯醇式丙酮酸 赤藓糖-4-磷酸
CH2
+ H2O
CH NH2
COOH
谷氨酸
这是异养真核生物(如真菌)的氨同化的主要 途径,要求[NH3]高。
精选
3、谷氨酸酰胺化为谷氨酰胺
由谷氨酸与氨再生成谷氨酰胺,合成谷氨酰胺要消耗ATP. 也能把氨转变为有机物。
COO│ H3N— C—H │ CH2 │ CH2 │ COO-
谷氨酸
COO-
│
+ NH4+
ATP ADP+Pi 谷氨酰胺合成酶
H3N— C—H │ CH2 │
CH2
│
C=O
(推荐)《王镜岩生物化学》PPT课件

平面偏振光
如果让光通过一个象栅栏一样的 Nicol 棱镜 (起偏镜) 就不是所有方向的光都能通过,而只有与棱镜晶轴方向 平行的光才能通过。这样,透过棱晶的光就只能在一个 方向上振动,象这种只在一个平面上振动的光,称为平
12
面偏振光,简称偏振光或偏光。
生物化学.第一篇 .生物分子的结构和化学
第一章 生物分子导论
细胞器(organelle)(细胞核、线粒体,高尔基体等)
6
细胞(原核细胞,真核细胞等)
生物化学.第一篇 .生物分子的结构和化学
第一章 生物分子导论
三.生物分子的三维结构
1.生物分子大小:生物分子不仅种类繁多,在大小方面跨度也很大,例如,丙 氨酸分子量是89,但烟草花叶病毒达到40000000.
2.立体异构与构型
故:分子的手性是对映体存在的必要和充分条件。
19
§3—4— 3 含一个手性碳原子化合物的对映异构 一、构型的表示法: 1. 透视式(三维结构):略 2.Fischer 投影式:
COOH
H
OH
COOH
H
OH
C H3
CH3
20
使用Fischer 投影式的注意事项: (1)可以沿纸面旋转,但不能离开纸面翻转。
一.什么是生物化学(Biochemistry、Biological chemistry )
D.通常将生物大分子结构、功能及其代谢调控的研究称为分子生物学 (Molecular biology).在某种意义上,分子生物学是生物化学发展的一个新阶段. 所以这门学科也称为生物化学与分子生物学 (Biochemistry & Molecular Biology).
第三十章 DNA的复制和修复
如果让光通过一个象栅栏一样的 Nicol 棱镜 (起偏镜) 就不是所有方向的光都能通过,而只有与棱镜晶轴方向 平行的光才能通过。这样,透过棱晶的光就只能在一个 方向上振动,象这种只在一个平面上振动的光,称为平
12
面偏振光,简称偏振光或偏光。
生物化学.第一篇 .生物分子的结构和化学
第一章 生物分子导论
细胞器(organelle)(细胞核、线粒体,高尔基体等)
6
细胞(原核细胞,真核细胞等)
生物化学.第一篇 .生物分子的结构和化学
第一章 生物分子导论
三.生物分子的三维结构
1.生物分子大小:生物分子不仅种类繁多,在大小方面跨度也很大,例如,丙 氨酸分子量是89,但烟草花叶病毒达到40000000.
2.立体异构与构型
故:分子的手性是对映体存在的必要和充分条件。
19
§3—4— 3 含一个手性碳原子化合物的对映异构 一、构型的表示法: 1. 透视式(三维结构):略 2.Fischer 投影式:
COOH
H
OH
COOH
H
OH
C H3
CH3
20
使用Fischer 投影式的注意事项: (1)可以沿纸面旋转,但不能离开纸面翻转。
一.什么是生物化学(Biochemistry、Biological chemistry )
D.通常将生物大分子结构、功能及其代谢调控的研究称为分子生物学 (Molecular biology).在某种意义上,分子生物学是生物化学发展的一个新阶段. 所以这门学科也称为生物化学与分子生物学 (Biochemistry & Molecular Biology).
第三十章 DNA的复制和修复
王镜岩生化第三版考研课件 第37章 遗传密码和蛋白质的生物合成ppt课件

3、核糖体是蛋白质合成的工厂
(二)蛋白质合成的步骤
1、氨酰tRNA的生成
氨酰tRNA合成酶
氨酰AMP
形成2’形式的酯
氨酰基团在2’ 3’间交换
形成3’形式的酯
形成3’形式的酯
2、氨酰tRNA合成酶识别:AA、tRNA 、ATP
Ⅰ型和Ⅱ型酶
3、氨酰tRNA合成酶的校正功能 ——水解非正确组合的AA和tRNA
• 异亮氨酰 – tRNAIle • 缬氨酰 – tRNAVal 缬氨酰 – tRNAIle则被水解: 缬氨酸+ tRNAIle
4、一个特殊的tRNA启动蛋白的合成
• 翻译起始于Met的参与
tRNAMet:携带Met掺入蛋白内部
tRNAiMet :起始Met 掺入
——由同一种tRNA合成酶合成
起始因子识别tRNAiMet 延伸因子识别tRNAMet
①与核糖体A位紧密结合,阻碍氨基酰tRNA进入 ②抑制肽酰转移酶活性,肽链延伸受到影响
50S大亚基蛋白组分
(2)毒素
白喉霉素 催化蛋白发生ADP-核糖基化
共价修饰使EF-2失活 一条多肽单链,2个二硫键,2个结构域 β 结构域与细胞表面受体结合→ 毒素蛋白水解断裂 二硫键还原,产生A、B两片段: B协助A通过细胞膜,A为蛋白修饰酶
已合成的多肽链无法释放, 抑制70S核糖体的解离
四环素(土霉素、金霉素)
①作用于细菌30S小亚基,抑制起始复合物形成 ②抑制氨酰tRNA进入核糖体A位,阻滞肽链延伸; ③影响终止因子与核糖体的结合
四环素类抗生素对真核细胞核糖体也有抑制
但不能通过真核生物细胞膜 对70S核糖体的敏感性更高
氯霉素——广谱抗生素
……UGUGUGUGUGUGUGU……
王镜岩生化第三版考研课件第章糖类

一些糖醇
(七)糖苷
糖苷前面已述,糖苷的配基为酚类、糖醇或含氮碱等 的单糖或寡糖衍生物。这类糖着大多都有苦味或特殊 香气,不少还是剧毒的物质.但微量时可作药用。 1. 苦杏仁苷(amygdarin)含于许多蔷薇科植物(如苦 扁桃、杏、李、花揪等)的果核中,尤以苦扁桃(苦 杏仁)中含量为多。配基是由氰氢酸残基和苯甲醛残 基组成的。
2.寡糖(oIigosaccharide)
寡糖包括的类别很多,双糖或称二糖 (disaccharide),水解时生成 2分子单糖,如 麦芽糖、蔗糖等;三糖(trisaccharide),水解 时产生3分子单糖,如棉于糖;以及四糖 (tetrasaccharide),五糖(pentasaccharide) 和六糖(hexasaccharide)等。
4、形成糖脎: 单糖与苯肼反应生成糖脎,糖脎相当稳定的结晶, 不同的单糖形成的糖脎结晶不同,可用来鉴定单 糖。
5、形成糖酯与糖醚: 单糖的许多化学行为很想简单的醇类,它的羟基 可以转变为脂基或醚基。如单糖和磷酸形成各种 磷酸酯,G-1-P,1,6-2P-F等。
6、形成糖苷:
环状单糖的半缩醛羟基与另一化合物发生 缩合形成缩醛的衍生物称为糖苷,这种糖 苷的配体可以是糖,也可以是非糖物质。 与糖形成糖苷如淀粉、纤维素等与非糖物 质形成核苷等。糖苷的性质比较稳定不易 发生化学反应和被氧化。
•3、溶解度:单糖分子具有多个羟基,所以易溶于水 (甘油醛微溶)。尤其在热水中有较大的溶解度。 单糖微溶于乙醇,不溶于乙醚和丙酮。
(二)单糖的化学性质
单糖是多羟基的醛或酮,因此是活跃的分子易于和其 他物质发生化学反应。
1、异构化(弱碱的作用):单糖对稀酸相当稳定,但 在碱溶液中能发生多种反应,产生不同的产物。单 糖在碱溶液中可发生分子重排通过烯二醇中间物互
生物化学王镜岩第三版ppt课件

NAD
胞液中:甘油-α-磷酸脱氢酶
甘油-α-磷酸
线
二羟丙酮磷酸
甘油-α-磷酸
粒
线粒体内:甘油-α-磷酸脱氢酶
体
内
FADH2
FAD
膜
NADH FMD CoQ b c1 c aa3 O2
38
2.肝、肾、心等组织的苹果酸穿梭作用
NADH
天冬 转氨酶
氨酸
草酰乙酸
NAD
胞液中:苹果酸脱氢酶
苹果酸
天冬 转氨酶
36
四、胞液中的NADH 的再氧化 139页
细胞溶胶中的NADH逆浓度梯度转运到线粒体内 膜进入电子传递进行氧化。
肌肉、神经组织中的甘油-α-磷酸穿梭作用 (1.5ATP)
肝、肾、心等组织的苹果酸穿梭作用 (2.5ATP)
37
139页
1.肌肉、神经组织中的甘油-α-磷酸穿梭作用
NADH 二羟丙酮 磷酸
第九章 生物氧化 第114页
第一节 第二节 第三节
生物氧化的方式和特点 生物氧化的历程 生物氧化与能量代谢
1
氧化-还原电势
117页
氧化还原对 ee-
Oxidized 氧化型
Reduced 还原型
某一化合物的氧化型和还原型,称为一对氧化 还原对。如Zn/Zn2+,Cu2+/Cu。
2
生物体中标准氧化还原电势 117页表
pH 7
H+
外
内
脂不溶
脂溶
34
2.氧化磷酸化抑制剂
氧化磷酸化抑制剂抑制氧的利用又抑制 ATP的形成,但不直接抑制电子传递链上 的载体的作用。
机制:干扰ATP生成过程(ATP合酶), 干扰由电子传递的高能状态形成ATP的过 程,结果也使电子传递不能进行。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
细胞色素还原酶 (Ⅲ , b, c1, c )
细胞色素c、细胞色素C氧化酶( Ⅳ)。 内外膜间
内
15
FADH2 FAD
末端氧化酶
氧化酶将电子和H+传递给氧的作用过程中处 于呼吸链的末端,故又称为末端氧化酶。
生物体中,末端氧化酶已知的主要有:
细胞色素氧化酶:细胞色素a a3以复合物形式存在. 黄素蛋白氧化酶 过氧化氢酶和过氧化物酶 酚氧化酶, 抗坏血酸氧化酶等
23
P/O比
指氧化磷酸化过程中每消耗1摩尔氧原子所消耗 的无机磷酸的摩尔值。
是一对电子通过呼吸链到氧所产生的ATP分子数。
NADH或NADPH FADH2
1 2 02
1 2 02
3ATP(2.5ATP) 2ATP (1.5ATP)
24
练习题
1.参与生物氧化的酶可分为_____、______和____三类。
生物氧化通常需要消耗氧,所以又称为
呼吸作用、细胞氧化、细胞呼吸、组织 呼吸。
生物氧化
(CH2O) + O2
H20 + CO2 + 能量
4
第一节 生物氧化的方式和特点
一、生物氧化的方式
脱氢(脱氢酶) 氧直接参加的反应(加氧酶、氧化酶) 物质失去电子
5
二、生物氧化的特点
在生物细胞内进行,反应条件温和。 氧化进行过程中,伴随生物还原反应的发生。 氧化过程中脱下来的氢质子和电子,通常由各种载体,
10
1.电子传递和氧化呼吸链 119页
电子传递过程:呼吸链:
呼吸链在真核细胞发生在线粒体内膜上,在原核细胞发 生在质膜上。
MH2
递氢体
NAD+、NADP+、 FMN、FAD、COQ
M
递氢体H2
脱氢酶
2e
递电子体 还原型
Cyt b, c1, c, aa3
½ O2
递电子体
O2-
氧化型
氧化酶
HH2O2O
E0 ’ --标准氧化还原电势
( E0’值的测定条件为pH=7.0、250C)
E0’越负,物质丢失电子的倾向愈大,愈容易成为还原剂。 E0’越正,物质接受电子的倾向愈大,愈易被还原。
3
生物氧化
有机物质在生物体内被氧化分解成 CO2
和水,并释放出能量的过程。
生物氧化可分两阶段
分解代谢 电子传递或氧化磷酸化
B.干扰氧的运输
C.微循环障碍
D.细胞呼吸受抑制
5.肌肉中能量的主要贮存形式是下列哪一种?
A.ADP B.磷酸肌酸 C.cAMP D.ATP
25
2.能量偶联假说
化学偶联假说 构象偶联假说 化学渗透假说
26
化学渗透假说 132页
27
化学渗透假说的要点是
线粒体内膜的电子传递链中有三个也是质子泵; 电子由高能状态传递到低能状态时释放出来的能量,用于驱
17
4.电子传递的抑制剂
128页
能够阻断呼吸链中某一部位电子传递的物质称为 电子传递抑制剂。
NADH-C0Q- Cytb-Cytc1-Cytc Cytaa3-O2
鱼藤酮,安密妥, 杀粉蝶菌素
抗霉素A
氰化物、硫化物、 叠氮化物、一氧化碳
18
第三节 生物氧化与能量代谢
能量的释放 高能磷酸化合物ATP的生成 氧化磷酸化的偶联机理 氧化磷酸化的解偶联和抑制 氧化磷酸化的调控 能量的利用
19
一、能量的释放
物质氧化分解过程中释放能量
20
二、氧化磷酸化--ATP的生成
氧化磷酸化作用是将生物氧化过程中释放出的自由能转移 而使ADP形成高能ATP的作用。
1.底物水平磷酸化
指ATP的形成直接与一个代谢中间物(例如磷酸烯醇式 丙酮酸)上的磷酸基团转移相偶联的作用。
21
2. 电子传递水平磷酸化(氧化磷酸化作用) 是指直接与电子传递相偶联由ADP形成ATP
13
根据接受氢的初受体不同,典型的呼吸链有两条 NADH呼吸链和FADH2呼吸链
GO’= - 52.6 kcal/mol
GO’= - 43.4 kcal/mol
14
3.呼吸链的组成 121页
各组分摩尔比并非1/1 NADHQ 泛醌还原型酶( Ⅰ,辅基为FMN) 琥珀酸-Q还原酶( Ⅱ,辅基为FAD)
2H+
11
线粒体图示
12
2.呼吸链电子传递成员的排列顺序 120页
MH2 NADH -0.32
FMN CoQ b c1
c
aa3
O2
-0.30 +0.10 +0.07 +0.22 +0.25 +0.29 +0.816
FAD -0.18
电位跨度最大的一步
呼吸链中NAD+/NADH的E0’值最小,而O2/H2O的E0’ 值最大,电子的传递方向是从NADH-O2
如 NADH、FAD2H等传递到氧并生成水。
每一步反应的产物都可以分离出来。能量逐步释放. 生物氧化释放的能量,通过与ATP合成相偶联.
6
2.非氧化脱羧
2
2
-COOH 草酰琥珀酸脱羧酶
2
+ CO2
草酰琥珀酸
α-酮戊二酸
9
二、生物氧化中水的生成
以脱氢酶、传递体及氧化酶组成生物氧化 体系,以促进水的生成。
第九章 生物氧化 第114页
第一节 第二节 第三节
生物氧化的方式和特点 生物氧化的历程 生物氧化与能量代谢
1
氧化-还原电势
117页
氧化还原对 ee-
Oxidized 氧化型
ReducedBiblioteka 还原型 某一化合物的氧化型和还原型,称为一对氧化 还原对。如Zn/Zn2+,Cu2+/Cu。
2
生物体中标准氧化还原电势 117页表
的磷酸化作用。 NADH+H+---------------- O2H2O
ATP
22
3. 氧化磷酸化作用机制 130页
(1)ATP的合成部位
伴随电子从底物到氧,释放自由能-52.74千卡/摩尔
FADH2
NADH
CoQ
细胞色素C 细胞色素aa3
1/2O2
ATP
ATP
ATP
1:G0’ =-12.4千卡/摩尔 2: G0’ =-9.2千卡/摩尔 3: G0’ =-24.8千卡/摩尔 3ATP分子的形成劫获了呼吸链中电子由NADH传递至氧 所产生的全部自由能的42%.
2.真核细胞的呼吸链主要存在于___,而原核细胞的呼吸 链存在于_____。
3.在下列的氧化还原系统中,哪个氧化还原电位最高?
A.氧化型泛醌/还原型泛醌
B. Fe3+细胞色素a/Fe2+细胞色素a
C. Fe3+细胞色素b/Fe2+细胞色素b
D. NAD+/NADH
4.氰化物引起的缺氧是由于
A. 中枢性肺换气不良
细胞色素c、细胞色素C氧化酶( Ⅳ)。 内外膜间
内
15
FADH2 FAD
末端氧化酶
氧化酶将电子和H+传递给氧的作用过程中处 于呼吸链的末端,故又称为末端氧化酶。
生物体中,末端氧化酶已知的主要有:
细胞色素氧化酶:细胞色素a a3以复合物形式存在. 黄素蛋白氧化酶 过氧化氢酶和过氧化物酶 酚氧化酶, 抗坏血酸氧化酶等
23
P/O比
指氧化磷酸化过程中每消耗1摩尔氧原子所消耗 的无机磷酸的摩尔值。
是一对电子通过呼吸链到氧所产生的ATP分子数。
NADH或NADPH FADH2
1 2 02
1 2 02
3ATP(2.5ATP) 2ATP (1.5ATP)
24
练习题
1.参与生物氧化的酶可分为_____、______和____三类。
生物氧化通常需要消耗氧,所以又称为
呼吸作用、细胞氧化、细胞呼吸、组织 呼吸。
生物氧化
(CH2O) + O2
H20 + CO2 + 能量
4
第一节 生物氧化的方式和特点
一、生物氧化的方式
脱氢(脱氢酶) 氧直接参加的反应(加氧酶、氧化酶) 物质失去电子
5
二、生物氧化的特点
在生物细胞内进行,反应条件温和。 氧化进行过程中,伴随生物还原反应的发生。 氧化过程中脱下来的氢质子和电子,通常由各种载体,
10
1.电子传递和氧化呼吸链 119页
电子传递过程:呼吸链:
呼吸链在真核细胞发生在线粒体内膜上,在原核细胞发 生在质膜上。
MH2
递氢体
NAD+、NADP+、 FMN、FAD、COQ
M
递氢体H2
脱氢酶
2e
递电子体 还原型
Cyt b, c1, c, aa3
½ O2
递电子体
O2-
氧化型
氧化酶
HH2O2O
E0 ’ --标准氧化还原电势
( E0’值的测定条件为pH=7.0、250C)
E0’越负,物质丢失电子的倾向愈大,愈容易成为还原剂。 E0’越正,物质接受电子的倾向愈大,愈易被还原。
3
生物氧化
有机物质在生物体内被氧化分解成 CO2
和水,并释放出能量的过程。
生物氧化可分两阶段
分解代谢 电子传递或氧化磷酸化
B.干扰氧的运输
C.微循环障碍
D.细胞呼吸受抑制
5.肌肉中能量的主要贮存形式是下列哪一种?
A.ADP B.磷酸肌酸 C.cAMP D.ATP
25
2.能量偶联假说
化学偶联假说 构象偶联假说 化学渗透假说
26
化学渗透假说 132页
27
化学渗透假说的要点是
线粒体内膜的电子传递链中有三个也是质子泵; 电子由高能状态传递到低能状态时释放出来的能量,用于驱
17
4.电子传递的抑制剂
128页
能够阻断呼吸链中某一部位电子传递的物质称为 电子传递抑制剂。
NADH-C0Q- Cytb-Cytc1-Cytc Cytaa3-O2
鱼藤酮,安密妥, 杀粉蝶菌素
抗霉素A
氰化物、硫化物、 叠氮化物、一氧化碳
18
第三节 生物氧化与能量代谢
能量的释放 高能磷酸化合物ATP的生成 氧化磷酸化的偶联机理 氧化磷酸化的解偶联和抑制 氧化磷酸化的调控 能量的利用
19
一、能量的释放
物质氧化分解过程中释放能量
20
二、氧化磷酸化--ATP的生成
氧化磷酸化作用是将生物氧化过程中释放出的自由能转移 而使ADP形成高能ATP的作用。
1.底物水平磷酸化
指ATP的形成直接与一个代谢中间物(例如磷酸烯醇式 丙酮酸)上的磷酸基团转移相偶联的作用。
21
2. 电子传递水平磷酸化(氧化磷酸化作用) 是指直接与电子传递相偶联由ADP形成ATP
13
根据接受氢的初受体不同,典型的呼吸链有两条 NADH呼吸链和FADH2呼吸链
GO’= - 52.6 kcal/mol
GO’= - 43.4 kcal/mol
14
3.呼吸链的组成 121页
各组分摩尔比并非1/1 NADHQ 泛醌还原型酶( Ⅰ,辅基为FMN) 琥珀酸-Q还原酶( Ⅱ,辅基为FAD)
2H+
11
线粒体图示
12
2.呼吸链电子传递成员的排列顺序 120页
MH2 NADH -0.32
FMN CoQ b c1
c
aa3
O2
-0.30 +0.10 +0.07 +0.22 +0.25 +0.29 +0.816
FAD -0.18
电位跨度最大的一步
呼吸链中NAD+/NADH的E0’值最小,而O2/H2O的E0’ 值最大,电子的传递方向是从NADH-O2
如 NADH、FAD2H等传递到氧并生成水。
每一步反应的产物都可以分离出来。能量逐步释放. 生物氧化释放的能量,通过与ATP合成相偶联.
6
2.非氧化脱羧
2
2
-COOH 草酰琥珀酸脱羧酶
2
+ CO2
草酰琥珀酸
α-酮戊二酸
9
二、生物氧化中水的生成
以脱氢酶、传递体及氧化酶组成生物氧化 体系,以促进水的生成。
第九章 生物氧化 第114页
第一节 第二节 第三节
生物氧化的方式和特点 生物氧化的历程 生物氧化与能量代谢
1
氧化-还原电势
117页
氧化还原对 ee-
Oxidized 氧化型
ReducedBiblioteka 还原型 某一化合物的氧化型和还原型,称为一对氧化 还原对。如Zn/Zn2+,Cu2+/Cu。
2
生物体中标准氧化还原电势 117页表
的磷酸化作用。 NADH+H+---------------- O2H2O
ATP
22
3. 氧化磷酸化作用机制 130页
(1)ATP的合成部位
伴随电子从底物到氧,释放自由能-52.74千卡/摩尔
FADH2
NADH
CoQ
细胞色素C 细胞色素aa3
1/2O2
ATP
ATP
ATP
1:G0’ =-12.4千卡/摩尔 2: G0’ =-9.2千卡/摩尔 3: G0’ =-24.8千卡/摩尔 3ATP分子的形成劫获了呼吸链中电子由NADH传递至氧 所产生的全部自由能的42%.
2.真核细胞的呼吸链主要存在于___,而原核细胞的呼吸 链存在于_____。
3.在下列的氧化还原系统中,哪个氧化还原电位最高?
A.氧化型泛醌/还原型泛醌
B. Fe3+细胞色素a/Fe2+细胞色素a
C. Fe3+细胞色素b/Fe2+细胞色素b
D. NAD+/NADH
4.氰化物引起的缺氧是由于
A. 中枢性肺换气不良
