大肠菌群最可能数(MPN)检索表
【微生物】大肠菌群检验及注意事项

【微生物】大肠菌群检验及注意事项!大肠菌群介绍大肠菌群并非细菌学分类命名,而是卫生细菌领域的用语,它不代表某一个或某一属细菌,而指的是具有某些特性的一组与粪便污染有关的细菌,这些细菌在生化及血清学方面并非完全一致,其定义为:需氧及兼性厌氧、在37℃能分解乳糖产酸产气的革兰氏阴性无芽胞杆菌。
一般认为该菌群细菌可包括大肠埃希氏菌、柠檬酸杆菌、产气克雷白氏菌和阴沟肠杆菌等。
大肠菌群分布较广,在温血动物粪便和自然界广泛存在。
调查研究表明,大肠菌群细菌多存在于温血动物粪便、人类经常活动的场所以及有粪便污染的地方,人、畜粪便对外界环境的污染是大肠菌群在自然界存在的主要原因。
粪便中多以典型大肠杆菌为主,而外界环境中则以大肠菌群其他型别较多。
大肠菌群是作为粪便污染指标菌提出来的,主要是以该菌群的检出情况来表示食品中有否粪便污染。
大肠菌群数的高低,表明了粪便污染的程度,也反映了对人体健康危害性的大小。
粪便是人类肠道排泄物,其中有健康人粪便,也有肠道患者或带菌者的粪便,所以粪便内除一般正常细菌外,同时也会有一些肠道致病菌存在(如沙门氏菌、志贺氏菌等),因而食品中有粪便污染,则可以推测该食品中存在着肠道致病菌污染的可能性,潜伏着食物中毒和流行病的威胁,必须看作对人体健康具有潜在的危险性。
大肠菌群是评价食品卫生质量的重要指标之一,目前已被国内外广泛应用于食品卫生工作中。
大肠菌群检验方法由于大肠菌群指的是具有某些特性的一组与粪便污染有关的细菌,即:需氧及兼性厌氧、在37℃能分解乳糖产酸产气的革兰氏阴性无芽胞杆菌。
因此大肠菌群的检测一般都是按照它的定义进行。
目前国内采用的食品大肠菌群检测方法主要有国家食品药品监督管理总局发布的国家标准和国家质量监督检验检疫总局颁布的进出口行业标准。
两个标准方法在检测程序上略有不同。
但两种方法都是采用推测、验证两大步骤。
推测试验:样品稀释后,选择三个稀释度,每个稀释度接种三管LST肉汤。
36±1℃培养48±2h,观察是否产气。
10食品中大肠菌群计数测定的标准操作规程

规范食品中大肠菌群计数测定的标准操作规程。
2范围本标准规定了食品中大肠菌群(Coliforms)计数的方法。
本标准适用于食品中大肠菌群的计数。
3术语和定义3.1 大肠菌群coliforms在一定培养条件下能发酵乳糖、产酸产气的需氧和兼性厌氧革兰氏阴性无芽胞杆菌。
3.2 最可能数most probable number,MPN基于泊松分布的一种间接计数方法。
4责任质量部组织制订、化验室负责实施。
5内容5.1 设备和材料除微生物实验室常规灭菌及培养设备外,其他设备和材料如下:5.1.1 恒温培养箱:36 ℃±1 ℃。
5.1.2 冰箱:2 ℃~5 ℃。
5.1.3 恒温水浴箱:46 ℃±1 ℃。
5.1.4 天平:感量0.1 g。
5.1.5 均质器。
5.1.6 振荡器。
5.1.7 无菌吸管:1 mL(具0.01 mL 刻度)、10 mL(具0.1 mL 刻度)或微量移液器及吸头。
5.1.8 无菌锥形瓶:容量500 mL。
5.1.9 无菌培养皿:直径90 mm。
5.1.10 pH 计或pH 比色管或精密pH 试纸。
5.1.11 菌落计数器。
5.2培养基和试剂5.2.1 月桂基硫酸盐胰蛋白胨(Lauryl Sulfate Tryptose,LST)肉汤:见附录A 中A.1。
5.2.2 煌绿乳糖胆盐(Brilliant Green Lactose Bile,BGLB)肉汤:见附录A 中A.2。
5.2.3 结晶紫中性红胆盐琼脂(Violet Red Bile Agar,VRBA):见附录A 中A.3。
5.2.4 磷酸盐缓冲液:见附录A 中A.4。
5.2.5 无菌生理盐水:见附录A 中A.5。
5.2.6 无菌1 mol/L NaOH:见附录A 中A.6。
5.2.7 无菌1 mol/L HCl:见附录A 中A.7。
5.3大肠菌群MPN 计数法5.3.1 检验程序大肠菌群MPN计数的检验程序见图1。
MPN法测定食品中大肠杆菌群数

知识点:MPN法测定大肠杆菌群数情境:微生物检测技术任务:MPN法测定大肠杆菌群数课程:食品微生物技术MPN 法测定大肠菌群原理一、大肠菌群什么叫大肠菌群大肠菌群是一群以大肠埃希氏菌为主的需氧及兼性厌氧的革兰氏阴性无芽孢杆菌,在37℃生长时,能在48h内发酵乳糖并产酸产气。
二、MPNMPN❞食品中大肠菌群数是以每100 mL(g)检样内大肠菌群最近似数(The most probable number,简称MPN)表示。
❞据此含义,所有食品卫生标准中所规定的大肠菌群均应以每mL(g)食品内允许含有大肠菌群的实际数值为报告标准。
三、MPN法测定原理MPN法是统计学和微生物学结合的一种定量检测法。
待测样品经系列稀释并培养后,根据其未生长的最低稀释度与生长的最高稀释度,应用统计学概率论推算出待测样品中大肠菌群的最大可能数。
大肠菌群测定步骤1.液体样品稀释以无菌吸管吸取25 mL样品置盛有225mL磷酸盐缓冲液或生理盐水的无菌锥形瓶(瓶内预置适当数量的无菌玻璃珠)或其他无菌容器中充分振摇或置于机械振荡器中振摇,充分混匀,制成1:10 的样品匀液。
2.梯度稀释❞用1 mL无菌吸管或微量移液器吸取(1:10)样品匀液1 mL,沿管壁缓缓注入9 mL磷酸盐缓冲液或生理盐水的无菌试管中(注意吸管或吸头尖端不要触及稀释液面),振摇试管混匀或换用1支1 mL无菌吸管反复吹打,使其混合均匀,作成1:100的样品匀液。
❞根据对样品污染状况的估计,按上述操作,依次制成十倍递增系列稀释样品匀液。
每递增稀释1次,换用1支1 mL灭菌吸管或吸头。
从制备样品匀液至样品接种完毕,全过程不得超过15min。
五、初发酵试验每个样品,选择3个适宜的连续稀释度的样品匀液(液体样品可以选择原液),每个稀释度接种3管月桂基硫酸盐胰蛋白胨(LST)肉汤,每管接种1mL(如接种量超过1mL,则用双料LST肉汤),36℃±1℃培养24h±2h,观察倒管内是否有气泡产生,24h±2h产气者进行复发酵试验(证实试验),如未产气则继续培养至48h±2h,产气者进行复发酵试验。
014大肠菌群计数作业指导书

陕西威水饮品有限公司质量管理文件1目的:规定了公司产品检验大肠菌群(Coliforms)的计数方法.2适用范围:适用于本公司成品中大肠菌群的计数。
3编写依据:GB4789.3-2010《食品安全国家标准食品微生物学检验大肠菌群计数》. 4术语和定义:4.1 大肠菌群coliforms在一定培养条件下能发酵乳糖、产酸产气的需氧和兼性厌氧革兰阴性无芽胞杆菌。
4.2 最可能数most probable number,MPN基于泊松分布的一种间接计数方法。
5.设备和材料:除微生物实验室常规灭菌及培养设备外,其他设备和材料如下:5.1 恒温培养箱:36℃±1℃5.2 冰箱:2℃~5℃5.3 恒温水浴箱:46℃±1℃5.4 天平:感量0.1g5.5 均质器5.6 振荡器5.7 无菌吸管:1mL(具0.01mL 刻度)、10mL(具0.1mL刻度)或微量移液器及吸头5.8 无菌锥形瓶:容量500 mL5.9 无菌培养皿:直径90 mm5.10 pH 计或pH 比色管或精密pH 试纸5.11 菌落计数器6.培养基和试剂:6.1 月桂基硫酸盐胰蛋白胨(Lauryl Sulfate Tryptose,LST)肉汤:见附录A 中A.1 6.2 煌绿乳糖胆盐(Brilliant Green Lactose Bile,BGLB)肉汤:见附录A 中A.2 6.3 结晶紫中性红胆盐琼脂(Violet Red Bile Agar,VRBA):见附录A 中A.36.4 磷酸盐缓冲液:见附录A 中A.46.5 无菌生理盐水:见附录A 中A.56.6 无菌1 mol/L NaOH:见附录A 中A.66.7 无菌1 mol/L HCl:见附录A 中A.7第一法大肠菌群MPN 计数法7检验程序:大肠菌群MPN计数的检验程序见图1。
图1 大肠菌群MPN计数法检验程序8操作步骤:8.1 样品的稀释8.1.1 固体和半固体样品:称取25g样品,放入盛有225mL磷酸盐缓冲液或生理盐水的无菌均质杯内,8000r/min~10000r/min 均质1min~2 min,或放入盛有225mL磷酸盐缓冲液或生理盐水的无菌均质袋中,用拍击式均质器拍打1min~2 min,制成1:10的样品匀液。
大肠菌群最可能数(MPN)检索表
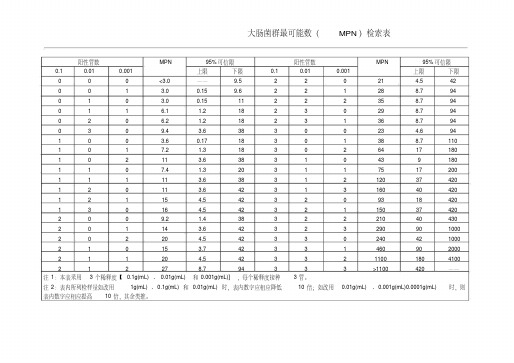
阳性管数MPN95%可信限阳性管数MPN95%可信限0.10.010.001上限下限0.10.010.001上限下限000<3.0——9.522021 4.542 001 3.00.159.6221288.794 010 3.00.1511222358.794 011 6.1 1.218230298.794 020 6.2 1.218231368.794 0309.4 3.63830023 4.694 100 3.60.1718301388.7110 1017.2 1.3183026417180 10211 3.638310439180 1107.4 1.3203117517200 11111 3.63831212037420 12011 3.64231316040420 12115 4.5423209318420 13016 4.54232115037420 2009.2 1.43832221040430 20114 3.642323********* 20220 4.542330********* 21015 3.742331460902000 21120 4.54233211001804100 212278.794333>1100420——注 1:本表采用 3 个稀释度【 0.1g(mL) 、 0.01g(mL)注 2:表内所列检样量如改用1g(mL) 、0.1g(mL) 和表内数字应相应提高10 倍,其余类推。
和 0.001g(mL)] ,每个稀释度接种0.01g(mL) 时,表内数字应相应降低3 管。
10 倍;如改用0.01g(mL)、0.001g(mL)0.0001g(mL)时,则一种微生物活菌数快速检测方法,其特征在于包括以下步骤:a)样品的选择:检测样品分为固体样品和液体样品;b)采样样品的制备:通过无菌操作取一定量溶液样品进行离心处理后,取上清液,再以更高的速度离心处理,弃去上清液,用移液器取出底部少量溶液;c)微生物活菌数的检测:将移液器取出的底部溶液,涂在载玻片上,经干燥固定,用美兰染色,冲洗后用生物显微镜镜检,记录被美兰染色且呈现空心状态的图像的个数来计数微生物数量。
大肠菌群检测作业标准书ok

大肠菌群系指一群能发酵乳糖、产酸产气、需氧和兼性厌氧的革兰氏阴性无芽胞杆菌。该菌主要来源于人畜粪便,故以此作为粪便污染指标来评价食品的卫生质量,推断食品中有否污染肠道致病菌的可能。
食品中大肠菌群数系以100mL(g)检样内大肠菌群最可能数(MPN)表示。
5.操作方法
5.1仪器:
5.1.1冰箱:0℃-4℃
下限
上限
0
0
0
0
0
0
0
0
0
1
2
3
<30
30
60
90
<5
90
0
0
0
0
1
1
1
1
0
1
2
3
30
60
90
120
<5
130
0
0
0
0
2
2
2
2
0
1
2
3
60
90
120
160
0
0
0
0
3
3
3
3
0
1
2
3
90
130
160
190
1
1
1
1
0
0
0
0
0
1
2
3
40
70
110
150
<5
10
200
210
1
1
1
1
1
1
1
1
0
1
2
3
70
110
150
5.4.1.2用1mL灭菌吸管吸取1∶10稀释液1mL,注入含有9mL灭菌生理盐水或其他稀释液的试管内,振摇试管混匀,做成1∶100的稀释液。
乳与乳制品微生物检验食品中大肠菌群的检测

乳与乳制品微生物检验食品中大肠菌群的检测YLNB 3.21、引用依据:GB/T4789.3-20032、术语和定义大肠菌群:指一群能发酵乳糖、产酸产气、需氧和兼性厌氧的革兰氏阴性无芽孢杆菌。
该菌主要来源于人畜粪便,故以此作为粪便污染指标来评价食品的卫生质量,推断食品中有否污染肠道致病菌的可能。
食品中大肠菌群数系以100ml(g)检样内大肠菌群最可能数(MPN表示。
3、仪器及器材3.1恒温培养箱:36 ± 1C;3.2 冰箱:0-4 C;3.3恒温水浴锅:46 ± 1C;3.4天平;3.5显微镜;3.6均质器或乳钵;3.7 灭菌平皿:直径90mm3.8 灭菌试管:18X 180 和20X 200;3.9灭菌吸管:1 ml和10 ml ;3.10灭菌广口瓶或三角烧瓶:容量为500ml ;3.11灭菌玻璃珠:直径约5mm 3.12载玻片;3.13酒精灯;3.14试管架;3.15灭菌刀、剪子、灭菌镊子等4、培养基和试剂4.1乳糖胆盐发酵管;4.2伊红美兰琼脂平板;4.3乳糖发酵管;4.4生理盐水;4.5革兰氏染色液。
5、检验程序6、方法6.1检样稀释6.1.1 以无菌操作将检样25ml (或g)放于装有225ml灭菌生理盐水或其他稀释液的灭菌玻璃瓶内(瓶内预置适当数量的玻璃珠)或灭菌乳钵内,经充分振摇或研磨做成1: 10的均匀稀释液。
固体检样最好用均质器,以8000〜10000r/min 的速度处理1min,做成1: 10的均匀稀释液。
6.1.2 用1ml灭菌吸管吸取1: 10稀释液1ml,注入含有9ml灭菌生理盐水或其他稀释液的试管内,振摇试管混匀,做成1: 100的稀释液。
6.1.3另取1ml灭菌吸管,按上条操作依次做10倍递增稀释液,每递增稀释一次,换用一支1ml灭菌吸管。
6.1.4根据食品卫生标准要求或对检样污染情况的估计,选择三个稀释度,每个稀释度接种3管。
6.2乳糖发酵实验:(通常所说的假定试验:其目的在于检查样品中有无发酵产生气体的细菌)将待检样品接种于乳糖胆盐发酵管内,接种量在1ml以上者,用双料乳糖胆盐发酵管,1ml及1ml以下者,用单料乳糖胆盐发酵管。
肉制品中大肠菌群的检验—第一法大肠菌群MPN计数法

菌海砂或玻璃砂研磨,磨碎后加入灭菌水225mL,混匀后即为1:10稀释
液。或用均质器以8000~10000r/min,均质1min,做成1:10稀释液。
一、样品的采集和处理
大
肠
4.2 鲜、冻家禽检样的处理
菌
群
先将检样进行表面消毒,再用无菌剪子取检样深层肌肉25g(一般可从
MPN
胸部或腿部剪取)。其他处理同生肉。带毛野禽去毛后,同家禽检样处理。
MPN
1.2 采样过程遵循无菌操作程序,防止一切可能的外来污染。
计 数
2. 采样方案
法
2.1 根据检验目的、食品特点、批量、检验方法、微生物的危害
程度等确定采样方案。
2.2 采样方案分为二级和三级采样方案。二级采样方案设有n、
c和m 值,三级采样方案设有n、c、m 和M 值。
一、样品的采集和处理
大
第一法:大肠菌群MPN计数法
目录页
样品的采集和处理 设备和材料 培养基和试剂
大肠菌群MPN计数检样程序 大肠菌群MPN计数检样操作步骤
样品的采集和处理
一
1. 采样原则和采样方案 2. 采样用品 3. 样品的采取和送检 4. 检样的处理
一、样品的采集和处理
大 肠
1. 采样原则
菌 群
1.1 样品的采集应遵循随机性、代表性的原则。
群
样品,
MPN
若5个样品的检验结果均小于或等于m 值(≤100CFU/g),则这种情况是允许的;
计 数
若≤2个样品的结果(X)位于m 值和M 值之间(100CFU/g<X≤1000CFU/g),
法
则这种情况也是允许的;
若有3个及以上样品的检验结果位于m 值和M 值之间,则这种情况是不允许的;
实验二 食品中大肠菌群的检验

③另取1mL灭菌吸管,按②操作依次做10倍递增稀释液,每
稀释一次,换用一支1 mL灭菌吸管。
2)乳糖发酵实验 接种1mL待检样品于乳糖胆盐 发酵管内。接种3个稀释度,每一 稀释度接种3管,置(36土1)℃
汤),36℃±1 ℃培养24 h±2 h,观察倒管内是
否有气泡产生,24 h±2 h产气者进行复发酵试验,
如未产气则继续培养至48 h±2 h,产气者进行复
发酵试验。未产气者为大肠菌群阴性。
LST结果判断
大肠菌群的产气量,多者可以使发酵倒管全部充 满气体,少者可以产生比小米粒还小的气泡。如 果对产酸但未产气的乳糖发酵如有疑问时,可以 用手轻轻打动试管。
阳性管 10ml 0 0 0 0 0 0 0 0 0 0 0 0 0 0 0 1 1 1 1 1 1 1 1 1ml 0 0 0 1 1 1 1 2 2 2 2 3 3 3 3 0 0 0 0 1 1 1 1 0.1ml 1 2 3 0 1 2 3 0 1 2 3 0 1 2 3 0 1 2 3 0 1 2 3 3 6 9 3 6 9 12 6 9 12 16 9 13 16 19 4 7 11 15 7 11 15 19 MPN 10ml 1 1 1 1 1 1 1 1 2 2 2 2 2 2 2 2 2 2 2 2 2 2 2 阳性管 1ml 2 2 2 2 3 3 3 3 0 0 0 0 1 1 1 1 2 2 2 2 3 3 3 0.1ml 0 1 2 3 0 1 2 3 0 1 2 3 0 1 2 3 0 1 2 3 0 1 2 11 15 20 24 16 20 24 29 9 14 20 26 15 20 27 34 21 28 35 42 29 36 44 MPN 10ml 2 3 3 3 3 3 3 3 3 3 3 3 3 3 3 3 3 阳性管 1ml 3 0 0 0 0 1 1 1 1 2 2 2 2 3 3 3 3 0.1ml 3 0 1 2 3 0 1 2 3 0 1 2 3 0 1 2 3 53 23 39 64 95 43 75 120 160 93 150 210 290 240 460 1100 1100+ MPN
国家食品卫生标准大肠菌群检验方法探究

国家食品卫生标准大肠菌群检验方法探究摘要:本文主要分析和探讨国家食品卫生微生物标准的大肠杆菌群测定的基本原理和具体方法,并针对现有检测方法的不足提出有针对性的完善意见,希望可以促进大肠菌群检测技术的不断进步。
关键词:大肠菌群;检验方法;修改建议大肠菌群只存在于温血动物和人的肠道中,来源非常专一,并且在粪便中含量较多,对外部环境的耐受性也较高。
大肠菌群是世界上绝大多数国家和组织评价食品卫生质量的重要指标。
我国的食品卫生微生物标准体系主要包括大肠菌群、菌落总数以及致病菌三大类,其中大肠菌群既属于菌落总数的一部分,同时作为粪便污染指示菌,与肠道致病菌之间存在着密切联系,所以大肠菌群在食品微生物指标体系中地位显著。
1.大肠菌群及其检验意义大肠菌群大量存在于人和动物的肠道内,并且在水分和营养物质充足的环境中能够长时间生存,大肠菌群的生长对营养物质的要求较低,能够在含有适宜浓度胆盐的培养基中生存。
大肠菌群能够产生发酵乳糖,并产生酸和气体。
大肠菌群不具备耐高温的特性,在巴氏杀菌条件下会很快死亡,而且在寒冷环境中也不易存活,所以冷冻食品中的大肠菌群含量极低。
(一)大肠菌群及其检验意义大肠菌群是指在37℃的环境中,在24小时之内能够发酵乳糖并产酸产气的革兰氏阴性无芽孢杆菌。
检测食品中大肠菌群的含量,就可以判断出食品被粪便的污染程度,同时也能反映出食品对人体健康的危害性。
粪便内不仅包含了正常细菌,同时也会存在着一些肠道致病菌,例如志贺氏菌、沙门氏菌等。
如果食品在生产过程中被粪便污染,那么食品就有很大可能会携带肠道致病菌,进而引起食物中毒或者流行性疾病,因此对于大肠菌群进行检验有着十分重要的意义。
(二)大肠菌群的相关标准大肠菌群作为检验食物粪便污染的指标,因为大肠菌群更容易分离和鉴定,现如今已经广泛应用在食品检测领域。
由于世界上不同国家的食品种类不同,而且对于粪便指示菌的认识也存在一定差异,所以在选择粪便污染指示菌时也存在着很大不同,但是通常多以大肠菌群、粪大肠菌群、粪链球菌等作为粪指示菌。
食品中大肠菌群的测定含MPN检索表

⾷品中⼤肠菌群的测定含MPN检索表实验六⾷品中⼤肠菌群的测定⼀、概述(⼀)⼤肠菌群的定义及范围根据国家1994年颁布的⾷品卫⽣检验⽅法微⽣物学部分,⼤肠菌群(coliform bacteria)系指⼀群在37℃、24h能发酵乳糖,产酸、产⽓,需氧和兼性厌氧的⾰兰⽒阴性⽆芽胞杆菌。
⼤肠菌群主要是由肠杆菌科中四个菌属内的⼀些细菌所组成,即艾希⽒菌届、拘橼酸杆菌属、克雷伯⽒菌属及肠杆菌属,其⽣化特性分类见表5-4。
表5-4 ⼤肠菌群⽣化特性分类表注:+,表⽰阳性;—,表⽰阴性;+/-,表⽰多数阳性,少数阴性。
由上表可以看出,⼤肠菌群中⼤肠艾希⽒菌I型和Ⅲ型的特点是,对靛基质、甲基红、v-P和拘橼酸盐利⽤四个⽣化反应分别为“⼗⼗⼀⼀”,通常称为典型⼤肠杆菌;⽽其他类⼤肠杆菌则披称为⾮典型⼤肠杆菌。
(⼆)⼤肠菌群的测定意义1、粪便污染的指标细菌早在1892年,沙尔丁格(Schardinger)⽒⾸先提出⼤肠杆菌作为⽔源中病原菌污染的指标菌的意见,因为⼤肠杆菌是存在于⼈和动物的肠道内的常见细菌。
⼀年后,塞乌博⽿德“斯密斯(Theobold.Smith)⽒指出,⼤肠杆菌因普遍存在于肠道内,若在肠道以外的环境中发现,就可以认为这是由于⼈或动物的粪便污染造成的;从此,就开始应⽤⼤肠杆菌作为⽔源中粪便污染的指标菌。
据研究发现,成⼈粪便中的⼤肠菌群的含量为:108个/g⼀109个/g。
若⽔中或⾷品中发现有⼤肠菌群,即可证实已被粪便污染,有粪便污染也就有可能有肠道病原菌存在。
根据这个理由,就可以认为这种含有⼤肠菌群的⽔或⾷品供⾷⽤是不安全的。
所以⽬前为评定⾷品的卫⽣质量⽽进⾏检验时,也都采⽤⼤肠菌群或⼤肠杆菌作为粪便污染的指标细菌。
当然,有粪便污染,不⼀定就有肠道病原菌存在,但即使⽆病原菌,只要被粪便污染的⽔或⾷品,也是不卫⽣的,不受⼈喜欢的。
2.粪便污染指标菌的选择作为理想的粪便污染的指标菌应具备以下⼏个特性,才能起到⽐较正确的指标作⽤。
腌制食品中细菌总数和大肠杆菌的测定

腌制食品中细菌总数和大肠杆菌的测定摘要食品富含有机物以及其他营养物质,在生产环节和储藏中倒有可能被微生物污染,而导致食品腐败变质,人食用后会危害人体健康,此前在国内有过多例食物中毒的报道,从此人们对食品安全有了更多的关注。
检测食品中的细菌总数是判别食品被污染程度的重要途径,同时也是食品卫生检验的一个重要指标。
它是将待检食品经过一定处理,在一定的条件下培养,记录下培养基上长出的细菌菌落数,由待检食品的稀释倍数来计算出1g(ml)中的细菌个数。
为了精确检验结果还应该配合大肠杆菌群的检测和其他的项目检测。
大肠杆菌是一种革兰氏阴性无芽孢杆菌,常存在于人畜的消化道内,可随粪便排出体外,因此它通常作为评价食品卫生质量的重要指标之一。
大肠杆菌可强烈利用分解乳糖,代谢过程中产气产酸,常用方法是将待检食品稀释成不同的浓度梯度,在发酵罐中发酵,记录下产气管的数量,再参照大肠杆菌MPN检索表查出100g(ml)待检食品大肠杆菌的最可能数。
同时,可以进行革兰氏染色和鉴别培养基培养,以排除其他细菌的干扰。
关键词:大肠杆菌、腌制食品、菌落总数、MPN表AbstractFoods rich in organic matter and other nutrients , in production and storage of microbial contamination may be down , which led to food spoilage , it will harm human health after human consumption,in the country had too many cases of food poisoning which have been reported , from then on, people paid more and more concerns to food safety.Total bacterial detection in food is not only an important way to determine the level of contamination of food , but also an important indicator of food hygiene inspection . It is to be tested through a food processing under certain culture conditions , the number ofbacterial colonies grown on the lower recording medium by dilution of the food to be tested to calculate the number of 1g (ml) of bacteria.For accurate test results should fit testing and other items to detect coliform . E. coli is a gram-negative bacillus no , the often found in the digestive tract of humans and animals , can be excreted from the body, so it is usually evaluated as an important indicator of the quality of food hygiene one . E. coli can utilize a strong decomposition of lactose metabolism of the acid gas , commonly used food to be tested is diluted to a concentration gradient of different fermentation in a fermentor , the number of the recording capacity of the trachea , the retrieval table MPN E. Referring again to check the of 100g (ml) of the most probable number of E. coli in the food to be tested . At the same time , we can carry on Gram stain and culture medium discrimination to eliminate interference from other bacteria.Key:E. coli, preserved foods, the total number of colonies, MPN retrieval table1、前言俗话说“民以食为天”,由此可见食物对于我们人类的生活和生存的重要性。
医疗机构污水和污泥中粪大肠菌群的检验方法

医疗机构污水和污泥中粪大肠菌群的检验方法A1 仪器和设备高压蒸汽灭菌器。
干燥灭菌箱。
培养箱:37℃。
恒温水浴箱。
电炉。
天平。
灭菌平皿。
灭菌刻度吸管。
酒精灯A2 培养基和试剂乳糖胆盐培养液A2.1.1成分蛋白胨20g猪胆盐(或牛、羊胆盐)5g乳糖5g%溴甲酚紫水溶液蒸馏水1000mLA2.1.2 制法将蛋白胨、猪胆盐及乳糖溶解于1000mL蒸馏水中,调整pH到,加入指示剂,充分混匀,分装于内有倒管的试管中。
115℃下灭菌20min。
贮存于冷暗处备用。
三倍浓度乳糖胆盐培养液A2.2.1成分蛋白胨60g猪胆盐(或牛、羊胆盐)15g乳糖15g%溴甲酚紫水溶液蒸馏水1000mLA2.2.2 制法制法同附录A2.1.2。
伊红美兰培养基(EMB培养基)A2.3.1 成分蛋白胨10g乳糖10g磷酸氢二钾2g琼脂20g2%伊红水溶液20mL%美蓝水溶液13mL蒸馏水1000mLA2.3.2 制法将琼脂加到900mL蒸馏水中,加热溶解,然后加入磷酸氢二钾和蛋白胨,混匀使溶解,再加入蒸馏水补足至1000mL,调整pH至~。
趁热用脱脂棉和砂布过滤,再加入乳糖,混匀,定量分装于烧瓶内,115℃灭菌20min。
作为储备培养基贮存于冷暗处备用。
临用时,加热融化储备培养基,待冷至60℃左右,根据烧瓶内培养基的容量,加入一定量的已灭菌的2%伊红水溶液和%美蓝水溶液,充分摇匀(防止产生气泡)。
倾注平皿备用。
乳糖蛋白胨培养液A2.4.1成分蛋白胨10g牛肉膏3g乳糖5g氯化钠5g%溴甲酚紫乙醇溶液1mL蒸馏水1000mLA2.4.2 制法将蛋白胨、牛肉膏、乳糖及氯化钠加热溶解于1000mL蒸馏水中,调整pH到~,加入%溴甲酚紫乙醇溶液1mL,充分混匀,分装于内有倒管的试管中。
115℃下灭菌20min。
贮存于冷暗处备用。
革兰氏染色液A2.5.1 结晶紫染色液结晶紫1g95%乙醇溶液20mL1%草酸铵水溶液1000mL将结晶紫溶于乙醇中,然后与草酸铵水溶液混合。
