直接碘量法测定维生素c含量
直接碘量法测定药片中维生素C的含量

直接碘量法测定药片中维生素C的含量11化学曾凯平11218022一实验目的1.掌握碘标准溶液的配制注意事项。
2. 通过维生素C的测定了解直接碘量法的过程。
二实验原理维生素C又叫抗坏血酸,分子式C6H4O6。
由于分子中的烯二醇基具有还原性,能被I2定量地氧化成二酮基,其反应式为:碱性条件下可使反应向右进行完全,但因维生素C还原性很强,在碱性溶液中尤其易被空气氧化,在酸性介质中较为稳定,故反应应在稀酸(如稀乙酸、稀硫酸或偏磷酸)溶液中进行,并在样品溶于稀酸后,立即用碘标准溶液进行滴定。
由于碘的挥发性和腐蚀性,不宜在分析天平上直接称取,需采用间接配制法;通常用基准As2O3对I2溶液进行标定。
As2O3不溶于水,溶于NaOH:As2O3+6NaOH═2Na3AsO3+3H2O由于滴定不能在强碱性溶液中进行,需加H2SO4中和过量的NaOH,并加入NaHCO3使溶液的pH=8。
I2与亚砷酸之间的反应为:AsO32-+I2+H2O═AsO43-+2I-+2H+三器皿和试剂酸式滴定管;NaHCO3、KI、I2(以上为AR),As2O3(于105 C 干燥至恒重),6mol·L-1NaOH,0.5mol·L-1H2SO4,10%HAc,1%淀粉溶液,维生素C片剂。
四实验步骤1. 0.1mol·L-1I2标准溶液的配制称取10.8gKI,溶于10mL蒸馏水中,再用表面皿称取I2约6.5g,溶于上述KI溶液,加1滴浓盐酸,加水稀释至300mL,摇匀,用玻璃漏斗过滤,贮存于棕色试剂瓶中并置于暗处。
2.0.1mol·L-1I2标准溶液的标定准确称取基准As2O30.15g,加6mol·L-1NaOH溶液10mL,微热使溶解,加水20mL,加甲基橙指示剂1滴,加0.5mol·L-1H2SO4试液至溶液由黄色变为粉红,再加NaHCO32g、水30mL、淀粉指示剂2mL,用碘标准溶液滴定至蓝色,半分钟内不褪色,计算I2的浓度。
碘量法测维生素C含量

I2 溶液的标定用Na2S2O3标准溶液: 基本反应式:2S2O32-+I2=S4O62-+2I-
I2溶液(0.05mol/L): Na2S2O3标准溶液(0.01mol/L) 淀粉溶液(2g/L) HAc(1+1) 固体Vc样品(维生素片剂) 重铬酸钾(A.R) KI溶液(约200g/L)
维生素C含量的测定:
Na2S2O3标准溶液浓度:
实验序号 记录项目 M药片质量/g V消耗I2体积/ml ω维C含量/% ω维C平均含量/% 1 2
I2标准溶液的浓度:
3
1. 配制I2标准溶液时,为什么要加过量KI?可否 将称得的I2和KI一起加水至一定体积? 2 .溶解样品时,为什么要用新煮沸并冷却的蒸馏 水? 3.加醋酸的目的是什么?
碱性条件下可使反应向右进行完全,但因维生素 C还原性很强,在碱性溶液中尤其易被空气氧化, 在酸性介质中较为稳定,但是在强酸性溶液中I也易被氧化。 故反应应在稀酸(pH为3—4)(如稀乙酸、稀 硫酸或偏磷酸)溶液中进行,并在样品溶于稀酸 后,立即用碘标准溶液进行滴定。
由于碘的挥发性和腐蚀性,不宜在分析天平上直 接称取,需采用间接配制法;用Na2S2O3标准溶 液标定I2 溶液。 标定Na2S2O3溶液: 6I-+Cr2O72-+14H+=2Cr3++3I2+7H2O 2S2O32-+I2=S4O62-+2I- n(K2C2O7): 6n(Na2S2O3)=1:6
I2微溶于水而易溶于KI溶液,但在稀的KI溶液中溶 解得很慢,所以配制I2溶液时不能过早加水稀释,应 先将I2和KI混合,用少量水充分研磨,溶解完全后 再加水稀释。 I与KI间存在如下平衡:I2+I- =I3- 游离I2容易挥发损失,这是影响碘溶液稳定性的原因 之一。因此溶液中应维持适当过量的I-离子 ,以减 少I2的挥发。空气能氧化I-离子,引起I2浓度增加: 4 I-+O2+4H+ =2I2+2H2O 此氧化作用缓慢,但能为光,热,及酸的作用而加 速,因此I2溶液应处于棕色瓶中置冷暗处保存。I2能 缓慢腐蚀橡胶和其他有机物,所以I应避免与这类物 质接触。
直接碘量法测定维生素c含量[整理版]
![直接碘量法测定维生素c含量[整理版]](https://img.taocdn.com/s3/m/448c533b5022aaea988f0f26.png)
直接碘量法测定维生素c含量[整理版] 一(实验目的1(掌握碘标准溶液的配制和标定方法;2(了解直接碘量法测定维生素C的原理和方法。
二(实验原理,1维生素C(Vc)又称抗坏血酸,分子式,分子量。
Vc具有还原性,可CHO176.1232/g•mol686被定量氧化,因而可用标准溶液直接滴定。
其滴定反应式为:。
II22由于Vc的还原性很强,较易被溶液和空气中的氧氧化,在碱性介质中这种氧化作用更强,因此滴定,宜在酸性介质中进行,以减少副反应的发生。
考虑到在强酸性溶液中也易被氧化,故一般选在pH=3~4I的弱酸性溶液中进行滴定。
三(主要试剂,1KI0.05mol•L 1(溶液(约):称取3.3g和5g,置于研钵中,加少量水,在通风橱中研磨。
待 III222全部溶解后,将溶液转入棕色试剂瓶中,加水稀释至250mL,充分摇匀,放阴暗处保存。
,10.1127mol•LNaSO 2(标准溶液() 223,12mol•L 3(HAc()4(淀粉溶液5(维生素C片剂6(KI溶液四(实验步骤I 1(溶液的标定 2NaSO 用移液管移取20.00mL标准溶液于250mL锥形瓶中,加40mL蒸馏水,4mL淀粉溶液,223,1然后用溶液滴定至溶液呈浅蓝色,30s内不褪色即为终点。
平行标定3份,计算。
Ic(I)/mol•L222(维生素C片剂中Vc含量的测定准确称取2片维生素C药片,置于250mL锥形瓶中,加入100mL新煮沸过并冷却的蒸馏水,10mLHAc溶液和5mL淀粉溶液,立即用标准溶液滴定至出现稳定的浅蓝色,且在30s内不褪色即为终点,记下I2消耗的。
平行滴定3份,计算试样中的Vc的质量分数。
V(I)/mL2五(数据记录与处理1(溶液的标定 I21 2 3 项目序号,1 c(NaSO)/mol•L0.1127 223V(NaSO)/mL20.00 223V(I)/mL23.39 23.35 23.33 2,1 0.04818 0.04827 0.04831 c(I)/mol•L2,1平均0.04825 c(I)/mol•L2dr/% 0.15 0.04 0.120.10 dr/%2(维生素C片剂中Vc含量的测定1 2 3 项目序号,1 0.04825 c(I)/mol•L2m(药片)/g0.2408 0.2395 0.2377V(I)/mL23.92 23.82 23.67 2,(Vc)/%84.41 84.52 84.62平均 ,(Vc)/%84.52dr/% 0.13 0 0.120.08 dr/%六(实验总结,1,(Vc),84.52%标定得,测得。
实验五 水果维生素c含量的测定 ---直接碘量法

(二)试剂
0.02 mol/L碘溶液、氯化氢的质量分数为2%的盐酸、可溶 性淀粉的质量分数为0.5%的溶液、蒸馏水、维生素C、碘 酸钾、碘化钾;
(三)器械
解剖刀、小烧杯、试管、广口瓶、量筒、玻璃棒、纱布、
研钵、pH试纸、标签纸、试管刷、100ml容量瓶、0.5、2、
2020/75/2m7 l移液管、滴定管、漏斗、分析天平。
2020/7/27
6
(二)样品试液的制备
将果蔬样品洗净,用纱布拭干其外部所附着的水分, 若样品清洁可不必洗涤。样品若为大型果蔬,先纵切 为4~8等分,取其20~30g为一份,除去不能食用部分, 切碎。若为大型叶菜,沿中脉切分为二分,取其一分 切碎,称取20g作分析用;
将称取的样品放研钵中,加2%的盐酸5~10ml,研磨 至呈浆状。小心无损地移研钵中样品于100ml容量瓶 中,研钵用2%盐酸液冲洗后,亦倒入量瓶中,并加 2%盐酸至100ml,充分混合。用清洁干燥二层纱布过 滤入干燥的烧杯中,滤液作测定用。
2020/7/27
7
(三)样品液的测定
在50ml的烧杯中,用移液管注入1%的KI0.5ml, 0.5%淀粉液2ml,以及上述制得的试液5ml;再加 蒸馏水至总体积10ml(加2.5毫升);
用0.001N KIO3液滴定,要一滴一滴加入,并时时 摇动烧杯,至微蓝色不褪为终点(一分钟不褪为 止);
5
四、操作方法
(一)试剂制备
1. 0.5%淀粉液:称取可溶性淀粉0.5g,用蒸馏水 调成浆状,注入100ml蒸馏水,煮沸至透明状, 冷后用棉花过滤;
2.0.001N KIO3液:精确称取KIO3 0.3568g(KIO3 预先在102℃烘2小时,在干燥器中冷却备用), 准确配成1000ml,得到0.01N KIO3液。再稀释10 倍即为0.001N。
维生素C的含量测定(直接碘量法)
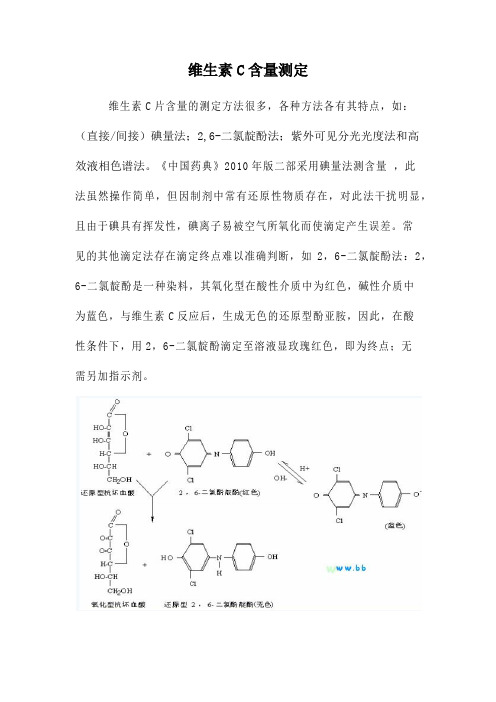
维生素C含量测定维生素C片含量的测定方法很多,各种方法各有其特点,如:(直接/间接)碘量法;2,6-二氯靛酚法;紫外可见分光光度法和高效液相色谱法。
《中国药典》2010年版二部采用碘量法测含量,此法虽然操作简单,但因制剂中常有还原性物质存在,对此法干扰明显,且由于碘具有挥发性,碘离子易被空气所氧化而使滴定产生误差。
常见的其他滴定法存在滴定终点难以准确判断,如2,6-二氯靛酚法:2,6-二氯靛酚是一种染料,其氧化型在酸性介质中为红色,碱性介质中为蓝色,与维生素C反应后,生成无色的还原型酚亚胺,因此,在酸性条件下,用2,6-二氯靛酚滴定至溶液显玫瑰红色,即为终点;无需另加指示剂。
分光光度法运用维生素C的旋光性能进行含量测定,但操作费时,而高效液相色谱法是目前发展较为迅速的一种方法,灵敏度高,选择性好,是一个准确高效的测定维生素C含量的方法。
我们主要介绍的是直接碘量法。
直接碘量法一.实验原理维生素C是人体重要的维生素之一,它影响胶元蛋白的形成,参与人体多种氧化-还原反应,并且有解毒作用。
人体不能自身制造维生素C,所以人体必须不断地从食物中摄入维生素C,通常还需储藏能维持一个月左右的维生素C。
缺乏时会产生坏血病,故又称抗坏血酸。
维生素C属水溶性维生素,分子式C6H8O6。
分子中的烯二醇基具有还原性,能被I2定量地氧化成二酮基,因而可用I2标准溶液直接测定。
简写为:C6H8O6+I2= C6H6O6+2HI使用淀粉作为指示剂,用直接碘量法可测定药片、注射液、饮料、蔬菜、水果中维生素C的含量。
由于维生素C的还原性很强,较容易被溶液和空气中的氧氧化,在碱性介质中这种氧化作用更强,因此滴定宜在酸性介质中进行,以减少副反应的发生。
考虑到I - 在强酸性中也易被氧化,故一般选在pH为3~4的弱酸性溶液中进行滴定。
由于碘具有挥发性,碘离子易被空气所氧化而使滴定产生误差;又由于碘的挥发性和腐蚀性,使碘标准滴定溶液的配制及标定比较麻烦。
直接碘量法测定维生素c含量

直接碘量法测定维生素c含量
维生素C,也被称为抗坏血酸,是一种水溶性维生素。
它在许多生物体内起着重要的生理作用,并且对人体有益。
维生素C含量测定是基于一种叫做碘量法的化学方法。
该方法利用碘酸钾溶液与维生素C反应的化学性质,通过了解反应后剩余的碘酸钾的含量来测定维生素C含量。
碘量法测定维生素C的过程如下:
准备样品:将要测定的样品加入到3%的浓磷酸中,并将其加热到约80℃,然后再冷却。
制备碘酸钾溶液:将20克的碘酸钾加入到1000毫升的蒸馏水中,并充分搅拌,以制备出0.1N的碘酸钾溶液。
测定过程:将取出的样品加入到定容瓶中,加入足够的蒸馏水,直至瓶子充满为止。
然后取出1毫升的样品溶液,并将其加入到滴定瓶中。
加入几滴淀粉溶液。
此时,溶液会变成淡蓝色。
准备滴定剂:将制备好的碘酸钾溶液滴加到另一个滴定瓶中,并加入适量的酒精。
通过滴加,将滴定剂加入到样品溶液中,直至溶液变成深蓝色。
读取数据:记录滴定剂滴入样品溶液的次数,并且根据已知的滴定剂浓度计算出维生素C的含量。
利用碘量法可以准确地测定含有维生素C的食物以及药品的维生素C含量。
然而,由于该测量方法需要使用化学试剂和复杂的实验过程,所以在实践中不太实用。
为了更加方便测量维生素C的含量,也出现了其他测量方法,例如高效液相色谱法和光谱法。
无论使用哪种方法测量维生素C的含量,都可以帮助人们了解他们摄入的营养成分,以及制定更加健康的膳食计划。
维生素c含量测定碘量法实验报告

维生素c含量测定碘量法实验报告
实验目的:
本实验旨在通过维生素c含量测定碘量法,掌握测定维生素c的方法和技能,同时加深对维生素c的认识。
实验原理:
碘量法是一种常用的测定维生素c含量的方法。
其原理是利用维生素c在氯化亚铁和碘酸钾的存在下,被氧化为脱氢抗坏血酸,然后用碘量法测定反应结束时残余的碘量,从而计算出维生素c的含量。
实验步骤:
1.将维生素c样品溶解于少量水中,加入5%的氯化亚铁溶液,使其完全还原。
2.加入2ml的碘酸钾溶液,并用0.1mol/L的氢氧化钠溶液调节溶液pH值为2-3。
3.用0.1mol/L的硫酸滴定溶液滴定反应液,直至溶液呈浅黄色,再加入几滴淀粉指示剂,继续滴定至溶液呈蓝色。
4.测量反应液的体积,计算出维生素c的含量。
实验结果:
在本实验中,我们测定了三个不同维生素c含量的样品,分别为0.1g、0.2g和0.3g。
在滴定过程中,我们发现反应液颜色会在滴定末几滴发生明显变化,这时需谨慎滴加滴定液,避免过度滴定。
最终的实验结果表明,三个样品的维生素c含量分别为0.096g、0.192g和0.284g。
实验结论:
通过本实验,我们掌握了维生素c含量测定碘量法的方法和技能,同时加深了对维生素c的认识。
实验结果表明,维生素c含量与样品添加量成正比,可以通过碘量法准确测定。
实验注意事项:
1.在实验过程中,应注意安全,避免溶液溅出,避免接触皮肤和眼睛。
2.在滴定时,应注意滴定液的速度,避免过度滴定。
3.实验前应检查所用试剂的质量和纯度,避免影响实验结果。
4.实验后应及时清洗实验器材,保持实验室卫生。
维生素C药片中Vc含量的测定(碘量法)

1、配制2mol/L醋酸溶液。量取6mL冰醋酸稀释至50mL
2、维生素C的提取。取10片药剂,准确称量其质量。研成细粉末并混均匀,准确称取粉末约0.6g(三份)。置于锥形瓶中,操作一定要快,加50mL蒸馏水稀释,马上进行下一步滴定。(若颜色太深可加蒸馏水稀释)
3、维生素C的测定。向锥形瓶中加入10mL2mol/LHAc溶液,2mL淀粉溶液,立即用标准碘液(酸式滴定管)进行滴定至溶液刚好呈现蓝色,30s内不褪色即为终点.记下体积,平行滴定三次,,计算Vc的含量。
C% %
M(药片)=176.13g/mol
六、注意事项
1、实验中所用指示剂为淀粉溶液。I2与淀粉形成蓝色的加合物,灵敏度很高。温度升高,灵敏度反而下降。淀粉指示剂要在接近终点时加入。
2、用心煮沸并冷却的蒸馏水:否则Na2S2O3因氧气和二氧化碳和微生物的作用而分解,使滴定时消耗Na2S2O3溶液的体积偏大。
2
3
V(I2) / mL
V(Na2S2O3) 初读数/ mL
V(Na2S2O3) 终读数/ mL
V(Na2S2O3) / mL
c (I2)=0.5×C(Na2S2O3)×25.00/V(I2)
表三:维生素C药片Vc含量的测定
1
2
3
m(药片)/ g
V(I2) 初读数/ mL
V(I2) 终读数/ mL
V(I2) / mL
Na2S2O3标定时有:n(K2C2O7): n(Na2S2O3)=1:6
三、实验药品及仪器
实验药品和试剂:
I2分析纯KI溶液100g·L-1Na2S2O3·5H2O溶液0.0170mol.L-1K2C2O7溶液淀粉指示剂5 g·L-1Na2CO3固体 HCl溶液 6mol.L-1冰醋酸维生素C药片
维生素C的含量测定

加淀粉指示
滴定 液1ml
精密量取续滤液50ml
五、实验结果
1、 计算本品含维生素C标示量的百分含量。
2、 计算相对偏差。 备注: 本品含维生素C应为标示量的93.0%-107.0%
五、注意事项
1. 使用减重法进行称样。 2. 使用滴定管前要进行试漏。 3. 滴定剩余的碘滴定液要放回回收瓶,禁 止直接放到水槽。
3. 取上述混合液适量使维生素C溶解并 转移至100ml量瓶,用混合液稀释至刻度, 摇匀,迅速滤过。
4. 精密量取续滤液50ml,淀粉指示液1ml, 用碘滴定液(0.5mol/L)滴定,至溶液显蓝 色并持续30秒钟不褪。
备注: 平行操作(即测二份供试品,双样单平行)
(二)操作流程
称样→50ml烧杯→100ml量瓶→过滤 混合液
2、设备:电子天平
3、试剂:碘滴定液(0.5mol\L) 淀粉指示液、稀醋酸、蒸馏水
4、样品:维生素C片
四、实验过程
(一)操作步骤 1. 取本品20片,精密称定,研细,精
密称取适量(相当于维生素C 0.2g)置 50ml烧杯中。
2. 量取稀醋酸10ml置200ml烧杯中, 加新沸过冷水100ml。
2、化学反应式
OH
OH
H
OH
CH3COOH H
O
+ O
I2
OH + HI
OO
HOபைடு நூலகம்
OH
O
O
去氢抗坏血酸
3、 计算公式
维生素C标示量%= VTF10-3W 100% ms
Rd A B 100% AB
三、实验器材
1、仪器:称量瓶(1个)、100ml容量瓶 (2个)、50ml移液管(1支)、洗耳球(1 个)、棕色酸式滴定管(1个)、锥形瓶(3 个)、漏斗(2个)、100ml量筒(1个)、 10ml量杯(1个)、烧杯(3个)、研钵、滤纸。
碘量法测定维生素C含量

3、用Na2S2O3标准溶液标定I2溶液 分别移取25.00mL Na2S2O3 溶液3份,分别依次加
入50mL水, 2mL淀粉溶液,用I2溶液滴定至稳定的蓝色 不褪,记下I2溶液的体积,计算I2溶液的浓度。 4、维生素C片中抗坏血酸含量的测定
将准确称取好的维生素C片约0.2克置于250mL的锥 形 瓶 中 , 加 入 煮 沸 过 的 冷 却 蒸 馏 水 50mL , 立 即 加 入 10ml 2mol/L HAc,加入3ml淀粉立即用I2标准溶液滴定 呈现稳定的蓝色。记下消耗I2标准溶液的体积,计算 Vc含量。(平行三份)
五 实验数据的记录与处理
1. Na2S2O3 溶液的标定
项目
编号
Ⅰ
Na2S2O3标准溶液标定I2溶液
Ⅱ
Ⅲ
m1/g
m1/g
m(K2Cr2O7)/g
V(Na2S2O3)/mL
C(Na2S2O3)/mol.L-1
平均C(Na2S2O3)/mol.L-1
相对平均偏差/%
V(Na2S2O3)/mL V(II2溶液
1 c( 2 I2 ) 0.10
mol/L
2. I2标准溶液 0.01 mol/L
3. As2O3基准物质 于105℃干燥2h
4. Na2S2O3标准溶液 0.01 mol/L
5. 淀粉溶液 5g/L
6. 醋酸 2 mol/L
7. NaHCO3 固体. 9. NaOH溶液 6 mol/L
七、参考文献
[1] 陈荣三等.无机及分析化学(第四版).高等教育出版社. [2] 分析化学实验(第三版).武汉大学编.高等教育出版 社.1994 [3] 基础分析化学实验(第二版).北京大学出版社,1998
直接碘量法测定维生素C的含量

实验四直接碘量法测定维生素C的含量一、实验目的1.掌握碘标准溶液的配制与标定方法。
2.了解直接碘量法的操作步骤及注意事项。
3.掌握直接碘量法的基本操作。
二、实验原理电对电位低的较强还原性物质,可用碘标准溶液直接滴定,这种滴定方法,称为直接碘量法。
维生素C(C6H8O6)又称抗坏血酸,其分子中的烯二醇基具有较强的还原性,能被I2定量氧化成二酮基,所以可用直接碘量法测定其含量。
其反应式如下:从反应式可知,在碱性条件下,有利于反应向右进行。
但由于维生素C的还原性很强,即使在弱酸性条件下,此反应也能进行得相当完全。
在中性或碱性条件下,维生素C易被空气中的O2氧化而产生误差,尤其在碱性条件下,误差更大。
故该滴定反应在酸性溶液中进行,以减慢副反应的速度。
三、实验器材、药品器材:分析天平,酸式滴定管(25mL,棕色),吸量管(2mL),量筒(15mL、5mL),锥形瓶(250m1)。
药品:维生素C注射液(20mL 2.5g),I2标准溶液(0.05mol·L-1),稀醋酸,丙酮,淀粉指示剂。
四、实验操作步骤1、I2标准溶液(0.05mol·L-1)的配制取KI 10.8g于小烧杯中,加水约15mL,搅拌使其溶解。
再取I2 3.9g,加入上述KI溶液中,搅拌至I2完全溶解后,加盐酸1滴,转移至棕色瓶中,用蒸馏水稀释至300mL,摇匀,用垂熔玻璃滤器过滤。
2、I2标准溶液(0.05mol·L-1)的标定精密称取在105℃干燥至恒重的基准物质As2O33份,每份在0.1080~0.1320g之间,置于3个锥形瓶中,各加NaOH溶液(1mol·L-1)4.00mL使溶解,加蒸馏水20.00mL与酚酞指示剂1滴,滴加H2SO4溶液(1mol·L-1)至粉红色褪去,再加NaHCO3 2g,蒸馏水30.00mL及淀粉指示剂2mL,用待标定的I2标准溶液滴定至溶液显浅蓝紫色,即为终点,记录所消耗碘标准溶液的体积。
碘量法测VC

直接碘量法测VC一.实验目的1.掌握碘标准溶液的配制和标定方法;2.了解直接碘量法测定维生素C 的原理和方法。
二.实验原理维生素C (Vc )又称抗坏血酸,分子式686O H C ,分子量1mol •176.1232/g 。
Vc 具有还原性,可被2I 定量氧化,因而可用2I 标准溶液直接滴定。
其滴定反应式为:。
由于Vc 的还原性很强,较易被溶液和空气中的氧氧化,在碱性介质中这种氧化作用更强,因此滴定宜在酸性介质中进行,以减少副反应的发生。
考虑到-I 在强酸性溶液中也易被氧化,故一般选在pH=3~4的弱酸性溶液中进行滴定。
使用淀粉作为指示剂,用直接碘量法可测定水果中维生素C 的含量。
I 2标准溶液采用间接配制法获得,用Na 2S 2O 3标准溶液标定,反应如下: 2S 2O 32-+I 2 = S 4O 62-+2I-器材和药品1.器材 天平(0.1mg ),碱式滴定管(50 mL)、酸式滴定管(50mL ),碘量瓶(250mL ),移液管(20mL )锥形瓶(250ml )、量筒、棕色瓶(250mL )。
从此以下未整理2.药品 果汁、K 2Cr 2O 7(基准试剂),Na 2S 2O 3(0.02mol·L-1),I 2(0.01 mol·L-1),KI (20%)、HCl,(6mol·L-1),HAc (2mol·L-1),淀粉指示剂(0.5%)。
Na2CO3固体 以上试剂未说明均为分析纯,水为蒸馏水所需试剂的用量及配制方法:1、 0.1 mol·L-1Na 2S 2O 3标准溶液的配制称取25g Na 2S 2O 3·5H 2O ,溶于1000mL 新煮沸并冷却的蒸馏水中,加入0.2gNa2CO3使溶液呈碱性,以防止Na 2S 2O 3的分解,保存于棕色瓶中,放置10天后过滤,再标定.放置长时间后,再用前应重新标定。
2、K 2Cr 2O 7标准溶液的配制准确称取基准试剂K 2Cr2O 7 0.26—0.28g 于小烧杯中,加入少量蒸馏水溶解后,移入200ml 容量瓶中,用蒸馏水稀释至刻度,摇匀.3、0.1 mol·L-1Na2S2O3标准溶液的标定用移液管吸取上述标准溶液20. 00ml 于250ml 碘瓶中,加8ml 6 mol·L HCl,5-8ml 20%KI 溶液,盖上表面皿,在暗处放5分钟后,加100ml 水,立即以用待标定的Na2S2O3溶液滴定至淡黄色,再加入2ml 0.5%淀粉溶液, 继续滴至溶液呈亮绿色为终点.平行滴定3次。
试验16维生素C片剂中VC含量的测定直接碘量法

实验16 维生素C片剂中VC含量的测定(直接碘量法)一、实验目的1、掌握碘标准溶液的配制和标定方法。
2、了解直接碘量法测定抗坏血酸的原理和方法。
二、实验原理维生素C(Vc)又称抗坏血酸,属于水溶性维生素。
分子式为C6H8O6。
它广泛存在于水果和蔬菜中,辣椒、山楂和番茄中含量尤为丰富。
Vc具有许多对人体健康有益的功能,临床上用于坏血病的预防和治疗。
维生素属外源性维生素,人体不能自身合成,必须从食物中摄取。
Vc具有还原性,可被I2定量氧化,因而可用I2标准溶液直接滴定。
其滴定反应式为:由于反应速率较快,因此可用I2 标准溶液直接滴定药片、注射液、饮料、蔬菜、水果等中的Vc含量。
由于Vc的还原性很强,较易被溶液和空气中的氧氧化,在碱性介质中这种氧化作用更强,因此滴定宜在酸性介质中进行,以减少副反应的发生。
考虑到I- 在强酸性溶液中也易被氧化,故一般选在pH=3~4的弱酸性溶液中进行滴定。
三、仪器试剂1.仪器:50 mL酸式滴定管一支;400 mL烧杯一个;250 mL锥形瓶三个;10 mL、25 mL 移液管各一支;滴管一支;吸耳球一个;10 mL,50 mL量筒各一个;分析天平一个;托盘天平一个。
2.试剂:I2标准溶液(0.05mol·L-1);Na2S2O3标准溶液(0.01mol·L-1);淀粉溶液(5.0g·L-1);醋酸(2mol·L-1);维生素C片剂。
四、实验步骤1. I2溶液的标定用移液管移取25.00 mL Na2S2O3标准溶液于250 mL锥形瓶中,加50 mL蒸馏水,5mL0.2%淀粉溶液,然后用I2溶液滴定至溶液呈浅蓝色,30 s内不褪色即为终点。
平行标定三份,计算I2溶液的浓度。
2. 维生素C片剂中VC含量的测定准确称取约0.2 g研碎了的维生素C药片,置于250 mL锥形瓶中,加入100 mL新煮沸过并冷却的蒸馏水,10 mL2 mol·L-1 HAc溶液和5 mL0.2%淀粉溶液,立即用I2标准溶液滴定至出现稳定的浅蓝色,且在30 s内不褪色即为终点,记下消耗的I2溶液体积。
碘量法测定维生素C

维生素C含量的测定

浓度 1 2
体积 3
2、维生素c含量的测定记录
实验编号
2溶液浓度/mol
1
2
3
/m3
维生素c的质量/g
滴定前读数/ml 滴定后读数/ml 滴定用I2溶液体积 /cm3
维生素c的含量%
维生素c的平均含 量%
维生素C含量的测定 ——直接碘量法
维生素C 定义:显示抗坏血酸生物活性的 化合物的通称,是一种水溶性维 生素,水果和蔬菜中含量丰富。 在氧化还原代谢反应中起调节作 用,缺乏它可引起坏血病。
键线式
实验目的 (1)了解测定维生素C的实验方法与原理 (2)掌握碘标准溶液的配制与标定的方法。 (3)掌握直接碘量法测定维生素C的原理、方
I2是中等强度的氧化剂,可以氧化许多具有还 原性的物质。维生素C分子中含有还原性的二烯醇 基,能被I2定量氧化成二酮基:
而且反应速率较快,所以可用I2标准溶液直接滴定 的方法,测定出样品中维生素C的含量。直接碘 量法适用于药片、注射液、蔬菜、水果中维生素 C的含量测定。维生素C易被空气氧化,特别是在 碱性溶液中更易被氧化,所以,在测定中须 加入稀 HAc,使溶液保持足够的酸度,以减少副反应的发 生。
法及其操作。
Ⅱ.实验用品
仪器:酸式滴定管,锥形瓶 试剂:2 mol/L HAc,0.1mol/L Na2S203标准溶液, 0.5%淀粉指示剂 材料:维生素C(s),I2 (s),KI(s)
Ⅲ.实验原理
维生素C(简写为Vc)又称抗坏血酸,是人体重要的 维生素之一,分子式为C6H8O6,在医 mo/L I2标准溶液的配制与标定
配制(由实验室预先做):将3.3 g I2与5 gKI置 于研钵中,在通风柜中加入少量水(切不可多加!) 研磨,待I2全部溶解后,将溶液转入棕色瓶中,加水 稀释至250 mL,摇匀。
直接碘量法测定绿茶中维生素C含量

直接碘量法测定绿茶中维生素C含量黄素梅(广西师范大学化学化工学院,桂林541004)摘要本文采用直接碘量法测定绿茶中维生素C的含量。
绿茶经草酸提取后,用I标准溶液直接滴定。
实2验结果表明:绿茶中维生素C的含量为25.20mg/10g。
采用直接碘量法测定绿茶中的维生素C含量,操作简便,快速。
关键词直接碘量法;绿茶;维生素C绿茶中含有丰富的维生素,其中以维生素C的含量最高,维生素C可作为衡量绿茶品质的一个重要生化指标。
一般绿茶中维生素C含量可达(100mg~250mg)/100g,高级龙井【】1茶(绿茶中的绝品)中的维生素C含量可达360mg/100g。
关于茶叶维生素的研究文献很少,仅20余篇,涉及茶叶维生素分析方法的文献只有10【】1余篇,其中涉及高效液相色谱法,分光光度法,荧光法,但据我了解,未涉及直接碘量法。
本文采用直接碘量法测定绿茶中维生素C的含量,操作简便,快速。
1 原理维生素C(Vc)属于水溶性维生素,它的分子式为CHO,由于分子中的烯二醇基具686有还原性,能被I定量地氧化成二酮基: 21mol维生素C与1mol I定量反应,维生素C的摩尔质量为176.12g/mol。
当溶液中有2淀粉存在,过量的碘遇淀粉变蓝色,指示滴定终点。
由于维生素C的还原性很强,在空气中极易被氧化,尤其是在碱性介质中,测定时采用草酸溶液提取绿茶中的维生素C,使样液呈弱酸性,减少维生素C的副反应。
2 仪器与试剂2.1 仪器碱式滴定管;25mL移液管2.2 试剂 0.05mol/L草酸溶液;0.01mol/LI标准溶液;1%淀粉溶液;绿茶:市售立顿绿2茶3 实验部分3.1 维生素C 提取液的制备准确称取10g绿茶,加入适量0.05mol/L草酸溶液,充分振荡4-5分钟。
过滤,洗涤,滤液转入250mL容量瓶中,用0.05mol/L草酸溶液定容至250mL。
3.2 用直接碘量法滴定绿茶中的维生素C用25mL移液管移取上述提取液于250mL锥形瓶中,加入1 mL淀粉溶液后,立即用0.01mol/LI标准溶液滴定至溶液变色,且30s内不退色,即为滴定终点。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
滴定K2Cr2O7的过程注意事项
(1)控制合适的酸度。溶液的酸度越高反应的速 率就会越快,但是酸度太大时,碘离子容易被空 气氧化,且Na2S2O3溶液分解,所以酸度应该以 0.2-0.4mol/L为宜。 (2)K2Cr2O7与KI的反应速率较慢,所以应将溶 液放在带塞的锥形瓶中,并且应该放在暗处一定 的时间,使二者充分的反应。
• 3)滴定终点的灵敏程度的影响。可能是果汁中 的某些成分影响了终点的显色的灵敏程度,致使 变色较为缓慢。 • 4)滴定的速度过慢,且有可能是摇晃的过于剧 烈,致使滴下的碘有一部分挥发了。从而增加了 碘溶液的消耗量,测得实际浓度存在误差。 • 5)果汁中可能存在一些其他的具有较强的还原 性的物质,在滴定的过程中与碘溶液发生了化学 反应,从而消耗了碘,使得实际测得的Vc的含 量明显地高于理论的值。
胡萝卜 百分含量
mVc 3 C I 2 VI 2 M Vc 1.689 10 2 g
Vc3 %
mVc3 100 g 1000mg 33.5mg /100 g 1 g m胡 / 5 100 g
苹果
mVc 4 C I 2 VI 2 M Vc 7.699 103 g
误差分析
• 所测值与理论含量相差较大,我们认为造成这 种结果可能的原因有: • 1)I2在滴定的过程中始终有挥发,致使原始 标定I2的实际真实浓度和用其测定Vc 的浓度 有较大的不同。 • 2)滴定过程中酸度等条件没有控制好,致使 I2溶液发生了化学反应,从而使其有效的浓度 不断地降低。或是酸度的控制致使反应的终点 受到影响。
27.35
27.40
24.88
24.87
用I2滴定橙子样液
用
量 橙子 V/ml 50.00
I 2 / ml
V前 V后 (ml) (ml)
1.49 31.02
VI2 / ml
29.53
序号 1 2
3
50.00
50.00
1.50
1.43
30.97
30.98
29.47
29.55
用I2滴定橘子样液
用量
序号 1 2 3 橘子 V/ml 50.00 50.00 50.00
VNa2 s2o3 / ml
1.47
1.53
27.73
26.76
26.26
25.23
用I2滴定Na2S2O3
用量
VNa2 s2o3 / ml
I 2 / ml
序号 1 25.00
V前 V后 (ml) (ml) 2.58 27.49 24.91
VI2 / ml
2
3
25.00
25.00
2.47
02.53
(3)胡萝卜,称取41.215g,切成小块,加入 20ml 2%的稀盐酸研磨至糊状,加入250ml 容量瓶中,加2%的稀盐酸定容250ml,然后 用真空泵抽滤,除去大颗粒和杂质,滤液密封 备用。 (4)苹果去皮,称取54.432g,切成小块,加入 20ml 2%的稀盐酸研磨至糊状,加入250ml 容量瓶中,加2%的稀盐酸定容250ml,然后 用真空泵抽滤,除去大颗粒和杂质,滤液密封 备用。
• 5 I2 溶液的标定 • 移取Na2S2O3 溶液25ml三份于锥形瓶中, 各加入25ml的水,5ml的淀粉溶液,用待标 定的碘的标准溶液滴定至稳定的蓝色,30s不 退色,即为终点。计算I2的标准浓度。
制备果蔬样液
(1)橙子去皮,称取109.409g,切成小块,加 入20ml 2%的稀盐酸研磨至糊状,加入 250ml容量瓶中,加2%的稀盐酸定容250ml ,然后用真空泵抽滤,除去大颗粒和杂质,滤 液密封备用。 (2)橘子去皮,称取69.592g,切成小块,加入 20ml 2%的稀盐酸研磨至糊状,加入250ml 容量瓶中,加2%的稀盐酸定容250ml,然后 用真空泵抽滤,除去大颗粒和杂质,滤液密封 备用。
I 2 / ml
V前 V后 (ml) (ml) 1.53 10.45 8.92 1.45 0.43 10.34 10.30 8.89 8.87
VI2 / ml
用I2滴定胡萝卜样液
用量
序号 1 2 3
I 2 / ml 胡萝卜 V 前 V 后 V/ml (ml) (ml) 50.00 0.80 5.58 4.78
• 4 Na2S2O3 溶液的标定 • 移液管移取25.00ml的标准K2Cr2O7溶液于 250ml的锥形瓶中,加固体KI1g和3g 浓盐 酸,充分摇匀,放在暗处5min。 • 然后用50ml蒸馏水稀释,用Na2S2O3滴定到 浅黄绿色,然后加入5ml淀粉溶液,滴定至终 点。记录消耗的体积。计算Na2S2O3溶液浓 度,平行滴定三次。
3、I2浓度
稀释后
C I2
C Na2 S2O3 VNa2 S2O3 2VI 2
0.1008mol / L
C
I2
C I2 4.034 103 mol / L 25
滴定果蔬样液
1、橙子 百分含量 2、橘子 百分含量
mVc1 C I2 VI2 MVc 0.1046 g
(3)KI溶液中不能有碘单质以及碘酸钾。如果KI 的溶液显黄色,或是酸化后加淀粉显蓝色,就应 该用Na2S2O3溶液将其滴定至无色后使用。 (4)滴定前须将溶液稀释,稀释既可以降低酸度 使得I离子被空气的氧化速率减慢又可使 Na2S2O3溶液的分解速率减小,而且稀释后Cr3+ 的绿色减弱,便于观察终点。
维生素C对人体健康的重要作用
• 1、促进骨胶原的生物合成。利于组织创伤口 的更快愈合; • 2、促进氨基酸中酪氨酸和色氨酸的代谢,延 长肌体寿命。 • 3、改善铁、钙和叶酸的利用。 • 4、改善脂肪和类脂特别是胆固醇的代谢,预 防心血管病。 • 5、促进牙齿和骨骼的生长,防止牙床出血。
维生素C对人体健康的重要作用
I 2 / ml
50.00 50.00
0.75 0.74
5.52 5.48
4.77 4.74
用I2滴定苹果样液
用量 苹果 V/ml 50.00
I 2 / ml
序号
1
V前 V后 (ml) (ml) 3.45 5.64 2.19
VI2 / ml
2
3
50.00
50.00
3.72
3.24
5.94
5.39
2.22
1.直接碘量法
【实验目的】
• 1.掌握直接碘量法测定维生素C的原理和方法。 2.了解间接碘量法的原理。 • 3.通过维生素C的含量测定,熟悉直接碘量法 基本原理及操作过程。 • 4.了解日常食用的蔬菜水果中维生素C的含量, 注意饮食质量,提高健康意识。
实验原理
实验原理
• Vc具有还原性,可被I2定量氧化,因而可用I2标 准溶液直接测定.其滴定反应式: • 通过消耗碘溶液的体积及其浓度,计算试样中 维生素C的含量。
Vc 4 %
mVc 4 100 g 1000mg 12.74mg /100 g 1 g m苹 / 5 100 g
百分含量
理论数值与测得数据比较
每100g果蔬中含Vc的值比较 果蔬种类 橙子 标准值 测量值 49mg 橘子 30mg 胡萝卜 没查到 苹果 5mg 12.74mg
105.8mg 48.93mg 33.5mg
2.Байду номын сангаас5
数据处理
1、K2Cr2O7浓度
CK2Cr2O7 m 1.241g /V 1000ml / l 0.0169mol / L M 294.16 g / mol 250ml
2、Na2S2O3浓度
C Na2 S2O3 6CK2Cr2O7 V K2Cr2O7 VNa2 S2O3 0.1004mol / L
实验数据与处理
名称 K2Cr2O7 Na2S2O3 I2 KI
质量/g
1.241
21.155
13.401
13.632
用Na2S2O3滴定 K2Cr2O7 用量
VK2Cr2O7 / ml
Na2 S2O3 / ml
序号
1 2
3
25.00 25.00
25.00
V前 V后 (ml) (ml) 1.32 26.58 25.26
碘量法测定维生素C含量
一.维生素C简介
1,物理性质 2,维生素C对人体健康的重要作用 3,化学性质
维生素C的物理性质
• 六碳多羟基酸性化合物 • 白色针状结晶 • 有酸味, 可溶于水
维生素C对人体健康的重要作用
• 增加免疫力,防感冒及病毒和细菌的感染
• 预防癌症
• 抗过敏 • 减少静脉中血栓的形成 • 天然的抗氧化剂 • 天然的退烧剂
2. K2Cr2O7 溶液的配制
称取1.241g的 K2Cr2O7 基准物质于小烧杯中,加 水溶解后,转移至250.00ml的容量瓶中,加水稀释 到刻度线,定容,摇匀。
• 3 I2
溶液的配制
称取13.632g的I2和21.155gKI,放入 250ml烧杯中,稀释到1000ml,摇匀,置于 无光处保存。
药品试剂及仪器
• 药品:I2 、 KI、Na2S2O3 、 K2Cr2O7 、淀 粉、Hcl、果蔬(橙子、橘子、苹果、胡萝卜) • 仪器:烧杯、容量瓶 (250mL)、量筒、酸式滴 定管、碱式滴定管、胶头滴管、锥形瓶、玻璃 棒、研钵、抽滤装置等
实验步棸
配制溶液
• 1 Na2S2O3 溶液的配置 • 称取13.401g的Na2S2O3 .5H2O(约0.05mol )固体于500ml的棕色试剂瓶中,加入 100ml新煮沸经冷却的蒸馏水,摇动使之溶解 ,等溶解完全后加入0.2gNa2CO3,再加入 400ml的新煮沸经冷却的蒸馏水反复摇匀,放 置于阴暗处。
