第十三章答案
西方经济学课后习题答案-第十三章

西方经济学课后习题答案-第十三章第十三章失业、通货膨胀和经济周期1.西方经济学是如何解释失业的?失业的影响表现在哪些方面?【参考答案】西方经济学家对失业的原因做出了不同的解释。
主要有:(1)古典经济学失业理论以“萨伊定律”为核心,认为供给能够创造需求,不会出现生产过剩,且每一个商品生产者都是理性的,都会尽力扩大生产、销售,这样社会的生产、销售就能达到最高水平,从而实现充分就业。
(2)凯恩斯提出了“非自愿失业”理论,认为有效需求是由消费需求与投资需求构成的,它是决定社会总就业量的关键性因素。
当“有效需求”不足时充分就业就无法实现。
凯恩斯提出边际消费倾向递减、资本边际效率递减和流动性偏好三个基本心理规律,使得经济中消费需求和投资需求不足,从而导致非自愿失业。
(3)新凯恩斯主义经济学以不完全竞争和不完全信息为前提,通过论证工资和价格黏性进而解释非自愿失业存在的原因,认为工资在短期内具有黏性,失业率并不会随劳动需求的变动做出充分调整。
对存在工资黏性的解释主要有劳动工资合同论、隐含合同论、“局内人-局外人”理论和效率工资理论。
(4)现代货币主义的失业理论可以简单归结为“自然失业率”假说,其否认菲利普斯曲线,认为,如果政府用增加货币量来刺激就业,而雇员没有预见到实际收入下降时,就愿意增加劳动供给。
但从长期看,不仅失业没有减少反而物价会持续上涨。
失业对经济和社会的影响主要有:一是给个人和家庭带来物质和精神的负面影响;二是影响社会稳定;三是增加经济运行成本,带来产出损失以及影响社会经济的信心从而加重整个经济的不景气,对经济运行产生不利影响。
2.新凯恩斯主义经济学是如何解释工资黏性的?【参考答案】西方经济学对于工资黏性的原因主要有以下解释:(1)劳动工资合同论。
在一些行业中,由于工会的力量,往往可能签订较有利于雇员的工资合同。
这些合同通常附加工资随生活费上涨而增加,而当经济衰退时工资率并不随之削减的条款。
(2)隐含合同论。
大学物理第十三章(热力学基础)部分习题及答案

第十三章热力学基础一、简答题:1、什么是准静态过程?答案:一热力学系统开始时处于某一平衡态,经过一系列状态变化后到达另一平衡态,若中间过程进行是无限缓慢的,每一个中间态都可近似看作是平衡态,那么系统的这个状态变化的过程称为准静态过程。
2、什么是可逆过程与不可逆过程答案:可逆过程:在系统状态变化过程中,如果逆过程能重复正过程的每一状态,而且不引起其它变化;不可逆过程:在系统状态变化过程中,如果逆过程能不重复正过程的每一状态,或者重复正过程时必然引起其它变化。
3、一系统能否吸收热量,仅使其内能变化? 一系统能否吸收热量,而不使其内能变化?答:可以吸热仅使其内能变化,只要不对外做功。
比如加热固体,吸收的热量全部转换为内能升高温度;4、简述热力学第二定律的两种表述。
答案:开尔文表述:不可能制成一种循环工作的热机,它只从单一热源吸收热量,并使其全部变为有用功而不引起其他变化。
克劳修斯表述:热量不可能自动地由低温物体传向高温物体而不引起其他变化。
5、什么是熵增加原理?答:一切不可逆绝热过程中的熵总是增加的,可逆绝热过程中的熵是不变的。
把这两种情况合并在一起就得到一个利用熵来判别过程是可逆还是不可逆的判据——熵增加原理。
6、什么是卡诺循环? 简述卡诺定理?答案:卡诺循环有4个准静态过程组成,其中两个是等温线,两个是绝热线。
卡诺提出在稳度为T1的热源和稳度为T2的热源之间工作的机器,遵守两条一下结论:(1)在相同的高温热源和低温热源之间工作的任意工作物质的可逆机,都具有相同的效率。
(2)工作在相同的高温热源和低温热源之间的一切不可逆机的效率都不可能大于可逆机的效率。
7、可逆过程必须同时满足哪些条件?答:系统的状态变化是无限缓慢进行的准静态过程,而且在过程进行中没有能量耗散效应。
二、选择题1、对于理想气体的内能,下列说法中正确的是( B ):( A ) 理想气体的内能可以直接测量的。
(B) 理想气体处于一定的状态,就有一定的内能。
答案:第十三章练习题-健康保险与健康管理

第十三章:健康保险与健康管理1.(多选)正确答案:AD,保险行业中应用健康管理,其主要目的是提供健康服务与控制诊疗风险,因此可以将其分为健康指导和诊疗干预两类,2.(单选)正确答案:A,保险责任是健康保险产品中最重要的部分,因其直接关系到最终保险产品的质量3.(单选)正确答案:D,疾病保险是指以约定疾病的发生为给付保险金条件的人身保险。
它具有以下特点:1)保险金的给付条件只依据疾病诊断结果,不与治疗行为的发生或医疗费用相关;2)疾病保险的主要产品类型是重大疾病保险,即当被保险人罹患保险合同中规定的重大疾病或疾病状态并符合其严重程度的定义时,保险公司按照约定保险金额履行给付责任的保险。
3)为了防止被保险人带病投保,降低逆选择的风险,疾病保险合同通常设有等待期。
4.(单选)正确答案:B,为了防止被保险人带病投保,降低逆选择的风险,疾病保险合同通常设有等待期。
5.(单选)正确答案:C,疾病保险的主要产品类型是重大疾病保险。
6.(单选)正确答案:A,医疗保险的保险金的给付条件是医疗行为的发生或医疗费用支出作为依据,与疾病诊断不直接相关。
医疗保险是以医疗行为的发生作为给付保险金的条件。
以财产损失为给付条件的是财产保险,以某种疾病或特定疾病的发生为给付条件的是疾病保险,均不属于医疗保险的范畴。
医疗保险关注的是过程。
7.(单选)正确答案:C,医疗保险的保险金给付条件是以医疗行为的发生或医疗费用支出作为依据,与疾病诊断结果不直接相关。
疾病保险是以约定疾病的发生为给付保险金条件的人身保险。
8.(单选)正确答案:C,失能收入损失保险以约定疾病或意外伤害导致工作能力丧失为给付保险金条件。
9.(单选)正确答案:C,考查健康保险风险控制方法的新进展;记忆型题目。
健康管理是将风险控制由单纯重视事后风险管控延伸到包括事前预防在内的全过程管理,从而达到预防风险、促进被保险人健康的目的,从而控制风险。
10.(单选)正确答案:A,考查健康保险的风险因素,记忆型题目。
第十三章-镇痛药(1)

答案部分一、A1、【正确答案】C【答案解析】吗啡具有碱性,与盐酸可生成稳定的盐肯定是因为吗啡中含有显碱性的基团,ABC三项均显碱性,但吗啡结构中只含有叔胺基团,所以选C。
【该题针对“吗啡”知识点进行考核】【答疑编号100024474】2、【正确答案】E【答案解析】吗啡及其盐类的化学性质不稳定,在光照下即能被空气氧化变质,这与吗啡具有苯酚结构有关。
氧化可生成伪吗啡和N-氧化吗啡。
伪吗啡亦称双吗啡,是吗啡的二聚物,毒性增大。
故本品应避光、密封保存。
【该题针对“吗啡”知识点进行考核】【答疑编号100024469】3、【正确答案】D【答案解析】盐酸吗啡注射液放置过久,颜色变深是由于吗啡具有苯酚结构在光照下即能被空气氧化变质。
【该题针对“吗啡”知识点进行考核】【答疑编号100024464】4、【正确答案】D【答案解析】药效构象是指当药物分子与受体相互作用时,药物与受体互补并结合时的构象。
而相似的电性性质应是由具有相似的物理及化学性质的基团或取代基,形成生物电子等排体所、具备相关、相似或相反的生物活性。
所以本题中吗啡及合成镇痛药具有相同的药效构象,从而具有相同的生物活性。
形成电子等排体则具有相同的电性性质。
【该题针对“吗啡”知识点进行考核】【答疑编号100024412】5、【正确答案】C【答案解析】吗啡结构:【该题针对“吗啡”知识点进行考核】【答疑编号100024409】6、【正确答案】B【答案解析】合成镇痛药按化学结构类型主要可分为:吗啡喃类、苯吗喃类、哌啶类和氨基酮类。
1.吗啡喃类:酒石酸布托啡诺2.苯吗喃类:喷他佐辛3.哌啶类:哌替啶、舒芬太尼、阿芬太尼4.氨基酮类:美沙酮、右丙氧芬【该题针对“其他镇痛药”知识点进行考核】【答疑编号100024480】7、【正确答案】C【答案解析】合成镇痛药按化学结构类型主要可分为:吗啡喃类、苯吗喃类、哌啶类和氨基酮类。
1.吗啡喃类:酒石酸布托啡诺2.苯吗喃类:喷他佐辛3.哌啶类:哌替啶、舒芬太尼、阿芬太尼4.氨基酮类:美沙酮、右丙氧芬【该题针对“其他镇痛药”知识点进行考核】【答疑编号100024458】8、【正确答案】B【答案解析】合成镇痛药按化学结构类型主要可分为:吗啡喃类、苯吗喃类、哌啶类和氨基酮类。
第13章责任会计习题答案

第十三章 责任会计
1、解:(1)投资利润率=营业利润/营业资产=50
5=10% (2)资产周转率=销售收入/营业资产=50
80=1.6 (3)剩余收益=营业利润-营业资产×最低投资报酬率=5-50×8%=1(万元)
2、解:(1)甲部门:
投资利润率=营业利润/营业资产=100
18=18% 剩余收益=营业利润-营业资产×最低投资报酬率=18-100×12%=6(万元)
乙部门:
投资利润率=营业利润/营业资产=300
51=17% 剩余收益=营业利润-营业资产×最低投资报酬率=51-300×12%=15(万元) 评价:由于甲乙两部门投资利润率相差很小(1%),此时,以剩余收益作为主要评价指标,乙部门业绩相对优异。
(2)详见教材P266—268
3、解:此题注意:原题丙工厂生产的产品与所需用的A 部件数量关系不清,故只能比较A 部件买卖价格。
A 部件单位成本情况:
单位固定制造费用=300000÷150000=2(元)
单位变动成本=5+2+2=9(元)
单位生产成本=9+2=11(元)
1)定价9元,即以单位变动成本定价,丁工厂(或“卖方”)亏损,不能达成一致。
2)定价11元,即以单位生产成本定价,丁工厂(卖方)无利可图,不能达成一致。
3)定价14元,对双方都有利,丁工厂(卖方)获得3元内部收益(14-11)丙工厂(买方)省1元成本(15-14)。
4)定价15元,等于市场价,买方无利可图,不能达成一致。
5)定价16元,高于市场价15元,买方亏损,不能达成一致。
有机化学课后习题答案第13章
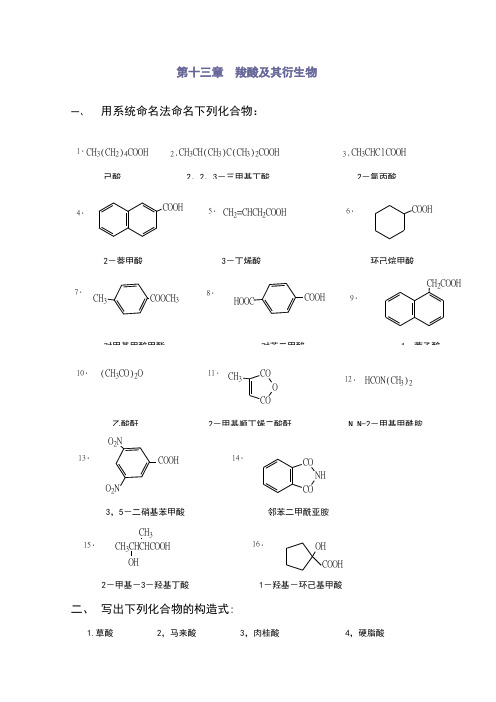
第十三章 羧酸及其衍生物一、 用系统命名法命名下列化合物:1.CH 3(CH 2)4COOH2.CH 3CH(CH 3)C(CH 3)2COOH3.CH 3CHClCOOH4.COOH5.CH 2=CHCH 2COOH6.COOH7.CH 3COOCH 38.HOOCCOOH9.CH 2COOH10.(CH 3CO)2O11.COO CO CH 312.HCON(CH 3)213.COOHO 2NO 2N14.CO NH3,5-二硝基苯甲酸 邻苯二甲酰亚胺15.CH 3CHCHCOOH CH 3OH16.OH COOH2-甲基-3-羟基丁酸 1-羟基-环己基甲酸二、 写出下列化合物的构造式:1.草酸 2,马来酸 3,肉桂酸 4,硬脂酸HOOCCOOHC C H H COOH COOHCH=CHCOOHCH 3(CH 2)16COOH5.α-甲基丙烯酸甲酯 6,邻苯二甲酸酐 7,乙酰苯胺 8,过氧化苯甲酰胺CH 2=C CH 3COOCH 3CO O CONHCOCH3CO C O OO NHC O H 2NCOOC 2H 5CNH C NHO OH 2N CNH 2NHCOO COnCH 2CH O C OCH 3[]n三、写出分子式为C 5H 6O 4的不饱和二元酸的所有异构体(包括顺反异构)的结构式,并指出那些容易生成酸酐:解:有三种异构体:2-戊烯-1,5-二酸;2-甲基-顺丁烯二酸;2-甲基-反丁烯二酸。
其中2-甲基-顺丁烯二酸易于生成酸酐。
CC H COOHCOOH C C H COOHCH 3HOOCCH 3HOOC CH=CHCH 2COOH2-戊烯-1,5-二酸; 2-甲基-顺丁烯二酸; 2-甲基-反丁烯二酸四、比较下列各组化合物的酸性强度:1,醋酸, 丙二酸, 草酸, 苯酚, 甲酸CH 3COOH ,HOOCCOOH HOOCCH 2COOH ,,OH ,HCOOHHOOCCOOHHOOCCH 2COOHHCOOHOHCH 3COOH>>>>2.C 6H 5OH ,CH 3COOH ,F 3CCOOH ,ClCH 2COOH ,C 2H 5OHF 3CCOOHClCH 2COOH CH 3COOH C 6H 5OHC 2H 5OH>>>>3.NO 2COOHCOOHNO 2COOHOHOHNO 2COOHCOOH NO 2COOH OHOH>>>>五、用化学方法区别下列化合物:1.乙醇,乙醛,乙酸2.甲酸,乙酸,丙二酸3.草酸,马来酸,丁二酸4,COOHCOOHCH 2OHOH2-羟基苯甲酸 苯甲酸 苯甲醇5.乙酰氯,乙酸酐,氯乙烷六、写出异丁酸和下列试剂作用的主要产物:1.Br 2/PCH 3CH 3CHCOOH Br /PCH 3CCOOH BrCH 32.LiAlH 4/H 2OCH 3CHCOOH CH 3LiAlH /H 2OCH 3CH 3CHCH 2OH 3.SOCl 2CH 3CH 3CHCOOH2CH 3CH 3CHCOCl4.(CH 3CO)2O/CH 3CH 3CHCOOH (CH 3CO)2O/CH 3CHCO)2CH 3(O +CH 3COOH5.PBr 3CH 3CH 3CHCOOH PBr (CH 3)2CHCOBr6.CH 3CH 2OH/H 2SO 4CH 3CH 3CHCOOH CH 3CH 2OH/H 2SO 4(CH 3)2CHCOOC 2H 57.NH 3/CH 3CH 3CHCOOHNH/(CH 3)2CHCONH 2七、分离下列混合物:CH 3CH 2COCH 2CH 3,CH 3CH 2CH 2CHO ,CH 3CH 2CH 2CH 2OH ,CH 3CH 2CH 2COOHCH 3CH 2CH 2COOH CH 3CH 2CH 2CH 2OH CH 3CH 2CH 2CHO CH 3CH 2COCH 2CH 3NaOHaqCH 2CH 2COONaCH 3CH 2CH 2COOHCH 3CH 2CH 2CH 2OH CH 3CH 2CH 2CHO CH 3CH 2COCH 2CH 3CH 3CH 2CH 2CHSO 3NaOHH +,H OCH 3CH 2CH 2CHOCH 3CH 2COCH 2CH 3NH 23NHOHCH 3CH 2CCH 2CH 3NNHOHHClCH 3CH 2COCH 2CH 3CH 3CH 2CH 2CH 2OH八、写出下列化合物加热后生成的主要产物:1, 1,2-甲基-2-羟基丙酸2, 2,β-羟基丁酸3, 3,β-甲基-γ-羟基戊酸 4, 4,δ-羟基戊酸5, 5,乙二酸九、完成下列各反应式(写出主要产物或主要试剂)1.CH 3CH 2CN (A)H 2O,H +CH 3CH 2COOHCH 3CH 2COCl(B)SOCl2(G)H 2,Pd/BaSO 4CH 3CH 2CHO2CONH 2P 2O 5(C)NH 3NaOBr,NaOH CH 3CH 2NH 22.C=O1.C 2H 5MgBr 2H 3O OH C 2H 5PBr 31.Mg,(C H )2O 2CO 2,H 3OC 2H 5COOH3.ClC ClO2NH 3H 2NC NH 2OH 2N CNH 2OH 2NC ONHC NH 2O4.C=O24OH CNH O +OH COOHOO OC O C十、完成下列转变:1.CH 3CH 2COOH CH 3CH 2CH 2COOHCH 3CH 2COOH CH 3CH 2CH 2OHPBr CH 3CH 2CH 2BrCH 3CH 2CH 2CN H O +CH 3CH 2CH 2COOH2.CH 3CH 2CH 2COH CH 3CH 2COOHCH 3CH 2CH 2COOH 2CH 3CH 2CHCOOHCl-OHCH 3CH 2CHCOOHOHKMnO ,H +CH 3CH 2COOH3.2CH 2COOHCH 2COOHC=CH 2+HBrROORCH 2Br25)OCH 2MgBr122,H 3O4.CH 3COCH 2CH 2CBr(CH 3)2CH 3COCH 2CH 2C(CH 3)2COOHCH 3COCH 2CH 2CBr(CH 3)222+CH 3CCH 2CH 2CBr(CH 3)2O OMg,(C 2H 5)OOOCH 3C CH 3CH 2CH 2CMgBrCH 3122.H 3OCH 3COCH 2CH 2C(CH 3)2COOH十一、试写出下列反应的主要产物:6.(R )-2-溴丙酸 + (S)-2-丁醇 H +/⊿C 2H 5HCH 3OO CBr H CH 3H +HCH 3OHCH 3CH 2+CH 3H COOHBr7.CH 3CH 2COONa+CH 3CH 2CH 2COClCH 3CH 2CH 2CO O CCH 2CHCH 3O 8.CH 2CH 2C CO O+2C 2H 5OHC 2H 5OC O CH 2CH 2COC 2H 5O9.CH 3CONH 2+NaOBr-OHCH 3NH 210.CNCONH 2+P 2O 5十二、预测下列化合物在碱性条件下水解反应的速度顺序。
第十三章.细胞分裂与细胞周期

第十三章细胞分裂与细胞周期一、选择题1.人类细胞最普遍的增殖方式是________A.无丝分裂B.有丝分裂C.减数分裂D.多极分裂E.核内分裂2.细胞分裂周期中DNA增加一倍发生在________A.G0期B.G1期C.G2期D.S期E.M期3.细胞分裂时纺锤丝的排列方式和染色体移动与下列哪个结构有关________ A.中心粒B.线粒体C.核糖体D.溶酶体E.过氧化物酶体4.细胞经过一次有丝分裂结果可产生________A.多个相同的子细胞B.多个不同的子细胞C.两个相同的子细胞D.两个不同的子细胞E.一个与母细胞相同的子细胞5.一个卵母细胞经过减数分裂形成几个卵细胞________A.1个B.2个C.3个D.4个E.8个6.有丝分裂后期的特点________A.着丝粒一分为二,染色体向两极移动B.同源染色体分开,向两极移动C.同源染色体配对时,位于赤道面上D.同源染色体交叉互换E.染色单体到达两极7.有丝分裂转变成为减数分裂的关键时间为________ A.G0期B.G1期C.S期D.G2期E.M期8.有丝分裂器是指________A.由微管、微丝、中间纤维构成的复合体B.由基粒、纺锤体、中心粒和染色体构成的复合体C.由纺锤体、中心体和染色体构成的复合体D.由纺锤体、星体、中心粒和染色体构成的复合体E.由纺锤体和中心体构成的复合体9.在S期未得到复制的0.3%的DNA称为________A.A-DNAB.B-DNAC.C-DNAD.mtDNAE.Z一DNA10.具有核增大,DNA含量增加1倍特点的时期是________ A.G1期B.S期C.G2期D.M期E.细胞周期11.细胞处于暂不增殖状态的时期是________A.G1期B.S期C.G2期D.M期E.细胞周期12.同源染色体联会发生在________A.细线期B.偶线期C.粗线期D.双线期E.终变期13.二价体形成发生在________A.细线期B.双线期C.粗线期D.偶线期E.终变期l4.GC含量较高的DNA序列在下列哪个时期复制________A.S期B.G1早期C.G1晚期D.早S期E.晚S期15.从细胞增殖角度看,不再增殖细胞称为________A.G1A态细胞B.G1B态细胞C.G1期细胞D.G2期细胞E.G0期细胞16.在细胞周期中,哪一时期最适合研究染色体的形态结构________ A.间期B.前期C.中期D.后期E.末期17.HeLa细胞周期中,G1和分裂期的时间分别为________A.4小时和12小时B.6小时和8小时C.12小时和4小时D.8小时和1.5小时E.l小时和1小时18.细胞周期的顺序是________A.M期、G1期、S期、G2期B.M期、G1期、G2期、S期C.G1期、G2期、S期、M期D.G1期、S期、M期、G2期E.G1期、S期、G2期、M期19.一般讲,细胞周期各时相中持续时间最短的是________A.G1期B.S期C.G2期D.G0期E.M期20.有丝分裂与无丝分裂的主要区别在于后者________A.不经过染色体的变化,无纺锤丝出现B.经过染色体的变化,有纺锤丝出现C.遗传物质不能平均分配D.细胞核先分裂,核仁后分裂E.细胞核和核仁同时分裂21.关于有丝分裂后期染色体的行为,下列哪项叙述错误________A.解螺旋成染色质B.着丝粒纵裂C.有染色单体形成D.染色体向两极移动E.所含DNA数减半22.细胞有丝分裂中期开始________A.核膜消失B.染色体排列成赤道板C.核仁消失D.染色体形成E.染色体复制23.细胞增殖周期可分为________A.G1期十S期B.G2期十M期C.S期十G2期D.G1+G2期E.以上都不是24.细胞周期中,决定一个细胞是分化还是增殖的控制点(R点)位于________ A.G1期末B.G2期末C.M期末D.高尔基复合体期末E.S期25.细胞分裂后期开始的标志是________A.核仁消失B.核膜消失C.染色体排列成赤道板D.染色体复制E.着丝粒区分裂,姐妹染色单体开始分离26.细胞周期中,DNA合成是在________A.G1期B.S期C.G2期D.M期E.G0期27.有丝分裂中,染色质浓缩,核仁、核膜消失等事件发生在________A.前期B.中期C.后期D.末期E.以上都不是28.细胞周期中,对各种刺激最为敏感的时期是________A.G0期B.G1期C.G2期D.S期E.M期29.组蛋白的合成是在细胞周期的________A.S期B.G1期C.G2期D.M期E.G0期30.下列哪种关于有丝分裂的叙述不正确________A.在前期染色体开始形成B.前期比中期或后期都长C.染色体完全到达两极便进入后期D.中期染色体最粗短E.当染色体移向两极时.着丝点首先到达31.着丝粒分离至染色单体到达两极是有丝分裂的________ A.前期B.中期C.后期D.末期E.胞质分裂期32.细胞增殖周期是指下列哪一阶段________A.细胞从前一次分裂开始到下一次分裂开始为止B.细胞从这一次分裂开始到分裂结束为止C.细胞从这一次分裂结束到下一次分裂开始为止D.细胞从前一次分裂开始到下一次分裂结束为止E.细胞从前一次分裂结束到下一次分裂结束为止33.细胞周期中,遗传物质的复制规律是________A.异染色质先复制B.常染色质先复制C.异染色质大量复制,常染色质较少复制D.常染色质大量复制,异染色质较少复制E.常染色质和异染色质同时复制34.高等植物细胞与动物细胞有丝分裂的区别之一在于________ A.形成染色体B.染色体要纵裂C.有纺锤体形成D.有染色体向两极移动E.无中心粒35.对于不同细胞的细胞周期来讲,时间变化最大的时相是________ A.G1期B.S期C.G2期D.M期E.G0期36.正常细胞核与细胞质的比值较恒定,一般在________A.0.5~0.8之间B.0.1~0.3之间C.0.3~0.5之间D.0.l~0.5之间E.以上都不是37.染色体纵裂为2条染色单体连于一个着丝粒是在有丝分裂的________ A.前期B.中期C.后期D.末期E.以上都不是38.下列哪一条不是调控细胞增殖的因素________A.DNA合成的诱导物和抑制物B.cAMP和cGMPC.细胞周期基因D.秋水仙素和长春花碱E.各种生长因子39.建立细胞周期概念主要的细胞代谢基础是________A.蛋白质含量的周期性变化B.RNA含量的周期性变化C.RNA、酶含量的周期性变化D.DNA含量的周期性变化E.以上都不是40.能进入增殖状态的细胞________A.DNA含量高B.RNA含量高、染色质凝集度低C.RNA含量低、染色质凝集度低D.DNA、RNA含量高、染色质凝集度亦高E.以上都不是41.动物有丝分裂的方向与下列哪种细胞结构有关________A.纺锤丝B.微管C.微丝D.中心粒E.中心球42.下列哪种药物不能抑制纺锤体的形成________ A.秋水仙素B.长春花碱C.巯基乙醇D.植物血凝素E.秋水酰胺43.对细胞周期调控,下列哪种因素不起作用________ A.基因B.生长因子C.胆固醇D.cAMP和cGMPE.抑素44.人类的一个体细胞在G1期的DNA含量为________ A.ICB.2CC.3CD.4CE.5C45.下列哪一组细胞可构成一个动力学系统________ A.精细胞、卵细胞、骨髓细胞B.上皮细胞、骨髓细胞、肝细胞C.干细胞、增殖细胞、成熟细胞、功能细胞D.肝细胞、肾细胞、小肠上皮细胞E.上皮细胞、精卵细胞、骨髓细胞46.哺乳动物的成熟红细胞处于下列哪一时期________ A.G1期B.S期C.G2期D.G0期E.深G0期47.下列哪种细胞具有增殖潜能________A.淋巴细胞B.红细胞C.角化细胞D.神经元细胞E.骨骼肌细胞48.有丝分裂中,被人们较多接受的关于染色体向两极移动的机理是________ A.纺锤丝徽管滑动说B.微管集散说C.肌动蛋白-微管相互作用说D.电磁场说E.溶胶和凝胶的变化说49.机体中不具增殖能力的细胞是________A.干细胞B.上皮细胞C.骨髓细胞D.神经细胞E.淋巴细胞50.在S期未得到复制的0.3%的DNA称为________A.A-DNAB.B-DNAC.C-DNAD.mtDNAE.Z-DNA51.细胞周期的长短主要取决于________A.G0期B.G1期C.G2期D.S期E.M期52.有丝分裂中,对细胞分裂极的确定起决定作用的是________A.染色体的移动方向B.中心粒分离的方向C.星体的方向D.纺锤丝的方向E.中心球的方向53.细胞的增殖周期中DNA聚合酶的大量合成发生在________A.G0期B.G1期C.G2期D.S期E.M期54.组成纺锤体和星体的结构是________A.中心粒B.中心体C.中心球D.微管E.微丝55.微管蛋白的合成是在细胞周期的________A.G0期B.G1期C.G2期D.S期E.M期56.胞质开始分裂发生在________A.染色体解螺旋和核膜形成时B.染色体到达两极时C.染色体解螺旋的同时D.核膜形成时E.纺锤体微管趋向消失的同时57.动物细胞有丝分裂前期不具有的特征________A.DNA复制B.染色体形成C.核膜消失D.核仁消失E.中心粒互相分开并移向细胞两极58.一个细胞在M期中不具有的现象是________A.蛋白质合成降至极低水平B.核有明显变化C.将遗传物质均等分配到两个子细胞D.RNA合成非常活跃E.染色体形成二、填空题1、在细胞有丝分裂中, 微管的作用是、;微丝的作用是。
生物化学课后习题答案-第十三章xt13

第十三章 蛋白质的生物合成一、课后习题1.在蛋白质分子中,通常含量较高的是Ser和Leu,其次是His和Cys,含量最少的是Met和Trp。
一种氨基酸在蛋白质分子中出现的频率与它的密码子数量有什么关系?这种关系得选择其优点如何?2.AUG和UAG是蛋白合成中特定的起始和终止密码,序列同5’-UUAUGAAUGUACCGUGGUAGUU-3’的mRNA中什么样的开放阅读框才能编码一个短肽?写出该短肽的氨基酸序列。
3.细菌的基因组通常含有多少个rRNA基因拷贝,他们能迅速地转录以生产大量rRNA装配成核糖体相对对比而言,编码核糖体蛋白的基因只有一份拷贝,试解释rRNA基因和核糖体蛋白基因数量的差别。
4.DNA中的点突变(一个碱基被另一个碱基取代)可能导致一个氨基酸被另一个氨基酸替换。
但在某些情况下,由于密码子的简并性,基因编码的氨基酸序列也可能不会改变。
一种细菌生产的胞外蛋白酶在其活性位点上(—Gly-Leu-Cys-Arg—)有一个半胱氨酸残基。
紫外线照射过后,分离得到两个突变菌株。
菌株1生产以Ser取代活性部位Cys的无活性酶(—Gly-Leu-Ser-Arg—);而在菌株2内,合成了一条C末端结束在活性部位内的以—Gly-Leu—COO-结尾的截断了的肽链,指出在每一种菌株中可能发生的突变。
5.一双螺旋DNA的模板链中一段序列如下:CTTAACACCCCTGACTTCGCGCCGTCG(1)写出转录出的mRNA核苷酸序列?(2)写出5’开始的该转录mRNA序列所对应得多肽的氨基酸序列?(3)假设此DNA的另一条链被转录和翻译,所得的氨基酸序列会与(2)中的一样吗?(2)与(3)得出的答案在生物学上有什么意义?6.假设反应从游离氨基酸、tRNA、氨酰tRNA合成酶、mRNA、80S核糖体以及翻译因子开始,那么翻译一分子牛胰核糖酸酶要用掉多少个高能磷酸键?翻译一分子肌红蛋白需要消耗多少个高能磷酸键?7.噬菌体T4 DNA的相对分子质量为1.3×108(双链),假定全部核苷酸均用于编码氨基酸,试问:(1)T4 DNA可为多少氨基酸编码?(2)T4 DNA可为多少相对分子质量等于35000的不同蛋白质编码?(核苷酸对的相对分子质量按618计,氨基酸平均相对分子质量按120计)8.核糖体的基本结构和功能有哪些?9.在蛋白质定向运输时,多肽本身有何作用?高尔基体的功能是什么?参考答案:1.在蛋白质分子中,一种氨基酸出现的频率与它密码子的数量具有一定的正向关系,如:亮氨酸,苏氨酸都有6个密码子,通常在蛋白质分子中出现的几率也最高;而甲硫氨酸和色氨酸只有一个密码子,在蛋白质中出现的频率相对小一些。
第13章 课后答案

第十三章 简单国民收入决定理论1.在两部门经济中,均衡发生于( )之时。
A.实际储蓄等于实际投资;B.实际消费加实际投资等于产出值;C.计划储蓄等于计划投资;D.总投资等于企业部门的收入。
解答:C2.当消费函数为c =a +by(a>0,0<b<1),这表明,平均消费倾向( )。
A .大于边际消费倾向;B .小于边际消费倾向;C .等于边际消费倾向;D .以上三种情况都可能。
解答:A3.如果边际储蓄倾向为0.3,投资支出增加60亿元,这将导致均衡收入GDP 增加( )。
A . 20亿元;B . 60亿元;C . 180亿元;D . 200亿元。
解答:D4.在均衡产出水平上,是否计划存货投资和非计划存货投资都必然为零?解答:当处于均衡产出水平时,计划存货投资一般不为零,而非计划存货投资必然为零。
这是因为计划存货投资是计划投资的一部分,而均衡产出就是等于消费加计划投资的产出,因此计划存货不一定是零。
计划存货增加时,存货投资就大于零;计划存货减少时,存货投资就小于零。
需要指出的是,存货是存量,存货投资是流量,存货投资是指存货的变动。
在均衡产出水平上,计划存货投资是计划投资的一部分,它不一定是零,但是非计划存货投资一定是零,如果非计划存货投资不是零,那就不是均衡产出了。
比方说,企业错误估计了形势,超出市场需要而多生产了产品,就造成了非计划存货投资。
5.能否说边际消费倾向和平均消费倾向总是大于零而小于1?解答:消费倾向就是消费支出和收入的关系,又称消费函数。
消费支出和收入的关系可以从两个方面加以考察,一是考察消费支出变动量和收入变动量的关系,这就是边际消费倾向(可以用公式MPC =Δc Δy 或MPC =d c d y表示),二是考察一定收入水平上消费支出量和该收入量的关系,这就是平均消费倾向(可以用公式APC =c y表示)。
边际消费倾向总大于零而小于1,因为一般说来,消费者增加收入后,既不会不增加消费即MPC =Δc Δy=0,也不会把增加的收入全用于增加消费,一般情况是一部分用于增加消费,另一部分用于增加储蓄,即Δy =Δc+Δs ,因此,Δc Δy +Δs Δy =1,所以,Δc Δy =1-Δs Δy 。
简爱第13章问题及答案

简爱第13章问题及答案第十三章夭折的婚礼婚礼如期举行,正当结婚仪式进行到一半时,梅森带了一个律师匆匆从伦敦赶来,阻挠婚礼的进行。
他揭发罗切斯特家里有一个活着的妻子,就是他的姐姐伯莎梅森,是原来罗切斯特年轻时,由父兄作主娶了大商人约纳斯梅森之女为妻室。
婚后,他才知道女方有遗传性精神病史,罗切斯特为了贵族的名誉和面子,把妻子带回庄园后,藏匿在三楼,并专门派了一个女仆人格雷斯普尔(即缝衣妇)照料她,对外人隐而不宣。
罗切斯特承认了这一事实,并带领人们看被关在三楼的疯女人,那就是他的合法妻子。
1 .罗切斯特和简·爱的婚礼在哪里举行?()A.桑菲尔德庄园B.芬丁庄园C.盖茨黑德府D.教堂2. 罗切斯特的疯妻和梅森先生是什么关系?()A.姐弟B.同事C.母子D.伴侣3 .()给罗切斯特和简·爱主持婚礼。
A.伍德牧师B.谭波尔小姐C.圣约翰牧师D.普尔太太4 .有两个人突然闯入教堂,阻止了婚礼的进行,他们说出了怎样一个石破天惊的秘密?()A.简·爱和罗切斯特是兄妹B.简·爱还有一个丈夫活着C.罗切斯特的妻子自杀了D.罗切斯特还有一个妻子活着5 .罗切斯特和伯莎·梅森于()年前在牙买加西班牙城某教堂结婚,当时他并不了解自己妻子的真实情况。
A.5B.10C.15D.206 .平时是谁在照顾罗切斯特的疯妻?()A.格雷斯·普尔B.费尔法克斯太太C.梅森先生D.罗切斯特自己7. 当疯女人袭击罗切斯特时,他并没有一拳打倒她,而是用绳子把她绑在了椅子上。
由此可见罗切斯特的()。
A.残酷B.善良C.懦弱D.果断8. 简·爱的叔父患的是什么病?()A.心脏病B.痨病C.高血压D.肺病9 .梅森是从()那里获知了罗切斯特要结婚的消息,他曾在梅森家做过地方通信员。
A.简·爱的舅舅B.普尔太太C.简·爱的叔叔D.英格兰姆小姐10 .罗切斯特和简·爱举行婚礼时,有两个陌生人突然闯入,这两人是谁?()A.里德太太和伊丽莎小姐B.罗切斯特的疯妻和山姆C.英格兰姆小姐和梅森先生D.律师布里格斯和梅森先生答案:1. D2. A3. A4. D5. C6. A7. B8. B9. C10. D。
管理学第十三章练习题与答案

管理学第⼗三章练习题与答案⼀、名词解释:※1.沟通;2.冲突;3.团队沟通;⼆、选择题:1.美国加利福尼亚州⽴⼤学通过研究得出:“来⾃领导层的信息只有20%-25%被下级知道并正确理解,⽽从下到上反馈的信息则不超过10%,平⾏交流的效率则可达到90%以上”,这就是著名的“沟通位差效应”。
你对这⼀研究结论的正确理解是:()A.在组织内部,同事之间的沟通是企业有效沟通的保证;B.在组织内部,要相互尊重,没有平等就没有真正的沟通;C.由于信息反馈效率极低,所以要⾼度重视单向沟通;D.由于下⾏沟通效率不⾼,所以领导要减少命令和指挥;2.横向沟通过程中最⼤的障碍来⾃:()A.个⼈间的冲突;B.企业内部部门化;C.管理暗者能⼒过低;D.个⼈理解能⼒存在差异;3.在组织中构成组织沟通最基本内容的是:()A.群体间沟通;B.个体间沟通;C.组织间沟通;D.单向沟通;4.下列情况下适合使⽤单向沟通的是:()A.时间⽐较充裕,但问题⽐较棘⼿;B.下属对解决⽅案的接受程度⾄关重要;C.上级缺乏处理负反馈的能⼒,容易感情⽤事;D.下属能对解决问题提供有价值的信息和建议;5.下列不是决定信息来源可靠性的因素是:()A.诚实;B.能⼒;C.客观;D.权威;6.有反馈传递的沟通是:()A.双向沟通;B.上⾏沟通;C.⾮正式沟通;D.下⾏沟通;7.选择沟通⼯具在很⼤程度上取决于:()A.信息种类;B.⽬的;C.外界环境;D.沟通双⽅;8.当冲突⽆关紧要的时候,或当冲突双⽅情绪极为激动,需要时间恢复平静时,可采⽤:()A.回避;B.迁就;C.强制;D.妥协;E.合作;9.如果发现⼀个组织中⼩道消息很多,⽽正式渠道的消息很少,这是否意味着该组织:()A.⾮正式沟通渠道中信息传递很通畅;B.知识沟通渠道中消息传递存在问题,需要调整;C.其中有部分⼈特别喜欢在背后乱发议论,传递⼩道消息;D.充分运⽤了⾮正式沟通渠道的作⽤,促进了信息的传递;10.协(合)作适⽤于下列何种冲突:()A.当事件重⼤,双⽅不可能妥协,要开诚布公的谈判;B.当认为维持和谐关系⼗分重要时;C.当双⽅势均⼒敌、争执不下需要才取权宜之计时;D.当必须对重⼤事件或紧急事件进⾏马上处理时;11.“冲突是组织保持活⼒的⼀种有效⼿段”,这种观点属于:()A.冲突的传统观点;B.冲突的⼈际关系观点;C.冲突的相互作⽤观点;D.A与C正确;12.“地位差别”属于影响有效沟通的障碍因素中的:()A.个⼈因素;B.⼈际因素;C.结构因素;D.技术因素;13.⼝头沟通的优点在于:()A.准确;B.有充⾜的时间进⾏思考应答;C.⽴即反馈;D.不受噪⾳⼲扰;14.信息接收者可以通过下列哪⼀个⼿段来提⾼沟通效果:()A.请求反馈;B.保持可信性;C.提问;D.运⽤⾮语⾔沟通;15.在沟通过程中,噪⾳最有可能成为下列哪⼀阶段的⼀个重要因素:()A.信息发送者发送信息;B.信息接受者接受信息;C.信息传递;D.反馈;16.下列不是优秀管理者实现有效谈判⼀般的原则:()A.理性分析谈判的事件;B.抱着诚意开始谈判;C.坚定与灵活相结合;D.妥善地选择处理办法;17.沟通在管理中的作⽤是:()A.协调各个体、各要素,使企业成为⼀个整体的凝聚剂;B.是领导者激励下属,实现领导职能的基本途径;C.沟通是企业与外部环境之间建⽴联系点桥梁;D.沟通是组织⽂化;18.沟通的⽬的有:()A.给交往者提供⾏为建议;B.以积极或消极的⽅式激励或约束他⼈⾏为;C.向上司、下属或合作单位与决策制定或执⾏有关的各种信息;D.获得选择或组织进⾏与⾃⼰的活动相关的各种信息;19.关于沟通的过程,下列说法不正确的是:()A.⾄少存在着⼀个发送者和⼀个接收者;B.发送者将信息译成接收者能够理解的⼀系列符号;C.接收者将接受的符号译为具有特定含义的信息;D.信息传递的有效性和接收者的翻译能⼒⽆关,只与发送者的翻译能⼒有关;20.许多企业和研究所都设有免费咖啡厅,这⼀设置的主要⽬的是:()A.促进⾮正式组织的形成;B.促进信息沟通;C.增强企业的凝聚⼒;D.给员⼯提供⼀个放松的场所,减轻员⼯的⼯作压⼒;21.冲突管理实际上包括:()A.管理者要设法消除冲突产⽣的负⾯效应;B.制造平等团结的环境;C.保持适度的冲突;D.要求管理者激发冲突,利⽤和扩⼤冲突对组织产⽣的正⾯效应;22.当冲突双⽅势均⼒敌,争执不下,同时事件重⼤,双⽅不可能妥协时,可采⽤:()A.回避;B.迁就;C.强制;D.妥协;E.合作;23.解决直线与参谋间冲突的⼀个主要⽅法是:()A.赋予直线管理⼈员职能职权;B.让直线⼈员更多地依靠参谋⼈员的知识;C.允许直线⼈员压制参谋⼈员;D.把直线与参谋的活动结合起来;24.某⼯⼚的销售科长和车间主任在产品⽣产数量上的意见发⽣分歧时,这属于哪⼀种冲突:()A.直线与参谋之间;B.直线与直线之间;C.委员会成员之间;D.正式组织与⾮正式组织之间;25.影响有效沟通的障碍性因素是:()A.双⽅的相互信任程度;B.发送者与接收者之间的相似程度;C.双⽅的地位差别;D.信息传递链的长短26.属于影响沟通障碍的个⼈因素的是:()A.沟通技巧的差异;B.有选择地接受;C.双⽅的相互信任程度;D.双⽅的地位差别;27.下列不是克服沟通中的障碍⼀般准则是:()A.创造⼀个相互信任,有利于沟通的⼩环境;B.组成⾮管理⼯作组;C.加强上下沟通,促进横向交流;D.培养“听”的艺术;28.关于团队沟通的说法正确的是:()A.团队沟通集中研究团队沟通集权的程度和团队任务的性质两个⽅⾯;B.集权沟通⽹络对简单问题能够解决快,对复杂问题解决慢;C.集权沟通⽹络对复杂问题能够解决快,对简单问题解决慢D.分权沟通⽹络对简单问题能够解决快,对复杂问题解决慢29.李总经理⼀向⾮常专权,最近参加了⼀次⾼级管理培训班后,认有必要在企业中推⾏新的领导⽅式。
第十三章 或有事项练习及答案

第十三章或有事项一、单项选择题1.根据企业会计准则规定,下列各项中,不属于或有事项的是()。
A.产品质量保证B.重组义务C.债务担保D.待执行合同【答案】D 【解析】待执行合同属于或有事项,只有待执行合同变为亏损合同的,才应当将其作为或有事项处理。
2.下列关于或有资产和或有负债的表述中,不正确的是()。
A.或有资产作为一种潜在资产,其结果具有较大不确定性B.或有负债可能是一项潜在义务,也可能是一项现时义务C.或有资产和或有负债应在资产负债表内予以确认D.或有资产和或有负债在一定的条件下可以转化为企业的资产和预计负债【答案】C 【解析】或有负债和或有资产符合负债或资产的定义和确认条件,企业应当确认或有负债和或有资产,在符合条件的情况下应当进行相应的披露。
3.下列关于或有事项确认为预计负债的条件中,表述不正确的是()。
A.该项义务是企业承担的潜在义务B.该项义务是企业承担的现时义务C.履行该义务很可能导致经济利益流出企业D.该义务的金额能够可靠地计量【答案】A 【解析】按照规定,与或有事项有关的义务同时满足下列条件时,应作为预计负债进行确认和计量:(1)该义务是企业承担的现时义务;(2)履行该义务很可能导致经济利益流出企业;(3)该义务的金额能够可靠地计量。
4.2010年10月20日,新龙公司因合同违约而被大成公司起诉。
2010年12月31日,新龙公司尚未接到人民法院的判决。
新龙公司预计,最终的判决很可能对其不利,并预计将要支付的赔偿金额为160~180万元之间的某一金额,而且这个区间内每个金额的可能性都大致相同。
2010年12月31日,新龙公司对该项诉讼应确认的预计负债金额为()万元。
A.160B.190C.170D.180【答案】C 【解析】预计负债应当按照履行相关现时义务所需支出的最佳估计数进行初始计量,所需支出存在一个连续范围,且该范围内各种结果发生的可能性相同的,最佳估计数应当按照该范7 / 12围内的中间值即上下限金额的平均数确定。
习题答案(第13章)

第13章思考与练习1.连接的主要作用是什么?分为哪几种方法?答:连接是将两个或两个以上的零件连合成一体的结构。
为了便于机器的制造、安装、维修等,常采用不同的连接方法将零、部件合成一整体。
连接分为三大类。
(1)不可拆连接,如焊连接、铆钉连接、胶接等。
(2)可拆连接,如键连接、销连接和螺纹连接等。
(3)过盈配合连接2.键连接的主要作用是什么?答:主要用于轴和轴上零件之间的轴向固定,有的还能实现轴零件的轴向固定或轴向滑动。
3.圆头、方头及单圆头普通平键各有何优、缺点?分别适用于什么场合?轴和轮毂孔上键槽是怎样加工的?答:A型平键键槽由立式键槽铣刀加工,键在槽中轴向固定较好,但键的头部侧面与轮毂上的键槽并不接触,因而键的圆头部分不能充分利用,而且轴上键槽端部的应力集中较大。
B型平键键槽用卧式键槽铣刀加工,避免了上述缺点,但对于尺寸较大的键,宜用紧定螺钉固定在轴上的键槽中,以防松动。
C型平键一般用于轴端。
4.如何选取普通平键的尺寸b×h×L?它的公称长度与工作长度之间有什么关系?答:根据轴的直径d从标准(见表17.1)中选择平键宽度b(高度h),键的长度L应略小于轮毂长度,并与标准中规定的长度系列相符。
公称长度L,工作长度l,其之间的关系为:A型键l=L-b,B型键l=L,C型键l=L-b/2。
5.普通平键连接有哪些失效形式?主要失效形式是什么?怎样进行强度校核?如强度不够,可采取哪些措施?答:普通平键连接属于静连接,其主要失效形式是连接中强度较弱零件的工作面被压溃。
导向平键和滑键连接属于动连接,其主要失效形式是工作面过度磨损。
故强度计算时,静连接校核挤压强度,动连接校核压力强度。
如果校核后键连接的强度不够,在不超过轮毂宽度的条件下,可适当增加键的长度,但键的长度一般不应超过2.25d,否则载荷沿键长方向的分布将很不均匀;或者相隔180°布置两个平键,因考虑制造误差引起的载荷分布不均,只能按1.5个键做强度校核。
大学物理(许瑞珍_贾谊明) 第13章答案

第十三章 振动13-1 一质点按如下规律沿x 轴作简谐振动:x = 0.1 cos (8πt +2π/3 ) (SI),求此振动的周期、振幅、初相、速度最大值和加速度最大值。
解:周期T = 2π/ ω= 0.25 s振幅A = 0.1m初相位φ= 2π/ 3V may = ωA = 0.8πm / s ( = 2.5 m / s )a may = ω2 A = 6.4π2m / s ( = 63 m / s 2)13-2 一质量为0.02kg 的质点作谐振动,其运动方程为:x = 0.60 cos( 5 t -π/2) (SI)。
求:(1)质点的初速度;(2)质点在正向最大位移一半处所受的力。
解:(1) )( )25sin(0.3 SI t dt dx v π--==0.3 20x m ma x ω-== (2) 2x m ma F ω-==5.13.052.0,2/ 2N F A x -=⨯⨯-==时13-3 如本题图所示,有一水平弹簧振子,弹簧的倔强系数k = 24N/m ,重物的质量m = 6kg ,重物静止在平衡位置上,设以一水平恒力F = 10 N 向左作用于物体(不计摩擦),使之由平衡位置向左运动了0.05m ,此时撤去力F ,当重物运动到左方最远位置时开始计时,求物体的运动方程。
解:设物体的运动方程为:x = A c o s (ωt +φ)恒外力所做的功即为弹簧振子的能量:F ⨯ 0.05 = 0.5 J当物体运动到左方最位置时,弹簧的最大弹性势能为0.5J ,即:1 /2 kA 2 = 0.5 J ∴A = 0.204 mA 即振幅ω2 = k / m = 4 ( r a d / s )2ω= 2 r a d / s按题目所述时刻计时,初相为φ= π∴ 物体运动方程为x = 0.204 c o s (2 t +π) ( SI ) 13-4 一水平放置的弹簧系一小球。
已知球经平衡位置向右运动时,v =100cm ⋅s -1,周期T =1.0s ,求再经过1/3秒时间,小球的动能是原来的多少倍?弹簧的质量不计。
(完整版)第十三章简单国民收入决定理论习题及答案

第十三章简单国民收入决定理论一、选择题:1.在两部门经济中,均衡发生于( )之时。
A.实际储蓄等于实际投资B.实际的消费加实际的投资等于产出值C.计划储蓄等于计划投资D.总支出等于企业部门的收入2.从短期来说,当居民的可支配收入等于零时。
消费支出可能( )A.大于零B.等于零C.小于零;D.以上几种情况都可能3.从长期来说,当居民的可支配收入等于零时,则消费支出( )A.可能大于零B.可能小于零C.等于零D.以上几种情况都有可能4.在短期内,居民的( )有可能大于可支配收入。
A.储蓄B.消费C.所得税D.转移支付5.直线型的消费函数表明平均消费倾向( )A.大于边际消费倾向B.小于边际消费倾向C.等于边际消费倾向D.以上几种情况都有可能6.假定净出口函数是X=X-mY,净出口余额为零,则增加投资支出将( )。
A.使净出口余额和收入增加B.收入增加,但净出口余额变为负值C.收入增加,净出口余额不受影响D.收入不受影响,但净出口余额变为负值7. 引致消费取决于:()。
A. 自发消费B. 边际储蓄倾向C. 收入和边际消费倾向8. 根据凯恩斯的消费函数,引起消费增加的因素主要是:()。
A. 价格水平下降B. 收入增加C. 储蓄增加9. 根据凯恩斯的储蓄函数,引起储蓄增加的因素是:()。
A. 收入增加B. 利息率提高C. 人们预期未来的价格水平要上升10. 在两部门经济中,当投资增加100万元时,国民收入增加了1000万元,那么此时的边际消费倾向为:()。
A.100%B.10%C.90%D.20%11. 如果边际消费倾向是0.8,在没有所得税的情况下,转移支付乘数是:()A.4B.5C.6D.812. 如果消费函数为C=100+ 0.8 (Y-T),那么政府支出乘数是:()。
A. 0.8B. 1.25C.4D.513. 下列哪项经济政策将导致收入水平有最大变化()。
A. 政府增加购买50亿元商品和劳务B. 政府购买增加50亿元,同时增加税收50亿元C. 税收减少50亿元D. 政府支出增加50亿元,其中30亿由增加的税收支付14.下列哪一项不是恒等式()。
宏观经济学第13章 课后练习 参考答案

第十三章课后练习·参考答案( P407-408 )1.C2.A3.D4.在均衡产出水平上,总产出等于计划总支出,所以非计划存货投资一定等于零,计划存货投资不一定等于零,主要看企业是否有计划存货投资。
5.边际消费倾向是指增加的收入中用于增加消费的比率。
由于增加的消费只能来自增加的收入,所以边际消费倾向的取值范围为[0,1],通常为(0,1),对单个个人而言,边际消费倾向可以为0或1,但对总体而言,不可能出现等于0或等于1的情况。
平均消费倾向一定是大于零的,但不总是小于1,当收入较低或为零时,消费支出大于收入,此时平均消费倾向大于1,当居民将所有的收入都用于消费时,平均消费倾向等于1,只有当收入较高,居民除消费之外还有剩余时,平均消费倾向才小于1。
6.凯恩斯定律是指不论需求量为多少,经济社会均能以不变的价格提供相应的供给量。
即社会总需求变动时,只会引起产量和收入的变动,使供求相等,而不会引起价格变动。
凯恩斯定律提出的社会经济背景是1929年到1933年的大萧条,工人大批失业,资源大量闲置。
在这种情况下,社会总需求增加时,只会使闲置的资源得到利用,生产增加,而不会使资源的价格上升,从而产品成本和价格大体上能保持不变。
凯恩斯定律只适用于短期,因为在短期中,价格不易变动,当社会总需求变动时,就只引起产量的变动。
(参看课本P381)7. 参见第十二章课后练习的第6题。
简单地说,就是转移支付已经包括在C和I里了。
8. 因为富人的边际消费倾向小于穷人的,当把一部分收入从富人那里转移给穷人时,富人减少的消费小于穷人增加的消费,所以整个社会的总消费或总支出是增加的,根据凯恩斯理论,整个社会的总收入就会得到提高。
9. 因为政府购买支出增加后首先直接引起总支出和总收入等额增加相当于政府购买支出的量,然后收入的增加又引起消费的增加,消费和收入之间的相互作用最终使收入的增加是政府购买支出增加的数倍,形成政府购买支出乘数。
第十三章课后习题答案

第十三章 热力学基础13 -1 如图所示,bca 为理想气体绝热过程,b1a 和b2a 是任意过程,则上述两过程中气体作功与吸收热量的情况是( )(A) b1a 过程放热,作负功;b2a 过程放热,作负功(B) b1a 过程吸热,作负功;b2a 过程放热,作负功(C) b1a 过程吸热,作正功;b2a 过程吸热,作负功(D) b1a 过程放热,作正功;b2a 过程吸热,作正功分析与解 bca ,b1a 和b2a 均是外界压缩系统,由⎰=V p W d 知系统经这三个过程均作负功,因而(C)、(D)不对.理想气体的内能是温度的单值函数,因此三个过程初末态内能变化相等,设为ΔE .对绝热过程bca ,由热力学第一定律知ΔE =-W bca .另外,由图可知:|W b2a |>|W bca |>|W b1a |,则W b2a <W bca <W b1a .对b1a 过程:Q =ΔE +W b1a >ΔE +W bca =0 是吸热过程.而对b2a 过程:Q =ΔE +W b2a <ΔE +W bca =0 是放热过程.可见(A)不对,正确的是(B).13 -2 如图,一定量的理想气体,由平衡态A 变到平衡态B ,且它们的压强相等,即p A =p B ,请问在状态A 和状态B 之间,气体无论经过的是什么过程,气体必然( )(A) 对外作正功 (B) 内能增加(C) 从外界吸热 (D) 向外界放热分析与解 由p -V 图可知,p A V A <p B V B ,即知T A <T B ,则对一定量理想气体必有E B >E A .即气体由状态A 变化到状态B,内能必增加.而作功、热传递是过程量,将与具体过程有关.所以(A)、(C)、(D)不是必然结果,只有(B)正确.13 -3 两个相同的刚性容器,一个盛有氢气,一个盛氦气(均视为刚性分子理想气体).开始时它们的压强和温度都相同,现将3J 热量传给氦气,使之升高到一定的温度.若使氢气也升高同样的温度,则应向氢气传递热量为( )(A) 6J (B) 3 J (C) 5 J (D) 10 J分析与解 当容器体积不变,即为等体过程时系统不作功,根据热力学第一定律Q =ΔE +W ,有Q =ΔE .而由理想气体内能公式T R i M m E Δ2Δ=,可知欲使氢气和氦气升高相同温度,须传递的热量 ⎪⎪⎭⎫ ⎝⎛⎪⎪⎭⎫ ⎝⎛=e e e 222e 2H H H H H H H H /:i M m i M m Q Q .再由理想气体物态方程pV =mM RT ,初始时,氢气和氦气是具有相同的温度、压强和体积,因而物质的量相同,则3/5/:e 2e 2H H H H ==i i Q Q .因此正确答案为(C).13 -4 有人想像了四个理想气体的循环过程,则在理论上可以实现的为( )分析与解由绝热过程方程pVγ=常量,以及等温过程方程pV=常量,可知绝热线比等温线要陡,所以(A)过程不对,(B)、(C)过程中都有两条绝热线相交于一点,这是不可能的.而且(B)过程的循环表明系统从单一热源吸热且不引起外界变化,使之全部变成有用功,违反了热力学第二定律.因此只有(D)正确.13 -5一台工作于温度分别为327 ℃和27 ℃的高温热源与低温源之间的卡诺热机,每经历一个循环吸热2 000 J,则对外作功()(A) 2 000J(B) 1 000J(C) 4 000J(D) 500J分析与解热机循环效率η=W/Q吸,对卡诺机,其循环效率又可表为:η=1-T2 /T1,则由W /Q吸=1 -T2 /T1可求答案.正确答案为(B).13 -6根据热力学第二定律()(A) 自然界中的一切自发过程都是不可逆的(B) 不可逆过程就是不能向相反方向进行的过程(C) 热量可以从高温物体传到低温物体,但不能从低温物体传到高温物体(D) 任何过程总是沿着熵增加的方向进行分析与解 对选项(B):不可逆过程应是指在不引起其他变化的条件下,不能使逆过程重复正过程的每一状态,或者虽然重复但必然会引起其他变化的过程.对选项(C):应是热量不可能从低温物体自动传到高温物体而不引起外界的变化.对选项(D):缺少了在孤立系统中这一前提条件.只有选项(A)正确. 13 -7 位于委内瑞拉的安赫尔瀑布是世界上落差最大的瀑布,它高979m.如果在水下落的过程中,重力对它所作的功中有50%转换为热量使水温升高,求水由瀑布顶部落到底部而产生的温差.( 水的比热容c 为4.18×103 J·kg -1·K -1 ) 分析 取质量为m 的水作为研究对象,水从瀑布顶部下落到底部过程中重力作功W =mgh ,按题意,被水吸收的热量Q =0.5W ,则水吸收热量后升高的温度可由Q =mc ΔT 求得.解 由上述分析得mc ΔT =0.5mgh水下落后升高的温度ΔT =0.5gh /c =1.15K13 -8 如图所示,一定量的空气,开始在状态A ,其压强为2.0×105Pa ,体积为2.0 ×10-3m 3 ,沿直线AB 变化到状态B 后,压强变为1.0 ×105Pa ,体积变为3.0 ×10-3m 3 ,求此过程中气体所作的功.分析 理想气体作功的表达式为()⎰=V V p W d .功的数值就等于p -V 图中过程曲线下所对应的面积.解 S ABCD =1/2(BC +AD)×CD故 W =150 J13 -9 汽缸内储有2.0mol 的空气,温度为27 ℃,若维持压强不变,而使空气的体积膨胀到原体积的3s 倍,求空气膨胀时所作的功.分析 本题是等压膨胀过程,气体作功()1221d V V p V p W V V -==⎰,其中压强p 可通过物态方程求得.解 根据物态方程11RT pV v =,汽缸内气体的压强11/V RT p v = ,则作功为 ()()J 1097.92/31112112⨯==-=-=RT V V V RT V V p W v v 13 -10 一定量的空气,吸收了1.71×103J 的热量,并保持在1.0 ×105Pa 下膨胀,体积从1.0×10-2m 3 增加到1.5×10-2m 3 ,问空气对外作了多少功? 它的内能改变了多少?分析 由于气体作等压膨胀,气体作功可直接由W =p (V 2 -V 1 )求得.取该空气为系统,根据热力学第一定律Q =ΔE +W 可确定它的内能变化.在计算过程中要注意热量、功、内能的正负取值.解 该空气等压膨胀,对外作功为W =p (V 2-V 1 )=5.0 ×102J其内能的改变为Q =ΔE +W =1.21 ×103J13 -11 0.1kg 的水蒸气自120 ℃加热升温到140℃,问(1) 在等体过程中;(2) 在等压过程中,各吸收了多少热量? 根据实验测定,已知水蒸气的摩尔定压热容C p,m =36.21J·mol -1·K -1,摩尔定容热容C V,m =27.82J·mol -1·K -1. 分析 由量热学知热量的计算公式为T C Q m Δv =.按热力学第一定律,在等体过程中,T C E Q ΔΔm V ,V v ==;在等压过程中, T C E V p Q ΔΔd m p,p v =+=⎰.解 (1) 在等体过程中吸收的热量为J 101.3ΔΔ3m V,V ⨯===T C Mm E Q (2) 在等压过程中吸收的热量为 ()J 100.4Δd 312m p,p ⨯=-=+=⎰T T C M m E V p Q 13 -12 如图所示,在绝热壁的汽缸内盛有1mol 的氮气,活塞外为大气,氮气的压强为1.51 ×105 Pa ,活塞面积为0.02m 2 .从汽缸底部加热,使活塞缓慢上升了0.5m.问(1) 气体经历了什么过程? (2) 汽缸中的气体吸收了多少热量? (根据实验测定,已知氮气的摩尔定压热容C p ,m =29.12J·mol -1·K -1,摩尔定容热容C V,m =20.80J·mol -1·K -1 )分析 因活塞可以自由移动,活塞对气体的作用力始终为大气压力和活塞重力之和.容器内气体压强将保持不变.对等压过程,吸热T C Q Δm p,p v =.ΔT 可由理想气体物态方程求出.解 (1) 由分析可知气体经历了等压膨胀过程.(2) 吸热T C Q Δm p,p v =.其中ν =1 mol ,C p,m =29.12J·mol -1·K-1.由理想气体物态方程pV =νRT ,得ΔT =(p 2V 2 -p 1 V 1 )/R =p(V 2 -V 1 )/R =p· S· Δl /R则 J 105.293m p,p ⨯==pS ΔSΔl C Q13 -13 一压强为1.0 ×105Pa,体积为1.0×10-3m 3的氧气自0℃加热到100 ℃.问:(1) 当压强不变时,需要多少热量?当体积不变时,需要多少热量?(2) 在等压或等体过程中各作了多少功?分析 (1) 求Q p 和Q V 的方法与题13-11相同.(2) 求过程的作功通常有两个途径.① 利用公式()V V p W d ⎰=;② 利用热力学第一定律去求解.在本题中,热量Q 已求出,而内能变化可由()12m V ,V ΔT T C E Q -==v 得到.从而可求得功W .解 根据题给初态条件得氧气的物质的量为mol 1041.4/2111-⨯===RT V p Mm v 氧气的摩尔定压热容R C 27m p,=,摩尔定容热容R C 25m V,=. (1) 求Q p 、Q V等压过程氧气(系统)吸热()J 1.128Δd 12m p,p =-=+=⎰T T C E V p Q v等体过程氧气(系统)吸热()J 5.91Δ12m V ,V =-==T T C E Q v(2) 按分析中的两种方法求作功值解1 ① 利用公式()V V p W d ⎰=求解.在等压过程中,T R Mm V p W d d d ==,则得 J 6.36d d 21p ===⎰⎰T T T R Mm W W 而在等体过程中,因气体的体积不变,故作功为()0d V ==⎰V V p W② 利用热力学第一定律Q =ΔE +W 求解.氧气的内能变化为()J 5.91Δ12m V,V =-==T T C Mm E Q 由于在(1) 中已求出Q p 与Q V ,则由热力学第一定律可得在等压过程、等体过程中所作的功分别为J 6.36Δp p =-=E Q W0ΔV V =-=E Q W13 -14 如图所示,系统从状态A 沿ABC 变化到状态C 的过程中,外界有326J 的热量传递给系统,同时系统对外作功126J.当系统从状态C 沿另一曲线CA 返回到状态A 时,外界对系统作功为52J ,则此过程中系统是吸热还是放热?传递热量是多少?分析 已知系统从状态C 到状态A ,外界对系统作功为W CA ,如果再能知道此过程中内能的变化ΔE AC ,则由热力学第一定律即可求得该过程中系统传递的热量Q CA .由于理想气体的内能是状态(温度)的函数,利用题中给出的ABC 过程吸热、作功的情况,由热力学第一定律即可求得由A 至C 过程中系统内能的变化ΔE AC ,而ΔE AC =-ΔE AC ,故可求得Q CA .解 系统经ABC 过程所吸收的热量及对外所作的功分别为Q ABC =326J , W ABC =126J则由热力学第一定律可得由A 到C 过程中系统内能的增量ΔE AC =Q ABC -W ABC =200J由此可得从C 到A ,系统内能的增量为ΔE CA =-200J从C 到A ,系统所吸收的热量为Q CA =ΔE CA +W CA =-252J式中负号表示系统向外界放热252 J.这里要说明的是由于CA 是一未知过程,上述求出的放热是过程的总效果,而对其中每一微小过程来讲并不一定都是放热.13 -15 如图所示,一定量的理想气体经历ACB 过程时吸热700J ,则经历ACBDA 过程时吸热又为多少?分析 从图中可见ACBDA 过程是一个循环过程.由于理想气体系统经历一个循环的内能变化为零,故根据热力学第一定律,循环系统净吸热即为外界对系统所作的净功.为了求得该循环过程中所作的功,可将ACBDA 循环过程分成ACB 、BD 及DA 三个过程讨论.其中BD 及DA 分别为等体和等压过程,过程中所作的功按定义很容易求得;而ACB 过程中所作的功可根据上题同样的方法利用热力学第一定律去求.解 由图中数据有p A V A =p B V B ,则A 、B 两状态温度相同,故ACB 过程内能的变化ΔE CAB =0,由热力学第一定律可得系统对外界作功W CAB =Q CAB -ΔE CAB =Q CAB =700J在等体过程BD 及等压过程DA 中气体作功分别为()⎰==0d BD V V p W()⎰-=-==J 1200d 12A DA V V P V p W则在循环过程ACBDA 中系统所作的总功为J 500D A BD A CB -=++=W W W W负号表示外界对系统作功.由热力学第一定律可得,系统在循环中吸收的总热量为J 500-==W Q负号表示在此过程中,热量传递的总效果为放热.13 -16 在温度不是很低的情况下,许多物质的摩尔定压热容都可以用下式表示2m p,2--+=cT bT a C式中a 、b 和c 是常量,T 是热力学温度.求:(1) 在恒定压强下,1 mol 物质的温度从T 1升高到T 2时需要的热量;(2) 在温度T 1 和T 2 之间的平均摩尔热容;(3) 对镁这种物质来说,若C p ,m 的单位为J·mol -1·K -1,则a =25.7J·mol -1·K-1 ,b =3.13 ×10-3J·mol -1·K-2,c =3.27 ×105J·mol -1·K.计算镁在300K时的摩尔定压热容C p,m ,以及在200K和400K之间C p,m 的平均值. 分析 由题目知摩尔定压热容C p,m 随温度变化的函数关系,则根据积分式⎰=21d m p,p T T T C Q 即可求得在恒定压强下,1mol 物质从T 1 升高到T 2所吸收的热量Qp .故温度在T 1 至T 2之间的平均摩尔热容()12p m p,/T T Q C -=. 解 (1) 11 mol 物质从T 1 升高到T 2时吸热为()()()()11122122122m p,p d 2d 21----+-+-=-+==⎰⎰T T c T T b T T a T cT bT a T C Q T T (2) 在T 1 和T 2 间的平均摩尔热容为()()21212p m p,//T T c T T a T T Q C -+=-=(3) 镁在T =300 K 时的摩尔定压热容为-1-12m p,K mol J 9.232⋅⋅=-+=-cT bT a C镁在200 K 和400 K 之间C p ,m 的平均值为()-1-12112m p,K mol J 5.23/⋅⋅=-+=T T c T T a C13 -17 空气由压强为1.52×105 Pa ,体积为5.0×10-3m 3 ,等温膨胀到压强为1.01×105 Pa ,然后再经等压压缩到原来的体积.试计算空气所作的功. 解 空气在等温膨胀过程中所作的功为()()2111121T /ln /ln p p V p V V RT Mm W == 空气在等压压缩过程中所作的功为()⎰-==12d V V p V p W 利用等温过程关系p 1 V 1 =p 2 V 2 ,则空气在整个过程中所作的功为()J 7.55/ln 11122111=-+=+=V p V p p p V p W W W T p13 -18 如图所示,使1mol 氧气(1) 由A 等温地变到B ;(2) 由A 等体地变到C ,再由C 等压地变到B.试分别计算氧气所作的功和吸收的热量.分析 从p -V 图(也称示功图)上可以看出,氧气在AB 与ACB 两个过程中所作的功是不同的,其大小可通过()V V p W d ⎰=求出.考虑到内能是状态的函数,其变化值与过程无关,所以这两个不同过程的内能变化是相同的,而且因初、末状态温度相同T A =T B ,故ΔE =0,利用热力学第一定律Q =W +ΔE ,可求出每一过程所吸收的热量.解 (1) 沿AB 作等温膨胀的过程中,系统作功()()J 1077.2/ln /ln 31⨯===A B B A A B AB V V V p V V RT Mm W 由分析可知在等温过程中,氧气吸收的热量为Q AB =W AB =2.77 ×103J (2) 沿A 到C 再到B 的过程中系统作功和吸热分别为W ACB =W AC +W CB =W CB =p C (V B -V C )=2.0×103JQ ACB =W A CB =2.0×103 J13 -19 将体积为1.0 ×10-4m 3 、压强为1.01×105Pa 的氢气绝热压缩,使其体积变为2.0 ×10-5 m 3 ,求压缩过程中气体所作的功.(氢气的摩尔定压热容与摩尔定容热容比值γ=1.41)分析 可采用题13-13 中气体作功的两种计算方法.(1) 气体作功可由积分V p W d ⎰=求解,其中函数p (V )可通过绝热过程方程pV C γ= 得出.(2)因为过程是绝热的,故Q =0,因此,有W =-ΔE ;而系统内能的变化可由系统的始末状态求出.解 根据上述分析,这里采用方法(1)求解,方法(2)留给读者试解.设p 、V 分别为绝热过程中任一状态的压强和体积,则由γγpV V p =11得 γγV V p p -=11氢气绝热压缩作功为J 0.231d d 121211121-=⎥⎦⎤⎢⎣⎡-⎥⎦⎤⎢⎣⎡-===⎰⎰-V V V V γp V V V p V p W V V γγ 13 -20 试验用的火炮炮筒长为3.66 m ,内膛直径为0.152 m ,炮弹质量为45.4kg ,击发后火药爆燃完全时炮弹已被推行0.98 m ,速度为311 m·s -1 ,这时膛内气体压强为2.43×108Pa.设此后膛内气体做绝热膨胀,直到炮弹出口.求(1) 在这一绝热膨胀过程中气体对炮弹作功多少?设摩尔定压热容与摩尔定容热容比值为 1.2γ=.(2) 炮弹的出口速度(忽略摩擦).分析 (1) 气体绝热膨胀作功可由公式1d 2211--==⎰γV p V p V p W 计算.由题中条件可知绝热膨胀前后气体的体积V 1和V 2,因此只要通过绝热过程方程γγV p V p 2211=求出绝热膨胀后气体的压强就可求出作功值.(2) 在忽略摩擦的情况下,可认为气体所作的功全部用来增加炮弹的动能.由此可得到炮弹速度.解 由题设l =3.66 m,D =0.152 m ,m =45.4 kg ,l 1=0.98 m ,v 1=311 m·s -1 ,p 1 =2.43×108Pa ,γ=1.2.(1) 炮弹出口时气体压强为()()Pa 1000.5//7112112⨯===γγl l p V V p p 气体作功J 1000.54π11d 6222112211⨯=--=--==⎰D γl p l p γV p V p V p W (2) 根据分析2122121v v m m W -=,则 -121s m 563⋅=+=v 2W/m v13 -21 1mol 氢气在温度为300K,体积为0.025m 3 的状态下,经过(1)等压膨胀,(2)等温膨胀,(3)绝热膨胀.气体的体积都变为原来的两倍.试分别计算这三种过程中氢气对外作的功以及吸收的热量.分析 这三个过程是教材中重点讨论的过程.在p -V 图上,它们的过程曲线如图所示.由图可知过程(1 ) 作功最多, 过程( 3 ) 作功最少.温度T B >T C >T D ,而过程(3) 是绝热过程,因此过程(1)和(2)均吸热,且过程(1)吸热多.具体计算时只需直接代有关公式即可.解 (1) 等压膨胀()()J 1049.23⨯==-=-=A A B AA AB A p RT V V V RT V V p W v()J 1073.8273,,⨯===-=+=A A m p A B m p p p T R T C T T C E ΔW Q v v (2) 等温膨胀 J 1073.12ln /3⨯===A A RT V W C T vRTlnV对等温过程ΔE =0,所以J 1073.13⨯==T T W Q(3) 绝热膨胀T D =T A (V A /V D )γ-1=300 ×(0.5)0.4=227.4K对绝热过程a 0Q =,则有 ()()J 1051.125Δ3,⨯=-=-=-=D A D A m V a T T R T T C E W v 13 -22 绝热汽缸被一不导热的隔板均分成体积相等的A 、B 两室,隔板可无摩擦地平移,如图所示.A 、B 中各有1mol 氮气,它们的温度都是T0 ,体积都是V0 .现用A 室中的电热丝对气体加热,平衡后A 室体积为B 室的两倍,试求(1) 此时A 、B 两室气体的温度;(2) A 中气体吸收的热量.分析 (1) B 室中气体经历的是一个绝热压缩过程,遵循绝热方程TVγ-1 =常数,由此可求出B 中气体的末态温度TB .又由于A 、B 两室中隔板可无摩擦平移,故A 、B 两室等压.则由物态方程pV A =νRT A 和pV B =νRT B 可知T A =2T B .(2) 欲求A 室中气体吸收的热量,我们可以有两种方法.方法一:视A 、B 为整体,那么系统(汽缸)对外不作功,吸收的热量等于系统内能的增量.即QA =ΔE A +ΔE B .方法二:A 室吸热一方面提高其内能ΔE A ,另外对“外界”B 室作功WA.而对B 室而言,由于是绝热的,“外界” 对它作的功就全部用于提高系统的内能ΔEB .因而在数值上W A =ΔE B .同样得到Q A =ΔE A +ΔE B . 解 设平衡后A 、B 中气体的温度、体积分别为T A ,T B 和V A ,V B .而由分析知压强p A =p B =p .由题已知⎩⎨⎧=+=022V V V V V B A B A ,得⎩⎨⎧==3/23/400V V V V BA (1) 根据分析,对B 室有B γB γT V T V 1010--=得 ()0010176.1/T T V V T γB B ==-;0353.2T T T B A == (2) ()()0007.312525ΔΔT T T R T T R E E Q B A A A A =-+-=+= 13-23 0.32 kg 的氧气作如图所示的ABCDA 循环,V 2 =2V 1 ,T 1=300K,T 2=200K,求循环效率.分析 该循环是正循环.循环效率可根据定义式η=W /Q 来求出,其中W 表示一个循环过程系统作的净功,Q 为循环过程系统吸收的总热量. 解 根据分析,因AB 、CD 为等温过程,循环过程中系统作的净功为()()()J 1076.5/ln /ln 32121211⨯=-==+=V V T T R M m V V RT Mm W W W CD AB由于吸热过程仅在等温膨胀(对应于AB 段)和等体升压(对应于DA 段)中发生,而等温过程中ΔE =0,则AB AB W Q =.等体升压过程中W =0,则DA DA E Q Δ=,所以,循环过程中系统吸热的总量为()()()()J 1081.325/ln /ln Δ42112121,121⨯=-+=-+=+=+=T T R M m V V RT Mm T T C M m V V RT Mm E W Q Q Q m V DAAB DA AB 由此得到该循环的效率为 %15/==Q W η13 -24 图(a)是某单原子理想气体循环过程的V -T 图,图中V C =2V A .试问:(1) 图中所示循环是代表制冷机还是热机? (2) 如是正循环(热机循环),求出其循环效率.分析 以正、逆循环来区分热机和制冷机是针对p -V 图中循环曲线行进方向而言的.因此,对图(a)中的循环进行分析时,一般要先将其转换为p -V 图.转换方法主要是通过找每一过程的特殊点,并利用理想气体物态方程来完成.由图(a)可以看出,BC 为等体降温过程,CA 为等温压缩过程;而对AB 过程的分析,可以依据图中直线过原点来判别.其直线方程为V =CT ,C 为常数.将其与理想气体物态方程pV =m/MRT 比较可知该过程为等压膨胀过程(注意:如果直线不过原点,就不是等压过程).这样,就可得出p -V 图中的过程曲线,并可判别是正循环(热机循环)还是逆循环(制冷机循环),再参考题13-23的方法求出循环效率.解 (1) 根据分析,将V -T 图转换为相应的p -V 图,如图(b)所示.图中曲线行进方向是正循环,即为热机循环.(2) 根据得到的p -V 图可知,AB 为等压膨胀过程,为吸热过程.BC 为等体降压过程,CA 为等温压缩过程,均为放热过程.故系统在循环过程中吸收和放出的热量分别为()A B m p T T C M m Q -=,1 ()()A C A A B m V V V RT Mm T T C M m Q /ln ,2+-= CA 为等温线,有T A =T C ;AB 为等压线,且因V C =2V A ,则有T A =T B /2.对单原子理想气体,其摩尔定压热容C p ,m =5R/2,摩尔定容热容C V ,m =3R/2.故循环效率为()()3/125/2ln 2312/5/2ln 321/112=+-=⎥⎦⎤⎢⎣⎡+-=-=A A A T T T Q Q η 13 -25 一卡诺热机的低温热源温度为7℃,效率为40%,若要将其效率提高到50%,问高温热源的温度需提高多少?解 设高温热源的温度分别为1T '、1T '',则有12/1T T η'-=', 12/1T T η''-=''其中T 2 为低温热源温度.由上述两式可得高温热源需提高的温度为K 3.931111Δ211=⎪⎪⎭⎫ ⎝⎛'--''-='-''=T ηηT T T 13 -26 一定量的理想气体,经历如图所示的循环过程.其中AB 和CD 是等压过程,BC 和DA 是绝热过程.已知B 点温度T B =T 1,C 点温度T C =T 2.(1) 证明该热机的效率η=1-T 2/T 1 ,(2) 这个循环是卡诺循环吗?分析 首先分析判断循环中各过程的吸热、放热情况.BC 和DA 是绝热过程,故Q BC 、Q DA 均为零;而AB 为等压膨胀过程(吸热)、CD 为等压压缩过程(放热),这两个过程所吸收和放出的热量均可由相关的温度表示.再利用绝热和等压的过程方程,建立四点温度之间的联系,最终可得到求证的形式. 证 (1) 根据分析可知 ()()⎪⎪⎭⎫ ⎝⎛-⎪⎪⎭⎫ ⎝⎛--=---=---=-=B A C D B C A B D CA B m p C D m p AB CD T T T T T T T T T T T T C MT T C M m Q Q η1/11111,, (1) 与求证的结果比较,只需证得BA C D T T T T = .为此,对AB 、CD 、BC 、DA 分别列出过程方程如下V A /T A =V B /T B (2)V C /T C =V D /T D (3) C γC B γB T V T V 11--= (4)A γA D γD T V T V 11--= (5)联立求解上述各式,可证得η=1-T C /T B =1-T 2/T 1(2) 虽然该循环效率的表达式与卡诺循环相似,但并不是卡诺循环.其原因是:① 卡诺循环是由两条绝热线和两条等温线构成,而这个循环则与卡诺循环不同;② 式中T 1、T 2的含意不同,本题中T 1、T 2只是温度变化中两特定点的温度,不是两等温热源的恒定温度.13 -27 一小型热电厂内,一台利用地热发电的热机工作于温度为227℃的地下热源和温度为27℃的地表之间.假定该热机每小时能从地下热源获取1.8 ×1011J的热量.试从理论上计算其最大功率为多少?分析 热机必须工作在最高的循环效率时,才能获取最大的功率.由卡诺定理可知,在高温热源T 1和低温热源T 2之间工作的可逆卡诺热机的效率最高,其效率为η=1-T 2/T 1 .由于已知热机在确定的时间内吸取的热量,故由效率与功率的关系式Q pt Q W η//==,可得此条件下的最大功率.解 根据分析,热机获得的最大功率为()-1712s J 100.2//1/⋅⨯=-==t Q T T t Q ηp13 -28 有一以理想气体为工作物质的热机,其循环如图所示,试证明热()()1/1/12121---=p p V V γη 分析 该热机由三个过程组成,图中AB 是绝热过程,BC 是等压压缩过程,CA 是等体升压过程.其中CA 过程系统吸热,BC 过程系统放热.本题可从效率定义CA BC Q Q Q Q η/1/112-=-=出发,利用热力学第一定律和等体、等压方程以及γ=C p,m 桙C V,m 的关系来证明.证 该热机循环的效率为CA BC Q Q Q Q η/1/112-=-=其中Q BC =m /M C p,m (T C -T B ),Q CA =m/M C V,m (T A -T C ),则上式可写为1/1/11---=---=C A CB C A B C T T T T γT T T T γη 在等压过程BC 和等体过程CA 中分别有T B /V 1 =T C /V 2,T A /P 1 =T C /P 2,代入上式得()()1/1/12121---=p p V V γη 13 -29 如图所示为理想的狄赛尔(Diesel)内燃机循环过程,它由两绝热线AB 、CD 和等压线BC 及等体线DA 组成.试证此内燃机的效率为()()()1//1/12312123---=-V V V V γV V ηγγ证 求证方法与题13-28相似.由于该循环仅在DA 过程中放热、BC 过程中吸热,则热机效率为 ()()B C AD B C m p A D m V BCDA T T T T γT T C M T T C M m Q Q η---=---=-=111/1,, (1) 在绝热过程AB 中,有1211--=γB γA V T V T ,即()121//-=γA B V V T T (2)在等压过程BC 中,有23//V T V T B C =,即23//V V T T B C = (3)再利用绝热过程CD,得1311--=γC γD V T V T (4)解上述各式,可证得()()()1//1/12312123---=-V V V V γV V ηγγ 13 -30 如图所示,将两部卡诺热机连接起来,使从一个热机输出的热量,输入到另一个热机中去.设第一个热机工作在温度为T 1和T 2的两热源之间,其效率为η1 ,而第二个热机工作在温度为T 2 和T 3 的两热源之间,其效率为η2.如组合热机的总效率以η=(W 1 +W 2 )/Q 1 表示.试证总效率表达式为η=(1 -η1 )η2 +η1 或 η=1 -T 3/T 1分析 按效率定义,两热机单独的效率分别为η1=W 1 /Q 1和η2=W 2 /Q 2,其中W 1 =Q 1-Q 2 ,W 2 =Q 2-Q 3 .第一个等式的证明可采用两种方法:(1) 从等式右侧出发,将η1 、η2 的上述表达式代入,即可得证.读者可以一试.(2) 从等式左侧的组合热机效率η=(W 1 +W 2 )/Q 1出发,利用η1、η2的表达式,即可证明.由于卡诺热机的效率只取决于两热源的温度,故只需分别将两个卡诺热机的效率表达式η1=1-T 2 /T 1 和η2=1-T 3 /T 2 代入第一个等式,即可得到第二个等式.证 按分析中所述方法(2) 求证.因η1=W 1 /Q 1 、η2=W 2 /Q 2 ,则组合热机效率12211211121Q Q ηηQ W Q W Q W W η+=+=+= (1) 以Q 2 =Q 1-W 1 代入式(1) ,可证得η=η1 +η2 (1-η1 ) (2) 将η1=1-T 2 /T 1 和η2=1-T 3 /T 2代入式(2),亦可证得η=1-T 2 /T 1 +(1-T 3 /T 2 )T 2 /T 1 =1-T 3 /T 113 -31 在夏季,假定室外温度恒定为37℃,启动空调使室内温度始终保持在17 ℃.如果每天有2.51 ×108 J 的热量通过热传导等方式自室外流入室内,则空调一天耗电多少? (设该空调制冷机的制冷系数为同条件下的卡诺制冷机制冷系数的60%)分析 耗电量的单位为kW·h ,1kW·h =3.6 ×106J.图示是空调的工作过程示意图.因为卡诺制冷机的制冷系数为212T T T e k -=,其中T 1为高温热源温度(室外环境温度),T 2为低温热源温度(室内温度).所以,空调的制冷系数为e =e k · 60% =0.6 T 2/( T 1 -T 2 )另一方面,由制冷系数的定义,有e =Q 2 /(Q 1 -Q 2 )其中Q 1为空调传递给高温热源的热量,即空调向室外排放的总热量;Q 2是空调从房间内吸取的总热量.若Q ′为室外传进室内的热量,则在热平衡时Q 2=Q ′.由此,就可以求出空调的耗电作功总值W =Q 1-Q 2 .解 根据上述分析,空调的制冷系数为7.8%60212=-=T T T e在室内温度恒定时,有Q 2=Q ′.由e =Q 2 /(Q 1-Q 2 )可得空调运行一天所耗电功W =Q 1-Q 2=Q 2/e =Q ′/e =2.89×107=8.0 kW·h13 -32 一定量的理想气体进行如图所示的逆向斯特林循环(回热式制冷机中的工作循环),其中1→2为等温(T 1 )压缩过程,3→4为等温(T 2 )膨胀过程,其他两过程为等体过程.求证此循环的制冷系数和逆向卡诺循环制冷系数相等.(这一循环是回热式制冷机中的工作循环,具有较好的制冷效果.4→1过程从热库吸收的热量在2→3过程中又放回给了热库,故均不计入循环系数计算.)证明 1→2 过程气体放热2111lnV V RT Q v = 3→4 过程气体吸热 2122lnV V RT Q v = 则制冷系数 e =Q 2 /(Q 1-Q 2 )= T 2/( T 1-T 2 ).与逆向卡诺循环的制冷系数相同.13 -33 物质的量为ν的理想气体,其摩尔定容热容C V,m =3R/2,从状态A(p A ,V A ,T A )分别经如图所示的ADB 过程和ACB 过程,到达状态B(p B ,V B ,T B ).试问在这两个过程中气体的熵变各为多少? 图中AD 为等温线.分析 熵是热力学的状态函数,状态A 与B 之间的熵变ΔSAB 不会因路径的不同而改变.此外,ADB 与ACB 过程均由两个子过程组成.总的熵变应等于各子过程熵变之和,即DB AD AB S S S ΔΔΔ+=或CB AC AB S S S ΔΔΔ+=. 解 (1) ADB 过程的熵变为()()D B p,m A D B D D A T BD P D A T DBAD AB T T C V V T T C T W T Q T Q S S S /ln /ln /d /d /d /d ΔΔΔm p,v vR v +=+=+=+=⎰⎰⎰⎰ (1)在等温过程AD 中,有T D =T A ;等压过程DB 中,有V B /T B =V D /T D ;而C p ,m =C V ,m +R ,故式(1)可改写为()()()()A B A B A B p,m A B B D ADB V T V V V T C V T V T S /ln 23/ln /ln /ln ΔvR vR v vR +=+=(2) ACB 过程的熵变为()()C B V,m A C p,m CB AC BA ACB T TC V T C S S Q/T S /ln /ln ΔΔd Δv v +=+==⎰ (2)利用V C =V B 、p C =p A 、T C /V C =T A /V A 及T B /p B =T C /p C ,则式(2)可写为()()()()()()()A B A B A A B B V,m A B A B A B V,m ACB V T V V V p V p C V V p p V V R C S /ln 23/ln /ln /ln /ln /ln ΔvR vR v vR v v +=+=++=通过上述计算可看出,虽然ADB 及ACB 两过程不同,但熵变相同.因此,在计算熵变时,可选取比较容易计算的途径进行.13 -34 有一体积为2.0 ×10-2m 3的绝热容器,用一隔板将其分为两部分,如图所示.开始时在左边(体积V 1 =5.0 ×10-3m 3)一侧充有1mol 理想气体,右边一侧为真空.现打开隔板让气体自由膨胀而充满整个容器,求熵变.分析 在求解本题时,要注意⎰=BA T Q S d Δ 的适用条件.在绝热自由膨胀过程中,d Q =0,若仍运用上式计算熵变,必然有ΔS =0.显然,这是错误的结果.由于熵是状态的单值函数,当初态与末态不同时,熵变不应为零.出现上述错误的原因就是忽视了公式的适用条件. ⎰=BA T Q S d Δ 只适用于可逆过程,而自由膨胀过程是不可逆的.因此,在求解不可逆过程的熵变时,通常需要在初态与末态之间设计一个可逆过程,然后再按可逆过程熵变的积分式进行计算.在选取可逆过程时,尽量使其积分便于计算.解 根据上述分析,在本题中因初末态时气体的体积V 1 、V 2 均已知,且温度相同,故可选一可逆等温过程.在等温过程中,d Q =d W =p d V ,而VRT M m p =,则熵变为 ()1-12K J 52.11/ln d 1d d Δ12⋅=====⎰⎰⎰V V R M m V V R M m T V p T Q S V V。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
COOH
(4)
COOC2H5
(1)NaOC2H5
COOC2H5 (2)CH3CH2Br
(1)NaOC2H5
(2)
Br
(1)5%NaOH (2)H3O,
(5) COCH3
(1)NaOC2H5
(1)5%NaOH
COOC2H5 (2)ClCH2COC6H5r
(2)H3O,
7. 用化学方法区别下列各组化合物:
C6H5C CHCOCH3 OH
(6) C6H5COCH2COC6H5
C6H5C CHCOC6H5
答案:
苯环和羰基的共轭效应使烯醇式更稳定,所以有上述结果。
烯醇式含量 1.5×10-4 7×10-4 7.5 76.5 90.0 96.0
问题 13.9 乙酰乙酸乙酯的成酸水解式克莱森酯缩合的逆反应,试写出其反应机理。 答案:
问题 13.2 完成下列转变:
(1) CH3CH2CH2COOH
O
(2)
CH3CH2CHCOOH
OH OH CH2COOC2H5
O
(3)
答案:
(1) CH3CH2CH2COOH
(2) CH3COOC2H5
Br2 P
Br2 P
OH COOH
CH3CH2CHCOOH Br
NaOH/H2O
Zn BrCH2COOC2H5
BrCH2CH2Br
H3O △
(3)
HCN
O
H3O
△
(4)
CH3COCl
Zn
H3O
AlCl3
BrCH2COOC2H5
△
6. 用丙二酸二乙酯或乙酰乙酸乙酯制备下列化合物:
(1) CH3CHCH2CH2CH2CH3
OH
(3)
COCH3
(2)
COOH
(4)
(5) CH3COCH2CH2COC6H5
答案:
9. 分子式为C4H4O5的化合物,由两个异构体A、B,都无旋光性,与NaHCO3作用放出CO2。A 与 2,4-二硝基苯肼作用生成相应的腙。B既能使三氯化铁溶液显色,也能与溴水反应。B经 催化加氢生成一对对映体。试写出A、B的结构式和有关化学反应式。 答案:
A. HOOCCOCH2COOH
O
B. HOOCC CHCOOH
(1) C2H5ONa (2) H
部分答案:
C2H5ONa H
O
(1)
O
(2)
(3) CH3CH=CHCOOH
O
O
CH3
O
(4)
CH2COOH (5) C6H5COCH2C6H5
(6) CH3CH2CH2CH2COCH2CH2CH2CH3
4. 有α-H 的酮和没有α-H 的酮也可以起克莱森缩合反应。试写出下列反应的产物:
+ HCOOH
OH
△
问题 13.5 Dieckmann 缩合是指二元羧酸酯进行的分子内的 Claisen 缩合反应。选择合适原料 合成下列化合物:
O
O
CO2C2H5
CO2C2H5
(1)
(2)
答案:
O
(1)
COOC2H5 (1) NaOC2H5
COOC2H5 (2) H3O
COOC2H5
O
COOC2H5
COOH
(5)
(6) COOH
OH O
3. 写出下列反应的主要产物:
H
(1) CH3CHCH2CH2CH2COOH
△
OH
COOH
(2)
△
COOH O
(3) CH3CHCH2COOH
△
CH2COOH
△
(4)
COOH
OH
(1)
(5) C6H5COOC2H5 + C6H5CH2COOC2H5
(2)
(6) CH3CH2CH2CH2COOC2H5
(1)
COCH3
(1)NaOC2H5
(1)5%NaOH
COOC2H5 (2)CH3CH2CH2CH2Br (2)H3O,
(2)
COOC2H5
(1)NaOC2H5
COOC2H5 (2)BrCH2CH2Br
(1)5%NaOH (2)H3O,
(3) COCH3
(1)NaOC2H5
(1)5%NaOH
COOC2H5 (2)BrCH2CH2CH2CH2Br(2)H3O,
(1)丙酮 α-羟基丙酸 丙酮酸
(2)2-丁酮 乙酰乙酸乙酯 丁酸乙酯
(3)水杨酸 乙酰水杨酸
水杨酸甲酯
答案:
(1)不显示酸性的是丙酮;能使溴水退色的是丙酮酸;
(2)不发生碘仿反应的是丁酸乙酯;能使溴水褪色的是乙酰乙酸乙酯;
(3)既能与溴水作用生成沉淀,又能与碳酸氢钠作用放出气体的是水杨酸;只有第一个现
10. 从白花蛇草中提取得到一种化合物,分子式为C9H8O3,能溶于氢氧化钠溶液和碳酸氢钠溶 液中,与三氯化铁作用曾红色,能使溴的四氯化碳溶液褪色,用高锰酸钾氧化得到对羟基苯 甲酸和草酸。试推测该化合物的构造式并写出有关化学反应式。 答案:
HO
CH CH COOH
11. 化合物A,分子式C5H10O,能使高锰酸钾溶液推着,能与乙酰氯反应得到分子式为C7H12O2 的醋酸酯,该酯仍然能使高锰酸钾溶液褪色,当A氧化后所得到的酸酸化时容易失去CO2得到 丙酮,写出A失望构造式和哟关化学反应式。 答案:
NO2
(2)
OCOCH3
(3)
O O 答案:
CHO O
(4)
O
(1)
C6H5CH2Br
Mg (C2H5)2O
(1) C6H5CHO (2) H3O
CH3COOH H
CHO
(2)
HNO3
CH3CHO
H2SO4
OH
(3) (CH3)2CHCHO
HCHO
CH2(COOH)2
△
OH
1. 命名下列化合物:
(1) CH3CH2COCH2COOH
(1)
(CH3)2CCOOH
△
(2) (3)
答案:
OH
(CH3)2CCOOH
OH
(CH3)2CCOOH
OH
稀H2SO4 △
浓H2SO4 △
(1)
(CH3)2CCOOH
△
OH
(2)
(CH3)2CCOOH 稀H2SO4
OH
△
O O
O O
O + CO + H2O
(3)
(CH3)2CCOOH 浓H2SO4
O
H H3C C H2CHC CH2
OH
象的是水杨酸甲酯,只有后一个现象的是乙酰水杨酸。
8. 按要求排列下列化合物的顺序: (1) 碱性由弱到强
OH
(a)
O
(b)
(c) HO
COO
COO (d)
COO
(2) 脱羧反应由易到难 (a)丁酸 (b)β-丁酮酸 (c)丙二酸二乙酯 (d)2-丁酮 (3)烯醇式百分含量由大到小 (a)2,4-戊二酮 (b)乙酰乙酸乙酯 (c)丙二酸二乙酯 (d)2-丁酮 答案: (1)adcb (2)cbad (3)abcd
2. 写出下列化合物的结构式: (1)苹果酸 (2)柠檬酸 (3)水杨酸苯酯 (4)草酸二乙酯 (5)(2S,3R)-2-羟基-3-苯基丁酸 (6)对乙酰基苯甲酸 答案:
OH
(1)
(2) COOH
HOOC
CH2COOH HO C COOH
(3)
CH2COOH
OH COOPh
(4)
COOC2H5
COOC2H5
NaOC2H5
COOC2H5
Br Cl
COOC2H5 COOC2H5
5% NaOH
H3O
COOC2H5 COOC2H5
5% NaOH
H3O
问题 13.12 写出下列反应的产物:
(1) CH3COCH2COCH3 + H2C CHC
(1)
N
KOH C2H5OH
(2) H3O
(2) CH3COCH2NO2 + H2C CHCOOCH3
习题
(2) CH3COCHCOOC2H5
CH3
(3) C6H5CH2COCH2COOC2H5
(4)
CH(COOC2H5)2
CH2CH2CH3
(5) H2C CH CH COOH
பைடு நூலகம்
COCH2C6H5
(6) HOOC CH CH2CH2COOH
答案:
(1)3-氧代戊酸 (2)2-甲基-3-氧代丙酸乙酯 (3)4-苯基-3-氧代丁酸乙酯 (4)2-环己基丙二酸二乙酯 (5)2-正丙基-3-丁烯酸 (6)2-苄基羰基戊二酸
OO O
OO
OH
O OH
O +
OH
O O
O
O
+ O
O
O
OH
O OH
O +O
OH
O
+
HO
O
问题 13.10 由乙酰乙酸乙酯合成下列化合物:
(1) CH3COCH2CH2COOH
答案:
(2) CH3COCH2CH2C6H5
(1) COCH3
NaOC2H5
COOC2H5
(2) COCH3
COOC2H5
NaOC2H5
问题 13.7 指出下列化合物中,哪些有红外光谱图上没有羟基吸收峰。
(1) CH3COCH2COCH3
(2) C6H5OCOCH2COOCH3
(3) CH3COCH2CH3
