第三节醛酮自制
醛和酮3
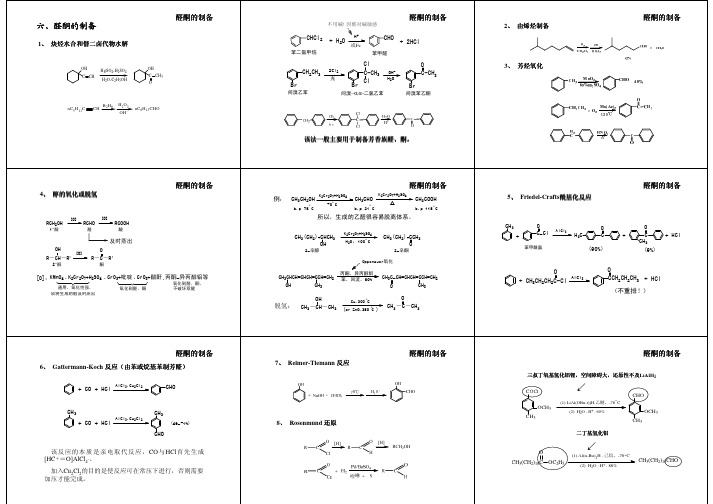
该法一般主要用于制备芳香族醛该法一般主要用于制备芳香族醛、。
R COCI[H]R COHRCH2OH[H]羰基合成由α-烯烃合成多一个碳的醛!+ COCH [Co(CO)4],加压CH -CH 八羰基二钴CH 3CH 2CH CHO CH 3CHCHOCH3正丁醛(多)异丁醛(少)H 2CH=CH 2+CO [Co(CO)4],加压CH CH-CH C OO=CNCH OOCC=CCOOH碳负离子的反应C CCH6HBrC CCHC6Br2EtCO2CHCCH3H5C=CH-OH35CHCHO -CO产生碳负离子OHC CHCO-BrH COOHCH 3COOH (RCH COOH)Benzoin condensation芳香醛在氰化钾的作用下芳香醛在氰化钾的作用下,,发生双分子缩合发生双分子缩合,,α-羟基酮的反应------安息香缩合反应安息香缩合反应。
俗称安息香ArCH-CAr OKCN 醇碳负离子的反应反应机理HNO 3C CO O 碳负离子的反应CHO碳负离子的反应反应机理反应机理::R 1R 2CH-Xph 3PR 1R 2C H -Pph 3 XphLi -HXR 1R 2C-Pph 3R 1R 2C=Pph 3蒽醌类染料的重要组成部分。
蒽醌类染料的重要组成部分。
醛酮的制备方法.
要控制氧化条件防止醛的进一步氧化。用CrO3-醋酐能防止醛
的氧化:
O
CH3
CH(OCCH3)2
CHO
CrO3-Ac2O
H2O
HOAc/H2SO4
Br
Br
Br
在这里生成的中间物二乙酸酯不易继续被氧化,它水解后即 得芳醛。
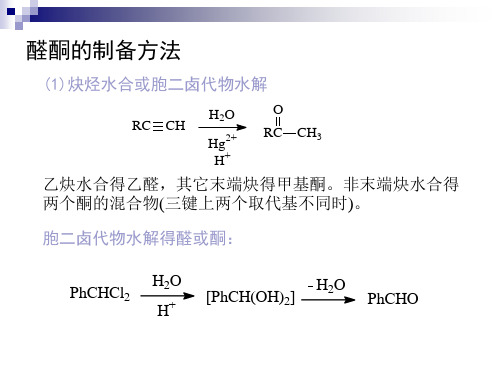
(4) 由醇氧化或脱氢(见醇酚醚章) (5) Friedal-Crafts酰基化(见芳香烃章) (6) Gattermann-Koch反应(见芳香烃章) (7) Reimer-Tiemann反应(见醇酚醚章) (8) Rosenm炔烃水合或胞二卤代物水解
RC CH
H2O
Hg2+ H+
O RC CH3
乙炔水合得乙醛,其它末端炔得甲基酮。非末端炔水合得 两个酮的混合物(三键上两个取代基不同时)。
胞二卤代物水解得醛或酮:
PhCHCl2
H2O H+
[PhCH(OH)2]
H2O
PhCHO
(2) 由烯烃制备 (a)烯烃氧化
i) 烯烃臭氧化然后还原水解得醛或酮 ii) 氢甲醛化
RCH=CH2
例如:
H2, CO, Co2(CO)8 加热,加压
RCH2CH2CHO (主) + RCHCH3 (次) CHO
H2, CO, Co2(CO)8 加热,加压
CHO 65%
(3) 由芳烃氧化
CH3 MnO2
65% H2SO4
CHO 40%
O RCCl + H2
Pd+BaSO4 喹啉+S
O RCH
(9) 酰氯与烷基铜锂作用
COCl + Me2CuLi
醚 78°C
COMe 81%
醛酮的合成

经典化学合成反应标准操作醛酮的合成编者:雷耀辉,周盛峰药明康德新药开发有限公司化学合成部目录1.前言 (4)2.由醇合成醛酮 (5)2.1铬(VI)试剂 (5)2.1.1 Jones氧化(Cr2O3/H2SO4/acetone) (5)2.1.2 Collins氧化(Cr2O3.2Py) (6)2.1.3 PCC(Pyrindium Chlorochromate)氧化 (9)2.1.4 PDC(Pyrindium Dichromate)氧化 (10)2.2 用活性MnO2氧化 (11)2.3用DMSO氧化 (12)2.3.1 DMSO-DCC氧化 (Pfitzner-Moffatt Oxidation or Moffatt Oxidation) (12)2.3.2 DMSO-(COCl)2氧化(Swern Oxidation or Moffatt-Swern Oxidation) (14)2.3.3 DMSO-Cl2,DMS-NCS (Corey-Kim氧化) (15)2.3.4 DMSO-SO3-Pyridine (17)2.4 用氧铵盐氧化 (18)2.5 用高价碘试剂氧化 (18)2.6 亚硝酸钠和醋酐氧化 (20)2.7 其它氧化方法 (21)2.8 1,2-二醇的氧化 (22)3.由卤化物合成醛酮 (25)3.1 由伯卤甲基和仲卤甲基的氧化合成醛酮 (25)3.1.1 用DMSO氧化(Kornblum反应) (25)3.1.2用硝基化合物氧化(Hass反应) (26)3.1.3用乌洛托品氧化(Sommelet反应) (26)3.1.4用对亚硝基二甲苯胺氧化吡啶翁盐氧化(Kröhnke反应) (28)3.1.5用胺氧化物氧化 (28)3.2 由二卤甲基或二卤亚甲基合成醛酮 (28)3.3 由有机金属化合物的酰化合成醛酮 (29)3.4 由Pd催化反应合成醛 (31)4.由活泼甲基或活泼亚甲基烷烃合成醛酮 (32)4.1 用SeO2氧化合成醛酮 (32)4.2用空气氧化合成酮 (34)4.3 用铬酸氧化合成酮 (35)4.4用高锰酸盐氧化合成酮 (36)4.5 用醌氧化合成酮 (36)5.由羧酸及其衍生物合成醛酮 (37)5.1由羧酸合成醛 (37)5.1.3由羧酸合成酮 (38)5.2由酰氯及酸酐合成醛酮 (40)5.2.1用Rosenmund法合成 (40)5.2.2用金属氢化物还原 (41)5.3由酯及内酯合成醛 (42)5.4由酰胺合成醛酮 (43)5.5由酯或酰氯经Weinreb酰胺合成醛酮 (46)5.6由氰合成醛酮 (49)6. 由烯烃合成醛酮 (53)6.1 由烯烃臭氧氧化合成醛 (53)6.2 烯烃用OsO4/NaIO4氧化合成醛 (55)6.3 烯烃经由有机硼化合物中间体的烯烃甲酰化合成醛 (56)6.4 由烯烃的加氢甲酰化合成醛(羰基合成法) (56)6.5 由烯烃的甲酰化合成醛 (57)6.6烯烃经加成-氧化反应合成酮 (58)6.7 其它方法 (60)7.由炔烃合成醛酮 (61)7.1 由加成-氧化反应合成醛酮 (61)7.2 由氧化反应合成酮 (61)7.3 由加成-水解反应合成酮 (61)7.4 由加成-还原反应合成酮 (62)7.5 由加成-烷基化,酰化等反应合成酮 (62)8. 由醚及环氧化合物合成醛酮 (63)8.1 Claisen重排 (63)8.2酸催化下环氧化物重排 (64)8.3氧化法 (65)8.4 水解法合成醛酮 (66)9. 由胺合成醛 (68)9.1胺的氧化 (68)9.2 由胺经由西佛碱的方法 (68)9.3 自苯胺衍生物合成 (69)10. 由硝基化合物合成醛酮 (71)11 由砜合成醛酮 (74)12.由芳环合成醛酮 (75)12.1 由芳环的Friedel-Crafts反应合成芳基酮 (75)12.2 由芳环的甲酰化反应合成芳香醛 (79)12.2.3 Reimer-Tiemann 甲酰化 (83)12.2.4 Gattermann甲酰化 (84)12.2.5 多聚甲醛/甲醇镁苯酚甲酰化 (85)12.2.6氯化锡/多聚甲醛苯酚甲酰化 (86)13. 由Dieckmann 缩合脱酸合成酮 (87)14 Michael 反应和类似反应(Addition, Condensation) (89)15 由合成子合成醛酮 (90)16. 参考文献 (94)1.前言醛和酮是一类重要的有机化合物,其合成在有机合成中占有非常重要的地位。
03-5 醛酮的合成

1,41,4-加成反应制酮
R2CH=CHY COR CN R' R2 RCOCHCHCH2Y COOR
酮与亲电试剂的1 加成(Michael反应 反应) ① 酮与亲电试剂的1,4-加成(Michael反应)
COH
烯胺与亲电烯的1 ② 烯胺与亲电烯的1,4-加成
N + RCH=CHY N CHCHY R CN COOR H2O O CHCH2Y R
⑤ 芳烃的侧链氧化
ArCH3 CrO3 (CH3CO)2
NO2 X
ArCH(OCOCH3)2
CN
HCl H2O
ArCHO
COOR 不受影响
ArCOCH3
SeO2
ArCOCHO
2. 还原反应
① 酰卤的还原
O RCCl H2 Pd-BaSO4 O RCH
酰胺、 ② 酯、酰胺、羧酸的还原
O RCZ Z=-OR' -NR'2 -OH LiAlH(OR')3 O RCH
O n-C6H13MgBr + CH3COCl THF n-C6H13CCH3
7. 缩合生成醛酮
① 羟醛缩合
RCH2CHO OHRCH2CH=CCHO R
② 酮酯缩合
CH3COCH2R + HCOOC2H5 NaOC2H5 CH3COCHCHO R
③ 酯缩合
RCH2COOC2H5 RCH2COCHCOOC2H5 R
ArH + HCN + HCl
OH
ZnCl2
ArCH=NHHCl
CHO
H2O
ArCHO
Zn(CN)2/HCl H2O OH
OH
OH
芳烃或烯烃用甲酰胺甲酰化(Vilsmeier反应 反应) ③芳烃或烯烃用甲酰胺甲酰化(Vilsmeier反应)
3.3醛酮教学设计2023-2024学年高二下学期化学人教版(2019)选择性必修3

3. 实验法:安排学生进行醛酮的制备实验,让学生通过实际操作观察实验现象,增强对醛酮化学性质的理解和记忆。
教学手段:
1. 多媒体课件:利用多媒体课件,以图文并茂的形式展示醛酮的结构、化学反应过程和实验操作,增强学生的直观感受,提高学习兴趣。
引导学生思考这些案例对实际生活或学习的影响,以及如何应用醛酮解决实际问题。
小组讨论:让学生分组讨论醛酮的未来发展或改进方向,并提出创新性的想法或建议。
4. 学生小组讨论(10分钟)
目标:培养学生的合作能力和解决问题的能力。
过程:
将学生分成若干小组,每组选择一个与醛酮相关的主题进行深入讨论。
小组内讨论该主题的现状、挑战以及可能的解决方案。
3.利用多媒体课件,生动展示实验过程和结果
4.注重课堂互动,鼓励学生提问和发表见解
5.及时给予反馈,帮助学生巩固所学知识
八、教学难点
1.醛酮的结构特点
2.醛酮的氧化反应、加成反应和缩合反应的机理
3.实验操作的安全性和注意事项
九、教学准备
1.教材和实验器材的准备
2.多媒体课件的制作
3.实验方案的设计和安全措施的落实
- 加成反应机理:醛酮中的醛基或酮基与氢气、卤素、醇等物质发生加成反应,形成新的化合物。
- 缩合反应机理:醛酮分子之间通过缩合反应,形成高分子化合物,如聚酮、聚醛等。
4. 题目:分析醛酮在有机合成中的应用实例。
答案:
- 实例1:将醛酮与氢气反应,生成相应的醇。
- 实例2:将醛酮与卤素反应,生成相应的卤化物。
- 醛酮的化学性质,包括氧化反应、加成反应和缩合反应
第三章 第三节 醛 酮-人教版高二化学选择性必修3课件

O
还原性
C
H
醛基中碳氢 碳 键较活泼,能被 氢 键 氧化成相应羧酸。
3、化学性质 (1)氧化反应
① 银镜反应
a、配制银氨溶液:取一洁净试管,加入1ml 2%的 AgNO3溶液,再逐滴滴入2%的稀氨水,至生成的 沉淀恰好溶解。
b、水浴加热生成银镜:在配好的上述银氨溶液中滴 入三滴乙醛溶液,然后把试管放在热水浴中静置。
微点拨:酮与醛可能为官能团异构,如丙醛与丙酮互 为同分异构体。
课堂小结
羰基的两端连有两个烃基的化合物 饱和的一元酮为CnH2nO(n≥3)
O R1—C—R2
主要化学性质
1、加成反应:
O
=
R1—C—R2
+ H2
Ni △
OH | R1—CH—R2
2、难被氧化(燃烧除外):难被银氨溶液或新制氢 氧化铜氧化。
主链的碳原子数称“某醛” 。
(2)编号位: 从醛基一端开始,醛基中的碳原子编
号为1 。
(3)写名称: 把取代基名称写在母体名称前,用
“二、三、四等”写出醛的个数。
CH3 CH3—CH—CHO
2-甲基丙醛
CHO CH3—CH—CH2—CH3
2-甲基丁醛
5、常见的醛
甲醛: HCHO是最简单的醛,为无色、有刺激性气味
混合加入40%的乙醛溶液加热至沸腾,无红色沉淀,
实验失败的原因是( B )
A.乙醛溶液太少
B.氢氧化钠不够用
C.硫酸铜不够用
D.加热时间不够
2、为了鉴别己烯、甲苯和丙醛,使用的试剂组先
后关系正确的是 ( A )
A. 新制氢氧化铜悬浊液及溴水 B. 高锰酸钾酸性溶液及溴水 C. 银氨溶液及高锰酸钾酸性溶液 D. 新制氢氧化铜悬浊液及银氨溶液
醛酮的合成

氧化成醛(和/或酸)和酮的方法。
OH
CrO3 C5H5N
O
Collins氧化法是在Sarett氧化法(以吡啶为溶剂)基础上的改进,
以二氯甲烷为溶剂氧化伯醇为醛
PCC (氯铬酸吡啶鎓盐)氧化
PCC易于合成和保存,操作简单,是将伯醇和仲醇氧化成 醛和酮的应用最广的氧化方法。PCC中所用的碱除吡啶外, 也可以是其它碱,且随着碱性部分碱性的增强,氧化的选择 性也提高。其中,DMAP· HCrO3Cl为适用于烯丙醇类及苄醇 类的选择性氧化试剂。
OH HO DMAP, HCrO3Cl O HO
PCC的氧化以均相反应为主,但有的方法是将催化剂吸附于 硅胶、氧化铝等无机载体或离子交换树脂等有机高分子载体 上,对醇作非均相催化氧化。后处理简单并可控制反应的选 择性。
2017/12/28
PDC(Pyrindium Dichromate)氧化
PDC的氧化能力较PCC强,其氧化作用一般在中性条件下进 行。PDC的氧化一般在二氯甲烷中进行,如在DMF中进行时, 氧化性增强,能将伯醇最终氧化成酸。
P OH N C N i-Pr O
H2PO4, DMSOI, benzene, 25 oC
(Organic Syntheses, Coll. Vol. 6, p.218; Vol. 56, p.99)
DMSO-Cl2,DMS-NCS
(Corey-Kim氧化)
2017/12/28
用DMSO-Cl2和DMS-NCS体系使醇氧化虽应用广泛且收率也高, 但还是以DMSO-(COCl)2氧化较为方便。
2017/12/28
DMSO-(COCl)2氧化
醛酮的合成-060331

经典化学合成反应标准操作醛酮的经典合成目录1.前言 (4)2.由醇合成醛酮 (4)2.1铬(VI)试剂 (4)2.1.1 Jones氧化(Cr2O3/H2SO4/acetone) (4)2.1.2 Collins氧化(Cr2O3.2Py) (5)2.1.3 PCC(Pyrindium Chlorochromate)氧化 (8)2.1.4 PDC(Pyrindium Dichromate)氧化 (9)2.2 用活性MnO2氧化 (10)2.2.1 用活性MnO2氧化示例一: (10)2.3用DMSO氧化 (11)2.3.1 DMSO-(COCl)2氧化(Swern Oxidation) (11)2.3.2 DMSO-SO3-Pyridine (12)2.4 用氧铵盐氧化 (13)2.4.1 用氧铵盐氧化示例: (13)2.5 用高价碘试剂氧化 (14)2.5 .1 Dess-Martin氧化反应示例: (14)2.5.2 IBX氧化反应示例: (15)2.6 亚硝酸钠和醋酐氧化 (15)2.6.1 亚硝酸钠和醋酐氧化示例 (15)2.6 TPAP-NMO 氧化 (16)2.6.1 TPAP-NMO 氧化示例 (16)2.7 1,2-二醇的氧化 (16)2.7.1 1,2-二醇的氧化示例一: (17)2.7.1 其他1,2-二醇的氧化相关文献: (18)3.由卤化物合成醛酮 (18)3.1 由伯卤甲基和仲卤甲基的氧化合成醛酮 (18)3.1.1 用DMSO氧化(Kornblum反应) (18)3.1.2用硝基化合物氧化(Hass反应) (20)3.1.3用乌洛托品氧化(Sommelet反应) (21)3.1.4用对亚硝基二甲苯胺氧化吡啶翁盐氧化(Kröhnke反应) (22)3.1.5用胺氧化物氧化 (22)3.2 由二卤甲基或二卤亚甲基合成醛酮 (23)3.2.1 由二卤甲基合成醛反应示例: (23)3.3 由有机金属化合物的酰化合成醛酮 (24)3.3.1 由有机金属化合物的酰化合成醛酮示例 (25)3.4 由Pd催化反应合成醛 (25)4.由活泼甲基或活泼亚甲基烷烃合成醛酮 (25)4.1 用SeO2氧化合成醛酮 (26)4.1.1 用SeO2氧化合成醛酮示例 (26)4.2用空气氧化合成酮 (26)4.2.1用空气氧化合成酮反应示例: (27)4.3 用铬酸氧化合成酮 (27)4.3.1 用铬酸氧化合成酮示例 (27)4.4用高锰酸盐氧化合成酮 (29)4.5 用醌氧化合成酮 (29)5.由羧酸及其衍生物合成醛酮 (30)5.1由羧酸合成醛 (30)5.1.1用金属氢化物还原 (30)5.1.2由脱CO2合成醛 (31)5.1.3由羧酸合成酮 (31)5.2由酰氯及酸酐合成醛酮 (33)5.2.1用Rosenmund法合成 (33)5.2.2用金属氢化物还原 (34)5.3由酯及内酯合成醛 (35)5.3.1 酯通过DIBAL还原为醛示例: (36)5.4由酰胺合成醛酮 (36)5.4.1 由酰胺合成醛酮 (37)5.4.2 McFadyen-Stevens Reaction (38)5.5由酯或酰氯经Weinreb酰胺合成醛酮 (39)5.5.1 由Weinreb酰胺还原合成醛反应示例一 (40)5.5.2由Weinreb酰胺还原合成酮反应示例: (41)5.6由氰合成醛酮 (41)5.6.1DIBAL 还原腈到醛示例(最重要的方法) (42)5.6.2Li(EtO)3AlH 还原腈到醛示例(较重要的方法) (43)5.6.3Ranney Ni 加氢还原氰到合成醛示例 (43)5.6.4有机金属试剂对腈加成合成酮示例 (44)6. 由烯烃、芳环合成醛酮 (46)6.1 由烯烃臭氧氧化合成醛 (46)6.2 烯烃用OsO4/NaIO4氧化合成醛 (47)6.3 烯烃经由有机硼化合物中间体的烯烃甲酰化合成醛 (47)6.5 由烯烃的甲酰化合成醛 (48)6.5.1 Vilsmeyer反应 (48)6.5.2 Duff’s 甲酰化 (51)6.5.3 Reimer-Tiemann 甲酰化 (52)6.5.4 Gattermann甲酰化 (53)6.5.5 多聚甲醛/甲醇镁苯酚甲酰化 (53)6.5.6氯化锡/多聚甲醛苯酚甲酰化 (54)6.5.7重氮化后甲酰化 (54)6.6烯烃经加成-氧化反应合成酮 (56)6.6.1 烯烃经加成-氧化反应合成酮示例 (56)7. 由炔烃合成醛酮 (57)7.1 由加成-氧化反应合成醛酮 (57)7.2 由氧化反应合成酮 (57)7.3 由加成-水解反应合成酮 (58)7.4 由加成-还原反应合成酮 (59)7.5 由加成-烷基化,酰化等反应合成酮 (59)8. 由醚及环氧化合物合成醛酮 (59)8.1 Claisen重排 (59)8.2酸催化下环氧化物重排 (61)8.2.1 酸催化下环氧化物重排合成醛酮示例一 (61)8.3氧化法 (61)8.4 水解法缩醛或酮合成醛酮 (61)9. 由胺合成醛 (62)9.1胺的氧化 (62)9.1.1 胺的氧化合成醛反应示例: (63)9.2 由胺经由西佛碱的方法 (64)9.2.1 由胺经由西佛碱合成醛示例 (64)9.3 自苯胺衍生物合成 (64)10. 由硝基化合物合成醛酮 (64)11. 由Friedel-Crafts反应合成芳基酮 (65)11.1 由Friedel-Crafts反应合成芳基酮示例 (68)12. Dieckmann 缩合脱酸 (69)13. 由合成子合成醛酮 (71)14. 由砜合成醛酮 (71)15. Michael 反应和类似反应(Addition, Condensation) (71)1.前言醛和酮是一类重要的有机化合物,其合成在有机合成中占有非常重要的地位。
醛酮的合成-060331

经典化学合成反应标准操作醛酮的经典合成编者:雷耀辉,周盛峰药明康德新药开发有限公司化学合成部目录1.前言 (4)2.由醇合成醛酮 (4)2.1铬(VI)试剂 (4)2.1.1 Jones氧化(Cr2O3/H2SO4/acetone) (4)2.1.2 Collins氧化(Cr2O3.2Py) (5)2.1.3 PCC(Pyrindium Chlorochromate)氧化 (7)2.1.4 PDC(Pyrindium Dichromate)氧化 (9)2.2 用活性MnO2氧化 (10)2.2.1 用活性MnO2氧化示例一: (10)2.3用DMSO氧化 (11)2.3.1 DMSO-(COCl)2氧化(Swern Oxidation) (11)2.3.2 DMSO-SO3-Pyridine (12)2.4 用氧铵盐氧化 (13)2.4.1 用氧铵盐氧化示例: (13)2.5 用高价碘试剂氧化 (14)2.5 .1 Dess-Martin氧化反应示例: (14)2.5.2 IBX氧化反应示例: (15)2.6 亚硝酸钠和醋酐氧化 (15)2.6.1 亚硝酸钠和醋酐氧化示例 (15)2.6 TPAP-NMO 氧化 (16)2.6.1 TPAP-NMO 氧化示例 (16)2.7 1,2-二醇的氧化 (16)2.7.1 1,2-二醇的氧化示例一: (17)2.7.1 其他1,2-二醇的氧化相关文献: (18)3.由卤化物合成醛酮 (18)3.1 由伯卤甲基和仲卤甲基的氧化合成醛酮 (18)3.1.1 用DMSO氧化(Kornblum反应) (18)3.1.2用硝基化合物氧化(Hass反应) (20)3.1.3用乌洛托品氧化(Sommelet反应) (21)3.1.4用对亚硝基二甲苯胺氧化吡啶翁盐氧化(Kröhnke反应) (22)3.1.5用胺氧化物氧化 (22)3.2 由二卤甲基或二卤亚甲基合成醛酮 (22)3.2.1 由二卤甲基合成醛反应示例: (23)3.3 由有机金属化合物的酰化合成醛酮 (24)3.3.1 由有机金属化合物的酰化合成醛酮示例 (25)3.4 由Pd催化反应合成醛 (25)4.由活泼甲基或活泼亚甲基烷烃合成醛酮 (25)4.1 用SeO2氧化合成醛酮 (26)4.1.1 用SeO2氧化合成醛酮示例 (26)4.2用空气氧化合成酮 (26)4.2.1用空气氧化合成酮反应示例: (27)4.3 用铬酸氧化合成酮 (27)4.3.1 用铬酸氧化合成酮示例 (27)4.4用高锰酸盐氧化合成酮 (29)4.5 用醌氧化合成酮 (29)5.由羧酸及其衍生物合成醛酮 (30)5.1由羧酸合成醛 (30)5.1.1用金属氢化物还原 (30)5.1.2由脱CO2合成醛 (31)5.1.3由羧酸合成酮 (31)5.2由酰氯及酸酐合成醛酮 (33)5.2.1用Rosenmund法合成 (33)5.2.2用金属氢化物还原 (34)5.3由酯及内酯合成醛 (35)5.3.1 酯通过DIBAL还原为醛示例: (35)5.4由酰胺合成醛酮 (36)5.4.1 由酰胺合成醛酮 (37)5.4.2 McFadyen-Stevens Reaction (38)5.5由酯或酰氯经Weinreb酰胺合成醛酮 (39)5.5.1 由Weinreb酰胺还原合成醛反应示例一 (40)5.5.2由Weinreb酰胺还原合成酮反应示例: (41)5.6由氰合成醛酮 (41)5.6.1DIBAL 还原腈到醛示例(最重要的方法) (42)5.6.2Li(EtO)3AlH 还原腈到醛示例(较重要的方法) (42)5.6.3Ranney Ni 加氢还原氰到合成醛示例 (43)5.6.4有机金属试剂对腈加成合成酮示例 (44)6. 由烯烃、芳环合成醛酮 (45)6.1 由烯烃臭氧氧化合成醛 (45)6.2 烯烃用OsO4/NaIO4氧化合成醛 (46)6.3 烯烃经由有机硼化合物中间体的烯烃甲酰化合成醛 (46)6.5 由烯烃的甲酰化合成醛 (47)6.5.1 Vilsmeyer反应 (47)6.5.2 Duff’s 甲酰化 (50)6.5.3 Reimer-Tiemann 甲酰化 (51)6.5.4 Gattermann甲酰化 (52)6.5.5 多聚甲醛/甲醇镁苯酚甲酰化 (52)6.5.6氯化锡/多聚甲醛苯酚甲酰化 (53)6.5.7重氮化后甲酰化 (53)6.6烯烃经加成-氧化反应合成酮 (55)6.6.1 烯烃经加成-氧化反应合成酮示例 (55)7. 由炔烃合成醛酮 (56)7.1 由加成-氧化反应合成醛酮 (56)7.2 由氧化反应合成酮 (56)7.3 由加成-水解反应合成酮 (57)7.4 由加成-还原反应合成酮 (58)7.5 由加成-烷基化,酰化等反应合成酮 (58)8. 由醚及环氧化合物合成醛酮 (58)8.1 Claisen重排 (58)8.2酸催化下环氧化物重排 (60)8.2.1 酸催化下环氧化物重排合成醛酮示例一 (60)8.3氧化法 (60)8.4 水解法缩醛或酮合成醛酮 (60)9. 由胺合成醛 (61)9.1胺的氧化 (61)9.1.1 胺的氧化合成醛反应示例: (62)9.2 由胺经由西佛碱的方法 (63)9.2.1 由胺经由西佛碱合成醛示例 (63)9.3 自苯胺衍生物合成 (63)10. 由硝基化合物合成醛酮 (63)11. 由Friedel-Crafts反应合成芳基酮 (64)11.1 由Friedel-Crafts反应合成芳基酮示例 (66)12. Dieckmann 缩合脱酸 (68)13. 由合成子合成醛酮 (70)14. 由砜合成醛酮 (70)15. Michael 反应和类似反应(Addition, Condensation) (70)1.前言醛和酮是一类重要的有机化合物,其合成在有机合成中占有非常重要的地位。
醛酮的合成与应用

醛酮的合成与应用作为有机化学中重要的官能团,醛酮在合成化学和药物化学领域具有广泛的应用。
本文将介绍醛酮的合成方法和其在不同领域的应用。
一、醛酮的合成方法1.1 氧化法:醛酮可以通过氧化反应合成,常用的氧化剂有氧气、过氧化氢等。
例如,醇可以通过氧化反应生成醛酮。
氧化反应可以由过渡金属催化剂或非金属催化剂促进。
1.2 重排法:通过醇的重排反应可以得到醛酮。
这种方法通常需要高温和特定的催化剂来进行反应。
1.3 羰基化合物的反应:醛酮可以由羰基化合物的还原、氧化或加成反应得到。
例如,醛可以通过氧化还原反应生成醛酮。
1.4 脱水反应:醛酮可以通过脱水反应合成。
在酸性条件下,两个醛分子可以进行脱水缩合反应生成醛酮。
二、醛酮的应用2.1 有机合成中的应用:醛酮是有机合成中重要的中间体。
它可以作为合成醇、酸、酮等有机化合物的起始物。
醛酮可以用于合成抗生素、激素、杀虫剂等药物。
2.2 化妆品中的应用:醛酮具有良好的防腐和抗菌作用,因此常被添加到化妆品中,用于保护化妆品的稳定性和延长其使用寿命。
2.3 食品工业中的应用:醛酮可以用作食品中的香精和香料,增添食物的味道和风味。
同时,醛酮还可以作为防腐剂,延长食品的保质期。
2.4 医药领域中的应用:醛酮是许多药物的重要结构单元。
通过调整醛酮的结构,可以获得不同的生物活性和药理作用。
例如,肾上腺皮质激素类药物中常含有醛酮结构。
2.5 材料科学中的应用:醛酮可以用于制备聚合物材料和涂料。
醛酮基团可以与其他功能基团反应,形成交联聚合物,提高材料的机械性能和热稳定性。
结论:综上所述,醛酮的合成方法多样,并且在有机合成、化妆品、食品工业、医药领域和材料科学等多个领域中有广泛的应用。
随着合成化学和有机化学的发展,醛酮的合成方法将继续改进,并且醛酮在更多领域的应用将不断扩展。
《醛酮的合成》课件

3. 氧化醛法
氧化醛法是合成醛的常用方法之一。通过一系列反应原理和机理,我们将介 绍氧化醛法的实验步骤、结果与分析。
4. 加成反应
加成反应是合成醛的另一种方法。了解加成反应的原理、机理以及实验步骤、 结果与分析。
5. 羟酮合成法
羟酮合成法是合成酮的一种常见方法。深入了解羟酮合成法的原理、机理以 及实验步骤、结果与分析。
6. 卡宾化反应
卡宾化反应是合成酮的又一种方法。探索卡宾化反应的原理、机理以及实验 步骤、结果与分析。
7. 总结
比较各种方法的优缺点,探讨醛酮合成的发展趋势。
8. 参考文献
整理了本课件涉及到的参考文献,供大家进一步学习和了解。 — 结束 —
《醛酮的合成》PPT课件
在这个课件中,我们将介绍醛酮的合成方法。通过一系列实验步骤和结果分 析,帮助您了解醛酮的应用及不同合成方法。
1. 介绍
醛酮是一种重要的有机化合物,具有广泛的应用领域。通过合成醛酮,我们可以得到各种有机化合物, 如药物和香料。
2. 类型
醛的合成
通过氧化醛法和加成反应可以合成醛。
醛酮制备实验报告(3篇)

第1篇一、实验目的1. 理解醛酮的制备原理和方法。
2. 掌握醛酮的实验室合成技术。
3. 学习有机合成实验的基本操作和注意事项。
二、实验原理醛和酮是重要的有机化合物,在药物、香料、塑料等领域有广泛的应用。
醛酮的制备方法主要有醇的氧化、烷烃或烯烃的氧化、卤代物的氧化等。
本实验采用醇的氧化法来制备醛酮。
三、实验仪器与药品1. 仪器:圆底烧瓶、冷凝管、蒸馏装置、滴定管、试管、酒精灯、磁力搅拌器、滤纸、布氏漏斗等。
2. 药品:甲醇、乙醇、异丙醇、浓硫酸、过氧化氢、NaOH、Na2SO4、CuSO4·5H2O、无水乙醇、乙醚、氯化钠等。
四、实验步骤1. 醇的氧化(1)将甲醇、乙醇或异丙醇加入圆底烧瓶中,加入浓硫酸作为催化剂。
(2)缓慢加热至回流,反应过程中需不断搅拌。
(3)反应一段时间后,停止加热,待反应液冷却后,加入过量的NaOH溶液,调节pH至碱性。
(4)将反应液转移至分液漏斗中,加入乙醚,振荡,静置分层。
(5)将有机层分离,水层用氯化钠饱和,再次振荡,静置分层。
(6)将有机层转移至圆底烧瓶中,加入CuS O4·5H2O溶液,加热回流,直至反应液呈蓝色。
(7)将反应液冷却,过滤,滤液即为醛酮。
2. 醛酮的纯化(1)将醛酮滤液蒸去乙醚,得到粗醛酮。
(2)将粗醛酮用无水乙醇重结晶,得到纯醛酮。
五、实验结果与分析1. 通过实验,成功制备了醛酮。
2. 实验过程中,控制反应条件对醛酮的产率和纯度有重要影响。
3. 在醇的氧化过程中,反应时间、温度、pH值等因素都会影响醛酮的产率和纯度。
六、实验讨论1. 醇的氧化法是制备醛酮的常用方法,具有操作简单、反应条件易控制等优点。
2. 在实验过程中,需注意安全操作,防止意外事故发生。
3. 实验结果与理论计算值有一定偏差,可能是由于实验条件控制不够精确、反应物纯度等因素所致。
七、实验总结1. 本实验成功制备了醛酮,掌握了醛酮的实验室合成技术。
2. 通过实验,加深了对醛酮性质的认识,提高了有机合成实验技能。
合成醛酮注意事项

合成醛酮注意事项合成醛酮是有机合成中常见的一种反应类型,通过氧化反应将醇或醚转化为醛或酮。
在进行合成醛酮的实验时,需要注意以下几个方面的问题。
首先,反应条件和底物的选择是合成醛酮的重要因素。
通常,合成醛酮的常用方法包括氧化醇和氧化醚两种路径。
氧化醇通常采用氧化剂如酸性高锰酸钾、酸性过氧化氢、酸性二氧化硫等。
氧化醚则常用过氧化氢、氧气、氧化银等作为氧化剂。
根据反应的需要,选择适当的氧化剂和底物。
其次,合成醛酮反应的温度和时间也需要特别关注。
在进行反应时,应根据具体的反应条件选择合适的温度和反应时间。
过高的温度可能导致副反应的发生,而过低的温度则可能导致反应速率过慢。
此外,反应时间也需要根据具体底物的性质和反应条件进行合理控制。
一般情况下,反应时间较长有助于产率的提高,但过长的反应时间可能会导致反应物的过度转化,产生不必要的副产物。
另外,合成醛酮过程中需要注意反应体系的酸碱性。
不同的合成方法会涉及到不同的反应条件,有些反应是在酸性条件下进行,有些则是在碱性条件下进行。
在进行反应时,应掌握好反应体系的酸碱性,并根据具体需要调节反应液的pH值。
此外,酸碱性的选择还与底物的性质有关,有些底物在酸性条件下更容易发生反应,而有些则在碱性条件下更容易发生反应。
此外,合成醛酮过程中需要注意化学品的安全操作。
氧化反应涉及到氧化剂的使用,应注意避免与易燃、易爆、易腐蚀等化学品接触,同时避免剧烈搅拌和过渡气泡的产生。
在操作过程中应佩戴防护设备,如实验手套、护目镜等,以免对身体健康造成伤害。
最后,合成醛酮的反应产物纯度的提高也是需要关注的问题。
在反应结束后,应采取适当的纯化手段,如结晶、蒸馏、萃取等,以提高产物的纯度。
纯度的提高有助于后续化学反应的进行以及产物的进一步应用。
综上所述,合成醛酮的注意事项包括反应条件和底物的选择、温度和时间的控制、反应体系的酸碱性、化学品的安全操作以及反应产物纯度的提高。
只有在合理选择条件、注意操作安全,并且做好后续处理工作,才能提高合成醛酮的产率和纯度,从而得到满意的实验结果。
醛和酮的制备和应用

醛和酮的制备和应用醛和酮是有机化合物中常见的两类功能团。
它们在化学合成、药物研究以及工业生产中具有重要的地位。
本文将探讨醛和酮的制备方法和它们在不同领域的应用。
一、醛的制备方法1. 氧化醛烯使用氧化剂如过氧化氢或过氧化苯甲酰,可以将醛烯氧化为醛。
这种方法较为常用且反应条件温和。
2. 醇的氧化将醇通过催化剂如醒蒸铬酸盐或焦磷酸三氯酯进行氧化,即可得到相应的醛。
3. 化合物的脱羧某些羧酸经过脱羧反应可以得到醛。
其中一种常用的方法是使用二甲基碳酸乙酯和三苯基膦催化剂。
二、酮的制备方法1. 同分异构体的缩合在碱催化下,两个醛分子或一个醛分子与一个酮分子发生缩合反应,生成相应的酮。
2. 醇的缩合将两个醇分子通过酸催化下的缩合反应,生成酮。
以酚醛缩合反应为例,需要使用酸催化剂如p-甲氧基苯甲醇。
3. 氧化醇通过将醇氧化,可以获得相应的酮。
常用的氧化剂有铬酸钠、碘等。
三、醛和酮的应用领域1. 化学合成醛和酮在有机合成中广泛应用。
它们可以作为合成其他有机化合物的起始物质,例如用醛合成酸、醇、酯等化合物。
同时,醛和酮也可通过巯基、氨基等活化反应,制备出具有特定功能的有机化合物。
2. 药物研究许多药物的合成过程中,往往需要醛和酮作为中间体。
例如,多种抗生素和抗癌药物的制备中都会用到酮。
醛和酮的引入能够增加化合物的活性和特异性。
3. 工业应用醛和酮的广泛应用也包括工业领域。
例如,醛可以用作染料、涂料和树脂的合成原料,酮则常被用作塑料生产中的原料。
总结:醛和酮作为有机化合物中常见的功能团,在化学合成、药物研究以及工业生产中具有重要的地位。
通过氧化醛烯、醇的氧化和化合物的脱羧等方法,可以制备醛。
而酮可以通过同分异构体的缩合、醇的缩合和氧化醇等方法得到。
醛和酮在化学合成、药物研究和工业领域有着广泛的应用。
在化学合成中,它们可以作为其他有机化合物的起始物质,同时还可以制备具有特定功能的化合物。
在药物研究方面,醛和酮可作为中间体用于合成多种药物。
第三节醛酮(三)

2. 官能团:酮羰基( )
3. 饱和一元酮的通式:CnH2nO (n≥3),简写为
(R和R'均为烃基)。
知识精讲
二、酮的命名
1. 选主链——选取分子中含有酮羰基的最长碳链作为主链,按主链中碳原子数称为“某酮”。
2. 编号码——从主链中离酮羰基最近的一端开始对主链碳原子编号。
3. 写名称——用阿拉伯数字标明酮羰基的位置。
第三节 醛 酮
课前引入
我们知道,羰基( )是一个碳原子和一个氧原子以双键相连形成 的一种原子团,如果羰基的碳原子连着一个氢原子便形成了醛基 ( )。因此,醛是由烃基或氢原子与醛基相连而构成的化合物,而 酮是由羰基与两个烃基相连而构成的化合物。模块三 酮知识精讲
一、酮的概述
1. 定义:分子中羰基与两个烃基相连而构成的化合物称为酮。
例如,
命名为:2己酮。
知识精讲
三、丙酮
1. 丙酮的物理性质 丙酮是一种无色透明的液体,沸点56.2 ℃,易挥发,能与水、乙醇等互溶。 2. 丙酮的化学性质 丙酮不能被银氨溶液、新制的氢氧化铜等弱氧化剂氧化。在催化剂存在的条件下,丙酮可以发 生催化加氢反应,生成2-丙醇。 化学方程式: 3. 丙酮的用途 酮是重要的有机溶剂和化工原料。例如,丙酮可用作化学纤维、钢瓶储存乙炔等的溶剂,还用 于生产有机玻璃、农药和涂料等。
醛酮的制备

醛酮的制备醛酮的制备1.炔烃的水合和胞二卤代物的水解①炔烃水合:适合于端炔或对称的炔。
用硼氢化一氧化法进行水合,由末端炔可以制得醛。
②胞二卤代物水解:2.由烯烃制备①烯烃的氧化②氢甲醛化法(Hydroformylation)不对称烯烃主要产物直链烃基醛,对称烯烃可得单一产物。
三、由芳烃侧链α-H的氧化①控制氧化条件,氧化剂不要过量。
② CrO3-醋酐作氧化剂二乙酸酯不易连续被氧化③4.由醇氧化或脱氢① Na2Cr2O7② CuO③ CrO3-吡啶(萨瑞特试剂)——CrO3(C5H5N)2氧化很好地控制在生成醛的阶段,且双键不受影响。
④ [(CH3)2CH-O]3Al (欧芬脑氧化法)双键不受影响⑤ CrO3-H2SO4(琼斯试剂)不饱和仲醇可得到相应的不饱和酮。
5.傅瑞德尔-克拉夫茨(Friedel-Crafts)酰基化是制备芳酮的重要方法,优点是不发生重排,产物单一,产率高。
可通过分子内酰基化制备环酮思考题:如何由芳烃制备?6.盖德曼-柯赫(Gattermann-Koch)反应在催化剂存在下,芳烃和HCl,CO混合物作用,可以制得芳醛该反应叫盖德曼-柯赫反应,它是一种特殊的傅氏酰基化反应。
如果芳环上有烃基、烷氧基,则醛基按定位规则导入,以对位产物为主。
如果芳环上带有羟基,反应效果不好,如果连有吸电子基,则反应不发生。
7.瑞默-梯曼反应(Reimer-Tiemann)苯酚在NaOH存在下和CHCL作用,生成酚醛。
3主要生成邻位产物:瑞默-梯曼(Reimer-Tiemann)反应按下列机理进行,首先氯仿在碱溶液中形成二氯卡宾:此外,二氯卡宾还可以攻击(ⅰ)的带甲基的碳原子,形成环己二烯酮衍生物:上的氢是来自溶剂,然后苯环在把一个氢给予溶剂,为了(ⅳ)或(ⅴ)中-CHCl22证实这点,肯普在含氚的水(THO)中进行了Reimer-Tiemann反应,生成的水杨醛中,醛基含有99.6%的氚只有不到0.4%的氚在苯环上,这表明醛基的氢是来自溶剂,即:8.维路斯梅尔反应(Vilsmeier-Haack反应)通常是指应用N,N-二取代甲酰胺和POCl3使芳环(主要是酚类和芳胺类)甲酰化反应。
醛酮的制备汇总

醛酮的制备汇总旧文重发,温故知新Nef反应1893年,M.Konovalov用稀酸(AcOH,H2SO4)处理1-苯基硝基乙烷的钾盐可以得到1-苯基硝基乙烷和苯乙酮。
而基本在同一时间的1894年,J.U.Nef独立地系统地研究了各种硝基烷钠盐的酸解反应,并发现此类反应的主要产物为相应的羰基化合物。
由于Nef独立地系统地对此类反应的研究,因此将硝基烷转化为相应的羰基化合物的反应被称为Nef反应。
Eschenmoser-Tanabe裂解反应α,β-环氧酮通过α,β-环氧磺酰腙中间体裂解为酮和炔的反应。
Polonovski反应叔胺的氮氧化物用活性试剂(如乙酸酐)处理,重排生成N,N-二取代乙酰胺和醛的反应。
Vilsmeier反应Reimer–Tiemann反应碱性条件下苯酚和氯仿反应生成邻甲酰基苯酚的反应。
Gattermann–Koch reactionStetter反应醛和α,β-不饱和酮在噻唑盐的催化下反应制备1,4-二羰基化合物的反应。
噻唑盐是氰离子的安全替代试剂。
此反应也被称为Michael-Stetter反应,机理和安息香缩合类似Baker-Venkataraman重排碱催化下邻酰氧基芳基酮重排得到相应的芳基β-二酮的反应被称为 Baker-Venkataraman重排。
Stork–Danheiser反应β 烷氧基烯酮和有机金属化合物(格氏试剂或有机锂)反应接着进行酸处理得到另一种烯酮的反应,新生成的烯酮的羰基的位置是原料中烯醇醚的烯碳的位置。
Stork烯胺烷基化反应此反应是Robinson关环反应的一个变体,大位阻的胺如吡咯烷与羰基化合物形成烯胺,接着在位阻较小的一侧与甲基乙烯基酮进行共轭加成。
Hajos–Wiechert反应(S)-(—)-脯氨酸催化的不对称Robinson关环反应。
Robinson关环反应环己酮先对甲基烯基酮进行迈克尔加成,然后进行分子内的羟醛缩合关环得到六元环的α,β-不饱和酮的反应。
第3章第3节 醛 酮 课件【新教材】人教版(新教材)高中化学选择性必修3

课
关 键
时
能
分
力
层
核
作
心
业
突
破
返 首 页
·
7
2.乙醛的物理性质与结构
必
双
备 知
(1)物理性质
基 达
识
标
·
自 主
乙醛是无色、具有 刺激性气味 的液体,密度比水的 小 ,沸点
随 堂
预
检
习 20.8 ℃,易挥发,易燃烧,能与水、乙醇等 互溶 。
测
·
课
关
键
能 力
(2) 结 构 : 分 子 式 为 C2H4O , 结 构 式 为
能
分
力 核
构体。
层 作
心
业
突
破
返 首 页
·
21
·
必
双
备 知
1.判断正误(对的在括号内打“√”,错的在括号内打“×”。)
基 达
识
标
·
自
主
预 习
(1)含有羰基( )的化合物一定是醛类。
随
堂
(
)
检 测
(2)乙醛能发生银镜反应是醛基决定的。
①与银氨溶液的反应方程式为
基 达
识
自 主
标
_C_H_3_C_H__O__+__2_[A__g_(N__H_3_)_2]_O_H__―__△―__→__C_H__3C__O_O__N_H__4+__2_A__g_↓__+__3_N_H__3
·
随 堂
预
检
习 _+__H_2_O________________。
层 作
心
业
突
破 味的无色液体。苯甲醛是制造染料、香料及药物的重要原料。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
甲酸:
甲酸酯:
甲酸盐:
麦芽糖
3.还原反应 加成反应
, (R )H R C O +H H
催化剂
, (R )H
R
C
H
OH 与H2反应
练习:写出HCHO、CH3CHO、
的方程式 小结: RCHO+H2 R R′ C=O+H2 催化剂 RCH2OH R
、
逆推RCH2OH — 醛
催化剂
CHOH 逆推RCHOH—酮 R′ R′
(5)与新制Cu(OH)2悬浊液反应 ① 新制Cu(OH)2悬浊液的制备: 向NaOH溶液中加入几滴CuSO4,充分振荡 2NaOH+CuSO4 = Cu(OH)2↓ + Na2SO4
②加乙醛0.5mL,加热至沸腾 CH3CHO+ 2 Cu(OH)2
现象:
产生砖红色沉淀
CH3COOH + Cu2O ↓ + 2 H2O ② NaOH 要过量
一乙酸铵
、HCHO的银镜反应方程式
注意:
①银氨溶液的制备(现用现配,不可长时间放置)
逐滴加氨水 边加边振荡
AgNO3溶液 至产生沉淀 恰好消失
得银氨溶液
AgNO3 + NH3·H2O=AgOH↓ + NH4NO3 AgOH +2NH3·H2O = [Ag(NH3)2]OH + 2H2O 银氨溶液主要成分:[Ag(NH3)2]OH
9% ,则氧元素的质量分数是(
A. 16%
B. 37%
C. 48%
D.无法计算
5.下列操作正确的是(
)
A.配制银氨溶液:在一定量AgNO3溶液中,滴加氨水至沉
淀恰好溶解
B.配制Cu(OH)2悬浊液:在一定量CuSO4溶液中加入少量
NaOH溶液
C.制溴苯时,为了充分吸收HBr,将导气管插入水中
D.制乙酸乙酯时,在一定量浓硫酸中,依次加入乙酸和乙醇
。
(2)检验分子中碳碳双键的方法是
,化学方程式为:
。
(3)实验操作中,哪一个官能团应先检验?
德州市实验中学高二化学组
2018.4. 27
乙醛
丙酮
丙醛
一、醛、酮的结构
醛: 1.官能团 酮:
或
醛基
酮羰基 R为烃基可同可不同
2.饱和一元醛酮通式: CnH2nO 同碳数的醛、酮互为同分异构体
3.醛酮同分异构体的书写: 先写碳骨架,再放官能团
分子式 结构数
CH2O C2H4O C3H6O 1 1 2
C4H8O
C5H10O
7
3
4.醛酮命名:
高二化学
有机化学基础
第二章 官能团与化学反应——烃的衍生物
第三节 醛和酮 糖类(Ⅰ)
学习目标
1.了解醛、酮组成和结构特点
2.了解几种常见的醛、酮的组成、结构、性质及用途
3.掌握饱和一元醛、酮的同分异构体的书写 4.能够用系统命名法对简单的醛、酮命名
常见的醛、酮
甲醛
甲醛、乙醛、丙醛、丙酮在结 构上有什么相同和不同之处?丙醛 和丙酮有什么关系?你能归纳出醛、 酮的概念吗?
可电离:[Ag(NH3)2]OH = [Ag(NH3)2]+ + OH-
②试管要洁净 ③必须水浴(60∽70℃)加热,不能用酒精灯直接加热
④加热时不能摇动试管否则得到黑色银粒
⑤氨水不能过量(防止生成易爆物)
⑥实验后试管的洗涤: 先用稀HNO3、再用水洗
⑦碱性条件下的反应 应用:检验醛基 、制镜、制瓶胆(葡萄糖)
后加热
6.下列醇不可由醛或酮与H2加成还原而来的是( A. CH3CH2CH2OH B. CH3CHCH3 OH D.
)
C.
7.下列关于醛 判断正确的是(
)
A.用溴水检验CH2=CHCHO中是否含有碳碳双键 B.1molHCHO发生银镜反应最多生成2molAg C.对甲基苯甲醛( )使酸性高锰酸钾溶液褪色
(1)醛:醛基碳为一号碳的最长碳链为主链,醛基位置不标 (2)酮:选择含羰基的最长碳链为主链
从离羰基最近一端开始编号
用阿拉伯数字标明羰基位置 如:
4,4—二甲基—2 —戊酮
3,4—二甲基戊醛
5.几种常见的醛酮:(P70) 甲醛 乙醛 苯甲醛 丙酮
甲醛 结构 简式 HCHO
乙醛 CH3CHO
苯甲醛 C6H5CHO
丙酮 CH3CCH3
强烈刺激性气 有刺激性气味 杏仁气味的液体 又称苦杏仁油 色、态、 味的无色气体 的无色液体 又叫蚁醛 味 溶解性
特殊气味的无色 液体
与水任意比互溶, 能溶解多种有机 化合物
易溶于水
遇水、乙醇 等互溶
微溶于水
应用
制造脲醛树脂 酚醛树脂等 福尔马林
重要的有机 化工原料
制造染料、香 料的中间体
催化剂
RCOOH
醛也可使溴水退色
2 CH3COOH
练习:写出
、 CH3CH2CHO 催化氧化反应方程式
(4)银镜反应
CH3CHO + 2[Ag(NH3)2]OH
H2O + 2Ag ↓+ 3NH3 + CH3COO NH4
一水 二银 三氨 现象:试管内壁形成光亮的银镜
练习:写出CH3CH2CHO 、 总结: RCHO ∽ 2Ag R(CHO)2 ∽ 4Ag HCHO ∽ 4Ag
A.丁醇和乙醚
)
B.丙醛和丙醇 C.丙醇和甘油 D.乙烯和丁二烯 )
3.某饱和一元醛与银氨溶液反应时生成21.6gAg,将等量的该醇 完全燃烧,生成标况下的CO2 13.44L,则该醛是( A.丙醛 B.丁醛 C.3-甲基丁醛 ) D.己醛
4.甲醛、乙醛、丙醛和丙酮组成的混合物中,氢元素的质量分数为
说明它含有醛基
D.能发生银镜反应的有机物不一定是醛类
8.可鉴别1-己烯、甲苯和丙醛三种物质的一组试剂的是( A.银氨溶液和酸性高锰酸钾溶液 B.酸性高锰酸钾溶液和溴的四氯化碳溶液 C.FeCl3溶液和银氨溶液 D.银氨溶液和溴的四氯化碳溶液
)
9.某醛的结构简式为CH2=CHCH2CHO
(1)检验分子原
醛
氧化
酸
酯
跟踪练习
1.下列关于常见的醛酮的说法中正确的是( )
A.甲醛和乙醛都是有刺激性气味的无色液体
B.丙酮是结构最简单的酮,也可以发生银镜反应和加氢还原
C.丙酮难溶于水,但丙酮是常用的有机溶剂
D.人体缺乏维生素A时,难以氧化生成视黄醛,从而引起夜盲症
2.下列各组物质属于同分异构体的是(
注意: ①Cu(OH)2悬浊液现用现配
③用酒精灯直接加热至沸
应用:检验醛基、检测尿糖
练习:写出CH3CH2CHO、
、HCHO 与新制氢氧化铜悬浊
液反应的方程式 总结: RCHO ∽ Cu2O
R(CHO)2 ∽ 2 Cu2O HCHO ∽ 2 Cu2O
小结: 含醛基的物质
可发生银镜反应
可与新制氢氧化铜悬浊液反应 葡萄糖: CH2OH(CHOH)4CHO
有机溶剂和有 机合成原料
二、醛、酮的化学性质
1. 羰基的加成反应 , (R )H
d+ d d + d - 催化剂
(R )H R , C O A 双键断裂,异电相吸
,
R
, (R )H R
C O +A B
B C
A
(R )H
催化剂
C O +A A
d+ d -
R
OA
d - d+
加成物质: HCN、NH3(H-NH2)、ROH(醇)
d+ d-
练习:写出CH3CHO、
分别与H2、HCN、NH3、
CH3OH的加成反应方程式(条件:催化剂)
2.氧化反应(醛) (1)燃烧: CnH2nO + O2
点燃
n CO2 + n H2O
KMnO4 H+
(2)与酸性高锰酸钾反应: RCHO 现象: 紫色退去 (3)催化氧化 2 CH3CHO + O2
