ISO6579食品和动物饲料微生物学沙门氏菌检测
食品沙门氏菌测试方法标准

食品沙门氏菌测试方法标准
食品沙门氏菌测试方法标准主要包括以下步骤:
1.样品采集:从待检测的食品中采集适量样品,确保样品的代表性。
2.样品处理:将采集的样品进行适当处理,如破碎、研磨等,以便后续的
检测操作。
3.增菌培养:将处理后的样品接种到选择性培养基中,进行增菌培养。
选
择性培养基可以抑制其他微生物的生长,促进沙门氏菌的增殖。
4.分离培养:将增菌培养后的样品划线接种到鉴别培养基上,进行分离培
养。
鉴别培养基可以进一步筛选出沙门氏菌,并对其进行鉴别。
5.生化鉴定:对分离培养得到的沙门氏菌进行生化鉴定,以确定其是否为
沙门氏菌。
常用的生化鉴定方法包括API 20E、三糖铁试验等。
6.血清学鉴定:对生化鉴定为沙门氏菌的菌株进行血清学鉴定,以确定其
具体血清型。
常用的血清学鉴定方法包括玻片凝集试验、试管凝集试验等。
7.药敏试验:对分离得到的沙门氏菌进行药敏试验,以确定其对不同药物
的敏感性,为临床治疗提供参考。
需要注意的是,食品沙门氏菌测试方法标准可能因不同国家和地区而有所差异。
因此,在实际操作中,应根据当地的标准和法规进行相应的调整和操作。
沙门氏菌检验国标检验步骤及接种方式

沙门氏菌检验国标检验步骤及接种方式沙门氏菌是一种常见的细菌引起的食源性疾病,可能会导致严重的胃肠道感染。
为了保障食品安全,确保公众的健康,我们需要进行沙门氏菌的国标检验。
下面是一份生动、全面且有指导意义的文章,详细介绍了沙门氏菌检验的国标检验步骤和接种方式。
第一步:样品准备在进行沙门氏菌检验之前,我们首先需要准备样品。
常见的样品包括食品、水、动物排泄物等,可能携带沙门氏菌。
样品应该收集自具有代表性的地点,并采取无菌采样容器进行收集。
收集样品时要注意避免污染,并确保样品的数量足够进行检验。
第二步:样品处理样品处理的目的是将潜在的沙门氏菌分离出来,并进行后续的检测。
可以采用不同的方法进行样品处理,常见的方法包括富集培养和选择性培养。
富集培养是将样品放入富集培养基中,利用培养基中的营养物质以及特定条件促使沙门氏菌生长。
选择性培养则是利用培养基中的特殊抑制剂抑制其他细菌的生长,从而使沙门氏菌生长出来。
第三步:菌落鉴定在样品处理后,我们需要对培养基上的菌落进行鉴定,确认是否为沙门氏菌。
常见的鉴定方法包括形态学鉴定、生理生化鉴定和分子生物学鉴定。
形态学鉴定主要通过观察菌落的形状、颜色和大小等特征来判断细菌的种类。
生理生化鉴定则是通过检测菌落对特定物质的代谢情况来确定细菌的种类。
分子生物学鉴定是利用特定的DNA序列来识别沙门氏菌的基因,通常使用PCR技术进行检测。
第四步:抗菌药敏试验沙门氏菌的抗菌药敏性检测是为了确定对何种抗生素具有敏感性。
通过抗菌药敏试验,我们可以选择合适的药物来治疗感染。
可以使用各种常见的抗生素盘进行试验,然后观察沙门氏菌对不同抗生素的反应。
根据抗生素的抑菌效果,可确定沙门氏菌的耐药性情况。
第五步:结果分析与报告最后一步是对检验结果进行分析,并撰写检验报告。
检验结果要结合国家标准进行评估,确定样品是否合格。
如果样品中检测到沙门氏菌,还需要评估其数量以及对公众健康可能造成的风险。
在撰写报告时,需要详细记录样品的来源、处理方法、检验步骤和结果,以及相应的建议和措施。
欧盟沙门氏菌检验标准

沙门氏菌(Salmonella)是一种常见的食源性病原菌,可以导致食物中毒。
为了确保食品安全,许多国家和地区都有相关的食品和饲料中沙门氏菌的检验标准。
欧盟是全球食品安全监管最为严格的地区之一,其对于沙门氏菌的检验标准非常严格。
以下是欧盟对于食品和饲料中沙门氏菌的一般检验标准:
1. 检测方法:欧盟推荐使用ISO 6579:2002、ISO 6579:2007或ISO 6579:2017等国际标准进行沙门氏菌的检测。
2. 样品数量:每个食品或饲料样品的检测数量至少为25克。
3. 检测频率:对于某些高风险食品,如生肉、家禽、蛋类和蛋制品,欧盟推荐在生产、加工、储存和销售过程中进行定期检测。
4. 阳性判定:如果在一个样品中检测到沙门氏菌,那么这个样品必须被视为阳性。
5. 报告:如果在一个食品或饲料样品中检测到沙门氏菌,那么必须立即报告给相关的监管机构。
6. 处理:如果在一个食品或饲料样品中检测到沙门氏菌,那么这个样品必须被销毁,并且相关的生产或加工设备必须进行清洁和消毒。
需要注意的是,具体的欧盟沙门氏菌检验标准可能会根据食品的种类、来源、加工方法等因素有所不同。
沙门氏菌的检验国标

沙门氏菌的检验国标沙门氏菌是一类常见的致病菌,引起人和动物的沙门氏菌感染,是一种重要的公共卫生问题。
为了保障食品安全和人民的健康,各国都制定了相应的沙门氏菌检验国标,以确保食品和水源的安全。
沙门氏菌的检验国标是根据沙门氏菌的特性和致病机制制定的,旨在检测食品和水源中是否存在沙门氏菌。
根据国际标准化组织(ISO)和国家标准化组织(CNS)的规定,沙门氏菌的检验国标主要包括以下几个方面。
首先是样品的采集和处理。
在进行沙门氏菌检验之前,需要采集样品并进行处理。
样品的采集应该规范,避免交叉污染。
在样品处理过程中,要注意避免沙门氏菌的繁殖和生长,以防止结果的误判。
其次是培养基的准备和使用。
沙门氏菌的培养需要适当的培养基,以提供菌种生长所需的营养物质。
培养基的制备要符合国家标准,以确保培养过程的准确性和可重复性。
此外,在培养过程中要注意温度、pH值和氧气含量等因素的控制,以保证沙门氏菌能够正常生长。
第三是沙门氏菌的检测方法。
常用的沙门氏菌检测方法包括传统的培养方法和分子生物学方法。
传统的培养方法主要是通过培养基的选择和培养条件的控制,将沙门氏菌培养出来并进行鉴定。
分子生物学方法则是通过检测沙门氏菌的DNA序列来确定是否存在沙门氏菌。
这些方法各有优缺点,可以根据实际情况选择合适的方法进行检测。
最后是结果的解读和报告。
沙门氏菌的检验结果应该进行准确的解读,并进行相应的报告。
根据国家标准,沙门氏菌的检测结果可以分为阴性和阳性。
阴性表示样品中未检测到沙门氏菌,阳性表示样品中存在沙门氏菌。
在报告中,应该详细说明检测的方法、结果和结论,以便相关部门和人员能够及时采取相应的措施。
沙门氏菌的检验国标是保障食品安全和人民健康的重要举措。
通过采集样品、准备培养基、选择合适的检测方法和解读结果,可以有效地检测和防控沙门氏菌感染的风险。
各国应该根据实际情况和国家标准,制定和执行相应的沙门氏菌检验国标,以确保食品和水源的安全,保障人民的健康。
国家食品沙门氏菌检测(内含简图很有用)

国家⾷品沙门⽒菌检测(内含简图很有⽤)国家⾷品沙门⽒菌检验前⾔沙门⽒菌是肠杆菌科中⼀种重要的⼈畜共患病原菌,⾰兰⽒阴性,是细菌性⾷物中毒的重要致病菌。
⾎清型种类繁多,⽬前全世界已分离出2523 个⾎清型,我国已发现216个[1].。
与⼈类疾病有关的⾎清型主要集中于A~E 群,包括伤寒沙门⽒菌、(甲、⼄、丙型)副伤寒沙门⽒菌、⿏伤寒沙门⽒菌、猪霍乱沙门⽒菌、肠炎沙门⽒菌等,其中以⿏伤寒沙门⽒菌、肠炎沙门⽒菌及猪霍乱沙门⽒菌最为常见。
它不仅能导致鸡⽩痢、鸡伤寒、副伤寒、仔猪副伤寒等动物疾病,还能使⼈类发⽣伤寒、副伤寒、败⾎症、胃肠炎和⾷物中毒[2]。
根据国际惯例, 要求对易受沙门⽒菌污染的⾷品进⾏分类管理, 以使⼤多数⾷物不含沙门⽒菌, 从⽽有效预防沙门⽒菌引发的各种疾病。
20 世纪50 年代以来,国内外学者进⾏了⼤量的研究, 从以传统⽅法为基础发展到以免疫学为基础的或以分⼦⽣物学为基础的快速检测⽅法, 并在实践检验中不断取得新进展。
这些⽅法包括酶联免疫吸附试验法、免疫磁珠法、免疫荧光标记法、噬菌体裂解试验法、核酸探针法等[3]。
本实验采⽤的是传统标准检测⽅法,包括前增菌,选择性增菌,选择性平板分离,⽣化试验,⾎清学分型鉴定五个步骤。
1材料与⽅法1.1设备和材料1.1.1 恒温培养箱:36℃±1℃,42℃±1℃1.1.2 拍击式均质器。
1.1.3 电⼦天平:感量0.1g。
1.1.4 ⽆菌锥型瓶:容量500ml,250ml。
1.1.5 微量移液器及吸头。
1.1.6 ⽆菌培养⽫:直径90mm。
1.1.7 ⽆菌试管:3mm×5mm、10mm×75mm。
1.1.8 ⽆菌⽑细管。
1.1.9 三⾓烧瓶。
1.2培养基和试剂1.2.1缓冲蛋⽩胨⽔(BPW):称取蛋⽩胨10g,NaCl 5g,Na2HPO4`12H2O 9g,KH2PO41.5g,加蒸馏⽔1L,搅拌加热煮沸⾄完全溶解,分装三瓶,121℃,灭菌20min。
食品卫生微生物学检验 沙门氏菌检验

C-BS
C-BS
I-BS
I-BS
C-BS
C-HE
I-HE
I-HE
C-HE
I-HE
C-HE
1) 采纳API 20E®或Vitek GNI®为传统 生化鉴定方法的选择性替代方法”。
2) 生化鉴定项目进行调整 原国标中生化鉴定是将可疑菌落同时接种于
三糖铁(TSI)琼脂、蛋白胨水 (供做靛基质试验)、尿素琼 脂 (pH7.2)、氰化钾 (KCN) 培养基和赖氨酸脱羧酶试验培 养基; 现修改为:在接种TSI琼脂和赖氨酸脱羧酶试验培养 基的同时增加一项营养琼脂(NA),经TSI琼脂和赖氨酸 脱羧酶试验培养基的选择后,可筛掉大部分非沙门氏菌 株,大大减少了工作量,同时也满足了API 20E®或Vitek GNI®鉴定的需要。
非沙门氏菌
细菌学分析手册(FDA/BAM)
样品(20类)25g
225mL 乳糖肉汤(LB)or 胰酪胨大豆肉汤( TSB)or 煌绿溶液 (BG)or 通用前增菌肉汤(UPB)or营养肉汤(NB)or 再造脱脂奶粉 or 四硫酸盐煌绿(TT) pH6.8±0.2 24±2 h 35℃ TT 43±0.2℃ or 35±2.0℃ 24±2h BS RV 24±2h 42±0.2℃
1. GB/T 4789.4 2. AOAC Official Method :967.26, 967.27,967.28 3. ISO :6579 4 . USFDA : Bacteriological Analytical Manual, Chapter 5: Salmonella。
1 前增菌; 2 选择性增菌; 3 分离; 4 生化鉴定; 5.血清学鉴定; 6.报告。
DUPONT Qualicon BAX System 应用DNA分子核酸探针或基因探针技 术制造的全自动PCR分析仪。将已知核 苷酸序列DNA片段用同位素或其他方法 标记,加入已变性的被检DNA样品中, 在一定条件下即可与该样品中有同源序 列的DNA区段形成杂交双链,从而达到 鉴定样品中DNA的目的。
沙门氏菌检验国家标准

沙门氏菌检验国家标准沙门氏菌是一种常见的致病菌,可以通过食物、水源和接触感染等途径传播,引起食物中毒和肠道感染等疾病。
为了保障食品安全和公共卫生,我国对沙门氏菌的检验标准进行了规范,制定了相应的国家标准。
首先,沙门氏菌检验国家标准明确了检验对象和范围。
该标准适用于食品、饮用水、环境样品等的沙门氏菌检验,包括沙门氏菌的定性和定量检验方法。
针对不同的检验对象,标准中规定了具体的检验方法和技术要求,确保检验结果的准确性和可靠性。
其次,标准对沙门氏菌的检验方法进行了详细的描述。
在样品的处理和预处理过程中,标准规定了严格的操作要求,包括样品的采集、保存、运输和处理等。
针对不同的样品类型,标准中还规定了不同的处理方法,以确保样品中沙门氏菌的检出率和准确性。
此外,标准还对沙门氏菌的培养和鉴定方法进行了规范。
在培养基的选择和制备过程中,标准明确了培养基的成分和制备方法,以及培养条件和培养时间等。
在沙门氏菌的鉴定过程中,标准规定了生化试剂的选择和使用方法,以及鉴定结果的判定标准,确保鉴定结果的准确性和可靠性。
最后,标准对沙门氏菌的定量检验方法进行了规定。
在定量检验过程中,标准规定了菌落计数方法和计数结果的表达方式,以及检验结果的判定标准。
同时,标准还规定了质控要求和质控方法,确保检验结果的可比性和可靠性。
总的来说,沙门氏菌检验国家标准的制定为我国食品安全和公共卫生提供了重要的技术支撑和保障。
通过严格执行该标准,可以有效地预防和控制沙门氏菌引起的食物中毒和肠道感染等疾病,保障人民群众的身体健康和生命安全。
希望各相关部门和单位能够认真贯彻执行该标准,不断提升沙门氏菌检验工作的水平和质量,为我国食品安全和公共卫生事业作出积极贡献。
沙门氏菌检验及分析

沙门氏菌检验及分析沙门氏菌是一种常见的致病菌,能引起人体消化系统的疾病,如沙门氏菌食物中毒和肠炎等。
对食品和环境样品中的沙门氏菌进行检验和分析是非常重要的。
沙门氏菌的检验方法主要包括培养法和分子生物学法。
培养法是传统的沙门氏菌检验方法,该方法使用一系列专门的培养基,如XLD(Xylose Lysine Deoxycholate Agar)和SS(Salmonella Shigella Agar)等,以培养和鉴定沙门氏菌菌株。
将样品加入适当的培养基,然后在适当的温度下进行培养。
经过一段时间后,观察培养基上的菌落形态特征,如形状、色素和粘度等,进一步进行鉴定。
还可以使用生化试剂和抗生素敏感性试验来确定菌株的身份。
分子生物学法是一种快速准确的沙门氏菌检验方法,其基于沙门氏菌特有的基因序列,如invA和fliC等。
通过PCR(聚合酶链反应)技术,可以扩增出这些目标序列,并通过相应的检测方法,如凝胶电泳或实时荧光PCR等,进行检测。
这种方法不仅能够快速鉴定沙门氏菌,还可以检测沙门氏菌的数量和种类等重要信息。
沙门氏菌的分析主要涉及其在食品和环境样品中的存在和数量。
对于食品样品,可以通过抽样和分析的方法来确定沙门氏菌的存在情况和数量。
一般来说,可以选择一些高风险的食品,如家禽肉类、蛋制品和生鲜蔬菜等,进行检测。
对于环境样品,主要包括水源、污水、土壤等,可以通过采样和培养法来确定沙门氏菌的存在。
沙门氏菌的分析结果可以提供重要的参考信息,用于评估食品和环境的安全性。
通过分析沙门氏菌的数量和种类等信息,可以判断食品和环境中是否存在潜在的健康风险,并采取相应的措施进行预防和控制。
沙门氏菌检验国标检验步骤及接种方式

沙门氏菌检验国标检验步骤及接种方式沙门氏菌是一种革兰氏阴性杆菌,广泛存在于食品、环境中,尤其是在沙门氏菌感染的食品中。
沙门氏菌检验是食品安全检测中的重要一环,其准确性和可靠性对保障公众健康至关重要。
下面将介绍沙门氏菌检验国标的检验步骤及接种方式。
一、检验步骤
1.原料准备:准备待检样品,包括食品、环境样品等。
2.样品采集:采集样品时应使用一次性餐具或清洁用具,确保样品的完整性和真实性。
3.样品处理:对采集的样品进行初步处理,包括去除杂质、研磨成粉末等。
4.检验样品:将处理后的样品放入含有适当浓度的试剂管中,进行沙门氏菌检验。
5.结果判断:根据检验结果判断样品是否存在沙门氏菌感染。
二、接种方式
1.沙门氏菌疫苗接种:在食品安全检测中,一般使用沙门氏菌疫苗进行接种。
疫苗接种后,人体免疫系统会产生针对沙门氏菌的抗体和免疫记忆,从而有效地预防沙门氏菌感染。
2.样品接种:对于食品样品,可以使用沙门氏菌疫苗进行接种。
在样品处理过程中,可以通过加入疫苗,使样品受到沙门氏菌的感染,进而进行检测以判断样品是否存在感染。
三、注意事项
1.接种疫苗前,应进行体检,确保没有患有其他疾病或感染。
2.接种疫苗后,应严格按照操作规程进行样品处理和检测,以确保检验结果的准确性和可靠性。
3.疫苗接种后可能会出现短暂的发热、乏力等症状,正常现象,不应影响检测结果。
沙门氏菌检验国标的检验步骤及接种方式非常重要,可以确保食品安全检测的准确性和可靠性。
在食品安全检测中,应严格遵守操作规程,确保疫苗接种的安全和有效性,以保证公众健康安全。
沙门氏菌检验及分析

沙门氏菌检验及分析沙门氏菌是一类常见的食源性病原微生物,引起的沙门氏菌感染会导致沙门氏菌病,主要症状包括腹泻、发热、恶心呕吐等。
为了确保食品安全,对食品中沙门氏菌的检验及分析显得尤为重要。
沙门氏菌的检验方法主要有传统培养法和分子生物学方法。
传统培养法是将食品样品转移到含有适当营养物质的培养基上进行培养,通过观察形状、颜色及生长情况来鉴别沙门氏菌的存在。
分子生物学方法则是借助PCR技术,通过特定引物扩增沙门氏菌的DNA片段,进而进行检测与鉴定。
沙门氏菌的分析主要包括对菌株的鉴定与分型。
鉴定主要通过形态学、生理特性及生化试验等方法,确定该菌株是否为沙门氏菌。
分型则是通过分子生物学方法,如多重引物随机扩增多态性DNA分析(MLVA)、多重引物PCR分型(MLST)等,对沙门氏菌进行分型,进一步了解其遗传多样性及流行病学相关信息。
沙门氏菌的检验标准主要参考国家标准或行业标准,如《食品安全国家标准沙门氏菌检验》(GB 4789.4-2016)、《食品微生物学沙门氏菌检验方法 GB/T 4789.5-2013》等。
这些标准明确了样品的采集方法、培养条件及检测指标等,确保了检验结果的准确性。
在食品安全监测中,沙门氏菌的检验通常应用于肉制品、蛋制品、禽肉及水产品等食品中。
在取样时,应注意避免污染或交叉感染,同时需确保样品代表性。
样品取回后,应尽快送达实验室进行检测,避免菌落生长过于旺盛,影响检验结果。
沙门氏菌的检验结果的解读需要参考相关标准。
通常来说,如果样品中沙门氏菌的检出数目超过规定标准,则判定为阳性,表示该样品存在沙门氏菌污染,不符合食品安全要求。
反之,如果检测结果未能检出沙门氏菌,则判定为阴性,表示该样品符合食品安全要求。
沙门氏菌的检验与分析是确保食品安全的重要环节。
通过合适的检验方法和分析技术,能够准确判断食品样品是否存在沙门氏菌污染,并提供科学依据来保障大众健康。
五种方法检测食品中沙门氏菌的结果比较

五种方法检测食品中沙门氏菌的结果比较
杨娟;许美玲;张丽;王君卫
【期刊名称】《中国食物与营养》
【年(卷),期】2013(019)009
【摘要】目的:通过参加能力验证,加强实验室间的技术交流,提高检测技能,验证实验室的检测能力.方法:采用SN0170-1992、mini-VIDAS、API20E、科玛嘉显色培养基、ISO6579-2002等方法对沙门氏菌进行检测.结果:采用这5种方法能准确鉴定出测试样品中的沙门氏菌,取得满意结果.结论:通过本次能力验证,证明没有任何一种培养基可以全面保证所有食品基质或各种沙门氏菌血清型生长,在日常检验中,为减少假阴性结果,同时使用两种或两种以上培养基平行地进行实验是完全有必要的.
【总页数】3页(P18-20)
【作者】杨娟;许美玲;张丽;王君卫
【作者单位】临沂出入境检验检疫局,山东临沂276034;临沂出入境检验检疫局,山东临沂276034;临沂出入境检验检疫局,山东临沂276034;临沂出入境检验检疫局,山东临沂276034
【正文语种】中文
【相关文献】
1.五种方法检测乙肝表面抗原结果比较 [J], 江新泉;刘洪爱
2.三种检测方法对样品中沙门氏菌的检测结果比较 [J], 周赞虎;郑天凌;田蕴;张永祥;杜娟;林俊君
3.乙肝五项标志物两种方法检测结果比较分析 [J], 吕旭军;茅利明;陈小燕;钱亚琼;
4.4种检测方法对巧克力中亚利桑那沙门氏菌的检测结果比较 [J], 张红莉;李勇;许均华;郑文;徐文泱;欧露真;代洪梅
5.API 20E鉴定系统等两种检测方法应用于食品中沙门氏菌的检测结果比较 [J], 韩志双;胡凤
因版权原因,仅展示原文概要,查看原文内容请购买。
食品中的致病微生物沙门氏菌的商业化检测技术
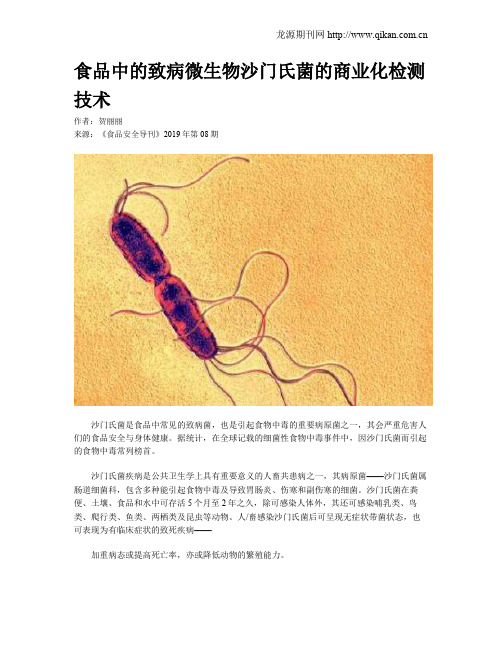
食品中的致病微生物沙门氏菌的商业化检测技术作者:贺丽丽来源:《食品安全导刊》2019年第08期沙门氏菌是食品中常见的致病菌,也是引起食物中毒的重要病原菌之一,其会严重危害人们的食品安全与身体健康。
据统计,在全球记载的细菌性食物中毒事件中,因沙门氏菌而引起的食物中毒常列榜首。
沙门氏菌疾病是公共卫生学上具有重要意义的人畜共患病之一,其病原菌——沙门氏菌属肠道细菌科,包含多种能引起食物中毒及导致胃肠炎、伤寒和副伤寒的细菌。
沙门氏菌在粪便、土壤、食品和水中可存活5个月至2年之久,除可感染人体外,其还可感染哺乳类、鸟类、爬行类、鱼类、两栖类及昆虫等动物。
人/畜感染沙门氏菌后可呈现无症状带菌状态,也可表现为有临床症状的致死疾病——加重病态或提高死亡率,亦或降低动物的繁殖能力。
家禽、蛋类和肉类产品是沙门氏菌的主要传播媒介,而受感染程度主要取决于沙门氏菌的血清类型和食用者的身体状况,因此,小孩、老年人及免疫缺陷的个体是较容易受到该菌威胁的群体。
根据国际惯例,要求对易受沙门氏菌污染的食品进行检测,并分类管理,以保证消费者接触到的食物不含沙门氏菌,从而有效预防疾病。
我国《食品安全法》规定,食品中沙门氏菌的限量标准为0,并要求食品在进入市场之前一定要检测是否含有沙门氏菌。
然而,传统的细菌学检测方法繁琐耗时,不能满足如今食品安全检测快速发展的需求。
本文介绍了德国拜发集团(以下简称“拜发”)在食品中沙门氏菌检测方面研发的3种检测方法,以期为相关人员进行日常检测提供参考。
1 实时荧光PCR方法(RT-PCR)1.1 应用原理RT-PCR(Real time-PCR)是在传统PCR反应体系中加入荧光基团,利用荧光信号的积累实时检测整个PCR进程,最后通过软件分析其积累的荧光信号,进而对需要检测的基因序列进行定性或定量分析。
拜发研制的用于沙门氏菌检测的荧光定量检测试剂盒SureFast? Salmonella ONE可进行100次扩增。
ISO标准参考译文沙门氏菌检验基准方法

国际标准 ISO 6579食品和动物饲料的微生物学——沙门氏菌检测的基准方法内容1 范围2 参考标准3 定义4 原理4.1 概要4.2前增菌——非选择性液体培养基4.3 增菌——选择性液体培养基4.4 划平板和鉴定4.5 确认5 培养基、试剂和血清5.1 概要5.2 培养基和试剂5.3 血清6 设备和玻璃器皿7 采样8 检验样品的制备9 程序9.1 试验样品和原始悬浮液9.2 非选择性前增菌9.3 选择性增菌9.4 划平板和鉴定9.5 确认10 结果表示11 检验报告12 质量保证附录A (标准化)程序图表附录B (标准化)培养基和试剂的成份及准备附录C (非标准化)实验室间试验结果参考书目ISO(国际标准化组织)是国际标准化团体的全世界同盟。
通常由ISO技术委员会来执行国际标准的制订工作(ISO成员体)。
通常由ISO技术委员会来完成国际标准的准备工作。
在委员会中,若对建立的技术委员会有兴趣的话,每个成员体有权作为代表。
国际组织、政府或非政府组织,通过ISO联系,也可以参加这项工作。
在所有电工标准方面,ISO与国际电工委员会(IEC)紧密合作。
国际标准按照ISO/IEC指南第三章所列的规则草拟。
技术委员会的主要任务是准备国际标准。
被技术委员会采用的国际标准草案以投票方式在成员体内运行。
至少要75%成员体的投票赞成,才能作为一个国际标准发布。
要引起注意的可能性是:本国际标准的一些要素可能是专利权主体。
ISO不应承担鉴定部分或全部的这种专利权。
ISO6579是由食品ISO/TC34技术委员会、微生物SC9分委员会所准备的。
第四版删除或更换了第三版(ISO6579:1993),并已作了技术性修订。
附录A和附录B形成了本国际标准的标准化部分。
附录C仅为资料。
因为有大量的不同种类的食品和饲料产品,本基准方法可能对某些产品并不完全适用,而另一些产品可能得用到其他方法。
既然这样,如果为论证技术上的原因而绝对需要时,那么就可使用这些产品指定的不同方法。
食品安全国家标准 食品微生物学检验 沙门氏菌检验(编制说明)

《食品安全国家标准食品微生物学检验沙门氏菌检验》(征求意见稿)编制说明一、工作简况(包括任务来源与项目编号、标准起草单位、协作单位、主要起草人、简要起草过程)1、任务来源受国家卫生和计划生育委员会食品安全标准与监测评估司委托,根据《中华人民共和国食品安全法》和国务院部署,按照《食品安全国家标准整合工作方案(2014年- 2015年)》的原则要求,按照国家卫生和计划生育委员会食品安全标准与监测评估司的工作安排,对该标准进行整合。
标准整合项目编号为ZHENGHE-2014-409和ZHENGHE-2015-409。
2、标准起草单位、协作单位、主要起草人本标准起草单位为:国家食品安全风险评估中心;标准主要起草人为:徐进、王伟、白莉、甘辛、闫韶飞、董银苹、韩海红、李志刚、杜春明、余东敏。
3、简要起草过程(1)2014年7月标准整合人员进行了实地学习、交流,对整合原则、技术要求和实施细则进行了讨论,2014年12月底完成数据的汇总。
(2)根据初审意见继续完善标准文本。
2015月4月底南宁标准专家研讨会再次提交起草组专家讨论。
(3)提交《食品安全国家标准食品微生物学检验沙门氏菌检验》(征求意见稿)、《编制说明》供公开征求意见。
二、确定各项技术内容(如技术指标、参数、公式、试验方法、检验规则等)的依据1、整合原则(1)、与国际接轨的原则,该标准的整合内容主要参考了美国FDA Bacteriological Analytical Manual Online(Chapter 5 Salmonella)、ISO 6579、USDA(MLG 4.08)、加拿大MFHPB-20(2009)等标准。
尽量做到与国际上的沙门氏菌检测方法相统一,便于与国际沙门氏菌检测接轨。
(2)、保持与原标准的连续性。
与现有国家标准协调统一,鉴于我国已有相关的检测方法标准,在内容设计时多参考了目前现行的标准条款,如样品前处理步骤与金黄色葡萄球菌、大肠菌群检测方法尽量相同,在常规生化、血清分型方面尽量沿用原标准中的方法。
ISO标准食品和动物饲料的微生物学

国际标准 ISO 6579食品和动物饲料的微生物学——沙门氏菌检测的基准方法内容1 范围2 参考标准3 定义4 原理4.1 概要4.2前增菌——非选择性液体培养基4.3 增菌——选择性液体培养基4.4 划平板和鉴定4.5 确认5 培养基、试剂和血清5.1 概要5.2 培养基和试剂5.3 血清6 设备和玻璃器皿7 采样8 检验样品的制备9 程序9.1 试验样品和原始悬浮液9.2 非选择性前增菌9.3 选择性增菌9.4 划平板和鉴定9.5 确认10 结果表示11 检验报告12 质量保证附录A (标准化)程序图表附录B (标准化)培养基和试剂的成份及准备附录C (非标准化)实验室间试验结果参考书目前言ISO(国际标准化组织)是国际标准化团体的全世界同盟。
通常由ISO技术委员会来执行国际标准的制订工作(ISO成员体)。
通常由ISO技术委员会来完成国际标准的准备工作。
在委员会中,若对建立的技术委员会有兴趣的话,每个成员体有权作为代表。
国际组织、政府或非政府组织,通过ISO联系,也可以参加这项工作。
在所有电工标准方面,ISO与国际电工委员会(IEC)紧密合作。
国际标准按照ISO/IEC指南第三章所列的规则草拟。
技术委员会的主要任务是准备国际标准。
被技术委员会采用的国际标准草案以投票方式在成员体内运行。
至少要75%成员体的投票赞成,才能作为一个国际标准发布。
要引起注意的可能性是:本国际标准的一些要素可能是专利权主体。
ISO不应承担鉴定部分或全部的这种专利权。
ISO6579是由食品ISO/TC34技术委员会、微生物SC9分委员会所准备的。
第四版删除或更换了第三版(ISO6579:1993),并已作了技术性修订。
附录A和附录B形成了本国际标准的标准化部分。
附录C仅为资料。
介绍因为有大量的不同种类的食品和饲料产品,本基准方法可能对某些产品并不完全适用,而另一些产品可能得用到其他方法。
既然这样,如果为论证技术上的原因而绝对需要时,那么就可使用这些产品指定的不同方法。
沙门氏菌检测卫生标准

沙门氏菌是一种常见的食源性病原体,可能导致食物中毒。
为了确保食品安全,各国政府和卫生部门制定了相应的沙门氏菌检测卫生标准。
以下是我国和国际上常见的沙门氏菌检测卫生标准:
1. 中国:
我国《食品安全国家标准食品中病原微生物检测方法》(GB/T 4789.1-2016)对沙门氏菌的检测方法进行了规定,包括分离、鉴定和计数等步骤。
此外,针对不同食品类别,如肉类、禽类、水产制品、冷藏食品等,还有相应的沙门氏菌检测标准,如GB 29921-2013《食品安全国家标准食品中致病菌限量》等。
2. 国际:
(1)世界卫生组织(WHO)和联合国粮农组织(FAO)制定的《国际食品卫生法典》(Codex Alimentarius Commission,CAC)对沙门氏菌检测方法有详细规定,包括样品处理、分离、鉴定和计数等环节。
(2)美国食品和药物管理局(FDA)的《食品微生物学检测手册》(FDA Microbiological Laboratory Manual)提供了针对各类食品的沙门氏菌检测方法。
(3)欧盟(EU)制定的《食品安全微生物检测标准》(EC)对沙门氏菌检测方法进行了规定,并要求成员国家遵循相同的标准。
3. 沙门氏菌检测卫生要求:
沙门氏菌检测的卫生要求包括:
(1)检测实验室应具备相应的资质和条件,如符合ISO 17025 等国际标准;
(2)检测人员应具备专业知识和技能,进行严格的培训;
(3)实验设备和环境应保持清洁、消毒和防护;
(4)检测过程应遵循标准操作规程,确保检测结果的准确性和可靠性;
(5)检测结果阳性者,应立即采取措施对食品进行召回、销毁或处理,以防止病原菌传播。
中美欧食品中沙门氏菌检验标准的比较分析

中美欧食品中沙门氏菌检验标准的比较分析■ 丁卫平1 张士财1 伊廷存2(1. 滨州市检验检测中心;2. 山东省食品药品检验研究院)摘 要:沙门氏菌是一种重要的食源性致病菌,与食品安全及人类健康息息相关。
检验标准是沙门氏菌鉴定的基础与依据。
为给我国现行食品沙门氏菌检验标准的修订提供参考依据,使我国食品中沙门氏菌的检测更加科学准确,本文收集了中国、美国及欧洲的食品沙门氏菌检验标准,从适用范围、预增菌、选择性增菌、平板分离、鉴定等方面进行了系统比较分析。
结果表明,我国沙门氏菌检验标准与欧洲所使用标准较为相似,与美国所使用标准差别较大,建议在我国食品沙门氏菌检验标准的制修订过程中,借鉴国外同类型标准先进经验,完善改进我国沙门氏菌检验标准,满足实验室检测需要。
关键词:食品,沙门氏菌,检验,方法,比较DOI编码:10.3969/j.issn.1002-5944.2024.03.034Comparative Analysis of Detection Standards in China, the United Statesand Europe for Salmonella in FoodDING Wei-ping1 ZHANG Shi-cai1 YI Ting-cun2(1. Binzhou Testing Center; 2. Shandong Institute of Food and Drug Control)Abstract:Salmonella is an important foodborne pathogen closely related to food safety and human health. Detection standards are the basis for the detection of salmonella. To provide a reference basis for the revision of China’s current detection standard on salmonella in food, and to make the detection of salmonella in food more scientific and accurate, this paper collects the detection standards on salmonella in food from China, the United States and Europe, systematically compares and analyzes these standards from aspects of scope of application, pre-enrichment, selective enrichment, plate separation, and identifi cation. The results show that China’s standard for salmonella detection is relatively similar to the European standard, but significantly differs from the standard implemented in the United States. It is recommended to learn from the foreign advanced experience of similar standards in the process of developing and revising China’s detection standard of salmonella in food, and improve this detection standard to meet the needs of laboratory testing. Keywords: food, salmonella, detection, method, comparison0 引 言沙门氏菌为革兰氏阴性杆菌,是一种重要的食源性致病菌[1],广泛分布于奶和奶制品、肉与肉制品、蛋及蛋制品等食物中[2-4]。
ISO6579食品和动物饲料微生物学沙门氏菌检测

ISO 6579:2002 食品和动物饲料微生物学—沙门氏菌检测序ISO是国际标准的全球性组织。
准备国际标准这项工作通常由ISO技术联盟来完成。
每一个团体成员负责各自的学科。
与ISO有合作的国际性机构、政府与非政府机构,也有参与这项工作。
ISO与国际电子组织(IEC)在电子标准化方面有着密切的合作关系。
国际性标准的起草原则在《ISO/IEC 细则》第三部分中有给出。
起草的国际性标准被技术委员会采用是通过全体成员投票决定的。
发布一个国际性标准需要至少75%成员投赞成票。
由于某些学科涉及到专利权。
而ISO没有责任去鉴别这些专利。
ISO 6579是ISO/TC 34起草的。
这个第四版取代了第三版(ISO 6579:1993),由于它在技术上已经落后了。
附录A和B是本标准的标准化部分。
附录C只为了提供信息。
绪论由于食品与饲料的种类繁多,这个标准不一定适合某一类产品。
在这种情况下,可使用不同的方法,但必须有绝对的技术上的理由。
否则,要尽可能地完全遵循本标准。
当这个标准下一次回顾时,将会对这个标准的使用做数据统计,特殊产品偏离本标准使用也会做相关统计。
同一类产品的检测方法也有可能不统一,国际性标准和/或国家标准也不一定完全与本标准相符合。
希望相关标准做回顾时,会遵循本标准做出相关的修改,以使只有已被证明的技术上的理由才能与本标准偏离。
警告——为了保护实验室人员的安全,必须确保沙门氏菌的检测,特别是伤寒沙门氏菌和副伤寒沙门氏菌,必须在一个有经验的微生物学家的指导下,在适当的实验室设备中进行,并处理好实验室废弃物。
1 范围这个国际标准主要提供沙门氏菌的检测方法,包括伤寒沙门氏菌和副伤寒沙门氏菌。
局限性已在绪论中给出,本标准适用于——用于人类消耗和动物饲养的产品;——食品生产和食品加工的环境样品。
警告——本方法可能不能复苏所有的伤寒沙门氏菌和副伤寒沙门氏菌。
2 参考标准以下标准文件是本标准的参考标准。
已过期的文献,后来改善或修订的,部分这种文献已经不适用。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
ISO 6579:2002 食品和动物饲料微生物学—沙门氏菌检测序ISO是国际标准的全球性组织。
准备国际标准这项工作通常由ISO技术联盟来完成。
每一个团体成员负责各自的学科。
与ISO有合作的国际性机构、政府与非政府机构,也有参与这项工作。
ISO与国际电子组织(IEC)在电子标准化方面有着密切的合作关系。
国际性标准的起草原则在《ISO/IEC 细则》第三部分中有给出。
起草的国际性标准被技术委员会采用是通过全体成员投票决定的。
发布一个国际性标准需要至少75%成员投赞成票。
由于某些学科涉及到专利权。
而ISO没有责任去鉴别这些专利。
ISO 6579是ISO/TC 34起草的。
这个第四版取代了第三版(ISO 6579:1993),由于它在技术上已经落后了。
附录A和B是本标准的标准化部分。
附录C只为了提供信息。
绪论由于食品与饲料的种类繁多,这个标准不一定适合某一类产品。
在这种情况下,可使用不同的方法,但必须有绝对的技术上的理由。
否则,要尽可能地完全遵循本标准。
当这个标准下一次回顾时,将会对这个标准的使用做数据统计,特殊产品偏离本标准使用也会做相关统计。
同一类产品的检测方法也有可能不统一,国际性标准和/或国家标准也不一定完全与本标准相符合。
希望相关标准做回顾时,会遵循本标准做出相关的修改,以使只有已被证明的技术上的理由才能与本标准偏离。
警告——为了保护实验室人员的安全,必须确保沙门氏菌的检测,特别是伤寒沙门氏菌和副伤寒沙门氏菌,必须在一个有经验的微生物学家的指导下,在适当的实验室设备中进行,并处理好实验室废弃物。
1 范围这个国际标准主要提供沙门氏菌的检测方法,包括伤寒沙门氏菌和副伤寒沙门氏菌。
局限性已在绪论中给出,本标准适用于——用于人类消耗和动物饲养的产品;——食品生产和食品加工的环境样品。
警告——本方法可能不能复苏所有的伤寒沙门氏菌和副伤寒沙门氏菌。
2 参考标准以下标准文件是本标准的参考标准。
已过期的文献,后来改善或修订的,部分这种文献已经不适用。
然而,有大部分学者正在争取发布最新版的文献如以下列出。
对于无限期的文献,最新版本都是适用的。
ISO和IEC成员保存当前有效国际性标准的记录。
ISO 6887-1,食物与动物饲料原料微生物学——样品准备原则,微生物检测样品原液及十倍法稀释——第一部分:样品原液和十倍法稀释的指导准则。
ISO 7218,食物与动物饲料原料微生物学——微生物检验指导准则。
ISO 8261,牛奶和奶制品——微生物检测样品准备、品原液和十倍法稀释的指导准则。
3 术语和定义以下术语和定义适用于本标准。
3.1 沙门氏菌按照本国际标准操作,在固体选择性培养基上形成典型或略典型的菌落,并且生物学反应和血清学反应符合要求。
3.2 检测沙门氏菌按照本国际标准操作,检查一定重量或体积的样品存在或不存在沙门氏菌。
4 原理4.1 概述沙门氏菌的检测有四个必须的连续阶段(也可见附录A)。
注意:沙门氏菌可能以很少数量存在,并伴随大量的肠杆菌属或其它属细菌存在。
此外,检测低数量的受损的沙门氏菌,前增菌是必要的。
4.2 使用非选择性液体培养基前增菌缓冲蛋白胨水环境温度培养是检测的一部分,然后37℃±1℃培养18h±2h。
对于特定的食品,使用其它的前增菌是必要的(见9.1.2)。
如果是大量的样品,在接种前,缓冲蛋白胨水必须先预热至37℃±1℃。
4.3 选择性液体培养基中增菌使用RV大豆培养基(RVS肉汤)和MK连四硫酸盐/新生霉素(MKTTn肉汤)肉汤。
RVS肉汤41.5℃±1℃,24h±3h。
MKTTn肉汤37℃±1℃,24h±3h。
4.4 平板划线和鉴定使用两种选择性固体培养基:——木糖赖氨酸脱氧胆酸盐琼脂(XLD琼脂);——任何对XLD琼脂做补充的固体选择性培养基,并能分离乳糖阳性的伤寒沙门氏菌和副伤寒沙门氏菌。
实验室可以自己选择使用哪一种培养基。
XLD琼脂37℃±1℃培养24h±3h。
另一种培养基根据生产商的要求培养。
注意:如亮绿琼脂(BGA),亚硫酸铋琼脂可供选择。
4.5 确认试验假定沙门氏菌菌落进行次培养,做适当的生化学和血清学试验来鉴定。
5 培养基和试剂、血清5.1 概述一般实验室实践,参照ISO 7218。
5.2 常规培养基和试剂注意:由于需使用到大量的培养基和试剂,其成分和准备查看附录B。
5.2.1 非选择性钱增菌培养基:缓冲蛋白胨水见B.1。
5.2.2 第一个选择性增菌培养基:RV大豆培养基(RVS肉汤)见B.2。
5.2.3 第二个选择性增菌培养基:MK连四硫酸盐/新生霉素(MKTTn肉汤)肉汤见B.3。
5.2.4 固体选择性平板培养基5.2.4.1 第一个培养基:木糖赖氨酸脱氧胆酸盐琼脂(XLD琼脂)见B.4。
5.2.4.2 第二个培养基第二种适当的培养基的选择取决于试验室的判断。
必须按照生产商的要求配制培养基。
5.2.5 营养琼脂见B.5。
5.2.6 三糖铁琼脂(TSI琼脂)见B.6。
5.2.7 尿素琼脂(西蒙氏)见B.7。
5.2.8 L-赖氨酸脱羧酶培养基见B.8。
5.2.9 牛乳糖检测试剂见B.9。
5.2.10 VP反应试剂见B.105.2.11 吲哚反应试剂见B.11。
5.2.12 半固体营养琼脂见B.12。
5.2.13 生理盐水溶液见B.13。
5.3 血清一般可买到含有一种或多种O抗原的血清。
例如:抗体血清包含一种或多种“O”,称为单价或多价“O”抗体血清,“Vi”血清。
还有包含一种或多种H抗原的血清。
必须确认所使用的血清适合检测所有类型的沙门氏菌。
6 设备和玻璃器皿使用一般微生物实验室设施(见ISO 7218),另有以下增加。
6.1 干热灭菌或湿热灭菌设备见ISO 7218。
6.2 干燥箱或烘箱,鼓风式,能达到37℃~55℃6.3 培养箱,可恒温37℃±1℃6.4 水浴锅,可恒温41.5℃±1℃6.5 水浴锅,可恒温44℃~47℃6.6 水浴锅,可恒温37℃±1℃6.7 接种环,直径3mm6.8 pH计6.9 试管或三角瓶6.10 刻度移液管或移液器,10ml和1ml6.11 平皿,小尺寸的(直径90mm~100mm)和大尺寸的(直径140mm)7 取样ISO 6888中并不涉及取样。
如果没有相关的国际标准,建议需经过多方同意。
微生物实验室接收到的样品必须是真实代表样品的,并在运输和储藏期间没有损坏或改变微生物的性状。
8 样品前处理参照样品的相关国际标准进行前处理。
如果没有相关的国际标准,建议需经过多方同意。
9 程序9.1 测试部分和样品原始悬液9.1.1 概述参照ISO 6887-1,相关细节可参考各个样品的标准。
牛奶或奶制品参照ISO 8261。
样品原始悬液的准备,一般使用钱增菌培养基。
如果取样量大于25g,使用前增菌培养基补足至1:10悬液。
当不只一份25g的样品进行检测时,为了降低检测工作量,并且合成物不会影响样品的检测,可以将多个检测部分合成为一个部分。
例如,如果有十份25g 的样品检测,可以把这十个样品合成成为一份250g的样品,添加2.25L前增菌肉汤。
可以选择,将0.1ml(在10mlRVS肉汤中)和1ml(在10mlMKTTn肉汤中)的前增菌肉汤合并为一份,添加至100ml选择性培养基中。
9.1.2 特殊食物样品原始悬液的准备注意:以下操作只用于沙门氏菌的检测。
详细的细节可参照ISO 6887-2,ISO 6887-3,ISO 6887-4和ISO 8261。
9.1.2.1 可可粉和含有可可粉的产品(大于20%)加入含50g/l 酪蛋白的缓冲蛋白胨水(避免使用酸酪蛋白),或100g/l灭菌脱脂奶粉,培养2h后,如果样品中含有大量的革兰氏阳性菌群,添加0.018g/l 亮绿。
9.1.2.2 酸性和变酸食品要确保前增菌过程中pH值不会低于4.5。
注意:如果使用双倍浓度缓冲蛋白胨水水会使酸性和变酸食品的pH值比较稳定。
9.2 非选择性前增菌将原始悬液在37℃±1℃下培养18h±2h。
9.3 选择性增菌9.3.1 接种0.1ml 9.2中的培养物至10ml RVS肉汤;接种1ml 9.2中的培养物至10ml MKTTn肉汤。
9.3.2 RVS肉汤41.5℃±1℃下培养24h±3h;MKTTn肉汤37℃±1℃下培养18h±3h。
必须检查培养温度不能超过限值42.5℃。
9.4 划线平板并鉴别9.4.1 培养24h±3h后,取一环RVS肉汤培养物划线至大尺寸的XLD平板,以便能很好的分离出单个菌落。
如果没有大尺寸的平板,使用两个小尺寸平板代替。
同样划线第二种选择性固体培养基。
9.4.2 培养24h±3h后,取一环MKTTn肉汤,重复9.4.1操作划线两种选择性平板。
9.4.3 倒置平板,放置于培养箱中。
XLD平板37℃培养,第二种培养基培养温度参照生产商要求。
9.4.4培养24h±3h后,检查是否存在典型的沙门氏菌菌落,或不典型的可能为沙门氏菌的菌落。
XLD平板上的典型沙门氏菌菌落为黑色中心,周围有一圈微红色的透明圈,由于培养基的指示剂。
注意:H2S阳性沙门氏菌为粉红色中心深粉红色。
乳糖阳性沙门氏菌为黄色有或没有黑色中心。
按照生产商的要求培养第二种培养基,检查有没有典型菌落出现。
9.5 证实9.5.1 概述商业的沙门氏菌生化鉴定盒如果确认可靠,即可供使用。
生化鉴定盒的使用涉及到菌落的生化特性确认。
必须按照生产商的说明使用。
注意:沙门氏菌菌落的辨别需要很大深度的经验,不仅是逐个逐个血清型,而且是一批批选择性培养基的使用。
9.5.2 挑选菌落做确认每个选择性平板至少挑选一个典型菌落或疑是菌落做确认,如果第一个菌落为阴性,必须重新挑选四个菌落。
流行病学研究一般会挑选五个菌落。
如果平板上少于五个典型或疑是菌落,挑选所有菌落做确认。
将挑选的菌落划线营养琼脂平板,更好地分离单个菌落。
37℃±1℃下培养24h±3h。
使用纯培养物做生化鉴定和血清学鉴定。
9.5.3 生化鉴定9.5.3.1 概述用接种针将9.5.2获得的菌落接种至9.5.3.2到9.5.3.7培养基中。
9.5.3.2 TSI琼脂在斜面琼脂上划线并穿刺。
37℃±1℃下培养24h±3h。
按照下面说明记录培养基的变化:a) 底层黄色:葡萄糖阳性(葡萄糖利用)红色或无变化:葡萄糖阴性(葡萄糖不理用)泡沫或葡萄糖产气形成龟裂b) 斜面黄色:乳糖和/或蔗糖阳性(乳糖和/或蔗糖利用)红色或无变化:乳糖和/或蔗糖阴性(乳糖和/或蔗糖不利用)典型沙门氏菌为碱性(红色)斜面和酸性(黄色)底部,产气(泡沫),并且(90%个例)产生硫化氢(琼脂变黑)(9.5.3.8)。
