2020年中考化学九大知识点搞定溶解度
九年级化学溶解度知识点

九年级化学溶解度知识点
化学溶解度是指某种物质在某种溶剂中的能力。
它可以用来比较不同的物质的水溶性。
物质的溶解度是化学反应的关键因素,它可以影响解离度,影响离子在溶液中的活动能力。
溶解度是一种熵因素,衡量溶剂和溶质之间的能量变化情况。
当溶剂与溶质混合时,溶质比溶剂中受到了能量。
通常来说,溶质越溶于溶剂,能量改变就越大,溶解度也就越大。
溶解度可以分为熔解度和溶解度,其中熔解度指的是物质在溶剂中的溶解程度,溶解度则指的是物质的溶解性。
这些物质可能是碱性物质、液体、气体等,它们的溶解度可能不同。
九年级学生学习溶解度要正确理解,学会分辨不同物质在溶剂中的溶解程度。
通过对比实验,结合实践活动,加深对溶解度的理解,学会掌握物质的溶解度变化规律,学会正确掌握和使用溶解度的相关概念。
比如,苏打粉和盐的溶解度是不同的,同样的溶剂中,苏打粉的溶解度大于盐的溶解度。
反之,糖的溶解度比盐的溶解度要小。
因此,学生要懂得溶解度并牢记它们之间的差异。
此外,温度也会影响溶解度,温度升高时,溶解度会增加,反之温度降低时,溶解度会降低。
学生要明白不同温度下溶解度的变化,及时利用温度变化、改变溶解度进行实验。
学习溶解度主要是为了帮助九年级学生懂得如何用实验和实践活动加深理解概念,并正确运用它们,正确掌握科学原理,提高学习效果。
总之,九年级学生在学习溶解度的过程中,要学会理解不同物质的溶解度,明白温度对溶解度的影响,以及正确使用溶解度的相关概念。
只有这样,才能有效提高学习效果,学好九年级化学溶解度。
九年级化学《溶解度》知识点总结及典型例题

九年级化学《溶解度》知识点总结及典型例题九年级化学《溶解度》知识点总结及典型例题【知识点总结】本部分内容包括饱和溶液、不饱和溶液、溶解度的内容,概念性的东西比较多,学习时要注意抓住概念的特点,注意去理解概念的内涵,要注意对相似概念进行比较学习,如对于饱和溶液和不饱和溶液,对比去理解。
1、饱和溶液和不饱和溶液的概念:饱和溶液:在一定温度下(溶质为气体时还需在一定压强下),向一定量溶剂里加入某种溶质,当溶质不能继续溶解时所得到的溶液,叫做这种溶质在这种溶剂里的饱和溶液。
不饱和溶液:在一定温度下(溶质为气体时,还需在一定压强下),向一定量溶剂里加入某种溶质,当溶质还能继续溶解时的溶液,叫做这种溶质在这种溶剂里的不饱和溶液。
2、饱和溶液和不饱和溶液之间的相互转化:大多数情况下饱和溶液和不饱和溶液存在以下转化关系(溶质为固体):但是,由于Ca(OH)2的溶解度在一定范围内随温度的升高而减小,因此将Ca(OH)2的不饱和溶液转化为饱和溶液,在改变温度时应该是升高温度;将熟石灰的饱和溶液转化为不饱和溶液,在改变温度时应该是降低温度。
3、饱和溶液和不饱和溶液的判断:一般说来,可以向原溶液中再加人少量原溶质,如果溶解的量不再增大则说明原溶液是饱和溶液,如果溶解的量还能增大则说明原溶液是不饱和溶液。
4、溶解度的含义:固体的溶解度:在一定温度下某固体物质在100g溶剂里达到饱和状态时所溶解的质量,叫做这种物质在这种溶剂里的溶解度。
如果不说明溶剂通常所说的溶解度是指物质在水里的溶解度。
影响因素:①溶质、溶剂的性质;②温度。
气体的溶解度:气体的溶解度是指该种气体在一定压强和一定温度时溶解在1体积水里达到饱和状态时的气体体积(气体的体积要换算成标准状况时的体积)。
影响气体溶解度的因素:内因:气体和水本身的性质。
外因:①温度:随温度升高而减小;②压强:随压强增大而增大。
5、溶解度曲线:当溶质一定、溶剂一定时.固态物质的溶解度主要受温度的影响,也就是说,固态物质的溶解度是温度的函数。
初三化学溶解度知识点归纳

初三化学溶解度知识点归纳
化学溶解度是指在一定温度下,溶质在溶剂中溶解的最大量。
溶解度可以用溶解度曲线、溶解度表和溶解度规律来描述和预测。
1. 溶解度曲线:溶解度曲线是描述溶解度随温度变化的图形。
通常溶解度随温度的升高而增加,但也有一些物质在温度升高时溶解度会减小。
2. 溶解度表:溶解度表是列出不同温度下物质的溶解度的表格。
通过溶解度表可以了解不同温度下物质的溶解度变化规律。
3. 溶解度规律:常见的溶解度规律有以下几种:
- 溶解度随温度升高而增加的物质,称为热溶质;
- 溶解度随温度升高而减小的物质,称为冷溶质;
- 溶解度随温度变化不大的物质,称为中性溶质;
- 溶解度随温度变化无规律的物质,称为理想溶质;
- 溶解度随温度升高或降低都有明显变化的物质,称为非理想溶质。
4. 影响溶解度的因素:溶解度受到温度、压力和溶液浓度等因素的影响。
一般情况下,溶解度随温度的升高而增加,但也有例外情况。
溶解度还受到物质之间的相互作用力、溶质和溶剂的极性等因素的影响。
5. 饱和溶液和过饱和溶液:当溶液中已经溶解了最大量的溶质时,称为饱和溶液。
过饱和溶液是指溶液中溶质的溶解度超过了饱和溶
液的溶解度,此时溶液处于不稳定状态,稍微的扰动就会使溶质析出。
6. 溶解度的单位:溶解度通常用摩尔溶解度(mol/L)或质量溶解度(g/L)来表示。
总结起来,化学溶解度是描述溶质在溶剂中溶解的最大量的性质。
溶解度受到温度、压力、溶液浓度和物质之间的相互作用力等因素的影响。
了解溶解度的规律可以帮助我们理解溶液的性质和溶解过程。
中考化学考点全解 考点十七 溶解度(含解析)-人教版初中九年级全册化学试题

考点十七:溶解度概念:在一定温度下,某固态物质在100g溶剂里达到饱和状态时所溶解的质量,叫做这种物质在这种溶剂里,该温度下的溶解度。
正确理解溶解度概念的要素:①条件:在一定温度下,影响固体物质溶解度的内因是溶质和溶剂的性质,而外因就是温度。
如果温度改变,则固体物质的溶解度也会改变,因此只有指明温度时,溶解度才有意义。
②标准:“在100g溶剂里”,需强调和注意的是:此处100g是溶剂的质量,而不是溶液的质量。
③状态:“达到饱和状态”,溶解度是在同一条件下某种物质溶解能力大小的标准,只有达到该条件下溶解的最大值,才可知其溶解度,因此必须要求“达到饱和状态”。
④单位:溶解度是所溶解的质量,常用单位为克(g)。
易错考点溶解度曲线的应用a.根据溶解度曲线可以查出某物质在一定温度下的溶解度;b.可以比较不同物质在同一温度下的溶解度大小;c.可以知道某物质的溶解度随温度的变化情况;d.可以选择对混合物进行分离或提纯的方法;e.确定如何制得某温度时某物质的饱和溶液的方法等。
例题分析例题1:为了探究影响物质溶解性的因素,老师演示了以下实验:如图所示是碘或高锰酸钾分别放入水或汽油中.(1)观察①②两支试管的现象,可以得出影响物质溶解性的因素之一是_____.(2)观察②④两支试管的现象,可以得出影响物质溶解性的因素之一是______.(3)影响物质溶解性的因素还有______.答案:(1)与溶剂的种类有关;(2)与溶质的种类有关;(3)温度.解析:【解答】(1)碘几乎不溶于水,但易溶于汽油,所以影响碘的溶解性的因素是溶剂不同,所以与溶剂的种类有关;(2)碘易溶于汽油,高锰酸钾几乎不溶于汽油,而溶质的种类不同,所以影响溶解性的因素还与溶质的种类有关;(3)升高温度,分子运动速度加快,物质溶解的速度加快,所以影响物质溶解性的因素还有温度.【分析】:溶解性的大小与溶质,溶剂的性质(内因)有关,也与温度,压强(外因)有关。
2020年中考化学物知识点之溶解度表的信息
2020年中考化学物知识点之溶解度表的信息
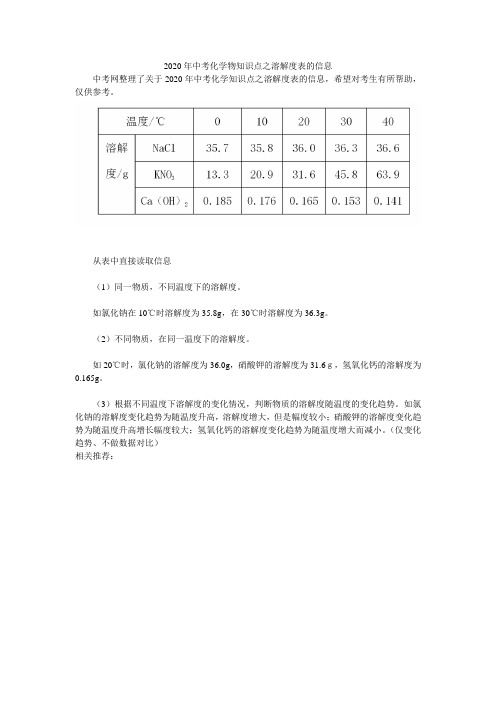
中考网整理了关于2020年中考化学知识点之溶解度表的信息,希望对考生有所帮助,仅供参考。
从表中直接读取信息
(1)同一物质,不同温度下的溶解度。
如氯化钠在10℃时溶解度为35.8g,在30℃时溶解度为36.3g。
(2)不同物质,在同一温度下的溶解度。
如20℃时,氯化钠的溶解度为36.0g,硝酸钾的溶解度为31.6g,氢氧化钙的溶解度为0.165g。
(3)根据不同温度下溶解度的变化情况,判断物质的溶解度随温度的变化趋势。
如氯化钠的溶解度变化趋势为随温度升高,溶解度增大,但是幅度较小;硝酸钾的溶解度变化趋势为随温度升高增长幅度较大;氢氧化钙的溶解度变化趋势为随温度增大而减小。
(仅变化趋势、不做数据对比)
相关推荐:。
初中化学溶解度表及口诀

初中化学溶解度表及口诀
初中化学溶解度表及口诀如下:
口诀:
钾钠铵盐硝酸盐,完全溶解不困难,氯化亚汞氯化银,硫酸钡和硫酸铅,生成沉淀记心间,氢硫酸盐和碱类,碳酸磷酸硝酸盐,可溶只有钾钠铵。
钾钠铵硝皆可溶,盐酸不溶银亚汞;硫酸不溶钡和铅,碳磷酸盐多不溶;多数酸溶碱少溶,只有钾钠铵钡钙。
钾钠铵盐硝酸盐,溶入水中都不见;硫酸盐类不溶钡,氯化物中不溶银;碳酸盐类多不溶,只有钾钠铵盐溶。
溶解度表:
钾盐、钠盐、铵盐、硝酸盐都溶于水。
硫酸盐除了硫酸钡、硫酸铅不溶,硫酸钙、硫酸银微溶外,其他都溶。
盐酸盐除了氯化银不溶外,其他都溶。
碳酸盐除了碳酸钾、碳酸钠、碳酸铵溶外,其他都不溶。
需要注意的是,口诀和表格只是帮助记忆的工具,具体物质的溶解度还需要参考实验数据和资料。
此外,溶解度不仅受物质本身性质的影响,还与温度、压强等条件有关。
因此,在理解和应用溶解度概念时,需要综合考虑各种因素。
初三化学溶解度知识点的归纳

初三化学溶解度知识点的归纳初三化学溶解度知识点的归纳在日常生活或是工作,学习中,大家一定都或多或少地接触过一些化学知识,下面是店铺为大家收集的有关初三化学溶解度知识点的归纳相关内容,仅供参考,希望能够帮助到大家。
初三化学溶解度知识点的归纳11、温度是影响固体物质溶解的唯一外界因素,振荡、搅拌只能加快固体物质的溶解速率,而不能改变固体的溶解度。
2、溶解度曲线既能定性地反映固体的溶解度受温度影响而变化的趋势(溶解度曲线的伸展方向),也能表示某固态物质在某温度下的溶解度,还能用于比较同一温度不同溶质的溶解3、气体的溶解度受温度和压强的影响。
温度一定,气体的溶解度随压强的增大而增大,随压强的减小而减小;压强一定,气体的溶解度随温度的升高而减小,随温度的降低而增大。
4、四点理解溶解度概念:①一定温度。
同一种固体物质在不同温度下对应的溶解度是不同的,因此必须指明温度。
②100g溶剂。
此处100g是指溶剂质量,不能误认为溶液质量。
③饱和状态。
在一定温度下,某固态物质在100g溶剂里所溶解的最大质量为这种物质在这种溶剂里的溶解度。
④单位:g[严格地说应该是g/100g(溶剂)]。
5、二角度比较饱和溶液与不饱和溶液:①首先要明确“一定条件”、“一定量的溶剂”。
在某一温度和一定量的溶剂里,对某种固态溶质来说饱和了,但若改变温度或改变溶剂的量,就可能使溶液不饱和了。
如室温下,100g水中溶解31.6gKNO3达到饱和,若升高温度或增大溶剂(水)量,原来饱和溶液就变为不饱和溶液。
所以溶液饱和与否,首先必须明确“一定条件”和“一定量的溶剂”。
②必须明确是某种溶质的饱和溶液或不饱和溶液。
如:在一定条件下不能再溶解食盐的溶液,可能还能继续溶解蔗糖,此时的溶液对于食盐来说是饱和溶液,但是对于蔗搪来说就是不饱和溶液。
6、根据溶解度曲线可以查出某温度下该物质的溶解度;也可以查出该物质已知溶解度所对应的温度。
曲线上的点即该物质对应温度时的溶解度,按其数据配成的溶液正好为饱和溶液;不同物质在同一温度下的溶解度的大小可借助不同物质的溶解度曲线加以比较。
2020年中考化学考点之溶解度

2020年中考化学考点之溶解度
中考网整理了关于2020年中考化学考点之溶解度,希望对考生有所帮助,仅供参考。
溶解度
固体物质溶解度:在一定温度下,某固态物质在100克溶剂里达到饱和状态时所溶解的质量,叫做这种物质在这种溶剂里的溶解度。
根据溶解度的概念和溶液中溶质、溶剂和溶液的量的关系,可进行如下的有关计算。
(1)根据在一定温度下,某物质饱和溶液里的溶质和溶剂的量,求这种物质的溶解度。
(2)根据某物质在某温度下的溶解度,求该温度下一定量的饱和溶液里含溶质和溶剂的质量。
(3)根据某物质在某温度下的溶解度,求如果溶剂质量减少(蒸发溶剂)时,能从饱和溶液里析出晶体的质量。
(4)根据某物质在某温度下的溶解度,求如果温度变化(降温或升温)时,能从饱和溶液里析出或需加入晶体的质量。
相关推荐:。
九年级下册化学溶解度知识点总结

九年级下册化学溶解度知识点总结化学溶解度是指在一定温度下,单位体积溶液中所能溶解的最大物质量,通常用溶质在100克溶剂中溶解的质量来表示。
对于溶解度这个概念,同学们可能早就接触过了,而在九年级下册化学教材中涉及了一些溶解度相关的知识点。
现在我们就来总结一下这些知识点,加深对溶解度及其相关概念的理解。
1. 溶解度的影响因素溶解度受温度、压强和溶质浓度的影响。
一般来说,温度升高溶解度增大,温度降低溶解度减小。
但对于固体在液体中的溶解度来说,有些固体在溶液中的溶解度随温度的升高而减小,这是因为在某些情况下固体在溶液中的溶解过程是放热的。
压强对气体的溶解度有较大影响,在温度不变的情况下,压强升高溶解度增大。
而溶质的浓度对溶解度的影响则比较复杂,一般来说溶质浓度增加,溶解度也增加,但在某些情况下可能会出现溶解度减小的情况。
2. 饱和溶解度与过饱和溶解度饱和溶解度指在一定温度下,溶质在溶剂中达到动态平衡时的溶质质量与溶剂质量的比例。
饱和溶液有一个固定的溶质质量。
而过饱和溶液则指在同样温度下,溶质的质量超过了饱和溶液所允许的最大溶质质量。
过饱和溶液是不稳定的,可以通过加热、振动等外界条件来使其结晶。
3. 饱和溶液中溶质质量计算在一定条件下,溶质在溶剂中达到饱和时,我们可以通过计算溶质的质量来确定溶液是否饱和。
计算公式为质量分数=溶质质量/溶液质量。
当质量分数等于饱和溶度时,溶液为饱和溶液。
4. 溶解度曲线溶解度曲线是指在一定温度下,溶质在溶剂中的饱和溶解度随溶质浓度的变化关系的曲线。
不同物质的溶解度曲线有所不同。
当溶质的溶解度随溶质浓度的增加而增加时,称为正溶解度曲线。
当溶质的溶解度随溶质浓度的增加而减小时,称为反溶解度曲线。
5. 溶解度的应用溶解度在日常生活和工业生产中有着广泛应用。
在农业生产中,我们可以通过调节肥料中溶质的浓度来控制肥料的效果。
在医药生产中,了解药物的溶解度,可以根据患者的需要来调节药物的剂量以达到最佳治疗效果。
中考化学考点知识点专题第二讲 溶解度

第二讲溶解度知识能力解读知能解读:(一)溶解性1.概念一种物质溶解在另一种物质里的能力叫做该物质的溶解性。
说明:①不同物质在同一溶剂里的溶解性不同。
如常温下高锰酸钾易溶解在水中,而碘几乎不溶于水。
②同一种物质在不同溶剂中的溶解性不同。
如常温下高锰酸钾易溶解在水中,却很难溶解在汽油里;碘微溶于水,却易溶于汽油。
③同一种物质在同一种溶剂中的溶解性与温度有关。
2.溶解性的表示方法溶解性的大小常用溶解度来表示。
知能解读:(二)固体物质的溶解度1.概念在一定温度下,某固态物质在100g溶剂里达到饱和状态时所溶解的质量,叫做这种物质在这种溶剂里的溶解度。
2.正确理解溶解度概念的要素(1)条件:在一定温度下。
影响固体物质溶解度的内因是溶质和溶剂的性质,而外因就是温度。
如果温度改变,则固体物质的溶解度也会改变,因此只有指明温度时,溶解度才有意义。
(2)标准:在100g溶剂里。
需强调和注意的是:此处100 g是溶剂的量,而不是溶液的量。
(3)状态:达到饱和状态。
溶解度是比较同一条件下某种物质溶解能力大小的标准,只有达到该条件下溶解的最大值,才可知其溶解度,因此要求必须“达到饱和状态”。
(4)单位:溶解度是所溶解的质量,常用单位为克(g)。
注意:①如果不指明溶剂,通常所说的溶解度是指固体物质在水中的溶解度。
②溶解度概念中的四个关健词:“一定温度、100 g溶剂、饱和状态、溶解的质量”是同时存在的,只有四个关键词都体现出来了,溶解度的概念和应用才是有意义的,否则没有意义,说法也是不正确的。
即“四定——定温、定剂(100 g)、定饱和、定单位(g)。
3.溶解度的含义(1)溶解度的含义是指某物质在某温度下,在100 g溶剂中达到饱和状态时所溶解的质量。
如3KNO在20℃时的溶解度为31. 6 g,就是指20℃时,3KNO在100 g水中达到饱和时所溶解的质量为31. 6 g (或20℃时,100 g水中最多溶解3KNO的质量为31. 6 g或20℃时,要完全溶解31. 6 g3KNO最少需要100 g水)。
备战2020中考化学知识点归类训练——溶解度

备战2020中考化学知识点归类训练——溶解度知识点一:溶解度1.增加二氧化碳在水中的溶解度,可行的操作是( )A.升温B.加压C.增加水量D.不断通入二氧化碳2.生活中的下列现象,能说明气体的溶解度随压强变化而变化的是( )A.夏天,鱼塘中的鱼常常会浮在水面呼吸B.烧开水时,沸腾前水中有气泡产生C.打开饮料瓶盖会有大量气泡冒出D.喝了汽水以后,常常会打嗝3.打开汽水瓶盖,有大量气体逸出,下列说法不正确的是( )A.溶质减少B.溶解度减小C.浓度减小D.饱和溶液变成不饱和溶液4.判断下列说法中正确的是( )A.20℃时,100 g水里最多溶解36 g氯化钠,所以20℃时氯化钠的溶解度为36 gB.硝酸钾的溶解度为31.6 gC.20℃时,在100 g水中加入35 g氯化钠完全溶解,则20℃时氯化钠的溶解度为35 gD.20℃时,100 g氯化钠的饱和溶液中有27 g氯化钠,则20℃时氯化钠的溶解度为27 g5.将2.5 g硼酸在20℃时溶于50 g水中即达到饱和,则一般把这种物质的溶解性划分为( )A.易溶物质B.可溶物质C.微溶物质D.难溶物质6. 25℃时,50 g水中最多可溶10 g A,30℃时,50 g水中最多可溶15 g B,则A、B溶解度比较为( )A.无法比较B.A大于BC.A小于BD.A等于B7.20℃时,氯化钠的溶解度为36 g。
将40 g氯化钠放入100 g水中,所得氯化钠溶液的质量是多少( )A.40 gB.140 gC.136 gD.100 g8.下列加速物质溶解措施中,能改变固体溶解度的是( )A.加热B.搅拌C.振荡D.把固体研细9.某温度时,将10 g饱和氯化钾溶液蒸干,得氯化钾晶体2 g,则氯化钾在此温度下的溶解度为( )A.10 gB.2 gC.20 gD.25 g10.控制变量法是科学探究中常用的方法之一。
(1)在探究固体物质的溶解度时,需要考虑的因素有①溶质的种类;②溶剂的种类;③溶质最多被溶解的质量;④溶剂的质量;⑤温度。
中考化学溶解度考点总结(大全)-精选学习文档

中考化学溶解度考点总结(大全)溶解度,在一定温度下,某固态物质在100g溶剂中达到饱和状态时所溶解的溶质的质量,叫做这种物质在这种溶剂中的溶解度。
物质的溶解度属于物理性质,更多关于中考化学溶解度考点的内容请看下文。
【溶解度相关概念】
通常把在室温(20度)下:
溶解度在10g/100g水以上的物质叫易溶物质;
溶解度在1~10g/100g水叫可溶物质;
溶解度在0.01g~1g/100g水的物质叫微溶物质;
溶解度小于0.01g/100g水的物质叫难溶物质.
可见溶解是绝对的,不溶解是相对的。
中考化学核心考点:溶解度曲线及其应用
【酸的溶解性】大部分酸及酸性氧化物能溶于水,(酸性氧化物+水→酸)大部分碱性氧化物不溶于水,能溶的有:氧化钡、氧化钾、氧化钙、氧化钠(碱性氧化物+水→碱)
【化学碱的溶解性】
溶于水的碱有:氢氧化钡、氢氧化钾、氢氧化钙、氢氧化钠和氨水,其他碱不溶于水。
难溶性碱中Fe(OH)3是红褐色沉淀,Cu(OH)2是蓝色沉淀,其他难溶性碱为白色。
(包括
Fe(OH)2)
【化学盐的溶解性】
含有钾、钠、硝酸根、铵根的物质都溶于水
含Cl的化合物只有AgCl不溶于水,其他都溶于水;
含SO42- 的化合物只有BaSO4 不溶于水,其他都溶于水。
含CO32- 的物质只有K2CO3、Na2CO3、(NH4)2CO3溶于水,其他都不溶于水。
初中化学中的溶解度知识点整理

初中化学中的溶解度知识点整理化学是一门研究物质以及其组成、性质、结构、变化规律的科学。
在初中阶段,学生将开始接触化学这门学科,并学习一些基本概念和知识。
其中,溶解度是化学中的一个重要概念,它涉及到物质在溶液中的溶解程度。
本文将对初中化学中的溶解度知识点进行整理。
首先,让我们来了解一下什么是溶解度。
溶解度是指在一定温度和压力下,单位溶剂中最多能溶解的溶质的量。
通常用质量比例来表示溶解度,即溶质质量与溶液质量的比值。
溶解度依赖于多个因素,包括温度、压力、溶剂和溶质之间的相互作用力。
其次,我们来了解一下溶解度与温度的关系。
一般情况下,随着温度的升高,溶解度会增加。
这是因为随着温度的升高,溶剂分子的平均动能也增加,使得其能够与溶质分子更好地相互作用,从而有利于溶解过程。
然而,有些物质的溶解度却会随着温度的升高而降低,这是因为在这些物质的溶解过程中伴随着放出热量,温度升高会导致放热反应的平衡位置移动,使得反应向左偏离,从而溶解度降低。
除了温度,压力对溶解度的影响也是需要考虑的因素。
对于气体溶于液体的溶解过程来说,压力对溶解度的影响十分显著。
根据亨利定律,气体溶解于液体中的溶解度与气体的压力成正比。
随着气体压力的增加,溶解度也会随之增加。
这是因为高压能够压缩气体分子,使其更容易溶解于溶剂中。
另外,溶质和溶剂之间的相互作用力也会影响溶解度。
溶质和溶剂之间的相互作用力越强,溶解度通常也会越大。
例如,极性分子倾向于与极性溶剂相互作用,而非极性分子倾向于与非极性溶剂相互作用。
这些相互作用力的强弱会影响到溶解度。
此外,溶解度知识还涉及到饱和溶液和过饱和溶液的概念。
当溶质以最大限度溶解于溶剂中时,我们称之为饱和溶液。
饱和溶液在一定温度下能够维持一定的溶解度。
当继续向饱和溶液中添加溶质时,会形成过饱和溶液。
过饱和溶液在一定条件下是稳定的,但稍微的扰动就会导致溶质析出。
最后,根据溶解度的概念,我们可以了解到溶液的浓度可以通过溶解度来控制。
九年级化学下册溶解度知识点

九年级化学下册溶解度知识点
九年级化学下册的溶解度知识点包括以下内容:
1. 溶液:溶质溶解在溶剂中形成的混合物,溶质是被溶解的物质,溶剂是进行溶解的物质。
2. 浓度:溶液中溶质的质量或物质的摩尔浓度。
常用的浓度单位有质量浓度(g/L),物质的摩尔浓度(mol/L)等。
3. 饱和溶解度:在一定的温度条件下,溶质溶解在溶剂中所达到的最大溶解度。
溶质的饱和溶解度与温度、溶剂的性质有关。
4. 温度对溶解度的影响:一般来说,固体在液体中的溶解度随温度的升高而增大,气体在液体中的溶解度随温度的升高而减小。
5. 非极性物质的溶解度:非极性物质在非极性溶剂中的溶解度常较大,而在极性溶剂中的溶解度较小。
6. 极性物质的溶解度:极性物质在极性溶剂中的溶解度较大,而在非极性溶剂中的溶解度较小。
7. 非极性溶质和非极性溶剂的溶解度:非极性溶质和非极性溶剂之间的溶解度往往较大。
8. 极性溶质和极性溶剂的溶解度:极性溶质和极性溶剂之间的溶解度往往较大。
9. 郁郁溶解度:某些物质的溶液,在特定的温度和压强条件下,存在一定的极限浓度,超过这个极限浓度后,物质不再溶解,而是沉淀出来。
以上是九年级化学下册涉及的溶解度知识点。
希望对你有帮助!。
九年级化学溶解度笔记

九年级化学溶解度笔记
溶解度是一个介于固体与液体之间的概念,溶解度定义为某种物质
在特定溶剂中的溶解量,即在单位体积或单位质量的溶剂中最多可以
溶解的物质的质量或体积。
溶解度受到物质的性质、温度、压力和溶剂的性质等多种因素的影响。
可以根据物质性质及其性质的变化,说明溶解度的大小。
溶解度的含量是根据物质的溶解度和溶剂种类决定的,容量可以用不
同的参数来表示,比如mol/L或kg/L,以及比重等指标。
一般来说,溶解度是不可逆变化的,决定着物体在溶液中的分布状态
和溶解度。
一般情况下,在常温下,不同种类的物质具有不同的溶解度,有些物质容易溶解,而有些物质则不易溶解。
初三新人教版化学下溶解度知识点

初三新人教版化学下溶解度知识点溶解度是某固态物质在一定温度下,在100g溶剂中达到饱和状态时所溶解溶质的质量。
查字典化学网为大家整理了溶解度知识点,希望对大家有帮助!知识点一、概念:1、固体的溶解度是指在一定的温度下,某物质在100克溶剂里达到饱和状态时所的克数。
在未注明的情况下,通常溶解度指的是物质在水里的溶解度。
2、气体的溶解度通常指的是该(其为1标准)在一定温度时溶解在1体积水里的数。
通常把在室温(20度)下:溶解度在10g/100g水以上的物质叫易溶物质;溶解度在1~10g/100g水叫可溶物质;溶解度在0.01g~1g/100g水的物质叫微溶物质;溶解度小于0.01g/100g水的物质叫难溶物质.可见溶解是绝对的,不溶解是相对的。
二、影响溶解度大小的因素;物质溶解与否,溶解能力的大小,一方面决定于物质的本性;另一方面也与外界条件如温度、溶剂种类等有关。
在相同条件下,有些物质易于溶解,而有些物质则难于溶解,即不同物质在同一溶剂里溶解能力不同。
通常把某一物质溶解在另一物质里的能力称为溶解性。
例如,糖易溶于水,而油脂不溶于水,就是它们对水的溶解性不同。
溶解度是溶解性的定量表示。
气体的溶解度还和压强有关。
压强越大,溶解度越大,反之则越小;温度越高,气体溶解度越低。
三、溶解度曲线:1点溶解度曲线上的每个点表示的是某温度下某种物质的溶解度。
2线溶解度曲线表示某物质在不同温度下的溶解度或溶解度随温度的变化情况。
根据溶解度曲线,选择分离某些可溶性混合物的方法。
3交点两条溶解度曲线的交点表示该点所示的温度下两物质的溶解度相同,此时两种物质饱和溶液的溶质质量分数也相同。
大部分固体随温度升高溶解度增大,如硝酸钾;少部分固体溶解度受温度影响不大,如食盐;极少数物质溶解度随温度升高反而减小,如氢氧化钙。
课后练习1.在一定温度下,某物质的饱和溶液一定是 ( )A.浓溶液B.稀溶液C.不能溶解任何物质的溶液D.不能继续溶解该物质的溶液2.下列说法中正确的是( )A.100g水中最多能溶解某物质40g,则该物质的溶解度为40gB.4℃时,溶质N的饱和溶液120g中含N 20g,所以4℃时,溶质N的溶解度为20gC.一定温度下,物质M的饱和溶液100g中含M物质30g,则物质M在该温度时的溶解度为30gD.20℃时,50g水中溶有溶质P 20g,则物质P在20℃时的溶解度为40g3.将60℃时的硝酸钾饱和溶液冷却到室温,下列叙述错误的是 ( )A.溶剂质量不变B.溶质质量分数变小C.溶液质量不变D.有KNO3晶体析出4.下列关于饱和溶液的说法中,错误的是( )A.在温度不变时,KNO3饱和溶液不能再溶解KNO3晶体B.改变条件可以使不饱和溶液变成饱和溶液C.室温下,与固体溶质共存的溶液一定是这种溶质的饱和溶液D.在温度升高时,某物质的饱和溶液一定能继续溶解该物质5.下列有关溶液的说法中,正确的是 ( )A、不饱和溶液转化为饱和溶液,其溶质的质量分数一定增大B、饱和溶液不蒸发溶剂而析出晶体后,溶液的溶质质量分数一定减小C、只要温度不变,某饱和溶液中溶质的质量分数一定不变D、降温时,饱和溶液肯定不析出晶体答案:1.D 2.B 3.C 4.D 5.B溶解度知识点的全部内容就是这些,不知道大家是否已经都掌握了呢?预祝大家可以更好的学习,取得优异的成绩。
九年级上化学溶解度知识点

九年级上化学溶解度知识点化学是一门研究物质组成、性质与变化规律的科学,溶解度是化学中一个重要的概念。
溶解度是指在一定温度下,单位体积溶剂中能溶解的溶质的最大量,通常用溶质在100g水中的溶解质量或溶质在100ml溶剂中的溶质体积来表示。
接下来,我们就来了解一下九年级上化学课程中关于溶解度的知识点。
一、什么是溶解度溶解度是指在一定温度下,溶质溶解在溶剂中所形成的饱和溶液中的溶质的量或浓度。
它是表示溶液中溶质溶解能力大小的物理量。
二、影响溶解度的因素1. 温度溶解度随着温度的升高而增大,大部分溶质在升温时溶解度增大,这是因为升高温度使溶质分子或离子的平均动能增大,溶质分子或离子更易离开晶体或稳定物质,进入溶剂中。
2. 压力对固体和液体来说,压力的改变对溶解度没有影响。
但对气体溶解度来说,压力的升高会增加气体在溶液中的溶解度。
当气体分子进入溶剂中时,溶剂压力增大,从而使溶解度增大。
3. 溶质和溶剂的性质溶质和溶剂的相互作用力对溶解度有着重要影响。
如果溶质和溶剂之间的相互作用力较强,溶解度就较小,反之亦然。
例如,极性溶质易溶于极性溶剂,而非极性溶质易溶于非极性溶剂。
4. 浓度溶质的浓度越大,其溶解度越小。
这是因为当溶质浓度较高时,溶质分子或离子之间的间距较小,难以离开溶质颗粒,从而导致溶解度降低。
三、溶解度曲线溶解度曲线是通过实验得到的一组关于溶质在溶剂中溶解度随温度变化的曲线。
溶解度曲线通常具有以下几种形态:1. 正曲线当溶质溶解度随温度升高而增大时,溶解度曲线呈现正曲线。
2. 负曲线当溶质溶解度随温度升高而减小时,溶解度曲线呈现负曲线。
3. 变曲线当溶液的溶质由于结晶水的结晶或溶剂由于化学反应而发生变化时,溶解度曲线可能会呈现出复杂的形状。
四、溶质的饱和溶解度和过饱和溶解度饱和溶解度指的是在一定温度下,溶液中溶质达到饱和状态时的溶质质量或浓度。
过饱和躶释是指溶液中溶质的溶液度大于其饱和溶解度。
过饱和溶液通常是在高温下饱和溶液逐渐冷却得到的。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
干货:2020年中考化学九大知识点搞定溶解度物质的溶解度
一、定义:
一种物质溶解在另一种物质里的能力叫溶解性.溶解性的大小与溶质和溶剂的性质有关.根据物质在20℃时溶解度的大小不同,把物质的溶解性通常用易溶、可溶、微溶、难溶等概念粗略地来描述.
二、固体的溶解度概念:
在一定温度下,某固体物质在100g溶剂里达到饱和状态时所溶解的质量,叫做这种物质在这种溶剂里的溶解度.
在理解固体的溶解度概念时,要抓住五个要点:
①“在一定温度下”:因为每种固体物质的溶解度在一定温度下有一个对应的定值,但这定值是随温度变化而变化的,所以给某固体物质的溶解度时,必须指出在什么温度下的溶解度才有意义。
②“在100g溶剂里”:溶剂质量有规定的值,统一为100g,但并不是100g溶液,在未指明溶剂时,一般是指水.
③“饱和状态”:所谓饱和状态,可以理解为,在一定温度下,在一定量的溶剂里,溶质的溶解达到了最大值.
④“所溶解的质量”:表明溶解度是有单位的,这个单位既不是度数(°),也不是质量分数(%),而是质量单位“g”.
⑤“在这种溶剂里”:就是说必须指明在哪种溶剂里,不能泛泛地谈溶剂.因为同一种物质在不同的溶剂里的溶解度是不相同的.
三、影响固体溶解度大小的因素
①溶质、溶剂本身的性质.同一温度下溶质、溶剂不同,溶解度不同.
②温度的高低也是影响溶解度大小的一个重要因素.固体物质的溶解度随温度的不同而不同.大多数固态物质的溶解度随温度的升高而升高;少数物质(如氯化钠)的溶解度受温度的影响很小;也有极少数物质(如熟石灰)的溶解度随温度的升高而降低.
四、固体物质溶解度的计算
1、纯净物与含杂质物质的换算关系:
含杂质物质的质量×纯物质质量分数=纯净物质的质量
纯净物质的质量÷纯物质质量分数=含杂质物质的质量
物质纯度= 纯净物质量/混合物质量×100% = 1—杂质的质量分数
2.含杂质物质的化学方程式的计算步骤:
(1)将含杂质的物质质量换算成纯净物的质量。
(2)将纯净物质质量代入化学方程式进行计算。
(3)将计算得到的纯净物质量换算成含杂质物质的质量。
五、溶解度曲线
1、定义:
用纵坐标表示溶解度,横坐标表示温度,根据某物质在不同温度时的溶解度,可以画出该物质的溶解度随温度变化的曲线,这种曲线叫做溶解度曲线。
2、溶解度曲线的意义:
①溶解度受温度变化而变化的趋势
②溶解度曲线上的任一点表示物质在该温度下的溶解度
③交点:表示几种物质在交点所示温度下的溶解度相等
3、溶解度曲线的应用:
①查阅某温度下指定物质的溶解度
②比较同一温度下,不同物质的溶解度的大小
③比较不同温度下,同种物质溶解度大小
④选择适宜方法(结晶法)分离混合物
六、溶质的质量分数
1、定义:溶液中溶质的质量分数是溶质质量与溶液质量之比。
2、关系式:溶质的质量分数= 溶质质量/溶液质量×100%
七、溶液的配制
1、步骤:①计算②称量③溶解④装配贴签
2、误差分析:⑴计算错误⑵天平称量错误⑶量筒量取水错误
八、溶液质量分数的计算
1、关系式的计算
2、溶液的稀释计算
溶液的稀释计算是根据稀释前后溶液中溶质的质量不变
稀释前溶液的质量×稀释前溶液中溶质的质量分数=稀释后溶液的质量×稀释后溶液中溶质的质量分数
3、溶质的质量分数与化学方程式的计算
九、混合物的分离
适用范围:固体与液体分离过滤
操作要点:“一贴、二低、三靠”
混合物的分离:
②、冷却热饱和溶液:适用于溶解度随温度变化(较大的固体物
质)
②、结晶:蒸发结晶适用于溶解度随温度变化,不大的固体物质。
