化学总复习思维导图 (2)
《邢其毅 基础有机化学 第3版 上册 笔记和课后习题 含考》读书笔记思维导图

思维导图PPT模板
本书关键字分析思维导图
习题
有机化学
考生
基础
考研
邢其毅
内容
真题
笔记
复习 教材
知识
名校
第版
免费
参考书目 书
命题
电子书
01 第1章 绪论
目录
02 第2章 有机化合物的 分类 表示方式命名
13.1 复习笔记
13.3 名校考研真 题详解
读书笔记
谢谢观看
4.1 复习笔记
4.3 名校考研真题 详解
第5章 紫外光谱 红外光谱 核磁 共振和质...
5.2 课后习题详解
5.1 复习笔记
5.3 名校考研真题 详解
第6章 脂肪族饱和碳原子上的亲 核取代反应...
6.2 课后习题详解
6.1 复习笔记
6.3 名校考研真题 详解
第7章 卤代烃 有机金属化合物
10.1 复习笔记
10.3 名校考研真 题详解
第11章 苯和芳香烃 芳香亲电取 代反应
11.2 课后习题详 解
11.1 复习笔记
11.3 名校考研真 题详解
第12章 醛和酮 亲核加成 共轭 加成
12.2 课后习题详 解
12.1 复习笔记
12.3 名校考研真 题详解
第13章 羧酸
13.2 课后习题详 解
目录
011 第11章 苯和芳香烃 芳香亲电取代反应
013 第13章 羧酸
012
第12章 醛和酮 亲核 加成 共轭加成
本书特别适用于参加研究生入学考试指定考研参考书目为邢其毅《基础有机化学》(第3版)(上册)的考 生。也可供各大院校学习邢其毅《基础有机化学》(第3版)(上册)的师生参考。《邢其毅主编的《基础有机化 学》(第3版)是我国高校化学类广泛采用的权威教材之一,也被众多高校(包括科研机构)指定为考研考博专业 课参考书目。为了帮助参加研究生入学考试指定参考书目为邢其毅主编的《基础有机化学》(第3版)的考生复习 专业课,我们根据该教材的教学大纲和名校考研真题的命题规律精心编写了邢其毅《基础有机化学》(第3版)辅 导用书(均提供免费下载,免费升级):1.[3D电子书]邢其毅《基础有机化学》(第3版)(上册)笔记和课后 习题(含考研真题)详解[免费下载]2.[3D电子书]邢其毅《基础有机化学》(第3版)(下册)笔记和课后习题 (含考研真题)详解[免费下载]3.[3D电子书]邢其毅《基础有机化学》(第3版)(上册)配套题库【名校考研 真题+课后习题+章节题库+模拟试题】[免费下载]4.[3D电子书]邢其毅《基础有机化学》(第3版)(下册)配 套题库【名校考研真题+课后习题+章节题库+模拟试题】[免费下载]本书是邢其毅主编的《基础有机化学》(第3 版)的配套e书,主要包括以下内容:(1)梳理知识脉络,浓缩学科精华。本书每章的复习笔记均对该章的重难 点进行了整理,并参考了国内名校名师讲授该教材的课堂笔记。因此,本书的内容几乎浓缩了该教材的所有知识 精华。(2)详解课后习题,巩固重点难点。本书参考大量相关辅导资料,对邢其毅主编的《基础有机化学》(第 3版)的课后思考题进行了详细的分析和解答,并对相关重要知识点进行了延伸和归纳。(3)精编考研真题,培 养解题思路。本书精选详析了部分名校近年来的相关考研真题,这些高校均以该教材作为考研参考书目。所选考
有机化学基础思维导图

人教版九年级化学中考复习必备《二氧化碳 思维导图》(24张 PPT)
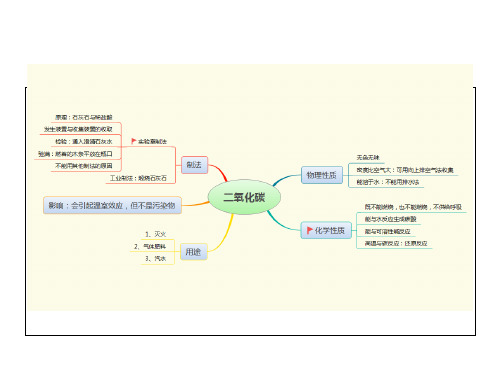
•
பைடு நூலகம்
•
•
•
•
•
•
•
•
•
•
•
•
•
•
•
•
•
•
•
•
•
•
•
卫 生 院 “ 健 康过大 -”主题 服务活 动实施 设计方 案 为 贯彻落 实 《XX市“健 健康康 过大年 ”主题 服务活 动实施 意见 》以及齐 卫发 【XX】 2号 文 件 精 神 ,根据 院委会 研究决 定,XX年 春节期 间,在我 镇卫生 院及16处定点卫生室
开 展 “ 健 健 康康过 大年” 主题服 务活动 ,特制订 本方案 : 一 、 为 更 好 、更快 、更稳 贯彻落 实“健 健康康 过大年 ”主题 服务活 动,经院 委会研
认 真 学 习 齐 卫发【XX】2号 文 件 精神。 2、 1月 26日 全 面 做 好辖区 宣传发 动、启 动实施 工作,坚 持院长 亲自抓 、负总责,明确 专 人 负 责 ,加 强舆论 宣传,通 过电子 显示屏 、设置 宣传栏 、悬挂 条幅等 形式,大 力宣
传 推 行 “ 健 健康康 过大年 ”主题 服务活 动。 3、 1月 27日 -2月 25日 公 共 卫生科 组织防 保人员 及全镇 乡村医 生集开 展针对 城乡外 出 务工、 就学回 乡过节 人员等 重点人 群 ,按照 服务规 范要求 ,建立城 乡居民 健康档 案,
究 ,决 定 成 立 服务活 动领导 小组:组 长:张 三 副 组 长 :李 四 成 员 :王 五 贾 六 小七小九 二、工作安排
1、 1月 25日 我 院 及 时召开 公共卫 生人员 及定点 卫生室 负责人 会议,通 报《德 州市 “ 健 健 康 康 过大年 ”主题 服务活 动实施 意见》以 及齐 卫发【XX】2号 文 件 精神,并
化学中考复习第二单元 我们周围的空气

化学反应方程式
第二单元 我们周围的空气
氧气的性质
图解: 木炭在空气中燃烧现象为红热, 无烟、 无焰, 放出热量; 在氧气 中剧烈燃烧,放出大量的热, 发出白光。
物质 木炭
空气中
持续红热、 无烟无焰
氧气中
剧烈燃烧、 发 出 白光、 放出 热 量、 生成使我们周围的空气
第二单元 我们周围的空气
氧气的性质 思维导图
第二单元 我们周围的空气
氧气的性质
第二单元 我们周围的空气
氧气的性质
第二单元 我们周围的空气
氧气的性质
物质 磷 硫
木炭
铁丝
空气中
氧气中
化学反应方程式
产生大量白烟
火光明亮, 产生大量白烟
发出微弱的淡蓝色火焰,放出 发出蓝紫色火焰、 放出热量、生成有 热量并成有刺激性气味气体 刺激性气味的体。
氧气的性质
图解: 硫在空气里燃烧时发出微弱的淡蓝色火焰, 放出有刺激性气 味的气体;硫在氧气里燃烧时发出明亮的蓝紫色火焰, 放出有刺激性 气味的气体。
物质 硫
空气中
发出微弱的淡 蓝色火焰, 放 出热量并成有 刺激性气味气 体
氧气中
发出蓝紫色火 焰、 放出热量、 生成有刺激性气 味的体。
化学反应方程式
瓶内气体减少, 压强降低。 打开弹簧夹后, 大气压将烧杯里的水压入集气瓶中。
集气瓶内被消耗的氧气的体积就是进入集气瓶中水的体积。
【实验结论】 : 空气中氧气的体积约占空气总体积的五分之一。
拓展: 氮气不能支持红磷燃烧, 水面不会继续上升, 说明氮气不易溶于水。
物质 空气中
氧气中
化学反应方程式
磷 产生大量白烟 火光明亮, 产生大量白烟
思维导图应用于化学复习教学的研究

而思维导图的绘制方法简单 , 的复习方法 , 缺乏 复习实施 的有效 策略 。 如果 能够找到一 复习提供 了理论上 的依据 。 种能使学生觉得复习是一种充满挑 战性 和有趣的学 习任 务的方法 , 那必然会改变他们对 复习教学的片面认识 。 笔
者在教学 过程 中尝试指 导学生利 用思维 导图进行 复 习 , 取得 了不错 的效果 。
处理能力 , 构建学 生 自身知识体 系的重要途径 , 并通过有 复 习不是单纯 的再现课堂上获得 的新 的知识 ,而是使新
效的复习途径不断提高独立 自 的学 习能力 。然而在教 学 的知识得到透彻 的理解 ,以达 到牢 固地掌握并能与其 主
学过程 中我们可 以发现对复 习的重要性 、 习的 目的 、 复 复
目就是复 习” 复习是浪费 时间 ,还不 如多做 几道题 目” “ “ 考试前才需要复 习”等片面的认识 在学生 中广泛存 在。
习过程 中必须要借助“ 积极 的智 力活动” 才能使知识有效
巩 固。 时 、 效的复 习是学 习过程 中必不可少 的环节 , 及 有
这里 , 固然有学生 自身学 习习惯 上的原因 , 但也与我们教 复习是有规律 和方法 的。思维导 图能 够很 好地反映知识
.
。
叠
质、 同素异形体等 , 由于是第一 次画 , 学生只画 了四个分
支, 实际上还可 以延伸出更 多分 支。 在二级主题上进一步 进行联 想 、 发散就 可以得 到三级 、 四级甚至 五级 主题 。 如 由氧气 的结构联想到它在 固态 时形成 的是分 子晶体 , 再
由分子 晶体联想到分子 晶体是通过分子 间作用力结合在
和基本技能” 要使学生具有较强 的问题 意识 , 于质疑 , “ 敢 勤于思索 ,逐步形 成独立思考 的能力 ” 能运 用 比较 、 “ 分
化学总复习(1-3单元)思维导图

D
鉴别三种白色固体
实验步骤 实验现象 结论
加水 不溶解 碳酸钙
加盐酸
产生气泡 碳酸钠
物理性质
颜色、状态、共性、个性等, 性质与用途的关系
防锈 措施
铁生锈
纯金属
保护金属 的有效途径
与氧气反应 化学性质
与盐酸、 稀硫酸反应 与盐溶液 反应
铝的耐腐蚀性 真金不怕火炼
的条件
金属活动性 顺序及其应用
金属资源的 利用与保护
第三单元 物质构成的奥秘
分子 概念 组成
定义 性质 小、动、有间隔
构成
构成 原子
由分子构成 的物质
H2 O2、N2、Cl2 H2O、CO2 、HCl等
分类
定义
性质 小、动、有间隔
核外电子排布
分布
元素
物质
元素符号
元素 周期表
构成
结构
由原子构成 的物质
元素符号 表示的意义
离子
Fe Cu Mg 、 He Ne、 C S P等
反应后溶液 质量的计算
溶解度
固体 溶解度 影响 因素
溶液 的浓度
结晶 方法
溶质的 质量分数
相关计算
概念
溶解性 内因: 溶质和溶剂的性质 划分方法 外因:温度
溶解度 曲线
蒸发结晶 降温结晶
液体的 体积分数
75%的 酒精溶液
溶液的配制 固体配制
计算 称量 溶解
溶液稀释
计算 量取 溶解
表示的意义: 点、交点、线 相关应用:
常见的酸
定义 实质
H++OH-=H2O
酸
中和 反应
PH
碱的通性
ቤተ መጻሕፍቲ ባይዱ
初中化学实验复习中思维导图的运用分析

02
思维导图在初中化学实验 复习中的应用
实验知识系统化
01
梳理实验知识点
通过思维导图将初中化学实验 涉及的知识点进行系统梳理,
形成完整的知识网络。
02
建立知识关联
利用思维导图中的节点和连线 ,展示实验知识点之间的内在 联系和逻辑关系,帮助学生理
解记忆。
03
层次化呈现
按照实验的难易程度、重要程 度等标准,将实验知识点进行 分层呈现,便于学生有针对性
自主学习能力提升
学生反映,在使用思维导图的过程中,他们的自 主学习能力得到了锻炼和提高。
教师评价及建议
教学效果显著
教师们普遍认为,在初中化学实验复习中引入思维导图,显著提高 了教学效果。
学生参与度提高
教师们发现,使用思维导图后,学生在课堂上的参与度明显提高, 积极发言和讨论的学生增多。
建议进一步完善
部分教师建议,可以进一步完善思维导图的制作和使用方法,如增加 更多的实例和练习题,以便更好地满足学生的需求。
06
结论与展望
研究结论总结
思维导图在初中化学实验复习中具有 显著的效果,能够帮助学生更好地理 解和记忆实验内容,提高复习效率。
思维导图在初中化学实验复习中的运 用,有助于培养学生的逻辑思维能力 和自主学习能力,提高学生的化学素 养。
加深理解和记忆
视觉化记忆
思维导图通过图形、颜色、线条 等元素将化学实验知识进行视觉 化呈现,有助于激发学生的视觉 记忆能力,加深对实验内容的印
象。
关联性思维
思维导图强调知识点之间的关联 性,可以帮助学生理解实验原理 、操作步骤等内容的内在联系,
形成更加深刻的记忆。
主动性思考
在绘制思维导图的过程中,学生 需要主动思考、归纳和总结实验 知识,这种主动性思考有助于加
思维导图在高三化学复习教学中的运用

思维导图是一种图形化的思维工具,可以帮助学生更好地理解、记忆和应用知识。
在高三化学复习教学中,思维导图可以用于帮助学生更好地理解和掌握化学知识。
在高三化学复习教学中,思维导图可以通过以下几种方式运用:
1.概括和归纳知识点: 思维导图可以帮助学生快速概括和归纳知识点,使学生能够更好地
理解和掌握知识。
2.帮助学生记忆知识:通过图形化的展示方式,思维导图可以帮助学生记忆知识,提高学
生记忆效率。
3.帮助学生分析和解决问题:思维导图可以帮助学生分析和解决问题,提高学生的分析和
解决问题的能力。
4.帮助学生总结知识:思维导图可以帮助学生总结知识,使学生能够更好地理解和掌握知
识。
药物化学复习思维导图

变
丙胺类(X=CH):氯苯那敏、溴苯那敏 三环类:赛庚啶、氯雷他定、地氯雷他定、异丙嗪、酮替芬
态 反
无嗜睡作用的H1受体拮抗剂
早期的:特非那定、咪唑斯汀、 无心脏毒性:氯雷他定、地氯雷他定、西替利嗪、羟嗪
应
过敏介质释放抑制剂:色甘酸钠
药 过敏反应的化学介质及其抑制剂 白三烯拮抗剂:孟鲁斯特、扎鲁司特
红霉素及其衍生物:红霉素A、阿奇霉素、泰利霉素
大环内酯类 麦迪霉素及其衍生物
螺旋霉素及其衍生物
其他类:氯霉素、盐酸林可霉素、磷霉素
MADE BY 张金泉 【版权所有 盗版必究】
苯二氮卓类:氯氮卓、地西泮、氟马西尼、艾司唑仑
镇 静
镇静催眠药
非苯二氮卓类
咪唑并吡啶类:酒石酸唑吡坦 吡咯酮类:佐匹克隆
催
药
苯氧乙酸类及其类似物:氯贝丁酯、吉非贝齐、双贝特、普罗布考
物
烟酸类:烟酸、阿昔莫司
血脂调节药 羟甲戊二酰CoA(HMG-CoA)还原酶抑制剂:洛伐他汀、辛伐他汀、氟伐他汀
不饱和脂肪酸(亚油酸) 其他 强碱性阴离子交换树脂(降胆宁)
抗氧化剂
MADE BY 张金泉 【版权所有 盗版必究】
咪唑类(第一代):西咪替丁、布立马胺
钠离子通道阻断剂 IB类:利多卡因
心
离子通道阻断剂
IC类:普罗帕酮、氟卡尼
钾离子通道阻断剂:胺碘酮、乙酰卡尼、索他洛尔
血 抗心律失常药
钙通道阻滞剂
管
β受体拮抗剂
系 统 药 抗心绞痛药 物
NO供体药物:硝酸甘油、单硝酸异山梨酯、吗多明
二氢吡啶类:硝苯地平、尼莫地平
选择性钙通道阻滞剂 芳烷基胺类:维拉帕米
吗啡喃类:左诺菲、布托啡诺
药物化学复习思维导图

心 血 管
抗高血压药
作用于离子通道的药物
钙拮抗剂 钾通道开放剂:米诺地尔、吡那地尔
影响肾上腺素能神经递质的药物:利舍平 作用于毛细小动脉的药物:地巴唑、长春胺
系
其他 中枢α2受体激动剂:可乐定、甲基多巴
统
肾上腺素能α1受体阻断剂:哌唑嗪、特拉唑嗪
钠离子通道阻断剂 IB类:利多卡因
心
离子通道阻断剂
IC类:普罗帕酮、氟卡尼
钾离子通道阻断剂:胺碘酮、乙酰卡尼、索他洛尔
血 抗心律失常药
钙通道阻滞剂
管
β受体拮抗剂
系 统 药 抗心绞痛药 物
NO供体药物:硝酸甘油、单硝酸异山梨酯、吗多明
二氢吡啶类:硝苯地平、尼莫地平
选择性钙通道阻滞剂 芳烷基胺类:维拉帕米
药 和
吡唑酮类:安乃近、安替比林
非
3,5-吡唑烷二酮类:羟布宗、保泰松
甾
芳基烷酸类:吲哚美辛、萘普生、芬不芬、布洛芬
体 非甾体抗炎药 N-芳基邻氨基苯甲酸类:甲芬那酸
抗
1,2-苯并噻嗪类:吡罗昔康
炎
COX-2选择性抑制剂:塞来昔布、罗非昔布
药
MADE BY 张金泉 【版权所有 盗版必究】
IA类:奎尼丁、奎宁、普鲁卡因胺
红霉素及其衍生物:红霉素A、阿奇霉素、泰利霉素
大环内酯类 麦迪霉素及其衍生物
螺旋霉素及其衍生物
其他类:氯霉素、盐酸林可霉素、磷霉素
MADE BY 张金泉 【版权所有 盗版必究】
苯二氮卓类:氯氮卓、地西泮、氟马西尼、艾司唑仑
镇 静
镇静催眠药
非苯二氮卓类
咪唑并吡啶类:酒石酸唑吡坦 吡咯酮类:佐匹克隆
初中化学第四单元自然界的水思维导图之欧阳术创编
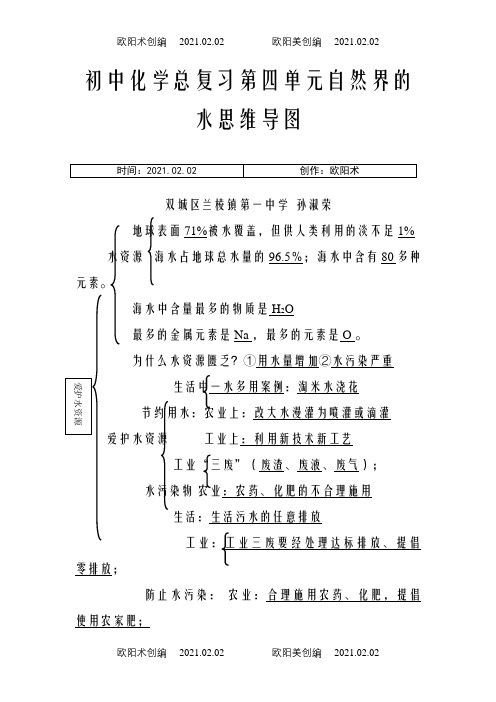
欧阳术创编 2021.02.02 欧阳美创编 2021.02.02 初中化学总复习第四单元自然界的水思维导图双城区兰棱镇第一中学 孙淑荣地球表面71%被水覆盖,但供人类利用的淡不足1% 水资源 海水占地球总水量的96.5%;海水中含有80多种元素。
海水中含量最多的物质是 H 2O最多的金属元素是Na ,最多的元素是 O 。
为什么水资源匮乏?①用水量增加②水污染严重 生活中一水多用案例:淘米水浇花节约用水:农业上:改大水漫灌为喷灌或滴灌 爱护水资源 工业上:利用新技术新工艺工业“三废”(废渣、废液、废气); 水污染物 农业:农药、化肥的不合理施用生活:生活污水的任意排放零排放;防止水污染: 农业:合理施用农药、化肥,提倡使用农家肥;爱护水资源欧阳术创编 2021.02.02 欧阳美创编 2021.02.02 生活:生活污水要集中处理达标排放、提倡零排放;效果由低到高的是 静置、吸附、过滤、蒸馏方法)其中净化效果最好的操作是蒸馏水的净化 净化方法 既有过滤作用又有吸附作用的净水剂是活性炭。
作用是:既能过滤又能吸附一些溶解性的杂质,出去臭味硬水与软水 A.定义 硬水是含有较多可溶性钙、镁化合物的水;软水是不含或含较少可溶性钙、镁化合物的水。
B .鉴别方法:取样加入用肥皂水,搅拌 。
有浮渣产生或泡沫较少的是硬水,泡沫较多的是软水C .硬水软化的方法:实验室:蒸馏 生活中:加热煮沸D .长期使用硬水的坏处:浪费肥皂,洗不干净衣服;锅炉容易结成水垢,不仅浪费燃料,使管道变形甚至引起锅炉爆炸。
A.装置―――水电解器 电源种类---直流电 电解水的实验欧阳术创编 2021.02.02 欧阳美创编 2021.02.02 B.加入硫酸钠或氢氧化钠的目的----增强水的导电性,加快水的电解速度C. 化学反应: 2H 2O通电 2H 2↑+ O 2↑ D. 产生位置 负极 正极体积比: 2 :1 (为什么体积比有时大于2:1氧气?)质量比: 1 : 8氧气比氢气更易溶于水,电极消耗氧气)E 水通电分解的微观实质是:水F 结论: ①水是由氢、氧元素组成的。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
防锈 措施
铁生锈
纯金属
保护金属 的有效途径
与氧气反应 化学性质
与盐酸、 稀硫酸反应 与盐溶液 反应
铝的耐腐蚀性 真金不怕火炼
的条件
金属活动性 顺序及其应用
金属资源的 利用与保护
金属和 金属材料
合金
原料
定义、常见铁合金——生铁和钢 合金与纯金属的性质比较 铁矿石、焦炭、石灰石 高温条件下,利用焦炭反应 生成的一氧化碳将铁从铁矿 石中还原出来
化学用语
化学式
单质 写法和读法 化合物 相对分子质量 相关计算
计算相对 分子质量
计算元素 质量比
计算元素的 质量分数
计算某 元素的质量
第五单元 化学方程式
应用 书写原则
内容
微观解释
原子的三不变 五个一定不变 两个一定改变 一个可能改变
质量守恒 定律
依 据
变与不变 定义 意义 读法
质的方面 量的方面
燃料
C+O2=CO2 CaO+H2O=Ca(OH)2 NaOH+HCl=NaCl+H2O Mg+2HCl=MgCl2+H2↑
点燃
氢气、酒精等 氢气的实验室制法
方法
破坏燃烧 常见灭火器 的条件 及适用范围 泡沫灭火器反应原理
清除可燃物 隔绝空气 降温至着火点以下
物理性质
颜色、状态、共性、个性等, 性质与用途的关系
(探究燃烧的条件 大本P56页)
条件
剧烈
可燃性气体点 燃前要验纯
煤的干馏 燃烧产物及危害 防治措施
高温 C+CO2=2CO 加热
爆炸
定义 燃烧
煤
化石燃料
(不可再生)
石油的分馏
CO+CuO=Cu+CO2
石油 天然气
新能源 物性,化性, 检验可燃物中 C,H的方法
吸热反应 放热反应
能量 变化
燃料 及其利用 灭火 原理
与指示剂作用 酸的通性 酸+活泼金属=盐+H2 酸+金属氧化物=盐+H2O + 酸中都含H 酸+碱=盐+H2O 酸+盐=新盐+新酸 与指示剂作用 碱+非金属氧化物=盐 +H2O 酸+碱=盐+H2O 碱+盐=新盐+新碱
常见的酸
定义 实质
H++OH-=H2O
酸
中和 反应
PH
碱的通性
应用
改变土壤酸碱 性,处理工厂 废水,医药 溶液酸碱性 与PH的关系 PH=7 溶液呈中性 PH<7 酸性,PH越小, 酸性越强 PH>7 碱性,PH越大, 碱性越强
碱
碱中都含OH-
常见的碱
测定溶液 的PH
Ca(OH)2
NaOH
课本P62, 实验10-9 俗名:熟石灰,消石灰 常用于检验CO2的存在 建筑,配制波尔多液
俗名:苛性钠, 火碱,烧碱 易潮解,可作干 燥剂,重要的化 工原料
现状 水资源 水污染原因 水的净化
水的电解 水的组成 氢气 实验结论 用途 可燃性 物理性质 化学性质
自然界的水
防治措施
还原性
第四单元 自然界的水
化合价
一般规律 应用
常见化合价 表示的意义 根据化学式求化合价 根据化合价写化学式
宏观
表示一种物质
微观
表示物质的一个分子 元素符号或 元素符号加小数字 根据化合价书写 三种以上含原子团
第三单元 物质构成的奥秘
分子 概念 组成
定义 性质 小、动、有间隔
构成
构成 原子
由分子构成 的物质
H2 O2、N2、Cl2 H2O、CO2 、HCl等
分类
定义
性质 小、动、有间隔
核外电子排布
分布
元素
物质
元素符号
元素 周期表
构成
结构
由原子构成 的物质
元素符号 表示的意义
离子
Fe Cu Mg 、 He Ne、 C S P等
粒子方面
已知反应物求生成物 含杂质的计算 涉及溶液的有关计算
书写步骤 配平方法
书写
化学方程式
相关计算
质量守恒定律
理论依据
计算步骤
设、方、关、比、算、答
常见类型
下列叙述不适合用质量守恒定律解释的是: AE A.水加热变成水蒸气,变化前后质量相等 B.要得到18g水,则参加反应的氢气和氧气的总质量 一定为18g C.1g硫与1g氧气化合生成2g二氧化硫 D.煤燃烧后剩余残渣的质量减轻了 E.一定条件下,CH4燃烧生成H2O 和 CO2 ,反应前 后分子总数不变 F.某有机物在空气中燃烧只生成CO2和H2O,则该有 机物一定含有碳、氢元素,可能含有氧元素
定义 分类
离子符号
由离子构成 的物质
NaCl、CuSO4 、NaOH 等
+ Na+ Mg2+ Al3+ H 常见离子 O2- F- Cl- S2- 等
第四单元 自然界的水
概念 吸附 过滤 沉淀 消毒 蒸馏 区分方法
加肥皂水
硬水的软化 煮沸或蒸馏 硬水的危害
现象 硬水和软水
正氧负氢 气体检验
净化方法
溶剂 组成
吸热 放热 溶解 现象
乳化
乳浊液和乳化现象
特征
温度和压强
饱和 溶液 分类 不饱和 溶液
定义
影响 因素 概念
溶液
气体 溶解度
定义、判断方法、 相互转化方法、 溶液的饱和不饱和 与浓稀的关系
反应后溶液 质量的计算
溶解度
固体 溶解度 影响 因素
溶液 的浓度
结晶 方法
溶质的 质量分数
相关计算
概念
溶解性 内因: 溶质和溶剂的性质 划分方法 外因:温度
溶解度 曲线
蒸发结晶 降温结晶
液体的 体积分数
75%的 酒精溶液
溶液的配制 固体配制
计算 量取 溶解
溶液稀释
计算 称量 溶解
表示的意义: 点、交点、线 相关应用:
挥发性 金属表面除锈,制 造药物,胃液主要 盐酸 成分,助消化
性质 用途
硫酸
吸水性,脱水性,溶于水 时放大量热。重要的化工 原料,可作干燥剂
与水反应 三个不能 物理性质 质软导电 润滑性 石墨 金刚石 无色透明 硬度大 与碱反应 化学性质 灭火制冷剂
性质
用途
原理
装置 收集
C60
常见 碳单质
二氧化碳
制法
验满
检验
用途
碳单质
一氧化碳
用途
性质
物理性质
常温 稳定性
可燃性
化学性质
性质
化学性质
可燃性
还原性
还原性
物理性质
作燃料冶金
毒性
可燃物,氧气,达到着火 点
金属的 存在形式
金银等——单质 大多数——化合物
铁的冶炼
反应原理
设备和产品 高炉——生铁 含杂质物质的
CO还原Fe2O3的 现象及注意事项 酒精灯迟到早退 尾气处理
必须将纯物质质量 化学方程式的计算 带入方程式计算
溶质和溶剂的判断 质量关系
均一性 稳定性 混合物
NH4NO3
NaOH、H2SO4等
溶质
