检验检测机构风险评估和控制2018
安全风险评估诊断分级应急(2018)19号

应急管理部关于印发危险化学品生产储存企业安全风险评估诊断分级指南(试行)的通知应急〔2018〕19号各省、自治区、直辖市及新疆生产建设兵团安全生产监督管理局,有关中央企业:为认真贯彻党的十九大精神,落实党中央、国务院决策部署,加快完善安全风险分级管控和隐患排查治理工作机制,提高监管针对性,提升监管效能,有效防范遏制重特大生产安全事故,根据《国务院安全生产委员会关于印发2018年工作要点的通知》(安委〔2018〕1号)部署,结合危险化学品生产储存企业(以下简称危险化学品企业)安全生产特点和近年来一系列危险化学品安全生产工作要求,重点考虑危险化学品企业的固有危险性,兼顾危险化学品企业对安全风险管控的现实情况,我部组织制定了《危险化学品生产储存企业安全风险评估诊断分级指南(试行)》(以下简称《指南》,见附件),现予以印发,请认真贯彻执行,并就有关事项通知如下:一、各地安全监管部门要高度重视危险化学品企业安全风险评估诊断工作,认真学习宣传《指南》,结合本地实际,进一步细化《指南》,并组织对辖区内危险化学品企业进行安全风险评估诊断分级,评估诊断采用百分制,根据评估诊断结果按照风险从高到低依次将辖区内危险化学品企业分为红色(60分以下)、橙色(60至75分以下)、黄色(75至90分以下)、蓝色(90分及以上)四个等级,对存在在役化工装置未经正规设计且未进行安全设计诊断等四种情形的企业可直接判定为红色;涉及环氧化合物、过氧化物、偶氮化合物、硝基化合物等自身具有爆炸性的化学品生产装置的企业必须由省级安全监管部门组织开展评估诊断;要按照分级结果,进一步完善危险化学品安全风险分布“一张图一张表”,落实安全风险分级管控和隐患排查治理工作机制。
危险化学品企业安全风险评估诊断分级实施动态管理,原则上每三年开展一次。
二、各地安全监管部门要根据分级情况,结合《国家安全监管总局关于进一步加强监管监察执法促进企业安全生产主体责任落实的意见》(安监总政法〔2018〕5号)要求,对诊断为红、橙、黄、蓝不同等级的危险化学品企业,采取针对性的监管措施,提高监管效能;要突出强化对红色及橙色等级危险化学品企业的监管,加大日常执法检查频次,依据《化工和危险化学品生产经营单位重大安全事故隐患判定标准(试行)》,依法严格处罚发现的事故隐患,加强危险化学品企业主要负责人安全生产培训考核;要督促各类危险化学品企业按照国家有关要求,采取有效措施,持续强化安全生产工作,不断提高本质安全水平和安全风险管控能力,有效降低安全风险,严防安全事故发生,坚决维护人民群众生命财产安全和社会稳定。
国家认监委关于发布2018年第一批认证认可行业标准的通知-国认科〔2018〕21号

国家认监委关于发布2018年第一批认证认可行业标准的通知正文:----------------------------------------------------------------------------------------------------------------------------------------------------国家认监委关于发布2018年第一批认证认可行业标准的通知国认科〔2018〕21号研究所、认可中心、认证认可协会,各相关认证机构、检验检测机构:经审查,现将《有机产品认证目录评估准则》等23项认证认可行业标准予以发布。
国家认监委2018年3月23日2018年第一批认证认可行业标准目录序号标准编号标准名称实施日期1RB/T164-2018有机产品认证目录评估准则2018-10-12RB/T165.1-2018有机产品产地环境适宜性评价技术规范第1部分:植物类产品2018-10-13RB/T165.2-2018有机产品产地环境适宜性评价技术规范第2部分:畜禽养殖2018-10-14RB/T165.3-2018有机产品产地环境适宜性评价技术规范第3部分:淡水水产养殖2018-10-15RB/T166-2018有机羊毛地毯认证技术规范2018-10-16RB/T167-2018有机葡萄酒加工技术规范2018-10-17RB/T168-2018有机液态乳加工技术规范2018-10-18RB/T169-2018有机产品(植物类)认证风险评估管理通用规范2018-10-19RB/T170-2018区域特色有机产品生产优势产地评价技术指南2018-10-110RB/T171-2018实验室测量审核结果评价指南2018-10-111RB/T172-2018实验动物机构标识系统要求2018-10-112RB/T173-2018实验动物人道终点评审指南2018-10-113RB/T174-2018司法鉴定/法庭科学机构能力认可专业要求2018-10-114RB/T175-2018生物质能可持续性认证要求2018-10-115RB/T220-2018检验检测机构资质认定能力评价信息安全检验检测机构要求2018-10-116RB/T251-2018钢铁企业温室气体排放核查技术规范2018-10-117RB/T252-2018化工企业温室气体排放核查技术规范2018-10-118RB/T253-2018电网企业温室气体排放核查技术规范2018-10-119RB/T254-2018发电企业温室气体排放核查技术规范2018-10-120RB/T255-2018电石企业温室气体排放核查技术规范2018-10-121RB/T256-2018合成氨企业温室气体排放核查技术规范2018-10-122RB/T257-2018甲醇企业温室气体排放核查技术规范2018-10-123RB/T258-2018乙烯企业温室气体排放核查技术规范2018-10-1——结束——。
检验检测机构的风险识别与评估

学术论坛/Academic Forum检验检测机构的风险识别与评估♦山西省阳泉市硅铝质耐火材料质量监督检验中心山西省耐火材料产品质量监督检验站李向威摘要:新形势下检验检测机构应有效识别内外部风险,并基于风险的思维对过程和管理体系进行管控,才能消除或减少非预期结果的风险。
本文着重分析了检验检测机构在检测过程中存在的各种风险,通过风险模型的方法对风险识别组织、风险识别过程、风险分级与整体风险评估作了重点阐述,以达到有效识别和评估风险的目的。
关键词:检验检测机构风险识别风险评估近年来,我国大力提倡“中国制造2025”以及高质量发展理念,人们对产品质量越来越重视,检验检测机构的科学性和准确性也备受关注。
对于检验检测机构来说,每一份检测报告就意味着一份风险。
在如何控制和降低检验检测机构风险,提高自身风险防范能力,成为所有检验检测机构面临和思考的问题。
2018年9月1日起实施的CNAS-CL01(ISO/IEC 17025:2017)《检测和校准实验室能力认可准则》中8.5应对风险和机遇的措施章节中也提出了明确的要求。
只有有效识别检验检测过程中的法律风险、质量责任风险、安全风险和环境风险等各类风险,并基于风险的思维对过程和管理体系进行管控,才能消除或减少非预期结果的风险。
通过对检验检测机构全程管理体系中所涉及公正性、质量等风险进行识别、评估、预防、控制,杜绝潜在风险或降低风险,并对识别出的机遇采取措施,达到管控风险的目的。
1风险识别组织1.1评估组织应对风险和机遇的措施应按计划开展,由质量负责人组织,一般每年至少一次全体参与的风险评估会议。
当出现以下情况时,应适当增加评估次数:a)与质量管理体系有关的法律、法规、标准及其他要求有变化时;b)组织机构、业务范围、资源配置发生重大调整时;c)发生重大质量事故或相关方投诉连续发生时;d)最高管理者认为有必要评审时;e)其他情况需要时。
1.2评估形式风险评估一般以会议讨论的形式幵展。
CNAS-RL02:2018《能力验证规则》

CNAS-RL02能力验证规则Rules for Proficiency Testing 中国合格评定国家认可委员会目录前言 (2)1 范围 (3)2 引用文件 (3)3 术语和定义 (3)4 对合格评定机构的要求 (4)5 对CNAS的要求 (7)6 其他说明 (7)附录A(资料性附录)能力验证活动适宜性核查表 (8)附录B(规范性附录)能力验证领域和频次表 (10)前言中国合格评定国家认可委员会(英文缩写:CNAS)将能力验证与现场评审作为CNAS对合格评定机构能力进行评价的两种主要方式,为了确保CNAS认可的有效性,保证CNAS认可质量,促进合格评定机构的能力建设,特制定本规则。
本规则规定了CNAS能力验证的政策和要求,包括对合格评定机构的要求和对CNAS的要求。
本规则内容为强制性要求。
本规则中的“注”是对条款的解释和说明。
本规则于2007年制订,2010年换版修订,2015年6月换版后第1次修订,2016年换版修订,本次修订主要是根据ISO/IEC 17011:2017《合格评定认可机构要求》标准的变化,对第4、5和6条款的内容进行了修改,同时,为方便合格评定机构使用,将CNAS AL07:2015《CNAS能力验证领域和频次表》作为本规则的附录B,本文件实施之日起,CNAS AL07:2015《CNAS能力验证领域和频次表》废止。
能力验证规则1 范围本规则适用于申请CNAS认可或已获准CNAS认可的合格评定机构,包括检测和校准实验室(含医学领域实验室)、标准物质/标准样品生产者以及检验机构(相关时)。
2 引用文件本文件引用了下列文件中的全部或部分条款。
所引用的文件不注明其发布日期,请各相关方注意使用这些文件的有效版本(包括其修订案)。
2.1 CNAS-R01《认可标识使用和认可状态声明规则》2.2 GB/T 27000《合格评定词汇和通用原则》(ISO/IEC 17000,IDT)2.3 ISO/IEC 17011《合格评定认可机构要求》2.4 ISO/IEC 17043《合格评定能力验证的通用要求》(GB/T 27043)2.5 APLAC MR001《建立和保持认可机构间APLAC互认协议的程序》2.6 ILAC-P9《ILAC对参加能力验证活动的政策》3 术语和定义GB/T 27000中的定义适用于本规则,同时,本规则还引用以下术语和定义:3.1 实验室间比对:按照预先规定的条件,由两个或多个实验室对相同或类似的物品进行测量或检测的组织、实施和评价。
CNAS-CL02-A003:2018《医学实验室质量和能力认可准则在临床化学检验领域的应用说明》

CNAS-CL02-A003:2018《医学实验室质量和能⼒认可准则在临床化学检验领域的应⽤说明》CNAS-CL02-A003医学实验室质量和能⼒认可准则在临床化学检验领域的应⽤说明Guidance on the Application of Accreditation Criteria for the Medical Laboratory Quality and Competence in the Field of Clinical Chemistry中国合格评定国家认可委员会前⾔本⽂件由中国合格评定国家认可委员会(CNAS)制定,是CNAS根据临床化学检验的特点,对CNAS-CL02:2012《医学实验室质量和能⼒认可准则》所作的进⼀步说明,并不增加或减少该准则的要求。
本⽂件与CNAS-CL02:2012《医学实验室质量和能⼒认可准则》同时使⽤。
在结构编排上,本⽂件章、节的条款号和条款名称均采⽤CNAS-CL02:2012中章、节条款号和名称,对CNAS-CL02:2012应⽤说明的具体内容在对应条款后给出。
本⽂件的附录A、B为规范性附录。
附录的序号及内容与CNAS-CL02:2012不对应。
本⽂件代替:CNAS-CL38:2012。
本次为换版修订,相对于CNAS-CL38:2012,本次换版仅涉及⽂件编号改变。
医学实验室质量和能⼒认可准则在临床化学检验领域的应⽤说明1 范围本⽂件规定了CNAS对医学实验室临床化学检验领域的认可要求。
适⽤时,医学实验室临床免疫学定量检验领域的认可,应符合本⽂件要求。
2 规范性引⽤⽂件下列⽂件对于本⽂件的应⽤是必不可少的。
凡是注⽇期的引⽤⽂件仅注⽇期的版本适⽤于本⽂件。
凡是不注⽇期的引⽤⽂件,其最新版本(包括修改单)适⽤于本⽂件。
GB/T 20468-2006 临床实验室定量测定室内质量控制指南WS/T 407-2012 医疗机构内定量检验结果的可⽐性验证指南CNAS-RL02 能⼒验证规则3 术语和定义4 管理要求4.1 组织和管理责任4.1.1.2医学实验室为独⽴法⼈单位的,应有医疗机构执业许可证;实验室为⾮独⽴法⼈单位的,其所属医疗机构的执业许可证书的诊疗科⽬中应有医学实验室;⾃获准执业之⽇起,实验室开展医学检验⼯作⾄少2年。
RBT214_2018年检验检测机构资质认定能力评价检验检测机构通用要求内容

4.1机构4.1.1检验检测机构应是依法成立并能够承担相应法律责任的法人或者其他组织。
检验检测机构或者其所在的组织应有明确的法律地位ie,对其出具的检验检测数据、结果负责,并承担相应法律责任。
不具备独立法人资格的检验检测机构应经所在法人单位授权。
4.1.2检验检测机构应明确其组织结构及管理、技术运作和支持服务之间的关系。
4.1.3检验检测机构及其人员从事检验检测活动,应遵循国家相关法律法规的规定,遵循客观独立、公平公正、诚实信用原则,恪守职业道德,承担社会责任。
4.1.4检验检测机构应建立和保持维护其公正和诚信的程序。
检验检测机构及其人员应不受来自内外部的、不正当的商业、财务和其他方面的压力和影响,确保检验检测数据、结果的真实、客观、准确和可追溯。
检验检测机构应建立识别出现公正性风险的长效机制。
如识别出公正性风险,检验检测机构应能证明消除或减少该风险。
若检验检测机构所在的组织还从事检验检测以外的活动,应识别并采取措施避免潜在的利益冲突。
检验检测机构不得使用同时在两个及以上检验检测机构从业的人员。
4.1.5检验检测机构应建立和保持保护客户秘密和所有权的程序,该程序应包括保护电子存储和传输结果信息的要求。
检验检测机构及其人员应对其在检验检测活动中所知悉的国家秘密、商业秘密和技术秘密负有保密义务,并制定和实施相应的保密措施。
4.2人员4.2.1检验检测机构应建立和保持人员管理程序,对人员资格确认、任用、授权、和能力保持等进行规范管理。
检验检测机构应与其人员建立劳动、聘用或录用关系,明确技术人员和管理人员的岗位职责、任职要求和工作关系,使其满足岗位要求并具有所需的权力和资源,履行建立、实施、保持和持续改进管理体系的职责。
检验检测机构中所有可能影响检验检测活动的人员,无论是内部人员还是外部人员,均应行为公正,受到监督,胜任工作,并按照管理体系要求履行职责。
4.2.2检验检测机构应确定全权负责的管理层,管理层应履行其对管理体系的领导作用和承诺:a)对公正性做出承诺;b)负责管理体系的建立和有效运行;c)确保管理体系所需的资源;d)确保制定质量方针和质量目标e)确保管理体系要求融入检验检测的全过程f)组织管理体系的管理评审g)确保管理体系实现其预期结果h)满足相关法律法规要求和客户要求i)提升客户满意度j)运用过程方法建立管理体系和分析风险、机遇4.2.3检验检测机构的技术负责人应具有中级及以上专业技术职称或同等能力,全面负责技术运作;质量负责人应确保管理体系得到实施和保持;应指定关键管理人员的代理人。
CNAS-CL01:2018《检测和校准实验室能力认可准则》

CNAS-CL01检测和校准实验室能力认可准则(ISO/IEC 17025:2017)Accreditation criteria for the competence of testing and calibration laboratories中国合格评定国家认可委员会目录前言 (3)1 范围 (4)2 规范性引用文件 (4)3 术语和定义 (4)4 通用要求 (6)4.1 公正性 (6)4.2 保密性 (7)5 结构要求 (7)6 资源要求 (8)6.1 总则 (8)6.2 人员 (8)6.3 设施和环境条件 (9)6.4 设备 (9)6.5 计量溯源性 (11)6.6 外部提供的产品和服务 (11)7 过程要求 (12)7.1 要求、标书和合同评审 (12)7.2 方法的选择、验证和确认 (13)7.3 抽样 (15)7.4 检测或校准物品的处置 (16)7.5 技术记录 (16)7.6 测量不确定度的评定 (16)7.7 确保结果有效性 (17)7.8 报告结果 (18)7.9 投诉 (21)7.10 不符合工作 (22)7.11 数据控制和信息管理 (22)8 管理体系要求 (23)8.1 方式 (23)8.2 管理体系文件(方式A) (24)8.3 管理体系文件的控制(方式A) (24)8.4 记录控制(方式A) (25)8.5 应对风险和机遇的措施(方式A) (25)8.6 改进(方式A) (25)8.7 纠正措施(方式A) (26)8.8 内部审核 (方式 A) (26)8.9 管理评审(方式 A) (27)附录A(资料性附录)计量溯源性 (29)A.1 总则 (29)A.2 建立计量溯源性 (29)A.3 证明计量溯源性 (29)附录 B(资料性附录)管理体系方式 (31)参考文献 (33)前言本准则等同采用ISO/IEC 17025:2017《检测和校准实验室能力的通用要求》。
医院感染预防与控制评价规范 (2018版)

• 其结果对医院感染预防及控制决策提供支 持作用。
2 .目标性监测要求
•1 )应有针对医院感染重点部门、重点人群与高 风险因素的监测计划与控制措施,并落实。 • 2 )有对呼吸机相关性肺炎、 血管导管相关血流 • 感染、导尿管相关尿路感染、 手术部位感染等主 要部位感染和多重耐药菌感染的监测。 • 3 )对目标性监测工作有定期(至少每季度)检 • 查、自查,对监测资料有定期(至少每季度)总 结、分析与反馈,能体现持续质量改进。
(三)医院感染管理部门职责与落实
1 .有年度工作总结与计划,工作计划有效 落实。 2 .开展的工作内容符合《医院感染管理办 法》的要求和医院工作的需要。 3 .专职人员每年参加医院感染管理及相关 学科知识医院感染管理职责与落实
1 .医务科的医院感染管理职责与落实, 包括以下内容:
• 5 )相关人员对医院感染暴发报告流程和 处 置预案知晓率达100%。
• 6 )有对存在问题所采取的改进措施和成 效 进行追踪。
•7 )医院感染暴发的调查与控制,遵循WS/T • 524的要求。
WS/T 524 医院感染暴发控制指南
院感暴发
•什么是院感暴发:院感暴发是指在医疗机 构或其科室的患者中,短时间内发生3例以 上同种同源感染病例的现象。
一、术语和定义
下列术语和定义适用于本文件
1.个案追踪
医院现场评价所使用的一种方法,即采用真实患者分析 医院所提供治疗、护理和服务的过程,以评估各学科、科 室、项目服务之间相互关系,以及他们所提供的治疗和服 务中的重要功能,旨在追踪某一患者在医院接受诊疗服务 的全过程。
中华人民共和国食品安全法(2018年修正)

中华人民共和国食品安全法(2018年修正)文章属性•【制定机关】全国人大常委会•【公布日期】2018.12.29•【文号】中华人民共和国主席令第二十二号•【施行日期】2018.12.29•【效力等级】法律•【时效性】已被修改•【主题分类】食品安全正文中华人民共和国食品安全法(2009年2月28日第十一届全国人民代表大会常务委员会第七次会议通过2015年4月24日第十二届全国人民代表大会常务委员会第十四次会议修订根据2018年12月29日第十三届全国人民代表大会常务委员会第七次会议《关于修改〈中华人民共和国产品质量法〉等五部法律的决定》修正)目录第一章总则第二章食品安全风险监测和评估第三章食品安全标准第四章食品生产经营第一节一般规定第二节生产经营过程控制第三节标签、说明书和广告第四节特殊食品第五章食品检验第六章食品进出口第七章食品安全事故处置第八章监督管理第九章法律责任第十章附则第一章总则第一条为了保证食品安全,保障公众身体健康和生命安全,制定本法。
第二条在中华人民共和国境内从事下列活动,应当遵守本法:(一)食品生产和加工(以下称食品生产),食品销售和餐饮服务(以下称食品经营);(二)食品添加剂的生产经营;(三)用于食品的包装材料、容器、洗涤剂、消毒剂和用于食品生产经营的工具、设备(以下称食品相关产品)的生产经营;(四)食品生产经营者使用食品添加剂、食品相关产品;(五)食品的贮存和运输;(六)对食品、食品添加剂、食品相关产品的安全管理。
供食用的源于农业的初级产品(以下称食用农产品)的质量安全管理,遵守《中华人民共和国农产品质量安全法》的规定。
但是,食用农产品的市场销售、有关质量安全标准的制定、有关安全信息的公XXX本法对农业投入品作出规定的,应当遵守本法的规定。
第三条食品安全工作实行预防为主、风险管理、全程控制、社会共治,建立科学、严格的监督管理制度。
第四条食品生产经营者对其生产经营食品的安全负责。
浅析检验检测机构的风险识别与控制

浅析检验检测机构的风险识别与控制摘要:本文从检验检测机构风险识别、风险控制两个方面进行分析与描述,并提出相应措施,提高检验检测机构风险预知及控制能力,进而发展壮大检验检测机构。
关键词:检验机构风险识别风险控制建议Abstract: This article analyzes and describes the risk causes and risk control of inspection and testing institutions, and proposes corresponding measures to improve the risk prediction and control capabilities of inspection and testing institutions, and then develop and strengthen inspection and testing institutions.前言《检验检测机构资质认定管理办法》[1]和RB/T 214—2017 《检验检测机构资质认定能力评价检验检测机构通用要求》[2]中对检验检测机构应考虑与检验检测活动有关的风险和机遇均有明确的要求,因此做好风险分析和有效控制显得尤为重要,本文将对检验检测机构风险识别与控制进行重点分析,确保质量管理体系持续高效有序运行。
1 风险识别检验检测机构风险分为四个方面,分别包括法律体系风险,如检验检测人员体系内容宣贯不彻底、培训不到位;质量责任风险,如合同评审、样品处置、仪器设备、试剂耗材、人员、方法、环境、报告、数据等;安全风险,如公正性、保密性、物理化学性危险;环境风险,一般指所在环境超出或不满足检验条件,影响检测结果的风险,或者一些物理、化学等因素所引入的风险。
针对上述风险,检验检测机构相关人员可以通过分析、预判这些风险因素,同时将所发现的风险及时向上级领导汇报,制定相应措施和解决方案。
CNAS-CL01:2018《检测和校准实验室能力认可准则

CNAS-CL01检测和校准实验室能力认可准则(ISO/IEC 17025:2017)Accreditation criteria for the competence of testing and calibration laboratories中国合格评定国家认可委员会CNAS-CL01:2018 第1 页共34 页目录前言 (3)1 范围 (4)2 规范性引用文件 (4)3 术语和定义 (4)4 通用要求 (6)4.1 公正性 (6)4.2 保密性 (7)5 结构要求 (7)6 资源要求 (8)6.1 总则 (8)6.2 人员 (8)6.3 设施和环境条件 (9)6.4 设备 (9)6.5 计量溯源性 (11)6.6 外部提供的产品和服务 (11)7 过程要求 (12)7.1 要求、标书和合同评审 (12)7.2 方法的选择、验证和确认 (13)7.3 抽样 (15)7.4 检测或校准物品的处置 (16)7.5 技术记录 (16)7.6 测量不确定度的评定 (16)7.7 确保结果有效性 (17)7.8 报告结果 (18)7.9 投诉 (21)7.10 不符合工作 (22)7.11 数据控制和信息管理 (22)8 管理体系要求 (23)8.1 方式 (23)8.2 管理体系文件(方式A) (24)8.3 管理体系文件的控制(方式A) (24)8.4 记录控制(方式A) (25)CNAS-CL01:2018 第2 页共34 页8.5 应对风险和机遇的措施(方式A) (25)8.6 改进(方式A) (25)8.7 纠正措施(方式A) (26)8.8 内部审核 (方式 A) (26)8.9 管理评审(方式 A) (27)附录A(资料性附录)计量溯源性 (29)A.1 总则 (29)A.2 建立计量溯源性 (29)A.3 证明计量溯源性 (29)附录B(资料性附录)管理体系方式 (31)参考文献 (33)前言本准则等同采用ISO/IEC 17025:2017《检测和校准实验室能力的通用要求》。
ISO27000:2018 术语和定义(中文)

1.访问控制确保根据业务和安全要求(56)对资产的访问进行授权和限制的方法。
2.攻击试图破坏、暴露、更改、禁用、窃取或获得未经授权的访问或使用资产。
3.审计为获取审计证据并客观地对其进行评价,以确定满足审计准则的程度而形成的系统的、独立的和文件化的过程(54)。
4.审计范围审计(3)程度和边界。
5.认证保证实体所声称的特征是正确的。
6.真实性一个实体是它所声称的性质。
7.可用性按授权实体的要求可访问和使用的特性。
8.基本指标量根据属性定义的指标量(42)及其量化的方法。
9.能力运用知识和技能达到预期结果的能力。
10.保密性信息不能向未经授权的个人、实体或过程(54)提供或披露的特性。
11.符合性满足要求(56)。
12.后果影响目标(49)的事件(21)的结果。
注1:一个事件可以导致一系列的后果。
注2:结果可以是确定的,也可以是不确定的,在信息安全的环境中,通常是负面的。
注3:结果可以定性或定量地表示。
注4:最初的后果可能会通过连锁反应逐步升级。
13.持续改进重复活动以提高绩效(52)。
14.控制修正风险(61)的措施。
注1:控制包括任何修正风险(61)的过程(54)、方针(53)、设备、做法或其他措施。
注2:有可能控制并不总是发挥预期的或假定的修正效果。
15.控制目标通过实施控制(14)将得到什么结果的声明描述。
16.纠正消除发现的不符合(47)的行动。
17.纠正措施采取措施消除不符合(47)的原因,防止不符合的再次发生。
18.派生测量定义为两个或多个基本测量(8)值的函数的指标量(42)。
19.文件化的信息需要由组织(50)控制和维护的信息及其所包含的媒介。
注1:文件化的信息可以是任何格式、媒体和任何来源。
注2:文件化的信息可能涉及:●管理体系(41),包括相关过程(54);●为组织(50)运行而创建的信息(文件化);●取得成果的证据(记录)。
20.有效性计划的活动得以实现和计划的结果得以实现的程度。
CNAS-CI01-G001:2018《检验机构能力认可准则的应用说明》

CNAS-CI01-G001检验机构能力认可准则的应用说明(ILAC P15:06/2014)Application of Accreditation Criteria for the Competence of Inspection Bodies中国合格评定国家认可委员会引言本文件为检验机构认可提供了CNAS—CI01:2012(ISO/IEC 17020:2012)《检验能力机构认可准则》的应用说明。
认可机构可使用本文件对检验机构进行认可评审。
检验机构也可通过使用本文件对自身的运作进行管理,从而满足认可要求。
为了便于参照,每个应用说明都用CNAS-CI01(ISO/IEC 17020)对应的条款号加上后缀来标注。
例如4.1.4a是标准第4.1.4条款的第一个应用说明。
术语“应”在本文件中表示相应的条款是强制性的。
这些条款表明了CNAS-CI01(ISO/IEC 17020)的要求,或有些情况下表明了对认可机构的运作要求。
术语“宜”在本文件中表示相应的条款尽管不是强制性的,却是CNAS用来确认满足要求的方法/途径。
术语“可”表示允许。
术语“能”表示可能或能力。
如果检验机构的制度没有遵循本CNAS文件中与“宜”相关条款的规定,只有能够向认可机构证明他们的解决方案等效或更好地满足CNAS-CI01(ISO/IEC 17020)相关条款的要求, 检验机构才有资格获得认可。
个别的检验方案可指定附加认可要求。
本文件并不想识别这类要求或确认如何予以实施。
使用CNAS-CI01(ISO/IEC 17020)和本应用文件时,CNAS既不宜增加也不宜减少CNAS-CI01(ISO/IEC 17020)的要求。
本文件代替:CNAS-CI02:2015。
本次为换版修订,相对于CNAS-CI02:2015,本次换版仅涉及文件编号改变。
检验机构能力认可准则的应用说明3 术语和定义3.1a 术语“安装”可定义为“对一批元件进行组装,以实现单个元件所不能实现的功能的活动”。
检测科学实验室的生物安全风险评定

检测科学实验室的生物安全风险评定介绍本文档旨在提供一份检测科学实验室的生物安全风险评定。
生物安全风险评定是确保实验室操作过程中生物材料的安全性和防范潜在危险的重要步骤。
通过评估实验室的生物安全风险,可以采取适当的措施来保护实验人员和环境免受潜在的生物危害。
方法以下是进行检测科学实验室生物安全风险评定的主要步骤:1. 识别潜在的生物危害:评估实验室中可能存在的生物危害,包括病原体、有害微生物、致病性细菌等。
通过检查实验室的操作流程和使用的生物材料,确定可能存在的生物危害。
2. 评估生物危害的潜在影响:评估生物危害对实验室人员和环境的潜在影响。
考虑到实验室操作的性质和规模,确定潜在的风险等级。
3. 确定适当的风险控制措施:根据评估结果,确定适当的风险控制措施来减轻生物危害。
这可能包括实施生物安全级别(BSL)措施、使用个人防护装备、采取生物安全操作规程等。
4. 制定应急响应计划:制定应急响应计划,以应对潜在的生物事故或泄漏。
确保实验室人员了解应急程序,并提供适当的培训和装备。
5. 定期评估和更新:定期评估实验室的生物安全风险,并根据需要更新风险评估和控制措施。
随着实验室操作的发展和新的生物危害的出现,保持风险评估的及时性和准确性。
结论通过进行检测科学实验室的生物安全风险评定,可以确保实验室操作的安全性,保护实验人员和环境免受潜在的生物危害。
在评估风险和制定适当的控制措施的基础上,实验室可以采取有效的措施来减轻生物危害的风险,并应对潜在的生物事故。
定期评估和更新风险评估是保持实验室安全的关键,以适应不断变化的实验室操作和新的生物危害。
质量风险管理规程2018

质量风险管理标准管理程序目的:建立公司内质量风险管理程序,规范产品生命周期中质量风险的评估、控制与审核操作行为,降低产品的质量风险。
范围:用于公司所有产品的质量风险评估、控制与审核管理。
职责:质量部负责组织进行质量风险评估、控制与审核协调、管理等相关事宜,各职能部门负责配合本制度的实施。
程序:1.1定义:质量风险:是一个系统化的过程,是对产品在整个生命周期过程中,对风险的识别、衡量、控制以及评价的过程。
质量风险管理:是对药品整个生命周期进行质量风险的识别、评估、控制、沟通、回顾的系统过程,运用时可采用前瞻或回顾的方式。
产品生命周期:产品从开始研发经上市直至产品废止的所有阶段.2.质量风险管理程序质量风险管理的程序主要为以下阶段:风险识别;(二)风险分析;(三)风险评估;(四)风险控制;(五)风险沟通;风险审核;(七)风险回顾.2.1.风险识别风险识别是风险管理过程的第一步,为质量风险管理程序中后续步骤提供了基础。
风险识别是指系统地利用各种信息和经验,确认人员、仪器设备、工艺、分析方法、物料、厂房和公用系统等影响因素中存在的风险。
这里所说的信息,包括历史数据,理论分析,成型的意见,以及影响决策的一些利害关系等。
通常需要考虑的风险包括:对患者的风险;产品不符合标准要求的风险;法规不符合的风险等.在此阶段还应确定风险管理小组人员组成及职责。
2.2.风险分析分析已经识别的风险,进而确定风险发生的可能性、危害的严重性及其可测量性,对其进行深入的描述。
风险发生的可能性是指风险发生的概率,危害的严重性是指风险可能导致的后果,可测量性是指风险能否及时发现。
在进行风险分析时,需要针对不同的风险项目,选择不同的分析工具。
2.3.风险评估在进行风险评估时,需要针对不同的风险项目,选择不同的分析工具。
根据确定的风险标准,对已经识别并分析的风险进行评价,即通过评价风险的严重性和可能性从而确认风险的等级,以便于最后做出是否对该风险采取措施的决定。
《危险性较大的分部分项工程安全管理规定》住建部令﹝2018...

《危险性较大的分部分项工程安全管理规定》住建部令﹝2018...【文档模板范本】危险性较大的分部分项工程安全管理规定住建部令﹝2018﹞第号第一章总则第一条为了保障危险性较大的分部分项工程(以下简称“本工程”)建设安全,防止和减少安全事故的发生,根据《中华人民共和国建筑法》等有关法律法规,制定本规定。
第二条本规定适用于所有的本工程建设单位、设计单位、施工单位、监理单位、检验检测单位等相关单位和个人。
第三条本规定所称危险性较大的工程,是指可能对人民群众的生命财产安全产生严重威胁或者安全管理难度较大的工程,包括但不限于民用建筑、公共建筑、工业建筑、交通工程、水利工程、矿山工程、高压设备工程、特种设备工程等。
第四条本规定的通用术语和定义参照《建设工程质量管理及安全生产条例》(中华人民共和国住房和城乡建设部令第101 号)。
第二章安全管理第五条本工程建设单位应当切实做好本工程的安全生产工作,建立本工程安全生产管理体系,明确安全生产管理职责,制定安全生产管理制度和操作规程,加强安全监管、安全教育及培训等工作。
第六条本工程施工单位应当从事本工程施工的人员必须符合国家法律法规及有关规定的条件,如取得所需的证书、执照等。
施工单位还应当制定本工程施工安全生产组织设计,实施责任制,强化安全管理,确保施工现场安全。
第七条本工程监理单位应当对施工单位的安全生产管理进行监督检查,发现存在问题或者发现违反法律法规的情况要及时上报相关部门,防止事故发生。
第八条本工程检验检测单位应当依据有关标准、规范和技术要求,对本工程的建设过程和建设结果进行检测和鉴定,并出具检测和鉴定报告。
检验检测单位应按有关法律法规和规定,对检测、鉴定结果负责。
第九条本工程进入使用后,建设单位应当进行安全评估和风险管控,确保本工程运营期间不会对人民群众的生命财产安全造成威胁。
第十条为了确保危险性较大的工程安全生产正常进行,本工程建设单位、设计单位、施工单位、监理单位、检验检测单位等单位和个人应当严格遵守国家法律法规和有关规定,不得违反国家安全生产标准和规范。
中国银行保险监督管理委员会关于印发银行业金融机构数据治理指引的通知-银保监发〔2018〕22号

中国银行保险监督管理委员会关于印发银行业金融机构数据治理指引的通知正文:----------------------------------------------------------------------------------------------------------------------------------------------------中国银行保险监督管理委员会关于印发银行业金融机构数据治理指引的通知银保监发〔2018〕22号各银监局,机关各部门,各政策性银行、大型银行、股份制银行,邮储银行,外资银行,金融资产管理公司,其他会管金融机构:现将《银行业金融机构数据治理指引》印发给你们,请遵照执行。
2018年5月21日银行业金融机构数据治理指引第一章总则第一条为指导银行业金融机构加强数据治理,提高数据质量,发挥数据价值,提升经营管理能力,根据《中华人民共和国银行业监督管理法》等法律法规,制定本指引。
第二条本指引适用于中华人民共和国境内经银行业监督管理机构批准设立的银行业金融机构。
本指引所称银行业金融机构,是指在中华人民共和国境内设立的商业银行、农村信用合作社等吸收公众存款的金融机构、政策性银行以及国家开发银行。
第三条数据治理是指银行业金融机构通过建立组织架构,明确董事会、监事会、高级管理层及内设部门等职责要求,制定和实施系统化的制度、流程和方法,确保数据统一管理、高效运行,并在经营管理中充分发挥价值的动态过程。
第四条银行业金融机构应当将数据治理纳入公司治理范畴,建立自上而下、协调一致的数据治理体系。
第五条银行业金融机构数据治理应当遵循以下基本原则:(一)全覆盖原则。
数据治理应当覆盖数据的全生命周期,覆盖业务经营、风险管理和内部控制流程中的全部数据,覆盖内部数据和外部数据,覆盖监管数据,覆盖所有分支机构和附属机构。
(二)匹配性原则。
数据治理应当与管理模式、业务规模、风险状况等相适应,并根据情况变化进行调整。
CNAS-CL01-2018实验室风险和机遇识别分析评估及控制措施表【实验室风险评估】
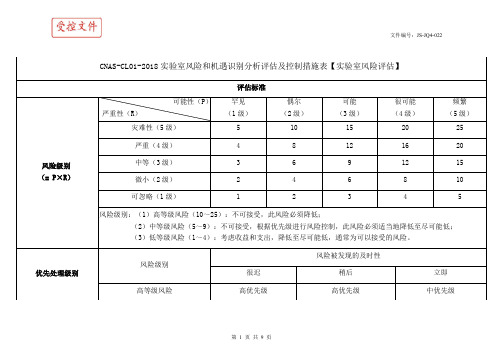
严重(4 级)
4
8
12
16
20
中等(3 级)
3
6
9
12
15
微小(2 级)
2
4
6
8
10
可忽略(1 级)
1
2
3
4
5
风险级别:(1)高等级风险(10~25):不可接受,此风险必须降低; (2)中等级风险(5~9):不可接受,根据优先级进行风险控制,此风险必须适当地降低至尽可能低; (3)低等级风险(1~4):考虑收益和支出,降低至尽可能低,通常为可以接受的风险。
确性
期内。
验证状态。
第4页共9页
文件编号:JS-JQ4-022
仪器未定期
计量器具、仪器每年经计量局检定,同时定
仪器
检定或校准, 计量器具、仪器未经检
定期检定和校准
3
4
1 12 低 期进行内部校准,始终保持其处于合格状
校准
造成检验结 定或定期校准。
态。
果不准确
试剂试 液管理
定期配制
试剂从可靠的供应商处购买。
文件编号:JS-JQ4-022
风险级别 (= P×R)
优先处理级别
CNAS-CL01-2018 实验室风险和机遇识别分析评估及控制措施表【实验室风险评估】
严重性(R)
可能性(P)
灾难性(5 级)
评估标准 罕见 (1 级)
5
偶尔 (2 级)
10
可能 (3 级)
15
很可能 (4 级)
20
频繁 (5 级)
低优先级
低等级风险
中优先级
低优先级
低优先级
可接受、不可接受
检验检测机构的风险识别与控制

ቤተ መጻሕፍቲ ባይዱ
检验检测机构的风险识别与控制
□ 李俊伟 鞠福龙 宋桂玲 王玉芝 黑龙江省质量监督检测研究院
摘 要:伴随着时代的发展和社会的进步,社会上出现了一些检验和检测机构,相关工作人员可以凭借自身的专业知识, 对风险进行准确的评估和有效的控制。鉴于此,本文将以绕检验检测机构的风险识别与控制为主线,进行简要的分析和描述。
关键词:检测机构;风险识别;风险控制
从 目 前 的 情 况 来 看, 当 前 几 乎 所 有的检测机构对于风险的识别和控制 工作重视程度不足,普遍将主要的工 作精力放在检测工作方面。但是对于 检验和检测机构自身而言,保证人员 健康和环境安全是做好检测工作的重 要基础和前提,只有打下坚实稳固的 基础,才能够保证日常的工作,全面 实现可持续发展 [1]。正因为如此,加 大检验检测机构的风险管理工作力度, 做好准确的风险分析和有效的控制显 得尤为重要,下文将针对检验检测机 构的风险识别和控制展开一系列讨论。
4 风险的控制
检验检测机构相关管理人员应该采 取有效的风险预防措施,最大程度避免 风险的出现和发展,同时也需要做好相 应的控制工作。具体工作内容如下。 4.1 做好质量风险的防控工作
在 进 行 检 测 工 作 之 前, 需 要 对 合 同内容进行仔细的评审,抽取具有代 表性的样品,保证相关材料的完整性 与详细性,由专门的工作人员负责保 存。在此同时,需要对信息的保险制 度和沟通进行严格的控制。在进行检 测的过程当中,要求所有的工作人员 都能够持证上岗,所使用的相关仪器 和设备都能够保证处于正常的运行状 态,将所有的操作进行记录,严格按 照相关的标准规范来执行。所有的检 测过程都需要质量管理人员全程跟进, 并做好人员的保护措施。在完成检测
2018检验科生物安全风险评估报告总结

2017年XX医院检验科生物安全风险评估总结依据《病原微生物实验室生物安全管理条例》、《实验室生物安全通用要求》、《微生物和生物医学实验室生物安全通用准则》、《医疗废物管理条例》,2017年上半年对检验科生物安全作风险评估,形成报告如下:一、生物因子已知或未知的特性评估我院检验科属于二级生物安全实验室,主要接触三类病原微生物,在临床工作中,必须强调高致病性病原微生物的检测,发现可疑高致病病原微生物,必须采取积极措施,及时报告。
1.病原:结核分枝杆菌、霍乱弧菌等;2.防控措施:2.1 立即对可疑高致病病原微生物培养物封存。
2.2 立即报告医院感染科、卫生局和市疾病预防控制中心。
2.3 对实验室进行全面消毒。
2.4 接触人员更换个人防护用品,并对用品进行消毒。
2.5 感控科收集病人相关信息资料,对病人实施隔离,协助市疾病预防控制中心进行流行病学调查。
2.6. 对接触者进行严密的健康监护。
二、实验室设施、设备等相关的风险评估:1.漏水风险:空调设备偶有漏水现象,生化仪器出现过积水,可能影响仪器运行的湿度,导致仪器故障;防控措施:常年配备接水容器,并及时联系相关人员进行检修盒维护,以消除隐患。
2.漏气风险:酒精检测试剂包含高危化学气体,需进行一定的隔离和监测防控措施:配备带锁气体安全柜及检测设备,严格按照《危化品实施管理方案》使用并做好登记。
3.虫害风险:实验室出现过一条类似蜈蚣样生物,可能对人员造成伤害;防控措施:注意观察,防止被虫害伤到,定期进行打扫、消毒。
三、实验室常规活动和非常规活动过程中的风险评估1.风险评估:实验室布局为清洁区、半污染区和污染区,实验室进出人员可能存在污染和感染的风险。
具体可能体现在:病原微生物的带入和带出,标本的污染,意外事件的发生(如跌倒、划伤等)2.防控措施:2.1本科室工作人员:进入实验室的本科工作人员,在缓冲间内穿戴好工作服、工作帽、手套等个人防护用具后方能进行实验室工作,任何原因需要离开实验室,必须洗手(七步法),脱去个人防护用品,方能离开实验室。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
1.目的
为了能够在检测工作中持续进行风险识别、风险评估和实施必要地控制措施。
2.适用范围
适用于本中心检测工作中所涉及的风险评估和风险控制领域。
3.职责
3.1 各岗位人员负责识别在检测工作中可能存在的各类风险以及风险预防和控制措施的实施;
3.2 检测业务办公室主任负责组织识别出风险的分析;
3.3 质量主管负责风险的评估和采取何种预防和控制措施
3.4最高管理者负责批准风险预防和控制的措施;
3.5 各部门负责人负责风险的监控和预防控制措施的跟踪验证。
4.工作程序
4.1风险的识别
4.1.1在整个的检测过程中可能存在的风险
4.1.1.1检测前:
a)合同评审的风险,例如:检测方法不适用与检测样品
b)样品风险,例如:检测样品信息与检测委托单不符的风险。
c)信息保密风险,例如:在与客户沟通时泄露其它客户检测过程中提供的样品、文件及传递过程中的信息
d)沟通风险,例如:未能将客户的检测需求有效地传递给相关人员风险。
4.1.1.2检测中:
a)人员风险,例如:检测人员资质不足;
b)仪器设备风险,例如:仪器设备未定期校准或核查;
c)试剂耗材风险,例如:使用无证标准物质;
d)检测方法风险,例如:未识别样品基质对检测方法带来的干扰;
e)安全风险,例如生物安全、化学安全、辐射安全等方面的风险
4.1.1.3检测后:
a)样品存储和处理的风险,例如:样品丢失;
b)数据结果风险,例如:人为更改或伪造检测结果;
c)报告风险,例如:检测报告未审核签字;
d)信息安全和保密风险,例如:客户信息、报告和数据信息泄露。
4.1.2各岗位人员都有责任和义务发现和识别整个体系运行过程中可能存在的风险,并告知检测业务办公室主任。
4.2风险的分析
4.2.1检测业务办公室主任在接到可能存在的风险情况后,立刻汇同相关部门和人员对识别出来的风险进行分析。
4.2.2分析如果风险发生,可能造成的影响情况:
1)检测数据错误
2)检测报告不准确、不规范
3)危害到检测人员的身心健康
4)影响环境等
4.2.3分析风险可能发生的频次。
4.3风险评估
4.3.1质量主管根据风险分析的情况组织相关人员进行风险评估。
4.3.2风险评估报告包括以下内容
1)确定风险评估小组成员;
2)本次风险评估的目的;
3)本次风险评估的范围;
4)评估原则;
5)风险评估的识别和分析过程
6)具体分析风险发生结果严重性;
7)根据风险发生后果的可能性采取的预防措施;
8)如发生不可控的情况所采取的补救和控制措施。
4.4风险防范措施的批准和实施
4.4.1最高管理者批准风险评估报告,并由档案管理员进行编号后受控发放给相关人员。
4.4.2风险评估报告中涉及的相关人员实施预防措施以防止风险的产生;
4.4.3检测业务办公室主任负责组织对风险产生后补救和控制措施进行演练。
4.5风险控制的验证
各部门负责人对预防措施、补救措施和控制措施执行情况实施监控和验证。
6.相关文件。
