弓形虫 ELISA检测 说明书 人用文档
弓形虫试纸测试操作方法

弓形虫试纸测试操作方法
1.准备操作材料:弓形虫试纸、采血器、消毒棉球、无菌采血管、计时器、标本采集管(EDTA管或干血滴管)等。
2.消毒手部和试纸操作区域,穿戴手套,使用无菌采血器采集静脉血或指尖血。
3.将采集的血液滴在弓形虫试纸上。
4.等待10-15分钟后,观察试纸变化,根据试纸说明书进行解读。
5.拍照记录试纸结果,方便日后查询。
6.在处理血液过程中,注意避免交叉污染和误操作。
7.操作完成后,将试纸和采血器打包装入医疗废弃物袋中,做好消毒和隔离处理。
弓形虫

弓形虫抗体IgG检测试剂盒(酶联免疫法)使用说明书【产品名称】通用名称:弓形虫抗体IgG检测试剂盒(酶联免疫法)英文名称:Diagnostic Kit for IgG Antibody to Toxoplasma gondii(ELISA)【包装规格】48人份/盒,96人份/盒【预期用途】本试剂盒主要用于定性检测人血清或血浆中的抗弓形虫IgG抗体和人体内TOXO-IgG抗体含量变化的动态检测,及TOXO-IgG抗体亲和指数的测定,适用于弓形虫感染的辅助诊断和弓形虫感染者的流行病学调查。
【检验原理】本试剂盒采用基因工程表达的重组弓形虫抗原包被反应板,以酶标记的鼠抗人IgG为示踪物及四甲基联苯胺作为显色系统,ELISA间接法检测人血清或血浆中的弓形虫IgG抗体。
【主要组成成份】半成品名称主要组分规格半成品名称主要组分规格1 TOX-IgG反应板TOX重组抗原4×12孔/ 8×12孔8 底物液A 过氧化氢溶液1瓶(4ml / 8.5ml)2 TOX-IgG酶结合物鼠抗人IgG-HRP1瓶(6.5ml/13ml) 9 底物液B TMB 1瓶(4ml / 8.5ml)3 TOX-IgG阴性对照山羊血清1瓶(1ml) 10 终止液硫酸1瓶(4ml / 8.5ml)4 TOX-IgG阳性对照TOX-IgG阳性血清1瓶(1ml) 11 封板膜3贴5 TOX-IgG Cut-off对照 TOX-IgG阳性血清1瓶(1ml) 12 说明书1份6 浓缩洗涤液(20×)磷酸盐1瓶(25ml / 50ml) 13 自封袋1个7 TOX-IgG标本稀释液NaCl 1瓶(6.5/13ml)【贮存条件及有效期】试剂盒应置2-8℃存放12个月。
【标本要求】血清标本按常规方法由静脉采集,血浆标本可采用常规用量的肝素或枸橼酸钠抗凝。
标本置于2~8℃可保存7天,-20℃可保存6个月。
已稀释的标本不宜存放,应避免溶血或反复冻融。
应用ELISA方法检测多种动物弓形虫抗体

弓形虫抗体 E LISA 试剂盒袁购自法国 ID vet公司袁批号 为 B 78遥 酶标仪袁购自奥地利 SU N R ISE 公司遥
4.3
基 4.2 质 4.1 效4 应 3.9 系 3.8 数 3.7
3.6 0
200
400
600
基质效应系数
标样浓度渊 单位院ng/m L冤 图 2 标样浓度与基质效应系数
1.6.1 结果讨论 可以从图 2 得知袁当盐酸克伦特罗浓度为 20ng/L耀 500ng/L 时袁无论是纯溶剂制备的标样还是猪尿基质 配制的标样袁其浓度都与出峰面积即响应值都呈正比例的线 性关系遥 而且线性相关系数 R 2 都大于 0.995袁可谓标准曲线 线性关系良好遥
2019 年第 07 期 35
试验研究
感染袁会引起流产尧死胎和先天的畸形袁对免疫缺陷或免疫力 差的人群危害很大遥 弓形虫严重影响了人类健康和畜牧业的 发展袁给公共卫生也带来很大的威胁遥 为了掌握东莞市多种 动物弓形虫感染的情况袁在屠宰场采集了猪血清袁采集作为 宠物饲养的犬尧猫血清袁应用 E LISA 方法进行抗体检测袁现将 试验结果报告如下遥 1 材料与方法
由表 2 得知袁 在盐酸克伦特罗浓度为 20ng/L耀 500ng/L 时袁基质效应系数在 3.67耀 4.12遥 在浓度范围为 2020ng/L耀 200ng/L 时袁 基质效应系数成常数袁 大约为 4遥 当浓度升到 500ng/L 的时候袁基质效应系数有细微的下降遥
快灵生物弓形虫抗体检测卡说明书

快灵生物弓形虫抗体快速检测试纸卡(TOXO Ab)产品用途:快灵生物犬猫弓形虫抗体快速检测试纸卡可以帮助兽医及宠物主人在10分钟内准确地鉴别诊断犬、猫是否产生弓形虫抗体。
检测样品:血清包装规格:10条/盒,独立包装适用情况:宠物医院,宠物饲养场,动物卫生监督部门,养宠家庭精密性:同批次产品在相同样品浓度下测定,反应结果一致,显色均一保存条件:阴凉干燥处保存,不可冷冻,避免阳光直晒,2-30℃可保存18个月。
常见问题:1)根据临床经验判断为阳性,但是检测卡检测为阴性?A、现在的动物疫病感染方式越来越复杂,而且呈现多种疫病混合感染,疫病的感染症状也不典型,所以单靠临床经验判断没有太大的说服力。
B 、感染初期或潜伏期,病毒含量较少,所以测不出来,建议过几天再测2)快灵试纸和其他家试纸检测出的结果不符合?A、病毒上面有不同的抗原决定簇,在试纸研发过程中,选用的特异性抗体都是对应不同的抗原决定簇,所以不能保证所有试纸厂家都是选用同一特异性抗体,也就有可能出现多个厂家的试纸结果不符合,好的试纸一定是选择了最具有代表性的特异性抗体。
B、病毒在流行过程中,其抗原决定簇可能也会发生变异,不同地区流行的毒株可能存在病毒抗原漂移。
因此同一品牌试纸未必能将某类病毒的各个变异型全部检出。
、C、各种试纸的灵敏度不一样,也会导致在病毒浓度较低时检测结果出现偏差。
D、患病宠物处于患病初期时,体液内病毒浓度偏低,取样方式或时间的差异,均会导致试纸卡反应结果的差异。
3)抗原检测阳性的实际意义是什么?抗原检测阳性能直接确诊动物病原的存在。
临床治疗中也可对抗原进行间歇检测来观察使用药物对病原的影响。
当然,刚注射疫苗不久的动物用试纸进行检测,结果也可能是阳性,但做为疫苗的抗原与具有攻击力的野毒在动物体内的浓度一般有较大差距,因此在T线反应颜色强度上也存在差异。
如果是灭活疫苗,则在动物体内很快就被中和了,试纸也就检测不出了。
4)T线出现慢若犬猫发病处于潜伏期,排泄的病毒量可能较少,相应采集溶液中的病毒浓度偏低。
ELISA法检测弓形虫IgM抗体测定(TOX-IgM)标准操作程序
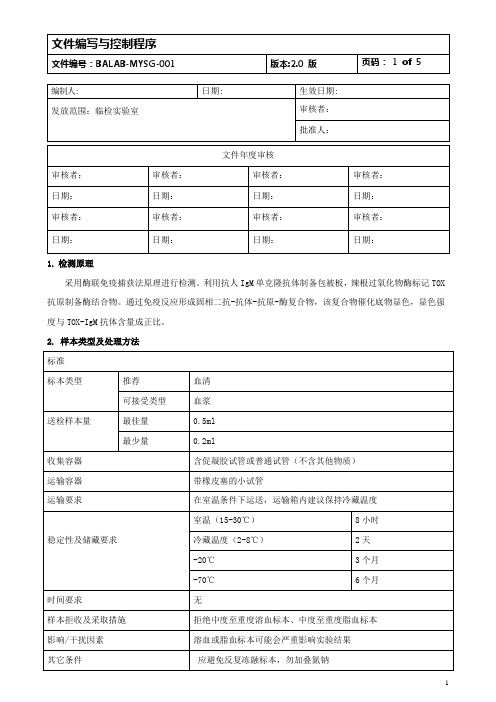
1.检测原理采用酶联免疫捕获法原理进行检测。
利用抗人IgM单克隆抗体制备包被板,辣根过氧化物酶标记TOX 抗原制备酶结合物。
通过免疫反应形成固相二抗-抗体-抗原-酶复合物,该复合物催化底物显色,显色强度与TOX-IgM抗体含量成正比。
2. 样本类型及处理方法3.试剂注意事项:开启所有试剂(包括校准品、标准品、质控品)需注明日期及签名。
每个试剂容器都需贴上写有以下内容的标签:启用日期、截止日期。
开启时应检查试剂是否变色,是否肉眼可见的细菌生长迹象、浊度、沉淀反应等,这些表示试剂已经变质或超过保质期。
不同批号试剂盒中各组份不可以互换,组份所标示量为最低分装量。
4.仪器设备备注:“溯源方式”栏填写送较、自校、送检、自检、比对等。
5.质量控制5.1使用的质控品5.2质控周期5.2.1每一批次标本均需运行一次质控。
5.2.2每一批标本最大量为:92个标本。
5.3变异系数CV<20%5.4质控判断标准即时质控法5.5失控处理:对质控失控需查找原因并进行分析5.5.1先观察整块酶标板显色是否正常。
5.5.2查找操作过程是否按照SOP文件进行。
5.5.3质控品S/CO值>3SD或质控品S/CO值<3SD,结合模式报告结果。
6.操作步骤6.1选用试剂:郑州安图生物工程股份有限公司6.2平衡:从冷藏环境中取出的试剂盒内全部瓶装试剂及待测标本所需微孔反应条应放置室温平衡30分钟后方可使用,余者应及时放入有干燥剂的自封袋封存于冰箱中备用。
在平衡试剂的同时,待测标本需放置室温平衡30分钟后再行测试。
6.3配液:取1包固体洗液用500ml纯化水溶解后备用。
配制好的洗涤液如用不完可放置2-8℃冷藏储存,使用前应放置室温平衡20分钟后方可使用。
6.4加样:用移液器在反应孔中分别加入阴、阳性对照血清和TOX-IgM质控品各100ul,测定孔中加入样品稀释液100ul,再依次加入待测血清样品10ul,用封口膜封板。
Toxoplasma IgG ELISA测试产品说明书

Toxoplasma IgG ELISA Catalog Number SE120126Storage Temperature 2–8 °CTECHNICAL BULLETINProduct DescriptionToxoplasma gondii causes toxoplasmosis, a common disease that affects 30–50 of every 100 people in North America by the time they are adults. The mean source of infection is direct contact with cat feces or from eating undercooked meats. Toxoplasmosis generally presents with mild symptoms in immunocompetent individuals. In the immunocompromised patient,however, the infection can have serious consequences. Acute toxoplasmosis in pregnant women can result in miscarriage, poor growth, early delivery, or stillbirth. Treatment of an infected pregnant woman may prevent or lessen the disease in her unborn child. Treatment of an infected infant will also lessen the severity of the disease as the child grows. IgG and IgM antibodies to Toxoplasma can be detected with 2–3 weeks after exposure. IgG remains positive, but the antibody level drops overtime. ELISA can detect Toxoplasma IgM antibody one year after infection in over 50% of patients. Therefore, IgM positive results should be evaluated further with one or two follow up samples if primary infection is suspected.The Toxoplasma IgG ELISA Kit is intended for the detection of IgG antibody to Toxoplasma in human serum or plasma. Diluted serum is added to wellscoated with purified Toxoplasma antigen. Toxoplasma IgG specific antibody, if present, binds to the antigen. All unbound materials are washed away and the enzyme conjugate is added to bind to the antibody-antigen complex, if present. Excess enzyme conjugate is washed off and substrate is added. The plate isincubated to allow the oxidation of the substrate by the enzyme. The intensity of the color generated isproportional to the amount of IgG specific antibody in the sample.ComponentsReagents and Equipment Required but Not Provided.1.Distilled or deionized water2.Precision pipettes3.Disposable pipette tips4.ELISA reader capable of reading absorbance at450 nm5.Absorbent paper or paper towel6.Graph paperPrecautions and DisclaimerThis product is for R&D use only, not for drug,household, or other uses. Please consult the Safety Data Sheet for information regarding hazards and safe handling practices.Preparation Instructions Sample Preparation1. Collect blood specimens and separate the serum.2.Specimens may be refrigerated at 2–8°C for up toseven days or frozen for up to six months. Avoid repetitive freezing and thawing.20x Wash Buffer ConcentratePrepare 1x Wash buffer by adding the contents of the bottle (25 mL, 20x) to 475 mL of distilled or deionized water. Store at room temperature (18–26 °C).2Storage/StabilityStore the kit at 2–8 °C.ProcedureNotes: The components in this kit are intended for use as an integral unit. The components of different lots should not be mixed.Optimal results will be obtained by strict adherence to the test protocol. Precise pipetting as well as following the exact time and temperature requirements is essential.The test run may be considered valid provided the following criteria are met:1.If the O.D. of the Calibrator is >0.250.2.The Ab index for Negative control should be <0.9.3.The Ab index for Positive control should be >1.2. Bring all specimens and kit reagents to room temperature (18–26 °C) and gently mix. 1.Place the desired number of coated strips into theholder.2.Negative control, positive control, and calibrator areready to use.Prepare 21-fold dilution of testsamples, by adding 10 µL of the sample to 200 µLof Sample Diluent. Mix well.3.Dispense 100 µL of diluted sera, calibrator, andcontrols into the appropriate wells. For the reagent blank, dispense 100 µL of Sample Diluent in 1Awell position. Tap the holder to remove air bubbles from the liquid and mix well. Incubate for20 minutes at room temperature.4.Remove liquid from all wells. Wash wells threetimes with 300 µL of 1x wash buffer. Blot onabsorbent paper or paper towel.5.Dispense 100 µL of enzyme conjugate to each welland incubate for 20 minutes at room temperature. 6.Remove enzyme conjugate from all wells. Washwells three times with 300 µL of1x wash buffer.Blot on absorbent paper or paper towel7.Dispense 100 µL of TMB substrate and incubate for10 minutes at room temperature.8.Add 100 µL of stop solution.9.Read O.D. at 450 nm using ELISA reader within15 minutes. A dual wavelength is recommendedwith reference filter of 600–650 nm.3ResultsCalculations1.Check Calibrator Factor (CF) value on thecalibrator bottle. This value might vary from lot tolot. Make sure the value is checked on every kit. 2.Calculate cut-off value: Calibrator OD x CalibratorFactor (CF).3.Calculate the Ab (Antibody) Index of eachdetermination by dividing the mean values of each sample by cut-off value.Example of typical results:Calibrator mean OD = 0.8Calibrator Factor (CF) = 0.5Cut-off Value = 0.8 x 0.5 = 0.400Positive control O.D. = 1.2Ab Index = 1.2/0.4 = 3Patient sample O.D. = 1.6Ab Index = 1.6/0.4 = 4.0Note:Lipemic or hemolyzed samples may cause erroneous results.InterpretationThe following is intended as a guide to interpretation of Toxoplasma IgG antibody index (Ab Index) test results; each laboratory is encouraged to establish its own criteria for test interpretation based on sample populations encountered.<0.9 –No detectable IgG antibody to Toxoplasma byELISA0.9–1.1 –Borderline positive. Follow-up testing isrecommend if clinically indicated.>1.1 –Detectable IgG antibody to Toxoplasma by ELISA References1.Wilson, M. et al., Evaluation of six commercial kitsfor detection of human immunoglobulin Mantibodies to Toxoplasma gondii. The FDAToxoplasmosis Ad Hoc Working Group.2.Obwaller, A. et al., An enzyme-linkedimmunosorbent assay with whole trophozoites ofToxoplasma gondii from serum-free tissue culturefor detection of specific antibodies. Parasitol. Res., 1995;81(5):361-4.3.Loyola, A.M. et al., Anti-Toxoplasma gondiiimmunoglobulins A and G in human saliva andserum. J. Oral Pathol. Med., 1997; 26(4):187-91. 4.Doehring, E. et al., Toxoplasma gondii antibodies inpregnant women and their newborns in Dar esSalaam, Tanzania. Am. J. Trop. Med. Hyg., 1995;52(6):546-8.5.Cotty, F. et al., Prenatal diagnosis of congenitaltoxoplasmosis: the role of Toxoplasma IgAantibodies in amniotic fluid [letter]. J. Infect. Dis.,1995;171(5):1384-5.6.Altintas, N. et al., Toxoplasmosis in last four yearsin Agean region,Turkey. J. Egypt. Soc. Parasitol.,1997;27(2):439-43.RGC,CH,MAM 10/14-1©2014 Sigma-Aldrich Co. LLC. All rights reserved. SIGMA-ALDRICH is a trademark of Sigma-Aldrich Co. LLC, registered in the US and other countries. Sigma brand products are sold through Sigma-Aldrich, Inc. Purchaser must determine the suitability of the product(s) for their particular use. Additional terms and conditions may apply. Please see product information on the Sigma-Aldrich website at and/or on the reverse side of the invoice or packing slip.。
弓形虫IgG酶联免疫法检测试剂盒.

弓形虫IgG 酶联免疫法检测试剂盒(TOXO IgG ELISA TEST SYSTEM )体外诊断试剂产品编号:8Z8651G简介:宙斯(Zeus)公司的弓形虫IgG酶联免疫检测试剂盒是应用酶联免疫技术定性或定量检测人血清中的弓形虫IgG 抗体的系统。
目的是为弓形虫的感染提供血清学证据,用于体外诊断。
本产品FDA 没有明确可以用于检测血液和献血者。
背景:刚地弓形虫是一类分布在世界范围内的细胞内原生动物寄生虫(1,2)。
虽然猫科动物是其终宿主,但该生物体却能感染几乎所有的哺乳动物和鸟类。
血清学数据表明虽然不同国家的人弓形虫盛行的种类不同,但大部分的工业化国家有大约30%的人都会慢慢受到该原虫的感染(3)。
弓形虫有三种存在形式:滋养体、包囊和卵囊(1,2)。
滋养体(速殖子)在急性感染阶段是具有攻击性的形式。
原虫在宿主细胞胞质中繁殖以后形成组织包囊形式,此时的包囊可以包含数千个生物体(缓殖子)。
卵囊只在猫科动物的小肠上皮细胞中发育,并未在其他宿主中发现。
卵囊随着猫科动物排泄的粪便排出体外,数天后发育成熟。
人类或其他动物摄取了具有包囊的生的、未加工的肉或具有卵囊的被猫的粪便污染了的食物便得到感染。
一旦消化,该寄生虫便从包囊中(缓殖子)被释放出来,卵囊(孢子体)被消化酶消化并侵染小肠粘膜。
寄生虫就地繁殖然后以包囊的形式转移到其他器官,包囊可以在宿主的生命中长期存在。
包囊主要存在于脑、心脏和骨骼肌中。
感染刚地弓形虫的人大多数(80~90%)是无症状的(4)。
感染急性弓形虫的成年人大多表现的临床症状为无症状的单结或多结淋巴结病症状,伴随淋巴结病症状还有发热、身体不适和非典型性淋巴细胞增多,症状与单核细胞增多症相同。
少数宿主患者通常会出现严重的并发症,像脑炎、心肌炎或局部急性肺炎等(1)。
尽管感染刚地弓形虫对于一般寄主通常并无疾病影响,但是,对于那些患有免疫缺陷疾病的寄主却是致命的(5)。
免疫缺陷的病人可以发展成具有严重传染性的弓形虫病,或弓形虫性脑炎,或者同时患上这两种病。
快速Dot-ELISA检测弓形虫IgG初探概要

快速Dot-ELISA检测弓形虫IgG初探中分类号:R382.5 文献标识码:B文章编号:1005-2534(2000)02-0070-02弓形虫病是一种人兽共患的寄生虫病,在我国平均感染率为5.84%[1]。
弓形虫(下简称Toxo)是专性细胞内寄生虫,病原检出率较低,所以免疫学检测仍是诊断本病的一种主要手段。
本文以集试验载体和试验容器合一的白色PVC为载体,以快速Dot-ELISA法[2]检测各类血清的Toxo-IgG,结果如下。
1. 材料及方法1.1 材料1.1.1 抗原制备用B36株弓形虫(中山医科大学陈观今教授惠赠)接种于小白鼠腹腔,3~4天处死小白鼠,以无菌生理盐水冲洗小白鼠腹腔,收集冲洗液,按文献[3]方法纯化速殖子及制备可溶性抗原(Toxo-Ag),以考马斯亮兰G250法测蛋白含量,低温贮存备用。
致敏白色PVC载体的蛋白含量为50μg/ml。
每点抗原2μl。
1.1.2 载体白色PVC系5×2孔平底凹孔板,孔径1cm,孔深0.5cm[2]。
1.1.3 试剂抗原稀释液为pH 9.6碳酸盐缓冲液。
血清、酶结合物稀释液及洗涤液为pH 7.4 PBS-NP40。
HRP-羊抗人IgG按改良过碘酸钠法标记[4],工作浓度1∶400。
显色底物为4-氯-1-萘酚-H2O2。
1.1.4 试验血清PCR检测证实Toxo为阳性血清12份(四川省计划生育研究所惠赠);病原学证实为阳性的血吸虫病、华支睾吸虫病和疟疾血清及B超或CT证实为包虫病和囊虫病血清共444份;其他疾病及未知人群血清986份。
试验血清稀释度1∶20。
1.2 方法取预致敏Toxo-Ag的白色PVC板,每孔加PBS 100μl及待测(或参考)血清5μl,混匀,置25℃以上室温或37℃温箱温育10min,倾去液体,加PBS快洗1次,自来水快洗5次,甩干水份,每孔滴加酶结合物1~2滴,如上温育、洗涤,每孔滴加底物1~2滴,如上温度下显色3min,用自来水冲洗终止反应,判读结果。
快灵生物弓形虫抗体检测卡说明书

快灵生物弓形虫抗体快速检测试纸卡(TOXO Ab)产品用途:快灵生物犬猫弓形虫抗体快速检测试纸卡可以帮助兽医及宠物主人在10分钟内准确地鉴别诊断犬、猫是否产生弓形虫抗体。
检测样品:血清包装规格:10条/盒,独立包装适用情况:宠物医院,宠物饲养场,动物卫生监督部门,养宠家庭精密性:同批次产品在相同样品浓度下测定,反应结果一致,显色均一保存条件:阴凉干燥处保存,不可冷冻,避免阳光直晒,2-30℃可保存18个月。
常见问题:1)根据临床经验判断为阳性,但是检测卡检测为阴性?A、现在的动物疫病感染方式越来越复杂,而且呈现多种疫病混合感染,疫病的感染症状也不典型,所以单靠临床经验判断没有太大的说服力。
B 、感染初期或潜伏期,病毒含量较少,所以测不出来,建议过几天再测2)快灵试纸和其他家试纸检测出的结果不符合?A、病毒上面有不同的抗原决定簇,在试纸研发过程中,选用的特异性抗体都是对应不同的抗原决定簇,所以不能保证所有试纸厂家都是选用同一特异性抗体,也就有可能出现多个厂家的试纸结果不符合,好的试纸一定是选择了最具有代表性的特异性抗体。
B、病毒在流行过程中,其抗原决定簇可能也会发生变异,不同地区流行的毒株可能存在病毒抗原漂移。
因此同一品牌试纸未必能将某类病毒的各个变异型全部检出。
、C、各种试纸的灵敏度不一样,也会导致在病毒浓度较低时检测结果出现偏差。
D、患病宠物处于患病初期时,体液内病毒浓度偏低,取样方式或时间的差异,均会导致试纸卡反应结果的差异。
3)抗原检测阳性的实际意义是什么?抗原检测阳性能直接确诊动物病原的存在。
临床治疗中也可对抗原进行间歇检测来观察使用药物对病原的影响。
当然,刚注射疫苗不久的动物用试纸进行检测,结果也可能是阳性,但做为疫苗的抗原与具有攻击力的野毒在动物体内的浓度一般有较大差距,因此在T线反应颜色强度上也存在差异。
如果是灭活疫苗,则在动物体内很快就被中和了,试纸也就检测不出了。
4)T线出现慢若犬猫发病处于潜伏期,排泄的病毒量可能较少,相应采集溶液中的病毒浓度偏低。
PCR-ELISA检测弓形虫实验研究

PCR-ELISA检测弓形虫实验研究李健;杨秀珍;梁东春;刘佩梅【期刊名称】《中国人兽共患病学报》【年(卷),期】2006(022)004【摘要】目的建立快速、敏感、特异、稳定的PCR-ELISA方法,并用其检测感染动物体内的弓形虫.方法将生物素标记的PCR产物与地高辛标记的特异性探针杂交,再通过酶免显色反应测出OD值,以判断弓形虫感染情况.测定该方法的敏感性、特异性及稳定性.再分别以104、103弓形虫RH株速殖子腹腔接种小鼠,取全血、肝组织用PCR-ELISA检测小鼠感染情况.结果本实验中,PCR-ELISA方法的检测阈值为20fg弓形虫DNA,其灵敏度是电泳法的10倍,并且与人、小鼠、疟原虫、旋毛虫等DNA均无交叉反应.同一样本重复测试5次,结果经统计学检验,一致性良好(Alpha=0.72).检测感染动物肝组织及全血标本,104、103组分别在感染后第二d、第三d即可测出阳性,两种标本的阳性检出效率无统计学差异( P >0.05).结论 PCR-ELISA是一种快速、敏感、特异、稳定的检测方法,可试用于临床弓形虫病的诊断及流行病学调查.【总页数】5页(P356-359,355)【作者】李健;杨秀珍;梁东春;刘佩梅【作者单位】天津医科大学基础医学院生物学教研室,天津,300070;天津医科大学基础医学院寄生虫学教研室;天津医科大学内分泌研究所;天津医科大学基础医学院寄生虫学教研室【正文语种】中文【中图分类】R382.5【相关文献】1.量子点标记技术同步检测抗弓形虫IgG和IgM抗体的实验研究 [J], 李玲;刘琳琳;白晓;罗慧琴;李蒙;蒲晓允2.RNA原位杂交法检测组织内弓形虫的实验研究 [J], 史晓燕;赵恒梅;曾宪忠;韩敏3.PCR技术检测RH株弓形虫组织内感染的实验研究 [J], 单连玉;杨秀珍;刘佩梅4.双抗体夹心免疫-PCR检测弓形虫循环抗原的实验研究 [J], 华海涌;周永华;薛忠权5.检测弓形虫PCR-ELISA方法的建立 [J], 李健;杨秀珍;梁东春;刘佩梅因版权原因,仅展示原文概要,查看原文内容请购买。
弓形虫病血清学诊断技术

弓形虫病血清学诊断技术一、实验目的及要求掌握弓形虫病血清学诊断技术,通过对弓形虫的检测和鉴定,为防治和预防弓形虫病提供科学依据。
二、实验器材弓形虫虫株、小白鼠、恒温箱、离心机、血清、G3砂蕊漏斗、纤维素滤膜、试管、载玻片、盖玻片、显微镜、荧光显微镜、冰冻切片机、吸管、湿盒、微量血凝试验型V反应板、微量加样器、无菌试管、一次性灭菌注射器、冰箱、胶乳试验玻璃板、常规石蜡切片机、染色缸、水浴锅、微量加样仪、ELISA 板、等。
药品:生理盐水、胰酶、美蓝染液、PBS、弓形虫诊断制剂(IHA抗原)、碘酒、70%酒精、无菌生理盐水、5%柠檬酸钠、DAB、Tris盐酸、牛血清白蛋白(BSA)等。
三、实验方法步骤和操作要领。
弓形虫病血清学诊断技术主要有以下几种方法:(一)染色试验(Sabin—Feldman dye tese,DT)染色试验(Sabin—Feldman dye tese,DT)。
是弓形虫特有的血清学诊断法,此法特异性高而且被认为是标准的诊断方法。
其原理是活的弓形虫速殖子与正常血清混合,在37℃作用1h或室温数小时后,大部分滋养体由原来的新月形变为圆形或椭圆形,细胞质对碱性美蓝具有较强的亲和力而被深染。
但当弓形虫与含特异性抗体和补体(辅助因子accessoryfactor.AF)的血清混合时,虫体受到抗体和补体的协同作用而变性,对碱性美蓝不着色。
计算着色与不着色虫体比例即可判断结果。
1.辅助因子。
存在于正常人新鲜血清内,不耐热。
用作辅助因子的血清需预先筛选,即将候选血清与弓形虫速殖子混合,37℃作用1h后,有90%以上虫体经美蓝染色后,着色者即含有辅助因子(AF)。
含辅助因子血清可分装后于一2O℃保存备用。
2.抗原制备。
弓形虫速殖子经腹腔感染小鼠,3d后抽取腹腔液,生理盐水洗涤3次 (300Or/min×lOmin),收集纯净虫体。
也可将小鼠腹腔悬液用胰酶消化,经G3砂蕊漏斗或纤维素滤膜过滤纯化,所获虫体用辅助因子血清稀释至每高倍视野50个左右虫体,即为抗原液。
快速Dot-ELISA检测弓形虫IgG初探

显色底物为 &8氯8!8萘酚 - G" J" 。 , #, # / 试验血清 35) 检测证实 0121 为阳性血清 !" 份 (四川省计划生育研究所惠赠) ; 病原学证实为阳性的血吸 虫病、 华支睾吸虫病和疟疾血清及 , 超或 50 证实为包虫 病和囊虫病血清共 &&& 份; 其他疾病及未知人群血清 (+$ 份。试验血清稀释度 ! I "%。 ,#方法 取预致敏 01218=> 的白色 345 板, 每孔加 3,< !%% C及 ! 待测 (或参考) 血清 ’ , 混匀, 置 以上室温或 温 C "’K *.K ! 箱温育 !%BLM, 倾去液体, 加 3,< 快洗 ! 次, 自来水快洗 ’ 次, 甩干水份, 每孔滴 加酶结合物 ! @ " 滴, 如上温育、 洗 涤, 每孔滴加底物 ! @ " 滴, 如上温度下显色 *BLM, 用自来 水冲洗终止反应, 判读结果。凡待测血清出现与参阳血清 一致的兰紫色斑点者为阳性。无色或呈浅灰色斑点 (环) 者为阴性。 -#, 结果 最佳试验条件选择
[!] 吸虫病的交叉阳性率达 ! " #$ , 与华支睾吸虫病的交叉 [#] 阳性率达 %% " &$ 。从这些结果和我们的试验表明, ’()(
与蠕虫类寄生虫都有较高的交叉阳性, 但从我们对 & 份 用 ’()(*., ’()(*+,- 阳性的包虫病血清中和试验又显示, 中和后 ’()(*+,- 全部转阴, 用包虫抗原中和后 ’()(*+,- 仍 这一结果又揭示, 有 / 0 & 血清呈阳性, ’()( 不仅与蠕虫类 寄生虫存在共同抗原而导致交叉阳性, 且 ’()( 与蠕虫混 合感染的可能性不能排除。 据蒋和柱等对我省 # 个县农村人群及动物 ’()( 感染 个别县高达 的血 清 学 调 查, 人 群 阳 性 率 平 均 1 " 2&$ , 动物中以羊 ( 34 " 2$ ) , 猪 ( 32 " 4!$ ) 的阳性率最 32 " 4!$ 。 [5] 高, 狗、 兔的阳性率也在 /$ 左右 。本文所检蠕虫病血 清均来自我省农村和牧区, 这些人群与动物接触十分密 切, 感染 ’()( 的可能相对较大, 所以, 我们认为 ’()( 除与 多种蠕虫有共同抗原而导致交叉阳性外, ’()( 与蠕虫混合 感染的可能性不能完全排除。由于本文只对包虫病血清 进行了中和试验, 所以这一问题有待进一步试验去证实。 本次试 验 中, 由 于 商 品 67+8. 试 剂 数 量 较 少, 只对 9:; 证实 ’()( 为阳性和 <(=*67+8. 试验 ’()(*+,- 为阳性的 部分血清, 用商品 67+8. 试剂进行了检测, 从初步结果看, 但 似乎 <(=*67+8. 的敏感性优于商品 67+8. 试剂的结果, 由于未对大批量的血清进行平行比较检测, 难以评价孰优 孰劣, 将在进一步的试验中去比较、 评价。总之, 从本次初
犬猫弓形虫抗原检测试剂盒说明书

犬(猫)弓形虫抗原检测试剂盒使用说明书【原理】本产品采用双抗体夹心一步法原理(ELISA),检测犬血清中弓形虫循环抗原(CAg)。
CAg的检测不能单独作为弓形虫感染的唯一诊断依据,而可作为弓形虫现症感染的辅助诊断指标。
【试剂组成】1.预包被板48T/96T;6.终止液(6号液) 1支;2.酶结合物(1号液,用前1:50稀释) 1支; 7.阳性对照品1支;3.浓缩洗涤液(2号液,兼做稀释液;用前以蒸馏水20倍稀释) 1支;8.阴性对照品1支;9.自封袋1个;4.底物(3号液) 1支; 10.不干胶膜1/2片;5.显色剂(4号液) 1支; 11.使用说明书1份;【操作程序】1. 加样反应:待测孔每孔加稀释的洗涤液(2号液)40ul、血清样本10ul,混匀。
同时设阴性、阳性及空白对照各一孔,分别加入阴性、阳性对照及稀释的洗涤液各50ul,混匀。
每孔再加稀释的酶结合物50ul(空白孔除外),混匀,37℃反应60分钟。
2. 显色反应:甩去孔内液体,用稀释的洗涤液洗涤五次,每次间隔1分钟,拍干。
每孔加底物(3号液)和显色剂(4号液)各一滴,37℃下避光反应10分钟,加终止液(6号液)一滴混匀,终止反应。
【结果判断】阴性对照呈无色或浅黄色,阳性对照呈明显黄色,表示试验有效。
以空白对照调零,用酶标仪于450nm(630nm作参比波长)读取吸光度(A值)。
待检孔A值大于阴性对照A值平均值的2.1倍者判为阳性。
如阴性对照A值的平均值低于0.08时按0.08计算。
【注意事项】1.试剂盒于2-8℃保存,有效期6个月。
每次使用前应先平衡至室温。
2.未使用完的板条应密封保存。
3.试剂盒中终止液具有腐蚀性,要小心使用。
4.瓶盖每次使用后要拧紧,各瓶盖之间不可混用。
不同批号试剂盒的试剂组份不可混用。
5.试验样本应为无染菌、无血脂、无溶血的血清。
任何样本都应视为传染源妥善处理。
6. 37℃孵育时,建议使用水浴箱。
如无条件,可在温箱中放置湿盒进行反应并同时用不干胶膜封盖板孔。
瑞必诊犬猫弓形虫说明书

瑞必诊犬猫弓形虫说明书摘要:一、瑞必诊犬猫弓形虫说明书简介1.产品背景2.适用范围3.产品特点二、弓形虫病的危害及诊断1.弓形虫病的危害2.弓形虫病的诊断方法三、瑞必诊犬猫弓形虫检测卡的使用方法1.产品组成2.操作步骤3.结果解读四、瑞必诊犬猫弓形虫检测卡的优势1.灵敏度高2.操作简便3.结果准确五、注意事项1.使用禁忌2.保存方法3.售后服务正文:一、瑞必诊犬猫弓形虫说明书简介瑞必诊犬猫弓形虫检测卡是一款专门用于检测犬猫弓形虫感染的产品,为广大兽医和宠物主人提供了方便快捷的检测手段。
本说明书将详细介绍瑞必诊犬猫弓形虫检测卡的使用方法和注意事项。
二、弓形虫病的危害及诊断弓形虫病是由弓形虫寄生引起的一种人畜共患寄生虫病。
弓形虫感染可导致动物出现流产、死胎、生长迟缓等症状,同时对人类健康也存在潜在威胁,尤其是孕妇感染弓形虫后可能导致胎儿先天性弓形虫病。
目前,诊断弓形虫病主要依靠血清学检测和病原学检测。
三、瑞必诊犬猫弓形虫检测卡的使用方法瑞必诊犬猫弓形虫检测卡主要由检测卡、样本收集棒和说明书组成。
使用时,只需按照以下三个步骤操作:1.使用样本收集棒采集犬猫的唾液样本;2.将唾液样本滴入检测卡的样本孔;3.等待10 分钟,观察检测卡上的显示结果。
四、瑞必诊犬猫弓形虫检测卡的优势瑞必诊犬猫弓形虫检测卡具有以下优势:1.灵敏度高:能够准确检测出弓形虫感染;2.操作简便:无需专业设备,轻松完成检测;3.结果准确:采用进口原料,确保检测结果的可靠性。
五、注意事项1.使用禁忌:请勿使用过期的检测卡或已开启的样本收集棒;2.保存方法:请将检测卡和样本收集棒存放在阴凉、干燥的地方,避免阳光直射;3.售后服务:如有产品质量问题,请及时联系售后服务人员。
通过以上介绍,相信大家对瑞必诊犬猫弓形虫检测卡有了更加全面的了解。
弓形虫病的检测方法和诊断流程

结果分析:根据检测结果判断弓形 虫病的感染情况
报告出具:出具检测报告,提供诊 断建议
诊断与鉴别诊断
临床症状:发热、头 痛、肌肉疼痛等
实验室检查:血常规、 尿常规、粪便常规等
影像学检查:X线、 CT、MRI等
病原学检查:PCR、 ELISA等
鉴别诊断:与其他寄 生虫病、病毒感染等
调查内容:弓形虫病的发病率、死 亡率、传播途径、易感人群等
调查方法:问卷调查、访谈、实验 室检测等
调查结果:分析弓形虫病的流行趋 势,提出预防和控制措施
临床表现观察
单击添加项标题
发热、头痛、肌肉酸痛等全身症状
单击添加项标题
神经系统症状,如癫痫、精神异常等
单击添加项标题
免疫学检查,如抗体检测、细胞因子检测等
断
免疫磁珠分离试验(IMS):
05 检测弓形虫特异性抗体,
用于早期诊断
免疫印迹试验(Western
03 Blot):检测弓形虫特异性抗
体,用于早期诊断
免疫荧光染色试验(IF):检
06 测弓形虫特异性抗体,用于早
期诊断
分子生物学检测
01
PCR技术:通过扩增弓形虫的 DNA片段进行检测
03
基因芯片:通过检测弓形虫的基因 表达进行检测
弓形虫病的检测方法和诊断 流程
汇报人:
汇报时间:20XX/XX/XX
YOUR LOGO
目录
CONTENTS
1 弓形虫病的检测方法 2 弓形虫病的诊断流程
弓形虫病的检测方法
病原学检测
显微镜检查: 观察弓形虫形 态和运动方式
免疫学检测: 检测弓形虫抗 体和抗原
弓形虫病 病情说明指导书

弓形虫病病情说明指导书一、弓形虫病概述弓形虫病(toxoplasmosis)是由刚地弓形虫引起的人畜共患疾病。
本病为全身性疾病,在人体多为隐性感染,临床表现复杂,易造成误诊,主要侵犯眼、脑、心、肝、淋巴结等。
孕妇感染后,病原可通过胎盘感染胎儿,直接影响胎儿发育,致畸严重,已引起广泛重视。
它是艾滋病患者重要的机会性感染之一。
英文名称:toxoplasmosis。
其它名称:弓形体病。
相关中医疾病:蛊病。
ICD疾病编码:暂无编码。
疾病分类:暂无资料。
是否纳入医保:部分药物、耗材、诊治项目在医保报销范围,具体报销比例请咨询当地医院医保中心。
遗传性:不会遗传,但可通过母婴传播传给胎儿。
发病部位:其他。
常见症状:视网膜剥离、白内障、斜视和眼球震颤、高热、癫痫。
主要病因:刚地弓形虫感染。
检查项目:血常规、病原学检查、染色试验、间接免疫荧光试验检测、皮肤试验。
重要提醒:胎儿可通过母婴传播感染此病,影响胎儿生长发育,因此母亲在怀孕期间应格外小心,勿食生食,勿饮生水。
临床分类:1、先天性弓形体病2、弓形体眼病3、弓形体性脑炎4、弓形体性淋巴结炎5、弓形体性心血管病6、弓形体性肝炎7、全身重症型弓形体病8、弓形体性肺炎9、输血、器官移植并发弓形体病10、其他类型:弓形体性免疫复合物性肾炎、皮肤弓形体病可现斑疹、猩红热样皮炎(多见于四肢躯干)或结节。
二、弓形虫病的发病特点三、弓形虫病的病因病因总述:本病由刚地弓形虫感染所致,可通过母婴传播、接触传播等方式来进行传染。
主要经消化道侵入人体,经局部淋巴结或直接进入血液循环,造成虫血症。
在正常情况下,感染者可产生有效的保护性免疫,多数无明显症状,当感染者有免疫缺陷或免疫功能低下时才引起弓形虫病。
基本病因:1、刚地弓形虫的生物学特性刚地弓形虫,属于球虫目、弓形虫科、弓形虫属。
弓形虫具有双宿主生活周期,分两个发育阶段。
前者在各中间宿主和终末宿主组织内发育,后者仅于终末宿主小肠黏膜上皮细胞内发育。
优生五项说明书-IgM-1

[ 包装规格 l
l 人份/袋、 10人份/盒、 20人份f盒、 25人份/盒、 40人份/盒、 50人份/盒 、 1 ∞人份/盒 。
l 预期用途 l 本试剂用于体外定性检测人血清中的弓形虫 I gM 、凤r;;病毒 I gM 、 巨细胞病毒 I gM 、 单纯炮捞病
毒 l 型 I g M 、单纯痕r;;病毒 H 型 I gM抗体。 TORC H - 词是数种孕妇患病后将引起于宫内胚胎(胎儿 ) 感染引发流产 、 甚至造成先天缺陷或 发育异常的病原体英文名称的第 一 个字母组合而成 。 它包括弓形虫(
l 、开始试验前将试剂和待检样品平衡至室温。 没有准备好之前,不可撕开铝筒袋 。 打开内包装后 l
小时内使用(湿度
20 %-90 % .温度
1O"C -50 "C )。
2 、 打开密封的铝?自袋,取出试剂板,平放干水平桌面上,编号(与样品相对应) 。
3 、用滴管在每个加中丰孔(共五个孔)内加入 2nlj (80-100μL ) 血清样品,于3时告钟时观察测试结果,
体征、病史、其他实验室检查(尤其是病原学检测)、治疗反应及流行病学等信息综合考虑。
4 - 30"C保存 , 避光、越热 、干燥处贮存,不得冻存,有效期 1 8个月 。
l 样本要求 ] 血清
I -lgM 、 HSV- II - l gM
取静脉血,静置使其自然收缩,离心得血泊。 血消标本2 - 8 "C冰箱存放最好不要超过3天,若不
能及时检测应 -20 "C冻存 。
2 、本试剂检测结果仅供临床参考,不作为临床诊治的唯一依据,对患者的临床管理应结合其症状/
[ 检验原理 ] 本试刑依据金标免疫层析试验 (Gold Immunochromat ography A臼 'y. C I CA) 原理 应用TOR C H ( TO X 、 RV 、 CMV 、 H SV- I , HSV- rr )基因重组抗原市l抗人 I gM单克隆抗体,以高度特异灵敏的捕 获法定性检测人血泊中的 I gM抗体,当待检标本中含TOR C H -lgM ( TOX-IgM 、 R V-l gM 、 CMV-I gM 、
鸡弓形虫循环抗原TCA酶联免疫分析ELISA
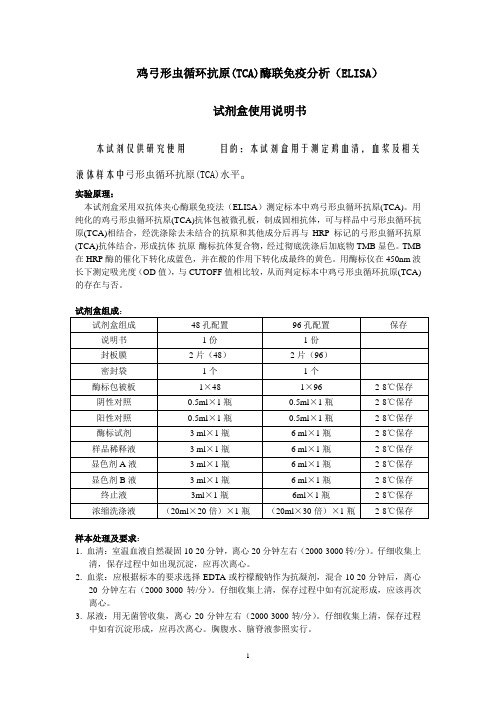
鸡弓形虫循环抗原(TCA)酶联免疫分析(ELISA)试剂盒使用说明书本试剂仅供研究使用目的:本试剂盒用于测定鸡血清,血浆及相关液体样本中弓形虫循环抗原(TCA)水平。
实验原理:本试剂盒采用双抗体夹心酶联免疫法(ELISA)测定标本中鸡弓形虫循环抗原(TCA)。
用纯化的鸡弓形虫循环抗原(TCA)抗体包被微孔板,制成固相抗体,可与样品中弓形虫循环抗原(TCA)相结合,经洗涤除去未结合的抗原和其他成分后再与HRP标记的弓形虫循环抗原(TCA)抗体结合,形成抗体-抗原-酶标抗体复合物,经过彻底洗涤后加底物TMB显色。
TMB 在HRP酶的催化下转化成蓝色,并在酸的作用下转化成最终的黄色。
用酶标仪在450nm波长下测定吸光度(OD值),与CUTOFF值相比较,从而判定标本中鸡弓形虫循环抗原(TCA)的存在与否。
样本处理及要求:1. 血清:室温血液自然凝固10-20分钟,离心20分钟左右(2000-3000转/分)。
仔细收集上清,保存过程中如出现沉淀,应再次离心。
2. 血浆:应根据标本的要求选择EDTA或柠檬酸钠作为抗凝剂,混合10-20分钟后,离心20分钟左右(2000-3000转/分)。
仔细收集上清,保存过程中如有沉淀形成,应该再次离心。
3. 尿液:用无菌管收集,离心20分钟左右(2000-3000转/分)。
仔细收集上清,保存过程中如有沉淀形成,应再次离心。
胸腹水、脑脊液参照实行。
4. 细胞培养上清:检测分泌性的成份时,用无菌管收集。
离心20分钟左右(2000-3000转/分)。
仔细收集上清。
检测细胞内的成份时,用PBS(PH7.2-7.4)稀释细胞悬液,细胞浓度达到100万/ml左右。
通过反复冻融,以使细胞破坏并放出细胞内成份。
离心20分钟左右(2000-3000转/分)。
仔细收集上清。
保存过程中如有沉淀形成,应再次离心。
5. 组织标本:切割标本后,称取重量。
加入一定量的PBS,PH7.4。
用液氮迅速冷冻保存备用。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
正文】
弓形虫IgG抗体检测试剂盒(酶联免疫法)说明书
一、制品名称
通用名:弓形虫IgG抗体检测试剂盒(酶联免疫法)
英文名:Diagnostic Kit for IgG Antibody to Toxoplasma(ELISA)
汉语拼音:Gongxingchong IgG Kangti Jiance Shijihe(Meilian Mianyifa)
二、原理与用途
体外诊断用试剂,本品系由纯化弓形虫抗原包被的微孔板和酶标记抗人IgG抗体及其他试剂配套组成,应用间接法原理检测人血清或血浆样品中的弓形虫IgG抗体。
本品对样本原液的最低检出量为100IU/ml。
三、试剂盒的组成
1、包被弓形虫抗原的微孔板96孔
2、酶标记抗人IgG抗体6.5ml
3、阳性对照血清0.8ml
4、临界阳性对照血清0.8ml
5、阴性对照血清0.8ml
6、显色液A 6.5ml
7、显色液B 6.5ml
8、终止液6.5ml
9、浓缩洗涤液(10倍) 50ml
10、样品稀释液52ml×2
四、样本要求
本试验用血清或血浆进行检测,用量为10μl。
勿使用染菌、脂血、溶血或黄疸样品。
按照标准方法收集血清,室温保存样品不要超过8小时,若实验在8小时以后进行,需将样品保存在2~10℃,如保存超过1周则保存在-20℃。
五、操作程序
1、试剂盒在室温平衡20~30分钟。
浓缩洗涤液用蒸馏水或去离子水10倍稀释。
2、样品1:100稀释:将样品稀释液1ml加入一洁净小管内,加10ml待检样品,充分混匀。
3、将板条固定于板架上,剩余的板条用不干胶密封并放入密封袋中保存。
每孔加入稀释后样品100ml,每个样品至少做2孔。
阳性对照、阴性对照各加2孔,临界对照血清加3孔,100ml/孔。
另留一孔不加任何液体为空白对照。
置37℃30分钟。
4、甩净孔中液体,洗板3次,每次停留1分钟后甩净拍干,除空白对照外每孔加酶标记物50ml(1滴),置37℃30分钟。
5、甩净孔中液体,同上洗板3次,拍干后各孔滴加显色液A、B各50ml(1滴),置37℃避光10分钟,每孔立即加入终止液50ml(1滴),混匀后用酶标仪450nm读数判定结果。
六、质量控制
以空白孔调零,450nm波长测定A值。
阳性对照A值平均值≥0.50,阴性对照A值平均值≤0.10,临界对照A值平均值介于0.12~0.35,证明实验成立。
七、结果判定
样品A值≥临界对照A值平均值判为阳性,样品A值<临界对照A值平均值则判为阴性。
八、注意事项
1、不同试剂组分不得混用;
2、试剂盒应按含有传染性材料对待;
3、凡是染菌、严重溶血、黄疸或高血脂的待检样品可能引起错误结果,应重新采样复试或
改用其他方法检测;
4、实验阳性提示弓形虫既往感染,临床医生应结合病史、体检等全面考虑诊断;
5、判断临床意义应动态观察,即对阳性者要求2周后进行复查,观察抗体水平的变化。
九、规格:96人份/盒
十、保存及效期
于2~8℃保存,有效期为6个月。
批准文号:
企业名称:珠海经济特区海泰生物制药有限公司
地址:广东省珠海市拱北夏湾港二路45号
邮政编码:519020。
