《无机化学》第十章 固体结构之课后习题参考答案
大连理工大学无机化学教研室《无机化学》(第5版)(课后习题详解固体结构)

⼤连理⼯⼤学⽆机化学教研室《⽆机化学》(第5版)(课后习题详解固体结构)10.2 课后习题详解1. 填充下表:解:根据已知条件可得表10.1:表 10.12.根据晶胞参数,判断下列物质各属于何种晶系?解:根据已知条件可得表10.2:表 10.23. 根据离⼦半径⽐推测下列物质的晶体各属何种类型。
解:上述物质都为AB 型离⼦键化合物,在不考虑离⼦极化的前提下,晶体的离⼦半径⽐与晶体构型的关系为:+-r r 当=0.225~0.414时,晶体为ZnS 型;+-r r =0.414~0.732时,晶体为NaCl 型;+-r r =0.732~1.000时,晶体为CsCl型。
+-r r4. 利⽤Born-Haber 循环计算NaCl 的晶格能。
解:设计循环如下:5. 试通过Born-Haber 循环,计算MgCl 2晶格能,并⽤公式计算出晶格能,再确定两者符合程度如何(已知镁的I 2为1457 kJ?mol -1)。
解:设计的循环如下:则通过Born-Haber 循环,计算MgCl 2晶格能为:⽤公式计算出晶格能为:通过⽐较两种⽅法计算出的晶格能⼤⼩,可见⽤两种⽅法计算的结构基本相符。
6. KF 晶体属于NaCl 构型,试利⽤公式计算KF 晶体的晶格能。
已知从Born-Haber 循环求得的晶格能为802.5 kJ?mol -1。
⽐较实验值和理论值的符合程度如何。
解:根据题意可知,晶体属于构型,即离⼦晶体构型,故查表可知KF NaCl 。
1.748A =⼜因为,,所以1(79)82n =+=0()()133136269R r K r F pm pm pm +-=+=+=与Born-Haber 循环所得结果相⽐,误差为7. 下列物质中,何者熔点最低?解:⼀般情况下,离⼦晶体的晶格能越⼤,则其熔点越⾼。
影响晶格能的因素很多,主要是离⼦的半径和电荷。
电荷数越⼤,离⼦半径越⼩,其晶格能就越⼤,熔点越⾼。
所以的熔点最低。
无机化学习题参考答案

第一章 原子结构和元素周期系1-1.答:(1)3×3+C 32×C 31=18 (2)2×3+C 22×C 31=91-2.答:出现两个峰1-3.答:Ar=78.9183×50.54%+80.9163×49.46%=79.90651-4. 解:fi 203Tl=x ,fi 205Tl=y ,则有x+y=100%, 202.97×x +204.97×y =204.39由此得到 fi 203Tl=29% fi 205Tl=71%1-5.解:M AgCl :M AgI =143.321(107.868+Ar)=1:1.63810Ar=126.911-6. 解:∆Ar=195.078-194.753=0.3251-8.答:因为元素的相对原子质量的取值决定于两个因素:一,同位素相对原子质量的准确性。
另一是某元素同位素丰度测量准确性。
对于那些只有一种同位素丰度特别大的元素,同位素 测量不准确对原子影响较小。
而几个同位素丰度较大的原子量准确性就不高。
1-9.答:地球上所有比氢重的原子,是在形成太阳系时从其它星体喷发物质中俘获的。
1-13.解:(1)r=c /λ=(3×108)/(633×10-9)=4.74×1014Hz 氦-氖激发是红光(2)r=c/λ=(3.0×108)/(435.8×10-9)=6.88×1014Hz 汞灯发蓝光(3)r=c/λ=(3.0×108)/(670.8×10-9)=4.47×1014Hz 锂是紫红1-14.解:r=E/h=(190×103)/(6.02×1023×6.63×10-34)=4.7676×1014Hzλ=c/r=(3×108)/(4.7676×1014)=638nm1-17. 解:r=E/h=(310×103)/(6.63×10-34×6.02×1023) 则λ=c/r397nm1-18. 解:λ=h×z/E=(6.63×10-34×3×108×6.02×1023)/(305×103)=392nm 属于紫外层当λ=320nm 时,则此时光的能量E=5.64×10-19>E 最低,所以会解离1-19.解:ΔE=hc/λ=(6.63×10-34×3×108)/(103×10-9)=10.2ev E1=-13.6ev E2=-3.4ev 它相应于氦原子核外电子的L-K 跃迁1-21.解:M li =7.02×1.66×10-27kg=1.165×10-26kgλ电子=h/p=(6.63×10-34)/(9.109×10-31×3.0×108×20%)=12pmλLi =h/p=(6063×10-34)/(1.165×10-26×3.0×108×20%)=9.48×10-4pm1-23.解:K 层电子最大数目:2 L 层电子最大数目:8 M 层电子最大数目:81-24.解:(b )1p (d) 2d (f) 3f 这些符号是错误的。
化学课后答案10
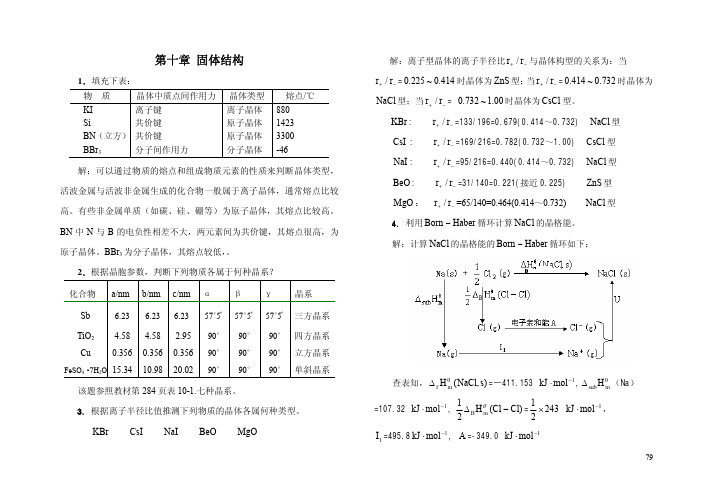
1.填充下表: 物 质 KI Si BN(立方) BBr3 晶体中质点间作用力 离子键 共价键 共价键 分子间作用力 晶体类型 离子晶体 原子晶体 原子晶体 分子晶体 熔点/℃ 880 1423 3300 -46
解:离子型晶体的离子半径比 r+ / r− 与晶体构型的关系为:当
r+ / r− = 0.225 ~ 0.414 时晶体为 ZnS 型; 当 r+ / r− = 0.414 ~ 0.732 时晶体为 NaCl 型;当 r+ / r− = 0.732 ~ 1.00 时晶体为 CsCl 型。 KBr : CsI : NaI : BeO : MgO : r+ / r− =133/196=0.679(0.414~0.732) r+ / r− =169/216=0.782(0.732~1.00) r+ / r− =95/216=0.440(0.414~0.732) r+ / r− =31/140=0.221(接近 0.225) r+ / r− =65/140=0.464(0.414~0.732) NaCl 型 CsCl 型 NaCl 型 ZnS 型 NaCl 型
熔点/℃
991
1396
1040
-90
-94
-56
-220
(3) 蒸汽压最小(298K) : CO 2 , SiO 2 , H 2 O ; (4) 汽化热最大: H 2 O , H 2 S , H 2 Se , H 2 Te ; (5) 熔化焓最小: H 2 O , CO 2 , MgO 。 解: (1)三物种从 NaCl 到 Na 再到 Cl 2 依次为离子晶体、金属晶体、 分子晶体,故其沸点依次降低, NaCl 的沸点最高。 (2) CO 为极性分子,分子之间存在色散、取向和诱导作用,其凝固点 比为非极性分子的 CH 4 和 H 2 要高; CH 4 和 H 2 中 H 2 的 M r 比 CH 4 的小 得多,故其凝固点最低。 (3) 常压下,298K 时 CO 2 为气体,H 2 O 为液体,SiO 2 为固体, 故 SiO 2 的蒸汽压最小。 (4) H 2 O , H 2 S , H 2 Se , H 2 Te 为同族元素的化合物,但是只有 H 2 O 能形成作用力很强的氢键,故其汽化热最大。 (5) MgO 是离子化合物,常态下为固体,晶格能较大,熔点较高,熔 化焓大; H 2 O 和 CO 2 均为共价化合物,都是分子晶体,通常条件下分别 为液体和气体,故它们的熔化焓较 MgO 低;H 2 O 和 CO 2 中 H 2 O 能形成 氢键,故熔化焓较 CO 2 要高。三者中 CO 2 的熔化焓最小。
无机化学习题解答讲解

《无机化学》习题解答第一章 溶液和胶体1. 求0.01㎏NaOH 、0.10㎏(2Ca 2+)、0.10㎏(21Na 2CO 3)的物质的量。
解:M (NaOH )= 40g·mol -1 M (2Ca 2+)= 80g·mol -1 M (21Na 2CO 3)= 53g·mol -1 它们的物质的量分别为()(NaOH)0.011000(NaOH) 0.25mol (NaOH)40m n M ⨯===()2+2+2+(2Ca )0.101000(2Ca ) 1.25mol (2Ca )80m n M ⨯=== ()2323231( Na CO )10.1010002( Na CO ) 1.89mol 1253( Na CO )2m n M ⨯===2. 将质量均为5.0g 的NaOH 和CaCl 2分别溶于水,配成500mL 溶液,试求两溶液的ρ(NaOH)、c (NaOH)、ρ(21CaCl 2)和c (21CaCl 2)。
解:M (NaOH )= 40g·mol -1 M (21CaCl 2)= 55.5g·mol -1()-1(NaOH) 5.0(NaOH)10.0g L 0.5m V ρ===⋅()-1(NaOH)10.0(NaOH)0.25mol L (NaOH)40c M ρ===⋅ ()2-121(CaCl )1 5.02(CaCl )10.0g L 20.5m V ρ===⋅ ()2-1221(CaCl )110.02(CaCl )0.18mol L 1255.5(CaCl )2c M ρ===⋅3. 溶液中KI 与KMnO 4反应,假如最终有0.508gI 2析出,以(KI +51KMnO 4)为基本单元,所消耗的反应物的物质的量是多少?解:题中的反应方程式为10KI + 2KMnO 4 +8H 2SO 4 = 5I 2 + 2MnSO 4 + 6K 2SO 4 + 8H 2O将上述反应方程式按题意变换为KI +51KMnO 4 +54H 2SO 4 =21I 2 +51MnSO 4 +53K 2SO 4 +54H 2O1mol 21moln (KI +51KMnO 4)mol 0.508254mol则所消耗的反应物的物质的量为n (KI +51KMnO 4)= 2×0.508254= 0.004(mol )4. 静脉注射用KCl 溶液的极限质量浓度为2.7g·L -1,如果在250 mL 葡萄糖溶液中加入1安瓿(10 mL)100 g·L -1KCl 溶液,所得混合溶液中KCl 的质量浓度是否超过了极限值?解:混合溶液中KCl 的质量浓度()-1(KCl)1000.010(KCl) 3.85g L 0.2500.010m V ρ⨯===⋅+ 所得混合溶液中KCl 的质量浓度超过了极限值。
《无机化学》习题解析和答案

《无机化学》习题解析和答案1、教材《无机化学》师大学、华中师大学、师大学无机化学教研室编,高等教育,2002年8月第4版。
2、参考书《无机化学》师大学、华中师大学、师大学无机化学教研室编,高等教育,1992年5月第3版。
《无机化学》邵学俊等编,大学,2003年4月第2版。
《无机化学》大学、大学等校编,高等教育,1994年4月第3版。
《无机化学例题与习题》徐家宁等编,高等教育,2000年7月第1版。
《无机化学习题精解》竺际舜主编,科学,2001年9月第1版《无机化学》电子教案绪论(2学时)第一章原子结构和元素周期系(8学时)第二章分子结构(8学时)第三章晶体结构(4学时)第四章配合物(4学时)第五章化学热力学基础(8学时)第六章化学平衡常数(4学时)第七章化学动力学基础(6学时)第八章水溶液(4学时)第九章酸碱平衡(6学时)第十章沉淀溶解平衡(4学时)第十一章电化学基础(8学时)第十二章配位平衡(4学时)第十三章氢和稀有气体(2学时)第十四章卤素(6学时)第十五章氧族元素(5学时)第十六章氮、磷、砷(5学时)第十七章碳、硅、硼(6学时)第十八章非金属元素小结(4学时)第十九章金属通论(2学时)第二十章s区元素(4学时)第二十一章 p区金属(4学时)第二十二章 ds区元素(6学时)第二十三章 d区元素(一)第四周期d区元素(6学时)第二十四章d区元素(二)第五、六周期d区金属(4学时)第二十五章核化学(2学时)1 .化学的研究对象什么是化学?●化学是研究物质的组成、结构、性质与变化的一门自然科学。
(太宽泛)●化学研究的是化学物质 (chemicals) 。
●化学研究分子的组成、结构、性质与变化。
●化学是研究分子层次以及以超分子为代表的分子以上层次的化学物质的组成、结构、性质和变化的科学。
●化学是一门研究分子和超分子层次的化学物种的组成、结构、性质和变化的自然科学。
●化学研究包括对化学物质的①分类;②合成;③反应;④分离;⑤表征;⑥设计;⑦性质;⑧结构;⑨应用以及⑩它们的相互关系。
无机答案第10章习题答案

第10章习题答案1. (a) (b)(d)(e)2. (a) BaSO 4 离子晶体 (b) NaOH 离子晶体 (c) Xe 分子晶体 (d) I 2 分子晶体 (e)Al 金属晶体 (f) 黄铜 金属晶体 (g) P 4 分子晶体 (h) P 4O 10 分子晶体3. (b)4. (a)5. Mg 2+的离子半径要小于Ca 2+,故MgO 的晶格能大于CaO ,MgO 中离子键较强,因而MgO 的晶体稳定性大于CaO ,溶解时MgO 中的离子键较CaO 难解离。
6. (a)立方密堆积Al 12 (b) 六方密堆积Mg 12(c) 体心立方Cr 8 (d) 简单立方Po 67. (b) 体心立方8.解:每个体心立方晶胞中含2个Cr 原子d = m/V = (NM/N A )/( 34r)3r =43(NM/N A d)1/3 =43 [2×51.996 g.mol -1/(6.022×1023 mol -1×7.2 g·cm -3)]1/3= 1.252 Å9.解:每个体心立方晶胞中含2个V 原子d = m/V = (NM/N A )/( 34r)3= (2×50.9415 g.mol -1)/[6.022×1023mol -1× (34×1.321×10-8cm)3]= 5.959g.cm -310.解:室温下:体心立方d 1 = m 1/V 1 = (N 1M/N A )/(34r)3 ①910 o C :面心立方d 2= m 2/V 2 = (N 2M/N A )/(22r)3 ②①/②:863)23(42)23(332121===N N d d==63812d d 8.56g.cm -3,故铁从体心立方转为面心立方结构密度增大,是收缩。
11. KBr :NaCl 型, CsI :CsCl 型, BeO :立方ZnS 型,MgO :NaCl 型。
江苏师范大学《无机化学》习题库及答案第十章 固体结构

化合物 CuBr CuI AgCl AgBr AgI CdS
NaCl NaCl
实际晶型 ZnS 型 ZnS 型
ZnS 型 ZnS 型
型
型
颜色
浅黄棕黄
白
白
白
黄色
色
色
r+/r-
0.49 0.44 0.69 0.65 0.58 0.53
理论晶型
5、根据离子极化理论解释下列化合物的溶解度大小变化: CuCl>CuBr>CuI(3
属(9~17)e-构型
Fe3+: 1s22s22p63s23p63d5
属(9~17)e-构型
离子的电子构型相同,由于 Fe3+的电荷高,所以极化力 Fe3+>Ni2+
(5) Li+:1s2
属 2e-构型
Be2+:1s2
属 2e-构型
离子的电子构型相同,由于 Be2+的电荷高,所以极化力 Be2+>Li+
(2) TiCl4 是共价型化合物,LiCl 是离子型化合物,所以 LiCl 的沸点比 TiCl4 高得
多。 7. NaCl、MgCl2、AlCl3 3 种物质中的离子极化作用依次增大,共价性增加,所 以熔点降低。 8. SiCl4、PCl3、Cl2 是共价化合物,且分子间的范德华力一般以色散力为主,因 此 SiCl4 的熔点最高,PCl3 次之,Cl2 的熔点最低。 9. 虽然 Cu+与 Na+的离子半径相近,但 Cu+为 18e-电子构型,Na+为 8e-电子构型, Cu+的极化作用比 Na+的极化作用大,因此 NaCl 易溶于水,而 CuCl 难溶。 10. 解:石墨是层状晶体,层与层间以范德华力结合。这种引力不仅较弱,而且 没有方向性和饱和性,层与层之间可以滑移,所以可以做润滑剂。石墨同一层中 的碳原子以 sp2 形式杂化,每个碳原子都有一个未参与杂化的 p 轨道和一个单电 子,而且相互平行构成大 π 键,因此可以导电。石墨的化学性质较稳定,故通常 用作惰性电极材料。
无机化学 第10章_固体结构

1.Born-Haber循环
K(s) +
1 2
Br
2
(l)
气化热 △ rHm,3
升 华 焓
△
rHm,1 1
2
1
2
键能
Br
△
2 (g)
rHm,4
△fHm
KBr(s)
U △ rHm,6
K(g)
Br (g)
△ rHm,5
电子亲和能
△ rHm,2
电离能
Br (g)
+
K + (g)
△fHm= △ rHm,1 + △ rHm,2 +△ rHm,3 +△ rHm,4 +△ rHm,5 + △ rHm,6
2.Born-Lande公式
UKA1ZZ2 (11)
R0
n
当R0以 pm , U以kJm o1为 l 单位时
U138A 91Z 42(011)kJmo 1 l
式中:
R0
n
R0—正负离子核间距离, Z1,Z2 —分别为正负离子电荷的绝对值,
A —Madelung常数,与晶体类型有关,
NH 3
同核:H 2 N 2 O 2
S
,
8
P4
BF 3 ,CH 4 ,CO 2
分子的偶极矩与键矩的关系: 极性键构成的双原子分子:
分子偶极矩 = 键矩 多原子分子的偶极矩 = 键矩的矢量和, 例如:μ(SF6) = 0,键矩互相抵消,
μ(H2O)≠0,键矩未能抵消。
分子的偶极矩μ(×10-30 C·m)
γ 分别是bc , ca , ab 所 组成的夹角。
晶胞的内容包括粒子的种类,数目及它在 晶胞中的相对位置。
第十章中级无机化学课后习题答案

第10章习题1 简要回答问题(1) 什么叫稀土元素? 什么叫镧系元素?答:参见本书10.1节《概述》。
(2) 镧系收缩的原因是什么? 简述镧系收缩造成的影响。
答:关于镧系收缩的原因参见本书10.1.2节《原子半径和离子半径》。
由于镧系收缩的影响,使第二、三过渡系的Zr和Hf、Nb与Ta、Mo与W三对元素的半径相近,化学性质相似,分离困难。
(3) 为什么Eu、Yb原子半径比相邻元素大? 而Ce又小?答:① Eu、Yb元素参与形成金属键的电子数为2,Ce为3.1,其余为3.0;② Eu、Yb具碱土性;③ Eu、Yb的f7、f14的半充满和全充满的结构能量低、稳定、屏蔽大,核对外面的6s电子吸引较弱。
(4) 为什么镧系元素的电子结构在固态和气态不同?解:参见本书10.1.1节《镧系元素的价电子层结构》。
(5) 镧系离子的电子光谱同d区过渡金属离子相比有何不同? 为什么?解:除La3+、Lu3+离子的4f电子层是全空(4f0)和全满(4f14)之外,其余Ln3+离子4f轨道上的电子数由1到14,这些电子可以在7条4f简并轨道上任意排布,这样就会产生各种光谱项和能级。
4f 电子在不同能级间跃迁可以吸收或发射从紫外经可见直至红外区的各种波长的电磁辐射。
通常具有未充满的4f电子壳层的原子或离子,可以观察到的光谱线大约有30 000条,而具有未充满d电子壳层的过渡金属元素的谱线约有7 000条。
在理论上,f→f跃迁产生的谱线强度不大。
但是某些f→f跃迁的吸收带的强度,随镧系离子周围环境的变化而明显增大(这种跃迁称为超灵敏跃迁)。
这可能是由于配体的碱性、溶剂的极性、配合物的对称性以及配位数等多种因素的影响,亦即离子周围环境的变化,再加上镧系离子本身的性质等诸因素的综合作用所引起的。
镧系离子的吸收谱带范围较广且镧系离子光谱谱带狭窄,表明电子跃迁时并不显示激发分子振动,狭窄的谱带意味着电子受激发时分子势能面几乎没有变化,这与f 电子与配体只存在弱相互作用相一致。
(完整word版)大学无机化学第十章试题及答案

第十章配位化合物本章总目标:1:掌握配合物的基本观点和配位键的实质2:掌握配合物的价键理论的主要论点,并能用此解说一些实例3:配离子稳固常数的意义和应用4:配合物形成时性质的变化。
各小节目标:第一节:配位化合物的基本观点1:掌握中心原子、配体、配位原子、配位键、配位数、螯合物等观点,○1 配位单元:由中心原子(或离子)和几个配位分子(或离子)以配位键向联合而形成的复杂分子或离子。
○2 配位化合物:含有配位单元的化合物。
○3 配位原子:配体中给出孤电子对与中心直接形成配位键的原子。
○4 配位数:配位单元中与中心直接成键的配位原子的个数。
2:学会命名部分派合物,要点掌握命名配体的先后次序:(1)先无机配体后有机配体( 2)先阴离子配体,后分子类配体(3)同类配体中,先后次序按配位原子的元素符号在英文字母表中的序次(4)配位原子同样时,配体中原子个数少的在前( 5)配体中原子个数同样,则按和配位原子直接相连的其余原子的元素符号的英文字母表序次;3:认识配合物的构造异构和立体异构现象第二节:配位化合物的价键理论1:熟习直线形、三角形、正方形、四周体、三角双锥、正八面体构型的中心杂化种类。
2:会分辨内轨型和外轨型配合物。
能够经过测定物质的磁矩来计算单电子数n(n 2)BM 。
3:经过学习羰基配合物、氰配合物以及烯烃配合物的 d p配键来熟习价键理论中的能量问题。
第三节:配合物的晶体场理论1:掌握配合物的分裂能、稳固化能观点2:掌握配合物的晶体场理论。
3;认识影响分裂能大小的要素○1 )晶体场的对称性p0t○2 中心离子的电荷数,中心离子的电荷高,与配体作用强,大。
○3 中心原子所在的周期数,对于同样的配体,作为中心的过渡元素所在的周期数大,相对大些。
( 4)配体的影响,配体中配位原子的电负性越小,给电子能力强,配体的配位能力强,分裂能大。
2IBrSCN ClFOHONOC2O4H 2 ONCS NH 3 en NO2 CN CO4:要点掌握( 1)配合物颜色的原由之一——d-d 跃迁以及颜色与分裂能大小的关系;(2)高自旋与低自旋以及与磁矩的大小的关系。
无机化学课后习题参考答案完全版(汪小兰第四版)

目录第一章绪论 (1)第二章饱和烃 (2)第三章不饱和烃 (6)第四章环烃 (14)第五章旋光异构 (23)第六章卤代烃 (28)第七章波谱法在有机化学中的应用 (33)第八章醇酚醚 (43)第九章醛、酮、醌 (52)第十章羧酸及其衍生物 (64)第十一章取代酸 (72)第十二章含氮化合物 (79)第十三章含硫和含磷有机化合物 (87)第十四章碳水化合物 (90)第十五章氨基酸、多肽与蛋白质 (101)第十六章类脂化合物 (106)第十七章杂环化合物 (115)Fulin 湛师第一章 绪论1.1扼要归纳典型的以离子键形成的化合物与以共价键形成的化合物的物理性质。
答案:1.2 NaCl 与KBr 各1mol 溶于水中所得的溶液与NaBr 及KCl 各1mol 溶于水中所得溶液是否相同?如将CH 4及CCl 4各1mol 混在一起,与CHCl 3及CH 3Cl 各1mol 的混合物是否相同?为什么? 答案:NaCl 与KBr 各1mol 与NaBr 及KCl 各1mol 溶于水中所得溶液相同。
因为两者溶液中均为Na +,K +,Br -, Cl -离子各1mol 。
由于CH 4与CCl 4及CHCl 3与CH 3Cl 在水中是以分子状态存在,所以是两组不同的混合物。
1.3碳原子核外及氢原子核外各有几个电子?它们是怎样分布的?画出它们的轨道形状。
当四个氢原子与一个碳原子结合成甲烷(CH 4)时,碳原子核外有几个电子是用来与氢成键的?画出它们的轨道形状及甲烷分子的形状。
答案:C+624H CCH 4中C 中有4个电子与氢成键为SP 3杂化轨道,正四面体结构CH 4SP 3杂化2p y2p z2p x2sH1.4写出下列化合物的Lewis 电子式。
a.C 2H 4b.CH 3Clc.NH 3d.H 2Se.HNO 3f.HCHOg.H 3PO 4h.C 2H 6i.C 2H 2j.H 2SO 4 答案:a.C C H HCC HH HH或 b.H C H c.H N Hd.H S H e.H O NOf.O C H Hg.O P O O H H Hh.H C C HHH H HO P O O H HH或i.H C C Hj.O S O HH OS H H或1.5下列各化合物哪个有偶极矩?画出其方向。
无机化学第十章作业参考答案

(8) 因氧化生成的Fe3+与Fe反应生成Fe2+,防止Fe2+氧 化 (9) Co2+与过量CN-形成配离子Co(CN)64-,由于此配离 子不稳定,稍加热即与H2O反应放出H2,自身变为 Co(CN)63- 。 (10) 由于形成[Ni(CN)4]2-时Ni2+的3d电子发生重排, 已经没有了成单电子,所以为抗磁性,但在[NiCl4]2中,因配体Cl-为弱场配体,不能使Ni2+的3d电子发生 重排,所以形成[NiCl4]2-仍有两个成单电子,为顺磁 性。
17解:(1)由题意可知:[CrO42-]=0.9mol/L; [Cr2O72-]=0.1mol/L; 代入平衡常数表达式:
[Cr2 O ] 0.1 14 1 . 0 10 2 2 [CrO4 ] [ H ]2 0.9 2 [ H ]2
[H+]=3.5×10-8 pH=7.45 (2)由题意可知:[CrO42-]=0.1mol/L; [Cr2O72-] =0.9mol/L; 代入平衡常数表达式:
23解:(1) MnO2;Co2O3
(2) V2O5; MnO2;Co2O3
(3) V2O5; TiO2 (4) Cr2O3;MnO2 (5) Fe2O3
26解:∵ Eθ(O2/H2O)>Eθ(Mn2+/Mn)
∴ O2可与Mn反应,即Mn不能稳定存在
O2+4H++2Mn==2H2O+2Mn2+
∵ Eθ(Co3+/Co2+)> Eθ(O2/H2O) ∴ Co3+可以氧化H2O,则Co3+不能稳定存在. 4Co3++2H2O==4Co2++O2+4H+
无机化学课后习题答案

第一章原子结构和元素周期律1-1. 不可能存在的是:(1)(2)(5)(6)(7)(8)1-2. C1-3. D1-4. D1-5. A1-6. B1-7. B1-8. A为Ca ,B为Mn ,C为Br ,D 为O1-9. A为Na ,B为Mg ,C为Al ,D 为Br ,E 为I ,F 为Cr第二章分子结构与晶体结构2-1. A2-2. C2-3. B2-4. B2-5. C2-6. AD2-7. BD2-8. D2-9. LiH属于s-s,HCl属于s-p,Cl2属于p-p2-10. 主要形成离子键的有:(1),(3),(8)主要形成极性共价键的有:(2),(5),(6),(7)主要形成非极性共价键的有:(4)第三章化学热力学基础3-1. C3-2. A3-3. D3-4.U3-6. (1)不对,可通过作功形式改变温度;(2)不对,热力学能的绝对值目前无法测得,热力学第一定律表达式中有ΔU而不是U;(3)对,冰熔化成0℃水需要吸热。
3-7.3-8.133 kJ·mol-13-9.解:(1)向真空膨胀W1 =-(2)恒外压膨胀J(3)两步恒外压膨胀J由于W3>W2>W1,说明膨胀次数愈多,则体系与环境的压力差愈小,做的功愈大。
3-10.解:=0.01 m3=810.5 JU =H = 0 ,Q = W = 810.6 J第四章化学动力学基础4-1. D 4-2. D 4-3. C 4-4. D 4-5. A4-6. C 4-7. D 4-8. B第五章 化学平衡与平衡原理5-1. 增加总压平衡向左移动;注入惰性气体平衡不变;升高温度平衡向右移动。
5-2. O H 2,+O H 3。
可以作为酸的有:-3HCO ;可以作为碱的有:33,,Ac NH HCO --。
5-3. 溶解度不变。
5-4. (1)AgCl 的溶解度会降低,但对溶度积没影响; (2)AgCl 的溶解度会增加,不影响溶度积; (3)AgCl 的溶解度会增加,不影响溶度积。
无机化学第三版课后习题答案(武汉大学版) 很全面哦

2.2
2.0
0.0
0.2
0.4
0.6
0.8
1.0
1.2
P (105pa)
解
可得出一氯甲烷的相对分子质量是 50.495
12.(1)用理想气体状态方程式证明阿佛加德罗定律;
(2)用表示摩尔分数,证明xi = ν i V总
(3)证明
μ2
3kT
=
M
证明:(1)PV=nRT
当 p 和 T 一定时,气体的 V 和 n 成正比
同?为什么愚人金有金的光泽?为什么 ZnS(闪锌矿)呈白色﹑ HgS(朱砂)呈红色而 PbS(方铅矿) 呈黑色?天然的金刚石为什么有蓝﹑红﹑黄﹑绿色而并非全呈无色?请阅读:拿骚.颜色的物理和化学. 科学出版社,1991,168~ 182(注:“费密能”的定义在 166 页上)。请通过阅读测试一下自己的知识和 能力,以调整自己的学习方法预定目标与学习计划安排。最好阅读后写一篇小文(主题任选)。 12、解:金属键的另一种理论是能带理论。能带理论是分子轨道理论的扩展,要点有: (1)能带中的分子轨道在能量上是连续的。 (2)按能带填充电子的情况不同,可把能带分为满带、空带和导带三类。 (3)能带和能带之间存在能量的间隙,简称带隙,又称禁带宽度。 (4)能带理论能够对金属导电进行解释。 (5)能带理论是一种既能解释导体,又能解释半导体和绝缘体性质的理论。 (6)由此可见,按照能带理论,带隙的大小对固体物质的性质至关重要。 3-13 二层﹑三层为一周期的金属原子二维密置层的三维垛积模型只是最简单的当然也就是最基本的金 属堆积模型。利用以下符号体系可以判断四层﹑五层为一周期的密置层垛积模型是二层垛积和三层垛积 的混合:当指定层上下层的符号(A﹑B﹑C)相同时,该指定层用 h 表示,当指定层上下层的符号不相 同时,该指定层用 c 表示。用此符号体系考察二层垛积,得到…hhhhhh …,可称为 垛积,用以考察 三层垛积时,得到…cccccc…,可称为 c 堆积。请问:四层﹑五层为一周期的垛积属于什么垛积型?为 什么说它们是二层垛积和三层垛积的混合?(注: h 是六方——hexagonal ——的第一个字母;c 是 立方——cubic ——的第一个字母。) 13﹑解:四面垛积是…hchchch…,即 hc 垛积型,说明六方垛积和立方垛积各占 50%;五 层垛积是…hhccchhccchhccc…,即 hhccc 垛积型,说明六方垛积和立方垛积分别占 2/5 和 3/5。 3-14 温度足够高时,某些合金晶体中的不同原子将变的不可区分,Cu3Au 晶体中各原子坐标上铜原子和 金原子可以随机地出现。问:此时,该合金晶胞是什么晶胞? 14﹑解:面心立方晶胞。 3-15 温度升得足够高时,会使某些分子晶体中原有一定取向的分子或者分子中的某些基团发生自由旋 转。假设干冰晶体中的二氧化碳分子能够无限制地以碳原子为中心自由旋转,问:原先的素立方晶胞将 转化为什么晶胞? 15﹑解:面心立方晶胞。 3-16 试在金属密堆积的面心立方晶胞的透视图上画出一个二维密堆积层,数一数,在该密堆积层上每个 原子周围有几个原子,在该原子的上下层又分别有几个原子?(参考 3-54) 16﹑解:6;3。参考图解如图 3-53。 3-17 找一找,在六方最密堆积的晶胞里,四面体空隙和八面体空隙在哪里?已知纤维锌矿(ZnS)的堆 积填隙模型为硫离子作六方最密堆积,锌离子作四面体填隙,请根据以上信息画出其晶胞。 17﹑解:见:周公度.结构和物性.高等教育出版社,1993,274~293 3-18 有一种典型离子晶体结构叫做ReO3 型,立方晶胞,Re6+ 的坐标为 0,0,0;O2- 的坐标为 0,1/2, 0;1/2,0,0;0,0,1/2。请问:这种晶体结构中,铼的配位数为多少?氧离子构成什么多面体?如何 连接? 18﹑解:Re 的配位数为 6;八面体;全部以顶角相连。 3-19 实验测得金属钛为六方最密堆积结构,晶胞参数为 a=295.0,c=468.6pm ,试求钛的原子半径和密 度。 19、解:晶胞体积:V=abcsin120°=295.0×295.0×468.6×0.866×10-24= 3.53×10-16
无机材料物理化学课后习题与答案

第一章几何结晶学基础1-1.晶体、晶胞的定义;空间格子构造的特点;晶体的基本性质。
1-2.参网页上的模型,运用对称要素组合定律,写出四方柱、六方柱、四方四面体、斜方双锥、六八面体、三方柱、复三方三角面体、四六面体的点群符号,并写出其所属的晶系和晶族。
1-3.参阅网页上的模型,请确定单型中的六八面体、复三方偏三角面体、复六方双锥、和聚型中2、3、4号模型在晶体定向中,各晶体的晶轴分别与哪些对称轴重或晶棱方向平行?1-4.请写出单型三方柱、四方柱、四方双锥、六方柱、菱面体、斜方双锥各晶面的主要晶面符号。
1-5.请写出下列聚型模型各晶面的晶面符号:1、2、3、4。
两个对称面相互成1)60°、2)90°、3)45°、4)30°,可组合成什么点群?1-6.由两根相交的二次轴互成1)90°、2)60°、3)45°、4)30°,可以组合成什么点群?试在面心立方格子中画出菱面体格子1-7.一晶面在X、Y、Z轴分别截得2、4、6个轴单位,请写出此晶面符号。
1-8.作图表示立方晶体的(123)、(012)、(421)晶面。
1-9.在六方晶体中标出晶面(0001)、(2110)、(1010)、(1120)、(1210)的位置。
1. 答:晶体最本质的特点是其部的原子、离子、或原子集团在三维空间以一定周期性重复排列而成, 晶体的空间格子构造有如下特点:结点空间格子中的点,在实际晶体中它们可以代表同种质点占有的位置,因此也称为晶体结构中的等同点位置。
行列结点在一维方向上的排列 . 空间格子中任意两个结点连接的方向就是一个行列方向。
面网结点在平面上的分布构成面网。
空间格子中,不在同一行列上的任意三个结点就可联成一个面网。
平行六面体空间格子中的最小单位。
它由六个两两平行且大小相等的面组成。
晶体的基本性质是指一切晶体所共有的性质,这些性质完全来源于晶体的空间格子构造。
大学本科无机化学 第十章 固体结构

能带理论 能带理论把金属晶体看成为一个大分子。 这个分子由晶体中所有原子组合而成。以Li 这个分子由晶体中所有原子组合而成。以Li 为例,Li原子有1s,2s两个轨道,两个Li原 为例,Li原子有1s,2s两个轨道,两个Li原 子有2 1s, 子有2个1s,2个2s轨道。按MO法,两个原子 2s轨道。按MO法,两个原子 相互作用时原子原子轨道重叠,形成成键轨 道和反键轨道,这样由原来的原子能量状态 变成分子能量状态。晶体中包含原子数愈多, 分子状态也愈多。分子轨道如此之多,分子 轨道之间的能级差就很小,可看作连成一片 成为能带。能带可看成是延伸到整个晶体的 分子轨道。
α
(8 e )(9~17e )(18 e )(18+2 e ) 大 小
−
−
−
−
影响离子极化力f 影响离子极化力f 的相关因素
① Z高, +小,f 大 R ② Z相同, +相近,与电子构型有关。 Z R (8 e )(9~17 e )(18 e )(18+2 e ) 大 f 小
− − − −
离子间的极化作用
1 Na :12× +1 = 4个 4
+
1 1 Cl : 8× + 6× = 4个 8 2
−
2、CsCl型(简单立方晶格) CsCl型 简单立方晶格)
8:8配位 8:8配位
Cs :1个
+
1 Cl : 8× =1个 8
-
3、ZnS型(面心立方晶格立方) ZnS型 面心立方晶格立方)
4:4配位 4:4配位
R+ / R− = 0.414
半径比规则:
最理想的稳定结构(NaCl)
R+ / R−
北师大《无机化学》第四版习题答案10

第十章沉淀溶解平衡10-1 (1)解:P b i2(s)=p b2+(aq)+2I-(aq)设溶解度为S.则:k sp(I2) =S×(2S)2=4S3=4×(1.29×10-3)3=8.6×10-9(2)解:溶解度S=2.91×10-3/253=1.15×10-5BaCrO4(s)=Ba2++CrO42- (BaCrO4)=S2 =(1.15×10-5)2 =1.32×10-10 10-2 .(1) Zn(OH)2(s)=Zn2++2OH-K sp (Zn(OH)2)=S×(2S)2=4S3=4.12×10-17S*=2.18×10-6=2.17×10-4g/L(2) 解:P b (s)=P b2++2F-K sp(PbF2(s))=S*×(2S*)2=4S3=7.12×10-7S*=2.61 mol/L=6.39 g/L10-3 (1) 解:设AgIO3溶解度为S1, 设Ag2CrO4溶解度为S2, 则: AgIO3(s)=Ag++ IO3-K sp(AgIO3)=S1× S1=S12S1=( K sp(AgIO3)) 1/2=(9.2×10-9) 1/2=9.59×10-5 mol/L.Ag2CrO4(s)=2Ag ++ CrO42—K sp(Ag2CrO4)=(2S2) S2=4S23S2=( K sp(Ag2CrO4)/4) 1/3=(1.12×10-12/4) 1/3=6.54×10-5 mol/L(2)解:设AgIO3溶解度为S1, 设Ag2CrO4溶解度为S2, 则:AgIO3(s)=Ag++ IO3-S1 S1S1+0.01S1K sp(AgIO3)=(S1+0.01)× S1=0.01×S12=9.2×10-9Ag2CrO4(s)=2Ag ++ CrO4—2S2 S22S2+0.01S2K sp(Ag2CrO4)=(2S2+0.01)× S2=0.01×S22=1.12×10-12S2=1.12×10-8 mol/L∴S1>S2AgIO3在0.01 mol*L-1的AgIO3溶液中的溶解度大10-4(1)解:沉淀Ca2+:[SO42-]1=K sp(CaSO4)/ [Ca2+]=7.1×10-5/0.01=7.1×10--3沉淀Ba2+:[SO42-]2=K sp(BaSO4)/ [Ba2+]=1.07×10-10/0.01=1.07×10-8=1.07×10-10/0.01/7.1×10-5/0.01=1.5×10--8 mol/L﹤1×10-5用Na2 SO4作沉淀剂能将Ca2+与Ba2+分离(2) 解:n(SO 42-)=100×10-3 ×0.01=1×10-3 mol/L∴ m(Na 2 SO 4) =142×1×10-3=0.142(g)∴加入0.142 g Na 2 SO 4才能达到BaSO 4完全沉淀的要求10-5解:C(MgCl 2) =10×0.1/20=0.05 mol/LC(NH 3.H 2O) =10×0.01/20=0.005∴C(Mg 2+)=0.05 mol/L∝C(NH 3)/K b =0.005/1.774×10-5=281﹤500 [OH -]=1.774×10-5+(3.147×10-10+3.548×10-10) =2.89×10-4 mol/LJ =C(Mg 2+)×C(OH -)2=0.05×(2.89×10-4)2 =4.81×10-9﹥K sp(Mg(OH)2)=5.61×10-12 ∴有Mg(OH)2沉淀生成 10-6解:沉淀Fe 3+[OH -]=( K sp(Fe(OH)3)/ [Fe 3+])1/3=(2.64×10-39/0.05) 1/3=3.75×10-13 mol/L 沉淀Fe 2+[OH -]=( K sp(Fe(OH)2)/ [Fe 2+])1/2=(4.87×10-17/0.05) 1/2 =3.12×10-8 mol/L当Fe 3+沉淀完全时,[Fe 3+]=10-5 mol ·L -1[OH -]完全=(2.64×10-39/10-5)1/3=6.42×10-12 mol ·L-1∴pH 完全=14-12+0.8=2.8 ∴pH 开始=14-8+0.5=6.5 ∴pH 的范围为2.8~6.510-7在10mL 0.201-⋅L mol 溶液中加入10mL 含的0.010氨水溶液,计算含多少克CL NH 4才不至于生成()2OH Mn 沉淀?[]1210.0-+⋅=Lmol Mn[]5310*8.1*10*10*01.0--=OH =410*42.0-离子积Q=[][]22-+OH Mn =1010*8.1-()[]13210*06.2-=OH Mn K sp θQ >>SP k 有沉淀生成要使不析出沉淀,应加抑制3NH 电离。
大连理工大学无机化学教研室《无机化学》(第5版)(课后习题详解 固体结构)

10.2 课后习题详解1. 填充下表:解:根据已知条件可得表10.1:表 10.12.根据晶胞参数,判断下列物质各属于何种晶系?解:根据已知条件可得表10.2:表 10.23. 根据离子半径比推测下列物质的晶体各属何种类型。
解:上述物质都为AB 型离子键化合物,在不考虑离子极化的前提下,晶体的离子半径比与晶体构型的关系为:+-r r 当=0.225~0.414时,晶体为ZnS 型;+-r r =0.414~0.732时,晶体为NaCl 型;+-r r =0.732~1.000时,晶体为CsCl型。
+-r r4. 利用Born-Haber 循环计算NaCl 的晶格能。
解:设计循环如下:5. 试通过Born-Haber 循环,计算MgCl 2晶格能,并用公式计算出晶格能,再确定两者符合程度如何(已知镁的I 2为1457 kJ•mol -1)。
解:设计的循环如下:则通过Born-Haber 循环,计算MgCl 2晶格能为:用公式计算出晶格能为:通过比较两种方法计算出的晶格能大小,可见用两种方法计算的结构基本相符。
6. KF 晶体属于NaCl 构型,试利用公式计算KF 晶体的晶格能。
已知从Born-Haber 循环求得的晶格能为802.5 kJ•mol -1。
比较实验值和理论值的符合程度如何。
解:根据题意可知,晶体属于构型,即离子晶体构型,故查表可知KF NaCl 。
1.748A =又因为,,所以1(79)82n =+=0()()133136269R r K r F pm pm pm +-=+=+=与Born-Haber 循环所得结果相比,误差为7. 下列物质中,何者熔点最低?解:一般情况下,离子晶体的晶格能越大,则其熔点越高。
影响晶格能的因素很多,主要是离子的半径和电荷。
电荷数越大,离子半径越小,其晶格能就越大,熔点越高。
所以的熔点最低。
KBr8. 列出下列两组物质熔点由高到低的次序。
解:两组离子晶体的熔点顺序由高到低分别为:9. 指出下列离子的外层电子构型属于哪种类型解:根据外层电子的排布规则可得:10. 指出下列离子中,何者极化率最大。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第十章固体结构之课后习题参考答案
7解:最低的为KBr。
因为它们均为离子晶体,其离子所带电荷越高,离子半径越小,离子键越强,即晶体熔点就越高。
MgO中正负离子均带2个电荷,离子键最强,而1价离子中,KBr的正负离子半径之和最大,则离子键最弱,熔点最低。
8解:(1)熔点:NaF>NaCl>NaBr>NaI。
因为阳离子相同时,阴离子从F-→I-离子半径增大,则离子键依次减弱,熔点也依次减弱。
(2)MgO>CaO>SrO>BaO。
原因同(1)。
9解:(1):8e-;(2)(9-17)e-:(3)(18+2)e-;(4)18e-
10解:(2)的。
因阴离子的极化率大于阳离子的,而体积越大,阴离子的极化率也越大。
11解:(4)>(3)>(1)>(2).因阳离子的电荷越高,半径越小,即Z/r值越大,其离子极化作用就越强。
13解:(1)色散力;(2)色散力;(3)取向力,诱导力,色散力,氢键;(4)取向力,诱导力,色散力;(5)色散力;(6)色散力;(7)取向力,诱导力,色散力。
14解:不含氢键的有:(1)和(2)。
15解:(1)两者均为分子晶体,但因HF中存在分子间氢键,增大了分子间作用力,使其沸点反高于HCl。
(2)两者均为典型的离子晶体,而离子晶体当电荷相同时,离子半径越小,其离子键越强,晶体的沸点就越高,所以NaCl的沸点高于CsCl。
(3)因Ti4+离子所带电荷高,离子半径又小,即Z/r值非常大,其极化作用很强,导致Ti-Cl 之间由离子键转化为了共价键,成为分子晶体,所以其沸点大大低于离子晶体LiCl。
(4)两者均为分子晶体,且分子量也相同。
但沸点相差较大。
这是因为乙醇分子(后者)之间存在分子间氢键,增大了分子间的作用力导致。
16解:因Ag+为18e电子构型的离子,其极化作用和变形性均大,而阴离子的半径从F-到I-依次增大,变形性也依次增加,导致Ag+与X-离子之间的极化作用从AgF到AgI依次增强,化学键从离子键逐步向共价键过渡,所以溶解度依次减小,即AgF易溶,其它难溶,且溶解度依次减小。
17解:(1)NaCl的沸点最高。
因其为离子晶体,沸点高。
而Na因金属键较弱,沸点较低。
(2)CaF2的溶解度最小。
因它们全为离子晶体,其离子键越强,打断所需能量高,则溶解度越小。
而CaF2的Z/r值最大,离子键最强,所以溶解度最小。
(3)H2O的气化热最大。
因它们均存在分子间的作用力,但H2O分子间还有氢键存在,增大了分子间的作用力,使其的气化热最大。
(4)CO2的熔化焓最小。
因SiO2为原子晶体,熔点非常高,MgO为离子晶体,熔点也高。
H2O和CO2为分子晶体,熔点低。
但CO2为非极性分子,分子间只有色散力,所以熔化焓最小。
1。
