b二羰基化合物.ppt
合集下载
二羰基化合物

2 CH3(CH2)3CO2C2H5
NaOC2H5
CH3(CH2)3COCHCO2C2H5 CH2CH2CH3 O CH3CH2CHC CH3 CH3 C CO2C2H5 CH2CH3
2 CH3CH2CHCO2C2H5 CH3
Ph3C Na
?
①亲核试剂生成 ②亲核加成
③消除
结果
复习第13章的内容——酰基上的亲核取代
苯甲酰乙酸乙酯
分子内酯缩合——Dieckmann (狄克曼)反应
二元酸酯若分子中的酯基被四个以上的碳原子隔 开时,就发生分子中的酯缩合反应,形成五员环或更 大环的酯,这种环化酯缩合反应称为狄克曼酯缩合。
CH2CH2COOC2H5 CH2CH2COOC2H5 O
(1) NaOC2H5, C6H6, 80℃ (2) H3O+, 80%
OC2H5
取代丙酮 (甲基酮)
乙酰乙酸乙酯
(1) 稀OH (2) H ,
+
CH2 R
实验条件较温 和,产率较好.
应用 1:制备取代丙酮(甲基酮)类化合物
O OC2H5 O OC2H5 R O H3C R
O H3C
R X NaOEt H3C
O
(1) 稀 OH (2) H+,
互变异构
OH H3C C CH 76%
O C CH3
O C H O C C H
O C OC2H5
C CH2 C
分子内氢键
烯醇式的特征:IR: 有OH吸收峰,1H NMR: 有OH和烯质子信号, 化学试验:与FeCl3显色
但下面的烯醇式存在
为什么乙酰乙酸乙酯是由酮式和烯醇式两种互 变异构体组成的? 因为,其烯醇式结构有一定的稳定性:
有机化学14章-二羰基

1) H2O, KOH; 2) H3O+
3)
I
CH3COCHCOOC 2H 5
2 CH3COCHCOOC2H5 Na+
-
CH3COCH2CH2COCH3 2, 5 – 己二酮
-
CH2Cl2
CH3COCHCOOC2H5 CH2 CH3COCHCOOC2H5 1) H2O, KOH; 2) H3O+
O C 6H 5C O E t O
4 种产物
-氢的酯分子
+ 不含-氢的酯
O O
+
C H 3C H 2C O E t
1) NaOEt, EtOH 2) H3O
+
C6H5CCHCOEt CH3
O O EtO C
O OEt
O O EtO C
O OEt
C OEt + CH3 C
C CH2 C
二、乙酰乙酸乙酯的合成及应用
成酮水解 CH3 CH3COCCOOC2H5 CH2CH2CH3 成酸水解
CH3COCH CH3
CH2CH2CH3
CH3 CH3CH2CH2CHCOOH
先大后小, 先惰后活
2)制备各种二酮
2 CH3COCHCOOC2H5 Na+
CH3COCHCOOC2H5
-
I I - NaI
CH3COCHCOOC2H5 CH3COCHCOOC2H5
第十四章 β-二羰基化合物
酮-烯醇互变异构
乙酰乙酸乙酯的合成及其应用
丙二酸酯的合成及其应用 Knoevenagel 缩合 Michael 加成
其它含活泼亚甲基的化合物
一、酮-烯醇互变异构
分子中含有两个羰基的化合物称为二羰基化合物,而两个羰 基中间被一个碳原子隔开的化合物称为β-二羰基化合物。此处 羰基的含义较广,包含简单的羰基也包括酯基等.
3)
I
CH3COCHCOOC 2H 5
2 CH3COCHCOOC2H5 Na+
-
CH3COCH2CH2COCH3 2, 5 – 己二酮
-
CH2Cl2
CH3COCHCOOC2H5 CH2 CH3COCHCOOC2H5 1) H2O, KOH; 2) H3O+
O C 6H 5C O E t O
4 种产物
-氢的酯分子
+ 不含-氢的酯
O O
+
C H 3C H 2C O E t
1) NaOEt, EtOH 2) H3O
+
C6H5CCHCOEt CH3
O O EtO C
O OEt
O O EtO C
O OEt
C OEt + CH3 C
C CH2 C
二、乙酰乙酸乙酯的合成及应用
成酮水解 CH3 CH3COCCOOC2H5 CH2CH2CH3 成酸水解
CH3COCH CH3
CH2CH2CH3
CH3 CH3CH2CH2CHCOOH
先大后小, 先惰后活
2)制备各种二酮
2 CH3COCHCOOC2H5 Na+
CH3COCHCOOC2H5
-
I I - NaI
CH3COCHCOOC2H5 CH3COCHCOOC2H5
第十四章 β-二羰基化合物
酮-烯醇互变异构
乙酰乙酸乙酯的合成及其应用
丙二酸酯的合成及其应用 Knoevenagel 缩合 Michael 加成
其它含活泼亚甲基的化合物
一、酮-烯醇互变异构
分子中含有两个羰基的化合物称为二羰基化合物,而两个羰 基中间被一个碳原子隔开的化合物称为β-二羰基化合物。此处 羰基的含义较广,包含简单的羰基也包括酯基等.
第14章β-二羰基化合物

(1)乙酰乙酸乙酯的制备 乙酰乙酸乙酯的制备
的酯在强碱 有α-H的酯在强碱(一般是用乙醇钠)的作用下与另一分子酯 的酯在强碱(一般是用乙醇钠)的作用下与另一分子酯 发生缩合反应,失去一分子醇 生成β-羰基酯 一分子醇, 羰基酯的反应叫做酯 发生缩合反应,失去一分子醇,生成 羰基酯的反应叫做酯 缩合反应,又称为克莱森( 缩合反应,又称为克莱森(Claisen)缩合。 )缩合。
有机化学
上页 下页
重要β 二羰基化合物 重要 –二羰基化合物
O O C 2 H 5 O-C-CH 2 -C-OC 2 H 5
丙二酸二乙酯
O O CH3-C CH2-C-OC2H5
乙酰乙酸乙酯
有机化学
上页
下页
三、 丙二酸酯在有机合成上的应用
一.丙二酸二乙酯的制备 丙二酸二乙酯的制备
O O O O NaCN C H OH CH2-C-OH CH2-C-ONa 2 5 C2H5O-C-CH2-C-OC2H5 OH H2SO4 Cl CN
OH O CH3-C=CH-C-OC H5 2 烯醇式 (7%)
有机化学
上页
下页
二、 β –二羰基化合物碳负离子的反应 二羰基化合物碳负离子的反应
碳负离子是带部分负电荷的碳原子或氧原子, 碳负离子是带部分负电荷的碳原子或氧原子,都具 是带部分负电荷的碳原子或氧原子 亲核性, 有亲核性,在碳原子和氧原子上都有可能发生亲核 反应,主要发生在碳原子上 常见的反应有下列几种: 在碳原子上。 反应,主要发生在碳原子上。常见的反应有下列几种: (1)碳负离子与卤代烷的反应 卤代烷的反应 )碳负离子与卤代烷 羰基化合物的缩合反应 (2)碳负离子和羰基化合物的缩合反应 )碳负离子和羰基化合物 不饱和羰基化合物的共轭加成 (3)碳负离子和 ,β-不饱和羰基化合物的共轭加成 )碳负离子和α, 不饱和 反应
的酯在强碱 有α-H的酯在强碱(一般是用乙醇钠)的作用下与另一分子酯 的酯在强碱(一般是用乙醇钠)的作用下与另一分子酯 发生缩合反应,失去一分子醇 生成β-羰基酯 一分子醇, 羰基酯的反应叫做酯 发生缩合反应,失去一分子醇,生成 羰基酯的反应叫做酯 缩合反应,又称为克莱森( 缩合反应,又称为克莱森(Claisen)缩合。 )缩合。
有机化学
上页 下页
重要β 二羰基化合物 重要 –二羰基化合物
O O C 2 H 5 O-C-CH 2 -C-OC 2 H 5
丙二酸二乙酯
O O CH3-C CH2-C-OC2H5
乙酰乙酸乙酯
有机化学
上页
下页
三、 丙二酸酯在有机合成上的应用
一.丙二酸二乙酯的制备 丙二酸二乙酯的制备
O O O O NaCN C H OH CH2-C-OH CH2-C-ONa 2 5 C2H5O-C-CH2-C-OC2H5 OH H2SO4 Cl CN
OH O CH3-C=CH-C-OC H5 2 烯醇式 (7%)
有机化学
上页
下页
二、 β –二羰基化合物碳负离子的反应 二羰基化合物碳负离子的反应
碳负离子是带部分负电荷的碳原子或氧原子, 碳负离子是带部分负电荷的碳原子或氧原子,都具 是带部分负电荷的碳原子或氧原子 亲核性, 有亲核性,在碳原子和氧原子上都有可能发生亲核 反应,主要发生在碳原子上 常见的反应有下列几种: 在碳原子上。 反应,主要发生在碳原子上。常见的反应有下列几种: (1)碳负离子与卤代烷的反应 卤代烷的反应 )碳负离子与卤代烷 羰基化合物的缩合反应 (2)碳负离子和羰基化合物的缩合反应 )碳负离子和羰基化合物 不饱和羰基化合物的共轭加成 (3)碳负离子和 ,β-不饱和羰基化合物的共轭加成 )碳负离子和α, 不饱和 反应
第14章-β-二羰基化合物

3.通过乙酰乙酸乙酯(Claisen酯缩合反应制备)的烷 基化和酰基化反应产物的酮式分解或酸式分解,可制 备甲基酮、二酮以及一元或二元羧酸.
4. -二羰基化合物的碳负离子通过Michael加成反应合 成1,5-二羰基化合物.
酮 -H活泼
◆常用丙酮或其他甲基酮和酯缩合来合成 -二酮。 比较克莱森(酯)缩合反应与羟醛缩合 反应的异同?
(5)克诺文格尔缩合反应 *——制备,-不饱和酸
◆醛、酮可以和-二羰基化合物(一般是丙二酸及其 衍生物),在弱碱(氨或胺)作用下缩合:
亲核加成-消除
肉桂酸 ◆这种制备制备,-不饱和酸的方法叫Knoevenagel
CH3COCHCOOC2H(C5 H2)2
CH3CO(CH2)4COCH3
CH3COCHCOOC2H5
用三乙法合成:
1,3-丁二烯与Br2的 1,4加成, 氢化.
与无-H的醛缩合
(6) 与酰卤或酸酐作用——羰基亲核加成-消除反应 例如:与酰氯的反应
NaH
非质子溶剂
酰基化产物
-二酮
◆在合成上乙酰乙酸乙酯更多的用来合成酮类。 (合成羧酸时,常有酮式分解)
乙醇得到乙酰乙酸乙酯(-丁酮酸酯):
乙酰乙酸乙酯
◆凡有-H原子的酯,在乙醇钠或其他碱性催化剂(如氨 基钠)存在下,都能进行克莱森(酯)缩合反应。克莱 森(酯)缩合反应是合成-二羰基化合物的方法。
(2)克莱森(酯)缩合反应历程——亲核加成-消除
乙酸乙酯 加成步骤 消除过程
(3)含有-H原子的酯与无-H原子的酯之间缩合 ①与苯甲酸酯缩合——位引入苯甲酰基 例如:-苯甲酰丙酸乙酯的合成
◆分子中含有两个羰基官能团的化合物叫二羰基化合物; 其中两个羰基为一个亚甲基相间隔的化合物叫-二羰 基化合物。
4. -二羰基化合物的碳负离子通过Michael加成反应合 成1,5-二羰基化合物.
酮 -H活泼
◆常用丙酮或其他甲基酮和酯缩合来合成 -二酮。 比较克莱森(酯)缩合反应与羟醛缩合 反应的异同?
(5)克诺文格尔缩合反应 *——制备,-不饱和酸
◆醛、酮可以和-二羰基化合物(一般是丙二酸及其 衍生物),在弱碱(氨或胺)作用下缩合:
亲核加成-消除
肉桂酸 ◆这种制备制备,-不饱和酸的方法叫Knoevenagel
CH3COCHCOOC2H(C5 H2)2
CH3CO(CH2)4COCH3
CH3COCHCOOC2H5
用三乙法合成:
1,3-丁二烯与Br2的 1,4加成, 氢化.
与无-H的醛缩合
(6) 与酰卤或酸酐作用——羰基亲核加成-消除反应 例如:与酰氯的反应
NaH
非质子溶剂
酰基化产物
-二酮
◆在合成上乙酰乙酸乙酯更多的用来合成酮类。 (合成羧酸时,常有酮式分解)
乙醇得到乙酰乙酸乙酯(-丁酮酸酯):
乙酰乙酸乙酯
◆凡有-H原子的酯,在乙醇钠或其他碱性催化剂(如氨 基钠)存在下,都能进行克莱森(酯)缩合反应。克莱 森(酯)缩合反应是合成-二羰基化合物的方法。
(2)克莱森(酯)缩合反应历程——亲核加成-消除
乙酸乙酯 加成步骤 消除过程
(3)含有-H原子的酯与无-H原子的酯之间缩合 ①与苯甲酸酯缩合——位引入苯甲酰基 例如:-苯甲酰丙酸乙酯的合成
◆分子中含有两个羰基官能团的化合物叫二羰基化合物; 其中两个羰基为一个亚甲基相间隔的化合物叫-二羰 基化合物。
第十四章_β-二羰基化合物
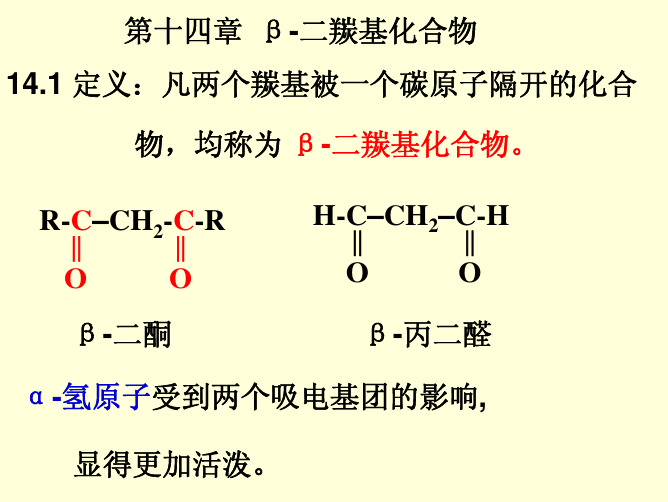
第十四章 β-二羰基化合物 14.1 定义:凡两个羰基被一个碳原子隔开的化合
物,均称为 β-二羰基化合物。
R-‖C–CH2-‖C-R
O
O
β-二酮
H-‖C–CH2–C‖-H
O
O
β-丙二醛
α-氢原子受到两个吸电基团的影响,
显得更加活泼。
14.2 命名
HO-‖C–CH2-‖C-OH
O
O
β- 丙二酸
R-‖C–CH2–C‖-OR’
CH3︱CH=CH‖COC2H5 OH O
NaOC2H5 H+
CH3‖C CH-‖COC2H5 OO
Na
+
CH3‖CCH2C‖OC2H5 OO
①5%NaOH CH3COCH2COOH
②H+
CH3COCH3
△,-CO2
?
CH3‖CCH2C‖OC2H540%△NaOH OO
CH3‖COON+a
C2H5OH
CH3‖CO︱CCHH‖O2CCOHC2C2HO①5O5C%2H︱CNHaO2CHH2CCHO3‖OCO︱CCHHH2‖OCCOHN2CaOONa ②H+ , ③△ CH3‖CCH2
O
CH3‖C︱CCHH‖2CCOHC2C2HO5OC酮2式H 分解 OO
C︱H2CH2COOH CH3‖CCH2
O
︱CH2CH2COO酸C2式H分5 解
CH3‖CCH2C‖OC2H5 OO
H2N-OH H+
CH3‖CCH2COOC2H5 N-OH
Na CH3︱C= CH ‖COC2H5 ONa O
CH3︱C = CHC‖OC2H5 OH O
+ H2
CH3‖C-CH-‖COC2H5Na +
物,均称为 β-二羰基化合物。
R-‖C–CH2-‖C-R
O
O
β-二酮
H-‖C–CH2–C‖-H
O
O
β-丙二醛
α-氢原子受到两个吸电基团的影响,
显得更加活泼。
14.2 命名
HO-‖C–CH2-‖C-OH
O
O
β- 丙二酸
R-‖C–CH2–C‖-OR’
CH3︱CH=CH‖COC2H5 OH O
NaOC2H5 H+
CH3‖C CH-‖COC2H5 OO
Na
+
CH3‖CCH2C‖OC2H5 OO
①5%NaOH CH3COCH2COOH
②H+
CH3COCH3
△,-CO2
?
CH3‖CCH2C‖OC2H540%△NaOH OO
CH3‖COON+a
C2H5OH
CH3‖CO︱CCHH‖O2CCOHC2C2HO①5O5C%2H︱CNHaO2CHH2CCHO3‖OCO︱CCHHH2‖OCCOHN2CaOONa ②H+ , ③△ CH3‖CCH2
O
CH3‖C︱CCHH‖2CCOHC2C2HO5OC酮2式H 分解 OO
C︱H2CH2COOH CH3‖CCH2
O
︱CH2CH2COO酸C2式H分5 解
CH3‖CCH2C‖OC2H5 OO
H2N-OH H+
CH3‖CCH2COOC2H5 N-OH
Na CH3︱C= CH ‖COC2H5 ONa O
CH3︱C = CHC‖OC2H5 OH O
+ H2
CH3‖C-CH-‖COC2H5Na +
第十五章 β-二羰基化合物

OH 90.0%
CH3 C CH2 C C6H5
CH3 C CH C C6H5
后三种具酮羰基性质, 后三种具酮羰基性质,如与 性质 具烯醇性质。如与 反应生成 具烯醇性质。如与Na反应生成 NH2OH、C6H5NHNH2等生 、 成肟、苯腙; 成肟、苯腙;与NaHSO3、 HCN等发生亲核加成反应; 等发生亲核加成反应; 等发生亲核加成反应 被还原成β-羟基酸酯 被还原成 羟基酸酯 紫红色 RONa;与PCl5作用生成 氯-2; 作用生成3-氯 丁烯酸乙酯, 丁烯酸乙酯,使Br2/CCl4溶液迅 速褪色; 速褪色;与FeCl3溶液作用呈现
O O O + CH3C CH C OC2H5 Na + Br CH2 C OC2H5 O O
CH3 C CHC OC2H5 CH2COOC2H5
酮 酸 分酸
O CH3C CH2CH2COOH
O 丙 酸 分酸
O OH
HO C CH2 CH2 C
④合成一元羧酸 如上述合成的α-丙基乙酰乙酸乙酯中间体进行酸式分解 丙基乙酰乙酸乙酯中间体进行酸式分解: 如上述合成的 丙基乙酰乙酸乙酯中间体进行酸式分解:
第十五章 β-二羰基化合物 羰基化合物
1. β-二羰基化合物 的互变异构 二羰基化合物 2.克莱森 克莱森(Claisen)酯缩合反应 克莱森 酯缩合反应 3.乙酰乙酸乙酯的性质及应用 乙酰乙酸乙酯的性质及应用
★
4.丙二酸二乙酯的性质及其应用 丙二酸二乙酯的性质及其应用 5.Knoevenagel (柯诺瓦诺格 缩合 柯诺瓦诺格)缩合 柯诺瓦诺格
5%NaOH
CH3COCH2COOC2H5
H
+
CH3COCH2COONa CH3COCH3 + CO2
第十四章 β-二羰基化合物

第十四章 β-二羰基化合物
(一) 命名下列化合物:
CH3 (1) HOCH2CHCH2COOH
(3) CH3CH2COCH2CHO
O (2) (CH3)2CHCCH2COOCH3
OH (4) (CH3)2C=CHCH2CHCH3
CHO
(5) ClCOCH2COOH
(7)
OCH3 NO2
OCH3 (6) OH
O
O
CH3C CH2C OC2H5 ( 以下同)
来自三乙 (1) 分析:
O
H3C C CH CH3
CH3
上2个 CH3I
O CH3C
解:
O CH2C
OC2H5
C2H5O-Na+ CH3 I
O CH3C
O CHC CH3
OC2H5
C2H5O-Na+ CH3 I
O CH3C
CH3 O CC CH3
(1) 稀OH- , (2) H+, (3) ∆
OC2H5
酮式分解
O H3C C CH CH3
CH3
CH3OH HI CH3I
OH
CH3CHCH2CH2CH2CH3
H2 Ni
(2) 分析:
O CH3CCH2CH2CH2CH3
上BrCH2CH2CH3
来自三乙
O
O
OO
CH3C CH2COC2H5 C2H5O-Na+ CH3CH2CH2Br CH3C CHCOC2H5
CH3
来自丙二
CH2(COOC2H5)2 C2H5O-Na+
解:
CH3CH=CHCOOC2H5
CH3CH CH2COOC2H5 CH(COOC2H5)2
(一) 命名下列化合物:
CH3 (1) HOCH2CHCH2COOH
(3) CH3CH2COCH2CHO
O (2) (CH3)2CHCCH2COOCH3
OH (4) (CH3)2C=CHCH2CHCH3
CHO
(5) ClCOCH2COOH
(7)
OCH3 NO2
OCH3 (6) OH
O
O
CH3C CH2C OC2H5 ( 以下同)
来自三乙 (1) 分析:
O
H3C C CH CH3
CH3
上2个 CH3I
O CH3C
解:
O CH2C
OC2H5
C2H5O-Na+ CH3 I
O CH3C
O CHC CH3
OC2H5
C2H5O-Na+ CH3 I
O CH3C
CH3 O CC CH3
(1) 稀OH- , (2) H+, (3) ∆
OC2H5
酮式分解
O H3C C CH CH3
CH3
CH3OH HI CH3I
OH
CH3CHCH2CH2CH2CH3
H2 Ni
(2) 分析:
O CH3CCH2CH2CH2CH3
上BrCH2CH2CH3
来自三乙
O
O
OO
CH3C CH2COC2H5 C2H5O-Na+ CH3CH2CH2Br CH3C CHCOC2H5
CH3
来自丙二
CH2(COOC2H5)2 C2H5O-Na+
解:
CH3CH=CHCOOC2H5
CH3CH CH2COOC2H5 CH(COOC2H5)2
有机化学二羰基化合物
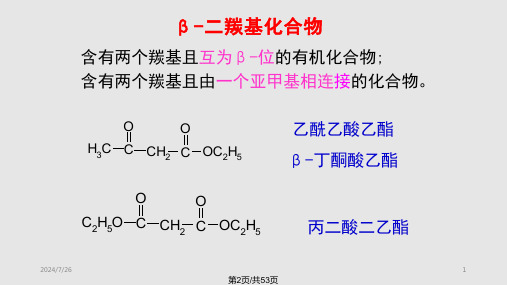
碳氧双键处于共轭体系,发生了电子的离域,使体
系能量降低而趋于稳定。
:OH
H3C C CH
O C OC2H5
2024/7/26
4
第5页/共53页
影响烯醇式含量的其它因素:
① 活泼亚甲基上连有吸电子基团,烯醇式含 量↑,连有供电子基团,烯醇式含量↓。
O
O
O
O
H3C
C
CH
C OC2H5 > H3C
C
CH2
2+
Hg
+
H
OH CH CH2
O CH3C H
β-二羰基化合物的烯醇式结构稳定性:乙酰乙酸乙酯
实验事实:
① 能与NaHSO3、HCN等发生加成反应; ② 能与羟胺、苯肼反应,生成肟、苯腙等; ③ 能被还原成β-羟基酸酯; ④ 经水解、酸化后,可以脱羧生成丙酮。
O
O
H3C C CH2 C OC2H5
有羰基
O CH3C CH
O COC2H5
Na+
Br(CH2)4Br
O CH3C
C2H5ONa
COCH3
成酮分解
COOC2H5
O CH COC2H5 CH2(CH2)3Br
O
CCH3
2024/7/26
28
第29页/共53页
② 制二酮
2024/7/26
制β-二酮(1,3-二酮)
O CH3C CH
O COC2H5
第11页/共53页
三、丙二酸二乙酯的合成及应用
1、丙二酸二乙酯的制法 2、丙二酸二乙酯在有机合成上的应用
① 制备烃基取代乙酸 ② 制备二元羧酸
2024/7/26
第14章 β-二羰基化合物(2012)

CO2H
Michael加成 加成
亲核取代 -CH(COOC H ) 2 5 2 亲 核加 成 (α,β-不饱和醛酮的亲核加成----Michael加成) 不 加
Michael加成是非常有用的合成 5—二羰基化合物的反应 加成是非常有用的合成1, 加成是非常有用的合成 二羰基化合物的反应
O CH2(COOC2H5)2 + NaOC2H5 HOC2H5 CH(COOC2H5)2 O - CO2 CH2COOH 90% 酸化 水解 CH(COOC2H5)2 OH
14.3 乙酰乙酸乙酯的反应及其在有机合成中的应用 乙酰乙酸乙酯的反应及其在有机合成中的应用
1. 乙酰乙酸乙酯的酯缩合逆反应 乙酰乙酸乙酯的酯缩合逆反应
O O
O-
O
CH3C-CH2-COC2H5
C2H5O-
CH3C-CH2-COC2H5 OC2H5
O CH3-COC2H5
O
+
-
CH2-COC2H5 O CH3-COC2H5
3. 乙酰乙酸乙酯的酸式分解 乙酰乙酸乙酯的酸式分解
OO-
O
O
CH3C-CH2-COC2H5
-OH(浓) (
CH3C-CH2-C-OC2H5 OH OH
O
O CH3-COH
+ -CH2-COH + C2H5OH2O H2用下, 在浓碱作用下,α−与β−位碳原子间断裂生成二分子羧酸。 位碳原子间断裂生成二分子羧酸。
生成的烯醇式稳定的原因 (1)形成共轭体系,降低了体系的内能 )形成共轭体系,
(2)烯醇结构可形成分子内氢键(形成较稳定的六元环体系) )烯醇结构可形成分子内氢键(形成较稳定的六元环体系)
苯酚的烯醇与酮式互换
第14章 β-二羰基化合物

CH3CCH2C-OH
CH3CCH2C-OH
十一、某酯类化合物A (C5H10O2),用乙醇钠的乙醇溶液处理,得到另一个 酯B (C8H14O3),B 能使溴水褪色,将B用乙醇钠的乙醇溶液处理后,再与碘 乙烷反应,又得到另一个酯C (C10H18O3). C和溴水在室温下不反应。把C用 稀碱水解再酸化,加热,即得一个酮D (C7H14O), D不发生碘仿反应。用锌 汞齐还原则生成3-甲基己烷,试推测A,B,C,D的结构,并写出各步反应式。 解:A,B,C,D的结构及各步反应式如下:
CH3CCH2C-OCH2CH3
ClCH2COOEt O O Cl2 , P ClCH2COOEt
CH3 C-CH-C-OCH2CH3 CH2 COOEt
CH3CCHC-OCH2CH3 + Na
4. 2,7-辛二酮
O O CH3CH2OH H+ CH2 = CH2 Cl2 O O + ClCH2 CH2Cl CH3CCHC-OCH2CH3 Na O O O CH3C-CH2 CH2 (1) 5 % NaOH (2) H
(A) CH3CH2COOEt C2 H5 (C) CH3CH2COCCOOEt CH3
(B) CH3 CH2COCHCOOEt CH3 C2 H5 (D) CH3CH2COCH CH3
CH3CH2 COOEt C2H5ONa
(A) C2 H5ONa
CH3CH2COCHCOOEt (B) CH3
Na CH3 CH2COCCOOEt CH3 C2H5I
(1) O 3 (2) Zn, H
5% NaOH
+
CHO CHCHCHO
∆
CHO
2
CH3COCH2 COO C2H5 NaOC2H5 CH3 Cl CHCOC2 H5
有机。第十四章 β –二羰基化合物

应用化学系
运城学院 若酯的α-碳上只有一个 ,则生成的β-羰基酯中 若酯的 碳上只有一个H,则生成的 羰基酯中 碳上只有一个 两个羰基之间的C原子上已无 原子, 原子上已无H原子 两个羰基之间的 原子上已无 原子,不能与碱作用 生成稳定的盐,反应便无法进行。必须用更强的碱, 生成稳定的盐,反应便无法进行。必须用更强的碱, 如三苯甲基钠为催化剂,使反应物全部生成α-负碳 如三苯甲基钠为催化剂,使反应物全部生成 负碳 离子,平衡向右,反应方能进行: 离子,平衡向右,反应方能进行:
O CH3 C CH2 RX CH3 O C OC2H5 NaOC 2H5 O CH3 C CH O C OC2H5
O R O C CH C OC2H 5 R'X CH3 O R O C C C OC2H 5 R' o
重复上述过程:
R,R'≠ 芳基、烯基(活性差)或3 (消除),最好为1o ≠
应用化学系
(β-diketone)
O RH 2C C R' keto form
β–二酮
(β-keto ester)
β–酮酸酯
丙二酸二酯 (malonic ester)
OH
§14.1 酮-烯醇互变异构(tautomerism ) 烯醇互变异构
互变 异构 RHC C R' enol form 应用化学系
运城学院 酸碱对酮-烯醇平衡的影响 §14.1.1 酸碱对酮 烯醇平衡的影响 酸、碱、玻璃都能催化酮式与烯醇式迅速达到平衡 酸催化 (acid-catalyzed): :
运城学院 §14.2.3 乙酰乙酸乙酯在合成上的应用 烃基化反应后进行酮式分解或酸式分解, 烃基化反应后进行酮式分解或酸式分解,可以 制备取代丙酮或取代乙酸。 制备取代丙酮或取代乙酸。
运城学院 若酯的α-碳上只有一个 ,则生成的β-羰基酯中 若酯的 碳上只有一个H,则生成的 羰基酯中 碳上只有一个 两个羰基之间的C原子上已无 原子, 原子上已无H原子 两个羰基之间的 原子上已无 原子,不能与碱作用 生成稳定的盐,反应便无法进行。必须用更强的碱, 生成稳定的盐,反应便无法进行。必须用更强的碱, 如三苯甲基钠为催化剂,使反应物全部生成α-负碳 如三苯甲基钠为催化剂,使反应物全部生成 负碳 离子,平衡向右,反应方能进行: 离子,平衡向右,反应方能进行:
O CH3 C CH2 RX CH3 O C OC2H5 NaOC 2H5 O CH3 C CH O C OC2H5
O R O C CH C OC2H 5 R'X CH3 O R O C C C OC2H 5 R' o
重复上述过程:
R,R'≠ 芳基、烯基(活性差)或3 (消除),最好为1o ≠
应用化学系
(β-diketone)
O RH 2C C R' keto form
β–二酮
(β-keto ester)
β–酮酸酯
丙二酸二酯 (malonic ester)
OH
§14.1 酮-烯醇互变异构(tautomerism ) 烯醇互变异构
互变 异构 RHC C R' enol form 应用化学系
运城学院 酸碱对酮-烯醇平衡的影响 §14.1.1 酸碱对酮 烯醇平衡的影响 酸、碱、玻璃都能催化酮式与烯醇式迅速达到平衡 酸催化 (acid-catalyzed): :
运城学院 §14.2.3 乙酰乙酸乙酯在合成上的应用 烃基化反应后进行酮式分解或酸式分解, 烃基化反应后进行酮式分解或酸式分解,可以 制备取代丙酮或取代乙酸。 制备取代丙酮或取代乙酸。
第十四章b二羰基化合物

O R' O
-NaX
CH3 C
C R
C
OC2H5
① R最好用1°,2°产量低,不能用3°和 乙烯式卤代烃(??碱性条件下)。
②二次引入时,第二次引入的R′要比R活泼。 (一般是体积先大后小)
③ RX也可是卤代酸酯和卤代酮。
(b) 酰基化:
OO CH3 C CH C OC2H5 Na
RCOX -NaX
2 CH3COOH + C2H5OH
OO CH3 C CH C OC2H5
ŨOH
CH3COOH + RCH2COOH + C2H5OH
R
OO
ŨOH
CH3 C CH C OC2H5
CH3COOH + RCOCH2COOH + C2H5OH
COR
14.3 丙二酸二乙酯
(1)制法:可以从氯乙酸的钠盐来制备丙二酸二乙酯。
H3C C
C C CH3 H
碳负离子和氧负离子都具有亲核性能,但反
应主要发生在亲核的碳原子上。
亚甲基活泼氢的性质:
1.酸性
α-H很活泼,具有一定的酸性,易与金属钠、乙醇 钠作用形成钠盐。
O
O
CH3 C CH2 C OC2H5 C2H5ONa
OO CH3 C CH C OC2H5 Na
Hale Waihona Puke pKa =1114.1.2 烯醇负离子的稳定性
乙酰乙酸乙酯:又叫β-丁酮酸乙酯。
以酮式和烯醇式两种结构以动态平衡而同时存在的互 变异构体。
1.互变异构现象
白() 白()
NaHSO3 OO
NH2OH CH3-C-CH2-C-OC2H5
Na H2 有活性氢 Br2/CCl4 溴褪色(具双键)
有机化学:β-二羰基化合物

第三节 丙二酸二乙酯的性质及其应用
丙二酸二乙酯为无色且具有香味的液体,沸点 199℃,微溶于水,能与醇、醚混溶,是重要的有机合 成中间体。 一、制法
N aC N
C 2H 5O HC O 2C 2H 5
C lC H 2C O 2H
C H 2C O 2N a
C H 2
N aO H C N
H 2S O 4 C O 2C 2H 5
CO2C2H5
1)OH-,H2O 2)H+;3)
RCHCO2H R'
一元羧酸
2、合成二元羧酸
C H 2 B r
C H 2 B r 2 [C H (C O 2 E t)2 ]-N a +
C H 2 C H (C O 2 E t)21 )O H -,H 2 OC H 2 C H 2 C O 2 H C H 2 C H (C O 2 E t)22 )H + ;3 ) C H 2 C H 2 C O 2 H
N a N H 2
R 'X
R CC H
R CC N a
R CC R '
N H 3 ( l )
(R’X:伯卤代烃)
炔烃
武慈反应
Na
2RX
R-R
对称烷烃
科里-豪思反应
1)L i
R 'X
R X
R 2C uL i
R -R '
2)C uI
付-克酰基化反应
对称或不对称烷烃
R C O C l A lC l3
C O R Z n -H g H C l
CH3C CH2 C ONa
O
O
H3O+
CH3C CH2 C OH
有机化学第十四章 β-二羰基化合物

CONR2,
烷基化反应:
CO2C2H5 (CH3)2CH I + CH2 CN
① C2H5ONa /C2H5OH ② (CH3)2CH I
① C2H5ONa /C2H5OH ② H 3O
+
CO2C2H5 CH(CH3)2 CN
(CH3)2CH C (95%)
Michael 加成反应:
CH3 CH2 C CN 2–甲基– 丙烯酸乙酯 氰基乙酸乙酯
3 2 5
C H2 C H3C O C HC O O2C H5 C H3C O C H 2C H2C H2C O C H 3
CH3COCH2COOC2H5
H5 (1)C2H5O Na C H3C O C HC O O2C (2) I2 酮式分解 C H3C O C HC O O2C H5 C H3C O C H 2C H2C O C H 3
O CH2 COEt
O CH2 COEt
第二步 烯醇负离子对另一酯分子的 亲核加成:
O O O CH3 C OEt CH2 COEt CH3 COEt + CH2 COEt
O CH2COEt
四面体 中间体
O
第三步 离去基团的消除,恢复羰基结构:
O CH3 C OEt CH2 COEt O CH3 O O C CH2 COEt + OC2H5
(1.5×10-4%)
比 C C 更稳定 键能差:45 ~ 60 kJ • mol-1
乙酰乙酸乙酯(β–丁酮酸乙酯): (ethyl acetoacetate) 互变异构
一般烯醇式不稳定,而乙酰乙酸乙酯的烯醇式较稳 定存在:
( 1 )酮式中亚甲基上的氢原子同时受羰基和酯基的影 响很活泼,很容易转移到羰基氧上形成烯醇式。 (2)烯醇式中的双键的π键与酯基中的π键形成π-π 共轭体系,使电子离域,降低了体系的能量。 :OH O CH 3 C CH C OC 2H5 (3)烯醇式通过分子内氢键的缔合形成了一个较稳定的 六员环结构。 O H O CH3 C CH C OC2H5
Beta二羰基化合物
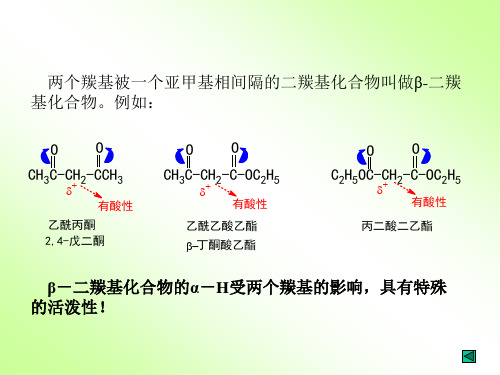
② 酮的酸性一般大于酯,所以在乙醇钠的作用下,酮更 易生成碳负离子。
例如:
O CH3-C-CH 3 C2H5ONa
O CH3-C-C-H 2
O-
CH3-C=CH 2
O
O
CH3-C-OC2H5 + -CH2-C-CH3
O- O CH3-C-CH2-C-CH3
OCH2CH3
OO CH3-C-CH2-C-CH3
R
C
CC
C O CH3
O
EtOH
OO
RC
C OEt
溴化后可以形成卡宾,可以合成小环化合物
O
C O CH3
H2C C
C O CH3
Br2
O
O
Br H
C O CH3
C
C
C O CH3
CuX
O
CH=CH2
O
C O CH3
Ar
CC
C O CH3
O
O
C O CH3
C
C
C O CH3
O
14.4Knoenenagel反应:
CF3
CH3
2. 烯醇式含量与溶剂有关,在极性溶剂(如:水或质
子性溶剂)中烯醇式含量↓,而在非极性溶剂中烯醇式
含量↑。如:
O
O
OH O
=
CH3 C CH2 C OC2H5
酮式
= CH3 C CH C OC2H5
烯醇式
H2O
99.6 %
0.4 %
C2H5O H
89.48 %
10.52 %
C6H12
53.6 %
46.4 %
这是因为在极性溶剂中,酮式或烯醇式均易 与水形成分子间氢键,从而减少了烯醇式形 成分子内氢键的几率;而在非极性溶剂中则 有利于烯醇式分子内氢键的形成。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
n = 0, 1, 2, 3
COOC2H5 COOC2H5
1) NaOH 2) H+,
COOH
思考:在与卤代烃反应生成C-C键反应中,比 较三乙及丙二酸酯的钠盐与RMgX的活性差异。
29
四、Knoevenagel缩合
在弱碱的催化下,醛、酮与含有活泼亚甲基的化合物发 生的失水缩合反应。
R' R
C=O
注意:当引入基团不同时,通常是先引入活性较高和体积较
大的基团。
23
2. 合成二羰基化合物
OO
CH3CCH2COC2H5
=
O CH2 C OC2H5
X (CH2)n
X
=
O CH2 C OC2H5
CH3COCl
CH3COCH2Cl 或 用I2偶合
CH3COCH2 CH3COCH2
(CH2)n
CH3CO CH2
20
2.乙酰乙酸乙酯活泼亚甲基上的反应
OO CH3CCH2COC2H5
OO
CH3I
CH3C-CH-COC 2H5
C2H5ONa
CH3 烃基化
OO
-C2H5OH
CH3CCHCOC2H5
BrCH2COOR
O
O
CH3C-CH-COC2H5
NaH
O- O
Na+CH3COCl
CH2COOR
CH3C=CHCOC2H5
O
CH3 C + OC2H5
CH2 C OC2H5
CH3 C CH2 C OC2H5 OC2H5
O
O
O
O
CH3 C CH2 C OC2H5
CH3 C CH2 C OC2H5
pKa = 11
O
+
C2H5O
C2H5OH CH3 C
+ C2H5O O
CH C OC2H5
= =
= =
=
=
=
=
=
O
O
CH3 C CH C OC2H5
O CH3 O H3C C C C C
CH3 CH3 OEt
思考:不同的酯能否发生选择性缩合?
14
2. 不同酯的交错缩合
含α-H的酯与不含α-H的酯(如:甲酸酯、苯甲酸酯、乙
二酸酯和碳酸酯)之间不仅可以缩合,而且具有应用价值。
如:
O HCOOEt+ CH3 C OC2H5
① C2H5ONa ② CH3COOH
CH3CO
β-二羰基化合物
CH3COCH2
CH3COCH2
γ- 二羰基化合物
思考:用I2偶合的机理?
24
3. 合成酮酸
CH3COCH 2(CH2)nCOOH
引入基团 (CH2)nCOOH
注意:在引入基团时,要用卤代酸酯X(CH2)nCOOC2H5, 而不能使用卤代酸X(CH2)nCOOH。
4. 合成一元羧酸
CF3
CH3
O
O
OH O
=
CH3 C CH2 C OC2H5 酮式
= CH3 C CH C OC2H5
烯醇式
H2O C2H5OH C6H12
99.6 % 89.48 % 53.6 %
0.4 % 10.52 % 46.4 %
➢活泼亚甲基上取代基的电子效应。
➢溶剂极性。
10
• 烯醇化导致立体异构化
Et
+
H2 C
Z' Z
弱碱 苯, 分水
R' R
C=C
Z' Z
O Z: CHO, CR, COOR, CN, NO2 等
OO CH3C-CH-COC2H5
CH3
COCH3
CH2COOR
同理,二取代乙酰乙酸乙酯进行酮式分解将得到二取代丙
酮;进行酸式分解将得到二取代乙酸。
22
1. 合成甲基酮
经乙酰乙酸乙酯合成:
引入基团
CH3COCH 2CH3
引入基团
CH3
CH3COCHCH 2CH3
✓甲基酮合成时一定要经过酮式分解; ✓将TM的结构与丙酮进行比较,确定引入基团; ✓确定合成路线。
3
一、酮-烯醇互变异构 二、乙酰乙酸乙酯的合成及其应用 三、丙二酸酯的合成及其应用 四、Knoevenagel缩合 五、Mickael加成
4
一、酮-烯醇互变异构
HC CH + H2O Hg++, H+
HC CH2 OH
•酸和碱对酮-烯醇平衡的影响 不 稳 定
CH3CHO
+OH
CH3CCH3
+ H+
CH3CH2CH2CHCOOH
CH3
二取代乙酸
引ቤተ መጻሕፍቲ ባይዱ基团:
CH3 CH2CH2CH3
COOC2H5 CH2
C2H5ONa
COOC2H5
COOC2H5
_ CH
CH3CH2Br
COOC2H5
COOC2H5 CH3CH2CH
COOC2H5
1) C2H5ONa 2) CH3I
COOC2H5 1) OHCH3CH2C CH3 2) H+
NaCl
Cl
CH2COONa C2H5OH
CN
H+
COOC2H5 H2C
COOC2H5
OO EtOCCH2COEt + EtONa
OO -
[ EtOCCHCOEt ]
Na+
OO EtO C C C OEt
H
26
1. 合成一元酸
CH3CHCH2CH2COOH CH3
一取代乙酸
引入基团: CH2CHCH3 CH3
O
O
=
=
H βC
α
CH2
C
OC2H5
= =
COOC2H5
O
+ CH3 C OC2H5
COOC2H5
① C2H5ONa COOC2H5 O
=
② CH3COOH
βCO
α
CH2
C
OC2H5
O 例: C2H5OCOC2H5 +
O
C6H5CH2COC2H5
1) C2H5ONa 2) H+
?
OO C2H5OCCHC OC2H5
= =
= =
O
O
CH3 βC
α
CH
C
OC2H5
( 酸式分解 ) R ( 酮式分解 )
① dil. OH② H+ ③ △
① 浓 OH② H+
O CH3 C CH R + CO2 + C2H5OH
一取代丙酮
O R CH2 C OH + CH3COOH + C2H5OH
OO CH3C-CH-COC2H5
O O一取代乙酸 CH3C-CH-COC 2H5
CH3CH2CH2COOH
CH3 PhCH 2CHCOOH
(1) TM为羧酸,经乙酰乙酸乙酯法合成时需酸式分解。
(2) 将TM看成取代乙酸,确定引入基团。
★由于酸式分解的同时必然伴随酮式分解,故合成羧酸 通常采用丙二酸酯法。
25
三、丙二酸酯的合成及其应用
CH2COOH Cl
NaOH H2O
CH2COONa NaCN
具有羰基的性质
✓能与金属钠作用,放出H2↑ ✓能与CH3COCl作用生成酯
✓可使溴水褪色
有醇羟基存在 有不饱和键存在
✓ 与FeCl3水溶液作用呈紫红色 具有烯醇式结构 ✓ 不能发生碘仿反应
8
OO CH3CCH2C OC2H5
OH O
CH3C
C H
C
OC2H5
在乙酰乙酸乙酯中存在着酮式和烯醇式的互变异构, 并形成一个平衡体系。
Me H
O H+ or OH-
Ph
(R)-(+)-仲丁基苯基甲酮
Et
Me H
O
Et
O
+H Ph Me
Ph
(+- )-仲丁基苯基甲酮
Et
OH
Me
Ph
11
二、乙酰乙酸乙酯的合成及应用
(一) 乙酰乙酸乙酯的制备
1.相同酯的自身缩合
O
O
O
= =
=
2
CH3COC2H5
① ②
C2H5ONa CH3COOH
CH3C
CH2
COC2H5
Claisen酯缩合反应:含α-H的酯在强碱(如:乙醇钠)
催化下缩合,生成β-酮酸酯的反应称为Claisen酯缩合。
12
= =
反应机理:
= =
= =
=
C2H5O
HO
pKa = 16 O
α
C2H5OH
+ CH2 C OC2H5
CH2 C OC2H5
pKa = 24
O
O
O
O CH2 C OC2H5
COOC2H5
COOH -CO2
CH3CH2CCH3 COOH
CH3CH2CHCOOH CH3
27
2. 合成二元酸
(1) 带支链的二元酸
CH2COOH RCHCOOH
在引入基团时要用卤代酸酯,而不能使用卤代酸。
(2) 高级直链二元酸
CH2 (CH2)n
CH2
CH2COOH CH2COOH
2 CH2(COOC2H5)2 C2H5ONa
(1) 乙酰乙酸乙酯在稀碱作用下,首先水解生成乙酰乙 酸,后者在加热条件下,脱羧生成酮。
=
