主要有机物之间转化关系
高中化学各类有机物之间的相互转化关系
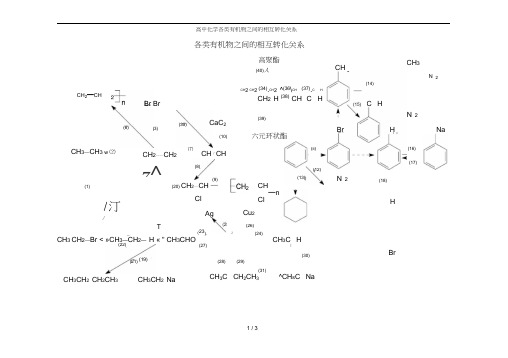
+3HO—NO2——a-
CH3
I NO2
Il+3H2O
CH2=CH2+Br2”CH2BrCH2Br
CH2=CH2+HBr尸CH3CH2Br
CH2=CH2+H2O浓H2S°4- CH3CH2OH
催化剂.
n CH2=CH2-^CH2—CH2十
催化剂
CH三CH+H2催化-CH2=CH2
CH三CH+HCl催化剂■CH2=CHCl
(30)
(28)
(29)
CH
(14)
C°°H
°H
(16)
(17)
N°2
(18)
N°2
Br
°H
Br
n°2
°Na
(31)
CH3C°°CH2CH3^CHsC°°Na
高中化学各类有机物之间的相互转化关系
光昭
CH3CH3+Br2光昭.CH3CH2Br+HBr
CH2=CH2+H2
催化剂
△
-CH3CH3
(14)
CH3
n CH2=CH
Cl
(15)
CH3
I酸性KMnO4
COOH
I I或酸性K2Cr2o7 I I
(16)
OH+NaOH
OH+Na2CO3
ONa+HCI
催化剂-一CH2—CH
_n
Cl
ONa+CO2+H2O
CaC2+2H2O» CH三CHf+Ca(OH)2
+Br2
催化剂*
A
HBr
(18)
+HO—NO2
重要有机物之间的转化关系

重要有机物之间的转化关系一、重要有机物之间的转化关系二、重要反应必背(1)CH 3CH 2Cl ―→CH 2==CH 2答案 CH 3CH 2Cl +NaOH ――→乙醇△CH 2==CH 2↑+NaCl +H 2O (2)CH 3CH 2OH ―→CH 2==CH 2答案 CH 3CH 2OH ―――→浓H 2SO 4170 ℃CH 2==CH 2↑+H 2O (3)CH 3CH 2OH ―→CH 3CHO答案 2CH 3CH 2OH +O 2――→Cu △2CH 3CHO +2H 2O (4)CH 3CH 2OH 和CH 3COOH 生成乙酸乙酯答案 CH 3COOH +CH 3CH 2OH浓H 2SO 4△CH 3COOC 2H 5+H 2O (5)OHC —CHO ―→HOOC —COOH答案 OHC —CHO +O 2――→催化剂△HOOC —COOH (6)乙二醇和乙二酸生成聚酯答案 n HOCH 2—CH 2OH +n HOOC —COOH 一定条件+2n H 2O(7)乙醛和银氨溶液的反应答案 CH 3CHO +2Ag(NH 3)2OH ―→△CH 3COONH 4+2Ag ↓+3NH 3+H 2O(8)乙醛和新制Cu(OH)2悬浊液的反应答案 CH 3CHO +2Cu(OH)2―→△CH 3COOH +Cu 2O ↓+2H 2O (9)答案 +2NaOH ――→醇△+2NaCl +2H 2O (10)答案 +Br 2――→FeBr 3+HBr (11)和饱和溴水的反应答案 +3Br 2―→↓+3HBr(12)和溴蒸气(光照)的反应答案 +Br 2―→光+HBr(13) 和HCHO 的反应答案 n +n HCHO ―→H ++n H 2O(14)酯在碱性条件的水解(以乙酸乙酯在NaOH 溶液中为例)答案 CH 3COOC 2H 5+NaOH ――→△CH 3COONa +C 2H 5OH (15)和NaOH 的反应答案 +2NaOH ――→△CH 3COONa ++H 2O三、有机物的检验辨析1.卤代烃中卤素的检验取样,滴入NaOH 溶液,加热至分层现象消失,冷却后加入稀硝酸酸化,再滴入AgNO 3溶液,观察沉淀的颜色,确定是何种卤素。
有机物 降解 机制

有机物降解机制有机物降解机制引言:有机物降解是指有机物在自然环境中经过一系列化学、生物或物理过程逐渐分解、转化为无机物的过程。
这一过程对于维持环境平衡和生物循环至关重要。
本文将从生物降解、化学降解和物理降解三个方面,探讨有机物降解的机制。
一、生物降解生物降解是指有机物在生物体内或生物作用下逐渐分解为较简单的无机物的过程。
生物降解是自然界最常见的降解方式,其机制主要包括酶催化、微生物作用和生态系统调控。
1. 酶催化酶是一类特殊的蛋白质,能够加速化学反应速率。
在有机物降解过程中,酶通过催化剂的作用,降低反应活化能,使有机物分子发生断裂、转化。
例如,多酚氧化酶能够催化酚类物质的氧化反应,将其转化为酚醛类物质。
2. 微生物作用许多微生物能够利用有机物作为能源和营养来源,通过降解有机物来获取生长所需的能量。
微生物分泌的酶能够将复杂的有机物分解为较简单的有机物,然后进一步降解为无机物。
例如,厌氧菌能够将有机酸降解为乙酸、氢气和二氧化碳。
3. 生态系统调控生态系统中的生物多样性和相互作用对有机物降解有重要影响。
生物多样性丰富的生态系统能够容纳更多的降解菌种,提高有机物降解的效率。
此外,生态系统中的生物之间还存在着协同作用和竞争关系,这些相互作用也会对有机物降解过程产生影响。
二、化学降解化学降解是指通过化学反应将有机物分解为较简单的无机物的过程。
化学降解的机制主要包括氧化、水解、光解等。
1. 氧化氧化是指有机物与氧发生反应,形成氧化产物的过程。
氧化反应可以通过氧气、过氧化氢等氧化剂催化进行。
例如,有机物中的醇可以被氧气氧化为醛、酮;烷烃可以被氧气氧化为醇。
2. 水解水解是指有机物与水发生反应,形成水解产物的过程。
水解反应通常需要在酸碱催化下进行。
例如,脂肪酸与水在碱催化下发生水解反应,生成相应的醛、酮和醇。
3. 光解光解是指有机物在光照条件下发生分解的过程。
光解反应通常需要吸收特定波长的光能才能进行。
例如,光能可以使有机物中的化学键断裂,产生自由基,进而引发链式反应,最终将有机物分解为无机物。
o有机物转化关系图

将下列19种有机化合物设计成物质转化关系图。CH3CH3、CH2=CH2、CH≡CH、CH3CH2Br、BrCH2CH2Br、C2H5OH、HOCH2CH2OH、
CH3CHOOHCCHO、CH3COOH、HOOCCOOH、CH3COOCH2CH3、CH3CH2ONa
已知:乙炔在一定条件下能三聚成苯;溴苯在高温、高压条件下,可以与氢氧化钠溶液反应得到苯酚钠。
要求:1、字迹工整、版面美观、创意新颖;2、物质间只允许用直箭头或可逆符号。不允许用折线箭头,更不能交叉;
3、在箭头上或下用①、②、③、④、⑤……标清序号;4、按序号在下面写出两种物质之间转化关系对应的反应方程式,写清反应条件。
重要有机化合物转化关系图
植物生理学:第五章 植物体内有机物质的代谢和运输

一、植物体内有机物质的运输系统
短距离运输系统
一、植物体内有机物质的运输系统
短距离运输系统
一、植物体内有机物质的运输系统
(二)长距离运输系统:指器官之间、源与库之间运输, 长距离运输系统:指器官之间、源与库之间运输, 距离从几厘米到上百米
1、微管束的组成:以导管为中心的富含纤维组织的木质部;以 微管束的组成:以导管为中心的富含纤维组织的木质部; 木质部 韧皮部; 筛管为中心的周围有薄壁组织伴连的韧皮部 筛管为中心的周围有薄壁组织伴连的韧皮部;穿插与包围木 质部和韧皮部的多种细胞,微管束鞘。 质部和韧皮部的多种细胞,微管束鞘。 微管束的功能: 2、微管束的功能: • 通常情况下,水分与无机盐通过木质部输送,有机物通过韧 通常情况下,水分与无机盐通过木质部输送, 皮部输送。 皮部输送。 • 信息(信使)物质传递的通道:如根部合成的细胞分裂素、 信息(信使)物质传递的通道:如根部合成的细胞分裂素、 脱落酸等通过木质部输送至地上部分; 脱落酸等通过木质部输送至地上部分;茎尖合成的生长素则 通过韧皮部向下运输;植物受环境刺激后产生的电波( 通过韧皮部向下运输;植物受环境刺激后产生的电波(膜电 也主要在微管束中传播。 位)也主要在微管束中传播。 • 两通道之间的物质运输:木质部与韧皮部之间侧向(横向) 两通道之间的物质运输:木质部与韧皮部之间侧向(横向) 运输可相互间运送水分和养分, 运输可相互间运送水分和养分,如筛管内的膨压变化就是由 于导管与筛管间发生水分交换产生的。 于导管与筛管间发生水分交换产生的。源自一、植物体内有机物质的运输系统
(二)长距离运输系统
2、微管束的功能 • 对同化物的吸收与分泌:韧皮部对同化物的吸收与分泌不 对同化物的吸收与分泌: 仅发生在库源端,而且在同化物的运输途中, 仅发生在库源端,而且在同化物的运输途中,微管束能与 周围组织发生物质交换。 周围组织发生物质交换。 • 对同化物的加工与贮存:同化物的运输过程中可卸至微管 对同化物的加工与贮存: 束中的某些薄壁细胞内合成淀粉,并贮存起来。 束中的某些薄壁细胞内合成淀粉,并贮存起来。是个中间 需要时再转运出去。 库,需要时再转运出去。 • 外源化学物质以及病毒等的传播通道:杀虫剂、灭菌剂、 外源化学物质以及病毒等的传播通道:杀虫剂、灭菌剂、 肥料、以及病毒分子经两通道的传输,能产生周身效应。 肥料、以及病毒分子经两通道的传输,能产生周身效应。 另外筛管汁液的蛋白抑制剂能抑制动物消化道内的消化酶, 另外筛管汁液的蛋白抑制剂能抑制动物消化道内的消化酶, 说明筛管本身存在一定的防卫机制。 说明筛管本身存在一定的防卫机制。 • 植物体的机械支撑:木质部导管、管胞。 植物体的机械支撑:木质部导管、管胞。
常见官能团的确定和转化关系

7、请认真阅读下列3个反应: 、请认真阅读下列 个反应 个反应:
利用这些反应,用四步从甲苯合成一种染料中间体 利用这些反应,用四步从甲苯合成一种染料中间体DSD 酸
请用合成反应流程图表示你的合成路线。 请用合成反应流程图表示你的合成路线。 标出反应物和反应条件) (标出反应物和反应条件)
6、A为有机合成中间体,在一定条件下发生消去反应,可能得 、 为有机合成中间体 在一定条件下发生消去反应, 为有机合成中间体, 到两种互为同分异构体的产物,其中的一种B可用于制取合成树 到两种互为同分异构体的产物,其中的一种 可用于制取合成树 染料等多种化工产品。 能发生如下图所示的变化 能发生如下图所示的变化。 脂、染料等多种化工产品。A能发生如下图所示的变化。试回答
一、常见有机官能团的确定
1.根据反应物性质确定官能团 根据反应物性质确定官能团
反应物性质
反应生成CO2、与新制 与NaHCO3反应生成 Cu(OH)2反应得到蓝色溶液
可能官能团 羧基 羧基、 羧基、酚羟基 羧基、酚羟基、 羧基、酚羟基、醇羟反应 能与Na反应 反应 与银氨溶液反应产生银镜或与 新制氢氧化铜产生红色沉淀 能使溴水褪色 加溴水产生白色沉淀、 加溴水产生白色沉淀、遇Fe3+ 显紫色
(3)C→D的反应类型是 的反应类型是____,E→F的反应类型是 的反应类型是_____ 的反应类型是 , 的反应类型是 a.氧化反应 b.还原反应 c.加成反应 d.取代反应 . . . . (4)写出化学方程式:A→B______________________。 写出化学方程式: 写出化学方程式 。 (5)写出 生成高聚物的化学方程式: 写出E生成高聚物的化学方程式: 写出 生成高聚物的化学方程式 ____________________________________________。 。 (6)C的同分异构体 l与C有相同官能团,两分子 l脱去两分 的同分异构体C 有相同官能团, 的同分异构体 有相同官能团 两分子C 子水形成含有六元环的C 写出C 的结构简式: 子水形成含有六元环的 2,写出 2的结构简式: ______________________________
有机化学知识点全归纳
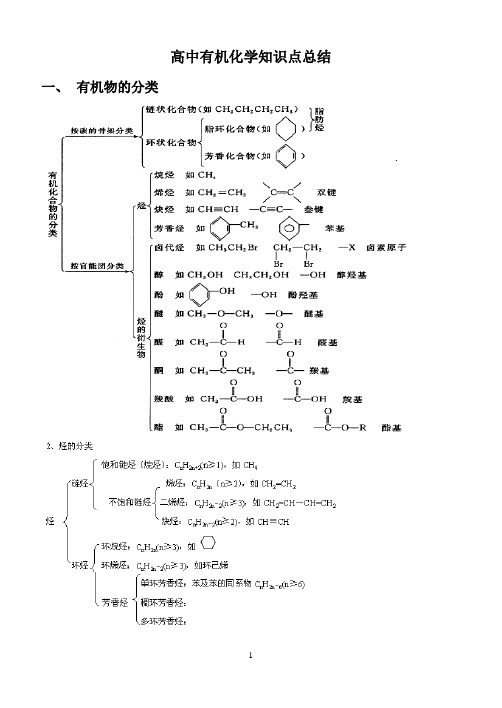
高中有机化学知识点总结一、有机物的分类二、有机物的转化关系1、常见链状有机物的转化(注意反应条件)2、常见环状有机物的转化二、 有机物的命名1.烷烃:选主链,称某烷;编号位,定支链;取代基,短线连;不同基,简在前,相同基,合并算。
长多近小写烃名,先简后繁位次清。
先小然后大,一基跟一位,数目汉数字,位置阿拉伯,字数短线隔,数字逗号撇。
其他类别的有机物:选含官能团的最长碳链为主链,从靠近官能团的一端编号,要指明官能团的位置。
练习2-甲基-1-丁烯与氢气加成以后的产物的名称为:三、有机物的组成和结构1.有机物的结构特点:化合价、成键方式、同分异构2.表示方法:(1)化学式:分子式 电子式 结构式 结构简式 最简式(实验式)键线式等 (2)模型:球棍模型 比例模型3.不饱和度:又称缺氢指数Ω=双键数+叁键数×2+环数 = (2n+2-m) /2ONaCOONa— —BrOH Br — Br(17) (18)4.同分异构:概念、分类、书写⑪碳链异构:指碳原子之间连接成不同的链状或环状结构而造成的异构。
如C5H12有三种同分异构体,即正戊烷、异戊烷和新戊烷。
⑫位置异构:指官能团或取代基在在碳链上的位置不同而造成的异构。
如1—丁烯与2—丁烯、1—丙醇与2—丙醇、邻二甲苯与间二甲苯及对二甲苯。
⑬异类异构:指官能团不同而造成的异构,也叫官能团异构。
如1—丁炔与1,3—丁二烯、丙烯与环丙烷、乙醇与甲醚、丙醛与丙酮、乙酸与甲酸甲酯、氨基乙酸和硝基乙烷、葡萄糖与果糖、蔗糖与麦芽糖等。
⑭其他异构方式:如顺反异构、对映异构(也叫做镜像异构或手性异构)等,在中学阶段的信息题中屡有涉及。
5.同系物的概念(1)定义:________相似,在分子组成上相差______________________的物质互相称为同系物。
注意:①同系物之间具有相似的分子结构,因此化学性质相似,物理性质则随碳原子数的增加而发生规律性的变化。
高三有机化学中有机物间相互转化关系图

一、有机物间相互转化关系二、能与溴水发生化学反响而使溴水褪色或变色的物质1、有机物:⑴ 不饱和烃〔烯烃、炔烃、二烯烃等〕⑵ 不饱和烃的衍生物〔烯醇、烯醛、烯酸、烯酯、油酸、油酸酯等〕 ⑶ 石油产品〔裂化气、裂解气、裂化汽油等〕⑷ 含醛基的化合物〔醛、甲酸、甲酸盐、甲酸酯、葡萄糖、麦芽糖等〕 ⑸ 天然橡胶〔聚异戊二烯〕 2、无机物:⑴ -2价的S 〔硫化氢及硫化物〕⑵ + 4价的S 〔二氧化硫、亚硫酸及亚硫酸盐〕 ⑶ + 2价的Fe6FeSO 4 + 3Br 2 = 2Fe 2(SO 4)3+ 2FeBr 3 6FeCl 2 + 3Br 2 = 4FeCl 3 + 2FeBr 3 2FeI 2 + 3Br 2 = 2FeBr 3 + 2I 2 ⑷ Zn 、Mg 等单质 如⑸ -1价的I 〔氢碘酸及碘化物〕变色 ⑹ NaOH 等强碱、Na 2CO 3和AgNO 3等盐 Br 2 + H 2O = HBr + HBrO2HBr + Na 2CO 3 = 2NaBr + CO 2↑+ H 2O变色Mg + Br 2 === MgBr 2 〔其中亦有Mg 与H +、Mg 与HBrO 的反响〕△HBrO + Na2CO3 = NaBrO + NaHCO3三、能萃取溴而使溴水褪色的物质上层变无色的〔ρ>1〕:卤代烃〔CCl4、氯仿、溴苯等〕、CS2等;下层变无色的〔ρ<1〕:直馏汽油、煤焦油、苯及苯的同系物、低级酯、液态环烷烃、液态饱和烃〔如己烷等〕等四、能使酸性高锰酸钾溶液褪色的物质1、有机物:⑴不饱和烃〔烯烃、炔烃、二烯烃等〕⑵不饱和烃的衍生物〔烯醇、烯醛、烯酸、烯酯、油酸、油酸酯等〕⑶石油产品〔裂化气、裂解气、裂化汽油等〕⑷醇类物质〔乙醇等〕⑸含醛基的化合物〔醛、甲酸、甲酸盐、甲酸酯、葡萄糖、麦芽糖等〕⑹天然橡胶〔聚异戊二烯〕⑺苯的同系物2、无机物:⑴氢卤酸及卤化物〔氢溴酸、氢碘酸、浓盐酸、溴化物、碘化物〕⑵ + 2价的Fe〔亚铁盐及氢氧化亚铁〕⑶-2价的S〔硫化氢及硫化物〕⑷ + 4价的S〔二氧化硫、亚硫酸及亚硫酸盐〕⑸ 双氧水〔H 2O 2〕五、常见的各类有机物的官能团,构造特点及主要化学性质(1)烷烃A) 官能团:无 ;通式:C n H 2n +2;代表物:CH 4B) 构造特点:键角为109°28′,空间正四面体分子。
(三)各类有机物之间的相互转化
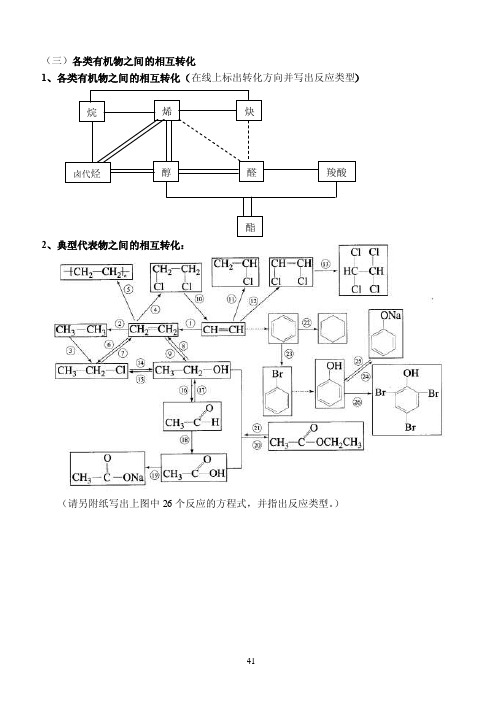
(三)各类有机物之间的相互转化1、各类有机物之间的相互转化(在线上标出转化方向并写出反应类型)2、典型代表物之间的相互转化:(请另附纸写出上图中26个反应的方程式,并指出反应类型。
)二、有机合成(一)有机合成的定义、过程及表达方式:1、定义:有机合成指利用简单、易得的原料,通过有机反应,生成具有特定结构和功能的有机化合物。
2、有机合成的过程:3、解题时的表达方式通常有两种:⑴按照设计的合成路线书写每步反应的化学方程式;⑵合成路线图(反应流程图)(二)合成方法:合成时通过基础反应(课本中的反应)及题中信息反应进行官能团的引入、消除、衍变、碳链的增减、官能团的保护等实现。
1、官能团的引入:⑴引入C =C 的方法:①②③④烷烃的热裂解和催化裂化⑵引入卤原子(一X )的方法:①②③⑶引入羟基(一OH )的方法:①②③④⑤醛氧化为羧酸。
A B C 反应物反应条件 反应物 反应条件 …… D……⑷碳碳三键的形成①二元卤代烃在强碱的醇溶液中消去2分子的HX②一元卤代烯烃在强碱的醇溶液中消去HX③实验室制备乙炔原理⑸苯环上官能团的引入:苯环上已有取代基的定位效应(题目往往会通过某种方式给出相关的信息,如:期中试卷1第19题)2、官能团的消除:⑴通过反应消除不饱和键;⑵通过、、、等消除羟基(一OH);⑶通过、等消除醛基(一CHO);⑷通过反应或反应可消除卤原子。
3、官能团间的衍变:⑴利用官能团的衍生关系进行衍变,如:醇→醛→酸⑵通过某种化学途径使一个官能团变为两个,如:CH3CH2OH→HOCH2CH2OH⑶通过某种手段,改变官能团的位置。
4、碳骨架的增减:⑴增长:有机合成题中碳链的增长,一般会以信息形式给出,如:HCN加成、卤代烃⑵变短:烃的裂化、裂解;某些烃(如苯的同系物、烯烃)的氧化,羧酸盐的脱羧反应等。
5、成环:⑴形成碳环:双烯成环(题给信息)⑵形成杂环:通过酯化反应形成环酯、通过成肽反应形成环肽6、官能团的保护:在有机合成中,某些不希望起反应的官能团,在反应试剂或反应条件的影响下产生副反应,这样就不能达到预计的合成目标,因此必须采取措施保护某些官能团,待完成反应后再除去保护基,使其复原。
高三有机化学中有机物间相互转化关系图
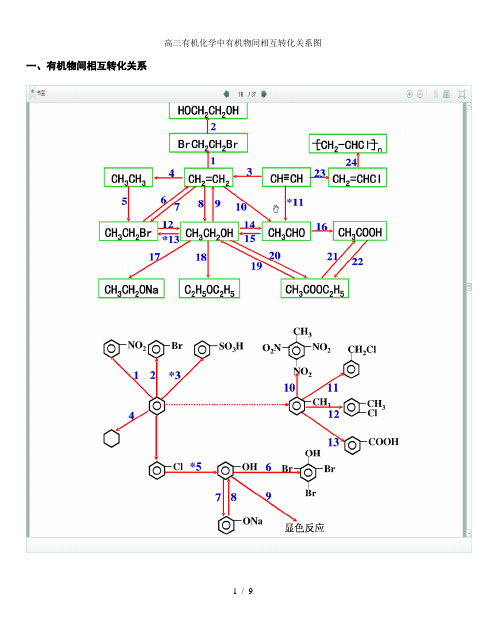
一、有机物间相互转化关系二、能与溴水发生化学反应而使溴水褪色或变色的物质1、有机物:⑴ 不饱和烃(烯烃、炔烃、二烯烃等)⑵ 不饱和烃的衍生物(烯醇、烯醛、烯酸、烯酯、油酸、油酸酯等) ⑶ 石油产品(裂化气、裂解气、裂化汽油等)⑷ 含醛基的化合物(醛、甲酸、甲酸盐、甲酸酯、葡萄糖、麦芽糖等) ⑸ 天然橡胶(聚异戊二烯)2、无机物:⑴ -2价的S (硫化氢及硫化物)⑵ + 4价的S (二氧化硫、亚硫酸及亚硫酸盐) ⑶ + 2价的64 + 32 = 22(4)3 + 2362 + 32 = 43 + 2322 + 32 = 23 + 2I 2⑷ 、等单质 如⑸ -1价的I (氢碘酸及碘化物)变色 ⑹ 等强碱、23和3等盐 2 + H 2O = +2 + 23 = 2 + 2↑+ H 2O + 23 = + 3三、能萃取溴而使溴水褪色的物质上层变无色的(ρ>1):卤代烃(4、氯仿、溴苯等)、2等;下层变无色的(ρ<1):直馏汽油、煤焦油、苯及苯的同系物、低级酯、液态环烷烃、液态饱和烃(如己烷等)等 四、能使酸性高锰酸钾溶液褪色的物质1、有机物:⑴ 不饱和烃(烯烃、炔烃、二烯烃等)⑵ 不饱和烃的衍生物(烯醇、烯醛、烯酸、烯酯、油酸、油酸酯等) ⑶ 石油产品(裂化气、裂解气、裂化汽油等) ⑷ 醇类物质(乙醇等)⑸ 含醛基的化合物(醛、甲酸、甲酸盐、甲酸酯、葡萄糖、麦芽糖等) ⑹ 天然橡胶(聚异戊二烯) ⑺ 苯的同系物变色 + 2 2 (其中亦有与、与的反应) △2、无机物:⑴ 氢卤酸及卤化物(氢溴酸、氢碘酸、浓盐酸、溴化物、碘化物) ⑵ + 2价的(亚铁盐及氢氧化亚铁) ⑶ -2价的S (硫化氢及硫化物)⑷ + 4价的S (二氧化硫、亚硫酸及亚硫酸盐) ⑸ 双氧水(H 2O 2)五、常见的各类有机物的官能团,结构特点及主要化学性质(1) 烷烃A) 官能团:无 ;通式:22;代表物:4B) 结构特点:键角为109°28′,空间正四面体分子。
主要有机物之间转化关系
化学性质: 请写出溴乙烷分别和NaOH水溶液、 NaOH醇溶液混合加热的化学方程式, 并指出其反应类型。 思考: 1、如何引入C=C? 2、如何引入羟基(—OH)?
10
3、卤代烃的制取及其主要化学性质
一卤代烃的消去反应引入C=C、 一卤代烃的水解引入—OH
11
问题三
化合物A最早发现于酸牛奶中,它是人体内糖代谢 的中间体,A的钙盐是人们喜爱的补钙剂之一。A在某 催化剂的存在下进行氧化,其产物不能发生银镜反应。 在浓硫酸存在下,A可发生如下图所示的反应:
逆向合成分析法示意图
【学以致用——解决问题 】
问题一 以2-丁烯为原料合成: 1) 2-氯丁烷 2) 2-丁醇 3) 2,3-二氯丁烷 4) 2,3-丁二醇
【学以致用——解决问题 】
问题二
写出由乙烯制备乙酸乙酯的设计思路,并 写出有关的化学方程式 :
乙烯
乙醇
乙醛
乙酸乙酯
乙酸
第一课时结束
3、卤代烃的制取及其主要化学性质
Fe
+ HBr
CH3CH2Br + H2O
CH3CH2OH + HBr
醇(酚)的取代反应
官能团衍变中表现出的特点归纳(一)——基团的引入
3、引入羟基的四种方法举例:
CH2=CH2 +H2O
催化剂
CH3CH2OH
烯烃与水的加成
CH3CH2Cl + NaOH
CH3CHO + H2
H2O △
CH3CH2OH + NaCl 卤代烃的水解
原料
顺 逆
中间产物
顺 逆
产品
感受“合成” 如何以乙烯为基础原料,无机原料可 以任选: (1)合成HOCH2CH2OH
有机推断题的解题思路和技巧

CH 2 = CHCl —CH 2—CH — [ ]n | Cl CH 2—O —C = O | | CH 2—O —C = O CH CH CH 2—Br CH 2—Br | CHO CHO | COOH COOH | CH 2OH CH 2OH | CH 2 = CH 2 CH 3CH 2OH CH 3CHO CH 3COOH—CH 2—CH 2— [ ]n CH 3-CH 3 CH 3CH 2Cl CH 3COOCH 2CH 3 有机推断题的解题思路和技巧有机推断题的解题关键是寻找突破口;解题重点是官能团的定性、定量推断以及碳骨架的确定。
一、有机推断题的六大突破口突破口一:物质的转化关系 突破口二:物质的特征性质突破口三:反应的特征条件 突破口四:物质燃烧相关量突破口五:物质式量的展开 突破口六:题目所给的信息技巧:1、找信息量最大的点;2、找特殊分子式、特殊反应、特 殊颜色等;3、如果不能直接推断某物质,可以先假设几种可能,再认真论证。
二、有机物的重要转化关系:(一)常见有机反应的特点:一般的:有机反应碳的骨架不变;有机反应碳原子数不变;反应官能团的位置不变;反应部位是官能团所在碳原子或者邻位碳原子。
(二)官能团的衍变通过某种途径使一个官能团变为两个,如:CH 3CH 2OH → HOCH 2CH 2OH ;通过某种途径可使官能团的位置改变,如CH 3CH 2CH 2OH → CH 3CHOHCH 3。
三、官能团的推断(一)、定性推断:1、据反应物性质确定官能团(1)与溴水反应:含碳碳双键、碳碳三键、醛基(醛、甲酸、甲酸盐、甲酸酯、葡萄糖、麦芽糖)、酚羟基(2)与酸性高锰酸钾反应:含碳碳双键、碳碳三键、醛基、酚羟基、苯的同系物(3)与金属钠反应:醇羟基 、酚羟基、羧基(4)与NaOH 反应或在其催化下可以进行的反应:酚羟基、羧基、酯(油脂)的水解、卤代烃(5)与碳酸氢钠反应: 羧基(6)与Na 2CO 3反应:酚羟基 、羧基(7)与银氨溶液([Ag(NH 3)2]OH )反应:醛基(醛、甲酸、甲酸盐、甲酸酯、葡萄糖、麦芽糖)(8)Cu(OH)2悬浊液:醛基(醛、甲酸、甲酸盐、甲酸酯、葡萄糖、麦芽糖)、羧基、多元醇(9)使FeCl 3溶液显特殊颜色的:酚羟基(10)含氢量最高的有机物是:CH 4(11)一定质量的有机物燃烧,耗氧气量最大的是:CH4(12)完全燃烧时生成等物质的量的CO2和H2O的是:烯烃、环烷烃、饱和一元醛、酮、饱和一元羧酸、酯、葡萄糖(即符合通式C n H2n O x的物质)2、由反应条件确定官能团(1)浓硫酸加热:醇的消去、酯化反应、硝化、磺化(2)稀硫酸:酯的水解、二糖、多糖的水解(3)H2、催化剂(Ni ):加成(4)O2/Cu、加热:醇羟基氧化(5)Cl2(Br2)/Fe:苯环(6)Cl2(Br2)/光照:烷烃或苯环上烷烃基(7)NaOH条件一般反应有酸(或钠盐)生成。
有机物的转化1

要点❷ 重要转化关系
1.按要求书写下列反应的化学方程式。
(1)
与足量 NaOH 溶液反应:___________________________
_____________________________________________________________________。
(2) 在 催 化 剂 作 用 下 ,
有机物的转化 课时1
要点❶ 常见有机反应类型
反应类型
实例
取 卤代 甲烷的卤代,苯及含苯环化合物的卤代
代 酯化 乙酸与乙醇的酯化反应
反 水解 酯、油脂的水解,二糖、多糖的水解
应 其他 苯及含苯环化合物的硝化
反应类型 消去 反应
加成反应 加聚反应
实例 醇在浓硫酸作用下羟基与相邻碳原子上的氢原子发生脱水反应 卤代烃在氢氧化钠醇溶液中发生的脱 HX 反应 烯烃与 H2、Br2、HCl 等的加成,苯及含苯环化合物与 H2 加成 乙烯、苯乙烯、氯乙烯等的加聚反应
与 足 量 H2 反 应 :
_____________________________________________________________________ ________________________________________________________合物,其结构简式如图所示:
在一定条件下,1 mol 该物质,最多能与________mol NaOH 完全反应;与溴水反应, 最多能消耗________mol Br2;最多可与________mol H2 发生加成反应。 【答案】8 4 6
3.
请根据图中所示转化关系,写出各步反应的条件: ①________________;②________________; ③________________;④________________。 【答案】①Cl2、光照 ②NaOH 的乙醇溶液、△ ③Br2 的 CCl4 溶液 ④NaOH 的 乙醇溶液、△
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
想一想:结合生产实际,同学们,你认为 在选择原料和合成途径时,你应该注意一 些什么问题? 反应条件必须比较温和 产率较高 原料低毒性、低污染、 原料低毒性、低污染、廉价 ·········
3、有机合成遵循的原则 、
1)起始原料要廉价、易得、低毒、低污染——通 )起始原料要廉价、易得、低毒、低污染 通 常采用4个 以下的单官能团化合物和单取代 常采用 个C以下的单官能团化合物和单取代 苯。 2)尽量选择步骤最少的合成路线 )尽量选择步骤最少的合成路线——以保证较高 以保证较高 的产率。 的产率。 3)满足“绿色化学”的要求。 )满足“绿色化学”的要求。 4)操作简单、条件温和、能耗低、易实现 )操作简单、条件温和、能耗低、 5)尊重客观事实,按一定顺序反应。 )尊重客观事实,按一定顺序反应。
问题三 分析: 分析:
A的结构简式为:CH3—CH—COOH OH CH 则B的结构简式为: 3—CH—COOC2H5 O OH 则C的结构简式为:CH3—CH—O—C—CH3 COOH 29
问题三 分析: 分析:
A的结构简式为:CH3—CH—COOH OH 则A→D的化学方程式为: CH3—CH—COOH OH
水解 氧化 氧化
CH3CH2-OH
CH3-CHO CH3-COOH
b.官能团数目变化: b.官能团数目变化: 官能团数目变化 CH3CH2-Br
消去
CH2=CH2
加Br2
CH2Br-CH2Br -
c.官能团位置变化: c.官能团位置变化: 官能团位置变化 CH3CH2CH2-Br
消去
加HBr
CH3CH=CH2
+2N aOH
H C C C C 2 +2NaCl H 2 H H
+2H O 2
浓硫酸
H2O+CH2=CHCOOH
反应类型: 消去反应
30
问题三 分析: 分析:
A的结构简式为:CH3—CH—COOH OH 对比A和E的分子式,我们发现E的C原子 对比 和 的分子式,我们发现 的 原子 的分子式 个数是A的 倍 推断可能是2分子的 分子的A反应生 个数是 的2倍,推断可能是 分子的 反应生 成E,再对比H和O原子发现: 2A—E=2H2O, ,再对比 和 原子发现: , 原子发现 结合A的结构简式 的结构简式, 结合 的结构简式,很明显是它们的羧基和醇 羟基相互反应生成酯基。所以: 羟基相互反应生成酯基。所以: 31
O C—OC2H5 C—OC2H5 O H2C—Cl H2C—Cl CH2 CH2 H2C—OH H2C—OH 2 C2H5OH + O C—OH C—OH O O C—H C—H O
有机合成的一般思路 1、正向合成分析法
此法采用正向思维方法, 已知原料入手, 此法采用正向思维方法,从已知原料入手, 入手 找出合成所需要的直接或间接的中间产物 中间产物, 找出合成所需要的直接或间接的中间产物,逐步 推向目标合成有机物 目标合成有机物。 推向目标合成有机物。
CH2=CH2 +HCl CH4 + Cl2 + Br2
催化剂 光照
CH3CH2Cl CH3Cl + HCl
烯(炔)的加成 炔 的加成
烃的取代 Fe △ Br + HBr CH3CH2Br + H2O
CH3CH2OH + HBr
醇(酚)的取代反应 酚 的取代反应
官能团衍变中表现出的特点归纳( 官能团衍变中表现出的特点归纳(一)——基团的引入 基团的引入 3、引入羟基的四种方法举例: 、引入羟基的四种方法举例:
试一试: 在日常生活中,饮料、 在日常生活中,饮料、糖果中常常添加一些有 水果香味的酯类香料, 水果香味的酯类香料,例如具有苹果香味的戊酸 戊酯,你能利用1-戊烯为原料合成戊酸戊酯这种 戊酯,你能利用 戊烯为原料合成戊酸戊酯这种 香料吗? 香料吗?
戊酸戊酯 1-戊烯 戊烯 O CH3(CH2)3C-O-CH2(CH2)3CH3 CH2=CH-CH2CH2CH3
分析: 问题三 分析:
则A生成E可表示为: O C CH3—CH—C—OH C O H O H HO—C—CH—CH3 C C O H
O
将A的结构简式改写为: 3—CH—C—OH CH
H2O
CH3 O CH—C 即: O C—CH O CH3 32 O
H2O
O
问题三 分析: 分析:
则A→E的化学方程式为: 2CH3—CH—COOH OH
浓硫酸
CH3 O CH—C 2H2O + O C—CH O CH3 33 O
反应类型:
酯化反应
1,35) 1,3-丁二烯
HC C C C 3 H 3 H H H H HC C C C 3 H 3 C C l l
+Cl2 C2H O 5 H 加 热
H H HC C C C 3 H 3 C C l l
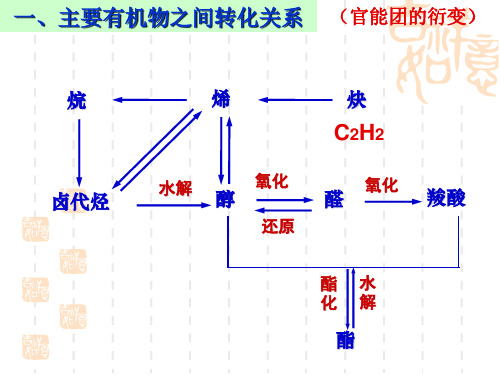
一、主要有机物之间转化关系
(官能团的衍变) 官能团的衍变)
烷
烯
炔
C2H2
卤代烃
水解
醇
氧化 还原
醛
氧化
羧酸
酯 化
水 解
酯
官能团衍变中表现出的特点归纳( 官能团衍变中表现出的特点归纳(一)——基团的引入 基团的引入
1、引入碳碳双键的三种方法举例: 、引入碳碳双键的三种方法举例:
醇 CH3CH2Cl + NaOH
原料
顺 逆
中间产物
顺 逆
产品
感受“合成” 感受“合成” 如何以乙烯为基础原料,无机原料可 如何以乙烯为基础原料, 以任选: 以任选: (1)合成HOCH2CH2OH 合成HOCH (2)合成CH3COOH 合成CH (3)合成CH3COOCH2CH3 合成CH (4)乙二酸二乙酯 (4)乙二酸二乙酯
CH3CH-CH3 Br
思考? 思考?
1、什么是有机合成? 什么是有机合成?
有机合成是利用简单、易得的原料, 有机合成是利用简单、易得的原料,通过有机 反应,生成具有特定结构和功能的有机化合物。 反应,生成具有特定结构和功能的有机化合物。
2、有机合成的任务有哪些? 有机合成的任务有哪些?
有机合成的任务包括目标化合物分子骨架构建 和官能团的转化。 和官能团的转化。
浓硫酸 170° °
△
CH2=CH2 + NaCl
卤代烃的消去 醇的消去
CH3O
CH=CH + H2
催化剂
CH2=CH2
炔烃的不完全加成
官能团衍变中表现出的特点归纳( 官能团衍变中表现出的特点归纳(一)——基团的引入 基团的引入 2、引入卤原子的三种方法举例: 、引入卤原子的三种方法举例:
CH2=CH2 +H2O
催化剂
CH3CH2OH
烯烃与水的加成
CH3CH2Cl + NaOH CH3CHO + H2
H2O △
CH3CH2OH + NaCl 卤代烃的水解 CH3CH2OH 稀硫酸 醛酮的还原
催化剂
CH3COOCH2CH3 + H2O
△
CH3COOH + CH3CH2OH 酯的水解
官能团衍变中表现出的特点归纳( 官能团衍变中表现出的特点归纳(二)——基团的变化 基团的变化 a.官能团种类变化: a.官能团种类变化: 官能团种类变化 CH3CH2-Br
基础原料
中间体
中间体
目标化合物
正向合成分析法示意图
2、逆向合成分析法
是将目标化合物倒退一步寻找上一步反应的 中间体, 中间体,该中间体同辅助原料反应可以得到目标 化合物。 化合物。
目标化合物 中间体 中间体 基础原料
逆向合成分析法示意图
【学以致用——解决问题 】 学以致用 解决问题
问题一 以2-丁烯为原料合成: 丁烯为原料合成: 1) 2-氯丁烷 222) 2-丁醇 2,33) 2,3-二氯丁烷 4) 2,3-丁二醇 2,3-
10
3、卤代烃的制取及其主要化学性质 、
一卤代烃的消去反应引入 一卤代烃的消去反应引入C=C、 消去反应引入 一卤代烃的水解引入 水解引入—OH 一卤代烃的水解引入
11
问题三
化合物A最早发现于酸牛奶中,它是人体内糖代谢 的中间体,A的钙盐是人们喜爱的补钙剂之一。A在某 催化剂的存在下进行氧化,其产物不能发生银镜反应。 在浓硫酸存在下,A可发生如下图所示的反应:
逆合成分析法
O HO-H CH3(CH2)3C-O-CH2(CH2)3CH3 目标化 合物
CH3CH2CH2CH2COOH + HO-CH2CH2CH2CH2CH3 CH3CH2CH2CH2CHO
中间体
CH3CH2CH2CH2CH2OH CH3CH2CH2CH=CH2
中间体
基础原 料
试用逆合成分析法研究合成草酸二乙酯的路线
试写出: (1) 化合物A、B、C的结构简式: 、 ,A→E (2) 化学方程式:A→D (3) 反应类型:A→D ,A→E
、
。 。 。
27
问题三 分析: 分析:
题中说“A的钙盐”,可知A含—COOH; 结合A的分子式,由A→C知,A还含有—OH, 由A在催化剂作用下被氧化的产物不能发生银 镜反应可知:A的—OH不在碳链的末端;3个 碳的碳链只有一种:C—C—C,—OH只能在中 间碳上。综上:A的结构简式为: CH3—CH—COOH OH 28
【学以致用——解决问题 】 学以致用 解决问题
问题二
写出由乙烯制备乙酸乙酯的设计思路, 写出由乙烯制备乙酸乙酯的设计思路,并 乙烯制备乙酸乙酯的设计思路 写出有关的化学方程式 :
乙烯
乙醇
乙醛 乙酸乙酯
乙酸
第一课时结束
3、卤代烃的制取及其主要化学性质 、
