第六章还原反应及其工艺
第六章还原反应及其工艺

C
C6 H5 CO 2C 2H 5
+ H2NCNH2
Zn/HCl
C 2H 5
选择性还原C=O成亚甲基,而不影响其它羰基。 选择性还原C=O成亚甲基,而不影响其它羰基。 C=O成亚甲基
搅拌的影响: 搅拌的影响:
铁粉比较重,需要良好的搅拌,否则容易沉到反应器底部。 铁粉比较重,需要良好的搅拌,否则容易沉到反应器底部。 衬有耐酸砖的平底钢槽和铸铁慢速耙式搅拌器。 衬有耐酸砖的平底钢槽和铸铁慢速耙式搅拌器。 耙式搅拌器 新式反应器:衬耐酸砖的球底钢槽和不锈钢快速螺旋桨式搅拌器。 新式反应器:衬耐酸砖的球底钢槽和不锈钢快速螺旋桨式搅拌器。 螺旋桨式搅拌器
铁粉的影响: 铁粉的影响:
洁净、粒细和质软的灰铸铁屑,优于组成比较纯净的钢屑。 洁净、粒细和质软的灰铸铁屑,优于组成比较纯净的钢屑。 通常使用60-100目铁粉。太粗的铁粉表面积小,反应慢; 通常使用60-100目铁粉。太粗的铁粉表面积小,反应慢;太细的 60 目铁粉 铁粉,后处理困难。 铁粉,后处理困难。 用量:每摩尔硝基物理论上需要2.25摩尔铁屑,实际为3 摩尔。 用量:每摩尔硝基物理论上需要2.25摩尔铁屑,实际为3-4摩尔。 2.25摩尔铁屑 思考:1mole间二硝基苯还原为间二氨基苯理论上需要多少摩尔 思考:1mole间二硝基苯还原为间二氨基苯理论上需要多少摩尔 铁屑? 铁屑?
2、锌粉还原
锌粉的还原能力
还原能力比铁粉强。 还原能力比铁粉强。 还原性与反应介质有关:可在碱性、酸性条件下进行。 还原性与反应介质有关:可在碱性、酸性条件下进行。 碱性 条件下进行 可用于还原硝基、亚硝基、氰基、羰基等多种官能团。 可用于还原硝基、亚硝基、氰基、羰基等多种官能团。 缺点:价格比铁粉贵得多。 缺点:价格比铁粉贵得多。
第六章 还原反应

硼烷可以选择性的把酰胺还原成相应的氨基,通常以四氢呋 喃为溶剂。
O2N O B H /THF C-N(CH3)2 2 6 O2N CH2-N(CH3)2
此外,乙硼烷可以选择性的把肟还原成相应的氨基。
B2H6,(CH3OCH2CH2 )2O 105 C~110 C
o o
O2N
C=NOH
O2N
CH2NH2
C H COCH3
Hg-Zn HCl Hg-Zn HCl
H3CH2 CH2CH2C
α,β-不 饱 和 醛 酮 同 时 被 还 原
PhHC
C H
CH2CH3
※ 可还原双键,包括非羰基双键;炔键还原为烯键
2、碱性条件下还原,锌可以把羰基还原成羟基。如:马尼地 平中间体的合成
Ph O Ph
Zn/NaOH C2H5 OH,70o C~74oC,2h
CH3
LiAlH4
CH3 CH 2NH 2
CH=NAlH2
H+
氢化锂铝可以使化合物活泼位置的卤素发生氢解,特别是苄 基位和烯丙位的卤原子更容易氢解。
CF3 NH2
LiAlH4 Et2O
CH3 NH2
(二) 氢化硼钠 氢化硼钠(NaBH4)的还原能力比LiAlH4弱,但是选择性较好。 使用条件水醇中进行,与LiAlH4正相反。
PhCH2CH2COOH
第二节
催化氢化反应
一、非均相催化氢化 催化反应发生在催化剂表面的反应。 (一)机理还没有完全研究清楚,通常认为氢吸附在金属的表 面,烯烃也通过p-轨道与金属络合,然后烯烃与氢加成。 (二)影响催化剂的反应因素 1、比表面积:一般催比表面积在数十到数百平方米每克。 2、载体:某些纯金属的催化剂往往吸附在活性炭、硅胶上。 3、助催化剂:反应中加入少量提高催化剂活性的物质。 4、毒剂和抑制剂:能是催化剂活性大大降低或完全丧失,并 难易恢复原有的活性。
第六章氧化-还原反应电化学

第六章 氧化─还原反应和电化学Chapter 6 Oxidation-Reduction Reactions & Electrochemistry本章研究另一类化学反应──氧化─ 还原反应(有电子转移的反应)§1 氧化─ 还原反应(Oxidation —Reduction Reactions )一、氧化数(Oxidation Number )1.氧化数是一个经验值,是一个人为的概念。
2.引入此概念,有以下几方面的应用:(1) 判断是否发生氧化──还原反应:氧化数升高、氧化反应、还原剂 reducing agent (reductant),氧化数降低、还原反应、氧化剂 oxidizing agent (oxidant). (2) 计算氧化──还原当量 (3) 配平氧化──还原反应方程式(4) 分类化合物,如Fe ( Ⅲ )、Fe (Ⅱ);Cu (Ⅰ)、Cu (Ⅱ)。
引入氧化数,可以在不用详细研究化合物的结构和反应机理的情况下,实现上述四点。
3.怎样确定氧化数(1) 在离子化合物中,元素的氧化数等于离子的正、负电荷数。
(2) 在共价化合物中,元素的氧化数为两个原子之间共用电子对的偏移数。
a .在非极性键共价分子(单质)中,元素的氧化数为零,如P 4、S 8、Cl 2中P 、S 、Cl 的氧化数都为零;b .在极性键共价分子中,元素的氧化数等于原子间共用电子对的偏移数,例如:11H :F +-,1111(-2)H :O :H +--+,1100111H :O :O :H +--+-,11+11(0)H :O :F +--。
(3) 具体规定:a .单质的氧化数为零,例如P 4、S 8中P 、S 的氧化数都为零,因为P -P 和S -S键中共用电子对没有偏移;b .除了在NaH 、CaH 2、NaBH 4、LiAlH 4中氢的氧化数为-1以外,氢的氧化数为+1;c .所有氟化物中,氟的氧化数为-1;d .氧的氧化数一般为-2,但有许多例外,例如2O (1/2)--、22O (1)--、3O (1/3)--、21/2O ()++、2OF 2)(+等;目前元素的最高氧化数达到+8,在OsO 4、RuO 4中,Os 和Ru 的氧化数均为+8,其它元素的最高氧化数至多达到其主、副族数。
第六章 还原反应.

(4)炔烃顺式加氢
(5)不发生双键迁移的氢化,前者不发 生双键的迁移。
第二节 化学还原
如果分子中有多个可被还原的基团,需 要氢化还原的是列于表6-2前列的较易还 原的基团,而保留的是该列表后列较难 还原的基团,则选用催化氢化法为佳; 反之,若需还原后列基团而保留前列基 团,通常选用具有反应选择性的化学还 原为好。
有的化学还原剂还是具有立体选择性, 即同一个被还原物,若采用不同的化学 还原剂,结果可得不同的空间构型的产 物。
常用的化学还原剂有:金属、金属复氢 化物、肼及其衍生物、硫化物、硼烷等。
一、活泼金属与供质子剂
金属与供质子剂的还原作用应看成是 “内部的”电解还原,即一个电子从金 属表面转移到待还原的有机分子上,形 成“负离子自由基”,然后随即与供质 子剂提供的质子结合成自由基,接着再 从金属表面取得一个电子,形成负离子, 再从供质子剂取得质子而完成还原反应 的全过程。 如下式所示:
非均相催化氢化反应具有工艺简便、原料低廉, 对许多基团的加氢、氢解均有较高的催化活性, 而且容易分离回收等优点, 均相催化剂的缺点是原料成本高,目对氧敏感, 常用惰性气体回流除氧,以保让氢化反应的顺 利进行。但尽管如此,其优点仍然引起人们极 大的兴趣和重视,无论在催化理论的研究上, 还是在有机合成的应用方面,都具有深远的意 义。
催化加氢
催化加氢是指具有不饱和键的有机物分 子,在催化剂存在下,与氢分子作用, 结果不饱和键全部或部分加氢的反应。 该反应应用范围很广,烯烃、炔烃、硝 基化合物、醛、酮、腈、芳环、芳杂环, 羧酸衍生物等均可采用此法还原成相应 的饱和结构。如下例:
催化氢解
通常指在催化剂存在下,含有碳—杂键的有机 物分子在氢化时发生碳—杂键断裂,结果分解 成两部分氢化产物。可用下列通式表示:
第六章-还原反应

硝基 R-NO2 伯胺 R-NH2
炔 R- C
C- R'
烯 R-HC
CH-R'
醛 R-CHO
伯醇 R-CH2OH
烯 RCH=CHR 烷 RCH2CH2R
酮 RCOR
仲醇 RCH(OH)R
5
还原基团
X =O, N X =Br,Cl
腈 RC N 含氮芳杂环
N
还原产物
CH3 CH3
2017年7月14日星期五 条件选择及活性比较
7
4. 催化转移氢化反应
催化转移氢化反应属于非均相催化氢化。特点是在金属催化剂存在下,用有
机化合物作为供氢体以代替气态氢作为反应氢源。
COOH
+
Pd/C, 甲苯 回流
COOH
+
常用的供氢体:不饱和脂环烃、不饱和帖及醇类 常用的催化剂:钯-碳
该反应特点:设备与操作简单、反应条件温和、基团还原选择性好
(5) 后处理方便,反应完毕,滤除催化剂蒸出溶剂即可,且干净无污染
(1). 常用催化剂
镍催化剂:Raney 镍、载体镍、还原镍、硼化镍
Raney 镍:为最常用氢化催化剂。具有多孔海绵状结构的金属镍微粒, 又称活性镍。它的制备是由铝镍合金粉末与氢氧化钠溶液反应。 钯和铂催化剂:载体钯和载体铂,用活性碳为载体的称为钯碳(Pd-C)和铂碳 (Pt-C); 用硫酸钡为载体,称为Lindlar催化剂;二氧化铂称为Adams催化剂
按机理分为
电子转移还原反应(Na, K, Li, ...)
1
生物还原反应:使用微生物发孝或活性酶进行底物特定结构底还原反应.
按还原方法分为
微生物发酵(jiao)法 酶催化法
2)按还原反应相的分为:
化学初中一年级上册第六章氧化还原反应的认识与运用

化学初中一年级上册第六章氧化还原反应的认识与运用氧化还原反应是化学学科中的重要内容,在初中一年级上册的化学课程中,也是必不可少的一章。
本文将对初中一年级上册第六章氧化还原反应的认识与运用进行论述。
一、氧化还原反应的基本概念氧化还原反应是指物质在化学反应中,电子的转移与分配所引起的相互转化。
在氧化还原反应中,一种物质失去电子称为氧化反应,而另一种物质得到电子称为还原反应。
例如,当铁和氧气发生反应时,铁失去电子转化为氧化铁,氧气得到电子转化为氧化氧。
二、氧化还原反应的表示方法氧化还原反应可以通过方程式表达出来。
方程式的左边表示还原反应,右边表示氧化反应。
例如,2Na + Cl2 → 2NaCl,表明钠发生氧化反应,氯发生还原反应。
三、氧化还原反应的实际应用1. 腐蚀反应:铁的腐蚀是一种常见的氧化还原反应。
当铁与空气中的氧气发生反应时,会生成铁(III)氧化物,即铁锈。
2. 电池反应:电池的工作原理是基于氧化还原反应的。
例如,锌-铜电池中,锌发生氧化反应,铜发生还原反应,从而产生电流。
3. 发酵反应:发酵是一种生物化学反应过程,也包含氧化还原反应。
例如,葡萄糖发酵产生乙醇的反应中,葡萄糖被氧化,生成乙醇,同时还有氧化剂参与反应。
四、氧化还原反应的学习方法1. 掌握氧化还原反应的基本概念和表示方法是学好本章内容的基础。
通过反复练习、思考,加深对概念的理解和方程式的运用能力。
2. 应用于生活实例的学习。
在学习氧化还原反应时,可以结合生活中的实际例子,例如电池、金属腐蚀等,加深对反应机理的理解。
3. 实验探究与讨论。
可以通过参加实验课程,观察和分析氧化还原反应的现象。
通过实验结果的观察和讨论,培养学生的实践能力和探究精神。
五、氧化还原反应的拓展应用1. 高级化学课程的基础。
氧化还原反应是许多高级化学知识的基础,例如电化学、配位化学等。
因此,对初中阶段的学生来说,学好氧化还原反应是为将来的学习做好准备。
2. 环境保护的应用。
第六章 氧化还原

4、根据氧化剂和还原剂得失电子数相等的原则, 找出最小公倍数,合并成一个配平的离子方程式。
①×2 ② ×5 2MnO4-+16H++10e10Cl- - 10e5Cl2 2Mn2++ 5Cl2 + 8H2O
14
2Mn2++8H2O
两式相加 2MnO4-+16H++10Cl-
5、将配平的离子方程式写为分子方程式。注意反 应前后氧化值没有变化的离子的配平。
21
常用电极类型: 常用的电极(半电池),通常有四种类型: 1. 金属-金属离子电极:将金属插入到其盐溶液中构 成的电极。如:银电极( Ag+ / Ag ) 。 电极组成式:Ag|Ag+ (c) 电极反应: Ag++eAg
2. 金属-难溶盐-阴离子电极: 将金属表面涂有其金属 难溶盐的固体,浸入与该盐具有相同阴离子的溶液 中所构成的电极。 如: Ag-AgCl电极。 电极组成式:Ag | AgCl(s) | Cl- (c) 电极反应: AgCl + eAg + Cl22
8
又如: Zn + 2HCl
ZnCl2 + H2
锌失去电子,氧化值升高,被氧化,称为还原
剂(reducing agent),又称电子的供体(electron donor)。 HCl中的H+得到电子,氧化值降低,被还原, HCl称为氧化剂(oxidizing agent),又称电子的受体 (electron acceptor)。 氧化还原反应的本质是反应过程中有电子转移 (电子的得失或电子云的偏移),从而导致元素的 氧化值发生变化。
式中:n=5,氧化态为MnO4-和8H+,还原态为Mn2+ (H2O是溶剂,不包括在内)。
第六章氧化还原滴定法

§6.2 氧化还原反应进行的程度
§6.2.1 条件平衡常数 n2Ox1 + n1Red2 n2Red1 + n1Ox2
氧化还原反应进行的程度,可用什么来衡量? 氧化还原反应进行的程度,可用什么来衡量?
Ox1 + n1eOx2 + n2eRed1 Red2
Ε1 = Ε
O' 1
c Ox1 0 . 059 + lg c Red1 n1 c 0 . 059 lg Ox2 n2 c Red2
4+ 3+ θ′
(1mol·L-1 H2SO4) ϕ (Fe /Fe )=0.68 V
3+ 2+
θ′
滴定反应: 滴定反应: Ce4+ + Fe2+ = Ce3+ + Fe3+ 对于滴定的每一点,达平衡时有: 对于滴定的每一点,达平衡时有:
ϕ(Fe3+/Fe2+)=ϕ(C 4+/C 3+) e e
分析 滴定前, 未知, 滴定前,Fe3+未知,不好计算
第六章 氧化还原滴定法
§6.1 氧化还原反应平衡 §6.2 氧化还原反应进行的程度 §6.3 氧化还原反应的速率与影响因素 §6.4 氧化还原滴定曲线及终点的确定 §6.5 氧化还原滴定法中的预处理 §6.6 高锰酸钾法 §6.7 重铬酸钾法 §6.8 碘量法 §6.9 其它氧化还原滴定法 §6.10 氧化还原滴定结果的计算
HClO4 0.75
HCl 0.70
ϕθ'(Fe3+ /Fe2+)
与Fe3+的络合作用增强
氧化态形成的络合物更稳定, 氧化态形成的络合物更稳定,结果是电位降低 计算pH pH为 NaF浓度为 浓度为0.2 mol/l时 P136 例2 计算pH为3.0, NaF浓度为0.2 mol/l时, Fe3+/ Fe 的条件电位。在此条件下,用碘量法测 Fe2+的条件电位 在此条件下, 的条件电位。 Fe 铜时,会不会干扰测定? pH改为 改为1.0 铜时,会不会干扰测定?若pH改为1.0 时,结果又 如何? 如何?
第六章 还原反应及其工艺

• 锌粉表面易被空气氧化而降低活性,应选用新制 的锌粉。
2019/9/12
26
6.3.1 芳磺酰氯还原成芳亚磺酸 6.3.2 芳磺酸氯还原成硫酚 6.3.3 碳硫双键还原脱硫成亚甲基 6.3.4 羰基还原成羟基 6.3.5羰基还原成亚甲基 6.3.6 硝基化合物还原成氧化偶氮、偶氮和氢
• 只有个别实例,也可用锌粉还原法或氢气还原法。 6.2.2.6 还原脱溴 • 例如 3,6-二溴 -2- 甲氧基萘还原脱溴制 6- 溴 -2- 甲
氧基萘(水-乙酸介质)。 • 只有少数实例 ,主要用催化氢化法。
2019/9/12
24
6.2.3 铁粉还原的主要影晌因素
• (1) 铁粉的质量:一般用干净质软的灰色铸铁。
R2C-OH R2C-OH
2019/9/12
15
2019/9/12
16
Clemmensen还原(酸性条件下反应)
O Zn-Hg/Zn
C
HCl
CH2
Zn-Hg 活性>Zn HgCl2+HCl+Zn
Zn-Hg
H3COCHC PhC C
C H COCH3
Hg-Zn H3CH2CH2CH2C HCl
Hg-Zn HCl
第六章 还原反应及其 工艺
Reduction and Technique
主要内容
• 还原反应的定义、方法、分类 • 不同官能团还原难易比较 • 活泼金属及其合金( Fe、Zn、Na、Zn-Hg )
反应机理、应用及主要影晌因素
• 硫化碱还原反应机理、应用 • 亚硫酸盐还原反应机理、应用 • 金属复氢化合物还原反应机理、应用 • 醇铝还原剂反应机理、应用 • 催化氢化
第六章 还原反应

CH3
6.3
金属还原剂
3 .以锂(钠)金属将苯还原成双烯类( diene ),称为 Brich 还原反应。此反应需在含质子溶剂中进行。
OCH3 Li,NH3 t BuOH OCH3 H3+O O
6. 2 金属氢化物还原
3. 硼烷(BH3)
硼烷(borane)是由硼氢化钠与三氟化硼制备,以
二硼烷 B2H6(diborane)的形式存在。
3 NaBH4 + 4 BF3
H B H H H B H H
2 B2H6 + 3 NaBF4
硼烷和二硼烷具有 Lewis Acid 的 特性,因此反应性与 NaBH4 或 LiAlH4 不同。 它容易与羧酸及烯烃反应,却 不与酰卤,卤代烷,砜或硝基化合物 等作用。
O H2,(Ph3P)3RhCl PhH, 25 ¡ æ ,1 atm O
6.1 催化氢化(加氢反应)
一般官能团化合物的加氢反应
反应性 最高 反应物 RCOCl RCH2NO2 RC≡CR′ RCHO RCH=CHR′ RCOR′ ArCH2X RC≡N RCO2R′ RCONHR′ 氢化产物 RCHO RCH2NH2 RCH=CHR′(Z,Cis) RCH2OH RCH2CH2R′ RCH(OH)R′ ArCH3 RCH2NH2 RCH2OH + R′OH RCH2NHR
6. 2 金属氢化物还原
1. 氢化锂铝
一般官能团化合物与氢化锂铝 LiAlH4 作用 反应性 最高 C=O COOR 递 减 CN CONR2 C-NO2 CHBr 最低 CH2OSO2Ar 反应物 CHOH CH2OH CH2NH2 CH2NR2 CNH2 CH2 CH3 氢化产物
第六章 还原反应

影响催化氢化反应的主要因素
• 催化剂 • 被氢化物的结构与性能 • 温度和压力 • 溶剂的极性与酸碱度 • 搅拌
影响催化氢化反应的主要因素
• 催化剂的影响
H2,Raney镍
COOC2H5
COOC2H5
50oC,10.13MPa H2,CuCr2O4 160oC,27.56MPa
CH2OH
催化剂应根据被氢化物结构和目的产物而定 在催化氢化中不允许任意加大催化剂用量,以避 免氢化反应难以控制
第六章 还原反应
§6.1概述 §6.2催化氢化 §6.3化学还原
6.1概述 • 定义 • 反应的重要性 • 还原剂 • 还原方法
定义
广义地讲,在还原剂的参与下,能使某 原子得到电子或电子云密度增加的反应称为 还原反应。 狭义地讲,在有机分子中增加氢或减少 氧的反应,或者兼而有之的反应称为还原反 应。
OH
OH
260oC
4
9.81×10 Pa
R C H
多
R‘ C H
少
R—C C—R‘
Lindlar催化剂 H2
室温 >0.29MPa 室温
RCH2CH2R’ + RCH=CHR’
•溶剂的极性的影响
甲醇或乙醇
苯或环己烷
•搅拌效率的影响
(1)影响催化剂在反应介质中的分布情况、 面积和催化效果; (2)有利于传热,防止局部过热。
RCH2OH + R'OH
RCONH2
RCH2NH2
R
R
RCOOH
RCH2OH
RCOONa
分子结构不同,催化氢化的难易程度不同: 炔>烯>ArH 醛>酮>腈>酸 空间效应越大,越不易靠近催化剂,需要强化反 应条件,如升高温度、增加压力、提高催化剂活 性等。
6章 还原

NH2
NH2
NH2
(3)能溶于热水、但在冷水中溶解度低的芳胺,如邻 苯二胺、氨基苯酚。 分离方法:热过滤、冷却结晶。
NH2 NH2 OH OH NH2
NH2
(4)含-SO3H和-COOH的芳胺,如氨基萘磺酸。 分离方法:加碱中和生成溶于水的盐,然后过滤, 再酸化析出或盐析。
OH NH2
OCH3 NH2 O 2N
OCH3 NH2
NH2
NH2
NH2
NH2
CH3 Cl
CH3 Cl
OCH3 NH2
OCH3
NH2
NH2 NH2
NH2 O NH2 O
NH2 NH2
O
NH2
O
第五节 催化氢化
催化氢化按其反应类型可分为氢化(加氢)反应和氢解 反应。 催化氢化:在催化剂的存在下,含有不饱和键的有机 物分子与氢分子反应,使不饱和键全部或部分加氢的 反应。 催化氢化是π 键断裂与氢加成的反应。 常发生氢化的不饱和键有:碳碳双键和叁键、羰基、 氰基、醛基、芳环和芳杂环等。
(3)金属复氢化合物:LiAlH4、NaBH4、KBH4等;
1.3.2 有机还原剂
乙醇、甲醛、甲酸、烷氧基铝(Al[OCH(CH3)2]3)等。
第二节
铁粉还原
2.1 铁粉还原硝基的反应历程 铁的还原反应是通过电子转移而实现的。首先是铁 失去电子转变成铁离子,被还原的基团(-NO2)得到 电子生成负离子自由基,然后再从质子给与体(如 水)得到质子,生成目的产物。 铁粉还原硝基苯的反应历程:
(1)被还原物结构:当芳环上有吸电子基团时,
(2)铁粉的质量和用量 粒度:60~100目;
质量:干净、质软灰铸铁(含有碳、硅、硫等杂质); 用量:3~4molFe/molArNO2(理论为2.25 mol),
轻化工合成原理第6章-讲义
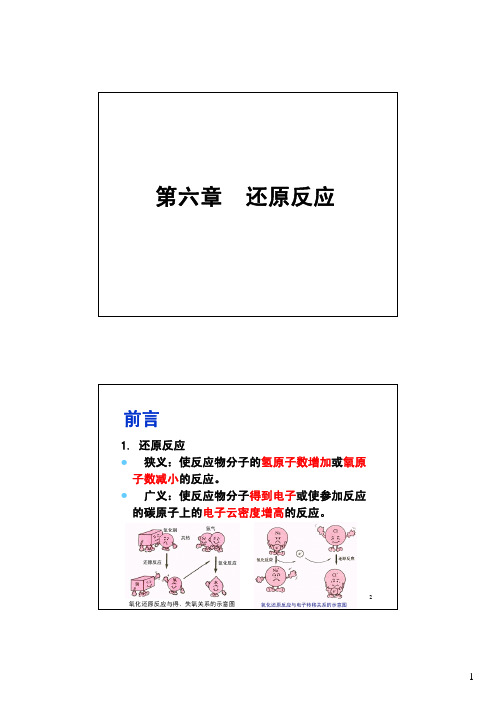
前言1. 还原反应z狭义:使反应物分子的氢原子数增加或氧原子数减小的反应。
z广义:使反应物分子得到电子或使参加反应的碳原子上的电子云密度增高的反应。
232. 还原方法z 化学还原:除氢以外的化学物质作还原剂的方法z 催化加氢:用氢在催化剂作用下进行还原的方法均相催化氢化:催化剂溶于反应介质非均相催化氢化液相催化氢化气固相催化氢化z 电解还原:在电解槽阴极室进行还原的方法4z 还原反应的分类:¾碳-碳不饱和键的还原¾碳-氧键的还原:如醛羰基还原成醇羟基或甲基;酮羰基还原为醇羟基或次甲基;羧基还原成醇羟基;羧酰氯还原成醛基或羟基等。
¾含氮基的还原:硝基和亚硝基还原为羟氨基和氨基等;硝基还原成氧化偶氮基、偶氮基或加氢偶氮基等。
56.1 化学还原有机还原剂:乙醇、甲醛、甲酸、烷氧基铝等。
金属:NaHS 、Na 2S 、Na 2S x 、Na 2SO 3、NaHSO 3、Na 2S 2O 4、SnCl 2、FeCl 2、TiCl 3非金属:SO 2、NH 2OH 和H 2NNH 2等活泼金属及其合金:Fe 、Zn 、Na 、Zn-Hg 、Na-Hg 低价元素化合物金属复氢化合物:NaBH 4、KBH 4、LiBH 4、LiAlH 4等无机还原剂66.1.1 铁粉还原z 以金属铁为还原剂,反应在电解质溶液中进行z 选择性还原剂(硝基或其它含氮的基团)z 工艺成熟、简单,适用范围广z 副反应少z 对设备要求低z 产生大量的含胺铁泥和废水11NH 4Cl >FeCl 2>(NH 4)2SO 4>BaCl 2>CaCl 2>NaCl 最常用的电解质是FeCl 2,可在还原前先加入少量盐酸及铁屑制成,工业上称为“铁的预蚀”。
3) 电解质-电解质可提高溶液的导电能力,加速铁的腐蚀过程,还原速度取决于电解质的性质和浓度。
4) 温度-一般为95-105℃。
铁粉还原为强烈放热反应,若加料太快,反应过于激烈,会导致暴沸溢料。
无机化学 氧化还原反应

E 与反应计量系数无关,无加和性 与反应式的书写方向无关
Fe3+ + e-=Fe2+ E = 0.771 V 2Fe3++ 2e-=2Fe2+ E = 0.771 V, 而非0.771×2 Fe2+ - e- =Fe3+ E = 0.771V, Fe2+ =Fe3+ + e- 而非 - 0.771 V
第六章 氧化还原
PLEASE ENTER YOUR TITLE HERE
第一节 氧化还原反应 第二节 电池的电动势和电极电势 第三节 氧化还原平衡 第四节 影响电极电势的因素 第五节 元素电势图
电负性:元素的原子在分子中吸引电子能力的相对大小
元素电负性的周期性变化与金属性、非金属性的一致
金属-金属离子电极
金属-金属难溶盐-阴离子电极
氧化还原电极
气体-离子电极
三、常用电极类型氧Leabharlann 还原电对: Ag+ / Ag
电极组成式: Ag+(c) | Ag(s)
电极反应:
由金属板插入到该金属的盐溶液中构成
01
03
02
04
例:银电极
1.金属-金属离子电极
将金属表面涂渍上其金属难溶盐的固体,然后浸入到与该电解质具有相同阴离子的溶液中构成的电极
(1) 两个半电池反应分别为: 正极 MnO4-+ 8H+ + 5e-=Mn2+ + 4H2O 负极 H2O2=2H+ + O2 + 2e- (2)电极组成为: 正极 MnO4- (c1), Mn2+ (c2), H+ (c3) | Pt (s) 负极 H+ (c4), H2O2 (c5) | O2 (p) | Pt (s) (3)电池组成式为: (-) Pt |O2 (p) | H2O2 (c5), H+ (c4)‖MnO4- (c1), Mn2+(c2), H+(c3) | Pt (+)
分析化学第6章氧化还原滴定法

表示:
Ox/Red
O Ox/Red
RT nF
ln
aOx aRed
O Ox/Red
0.059 lg n
aOx aRed
: 电对的标准电极电位(Standard Electrode Potential)
2019年10月23日5时5分
Ox/Red
O Ox/Red
RT ln aOx nF aRed
Cu 2/Cu
O C u2 /C u
0.059
lg
[Cu2 ] [Cu ]
O 0.059 lg [Cu2 ][I ]
C u2 /C u
KSp[CuI]
若控制[Cu2+] = [I-] = 1.0 mol ·L-1则: Cu2/Cu 0.87 V
2019年10月23日5时5分
第六章 氧化还原滴定法
6.1 氧化还原反应平衡 6.2 O.R反应进行的程度 6.3 O.R反应的速率与影响因素 6.4 O.R滴定曲线及终点的确定 6.5 O.R滴定法中的预处理 6.6 高锰酸钾法 6.7 重铬酸钾法 6.8 碘 量 法 6.9 其他氧化还原滴定法 6.10 氧化还原滴定结果的计算
2019年10月23日5时5分
n2 Ox1 + n1 Red2 = n2 Red1 + n1 Ox2 两个半电池反应的电极电位为:
1
1O'
0.059 n1
lg
cOx1 cRed1
2
O' 2
0.059 n2
lg
cOx2 cRed2
滴定过程中,达到平衡时(1 = 2):
第六章 还原反应jxau

Nitriles to aldehydes
Vinyl esters to allylic alcohols
Reduction Reactions
6.2 Metal hydride
环氧乙烷类及羰基化合物被氢化锂铝或二异丁基氢化铝还原成醇类,反 应的进行可能受动力学控制,也可能受热力学控制(溶剂对反应的影响)。
H
H2,Pd C EtOAc,r.t; 97%
Lindlar(林德拉)催化剂 Pd/BaSO4/喹啉
炔
Lindlar
烯
Reduction Reactions
6.1 Hydrogenation
Rosenmund Reduction(罗森蒙德反应)
催化氢化选择性还原醛的反应
酰氯用受过硫-喹啉毒化的钯催化剂进行催化还原,生成相应的醛
反应性
最高
反应物
RCOCl RCH2NO2 RC≡CR′ RCHO RCH=CHR′ RCOR′ ArCH2X RC≡N RCO2R′ RCONHR′
氢化产物
RCHO RCH2NH2 RCH=CHR′(Z,Cis) RCH2OH RCH2CH2R′ RCH(OH)R′ ArCH3 RCH2NH2 RCH2OH + R′OH RCH2NHR
O R C H + (Ph3P)RhCl R H + (Ph3P)2RhCl(CO) + Ph3P
H2
Reduction Reactions
6.1 Hydrogenation
3)加氢反应受催化剂,取代物及溶剂等诸方面的影响, 可能产生不同的异构产物,但真正的反应机理则尚待 研究中。
H H2 OH O PtO2 Pd C cat cat OH
6 第六章 还 原(学习要点)

(3)
Cl
2013年
7
(4) 、金属复氢化合物既可以对碳-杂原子或杂原子-杂原子间极化双键(C=O、C=N、N=O、S=O等) 可发生亲核进攻而加氢,又 可以对极化程度此较弱双键(C=C) 发生加氢反应。 ( ) 。 (5) 、四氢铝锂遇到水、酸、含羟基或巯基(SH)的有机化合物会放出氢气而生成相应的铝盐,,因此必须无水条件下使用。 (6) 、对硝基苯甲醛的还原制备对硝基苯甲醇时,既可以用LiAlH4又可以用NaBH4做还原剂。 (7) 、骨架镍催化剂的使用条件:弱碱性或中性条件下使用。 12、讲过的课后作业。
本章学习要点:
1、基本概念:还原 2、不同官能团还原难易的比较。 3、写出以硝基苯为为原料,铁粉、锌粉以还原剂的反应历程? 4、铁粉作为还原剂时,铁粉的质量和用量如何控制?为什么? 5、锌粉在NaOH水溶液的强碱性条件下,可使硝基苯发生双分子还原反应,依次生成( )、( )、( )。
6、锌粉在NaOH水溶液的强碱性条件下,可使硝基苯发生双分子还原反应,依次生成氧化偶氮苯、偶氮苯、氢化偶氮苯,为了 得到苯基羟胺、氧化偶氮苯、氢化偶氮苯,如何控制碱度和温度? 7、新制骨架镍催化剂和干燥骨架镍催化剂各有什么特点?新制骨架镍催化剂如何存放?废弃骨架镍催化剂处理如何处理? 8、骨架镍催化剂和铂催化剂的毒物是什么? 10、 11、下列陈述是否正确: (1)、 芳环上的磺酸基活性很高,可以被铁还原成芳磺酰氯或亚磺酸。 (2) 、对于芳香族多硝基化合物的部分还原,通常采用Na2S2、NaHS或Na2S+NaHCO3作为还原剂,羟基和甲氧基对位的硝基优 先还原。 (3) 、对于2,4-二硝基甲苯的部分还原,可以采用Na2S2、NaHS或Na2S+NaHCO3作为还原剂3年
第六章还原反应

(R3P)3RhCl
1.机理
H-H H H
C
C H H C C
catalyst surface C H H C C H C H
多相催化 :在不溶于反应体系中的固体催化剂 的作用下,氢气还原在液相中的底物的反应。
2. 类型
催化氢化 Hydrogenation
催化氢解
Hydrogenolysis
均相催化 Heterogenous 多相催化 Homogenous
b.脱硫
(2)铂催化剂 活性很强
可以还原除了酯、羧酸和酰胺外,各种不饱和基 团均可被还原。如:醛酮、腈、硝基化合物,还 原氨化反应等。反应通常可在较低温度和较低氢 气压力下反应。 铂黑、铂炭、二氧化铂等。
比较最常用的是二氧化铂(PtO2),(Adams catalyst), 在使用时被还原成铂。
还原活性从高到低:
C=O > COOR> CN> CONR2> C-NO2> CHBr > CH2OSO2Ar
制备:
4LiH + AlCl3 Et2O 3LiCl3 + LiAlH4
遇水分解:
(1)用1M氢化铝锂溶液进行还原时很方便. (2)用较少量溶剂和粉状铝氢化锂混合成稀糊状直 接应用. 此时要注意氢化铝锂用量,至少要过量10%,以保证 有足够的纯LiAlH4进行反应.在特殊的情况下有时甚 至过量2—4倍,才能使反应进行完全。
PhNHOH
PhCH2OH NH2
NH2
特点:较氧化反应易于控制。 类型: (1)活泼金属Fe/HCl, Zn/HOAc,Na/ROH, ZnHg/HCl,Na-Hg/EtOH等 (2)低价元素的化合物 Na2S2O4, NaS, FeCl2, SnCl2, TiCl3, TiCl2等 (3)金属氢化物 NaBH4, LiAlH4, (4)催化加氢 Pd, Pt, Ni, /H2. (5) 有机金属还原剂: 异丙醇铝,叔丁醇铝,甲醛,葡 萄糖。 (6)非金属:Me2S, Ph3P
无机化学第六章氧化还原总结

298.15K,忽略 离子强度时
0.0592 n
lg
Ox Red
n 为电极反应中转移的电子数; 式中: [Ox ]为电极反应中氧化型一侧各物质浓度幂的乘积
注意
[Red]为电极反应中还原型一侧各物质浓度幂的乘积
1)纯液体、固体不出现在方程式中。气体用分压(p/p) 表示;(p以kPa为单位, p=100kPa)
已知 (Cl2 / Cl-) = 1.36 V, 当[ Cl- ] = 10 mol·L-1 , p(Cl2) = 1.0 kPa 时, (Cl2 / Cl-) 的值是 ( 1.24V )
I2 + 2e- 2I-
(I2/ I )
(I2/ I )
0.0592 1 2 lg [ I ]2
0.535
利用 ´计算 的 Nernst 方程:
/ 0.0592 lg cOx
n
cRe d
2、氧化还原滴定曲线计算(电极电势)
(1)计量点前——根据被滴定电对计算
(2)化学计量点sp
SP
n11 '
n1
n22 '
n2
适用于对称电对——电极反应中 氧化型、还原型前的系数相同。
(3)计量点后——根据滴定剂电对计算
AgI /Ag :
AgI + e- Ag + I- ;
Cl2/Cl- :
Cl2 + 2e- 2Cl-
(-)Ag ︱ AgI (s) | I- (c1) ‖Cl- (c2)︱Cl2 (P ) ,Pt (+)
:写出反应 I2 + 2S2O32- = 2I- + S4O62- 所对应的原电池符号: 解:根据反应式可知:
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
在电解质存在下将硝基还原为氨基时,先加入大部分铁粉, 再慢慢加入被还原物。 不可行。会有部分铁粉与水作用释放氢气而损失铁粉,并增 加搅拌器的动力消耗。应先加入盐酸和少量铁粉进行预蚀, 然后加入硝基物,并慢慢加入铁粉。
第六章还原反应及其工艺
2、锌粉还原
锌粉的还原能力
还原能力比铁粉强。 还原性与反应介质有关:可在碱性、酸性条件下进行。 可用于还原硝基、亚硝基、氰基、羰基等多种官能团。 缺点:价格比铁粉贵得多。
冷凝器
第六章还原反应及其工艺
铁粉还原适用范围:
硝基还原为氨基:铁粉还原法生产维生素B6,可避免发生氯的脱落
、氰基还原、酯基的水解等副反应,收率达到90%。加氢还原,收
率只有50%。
O2N
CO2C2H5 CN Fe/HCl
H2N
CO2C2H5 CN
H3C N Cl CH3CO2H H3C N Cl
N H 2+ 3 F e 3 O 4
ΔfHm 4x12.5
0 4x(-258.83) 4x31.3
硝基苯铁屑还原的摩尔焓变:
3x(-1184.4)
ΔfHm=1/4【4x31.3+3x(-1184.4)-4x(-285.83)】=-534.17kJ/mol 因为铁原子氧化成Fe3O4是强放热反应,铁粉还原反应表现为强放热反应。
NaHSO3、SnCl2等。 金属复氢化合物:
NaBH4、KBH4、LiAlH4等。
第六章还原反应及其工艺
1、铁粉还原
1854年Bechamp发现硝基化合物的铁屑还原法。由于工 艺简单、对设备要求低等优点,曾占有重要地位。 缺点:产生大量含有芳胺的铁泥和废水,造成严重的环 境污染。逐步为加氢还原法所代替。 优点:铁的给电子能力较弱,只适用于容易还原的基团 的还原,而卤素等不被还原。因此,可选择性还原某些 基团。
C
N H
O
C
Zn/HCl C2H5
S
C
C6H5 C
O
H N
2
N H
选择性还原C=O成亚甲基,而不影响其它羰基。 扑痫酮
第六章还原反应及其工艺
水和反应溶剂的影响: 水是质子给体,是必需的。用量是被还原物的50-100倍(mole)。 当反应物在水中难溶解时,可适当加入甲醇或乙醇。 反应温度的影响:
通常在接近反应液沸腾温度下反应。 铁粉还原反应是强放热反应,加料太快,反应过于剧烈,会导致爆沸甚
至溢锅。
4
N O 2+ 9 F e+ 4 H 2 O 4
本章内容
化学还原:使用氢以外的化学物质作还原剂。
金属与供质子剂还原法 含硫负离子还原法 金属氢化物还原法
催化氢化:氢在催化剂的作用下使有机物还原。
第六章还原反应及其工艺
一、化学还原
化学还原:使用氢以外的化学物质作还原剂。
活泼金属及其合金:铁粉、锌粉、铝粉等。 低价元素的化合物:NaHS、Na2S、Na2Sx、Na2SO3、
Ar-NO+2e+2H+
Ar-NHOH
Ar-NHOH+2e+2H+
Ar-NH2+H2O
总反应:4 A r N O 2 + 9 F e + 4 H 2 O 4 A r - N H 2 + 3 F e 3 O 4
由反应可知:每摩尔硝基物理论上需要2.25摩尔铁屑,实际为3-4摩尔。
第六章还原反应及其工艺
维生素B6
羰基还原为羟基:醛还原为醇通常采用加氢还原法,但正庚醛还原 为正庚醇采用铁粉还原法。
F e/H C l
C 6 H 1 3 -C H O
C 6 H 1 3 -C H 2 O H
1 0 0 O C
第六章还原反应及其工艺
制备硫酚类化合物:
芳磺酸相当稳定,不易被还原为硫酚,通常由芳磺 酰氯还原制得(硫酚易被空气氧化为二硫化物,常 加入抗氧剂)。
锌粉的储存:
锌粉容易被氧化,因此不宜久存。 特别是在碱性条件下还原时,须采用新鲜的锌粉。
第六章还原反应及其工艺
酸性条件下还原
C=S双键选择性还原脱硫成亚甲基,而不影响其它C=O双键。
C2H5 C6H5
CO2C2H5
S
C
+ H2NCNH2
CO 2C 2H 5
O
C C2H5
C C6H5
C
O
H N
铁屑?
第六章还原反应及其工艺
电解质的影响:
微电池反应原理:电解质增加水溶液的导电性,加速铁的电化学 腐蚀,反应速度加快。
保持介质的pH=3.5-5,使溶液中有铁离子存在。间歇还原时 ,需 补加电解质。
常用电解质是氯化铵、氯化亚铁,用量为被还原物的10-20%,浓 度在3%左右。
适当增加电解质的浓度可使还原速度加快。浓度过高,则将使还 原速度减慢。如氯化亚铁达到0.4mol时,由于氧化铁表面的吸附而 使还原速率降低。
铁屑还原反应的影响因素
硝基化合物结构的影响:
芳环上有吸电子基团时,硝基接受电子能力增加,容易被还原。 芳环上有给电子基团时,硝基接受电子能力减弱,不易被还原。
铁粉的影响:
洁净、粒细和质软的灰铸铁屑,优于组成比较纯净的钢屑。 通常使用60-100目铁粉。太粗的铁粉表面积小,反应慢;太细的
铁粉,后处理困难。 用量:每摩尔硝基物理论上需要2.25摩尔铁屑,实际为3-4摩尔。 思考:1mole间二硝基苯还原为间二氨基苯理论上需要多少摩尔
Cl
Cl
Fe /H 2SO 4 105-110OC
SO 2C l
SH
第六章还原反应及其工艺
思考题
在电解质存在下将硝基还原为氨基时,先加入全部被还原物, 然后一次加入大部分铁粉或全部铁粉。 不可行。用铁粉将硝基还原为氨基是强放热反应,在沸腾温 度下,加铁屑太快,会使反应物爆沸或溢锅。应慢慢加入铁 粉。
第六章还原反应及其工艺
还原过程
铁粉还原反应原理:
通过电子转移而实现的,其中铁是给电子体,被还原物首先在铁表 面得到电子,再从质子给体(水、醇等)得到质子被还原。
电解质:稀盐酸、稀硫酸、醋酸、氯化铵或FeCl2等水溶液。 负极:F e0 F e2 + + 2 e
正极: ArNO2+2e+2H+
Ar-NO+H2O
第六章还原反应及其工艺
搅拌的影响:
铁粉比较重,需要良好的搅拌,否则容易沉到反应器底部。 衬有耐酸砖的平底钢槽和铸铁慢速耙式搅拌器。 新式反应器:衬耐酸砖的球底钢槽和不锈钢快速螺旋桨式搅拌器。
耙式搅拌器
耙臂上安装 多组可调节刮 板,搅拌物质 可从弧线形刮 板的间隙通过, 搅拌阻力小, 降低搅拌电机 的功耗。
