酯的氨解
苯甲酸甲酯的氨解

苯甲酸甲酯的氨解苯甲酸甲酯,化学式为C8H8O2,是一个广泛应用于化学工业的有机化合物。
它具有特殊的化学性质,其中包括氨解反应。
本文将重点介绍苯甲酸甲酯的氨解反应及其相关应用。
一、苯甲酸甲酯的氨解反应概述苯甲酸甲酯的氨解反应是指苯甲酸甲酯与氨(NH3)在适当条件下发生反应,生成苯甲酸和甲胺。
该反应是一种酯的水解反应,也被称为酯水解。
苯甲酸甲酯的氨解反应可以通过加热或催化剂的作用来进行。
在常温下,苯甲酸甲酯与氨的反应速度较慢,需要较长的反应时间。
但是,使用催化剂可以加速反应速率,提高反应效率。
二、苯甲酸甲酯氨解反应的机理在苯甲酸甲酯的氨解反应中,催化剂通常起到促进反应的作用。
常用的催化剂包括氢氧化钠(NaOH)、氨基催化剂等。
这些催化剂能够提高反应中间体的活性,降低反应活化能,从而加速反应进程。
苯甲酸甲酯的氨解反应可以分为以下几个步骤:1. 水解反应:苯甲酸甲酯在水的存在下与氢氧化钠发生水解,生成苯甲酸盐。
C8H8O2 + NaOH → C6H5COONa + CH3OH2. 中和反应:苯甲酸盐与氨发生中和反应,生成苯甲酸和甲胺。
C6H5COONa + NH3 → C6H5COOH + CH3NH23. 氨解反应:甲酯中的甲基与甲胺发生反应,生成苯甲酸和二甲胺。
CH3OC6H5 + CH3NH2 → C6H5COOH + CH3NHCH3以上反应步骤是苯甲酸甲酯的氨解反应的主要过程,并且受催化剂的调节。
三、苯甲酸甲酯的氨解反应的应用1. 生产苯甲酸:苯甲酸甲酯的氨解反应是常见的合成苯甲酸的方法之一。
通过该反应,可以将苯甲酸甲酯转化为苯甲酸,用于医药、染料、香料等行业的生产。
2. 生产甲胺:苯甲酸甲酯的氨解反应还可用于甲胺的合成。
甲胺是一种重要的有机合成中间体,广泛应用于医药、农药等领域。
3. 催化剂研究:苯甲酸甲酯的氨解反应中,催化剂起到了关键作用。
通过研究不同催化剂的应用,可以提高反应效率,优化反应条件,推动催化剂领域的发展。
酯交换为酰胺-060123

经典化学合成反应标准操作酯交换为酰胺编者:杜晓行药明康德新药开发有限公司化学合成部目录1.前言 (2)2.酯交换为酰胺 (2)3.酯交换为N-取代酰胺 (2)1.前言酯和氨水反应可以很方便地得到酰胺。
N-取代酰胺一般可以利用相应的胺与酯直接反应得到,在有些条件下,需要有铝试剂的存在反应才能够顺利进行。
2.酯与氨交换一般酯的氨解通过氨的醇溶液或氨水来进行。
氨的醇溶剂氨解反应可通过加入适量的甲醇钠和氰化钠来催化。
用氨水直接氨解一般需要加热(当该反应温度到100度时,一定要用高压釜做这一反应),这类反应一般可以通过硫酸铜来进行催化。
反应的条件选择主要看酯的活性程度,一般脂肪酸酯的交换要比芳香羧酸酯来得容易,甲酯要比乙酯来得快。
对脂肪酸酯,α位的位阻大小也决定了反应的快慢。
酯通过甲酰胺在乙醇钠的存在下,高温也可得到相应的酰胺。
这一方法对各类的酯都比较有效,只是产品的分离比直接氨解稍微麻烦一些,但反应较快。
另外近年来,AlMe 3-NH 4Cl 或Me 2AlNH 2在多官能团及复杂化合物的合成中用的较多,该方法条件较强,各类酯都能很快的氨解。
其缺点是AlMe 3易自燃,操作不是太方便。
2.1 氨水用于脂肪羧酸酯氨解示例[1]NO OOOO NO H 2NOO NH OHTo ethyl 5-ethoxycarbonylmethyl-3-methylisoxazole-4-carboxylate (1.00 g, 4.15 mmol) was added an excess of conc. aqueous ammonia (d = 0.88 kg·dm -3, 5.0 cm 3) and EtOH (3.0 cm 3), and the suspension was stirred vigorously at room temperature for 14 h. After this period a white solid had precipitated which was filtered and recrystallized (EtOAc) to yield the desired product as a white solid (0.81 g, 92%).NO OOOO NO HNOOO MeNH 2 / toluenePrepared as described above for ethyl 5-carbamoylmethyl-3-methylisoxazole-4-carboxylate but using methyl-5-ethoxycarbonyl- 3-methylisoxazole-4-carboxylate (1.00 g, 4.15 mmol) and methylamine in toluene (30% w/v, 10.0 cm 3), to yield the desired product as a white solid (0.93 g, 99%).2.2 氨甲醇氨解脂肪羧酸酯示例[2] [3]NH O OCOOEtNH OO CONHMe MeNH / MeOHThe ester (4.11 g, 14 mmol) was dissolved in absol. methanolic ammonia (100 ml, 20 % NH 3), and the solution was allowed to stand at temperature for 3 days, the solvent was then evaporated, and the resulting crystalline was purified by recrystallization.2.3 氨水用于芳香羧酸酯氨解示例[4]NNCONH 2To an autoclave, was added methyl 6-methylniconate (500 g, 3.31 mol), sat. aq. NH 4OH (500 ml) and ethanol (500 ml). After sealing, the reaction was heated to 80℃ for 2 days. The cooled reaction mixture was filtrated, and the filter cake was recrystallized to afford white solid (247 g, 54.8%)。
酯的氨解
亲核试剂:在反应过程中供给电子进攻反应物中带部分正电荷原子的试剂称为亲核试剂。
常见的亲电试剂与亲核试剂如下:酯与胺反应生成酰胺双分子亲核取代反应S N2反应(双分子亲核取代反应)是亲核取代反应的一类,其中S代表取代(Substitution),N代表亲核(Nucleophilic),2代表反应的决速步涉及两种分子。
与S N1反应相对应,S N2反应中,亲核试剂带着一对孤对电子进攻具亲电性的缺电子中心原子,形成过渡态的同时,离去基团离去。
反应中不生成碳正离子,速率控制步骤是上述的协同步骤,反应速率与两种物质的浓度成正比,因此称为双分子亲核取代反应。
反应机理S N2反应最常发生在脂肪族sp3杂化的碳原子上,碳原子与一个电负性强、稳定的离去基团(X)相连。
亲核试剂(Nu)从离去基团的正后方进攻碳原子,Nu-C-X角度为180°,以使其孤对电子与C-X键的σ*反键轨道可以达到最大重叠。
然后形成一个五配位的反应过渡态,碳约为sp2杂化,用两个垂直于平面的p轨道分别与离去基团和亲核试剂成键。
C-X的断裂与新的C-Nu键的形成是同时的,X很快离去,形成含C-Nu键的新化合物。
由于亲核试剂是从离去基团的背面进攻,故如果受进攻的原子具有手性,则反应后手性原子的立体化学发生构型翻转,也称“瓦尔登翻转”。
这也是S N2反应在立体化学上的重要特征。
反应过程类似于大风将雨伞由里向外翻转。
例如溴乙烷与氢氧根离子发生S N2生成乙醇和溴离子。
上例中,OH−(亲核试剂)进攻C2H5Br(底物)发生S N2反应,经过不稳定的过渡态,最终Br−离去,得到乙醇。
S N2反应一般发生在伯碳原子上,很难成为有位阻分子的反应机理,并且取代基越多,按S N2机理反应的可能性越小。
基团在空间上比较拥挤的分子一般采用S N1机理,可以缓解一部分的位阻,也可生成较稳定的碳正离子(通常为三级碳正离子)。
影响因素离去基团的碱性:离去基团的碱性越强,其离去能力越弱,反之亦然。
酯交换为酰胺-060123

经典化学合成反应标准操作酯交换为酰胺目录1.前言 (2)2.酯交换为酰胺 (2)3.酯交换为N-取代酰胺 (2)1.前言酯和氨水反应可以很方便地得到酰胺。
N-取代酰胺一般可以利用相应的胺与酯直接反应得到,在有些条件下,需要有铝试剂的存在反应才能够顺利进行。
2.酯与氨交换一般酯的氨解通过氨的醇溶液或氨水来进行。
氨的醇溶剂氨解反应可通过加入适量的甲醇钠和氰化钠来催化。
用氨水直接氨解一般需要加热(当该反应温度到100度时,一定要用高压釜做这一反应),这类反应一般可以通过硫酸铜来进行催化。
反应的条件选择主要看酯的活性程度,一般脂肪酸酯的交换要比芳香羧酸酯来得容易,甲酯要比乙酯来得快。
对脂肪酸酯,α位的位阻大小也决定了反应的快慢。
酯通过甲酰胺在乙醇钠的存在下,高温也可得到相应的酰胺。
这一方法对各类的酯都比较有效,只是产品的分离比直接氨解稍微麻烦一些,但反应较快。
另外近年来,AlMe 3-NH 4Cl 或Me 2AlNH 2在多官能团及复杂化合物的合成中用的较多,该方法条件较强,各类酯都能很快的氨解。
其缺点是AlMe 3易自燃,操作不是太方便。
2.1 氨水用于脂肪羧酸酯氨解示例[1]NO OOO NO H 2NOOO NH OHTo ethyl 5-ethoxycarbonylmethyl-3-methylisoxazole-4-carboxylate (1.00 g, 4.15 mmol) was added an excess of conc. aqueous ammonia (d = 0.88 kg·dm -3, 5.0 cm 3) and EtOH (3.0 cm 3), and the suspension was stirred vigorously at room temperature for 14 h. After this period a white solid had precipitated which was filtered and recrystallized (EtOAc) to yield the desired product as a white solid (0.81 g, 92%).NO OOO NO HNOO MeNH 2 / toluenePrepared as described above for ethyl 5-carbamoylmethyl-3-methylisoxazole-4-carboxylate but using methyl-5-ethoxycarbonyl- 3-methylisoxazole-4-carboxylate (1.00 g, 4.15 mmol) and methylamine in toluene (30% w/v, 10.0 cm 3), to yield the desired product as a white solid (0.93 g, 99%).2.2 氨甲醇氨解脂肪羧酸酯示例[2] [3]NH O OCOOEtNH OO CONHMe MeNH / MeOHThe ester (4.11 g, 14 mmol) was dissolved in absol. methanolic ammonia (100 ml, 20 % NH 3), and the solution was allowed to stand at temperature for 3 days, the solvent was then evaporated, and the resulting crystalline was purified by recrystallization.2.3 氨水用于芳香羧酸酯氨解示例[4]NNH OHNCONH 2To an autoclave, was added methyl 6-methylniconate (500 g, 3.31 mol), sat. aq. NH 4OH (500 ml) and ethanol (500 ml). After sealing, the reaction was heated to 80℃ for 2 days. The cooled reaction mixture was filtrated, and the filter cake was recrystallized to afford white solid (247 g, 54.8%)。
酯交换为酰胺

经典化学合成反应标准操作酯交换为酰胺编者:杜晓行药明康德新药开发有限公司化学合成部目录1.前言 (2)2.酯交换为酰胺 (2)3.酯交换为N-取代酰胺 (2)1.前言酯和氨水反应可以很方便地得到酰胺。
N-取代酰胺一般可以利用相应的胺与酯直接反应得到,在有些条件下,需要有铝试剂的存在反应才能够顺利进行。
2.酯与氨交换一般酯的氨解通过氨的醇溶液或氨水来进行。
氨的醇溶剂氨解反应可通过加入适量的甲醇钠和氰化钠来催化。
用氨水直接氨解一般需要加热(当该反应温度到100度时,一定要用高压釜做这一反应),这类反应一般可以通过硫酸铜来进行催化。
反应的条件选择主要看酯的活性程度,一般脂肪酸酯的交换要比芳香羧酸酯来得容易,甲酯要比乙酯来得快。
对脂肪酸酯,α位的位阻大小也决定了反应的快慢。
酯通过甲酰胺在乙醇钠的存在下,高温也可得到相应的酰胺。
这一方法对各类的酯都比较有效,只是产品的分离比直接氨解稍微麻烦一些,但反应较快。
另外近年来,AlMe 3-NH 4Cl 或Me 2AlNH 2在多官能团及复杂化合物的合成中用的较多,该方法条件较强,各类酯都能很快的氨解。
其缺点是AlMe 3易自燃,操作不是太方便。
2.1 氨水用于脂肪羧酸酯氨解示例[1]NO OOO NO H 2NOOO NH OHTo ethyl 5-ethoxycarbonylmethyl-3-methylisoxazole-4-carboxylate (1.00 g, 4.15 mmol) was added an excess of conc. aqueous ammonia (d = 0.88 kg·dm -3, 5.0 cm 3) and EtOH (3.0 cm 3), and the suspension was stirred vigorously at room temperature for 14 h. After this period a white solid had precipitated which was filtered and recrystallized (EtOAc) to yield the desired product as a white solid (0.81 g, 92%).NO OOOO NO HNOOO MeNH 2 / toluenePrepared as described above for ethyl 5-carbamoylmethyl-3-methylisoxazole-4-carboxylate but using methyl-5-ethoxycarbonyl- 3-methylisoxazole-4-carboxylate (1.00 g, 4.15 mmol) and methylamine in toluene (30% w/v, 10.0 cm 3), to yield the desired product as a white solid (0.93 g, 99%).2.2 氨甲醇氨解脂肪羧酸酯示例[2] [3]NH O OCOOEtNH OO CONHMe MeNH / MeOHThe ester (4.11 g, 14 mmol) was dissolved in absol. methanolic ammonia (100 ml, 20 % NH 3), and the solution was allowed to stand at temperature for 3 days, the solvent was then evaporated, and the resulting crystalline was purified by recrystallization.2.3 氨水用于芳香羧酸酯氨解示例[4]NNH OHNCONH 2To an autoclave, was added methyl 6-methylniconate (500 g, 3.31 mol), sat. aq. NH 4OH (500 ml) and ethanol (500 ml). After sealing, the reaction was heated to 80℃ for 2 days. The cooled reaction mixture was filtrated, and the filter cake was recrystallized to afford white solid (247 g, 54.8%)。
名词解释酯的氨解反应

名词解释酯的氨解反应酯的氨解反应是一种有机化学反应,主要指酯与氨(或胺类物质)在适当条件下发生水解作用,生成相应的酰胺和醇。
这一反应常用于有机合成和药物合成领域,具有广泛的应用价值。
在本文中,将介绍酯的氨解反应的基本原理、反应机制、反应条件及其应用领域。
1. 基本原理:酯的氨解反应基于水解的原理,即通过水分子的加入使酯分子的酰基与氨基或胺基发生断裂,生成酰胺和醇。
酯的氨解反应是一个亲核取代反应,其中氨或胺作为亲核试剂进攻酯的羰基碳,攻击后产生过渡态,然后发生脱水、质子转移等步骤,最终得到酰胺和醇。
2. 反应机制:酯的氨解反应经历了几个关键步骤。
首先,亲核试剂(氨或胺)的氢原子被酯的羰基氧原子中间的C-O键的电子吸引,形成一个亲核试剂攻击羰基碳原子的过程。
然后形成临时的过渡态,即酯酰氧负离子与亲核试剂结合形成一个酰胺酰基加合物。
接下来,通过脱水和质子转移的步骤,酰胺酰基加合物分解为酰胺和醇的生成。
最后通过中和或其他化学转化,得到最终产物。
3. 反应条件:酯的氨解反应的条件可以在不同的实验室设定下变化,主要取决于反应底物和所需产物的特性。
一般来说,这一反应需要保持适当的催化剂存在,通常是氢氧化物、醇或酸等。
此外,反应中需要提供恰当的温度和反应时间,以确保反应的进行和产物的优化。
4. 应用领域:酯的氨解反应在有机合成和药物合成领域具有广泛的应用。
其中一个重要的应用是在药物合成过程中,通过酯的氨解反应可以转化合成药物中的酯基团。
此外,酯的氨解反应还可以用于合成具有特定结构和功能的材料,如高分子聚酰胺的合成。
此外,该反应还能被应用于有机合成过程中的其他反应,如酯键的断裂等。
在总结中,酯的氨解反应是一种有机化学反应,通过水解作用将酯转化为酰胺和醇。
这一反应具有重要的应用价值,在药物合成和有机合成领域得到广泛应用。
深入了解酯的氨解反应的原理、机制、反应条件和应用领域,有助于我们更好地理解和应用这一反应,推动有机化学的发展。
酯的氨解成酰胺反应温度

酯的氨解成酰胺反应温度1.引言1.1 概述酯的氨解成酰胺反应是一种重要的有机化学反应,通过在酯分子中加入氨基基团,将酯转化为相应的酰胺化合物。
这一反应在化学合成和药物制造等领域有着广泛的应用。
在酯的氨解成酰胺反应中,酯与氨基化合物在适当的条件下反应生成酰胺化合物。
这个化学过程涉及到酯的酯基与氨基之间的交换,同时伴随着水的生成。
该反应是一个平衡反应,其速率和平衡位置受到多种因素的影响。
本文将重点讨论这一反应中反应温度的选择对反应速率和产物选择性的影响。
在不同的温度条件下,反应的动力学和平衡性质可能发生变化,从而影响到反应的效果和产物的结构。
通过合理选择反应温度,可以控制反应速率和产物的组成,从而实现对合成过程的精确控制。
进一步了解酯的氨解成酰胺反应及其温度调控的相关内容,将对有机合成和药物制造等领域的研究和应用具有重要的指导意义。
在本文的后续部分中,将详细介绍影响反应温度选择的因素并探讨低温和高温条件下的反应特点。
通过对这些内容的探究,我们希望能为进一步优化反应条件和合成策略提供一定的参考和指导。
文章结构部分的内容如下:1.2 文章结构本文共分为三个主要部分:引言、正文和结论。
引言部分主要包括概述、文章结构和目的。
首先,文章将概述酯的氨解成酰胺反应这一化学反应过程,并介绍其在有机合成中的重要性和应用。
其次,文章将介绍整篇文章的结构安排,以使读者能够清晰地了解文章的逻辑和内容组织。
最后,文章将明确阐述本文的目的,即通过研究和分析影响酯的氨解成酰胺反应温度的因素,探讨反应温度的选择及其对反应结果的影响。
正文部分包括两个主要的子节:酯的氨解成酰胺反应和反应温度的选择。
在酯的氨解成酰胺反应一节中,将详细介绍该反应的原理和机制,并探讨影响反应温度的因素,包括催化剂的选择、底物的结构和浓度、反应时间等。
在反应温度的选择一节中,将讨论在低温和高温条件下酯的氨解成酰胺反应的特点和优缺点,以及如何选择合适的反应温度以达到预期的反应结果。
酯的氨解催化剂_概述及解释说明

酯的氨解催化剂概述及解释说明1. 引言1.1 概述本文将对酯的氨解催化剂进行综述和解释说明。
酯的氨解是一种重要的有机合成反应,通过在酯分子中引入氨基团,可以生成多种有机化合物。
鉴于其广泛的应用前景和产生的化学品多样性,研究人员已经开发了各种催化剂来促进此类反应。
本文旨在概述酯的氨解催化剂的研究进展,并探讨影响反应速率和产物选择性的因素。
1.2 文章结构文章将按以下顺序展开讨论:首先介绍引言部分,然后详细介绍酯的氨解催化剂(包括反应机制、催化剂种类及特点以及催化活性和选择性研究)。
随后,我们将探讨反应条件对氨解酯反应以及催化剂对反应速率和产物选择性的影响。
最后,在分析了其他影响因素及调控方法后,我们将探讨酯的氨解催化剂在有机合成中的应用潜力,并提出技术发展和改进方向需求分析。
最后,我们将讨论持续提高催化活性和选择性所面临的挑战与展望。
1.3 目的本文的目的是系统地总结和分析酯的氨解催化剂在有机合成中的重要性及研究进展,并对其应用前景和挑战进行评估。
通过深入理解反应机制、催化剂种类及特点以及反应条件对反应结果的影响,我们将为酯的氨解催化剂领域的未来发展提供新思路和方向。
2. 酯的氨解催化剂2.1 酯的反应机制酯的氨解指的是酯与氨在催化剂存在下发生反应生成胺和醇的过程。
在这个反应中,催化剂起到了促进反应速率和选择性的作用。
该反应一般分为两个步骤:氨解和氧化脱羧。
第一步,酯与氨先发生氨解,生成相应的胺和醇,并释放出水分子。
第二步,生成的胺进一步经历氧化脱羧,产生亚胺中间体,然后将亚胺加氢生成相应的胺。
2.2 催化剂种类及特点目前已经开发出多种类型的催化剂用于酯的氨解反应。
常见的催化剂包括金属催化剂、有机催化剂和生物催化剂。
金属催化剂如钯、铜、铁等具有高效且广泛适用于不同类型酯底物的特点。
有机催化剂如吡啶、三甲基溴硷等对高活性要求较低,但对底物选择性较差。
而生物催化剂如酯酶具有良好的底物选择性和环境适应性。
酯的胺解条件

酯的胺解条件酯的胺解条件,这听起来好像有点复杂,不过没关系,咱们就像唠家常一样把它搞清楚。
咱先来说说什么是酯的胺解。
就好比一场特殊的聚会,酯分子和胺分子凑到了一块儿,然后发生了一些奇妙的变化。
在这个过程中,胺就像一个热情的访客,想要和酯这个“主人”进行互动,然后改变这个聚会的气氛,也就是改变分子的结构。
那这酯的胺解得在啥条件下才能顺利进行呢?温度就是一个挺关键的因素。
你可以把温度想象成这个聚会的热闹程度。
如果温度太低,就像这个聚会冷冷清清的,胺和酯分子都没什么活力,它们之间的反应就会特别慢,就像大家都懒懒散散的不想互动。
不过这温度也不能太高,要是太高了,那就乱套了,就像聚会的音乐声太大,大家都慌慌张张的,可能会产生一些我们不想要的反应,生成乱七八糟的东西。
所以温度得合适,不同的酯和胺组合可能需要的最佳温度不一样,这就需要我们像一个细心的组织者一样去摸索。
溶剂也很重要啊。
溶剂就像是这个聚会的场地。
有些溶剂就像豪华的大礼堂,能给胺和酯分子提供宽敞舒适的空间,让它们能够自由地接触、互动。
而有些溶剂就像狭窄的小房间,分子们在里面挤来挤去,很不方便,反应也就不那么顺利了。
比如说,一些极性溶剂就比较适合酯的胺解反应,因为它们能更好地让胺和酯分子溶解在其中,就像在一个和谐的社区里,大家相处融洽。
胺的种类也会影响胺解条件。
不同的胺就像不同性格的人。
有的胺比较活泼,就像性格开朗的人,很容易就和酯分子搭上话,开始反应。
而有的胺就比较“害羞”,需要我们创造更多的条件去鼓励它参与反应。
比如一些碱性比较强的胺,它就像一个充满活力的运动员,在反应中可能会更加积极主动。
催化剂有时候也得加入到这个“聚会”里。
催化剂就像是一个神奇的魔法棒。
它自己虽然不参与这个聚会的核心互动,但是却能让胺和酯分子的互动变得更加顺畅。
没有它的时候,反应可能要进行很久很久,就像大家走路去一个很远的地方。
有了催化剂呢,就像给大家都配上了自行车,速度一下子就快起来了。
酯跟氨水反应副产物

酯跟氨水反应副产物全文共四篇示例,供读者参考第一篇示例:酯是一类含氧醇基和酸基的有机化合物,具有特定的酣味和香气。
酯的合成常常涉及与其他化合物或试剂的反应,其中酯与氨水的反应是一种常见的化学反应。
在这种反应中,除了形成目标产物外,还会生成一些副产物。
本文将涉及酯与氨水反应的机理、条件以及副产物的生成及其性质。
1. 酯与氨水反应的机理酯与氨水的反应是一种酯酶反应,一般在碱性条件下进行。
在反应中,酯的酯基(O–C=O)和氨水中的氨基(-NH2)发生亲核取代反应,酒石酸二乙酯和氨水反应的步骤如下:R–COOCH2CH2COOR + NH3 → R–COOCH2CH2CONH4R代表酯基团,COO代表酯基。
在反应中,氨水中的氨基攻击酯中的羰基,形成一个中间产物,随后发生酯基和氨基的亲核取代反应,生成酯酰胺产物。
酯与氨水的反应一般是在碱性条件下进行的,通常使用氢氧化钠或氢氧化钾等碱性剂来提供反应条件。
在反应中,碱性条件有助于促进酯的开环和氨基的亲核攻击,加快反应速率。
反应通常在温和的温度和压力下进行,以避免不必要的副反应和降解。
酯与氨水反应副产物的性质与它们的结构和性质密切相关。
一般来说,副产物中的酸性物质具有较强的酸性,可以与金属离子形成盐类,并且具有腐蚀性。
而生成的醇类物质一般为液态或固态,具有较高的溶解性和挥发性。
第二篇示例:酯跟氨水反应是一种常见的化学反应过程,通常会产生一些副产物。
在这篇文章中,我们将探讨酯跟氨水反应的机理以及可能产生的副产物。
让我们来了解一下酯和氨水的性质。
酯是一类有机化合物,其中含有一个羰基碳原子和一个氧原子。
而氨水是一种由氨气溶解在水中而成的碱性溶液。
当酯与氨水发生反应时,通常会发生酯水解反应,生成醇和胺化合物。
酯跟氨水反应的机理通常分为两个步骤。
氨水中的氨离子(NH4+)会攻击酯分子的羰基碳原子,形成中间体。
接着,中间体会经过质子化和消除氨分子的步骤,最终生成醇和胺化合物。
酯跟氨水反应副产物

酯跟氨水反应副产物
酯和氨水发生反应时,通常会生成相应的醇和氨盐。
具体来说,酯与氨水反应会产生相应的醇和氨盐。
这是因为酯的酯基(-COO-)
与氨水中的氨基(NH2)发生置换反应,生成醇和氨盐。
置换反应是
一种常见的化学反应类型,其中一个官能团被另一个官能团取代。
例如,乙酸乙酯(乙酸乙酯)与氨水反应会生成乙醇和乙酸铵。
反应方程式如下所示:
CH3COOCH2CH3 + NH3 → CH3CH2OH + CH3COONH4。
需要注意的是,酯和氨水的反应条件(如温度、浓度等)会影
响副产物的生成和反应速率。
此外,还有一些特殊情况下可能会生
成其他副产物,但一般情况下,酯和氨水反应的主要产物是相应的
醇和氨盐。
总的来说,酯和氨水反应的副产物主要是相应的醇和氨盐,这
一反应在化工和有机合成中具有一定的应用。
希望这个回答能够满
足你的需求,如果你还有其他问题,请随时告诉我。
酯与酰胺的结构与性质

酯与酰胺的结构与性质酯与酰胺是有机化合物中常见的结构,它们在化学反应和生物活动中发挥着重要的作用。
本文将对酯与酰胺的结构与性质进行详细探讨。
酯是一类通过羧酸和醇反应生成的有机化合物。
在酯分子中,羧基的氧原子与一个碳元素发生共价键连接,称为酯基;另一个氧原子与同一个碳元素连接,形成一个羟基。
酯的一般分子结构可以表示为R-COO-R',其中R和R'可以是相同或不同的有机基团。
酯的性质主要取决于它的结构,包括碳酯键的键能和键长,以及酯基团的大小和极性。
酯的化学性质主要表现在它的水解反应和酯交换反应。
在水解反应中,酯可以被酶或酸催化下水分解成相应的羧酸和醇。
酯交换反应是指酯与另一种醇反应生成新的酯。
酯的物理性质包括熔点、沸点、溶解度等,通常酯具有愉悦的香气,可用于食品、香精等行业。
酰胺是通过酰氯和胺反应制备得到的有机化合物。
酰胺的一般结构可以表示为R-CO-NH-R',其中R和R'可以是相同或不同的有机基团。
酰胺中的氨基与酰基通过共价键连接,形成酰胺键。
酰胺的性质取决于其结构,包括酰胺键的键能和键长,以及酰胺基团的大小和极性。
酰胺的化学性质主要表现在它的水解和氨解反应。
在水解反应中,酰胺可以被酶或酸水解成相应的酰氨基和相应的酸。
氨解反应是指酰胺与氢氨化钠等碱反应生成胺和相应的金属氨盐。
酰胺的物理性质包括熔点、沸点、溶解度等,酰胺具有比较好的溶解性,可用于制备有机合成镜头。
综上所述,酯和酰胺是有机化合物中常见的结构,它们的性质取决于其分子结构,包括碳氧键和酰氮键的键能和键长,以及酯基团和酰胺基团的大小和极性。
通过研究酯和酰胺的结构与性质,可以更好地理解有机化合物的反应规律和应用价值。
一种酯氨解反应催化剂组合物及L-薄荷酰胺的制备方法[发明专利]
![一种酯氨解反应催化剂组合物及L-薄荷酰胺的制备方法[发明专利]](https://img.taocdn.com/s3/m/b25200c29f3143323968011ca300a6c30c22f106.png)
(19)中华人民共和国国家知识产权局(12)发明专利申请(10)申请公布号 (43)申请公布日 (21)申请号 202010374890.8(22)申请日 2020.05.07(71)申请人 万华化学集团股份有限公司地址 264006 山东省烟台市经济技术开发区天山路17号(72)发明人 陈来中 钟子太 郭小安 李文滨 李晶 何勇 张永振 (51)Int.Cl.C07C 67/343(2006.01)C07C 69/75(2006.01)B01J 31/22(2006.01)(54)发明名称一种酯氨解反应催化剂组合物及L-薄荷酰胺的制备方法(57)摘要本发明公开一种酯氨解反应催化剂组合物及L -薄荷酰胺的制备方法。
所述酯氨解反应催化剂包含催化剂和配体,所述催化剂为一价铜盐CuX,所述配体为(R )-N ,N ,N ,N -四烷基联萘胺类化合物其中R 1、R 2、R 3、R 4相互独立的选自所述方法使用薄荷基氯为起始原料,与金属镁反应制备薄荷基氯化镁,再与不同取代基的氯甲酸酯反应得到薄荷甲酸酯,然后在酯氨解催化剂组合物催化下经过氨解得到L -薄荷酰胺。
收率提升,降低生产成本,光学纯度高,环保无废水排放。
权利要求书2页 说明书7页CN 111393293 A 2020.07.10C N 111393293A1.一种酯氨解反应催化剂组合物,包含催化剂和配体,所述催化剂为一价铜盐CuX,其中X为Cl、Br、I或AcO;优选Br或I;所述配体为(R)-N,N,N,N-四烷基联萘胺类化合物其中R1、R2、R3、R4相互独立的选自表示取代基位置,优选和/或更优选所述配体与催化剂摩尔量相等。
2.一种L-薄荷酰胺的制备方法,包括以下步骤:(1)薄荷甲酸酯的制备:薄荷基氯和镁屑反应制备薄荷基氯化镁然后薄荷基氯化镁与氯甲酸酯进行缩合反应,得到薄荷甲酸酯其中R为表示取代基位置;(2)氨解反应:薄荷甲酸酯与乙胺在权利要求1所述的氨解催化剂组合物的作用下反应制备薄荷酰胺3.根据权利要求2所述的方法,其特征在于,所述步骤(1)中的薄荷基氯化镁与氯甲酸酯的反应温度为20-30℃。
第六章 氨解反应

OH 烯醇式
NH4HSO3 加成
OH SO3NH4 H H H SO3NH4 醇式加成物
SO3NH4 H H H SO3NH4 胺式加成物 -2NH4HSO3
H H +NH3 氨解 NH2 SO3NH4 胺式加成物 NH4HSO3
H H NH 互变异构 亚胺式
NH2
萘胺
萘酚的磺酸衍生物的规律:
H2O
ArCONH2
ArCH2NH2
6.1 概述
定义 反应的目的 氨基化试剂(氨解剂)
6.1.1 定义
利用氨基化试剂将已有取代基置换成氨基 (或芳氨基)的反应叫做氨解反应。
R Y + NH3 R NH2 + HY
R=烷基、芳基;Y=OH, Cl, SO3H, NO2
6.1.2 反应的目的
生产实例 (1)硝基苯胺类的制备(非催化)
NH2 NH2 NO2 NH2 NO2 NO2 NH2 NO2 Cl NH2 Cl NO2
NO2
(2)2-氨基蒽醌
O Cl + 2NH3 O
P143 O
CuSO4,210-218 C 5MPa,5-10h
o
O NH2 + NH4Cl O
O
6.2.3 脂肪族卤化物的氨解
6.3.2 酚类的氨解
气相氨解法:
催化剂(硅酸铝),气态酚类与氨进行的气固相催 化反应
液相氨解法:
酚类与氨水在SnCl2,AlCl3,NH4Cl下,在高温高压 下反应
酚类典型的重要的氨解-苯酚的气相氨解法
特点: 可逆 , 放热, 采用较高浓度的氨和 苯酚摩尔比对反应有利。
2-萘酚的氨解
N-苯基-2-萘胺,防老剂丁
精细有机合成技术:脂肪族化合物的氨解反应历程

感谢观看
酯氨解的反应历程可以表示如下:
式中ROH代表含羟基的催化剂, R1和R2表示酯中的脂肪烃或芳烃基团。
注意,在进行酯氨解反应时,水的存在将会使氨解反应产 生少部分水解副反应。
另外,酯中烷基的结构对氨解反应速度的影响很大。表 10-2是各种醋酸酯在进行氨解时的相对速度。
由上表可知,酯中烷基或芳基的分子量越大,结构 越复杂,则氨解反应速度越慢。
精细有机合成技术
黄锋涛
目
录
Contents
1 2
脂肪族化合物的氨解反应 注意事项
一、脂肪族化合物实际上是一个二
级反应。 当进行酯的氨解时,几乎仅得到酰胺一种产物。 而脂肪醇与氨反应则可以得到伯、仲、叔胺的平衡混合物,
因此研究较多的是酯类氨解的反应历程。
酯的氨解反应

酯的氨解过程
说起那个酯的氨解过程噻,其实就跟咱们四川人炖肉的火候掌握差不多,要得就是那个恰到好处。
你看哈,酯嘛,就是那个酸和醇搞出来的东西,味道有时候酸溜溜的,有时候又带点酒香。
要把它氨解,就得找个“媒婆”——氨气,来给它牵个线,换个新面貌。
过程是这样的:先把酯放到个反应釜里头,温度要调得刚刚好,不能太高也不能太低,就跟咱们炖肉一样,火大了肉就柴了,火小了又炖不耙。
然后嘞,把氨气慢慢通进去,就像给肉加香料,一点一点来,不能心急。
这时候,酯和氨气就开始“谈情说爱”了,它们你中有我,我中有你,慢慢地就生成了新的东西——酰胺。
这个过程就像咱们四川人说的“融合”,两种味道、两种性格,在一起就整出了新花样。
但这个过程也不是一帆风顺的,得有催化剂来帮个忙,就像炖肉的时候要加点八角、桂皮,才能让味道更巴适。
催化剂就是那个让反应更快、更顺当的小助手。
最后,等反应完了,还得把里头的东西分一分,把酰胺给提出来。
这就跟咱们炖完肉,把肉和骨头分开一样,得有个取舍。
所以说嘛,酯的氨解过程,就像咱们四川人做饭一样,讲究个火候、调料和耐心,只有这样才能整出好味道、好结果。
双酚a型聚碳酸酯氨解

双酚a型聚碳酸酯氨解双酚A型聚碳酸酯(BPA-PC)是一种广泛应用于塑料制品和工业材料的合成材料。
它具有优异的物理性能和化学稳定性,因此被广泛用于生产瓶子、容器、食品包装、电子设备外壳等各种产品。
然而,近年来,对BPA-PC的安全性和环境影响产生了广泛关注。
BPA-PC的生产过程中,通常使用氨解法,即通过与氨反应,将BPA-PC降解成双酚A和聚碳酸酯两种成分。
这种氨解法是一种有效且经济的方法,可以高效地回收利用BPA-PC。
在氨解过程中,BPA-PC首先与氨反应,形成双酚A和聚碳酸酯的中间产物。
随后,通过加热和蒸馏等步骤,将中间产物分离得到双酚A和聚碳酸酯。
这种氨解方法不仅能够回收利用BPA-PC,还可以减少对环境的污染,具有较高的环保性。
然而,BPA-PC的安全性引发了广泛的争议。
研究表明,BPA-PC中的双酚A可能会渗入食品和饮料中,对人体健康产生潜在风险。
双酚A被认为具有内分泌干扰物的特性,可能对生殖系统、神经系统和免疫系统等产生负面影响。
因此,许多国家和地区已经限制或禁止使用BPA-PC制品。
为了解决这一问题,科学家们正致力于开发与BPA-PC具有相似性能但更安全的替代物。
这些替代物可以保持BPA-PC的物理性能和化学稳定性,同时降低对人体健康和环境的风险。
目前,一些替代物已经在市场上得到应用,并受到了广泛关注和接受。
BPA-PC作为一种重要的合成材料,在各个领域得到了广泛应用。
尽管其安全性存在争议,但科学家们正致力于寻找更安全的替代物。
通过合理的生产和使用,我们可以最大限度地减少对环境的污染,保护人类健康。
在未来的发展中,我们相信会有更多安全可靠的替代物出现,推动塑料制品的可持续发展。
酯的氨解反应方程式

酯的氨解反应方程式1. 引言酯是一类重要的有机化合物,常用于制备香料、溶剂和某些药物。
酯的氨解反应是酯与氨反应生成相应的醛(或酮)和胺的过程。
这一反应在有机合成中具有广泛的应用价值。
本文将介绍酯的氨解反应方程式,包括反应机理、影响因素以及实验条件等内容。
2. 反应方程式酯的氨解反应可以用下列方程式表示:酯 + 氨→ 醛(或酮)+ 胺例如,乙酸乙酯与氨发生氨解反应后,生成乙醛和乙胺:CH3COOCH2CH3 + NH3 → CH3CHO + CH3CH2NH23. 反应机理在酯的氨解反应中,首先发生亲核加成,产生一个中间体(亚胺),然后通过水解产生相应的胺和醛(或酮)。
具体来说,该反应可分为以下几个步骤:1.氨进攻:亚胺形成首先,氨中的亲核氮原子进攻酯的羰基碳,形成一个中间体亚胺。
这一步骤是整个反应的关键步骤。
2.水解:亚胺分解中间体亚胺通过水解反应,断裂C-N键,生成相应的胺和醛(或酮)。
3.产物生成:生成醛(或酮)和胺通过水解反应生成的产物即为所需的醛(或酮)和胺。
4. 影响因素4.1 底物结构底物的结构对氨解反应具有重要影响。
一般来说,底物中羰基碳与邻近取代基之间的空间位阻较小,反应活性较高。
而底物中存在大体积取代基或环状结构等情况时,空间位阻增大,反应活性降低。
4.2 反应条件反应条件也对氨解反应有一定影响。
在常见实验条件下,氨解反应通常在室温下进行,并加入催化剂如氢氧化钠、盐酸等。
此外,溶剂选择和底物摩尔比例等也会对反应结果产生影响。
4.3 催化剂选择催化剂的选择对氨解反应的速率和产物选择性具有重要影响。
常用的催化剂包括碱性金属盐(如氢氧化钠、氢氧化钾等)和酸性催化剂(如盐酸、硫酸等)。
不同的催化剂会导致不同的反应路径和产物生成。
5. 实验条件以下是一种常见的实验条件,用于乙酸乙酯与氨发生氨解反应:•反应物:乙酸乙酯、氨水•催化剂:氢氧化钠•反应温度:室温•反应时间:数小时•溶剂:无需溶剂具体实验步骤如下:1.在干燥皿中称取适量乙酸乙酯。
酯到酰胺方法

将酯转化为酰胺有多种方法,其中一种常见的方法是使用氨酯交换法。
具体步骤如下:
酯的氨解:将酯与氨或氨的醇溶液反应,生成相应的铵盐。
这一步通常需要在加热条件下进行,以促进反应的进行。
氨水处理:将生成的铵盐与适量的氨水反应,得到相应的酰胺。
这一步可以通过加热和搅拌来加速反应。
另外,还有其他方法可以将酯转化为酰胺,例如使用酸酐或酸作为催化剂,或者通过酯的氨氧化来制备。
这些方法的具体步骤和条件可能会有所不同,因此在实际操作时需要仔细选择和调整。
需要注意的是,酯到酰胺的转化方法各有优缺点,适用于不同的情况和需求。
因此,在实际应用中需要根据具体情况选择最适合的方法。
同时,由于有机合成反应的复杂性,操作过程中需要注意安全问题,并遵循相关的实验规范和操作程序。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
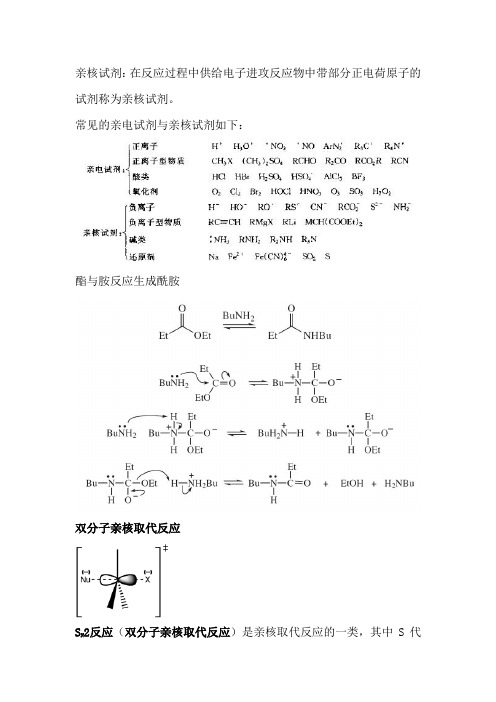
亲核试剂:在反应过程中供给电子进攻反应物中带部分正电荷原子的试剂称为亲核试剂。
常见的亲电试剂与亲核试剂如下:
酯与胺反应生成酰胺
双分子亲核取代反应
S N2反应(双分子亲核取代反应)是亲核取代反应的一类,其中S代
表取代(Substitution),N代表亲核(Nucleophilic),2代表反应的决速步涉及两种分子。
与S N1反应相对应,S N2反应中,亲核试剂带着一对孤对电子进攻具亲电性的缺电子中心原子,形成过渡态的同时,离去基团离去。
反应中不生成碳正离子,速率控制步骤是上述的协同步骤,反应速率与两种物质的浓度成正比,因此称为双分子亲核取代反应。
反应机理
S N2反应最常发生在脂肪族sp3杂化的碳原子上,碳原子与一个电负性强、稳定的离去基团(X)相连。
亲核试剂(Nu)从离去基团的正后方进攻碳原子,Nu-C-X角度为180°,以使其孤对电子与C-X键的σ*反键轨道可以达到最大重叠。
然后形成一个五配位的反应过渡态,碳约为sp2杂化,用两个垂直于平面的p轨道分别与离去基团和亲核试剂成键。
C-X的断裂与新的C-Nu键的形成是同时的,X很快离去,形成含C-Nu键的新化合物。
由于亲核试剂是从离去基团的背面进攻,故如果受进攻的原子具有手性,则反应后手性原子的立体化学发生构型翻转,也称“瓦尔登翻转”。
这也是S N2反应在立体化学上的重要特征。
反应过程类似于大风将雨伞由里向外翻转。
例如溴乙烷与氢氧根离子发生S N2生成乙醇和溴离子。
上例中,OH−(亲核试剂)进攻C2H5Br(底物)发生S N2反应,经过不稳定的过渡态,最终Br−离去,得到乙醇。
S N2反应一般发生在伯碳原子上,很难成为有位阻分子的反应机理,并且取代基越多,按S N2机理反应的可能性越小。
基团在空间上比较拥挤的分子一般采用S N1机理,可以缓解一部分的位阻,也可生成较稳定的碳正离子(通常为三级碳正离子)。
影响因素
离去基团的碱性:离去基团的碱性越强,其离去能力越弱,反之亦然。
氨是碱性物质,但当氨分子中的氢原子被酰基取代后则碱性减弱,它不能使石蕊变色,一般认为是中性化合物。
这是由于酰胺中氮原子上未共用电子对与碳氧双键形成p,π-共轭,从而使氮原子上电子云密度降低,因此减弱了它接近质子的能力,故碱性大大降低。
与此同时,氮氢键的极性又有所增强,从而又表现了微弱的酸性。
所
以,是一个很好的离去基团,有利于反应的进行。
亲核试剂的亲核性:亲核性需要与上面的碱性相区别。
碱性是试剂对质子的亲和能力,而亲核性是试剂形成过渡态时,对碳原子的亲和能力。
一般来讲,试剂的负电性、碱性和可极化性越强,其亲核性也越强。
实际上通常需要综合考虑这几个因素以及溶剂的影响。
而亲核性:I-<CH3COO-<OH-<<RO- < NH2-,所以,反应容易进行。
溶剂:S N2反应在质子溶剂中进行时,一方面,溶剂化作用有利于
离去基团的离去;另一方面,溶剂也会与亲核试剂发生作用,使亲核试剂与底物的接触变得困难。
最后的影响是这两种因素的综合结果。
相对而言,极性非质子性分子很少包围负离子,因此对S N2反应是有利的。
而DMF,DMSO都是极性疏质子性溶剂,也有利于实验的进行。
空间效应:立体阻碍性(含体积大的取代基)会使亲核试剂的亲核性下降。
空间效应基本上与链长短无关,主要与碳原子上的取代基多少有关,如果取代基越多,那各取代基的空间位置基本固定,键就无法自由旋转,所以我们说空间效应比较大。
而与链长无关。
NHS ester reaction scheme for chemical conjugation to a primary amine. (R) represents a labeling reagent or one end of a crosslinker having the NHS ester reactive group; (P) represents a protein or other molecule that contains the target functional group (i.e., primary amine).
综上反应条件
1、Calculate required amount of NHS ester:
NHS_ester_weight [mg] = 8 ×amino_compound_weight [mg] ×NHS_ester_molar_weight [Da] / amino_compound_molar_weight [Da].
2、Dissolve NHS ester in 1/10 reaction volume of DMF or DMSO. Amine-free DMF is preferred solvent.
3、Dissolve biomolecule in 9/10 reaction volume of buffer with pH
8.3-8.5. The reaction of NHS esters with amines is strongly pH-dependent: at low pH, the amino group is protonated, and no modification takes place. At
higher-than-optimal pH, hydrolysis of NHS ester is quick, and modification yield diminishes. Optimal pH value for modification is 8.3-8.5.
配制100ml pH8.34的磷酸缓冲液(PBS)配制方法可以这样配制:
1/15 mol/L Na2HPO4溶液的配制:准确称取Na2HPO4•12H2O 2.3876 g,用水溶解,定容至100 mL;
1/15 mol/L KH2PO4溶液的配制:准确称取KH2PO4 0.4540 g,用水溶解,定容至100 mL;再取上述1/15 mol/L Na2HPO4溶液97.5ml+l/15 mol/L KH2PO4溶液2.5ml即得
0.1 M Sodium bicarbonate solution has appropriate pH. Other alternatives are 0.1 M Tris buffer(although Tris has amino group, it is hindered and does not react with NHS esters), or 0.1 M phosphate buffer. Note pH is the most important thing. While Tris is primary amine is not compatible, because it competes for reaction; however, in some procedures, it is useful to add Tris or glycine buffer at the end of a conjugation procedure to quench (stop) the reaction.
4、Add NHS ester solution to the solution of biomolecule, and vortex well. Keep on ice overnight, or at room temperature during at least 4 hours.
5、Purify the conjugate using appropriate method: gel-filtration for macromolecules is most universal. Precipitation and chromatography is another alternative. Organic impurities (such as N-hydroxysuccinimide, NHS ester, acid produced by hydrolysis) are almost always easily separated. For proteins and nucleic acids, ethanol or acetone precipitation can be used.。
