电负性表
元素电负性的影响因素分析_文君

N a 1 /2H 2C 2 + 2←
3
胺 R N H P 杂化 ; 吡啶 2 分 子中氮原 子是 S C 分子中氮是 S P 杂化 ; 腈 RC= N 分子中 5H 5N 氮是 S P 杂化 , 随着杂化轨道中 S 成分的增多 , 轨道 吸引电子能力增强 , 电负性变大 。 因此氮原子越不 容易给出孤对电子而呈碱性 。 例如下面几种含氮 化合物的碱性相应减弱 。 25 %S : R N H H 2 + 2O P k b = 34 33 %S : C H 5H 5 N+ 2O P k b = 8. 8 50 %S : RC N+ H 无反应 。 2O 由此可见 , 原子在分子中所采用的杂化轨道形 式对原子的电负性有很大的影响 。 密立根等人曾用 公式计算出原子在不同杂化状态的电负性 , 见表 1。
2 轨道杂化方式对电负性的影响
许多元素在形成各种化合物时 , 常采用不同的 杂化轨道 。 轨道的杂化方式对电负性的影响是很 大的 。 一般而言 , 杂化轨道中含 S 成分越多 , 原子 的电负性越大 。 这是因为 S 轨道钻穿本领大 , 在核 附近出现的机会多 。 S 电子受内层电子屏蔽作用 小 , 轨道 有较 大吸 引电 子 的能 力 。 例如 在 C H 4、 C P、S P、 2H 4 、C 2H 2 中碳原子的杂化方式分别为 S S P 。S P 杂化轨道 S 占 50%; S P中 S 占 33%; S P 中 S 占 25%, C H 4 中碳的电负性增大到近似于氢 的电负性 , 使甲烷分子不活泼 。 乙炔分子中 , 碳的 电负性增大到近似于氧的电负性 3. 44。 因此 C 2H 2 中 C-H 键上的电子云比在 C H 4 、C 2H 4 中更加靠 近碳原子 , 增加了 CH键的极性 , 使乙炔中的氢 原子具有一定的酸性 , 而可以被金属钠置换 。 N a + C N a H C 1 /2H 2H 2 2 + 2← N a H C N a 2 +
元素的电负性及其变化规律PPT 鲁科版
4、教学必须从学习者已有的经验开始。——杜威 5、构成我们学习最大障碍的是已知的东西,而不是未知的东西。——贝尔纳 6、学习要注意到细处,不是粗枝大叶的,这样可以逐步学习摸索,找到客观规律。——徐特立 7、学习文学而懒于记诵是不成的,特别是诗。一个高中文科的学生,与其囫囵吞枣或走马观花地读十部诗集,不如仔仔细细地背诵三百首诗。——朱自清 8、一般青年的任务,尤其是共产主义青年团及其他一切组织的任务,可以用一句话来表示,就是要学习。——列宁 9、学习和研究好比爬梯子,要一步一步地往上爬,企图一脚跨上四五步,平地登天,那就必须会摔跤了。——华罗庚 10、儿童的心灵是敏感的,它是为着接受一切好的东西而敞开的。如果教师诱导儿童学习好榜样,鼓励仿效一切好的行为,那末,儿童身上的所有缺点就会没有痛苦和创伤地不觉得难受地逐渐消失。——苏霍姆林斯基 11、学会学习的人,是非常幸福的人。——米南德 12、你们要学习思考,然后再来写作。——布瓦罗14、许多年轻人在学习音乐时学会了爱。——莱杰 15、学习是劳动,是充满思想的劳动。——乌申斯基 16、我们一定要给自己提出这样的任务:第一,学习,第二是学习,第三还是学习。——列宁 17、学习的敌人是自己的满足,要认真学习一点东西,必须从不自满开始。对自己,“学而不厌”,对人家,“诲人不倦”,我们应取这种态度。——毛泽东 18、只要愿意学习,就一定能够学会。——列宁 19、如果学生在学校里学习的结果是使自己什么也不会创造,那他的一生永远是模仿和抄袭。——列夫· 托尔斯泰 20、对所学知识内容的兴趣可能成为学习动机。——赞科夫 21、游手好闲地学习,并不比学习游手好闲好。——约翰· 贝勒斯 22、读史使人明智,读诗使人灵秀,数学使人周密,自然哲学使人精邃,伦理学使人庄重,逻辑学使人善辩。——培根 23、我们在我们的劳动过程中学习思考,劳动的结果,我们认识了世界的奥妙,于是我们就真正来改变生活了。——高尔基 24、我们要振作精神,下苦功学习。下苦功,三个字,一个叫下,一个叫苦,一个叫功,一定要振作精神,下苦功。——毛泽东 25、我学习了一生,现在我还在学习,而将来,只要我还有精力,我还要学习下去。——别林斯基 13、在寻求真理的长河中,唯有学习,不断地学习,勤奋地学习,有创造性地学习,才能越重山跨峻岭。——华罗庚52、若不给自己设限,则人生中就没有限制你发挥的藩篱。 53、希望是厄运的忠实的姐妹。 54、辛勤的蜜蜂永没有时间悲哀。 55、领导的速度决定团队的效率。 56、成功与不成功之间有时距离很短只要后者再向前几步。 57、任何的限制,都是从自己的内心开始的。 58、伟人所达到并保持着的高处,并不是一飞就到的,而是他们在同伴誉就很难挽回。 59、不要说你不会做!你是个人你就会做! 60、生活本没有导演,但我们每个人都像演员一样,为了合乎剧情而认真地表演着。 61、所谓英雄,其实是指那些无论在什么环境下都能够生存下去的人。 62、一切的一切,都是自己咎由自取。原来爱的太深,心有坠落的感觉。 63、命运不是一个机遇的问题,而是一个选择问题;它不是我们要等待的东西,而是我们要实现的东西。 64、每一个发奋努力的背后,必有加倍的赏赐。 65、再冷的石头,坐上三年也会暖。 66、淡了,散了,累了,原来的那个你呢? 67、我们的目的是什么?是胜利!不惜一切代价争取胜利! 68、一遇挫折就灰心丧气的人,永远是个失败者。而一向努力奋斗,坚韧不拔的人会走向成功。 69、在真实的生命里,每桩伟业都由信心开始,并由信心跨出第一步。 70、平凡的脚步也可以走完伟大的行程。 71、胜利,是属于最坚韧的人。 72、因害怕失败而不敢放手一搏,永远不会成功。 73、只要路是对的,就不怕路远。 74、驾驭命运的舵是奋斗。不抱有一丝幻想,不放弃一点机会,不停止一日努力。3、上帝助自助者。 24、凡事要三思,但比三思更重要的是三思而行。 25、如果你希望成功,以恒心为良友,以经验为参谋,以小心为兄弟,以希望为哨兵。 26、没有退路的时候,正是潜力发挥最大的时候。 27、没有糟糕的事情,只有糟糕的心情。 28、不为外撼,不以物移,而后可以任天下之大事。 29、打开你的手机,收到我的祝福,忘掉所有烦恼,你会幸福每秒,对着镜子笑笑,从此开心到老,想想明天美好,相信自己最好。 30、不屈不挠的奋斗是取得胜利的唯一道路。 31、生活中若没有朋友,就像生活中没有阳光一样。 32、任何业绩的质变,都来自于量变的积累。 33、空想会想出很多绝妙的主意,但却办不成任何事情。 34、不大可能的事也许今天实现,根本不可能的事也许明天会实现。 35、再长的路,一步步也能走完,再短的路,不迈开双脚也无法到达。 36、失败者任其失败,成功者创造成功。 37、世上没有绝望的处境,只有对处境绝望的人。 38、天助自助者,你要你就能。 39、我自信,故我成功;我行,我一定能行。 40、每个人都有潜在的能量,只是很容易:被习惯所掩盖,被时间所迷离,被惰性所消磨。 41、从现在开始,不要未语泪先流。 75、自己选择的路,跪着也要走完。
电负性知识点总结

电负性知识点总结电负性是化学中用来描述原子或化合物对电子的亲和力的一个重要概念。
在化学反应和化学键的形成过程中,电负性起着至关重要的作用。
本文将以电负性的定义、性质、周期表上的分布和应用为主线,系统总结电负性的相关知识点。
一、电负性的定义电负性是一个描述原子或化合物对电子的亲和力的物理量。
正式的定义是:一个原子吸引其上电子的能力的相对度量。
通常来说,原子的电负性取决于其核的电荷数和电子排布在轨道中的情况。
电负性的大小决定了化学键的极性和物质的性质。
二、电负性的性质1. 电负性的大小在国际上,通常采用电负性最高的氟元素的电负性为4.0作为基准,其他元素的电负性则根据相对氟元素的吸电子能力来确定。
一般来说,电负性越大的元素,其吸引电子的能力也越强。
2. 电负性的变化元素的电负性随着元素的周期和族别的变化而变化。
通常来说,越往右和上方的元素,其电负性越大;越往左和下方的元素,其电负性则越小。
3. 化合物的电负性化合物的电负性是由组成化合物的原子的电负性来决定的。
如果两个原子的电负性相差很大,那么它们形成的化合物就会具有明显的极性。
三、电负性的周期表分布1. 周期性根据周期表来看,元素的电负性随着元素周期的变化而变化。
一般来说,原子的电负性随着周期数的增加而增加,但是每个周期的最后一个元素(惰性气体)除外。
2. 组内性在同一族别内,原子的电负性随着原子序数的增加而增加。
但是,惰性气体除外,它们是周期表上电负性最小的几个元素。
四、电负性的应用1. 化学键的类型根据化合物中原子间电负性的差异可分为离子键、共价键和极性共价键。
当两个原子的电负性差异大于1.7时,它们之间的键被认为是离子键;当两个原子的电负性差异介于0.5到1.7之间时,它们之间形成的是极性共价键;当两个原子的电负性差异小于0.5时,它们之间形成的是非极性共价键。
2. 分子极性根据分子中原子间电负性的差异,可以确定分子的极性。
具有极性共价键的分子通常是极性分子,而具有非极性共价键的分子则是非极性分子。
鲍林电负性

鲍林电负性1定义电负性综合考虑了电离能和电子亲合能,首先由莱纳斯·鲍林于1932年提出。
它以一组数值的相对大小表示元素原子在分子中对成键电子的吸引能力,称为相对电负性,简称电负性。
元素电负性数值越大,原子在形成化学键时对成键电子的吸引力越强。
2计算方法电负性的计算方法有多种,每一种方法的电负性数值都不同,比较有代表性的有3种:① .鲍林提出的标度。
根据热化学数据和分子的键能,指定氟的电负性为,计算其他元素的相对电负性。
②.密立根从电离势和电子亲合能计算的绝对电负性。
③.阿莱提出的建立在核和成键原子的电子静电作用基础上的电负性。
利用电负性值时,必须是同一套数值进行比较。
同一周期从左至右,有效核电荷递增,原子半径递减,对电子的吸引能力渐强,因而电负性值递增;同族元素从上到下,随着原子半径的增大,元素电负性值递减。
过渡元素的电负性值无明显规律。
就总体而言,周期表右上方的典型非金属元素都有较大电负性数值,氟的电负性值数大();周期表左下方的金属元素电负性值都较小,铯和钫是电负性最小的元素()。
一般说来,非金属元素的电负性大于,金属元素电负性小于。
电负性概念还可以用来判断化合物中元素的正负化合价和化学键的类型。
电负性值较大的元素在形成化合物时,由于对成键电子吸引较强,往往表现为负化合价;而电负性值较小者表现为正化合价。
在形成共价键时,共用电子对偏移向电负性较强的原子而使键带有极性,电负性差越大,键的极性越强。
当化学键两端元素的电负性相差很大时(例如大于)所形成的键则以离子性为主。
3常见元素电负性鲍林标度鲍林指定氟的电负性为,并以此为标准确定其他元素的电负性。
氢锂铍硼碳氮氧氟钠镁铝硅磷硫氯钾钙锰铁镍铜锌镓锗砷硒溴铷锶银碘钡金铅一般来说,电负性大于的是非金属元素,而小于等于的往往是金属元素(当然,其中也存在例外)电负性对应氧化性特殊元素O的电负性比N的大呀,N的第一电离需要破坏2P半充满的低能状态,O的第一电离形成了 2P半充满的低能状态,所以N的第一电离能比O的大,O的非金属性比N强,所以O的电负性比N的大4在周期表内的递变规律1.随着原子序号的递增,元素的电负性呈现周期性变化。
元素周期律-元素的电负性

PART 02
元素周期表与电负性关系
REPORTING
WENKU DESIGN
周期表中元素电负性变化规律
1
从左到右,随着原子序数的增加,元素的电负性 逐渐增大。
2
从上到下,随着电子层的增加,元素的电负性逐 渐减小。
3
金属元素的电负性通常较低,而非金属元素的电 负性较高。
同一周期内元素电负性比较
PART 05
实验测定元素电负性的方 法与技术
REPORTING
WENKU DESIGN
电离能法测定原理及操作步骤
电离能法测定原理及操作步骤
01
操作步骤
02 1. 准备所需仪器和试剂,包括电离能测定仪、标 准电极、待测元素样品等。
03 2. 将待测元素样品放入电离能测定仪中,并连接 好电路。
电离能法测定原理及操作步骤
其他测定方法简介
光谱法
利用原子或离子在特定波长光的照射下发生 能级跃迁而产生的发射光谱或吸收光谱进行 元素电负性的测定。该方法具有灵敏度高、 选择性好等优点,但需要昂贵的仪器设备和 专业的操作技术。
电化学法
通过测量元素在电化学反应中的电极电位来 推算元素的电负性。该方法具有设备简单、 操作方便等优点,但受溶液组成、温度等因 素的影响较大。
电子亲和能法测定原理及操作步骤
01 操作步骤
02
1. 准备所需仪器和试剂,包括电子亲和能测定仪、标
准电极、待测元素样品等。
03
2. 将待测元素样品放入电子亲和能测定仪中,并连接
好电路。
电子亲和能法测定原理及操作步骤
3. 打开电子亲和能测定仪的电源,调 整仪器参数,使仪器处于正常工作状 态。
4. 记录测定结果,并根据标准电极的 电子亲和能值计算出待测元素的电子 亲和能。
2023届高考化学二轮复习备课素材:常见易错元素的化合价

常见易错元素的化合价1、HCN中C的化合价?HCN分子结构式为H-C≡N,电负性(吸电子能力) N>C>H,则碳氮三键的电子对偏向原子,N为-3价,碳在这里为+3;但碳氢单键的电子偏向碳,电子指定给碳,碳就得到了1个电子,这部分碳显-1;氢就为+1.碳两部分加起来:+3+(-1)=+2,就是+2价.2、KSCN中硫为-2价,则C为多少价?C为+4价,N为-3,S为-2注:硫氰化氢H—S—C≡N,异硫氰酸H—N=C=S两种。
但元素化合价相同。
3、NaBH4中氢的化合价?NaBH4为离子化合物,BH4-为四面体结构,化合价可认为B只有+3,H为-1价。
可见,若能写出结构式,则可据电负性分析电子对的偏向与偏移,标出化合价4、FeCuS2中S的化合价?Fe5O7呢?S为-2,实际上见下面12条所示!中学生常见错误变形为FeS·CuS,Fe5O7,变形为FeO·Fe2O3,易分析。
变形法能分析陌生化合物中元素化合价,甚至能分析化合物的形成方法及分解产物。
5、SiH4中H的化合价?H为-1价,电负性:Si—1.9,H—2.2,即电子对偏向电负性大的原子一边。
注:NH3中N-3,H+1;N中N-3,H+1;CH4中C-4,H+1.6、Na2S2O8中硫的化合价?7、草酸中碳的化合价?其实,无机物与有机物是相通的,分析方法可借用。
8、关于碳元素的化合价碳原子的最外层上的电子数目为4,最多有四次成键的机会。
有机物中的碳原子能且只能成键4次。
(1)碳元素只有同氢元素结合时才显负价,即C—H中C为-1价,故甲烷中碳为-4价。
(2)碳元素同其它非金素元素结合时都显正价,如:C—X中C为+1价,C—O中C为+1价,C—N中C为+1价,C=O中C为+2价,C≡N中C为+3价。
所以,H-C≡N中C为+2价。
(3)碳原子与碳原子相结合时均为0价,即C—C、C=C、C≡C中全为0价。
形成CH3CH3、CH2=CH2、CH≡CH后,碳的化合价分别为:-3、-2、-1.总结归纳:根据有机物的分子结构确定C元素的化合价。
元素的电负性及其变化规律PPT课件(上课用)
109.每个人皆有连自己都不清楚的 潜在能 力。无 论是谁 ,在千 钧一发 之际, 往往能 轻易解 决从前 认为极 不可能 解决的 事。― ―[戴尔·卡内基 ]
4、无论你觉得自己多么了不起,也永 远有人 比更强 ;无论 你觉得 自己多 么不幸 ,永远 有人比 你更不 幸。 5、也许有些路好走是条捷径,也许有 些路可 以让你 风光无 限,也 许有些 路安稳 又有后 路,可 是那些 路的主 角,都 不是我 。至少 我会觉 得,那 些路不 是自己 想要的 。 6、在别人肆意说你的时候,问问自己 ,到底 怕不怕 ,输不 输的起 。不必 害怕, 不要后 退,不 须犹豫 ,难过 的时候 就一个 人去看 看这世 界。多 问问自 己,你 是不是 已经为 了梦想 而竭尽 全力了 ?
113.人生的目的有二:先是获得你 想要的 ;然后 是享受 你所获 得的。 只有最 明智的 人类做 到第二 点总与 幽默的 人相伴 ,健康 总与阔 达的人 相伴。 20、对所学知识内容的兴趣可能成 为学习 动机。 ——赞 科夫 21、游手好闲地学习,并不比学习游手 好闲好 。—— 约翰·贝 勒斯
22、读史使人明智,读诗使人灵秀,数 学使人 周密, 自然哲 学使人 精邃, 伦理学 使人庄 重,逻 辑学使 人善辩 。—— 培根 23、我们在我们的劳动过程中学习思考 ,劳动 的结果 ,我们 认识了 世界的 奥妙, 于是我 们就真 正来改 变生活 了。— —高尔 基 24、我们要振作精神,下苦功学习。下 苦功, 三个字 ,一个 叫下, 一个叫 苦,一 个叫功 ,一定 要振作 精神, 下苦功 。—— 毛泽东
电负性

电负性本页解释何谓电负性、周期表中元素电负性的变化规律及原因;元素电负性差异对成键造成的影响、极性键和极性分子的意义。
什么是电负性定义电负性是原子对成键电子吸引倾向的量化(相对标度);元素的电负性愈大,吸引成键电子对的倾向就愈强。
鲍林标度(Pauling scale)是使用最广泛的电负性标度。
其标度值的范围从电负性最强的元素氟(F)——标度值为3.98,到电负性最弱的元素钫(Fr)——标度值为0.7。
两个电负性相同的原子成键会发生什么?如下图,原子A和原子B之间存在一个成键。
当然除了这个成键以外,每个原子可以同时与更多的原子之间存在着成键——不过这与我们所要讨论的问题无关。
如果原子的电负性相同,那么它们对成键电子对的吸引能力也相同。
因而电子出现在两个原子附近的概率相等,电子在平均意义上会出现在两个原子间的正中。
此类成键,A 和B通常为同一种原子,例如H2分子或Cl2分子。
注意: 上边的示意图表示的是电子在平均意义上的位置。
电子实际上存在于分子轨域当中,并且其位置在不断的变换。
此类成键被看作是"纯粹" 的共价键——电子均匀的为两个原子所共享。
如果B的电负性稍强于A呢?B对电子对的吸引能力会比A稍强一些。
这意味着在成键的B端电子密度会更高一些,因此略微带负电。
同时,A 端(有点缺乏电子)略微带正电。
图中,"" (读做"delta") 的意思为"略微的","+" 表示"略微带正电"。
什么是极性键?我们用极性键一词形容成键两端电荷不均匀分布的共价键——换一句话说就是成键的一端略微带正电荷而另一端略微带负电荷。
大多数共价键为此类成键。
HCl中的氢—氯成键以及水分子中的氢—氧成键皆为典型的极性键。
如果B的电负性远远超过了A呢?电子对会被吸引到成键的B端。
A失去了它对成键电子对的控制权,而B 完全控制住了这两个电子。
电负性

周期变化
氢 2.20锂0.98铍 1.57硼 2.04碳 2.55氮 3.04氧 3.44氟 3.98 钠 0.93镁 1.31铝 1.61硅 1.90磷 2.19硫 2.58氯 3.16 钾 0.82钙 1.00锰 1.55铁 1.83镍 1.91铜 1.9锌 1.65镓 1.81锗 2.01砷 2.18硒 2.48溴 2.96 铷 0.82锶 0.95银 1.93碘 2.66钡 0.89金 2.54铅 2.33 一般来说,周期表从左到右,元素的电负性逐渐变大;周期表从上到下,元素的电负性逐渐变小。 电负性也可以作为判断元素的金属性和非金属性强弱的尺度。一般来说,电负性大于1.8的是非金属元素,小 于1.8的是金属元素,而位于非金属三角区边界的“类金属”(如锗、锑等)的电负性则在1.8左右,它们既有金 属性又有非金属性。
电负性
化学术语
01 计算方法
03 递变规律
目录
02 周期变化 04 主要应用
电负性是元素的原子在化合物中吸引电子的能力的标度。元素的电负性越大,表示其原子在化合物中吸引电 子的能力越强。又称为相对电负性,简称电负性,也叫电负度。电负性综合考虑了电离能和电子亲合能,首先由 莱纳斯·卡尔·鲍林于1932年引入电负性的概念,用来表示两个不同原子间形成化学键时吸引电子能力的相对强弱, 是元素的原子在分子中吸引共用电子的能力。通常以希腊字母χ为电负性的符号。
鲍林的计算方法是:原始鲍林电负性表 其中,,分别指AB、A2、B2分子的键能 阿莱-罗周电负性表(上)和修正鲍林电负性表(下) ②1934年R.S.马利肯从电离势和电子亲合能计算的绝对电负性,即电离能和电子亲和能的平均值。 I为电离能,A为电子亲和能(放热为正,吸热为负) ③1956年A.L.阿莱和E.罗周提出的建立在核和成键原子的电子静电作用基础上的电负性。
鲍林电负性

鲍林电负性1定义电负性综合考虑了电离能和电子亲合能,首先由莱纳斯·鲍林于1932年提出。
它以一组数值的相对大小表示元素原子在分子中对成键电子的吸引能力,称为相对电负性,简称电负性。
元素电负性数值越大,原子在形成化学键时对成键电子的吸引力越强。
2计算方法电负性的计算方法有多种,每一种方法的电负性数值都不同,比较有代表性的有3种:① L.C.鲍林提出的标度。
根据热化学数据和分子的键能,指定氟的电负性为3.98,计算其他元素的相对电负性。
②R.S.密立根从电离势和电子亲合能计算的绝对电负性。
③A.L.阿莱提出的建立在核和成键原子的电子静电作用基础上的电负性。
利用电负性值时,必须是同一套数值进行比较。
同一周期从左至右,有效核电荷递增,原子半径递减,对电子的吸引能力渐强,因而电负性值递增;同族元素从上到下,随着原子半径的增大,元素电负性值递减。
过渡元素的电负性值无明显规律。
就总体而言,周期表右上方的典型非金属元素都有较大电负性数值,氟的电负性值数大(4.0);周期表左下方的金属元素电负性值都较小,铯和钫是电负性最小的元素(0.7)。
一般说来,非金属元素的电负性大于2.0,金属元素电负性小于2.0。
电负性概念还可以用来判断化合物中元素的正负化合价和化学键的类型。
电负性值较大的元素在形成化合物时,由于对成键电子吸引较强,往往表现为负化合价;而电负性值较小者表现为正化合价。
在形成共价键时,共用电子对偏移向电负性较强的原子而使键带有极性,电负性差越大,键的极性越强。
当化学键两端元素的电负性相差很大时(例如大于1.7)所形成的键则以离子性为主。
3常见元素电负性鲍林标度鲍林指定氟的电负性为4.0,并以此为标准确定其他元素的电负性。
氢 2.1 锂 0.98 铍 1.57 硼 2.04 碳 2.55 氮 3.04 氧 3.44 氟 3.98 钠 0.93 镁 1.31 铝 1.61 硅 1.90 磷 2.19 硫 2.58 氯 3.16钾 0.82 钙 1.00 锰 1.55 铁 1.83 镍 1.91 铜 1.9 锌 1.65 镓 1.81 锗2.01 砷 2.18 硒 2.48 溴 2.96铷 0.82 锶 0.95 银 1.93 碘 2.66 钡 0.89 金 2.54 铅 2.33一般来说,电负性大于1.8的是非金属元素,而小于等于1.8的往往是金属元素(当然,其中也存在例外)电负性对应氧化性特殊元素O的电负性比N的大呀,N的第一电离需要破坏2P半充满的低能状态,O 的第一电离形成了 2P半充满的低能状态,所以N的第一电离能比O的大,O的非金属性比N强,所以O的电负性比N的大4在周期表内的递变规律1.随着原子序号的递增,元素的电负性呈现周期性变化。
元素电负性表格

Theoretical Method Density Functional Electronegativity Formulation In DFT the electronegativity assumes the general form [37]: ∂E χ ( N ) = − ∂N V (1)
χM =
b + N −1 2 a
N −1 b + N +1 N + 1 C A − 1 a + ( N − 1) 2 arctan arctan − + 4 ln a + ( N + 1) 2 2 a a a
(4)
where in order to simplify the expression, the following definitions have been introduced:
*
Permanent address: Chemistry Department, West University of Timisoara, Str. Pestalozzi
No.16, Timisoara, RO-1900, Romania.
In the framework of the density functional theory a new electronegativity formulation via the Feynman-Kleinert path integral formalism in the markovian limit is proposed. The computation of the electronic density follows, in terms of partition function, the same procedure of the Levy’s constrained-search for the wave function. The obtained electronegativity scale seems to respect the main criteria largely used for its acceptability.
电负性

电负性鲍林标度电负性表电负性的定义电负性(Electronegativity)又称为相对电负性,简称电负性。
电负性综合考虑了电离能和电子亲合能,首先由莱纳斯·卡尔·鲍林于1932年引入电负性的概念,用来表示两个不同原子形成化学键时吸引电子能力的相对强弱,是元素的原子在分子中吸引共用电子的能力。
通常以希腊字母χ为电负性的符号。
鲍林给电负性下的定义为“电负性是元素的原子在化合物中吸引电子能力的标度”。
元素电负性数值越大,表示其原子在化合物中吸引电子的能力越强;反之,电负性数值越小,相应原子在化合物中吸引电子的能力越弱(稀有气体原子除外)。
一个物理概念,确立概念和建立标度常常是两回事。
同一个物理量,标度不同,数值不同。
电负性可以通过多种实验的和理论的方法来建立标度。
计算方法首先需要说明,电负性是相对值,所以没有单位。
而且电负性的计算方法有多种(即采用不同的标度),因而每一种方法的电负性数值都不同,所以利用电负性值时,必须是同一套数值进行比较。
比较有代表性的电负性计算方法有3种:① L.C.鲍林提出的标度。
根据热化学数据和分子的键能,指定氟的电负性为4.0,锂的电负性1.0,计算其他元素的相对电负性。
②R.S.密立根从电离势和电子亲合能计算的绝对电负性。
③A.L.阿莱提出的建立在核和成键原子的电子静电作用基础上的电负性。
常见元素的电负性变化氟〉氧〉氮= 氯〉溴〉碘= 硫= 碳铝>铍>镁>锂=钙>钠>钾电负性的周期性变化氢 2.1 锂1.0铍 1.57 硼 2.04 碳 2.55 氮 3.04 氧 3.44 氟 4.0 钠 0.93 镁 1.31 铝 1.61 硅 1.90 磷 2.19 硫 2.58 氯 3.16 钾 0.82 钙 1.00 锰 1.55 铁 1.83 镍 1.91 铜 1.9 锌 1.65 镓1.81 锗2.01 砷 2.18 硒 2.48 溴 2.96铷 0.82 锶 0.95 银 1.93 碘 2.66 钡 0.89 金 2.54 铅 2.33一般来说,周期表从左到右,元素的电负性逐渐变大;周期表从上到下,元素的电负性逐渐变小。
贾-电负性表精编版
……………………………………………………………最新资料推荐…………………………………………………
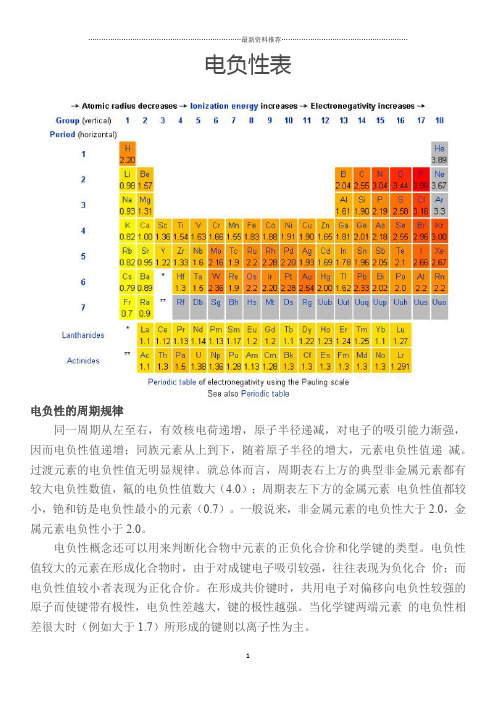
电负性表
电负性的周期规律
同一周期从左至右,有效核电荷递增,原子半径递减,对电子的吸引能力渐强,因而电负性值递增;同族元素从上到下,随着原子半径的增大,元素电负性值递减。
过渡元素的电负性值无明显规律。
就总体而言,周期表右上方的典型非金属元素都有较大电负性数值,氟的电负性值数大(4.0);周期表左下方的金属元素电负性值都较小,铯和钫是电负性最小的元素(0.7)。
一般说来,非金属元素的电负性大于2.0,金属元素电负性小于2.0。
电负性概念还可以用来判断化合物中元素的正负化合价和化学键的类型。
电负性值较大的元素在形成化合物时,由于对成键电子吸引较强,往往表现为负化合价;而电负性值较小者表现为正化合价。
在形成共价键时,共用电子对偏移向电负性较强的原子而使键带有极性,电负性差越大,键的极性越强。
当化学键两端元素的电负性相差很大时(例如大于1.7)所形成的键则以离子性为主。
1。
