zxy-13杂环化合物
第十三章 杂环化合物和生物碱 - 药学系-盐城卫生职业技术学院

吡咯
呋喃
噻吩
在呋喃、噻吩、吡咯分子中,由于杂原子的未共用电子对参与了共轭体系(6 个π电子
分布在由 5 个原子组成的分子轨道中),使环上碳原子的电子云密度增加,因此环中碳原子
的电子云密度相对地大于苯中碳原子的电子云密度,所以此类杂环称为富电子共轭体系或多
π电子共轭体。
杂原子氧、硫、氮的电负性比碳原子大,使环上电子云密度分布不象苯环那样均匀,所
以呋喃、噻吩、吡咯分子中各原子间的键长并不完全相等,因此芳香性比苯差。由于杂原子
的电负性强弱顺序是:氧>氮>硫,所以芳香性强弱顺序如下:苯>噻吩>吡咯>呋喃。
9
8
嘌呤
(Purine)
5 6 7
8
4 3
N2 1
5 6 7
8
4 3
N2 1
喹啉
异 喹啉
(Quinoline)
8 91
7
2
(Iso-quinoline)
9 8
H
N 10
1 2
6 5
3
N 10
4
吖啶
7 6
3
S 5
4
吩噻嗪
(Acridine)
(Phenothiazine)
二、杂环化合物的命名
杂环化合物的名称包括杂环母环和环上取代基两方面。取代基的命名原则与前述基本一
相当。
四、六元杂环化合物的性质
(一)溶解性
吡啶分子中氮原子上的未共用电子对不参与形成闭合的共轭体系,氮原子可与水分子形
13-杂环

吡唑 pyrozole
噁唑 oxazole
六 元 杂 环
5 6 1
3 2
5 6 1
3 2
5 6 1
3 2
5 6 1
3 2
吡啶 pyridine
嘧啶 pyrimidine
哒嗪 pyridazin
吡喃 pyran
稠杂环
6 7 5 4 3 2 6 7 5 4 3 2 5 6 4 1 7 3 2 2 1 6 4 3 5 9 7 8
E N H H
E H
E N H H
E H
E N H H
E H
八隅体结构最稳定 无最稳定结构
这些杂环进行亲电取代反应时,须 用缓和的试剂在温和的条件下进行.
*1 亲电取代反应的活性顺序
N H
>
O
>
S
>
吸电子诱导:O(3.5) > N(3.0) > S(2.6) 给电子共轭:N > O > S 综合:N贡献电子最多,O其次,S最少 *2 取代反应主要发生在α-C
第二节 五元杂环化合物 一、呋喃、噻吩、吡咯 1. 结构
O S
呋喃
噻吩
吡咯
与苯环的6原子共6π电子比,呋喃、噻吩、 吡咯为5原子共用6个π电子,故环上π电子 密度比苯环大,属于“富π芳杂环”。
所有成环原子都以sp2杂化轨道重叠形成σ键; 碳原子p轨道互相平行重叠形成6电子 环状共轭大π键。 呋喃环 中的杂原子 O (噻吩中为 S) 的 1 个 sp2 杂化轨道上 有一对未共 用电子对。
Z
G (m)
2-取代呋喃在强亲电试剂的作用下则进入5-位:
O
G (o, p, m)
(2) 呋喃、噻吩、吡咯的硝化反应 呋喃, 噻吩和吡咯易氧化, 一般不用硝酸 直接硝化; 通常用比较温和的非质子硝化试剂, 如:硝酸乙酰酯。反应在低温下进行。
杂环化合物的命名
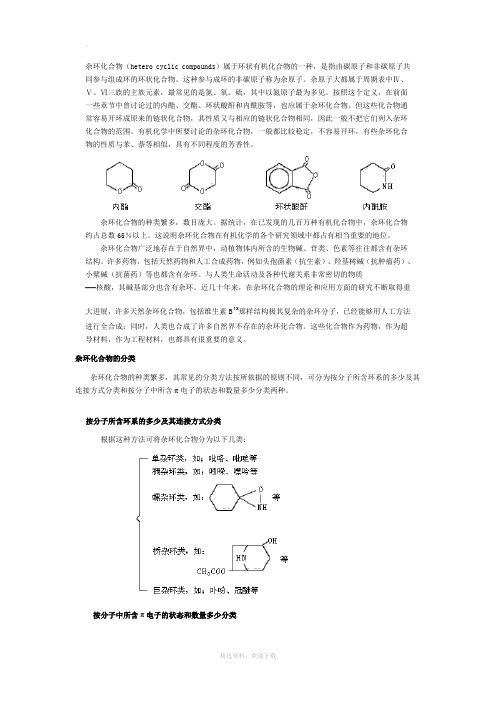
杂环化合物(hetero cyclic compounds)属于环状有机化合物的一种,是指由碳原子和非碳原子共同参与组成环的环状化合物。
这种参与成环的非碳原子称为杂原子。
杂原子大都属于周期表中Ⅳ、Ⅴ、Ⅵ三族的主族元素,最常见的是氮、氧、硫,其中以氮原子最为多见。
按照这个定义,在前面一些章节中曾讨论过的内酯、交酯、环状酸酐和内酰胺等,也应属于杂环化合物。
但这些化合物通常容易开环成原来的链状化合物,其性质又与相应的链状化合物相同,因此一般不把它们列入杂环化合物的范围。
有机化学中所要讨论的杂环化合物,一般都比较稳定,不容易开环,有些杂环化合物的性质与苯、萘等相似,具有不同程度的芳香性。
杂环化合物的种类繁多,数目庞大。
据统计,在已发现的几百万种有机化合物中,杂环化合物约占总数65%以上。
这说明杂环化合物在有机化学的各个研究领域中都占有相当重要的地位。
杂环化合物广泛地存在于自然界中,动植物体内所含的生物碱、苷类、色素等往往都含有杂环结构。
许多药物,包括天然药物和人工合成药物,例如头孢菌素(抗生素)、羟基树碱(抗肿瘤药)、小檗碱(抗菌药)等也都含有杂环。
与人类生命活动及各种代谢关系非常密切的物质──核酸,其碱基部分也含有杂环。
近几十年来,在杂环化合物的理论和应用方面的研究不断取得重大进展,许多天然杂环化合物,包括维生素B那样结构极其复杂的杂环分子,已经能够用人工方法进行全合成;同时,人类也合成了许多自然界不存在的杂环化合物。
这些化合物作为药物,作为超导材料,作为工程材料,也都具有很重要的意义。
杂环化合物的分类杂环化合物的种类繁多,其常见的分类方法按所依据的原则不同,可分为按分子所含环系的多少及其连接方式分类和按分子中所含π电子的状态和数量多少分类两种。
按分子所含环系的多少及其连接方式分类根据这种方法可将杂环化合物分为以下几类:按分子中所含π电子的状态和数量多少分类按照这种方法可将杂环化合物大致分为四类,即:(1)多π-(π-excessive)杂环。
杂环化合物HeterocyclicCompounds

43
H3C 4 N3
5
O
2 CHO
1
5
2
N1
H
4 N3
5 H3C
S
2
1
2-呋喃甲醛
4-甲基咪唑 5-甲基噻唑
上页 下页 返回 退出
β' β
α'
α
H3C
O
CH3
α ,α'-二甲基呋喃 ,?
CH3 γ β
Nα
γ-甲基吡啶 -
上页 下页 返回 退出
12.3 五元杂环化合物
12.3.1 呋喃、噻吩和吡咯旳构造 12.3.2 呋喃、噻吩和吡咯旳性质 12.3.3 糠醛
有机化学
12 杂环化合物
(Heterocyclic Compounds)
下页 返回 退出
基本内容和要点要求
杂环化合物旳分类和命名; 杂环化合物旳构造和芳香性; 五元杂环化合物旳化学性质; 六元杂环化合物旳化学性质; 生物碱
要点要求掌握芳香性;五元、六元杂环化合物 旳化学性质,杂环化合物旳亲电取代反应旳活性及 规律;酸碱性规律。
呋喃是无色液体,沸点32℃,具有类似氯仿旳气 味,微溶于水,易溶于乙醇、 乙醚等有机溶剂。呋喃 能使盐酸浸过旳松木片显绿色,此现象可检验呋喃旳存 在。
噻吩与苯共存于煤焦油中, 噻吩是无色而有特殊 气味旳液体,沸点84℃。噻吩和靛红(吲哚满二酮)在 硫酸作用下呈蓝色,此现象可检验噻吩旳存在。
吡咯存在于煤焦油和骨焦油中,是无色液体,沸点 131℃,有弱旳苯胺旳气味。其蒸气遇盐酸浸湿旳松木 片则呈红色,可检验吡咯旳存在。
(1)制备
+ (C5H8O4)n
H2O
稀 H2SO4 加热
n C5H10O5 戊醛糖
杂环化合物——精选推荐

杂环化合物杂环化合物杂环化合物是⼀种含有环的化合物,这个环由⼀种以上原⼦所组成。
⼀般将杂环化合物分为两类:⼀类是脂肪族杂环化合物,另⼀类是具有⽅向性的杂环化合物。
杂环化合物在⽇常⽣活中应⽤⼴泛。
是合成药物,合成染料,合成材料的重要原料之⼀。
是⼀⼤类有机化合物。
在理论上和实际中都有⼗分重要意义。
杂环化合物已经成为芳⾹性杂环化合物的代名词。
杂环化合物数⽬很多,根据环的⼤⼩,杂原⼦的多少和单环、稠环来分类。
最常见的和最稳定的是五元和六元单杂环及其相应的稠杂环,咋换上的编号⼀般是从杂原⼦开始,从阿拉伯数字1、2、3表⽰顺次,如同环中含有不同杂原⼦时,按O\S\N先后顺序排列进⾏编号,若有取代基则要考虑到取代基编号最⼩。
五元杂环--五元杂环中含有两个杂原⼦,其中⼀个必须是N原⼦(称固定氮原⼦)的叫做唑,第⼆个原⼦为氧原⼦的叫恶唑;第⼆个原⼦为硫原⼦的叫噻唑,第⼆个原⼦为氮原⼦的叫咪唑或吡唑,命名时还要标出两个杂原⼦的位置。
即为1,2-唑六元杂环含有两个杂原⼦的六元环有三种情况:杂原⼦互为邻位、间位、和对位。
含有两个氮原⼦的叫⼆嗪。
如”吡啶“含⼀个氮原⼦的吡啶稠杂环稠杂环是两个以上环稠合⽽成,其中⼀个是基本环,另⼀个是附加环,命名时附加环在前,基本环在后。
单环都可以作为基本环,个别稠杂环是基本环,如吲哚(苯并吡咯),喹啉(苯并吡啶),嘌啉(嘧啶并吡唑)由芳环与杂环组成的稠杂环。
杂环优先(即杂环为基本环),如:苯并呋喃、苯并咪唑,由两个杂环组成的稠杂环,⼤环优先于⼩环。
环数相同时,N、O、S杂原⼦顺序确定。
如;吡咯并吡啶,噻吩并吡咯。
环上杂原⼦数⽬多的优先,杂原⼦数⽬相同时,杂原⼦种类多的优先例如:吡啶并嘧啶、咪唑并恶唑、咪唑并噻唑。
环上杂原⼦数⽬及种类都相同时,同环杂原⼦编号低的优先。
(2)稠环共⽤边的标记。
附加环按其杂环的编号顺序编号,并以阿拉伯数字1、2、3.。
将各原⼦进⾏标记,苯环上的原⼦不需要编号,命名时在附加环名称的后⾯加⼀个并字。
杂环化合物 名词解释(一)

杂环化合物名词解释(一)
杂环化合物名词解释
1. 什么是杂环化合物?
•杂环化合物是指分子中包含由不同原子构成的环结构的有机化合物。
•这些不同原子可以是碳、氮、氧、硫、磷等元素。
2. 杂环化合物的命名规则
•杂环化合物的命名通常采用系统命名法,根据杂环中的原子种类和连接方式进行命名。
•常见的命名方式包括简化命名法、希伯来命名法、Carothers命名法等。
3. 杂环化合物的例子
含氮杂环化合物
•吡嗪(Pyridine)是一种含氮杂环化合物,分子式为C5H5N。
它是一种具有特殊芳香性的有机溶剂,在制药、农药、染料等领域广泛应用。
含氧杂环化合物
•苯并噁嗪(Benzoxazine)是一种含氧杂环化合物,分子式为C7H5NO。
它是一种具有高分子量和高热稳定性的树脂,常用于复
合材料、涂层和粘合剂等领域。
含硫杂环化合物
•噻吩(Thiophene)是一种含硫杂环化合物,分子式为C4H4S。
它是一种具有特殊芳香性的有机化合物,在染料、橡胶、涂层等领
域有广泛应用。
含磷杂环化合物
•噁磷酮(Oxaphosphole)是一种含磷杂环化合物,分子式为C4H5PO。
它是一种重要的有机合成中间体,广泛应用于有机合成
和均相催化反应中。
4. 总结
•杂环化合物是一类具有不同原子构成的环结构的有机化合物。
•杂环化合物的命名规则包括系统命名法和常用的简化命名法。
•各种杂环化合物在不同领域有广泛应用,如溶剂、树脂、染料等。
第十三章杂环化合物

第三节 重要的杂环化合物及其衍生物~糠醛 重要的杂环化合物及其衍生物~
一、呋喃衍生物
1.糠醛 1.糠醛 糠醛具有芳香醛的特征。性质与苯甲醛相似, 糠醛具有芳香醛的特征。性质与苯甲醛相似,可 以发生氧化、还原、歧化及环上取代等反应。 以发生氧化、还原、歧化及环上取代等反应。 2.呋喃唑酮 呋喃唑酮( 2.呋喃唑酮(痢特灵 ) 3.呋喃妥因( 3.呋喃妥因(呋喃坦丁 ) 呋喃妥因
三、重要的生物碱
1.烟碱 1.烟碱
又名尼古丁 剧毒,属吡啶衍生物类生物碱。 又名尼古丁,剧毒,属吡啶衍生物类生物碱。为 尼古丁, 无色或微黄色液体,在烟草中以柠檬酸盐或苹果酸盐 无色或微黄色液体, 的形式存在。烟碱也是有效的农业杀虫剂。 的形式存在。烟碱也是有效的农业杀虫剂。 2.麻黄碱
Pd
S
+ 2H2
0.2~0.4MPa
S 四氢噻吩 N H 四氢吡咯
N H
Ni + 2H2 200℃
第四节 六元杂环化合物
一、吡啶的结构
..
N原子为sp2杂化
. .
. .
. .
吡啶π电子数符合休克尔规则,具有芳香性。 吡啶π电子数符合休克尔规则,具有芳香性。吡 啶的芳香性比苯弱。 啶的芳香性比苯弱。
呋喃
噻吩
吡咯
二、呋喃、噻吩、吡咯的性质 呋喃、噻吩、
呋喃存在于松木焦油中,其蒸气遇到浸过盐酸的 呋喃存在于松木焦油中, 松木片时呈绿色 叫做松木片反应 绿色, 松木片反应。 松木片时呈绿色,叫做松木片反应。此现象可用来鉴 定呋喃。 定呋喃。 噻吩存在于煤焦油的粗苯及石油中,在浓硫酸存 噻吩存在于煤焦油的粗苯及石油中, 在下,与靛红一同加热显示蓝色 反应灵敏。 蓝色, 在下,与靛红一同加热显示蓝色,反应灵敏。可用来 检验噻吩。 检验噻吩。 吡咯存在于煤焦油和骨焦油中,其蒸气或其醇溶 吡咯存在于煤焦油和骨焦油中, 液能使浸过盐酸的松木片呈红色 红色, 液能使浸过盐酸的松木片呈红色,此反应可用来鉴定 吡咯。 吡咯。
杂环化合物

(a)硝化
S
+ CH3COONO2
0oC
Ac2O
AcOH
(b)磺化
+
S NO2
66 %
NO2
S
10%
+
N H
(c)卤化
+
N
-
SO3
100 oC
N
SO3H
H 90%
1,4- 二氧六环
+ Br2
O
25oC
75 %
O Br
(d)Friedel-Crafts酰基化
+ Ac2O 150 200 oC
N H
O H
O H
O
Br2
CH3COOK CH3OH
H
H
CH3O O OCH3
H
H
Br O Br
1,4加成
CH3OH
(2)噻吩
Cl2 S Cl Cl S Cl
亲电加成 H2SO4
S SO3H
(CH3CO)2O
O
S
H3PO4
S CCH3
催H化2,加N氢i S
H
H
H
H
S
(3)吡咯
碱性
极弱
NH2
N H<
< NH3
O
O
H H
O
O
H
O2N
O CH=N N
N
N
H O
呋喃唑酮(痢特灵)
H
H
O2N
H O
H H
N
O
O
H
O CH= CHCNHCH(CH3)2 O
H N
H H
H
H
H H
O H
13杂环化合物

卟吩胆色素原
卟吩胆色素原; 通过生物体内特定酶的作用可转变成 卟啉、叶绿素和维生素B12等重要生物活性物质
NH N
N HN
卟吩 (P ro p h in e)
卟吩由四个吡咯和四个次甲基(=CH)交替相 连组成的共轭体系。
卟吩呈平面结构,环中间的空隙里四个氮原 子可分别以共价键、配价键与不同的金属离 子结合。
K O H
- +H 2 O
N
N
H
K +
C H 3 M g I N 乙 醚 H
2) 呋喃、噻吩、吡咯的反应
(1) 亲电取代反应
+ C H 4 N
M g I
呋喃、吡咯和噻吩的亲电取代反应都比苯活 泼(吡咯>呋喃>噻吩>苯) 。由于它们的高度活泼 性以及呋喃和吡咯对于无机强酸的敏感性,其亲 电取代反应需要比较温和的条件。
H 3 C
C H 3
H 3 C
T sO H
C H 3 H 3 C
C H 3
H 3 C
H-H 2 O
C H 3
O O 甲 苯 , H OO
O O H
O
C H 3
C H 3 O O
P 2 S 5
CH3
OO
NH3 CH3 甲苯,
C H 3 S
CH3
CH3 N H
C H 3
4) 呋喃、吡咯、噻吩的衍生物 (1) 糠醛
1). 结构与物理性质
N
N
N N H
吡唑
S
噻唑
O
噁唑
N O
异噁唑
N
HN
H
N
H
H
咪唑
N
sp2
杂环化合物

杂环化合物杂环化合物(Heterocyclic compounds)是分子中含有杂环结构的有机化合物。
构成环的原子除碳原子外,还至少含有一个杂原子。
是数目最庞大的一类有机化合物。
最常见的杂原子是氮原子、硫原子、氧原子。
可分为脂杂环、芳杂环两大类。
杂环化合物普遍存在于药物分子的结构之中。
是数目最庞大的一类有机物。
杂环化合物广泛存在于自然界,与生物学有关的重要化合物多数为杂环化合物,例如核酸、某些维生素、抗生素、激素、色素和生物碱等。
此外,还合成了多种多样具有各种性能的杂环化合物,其中有些可作药物、杀虫剂、除草剂、染料、塑料等。
分类方法按碳原子数最常见的杂环化合物是五元和六元杂环及苯并杂环化合物等。
五元杂环化合物有:呋喃、噻吩、吡咯、噻唑、咪唑等。
六元杂环化合物有:吡啶、吡嗪、嘧啶、哒嗪等。
稠环杂环化合物有:吲哚、喹啉、蝶啶、吖啶等。
杂环化合物中,最小的杂环为三元环,最常见的是五、六元环,其次是七元环。
杂环的成环规律和碳环一样,最稳定、最常见的杂环也是五元或六元的。
一些芳杂环化合物命名方法杂环化合物常以俗名命名,较少用系统命名。
系统命名是指以相应的碳环为母体而命名。
例如,含两个不饱和键的环戊二烯称为茂,与之相应的一种杂环化合物,例如吡咯,可以看成是由“NH”取代了茂中的“CH2”而成,称为氮(杂)茂。
依此类推,吡啶称为氮(杂)苯,喹啉称为氮(杂)萘等,但一般仍习惯于用俗名命名。
杂环化合物的中文名称是以口字旁标明其为杂环,另半部分表明杂原子的种类。
例如,以喃、噻分别表示为含氧、硫的杂环;以咯、唑、嗪、啶、啉表示为含氮的杂环,这些字是根据英文字的尾音创造的,其中咯、唑表示为五元含氮杂环,其余的指六元含氮杂环。
杂原子超过一个者分别以二、三等字表示相同杂原子的数目,例如:二唑,表示该杂环化合物为含有一个氧和两个氮杂原子的五元杂环。
在环中不同的原子可有不同的排列方式,命名时各原子的位置编号遵循下列原则:1、只含一个杂原子或一个以上相同杂原子的杂环,杂原子编最小号;2、含两个不同杂原子时,不同杂原子的编号顺序为氧、硫、氮。
杂环化合物的命名知识讲解

基本环各边用英文 字母表示。1,2原 子之间为a,2,3原 子之间为b …
3e d
aN
N
2
cb
N
1
吡啶并[2,3-d] 嘧啶
35
附加环 附加环
4
3
c b
d
5
2
S
a
e
O
1
噻吩并[2,3-b]呋喃
3 a NH
b
O2 c
1 呋喃并 [3,2-b]吡咯
36
基本环
基本环
数字走向与基 本环一致
32N1N54deNcaNb HH
212. 喹啉和异喹啉源自8 71N2
6
5 性质
3 4
与萘的结构相似
8 7
6 5
1
N2
3 4
喹啉和异喹啉是由一个苯环和一个吡啶环稠 合而成的。
22
3. 嘌呤
嘧啶环与咪唑环稠合
65
1N
N7
2
8
N
3
4 N9 H
9H - 嘌呤
65 7
1N
NH
2 N 4N 8
39
7H - 嘌呤
NH2
6 1N
5N
2
N 3
4
Fe
二茂铁
OS
N
H
茂 氧杂茂 硫杂茂 氮杂茂
呋喃 噻吩 吡咯
8
N
N
N
S
N
N
H
H
噻唑
吡唑
咪唑
1,3-硫氮杂茂 1,2-二氮杂茂 1,3-二氮杂茂
• 在没有误会的情况下,“杂”字可以省去。
9
N
O
苯
芑
氮杂苯 氧杂芑
有机化学 第13章 杂环化合物

π66离域大π键。芳香体系
吡啶结构与性能 结构:吡啶N是sp2杂化,孤电子对不参与共轭 反应: N: 孤电子对不参与共轭, 碱性较强 N:共轭效应和诱导效应都是吸电子性 亲电取代: 难 ,发生在环上N的间位(即N的β位)。 亲核 取代:较易 ,亲核取代反应发生在N的邻、对位。
二. 吡啶的化学性质
5 4 1
N N H
3 2
CH3
5
NH N
3 2
1
4 5
3
4 3
5
4
CH3
N H
1
N2 CH3
N
2
NH 1
4-甲基咪唑 5-甲基咪唑 4(5)-甲基咪唑
6 1
5-甲基吡唑 3-甲基吡唑 3(5)-甲基吡唑
6 5 7
9H - 嘌啉
N N
3
5 9
N7 N H
8
1 2
N N
3
NH N
9 8
2
4
4Байду номын сангаас
7H - 嘌啉
苯并吡咯 吲哚 (indole)
唑类:含至少一个N的两个杂原子的五元杂环,称为唑。
1,2-唑
4 5
3 N2 O 1 5
4
3 N2 S 1
5
4 N H1
3 N2
异噁唑(isoxazole) 异噻唑(isothiazole)
吡唑(pyrazole)
1,3-唑
4 5
N3 O1 2
4 5
N S1
3 2
5
4
2
AcONO2 O oC
N H
Ac2O/AcOH
N H 51 %
(2)呋喃、噻吩、吡咯的磺化反应
杂环化合物及生物碱详解演示文稿

完成下列化学反应方程式:
1) O
CH3COONO2 C2H5
OCH3
2) S
HNO3 H2SO4
3) S
第十四页,共26页。
NO2
Br2 醋酸
4)
(CH3CO)2O
N
~200℃
H
吡啶化学活泼性比苯环小,不发生付克烃基化和酰化反应。
第十五页,共26页。
N
浓H2SO4 N 浓HNO3
OH
N NO2 Fe/HCl N
结构
单杂环化合物的性质
N
H
N
第八页,共26页。
吡啶
吡咯
芳杂环结构特点: ① 五元杂环:富π电子环系,比苯环更 发生亲电取代;
② 六元杂环:缺π电子环系,比苯环 更。
第九页,共26页。
一、物理性质(自学); 二、化学性质:
1. 亲电取代反应:
芳香性:
<
<
<
O
N
S
H
第十页,共26页。
吡咯、呋喃在位反应,反应用特
⑵ 环的编号从杂原子开始:
O
CH3
2-甲基呋喃 α-甲基呋喃
O
CHO
2-呋喃甲醛 (糠醛)
N
CH3 N-甲基吡咯 1-甲基吡咯
第四页,共26页。
含多个杂原子的杂环,按 O, S , N的 次序编号:
43 N
5
2
O
1
噁唑 (oxzole)
N
S
噻唑 (thiazole)
43 N
5
2
N H
1
咪唑 (imidazole)
3. 含氮杂环的酸碱性:
吡咯弱酸性:
13 杂环化合物

6
N2
N
1
哒嗪
pyridazine
6
2
6
N
1
嘧啶
pyrimidine
4
3
N
5
2
N H
1
咪唑
4
N
3
2
N
1
吡嗪
pyrazine
杂环分类
碳环母核
萘
稠
杂
环
茚
蒽
Chapter 13
重要的杂环
5 6
4 3
7 8
2
N1
喹啉
quinoline
5 6
4 3
7 8
N2
1
异喹啉
isoquinoline
4
5
3
6 7
2
N1 H
叶绿素a
Chapter 13
13.3.4 五元杂环的亲电取代规律
第二个取代基进入五元环,第一个取代基有定位 作用,杂原子也有α-定位作用。
1. α-位有邻对位定位基(x)时,E +进入5位,3 位 次之。
E
XE Z
E
X
X
Z
Z
主要
次要
Chapter 13
2. β -位有邻对位基(X)时,E 进+ 入2 位,少量 进入5位。
2. 反 应 (1) 水解
O
+ H 2O CHO
ZnO-Cr2O3-MnO 2 400 ~415oC
制备呋喃方法
(2) 有醛的性质
Cannizzaro反应:
+ CO2 + H 2 O
2
+Na O H
O C H O
1213杂环化合物的化学性质

。
。
+ CH3COONO2 -5 C ~ − 30 C
O
+ CH3COONO2 S
(CH3CO)2O 。
-10 C
+ CH3COONO2 N H
(CH3CO)2O 。
-10 C
O NO2 + CH3COOH
S NO2 + CH3COOH
N NO2 + CH3COOH H
吡啶的硝化反应要在浓酸和高温条件下才能进行:
N
H
H
Na + C2H5OH + 6[H]
N
N
H
呋喃的芳香性最弱,它还可以发生 1,4-加成反应,例如它能与顺丁烯二 酸酐发生双烯合成反应:
O
+
O
OOO
OO O
(3)吡咯和吡啶的酸碱性。吡咯由于其氮原子上的孤电子对参与共轭,使 氮原子的电子云密度降低,N—H 键的极性增强,所以它的碱性(pKb=13.6) 不但比苯胺(pKb=9.4)弱得多,而且显微弱的酸性(pKa=15),能与氢氧化钾 作用生成吡咯钾盐:
12.1.3 杂环化合物的化学性质 Chemical Properties of Heterocyclic Compounds
(1)亲电取代反应。五员杂环属于富电子体系,亲电取代反应容易进行, 一般在较缓和的条件下弱的亲电试剂就可以取代环上的氢原子。而六员杂环吡 啶是缺电子体系,较难发生亲电取代反应,一般要在较强烈的条件下才能发生 反应。
CH2CH3 HNO3
N
HNO3
N
COOH N
COOH N COOH
(5)氧化反应。富电子的五员杂环上的碳原子的电子云密度比苯环上的相 对增加,吡咯和呋喃易与氧化剂作用,特别是在酸性条件下氧化反应更易发生, 氧化的结果导致环的破裂或聚合物的生成,噻吩相对要稳定些。吡啶对氧化剂 比苯还稳定很难氧化,即使用浓硫酸或酸性高锰酸钾作氧化剂,在加热的情况 下也不被氧化,吡啶的烃基衍生物在强氧化剂的作用下只发生侧链氧化,生成 吡啶甲酸:
杂环化合物
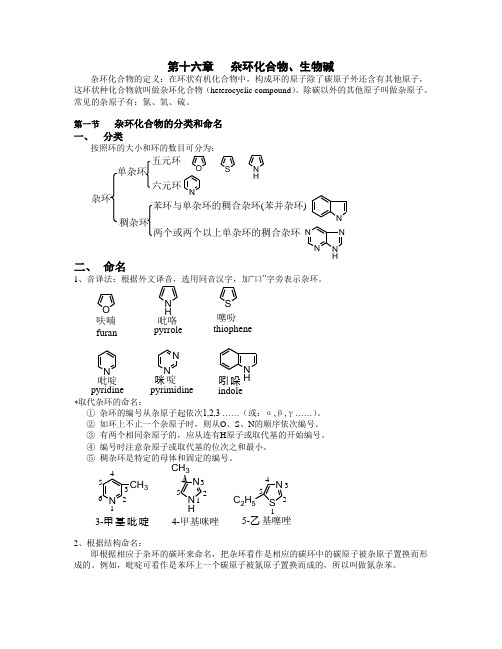
第十六章 杂环化合物、生物碱杂环化合物的定义:在环状有机化合物中,构成环的原子除了碳原子外还含有其他原子,这环状种化合物就叫做杂环化合物(heterocyclic compound )。
除碳以外的其他原子叫做杂原子。
常见的杂原子有:氮、氧、硫。
第一节 杂环化合物的分类和命名一、 分类按照环的大小和环的数目可分为:杂环单杂环五元环六元环苯环与单杂环的稠合杂环(苯并杂环)两个或两个以上单杂环的稠合杂环O SN H稠杂环NNNNN HN二、 命名1、音译法:根据外文译音,选用同音汉字,加―口‖字旁表示杂环。
O S N H 吡咯呋喃噻吩吡啶N pyrrolefuranthiophenepyridine N H 吲哚indole N N咪啶pyrimidine取代杂环的命名: ① 杂环的编号从杂原子起依次1,2,3 ……(或:α,β,γ……)。
② 如环上不止一个杂原子时,则从O 、S 、N 的顺序依次编号。
③ 有两个相同杂原子的,应从连有H 原子或取代基的开始编号。
④ 编号时注意杂原子或取代基的位次之和最小。
⑤ 稠杂环是特定的母体和固定的编号。
N S 512435-乙基噻唑N N H23454-甲基咪唑CH 3C 2H 5N CH 31234563-甲基吡啶2、根据结构命名:即根据相应于杂环的碳环来命名,把杂环看作是相应的碳环中的碳原子被杂原子置换而形成的。
例如,吡啶可看作是苯环上一个碳原子被氮原子置换而成的,所以叫做氮杂苯。
O SN HN茂(环戊二烯)氮茂氧茂硫茂NN苯氮苯1,3-二氮苯第二节 一杂五元杂环化合物含有一个杂原子的典型五元杂环是呋喃、噻吩、吡咯。
OSN H一、 呋喃、噻吩、吡咯的结构 1、据现代物理方法证明:① 呋喃、噻吩、吡咯都是一个平面的五元环结构,即成环的四个C 原子和一个杂原子都是以SP 2杂化轨道成键的。
②环上每个碳原子的P 轨道有一个电子,杂原子P 轨道上有两个电子。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
+ PhN Li 加成
H Ph N Li
-H
+
O2 or HNO 3
+ Li+ Ph N Li Ph N
消除
(3)齐齐巴宾(Chichibabin, A.E.)反应——氨化
定义:吡啶与氨基钠作用生成2-氨基吡啶的反 应称为齐齐巴宾反应。
+ NaNH2
N
100oC C6H5N(CH3)2
N
浓 H2SO4,HgSO4 220 C
o
N
300 C,1d
o
6%
浓 H2SO4,KNO3
NO2
Br2,浮石
Br N 66 %
H3C
N
CH3
100 C
o
H3C
N 66 %
CH3
N
300 C
o
反应特点: 不能发生傅氏烷基化、酰基化反应。 硝化、磺化、卤化必须在强烈条件下才能发生; 吡啶环上有给电子基团时,反应活性增高; 吡啶N可以看作是一个间位定位基。
G A G G
• 三个共振式 • 推电子基使 稳定
E
A 进入2位
E
E
最稳定
A
E
4 5
G
E
2
E 进入4位 A
G
E A
不稳定
G
• 二个共振式 • 推电子基未 起作用
A
进入5位
E
G
G
G
E
A
E
A
较稳定
• 三个共振式 • 推电子基未 起作用
E
A
(iv) b位有吸电子基
W W W
• 三个共振式 • 吸电子基使 不稳定
O 1
3β 2α
4 5
S 1
3β 2α
4 5 1N H
3β 2α
呋喃(furan)
噻吩(thiophene)
吡咯(pyrrole)
五元杂环苯并体系
4 5 6 7 O 1 3 2
4 5 6 7 S 1 3 2
4 5 6 7 N H1 3 2
苯并呋喃 (benzofuran)
苯并噻吩 (benzothiophene)
应用:除去苯或甲苯中的噻吩
H2SO4 S
(少量) 反应快 溶解于硫酸中
&
r. t. S SO3H
C、其它亲电取代反应
• 卤代反应
Br2 / 0oC O 稀溶液 O Br
• Friedel-Crafts反应
Ac2O O BF3 O Ph C
S Br
O
C O
CH3
Br2 S HOAc
Cl Ph S C O
CH2
NaNH 2
CH2CH3 CH2CH3
CH3I
CH2CH3 (80 %) N
CH2 H+ +
N
CH CHC6H5
烷基化
CH3
N
ZnCl 2
N
N H
N H
5、吡啶N-氧化物的反应
N
浓 H2SO4 浓 HNO 3 300 ℃ , 4h
RCH=O +
NO2 N
N
13.5 重要的稠杂环化合物 一、喹啉
a 位给电子基
HNO3 S NO2 O2N
+ S 85% NO2
O2N
S 15%
NO2
a位吸电子基
例外:
O NO2
HNO3 O2N O NO2
呋喃的特殊性
a位吸电子基
主要产物
Br HNO3 / Ac2O S
b位给电子基
Br
S
NO2
主要产物
COOH
Br2 CH3COOH Br S
COOH
S
b位吸电子基
原子序数小
S
2价
N
3价 原子序数大
1,2-唑
4 5 3 N2 O 1 5 4 3 N2 S 1
4 5 N H1
3 N2
异噁唑(isoxazole) 异噻唑(isothiazole)
吡唑(pyrazole)
1,3-唑
4 5 N3 O1 2 5 4 N S1 3 2
4 5
3 N N1 H 2
噁唑(oxazole)
1、结构
6 7 5 4 3 2
8 N 1 喹啉
2、化学性质 (1)弱碱性 (2)亲电取代反应
喹啉及异喹啉的亲电取代反应比吡啶容易进行,亲电试 剂主要进攻分子中苯环部分,因为苯环上电子密度高于 吡啶环;而亲核取代反应则发生在吡啶环上,其中喹啉 主要在 2 位取代,而异喹啉主要在 1 位。
(3) 亲核取代:主要发生在吡啶环(2或4位)
第十三章 杂环化合物
13.1 分类与命名 13.2 结构与芳香性 13.3 重要的五元杂环化合物
13.4 重要的六元杂环化合物
13.5 重要的稠杂环化合物
13.1 分类与命名
一、分类
1、结构特点 具有环状结构,成环的原子除了碳原子之外还含有其 它原子(N、O、S)的化合物称为杂环化合物。 2、芳香性 芳香性杂环:(吡咯、吡啶、喹啉等) •杂环: 非芳香性杂环:(四氢呋喃、四氢吡咯、 六氢吡啶等)
提示:五元杂环较活泼,遇酸不稳定
HNO3/H2SO4(硝化) 或 H2SO4 (磺化) 强酸
氧化
聚合
分解
A
A = NH,O,S
反应剧烈
解决办法:用温和试剂替代
A、五元杂环的硝化反应
硝化试剂
Ac2O + HNO3 AcONO2 硝基乙酰酯 AcO
+
NO2
亲电取代反应
NO2 AcONO2 N H Ac2O,-10 C
苯并吡咯 吲哚 (indole)
4、 唑的命名
含有两个杂原子的五元杂环,若至少有一个杂原子是氮,则该
杂环化合物称为唑。
命名时的编号原则是: 1) 让杂原子的位号尽可能小; 2)当两个杂原子不相同时,编号的次序是:价数小的在前, 大的在后; 3)价数相等时,原子序数小的在前,大的在后。 O O、S、N的 次序如左:
2、吡啶的亲核取代反应
(1) 置换氢的亲核取代反应
一般机制:
γ Nu (亲核取代)
-
H N Nu
Z (负氢接受体)
+ ZHN Nu
N
α
特点: ① 负氢不易离去,一般需要一个氧化剂作为负氢的接受体; ②亲核取代优先在α位上发生,如果α位上有取代基,则 反应在γ位上发生。
(2)烷基化、芳基化反应
+ N Li
o
+ NO2 N H 51% N H 13% NO2
AcONO2 S Ac2O-AcOH, 0 C
o
+ S 60% NO2 S 10%
AcONO2 O -5 ~ -30oC AcO O NO2
碱 或 - HOAc O NO2
B、五元杂环的磺化反应
磺化试剂:
CH2Cl2
N SO3
N
+
SO3
吡啶-SO3加合物
NH-Na+
H2O
N
NH 2
3、吡啶的氧化还原反应
吡啶环本身不易被氧化,但它的侧链很容易被氧化成醛或羧酸。
CH3 N COOH
O2, DMF t-BuOK, 室 温
SeO2
N
N
CH3
KMnO 4
N
CHO
COOH
COOH N N CH3
HNO 3
N
30% H 2O2 - HOAc
N
N
COOH
N O
(吡啶氧化物)
二、命名 1、命名:音译法(带“口”旁的同音汉字) 2、编号:
3,4,5…编号。(α,β,γ…则从杂原子相邻的碳原
子依次编号);
(杂环上有取代基时),从杂原子算起依次用1,2,
如果杂环上不止一个杂原子时,则从O、S、N顺序
编号。编号时杂原子的位次数字之和应最小。
3、五元杂环的命名
五元杂环
4 5
(4)氧化反应与还原反应
喹啉发生氧化反应时,由于吡啶环上电子云密度较低, 苯环容易破裂;加氢还原时,则吡啶环容易被加氢还 原:
3、合成方法
喹啉的合成方法有多种,常用的是斯克劳普法。是用苯 胺与甘油、浓硫酸及一种氧化剂如硝基苯共热而生成。
NH2 + CH2-CH-CH 2 OH OH OH H2SO4 硝基苯 N 84~91%
.. N H
.. S ..
H
C
H
呋喃
吡咯
噻吩
•杂原子(O、S、N)杂化态均为sp2杂化 二、吡咯、呋喃和噻吩的化学性质
1、亲电取代反应
(1)取代位置
E E A A E + A
a-取代 主要产物
b-取代
(2)亲电取代反应相对活性
>
N H O
>
S
>
5×109 1
3×1018
6×1011
(3) 亲电取代反应的举例
(quinoline)
O
(isoquinoline)
(benzopyran)
6 1N 2 7 5 N 8 N 4 N 9 H 3
O
(benzo--pyrone)
苯并--吡喃酮
嘌呤(purine)
13.3 重要的五元杂环化合物
一、吡咯、呋喃和噻吩的结构
H H C C C A
β’ 4 3β α’ 5 .. 2 α O .. 1
A
E
E
A
E
不稳定
A
E
进入2位
4 5
