2020-2021备战高考化学铁及其化合物推断题综合题附答案解析
2020-2021高考化学铁及其化合物推断题综合经典题含答案解析

2020-2021高考化学铁及其化合物推断题综合经典题含答案解析一、铁及其化合物1.A-J分别表示中学化学中常见的一种物质,它们之间相互关系如图所示(部分反应物、生成物没有列出),且已知G为主族元素的固态氧化物,A、B、C、D、E、F六种物质中均含同一种元素。
请填写下列空白:(1)A、B、C、D、E、F六种物质中所含同一种元素在周期表中位置_________(2)写出检验D溶液中阳离子的方法____。
(3)写出反应④的离子方程式________。
(4)若向气体K的水溶液中加入盐酸,使其恰好完全反应,所得溶液的pH_____7(填“>”、“<”或“=”),用离子方程式表示其原因:______;(5)若向气体K的0.1mol/L水溶液中加入pH=1的硫酸,且氨水与硫酸的体积比为1:1,则所得溶液中各离子物质的量浓度由大到小....的关系是______。
【答案】第四周期Ⅷ族取少量D溶液,加KSCN溶液,出现红色 2Al+2OH-+2H2O=2AlO2-+3H2↑< NH4++ H2OƒNH3·H2O+OH- c(NH4+)> c(SO42-)> c(H+)>c(OH-)【解析】【分析】G为主族元素的固态氧化物,在电解条件下生成I和H,能与NaOH溶液反应,说明G为Al2O3,与NaOH反应生成NaAlO2,而I也能与NaOH反应生成NaAlO2,则I为Al,H为O2,C和碱、D和气体K反应生成E、F,则说明E、F都为氢氧化物,E能转化为F,应为Fe(OH)2→Fe(OH)3的转化,所以E为Fe(OH)2,F为Fe(OH)3,则C为FeCl2,D为FeCl3,K 为NH3,B为Fe3O4,与Al在高温条件下发生铝热反应生成A,即Fe,结合对应单质、化合物的性质解答该题。
【详解】(1)A、B、C、D、E、F六种物质中都含有铁元素,在周期表中位于周期表第四周期Ⅷ族,(2)溶液D为氯化铁溶液,检验三价铁离子的存在,取少许D溶液于试管中,滴加KSCN 溶液,溶液变红色,证明D溶液中含有Fe3+;(3)反应④是金属铝和氢氧化钠溶液的反应,Al与NaOH溶液反应生成NaAlO2和H2,反应的离子方程式为:--2222Al+2OH +2H O=2AlO +3H ;(4)气体K 的水溶液为一水合氨溶液,加入盐酸,使其恰好完全反应生成氯化铵和水,氯化铵在水溶液中水解显酸性,所以pH <7;反应的离子方程式为:++4232NH +H O NH H O+H g ƒ;(5)若向气体NH 3的0.1mol/L 水溶液中加入pH=1的硫酸,且氨水与硫酸的体积比为1:1,假设条件均为1L ,发生反应:++3242NH H O+H =NH +H O g ,n (NH 3•H 2O)=0.1mol ,n (H +)=0.1mol ,所以一水合氨和硫酸反应生成硫酸铵溶液,铵根离子水解显酸性,溶液中离子浓度大小顺序为:c (+4NH )>c (2-4SO )>c (H +)>c (OH -)。
2020-2021高考化学 铁及其化合物推断题 综合题及详细答案

2020-2021高考化学铁及其化合物推断题综合题及详细答案一、铁及其化合物1.X、Y、Z、W 为四种常见元素,其中 X、Y、Z 为短周期元素。
ZX4分子是由粗Z提纯Z的中间产物,X的最高价氧化物对应的水化物为无机酸中的最强酸,Y的离子在同周期中离子半径最小,其氧化物有两性且可用于制造一种极有前途的高温材料,Z是无机非金属材料的主角,其单质是制取大规模集成电路的主要原料,W原子的最外层电子数小于4且W 的常见化合价有+3、+2,WX3的稀溶液呈黄色,回答下列问题:(1)X在元素周期表的位置________________,其简单阴离子的结构示意图为____________________,用电子式表示X的氢化物的形成过程______________________________。
(2)Z的氧化物在通讯领域用来作_______________。
锗与Z是同一主族元素,它可用来制造半导体晶体管。
研究表明:有机锗具有明显的抗肿瘤活性,锗不与 NaOH溶液反应但在有H2O2存在时可与NaOH溶液反应生成锗酸盐,反应的化学方程式为:_______________________________(3)W(OH)2在空气中不稳定,极易被氧化,由白色迅速变成灰绿色,最后变成红褐色,反应的化学方程式为:____________________________________,若灼烧W(OH)2固体得到___________。
【答案】第三周期ⅦA族光导纤维 Ge + 2H2O2 +2NaOH = Na2GeO3 + 3H2O 4Fe(OH)2 + O2 + 2H2O = 4Fe(OH)3 Fe2O3【解析】【分析】根据元素的性质及用途等信息分析元素的种类;根据核外电子排布情况确定在元素周期表中的位置;根据物质的性质及反应的现象书写反应方程式,及用相关化学用语表示物质的组成和结构。
【详解】Z是无机非金属材料的主角,其单质是制取大规模集成电路的主要原料,则Z为硅;ZX4分子是由粗Z提纯Z的中间产物,X的最高价氧化物对应的水化物为无机酸中的最强酸,则X 为氯;Y的离子在同周期中离子半径最小,其氧化物有两性且可用于制造一种极有前途的高温材料,则Y为铝;W原子的最外层电子数小于4且W的常见化合价有+3、+2,WX3的稀溶液呈黄色,则W为铁;(1)X为氯元素,在元素周期表的位置为:第三周期ⅦA族;氯离子的结构示意图为:;用电子式表示HCl的形成过程:;(2)Z为硅,二氧化硅在通讯领域用作光导纤维;根据题干信息知锗NaOH溶液在有H2O2存在时反应生成锗酸盐,反应的化学方程式为:Ge + 2H2O2 + 2NaOH = Na2GeO3 + 3H2O;(3)反应现象知该反应为氢氧化亚铁被氧化为氢氧化铁,反应的化学方程式为:4Fe(OH)2 + O2 + 2H2O = 4Fe(OH)3,Fe(OH)3不稳定,灼烧分解得到固体Fe2O3。
2020-2021高考化学铁及其化合物推断题综合题及详细答案

2020-2021高考化学铁及其化合物推断题综合题及详细答案一、铁及其化合物1.A~I分别表示中学化学中常见的一种物质,它们之间相互关系如图所示(部分反应物、生成物没有列出)。
已知H为固态氧化物,F是红褐色难溶于水的沉淀,且A、B、C、D、E、F六种物质中均含同一种元素。
请填写下列空白:(1)A、B、C、D、E、F六种物质中所含的同一种元素的名称是___。
(2)反应①的化学方程式为___。
(3)反应③的离子方程式为___。
(4)反应⑧的化学方程式为___。
(5)反应⑥过程中的现象是____。
(6)1molI发生反应后生成的A高温下与足量的水蒸气反应,生成的气体换算成标准状况下占___L。
【答案】铁元素 8Al+3Fe3O44Al2O3+9Fe Fe3O4+8H+=2Fe3++Fe2++4H2O Al2O3+2NaOH=2NaAlO2+H2O 生成的白色沉淀在空气中迅速变成灰绿色,最后变成红褐色 33.6 【解析】【分析】F是红褐色难溶于水的沉淀,则F为氢氧化铁;E能在空气中转化为F,且E是C和氢氧化钠反应生成,则E为氢氧化亚铁,C为氯化亚铁;B能与盐酸反应生成氯化亚铁和D,则B 为四氧化三铁,D为氯化铁;A在空气中燃烧能够生成四氧化三铁,则A为铁单质;四氧化三铁与I在高温条件下反应生成铁单质,I又能与氢氧化钠反应,推知I为铝单质,与四氧化三铁在高温条件下发生铝热反应,生成H为氧化铝;铝和氧化铝都能与氢氧化钠反应生成G,则G为偏铝酸钠。
【详解】(1)A为铁、B为四氧化三铁、C为氯化亚铁、D为氯化铁、E氢氧化亚铁、F为氢氧化铁,则六种物质中都含有铁元素,故答案为:铁元素;(2)①是铝与四氧化三铁发生铝热反应,其反应的方程式为8Al+3Fe3O44Al2O3+9Fe,故答案为:8Al+3Fe3O44Al2O3+9Fe;(3)③是四氧化三铁与盐酸反应,其反应的离子方程式为Fe3O4+8H+=2Fe3++Fe2++4H2O,故答案为:Fe3O4+8H+=2Fe3++Fe2++4H2O;(4)⑧是氧化铝与氢氧化钠发生反应,反应的化学方程式为Al2O3+2NaOH=2NaAlO2+H2O,故答案为:Al2O3+2NaOH=2NaAlO2+H2O;(5)⑥氢氧化亚铁在空气中转化为氢氧化铁,其现象为生成的白色沉淀在空气中迅速变成灰绿色,最后变成红褐色,故答案为:生成的白色沉淀在空气中迅速变成灰绿色,最后变成红褐色;(6)1mol铝与四氧化三铁反应生成铁单质与氧化铝,生成的铁单质再与水蒸气反应生成氢气,根据得失电子守恒可知,铝失去的电子数等于生成氢气得到的电子数,可列式1×3=2×n(H2),则n(H2)=1.5mol,则标准状况下,氢气的体积V(H2)=1.5mol×22.4L/mol=33.6L,故答案为33.6。
2020-2021高考化学铁及其化合物推断题的综合题试题及详细答案

2020-2021高考化学铁及其化合物推断题的综合题试题及详细答案一、铁及其化合物1.利用废旧镀锌铁皮可制备磁性Fe3O4胶体粒子并得到副产物ZnO。
制备流程如图所示:(已知ZnO能溶于强碱)已知:Zn及其化合物的性质与Al及其化合物的性质相似。
请回答下列问题:(1)用NaOH溶液处理废旧镀锌铁皮的目的是________(填字母)。
A 去除油污B 溶解镀锌层C 去除铁锈D 钝化铁皮(2)调节溶液A的pH可产生Zn(OH)2沉淀,为制得ZnO,后续操作步骤是抽滤______。
(3)加适量H2O2 目的是________ 溶液B制得Fe3O4胶体粒子的过程中,须持续通入N2,其原因是_____。
(4)副产物ZnO常用于制备锌单质。
我国早有炼锌技术的记载,明代宋应星著的《天工开物》中有“升炼倭铅”的记载:“每炉甘石十斤,装载入一泥罐内……然后逐层用煤炭饼垫盛,其底铺薪,发火煅红冷定毁罐取出…即倭铅也。
”该炼锌工艺过程涉及主要反应的化学方程式为_________,(注:炉甘石的主要成分为碳酸锌,“倭铅”是指金属锌)。
(5)用重铬酸钾法(一种氧化还原滴定法)可测定产物Fe3O4中的二价铁含量。
若需配制浓度为0.01 mol·L-1的K2Cr2O7标准溶液250 mL,应准确称取________g K2Cr2O7[保留4位有效数字,已知M r(K2Cr2O7)=294]。
配制该标准溶液时,下列仪器中用不到的有________(填编号)。
①电子天平②烧杯③量筒④玻璃棒⑤250 mL容量瓶⑥胶头滴管⑦移液管(6)滴定操作中,如果滴定前装有K2Cr2O7标准溶液的滴定管尖嘴部分有气泡,而滴定结束后气泡消失,则测定结果将________(填“偏大”“偏小”或“不变”)。
【答案】AB 洗涤、灼烧将部分亚铁离子氧化成铁离子防止Fe2+被氧化 ZnCO3+2C 高温Zn+3CO↑ 0.7350 ③⑦偏大【解析】【分析】【详解】(1)A.氢氧化钠溶液与油污反应生成高级脂肪酸盐,具有去除油污作用,A符合题意;B.根据Zn及化合物的性质与Al及化合物的性质相似,Zn也能和氢氧化钠溶液反应,氢氧化钠溶液起到溶解镀锌层,B符合题意;C.氢氧化钠和铁不反应,C不符合题意;D.氢氧化钠不能钝化铁皮,故D不符合题意;答案为:AB;(2)调节溶液A的pH可产生Zn(OH)2沉淀,抽滤就可以得到氢氧化锌沉淀,洗涤除去附着的离子,高温灼烧氢氧化锌分解得到ZnO;(3)Fe3O4中有+3价铁,因此加适量H2O2目的是将部分亚铁离子氧化成铁离子,将亚铁离子和铁离子达到Fe3O4中+2价铁与+3价铁的比例关系,持续通入N2,主要防止Fe2+被氧化;故答案为:将部分亚铁离子氧化成铁离子;防止Fe2+被氧化;(4)该炼锌工艺参加反应的物质是煤炭饼和炉甘石(碳酸锌),得到的物质是倭铅(金属锌)和CO,联想初中所学高炉炼铁原理,则炼锌过程涉及主要反应的化学方程式为ZnCO3+2C 高温Zn+3CO↑;(5)m(K2Cr2O7)=0.01 mol·L-1×0.250 L×294 g·mol-1=0.7350 g,电子天平用于准确称量固体质量,烧杯用于溶解固体,玻璃棒用于搅拌和引流,容量瓶用于配制溶液,胶头滴管用于加水定容。
2020-2021高考化学 铁及其化合物推断题 综合题及答案

2020-2021高考化学铁及其化合物推断题综合题及答案一、铁及其化合物1.纳米Fe3O4在生物医学和催化剂载体等领域应用前景光明。
其制备流程如下:已知:锌单质溶于强碱生成ZnO22-;Zn(OH)2既能溶于强酸又能溶于强碱。
请回答下列问题:(l)用NaOH溶液处理废旧锌铁皮的作用有___。
A.去除油污B.溶解镀锌层C.去除铁锈D.钝化(2)步骤②生成Zn(OH)2沉淀的离子方程式为____,用离子方程式结合文字说明该步骤pH 不能过小的原因____。
调节pH的最佳方法是向溶液中通入____(填化学式)。
(3)步骤④反应的离子方程式为_____;为确保纳米Fe3O4粒子的纯度,应调整原溶液中Fe2+与所加H2O2的物质的量之比为_______。
(4)步骤⑤制得Fe3O4纳米粒子的过程,需要在无氧环境下进行,说明理由__________;T 业生产中可采取___________措施提供无氧环境。
(5)步骤⑤ _______(填“能”或“不能”)用减压过滤(抽滤)得到纳米Fe3O4粒子?理由是___________。
【答案】AB ZnO22-+2H+=Zn(OH)2↓加入酸是为了使ZnO22-转化为Zn(OH)2沉淀,但加入酸不能过多,要防止发生Zn(OH)2+2H+=Zn2++2H2O,降低ZnO产量 CO22Fe2++H2O2+2H+=2Fe3++2H2O 3:1 防止Fe2+[或Fe(OH)2]被氧化持续通入N₂不能纳米粒子太小,抽滤时容易透过滤纸【解析】【分析】根据流程图及已知信息分析得:废旧镀锌铁皮加入氢氧化钠溶液中反应,锌溶解生成偏锌酸钠和氢气,铁不溶解,过滤得到滤液A为Na2ZnO2,不溶物为Fe,溶液A加稀硫酸使溶液中ZnO22-转化为Zn(OH)2沉淀,再经过过滤、洗涤、干燥,灼烧得到ZnO,不溶物Fe 中加入稀盐酸,反应生成氯化亚铁,加入适量H2O2,氧化部分亚铁离子为铁离子,得到含Fe2+、Fe3+的B溶液,再加入NaOH,并通入氮气排除氧气,加热分解,生成四氧化三铁胶体粒子,据此分析解答。
2020-2021高考化学 铁及其化合物推断题 综合题含答案解析

2020-2021高考化学 铁及其化合物推断题 综合题含答案解析一、铁及其化合物1.某淡黄色固体A (仅含三种元素,式量小于160)可用于制药,为探究其组成和性质,设计并完成如下实验:已知:①上述流程中所涉及的反应都充分进行。
②B 、C 、D 均为常见气体。
相同情况下气体B 的密度大气体C 。
③黑色固体E 溶于盐酸后滴加KSCN ,无明显现象,加适量氯水后,溶液变红。
请问答:(1)写出气体B 的电子式__,固体A 的化学式是__。
(2)黑色固体E 与足量浓硝酸反应的离子反应方程式是__。
【答案】FeC 2O 4 3FeO + 10H + + NO 3- = NO + 3Fe 3+ + 5H 2O 【解析】【分析】B 、C 、D 均为常见气体说明D 单质为氧气,物质的量为1m 3.2g n=0.1mol M 32g mol-==⋅,相同情况下气体B 的密度大气体C 则说明B 为二氧化碳,B 与过氧化钠反应,则C 为一氧化碳,气体物质的量为1m V 8.96L n==0.4mol V 22.4L mol -=⋅由于生成0.1mol 氧气,根据2CO 2 + 2Na 2O 2 = 2Na 2CO 3 + O 2,因此二氧化碳的物质的量为0.2mol ,CO 物质的量为0.2mol ,黑色固体E 溶于盐酸后滴加KSCN ,无明显现象,说明无铁离子,加适量氯水后,溶液变红,说明原物质为FeO ,则m(FeO) = 28.8g−0.2mol×28 g∙mol −1− 0.2mol×44 g∙mol −1 = 14.4g ,则FeO 物质的量1m 14.4g n=0.2mol M 71g mol-==⋅,因此n(Fe): n(C): n(O) = 0.2mol:(0.2mol+0.2mol):(0.2mol+0.2mol+0.2mol×2) =1:2:4,则化学式为FeC 2O 4。
2020-2021备战高考化学铁及其化合物推断题综合经典题附答案解析

2020-2021备战高考化学铁及其化合物推断题综合经典题附答案解析一、铁及其化合物1.利用废旧镀锌铁皮可制备磁性Fe3O4胶体粒子并得到副产物ZnO。
制备流程如图所示:(已知ZnO能溶于强碱)已知:Zn及其化合物的性质与Al及其化合物的性质相似。
请回答下列问题:(1)用NaOH溶液处理废旧镀锌铁皮的目的是________(填字母)。
A 去除油污B 溶解镀锌层C 去除铁锈D 钝化铁皮(2)调节溶液A的pH可产生Zn(OH)2沉淀,为制得ZnO,后续操作步骤是抽滤______。
(3)加适量H2O2 目的是________ 溶液B制得Fe3O4胶体粒子的过程中,须持续通入N2,其原因是_____。
(4)副产物ZnO常用于制备锌单质。
我国早有炼锌技术的记载,明代宋应星著的《天工开物》中有“升炼倭铅”的记载:“每炉甘石十斤,装载入一泥罐内……然后逐层用煤炭饼垫盛,其底铺薪,发火煅红冷定毁罐取出…即倭铅也。
”该炼锌工艺过程涉及主要反应的化学方程式为_________,(注:炉甘石的主要成分为碳酸锌,“倭铅”是指金属锌)。
(5)用重铬酸钾法(一种氧化还原滴定法)可测定产物Fe3O4中的二价铁含量。
若需配制浓度为0.01 mol·L-1的K2Cr2O7标准溶液250 mL,应准确称取________g K2Cr2O7[保留4位有效数字,已知M r(K2Cr2O7)=294]。
配制该标准溶液时,下列仪器中用不到的有________(填编号)。
①电子天平②烧杯③量筒④玻璃棒⑤250 mL容量瓶⑥胶头滴管⑦移液管(6)滴定操作中,如果滴定前装有K2Cr2O7标准溶液的滴定管尖嘴部分有气泡,而滴定结束后气泡消失,则测定结果将________(填“偏大”“偏小”或“不变”)。
【答案】AB 洗涤、灼烧将部分亚铁离子氧化成铁离子防止Fe2+被氧化 ZnCO3+2C 高温Zn+3CO↑ 0.7350 ③⑦偏大【解析】【分析】【详解】(1)A.氢氧化钠溶液与油污反应生成高级脂肪酸盐,具有去除油污作用,A符合题意;B.根据Zn及化合物的性质与Al及化合物的性质相似,Zn也能和氢氧化钠溶液反应,氢氧化钠溶液起到溶解镀锌层,B符合题意;C.氢氧化钠和铁不反应,C不符合题意;D.氢氧化钠不能钝化铁皮,故D不符合题意;答案为:AB;(2)调节溶液A的pH可产生Zn(OH)2沉淀,抽滤就可以得到氢氧化锌沉淀,洗涤除去附着的离子,高温灼烧氢氧化锌分解得到ZnO;(3)Fe3O4中有+3价铁,因此加适量H2O2目的是将部分亚铁离子氧化成铁离子,将亚铁离子和铁离子达到Fe3O4中+2价铁与+3价铁的比例关系,持续通入N2,主要防止Fe2+被氧化;故答案为:将部分亚铁离子氧化成铁离子;防止Fe2+被氧化;(4)该炼锌工艺参加反应的物质是煤炭饼和炉甘石(碳酸锌),得到的物质是倭铅(金属锌)和CO,联想初中所学高炉炼铁原理,则炼锌过程涉及主要反应的化学方程式为ZnCO3+2C 高温Zn+3CO↑;(5)m(K2Cr2O7)=0.01 mol·L-1×0.250 L×294 g·mol-1=0.7350 g,电子天平用于准确称量固体质量,烧杯用于溶解固体,玻璃棒用于搅拌和引流,容量瓶用于配制溶液,胶头滴管用于加水定容。
2020-2021高考化学铁及其化合物推断题的综合题试题及答案解析

2020-2021高考化学铁及其化合物推断题的综合题试题及答案解析一、铁及其化合物1.X、Y、Z、W 为四种常见元素,其中 X、Y、Z 为短周期元素。
ZX4分子是由粗Z提纯Z的中间产物,X的最高价氧化物对应的水化物为无机酸中的最强酸,Y的离子在同周期中离子半径最小,其氧化物有两性且可用于制造一种极有前途的高温材料,Z是无机非金属材料的主角,其单质是制取大规模集成电路的主要原料,W原子的最外层电子数小于4且W 的常见化合价有+3、+2,WX3的稀溶液呈黄色,回答下列问题:(1)X在元素周期表的位置________________,其简单阴离子的结构示意图为____________________,用电子式表示X的氢化物的形成过程______________________________。
(2)Z的氧化物在通讯领域用来作_______________。
锗与Z是同一主族元素,它可用来制造半导体晶体管。
研究表明:有机锗具有明显的抗肿瘤活性,锗不与 NaOH溶液反应但在有H2O2存在时可与NaOH溶液反应生成锗酸盐,反应的化学方程式为:_______________________________(3)W(OH)2在空气中不稳定,极易被氧化,由白色迅速变成灰绿色,最后变成红褐色,反应的化学方程式为:____________________________________,若灼烧W(OH)2固体得到___________。
【答案】第三周期ⅦA族光导纤维 Ge + 2H2O2 +2NaOH = Na2GeO3 + 3H2O 4Fe(OH)2 + O2 + 2H2O = 4Fe(OH)3 Fe2O3【解析】【分析】根据元素的性质及用途等信息分析元素的种类;根据核外电子排布情况确定在元素周期表中的位置;根据物质的性质及反应的现象书写反应方程式,及用相关化学用语表示物质的组成和结构。
【详解】Z是无机非金属材料的主角,其单质是制取大规模集成电路的主要原料,则Z为硅;ZX4分子是由粗Z提纯Z的中间产物,X的最高价氧化物对应的水化物为无机酸中的最强酸,则X 为氯;Y的离子在同周期中离子半径最小,其氧化物有两性且可用于制造一种极有前途的高温材料,则Y为铝;W原子的最外层电子数小于4且W的常见化合价有+3、+2,WX3的稀溶液呈黄色,则W为铁;(1)X为氯元素,在元素周期表的位置为:第三周期ⅦA族;氯离子的结构示意图为:;用电子式表示HCl的形成过程:;(2)Z为硅,二氧化硅在通讯领域用作光导纤维;根据题干信息知锗NaOH溶液在有H2O2存在时反应生成锗酸盐,反应的化学方程式为:Ge + 2H2O2 + 2NaOH = Na2GeO3 + 3H2O;(3)反应现象知该反应为氢氧化亚铁被氧化为氢氧化铁,反应的化学方程式为:4Fe(OH)2 + O2 + 2H2O = 4Fe(OH)3,Fe(OH)3不稳定,灼烧分解得到固体Fe2O3。
2020-2021高考化学综合题专练∶铁及其化合物推断题及答案解析

2020-2021高考化学综合题专练∶铁及其化合物推断题及答案解析一、铁及其化合物1.下列各物质是中学化学中常见的物质,甲为常见金属单质,丙为黄绿色的单质气体,乙、丁是常见无色气态非金属单质,其它均为化合物,C 常温下为一种液体,B 、D 分别为黑色粉末和黑色晶体,G 为淡黄色固体,J 为生活中常见的调味品,I 为红褐色固体,F 为棕黄色溶液。
①是实验室制取丁的反应之一。
各物质间的转化如下图所示,回答下列问题(部分生成物未列出):(1)物质I 的化学式为________;F 中阴离子是______________;(2)反应①的化学方程式为为____________;(3)B 与K 的反应是实验室制取丙的反应,其离子方程式为____________;(4)反应②的化学方程式为_____________;(5)若E 与G 以物质的量比为1:1投入足量水中,反应的化学方程式为_________;生成1mol 气体转移电子的个数为__________。
【答案】Fe(OH)3 Cl - 2H 2O 22MnO 2H 2O+O 2 MnO 2+4H ++2Cl -ΔMn 2++Cl 2↑+2H 2O 3Fe + 4H 2O(g)高温Fe 3O 4 +4H 2 4FeCl 2+4Na 2O 2 + 6H 2O = 4Fe(OH)3↓+8NaCl + O 2↑ 6N A【解析】【分析】丙为黄绿色单质气体,所以丙为Cl 2,B 与K 的反应是实验室制取丙的反应,且B 为黑色粉末,则B 为MnO 2,K 为HCl ;①是实验室制取丁的反应之一,则该反应为双氧水在二氧化锰的催化作用下制取氧气的反应,所以C 为H 2O ,丁为氧气;G 为淡黄色固体,且可以生成氧气,则G 应为Na 2O 2,则J 为生活中常见的调味品,应为NaCl ,I 为红褐色固体应为Fe(OH)3;F 为棕黄色溶液,应含Fe 3+,E 与氯气反应可生成F ,则F 为FeCl 3,E 为FeCl 2;氯化铁可以与单质铁反应生成氯化亚铁,所以甲为铁单质,Fe 可以在高温条件下与水反应生成氢气和四氧化三铁,所以乙为氢气,D 为Fe 3O 4。
2020-2021高考化学综合题专练∶铁及其化合物推断题含答案解析

2020-2021高考化学综合题专练∶铁及其化合物推断题含答案解析一、铁及其化合物1.钛(Ti )被称为继铁、铝之后的第三金属,钛白(2TiO )是目前使用最广泛的白色颜料。
制备2TiO 和Ti 的原料是钛铁矿,用含23Fe O 的钛铁矿(主要成分为3FeTiO )制备2TiO 的流程如下:(1)步骤①加Fe 的目的是________________________;步骤②冷却的目的是__________________。
(2)考虑成本和废物的综合利用等因素,水浸后的废液中应加入_______处理。
(3)由金红石(2TiO )制取单质钛(Ti )的过程为,其中反应42800C TiCl 2Mg2MgCl Ti ︒++在氩气气氛中进行的理由是______________________________。
【答案】将3+Fe 还原为2+Fe 析出绿矾(42FeSO 7H O ⋅) 生石灰(或碳酸钙、碱) 高温下镁或钛与2O 、2N 等反应【解析】【分析】根据钛铁矿中23Fe O 、3FeTiO 与浓硫酸反应的溶液中加入铁粉、过滤后,滤液冷却得到硫酸亚铁晶体推知,铁粉与铁离子发生反应得到亚铁离子。
水浸后的溶液成酸性。
【详解】(1)分析题图可知,钛铁矿中的铁最终转化成副产品绿矾,所以要将+3价Fe 转化为+2价Fe ;降低温度,减小了42FeSO 7H O ⋅的溶解度,有利于绿矶结晶析出。
(2)水浸过程发生的离子反应为2223TiO 2H O H TiO 2H +++=↓+,废液呈酸性,所以处理水浸后的废液应加入CaO 、3CaCO 或碱。
(3)由于Ti 和Mg 易与空气中的2O 、2N 等反应,故该反应应在氩气气氛中进行。
2.常见物质A~K 之间存在如图所示的转化关系,其中A 、D 、E 、H 为单质,请回答下列问题。
(1)下列物质的化学式是:C______,H______。
(2)反应“I→J”的离子方程式是____。
2020-2021高考化学铁及其化合物推断题综合题附答案解析

2020-2021高考化学铁及其化合物推断题综合题附答案解析一、铁及其化合物1.X、Y、Z、W 为四种常见元素,其中 X、Y、Z 为短周期元素。
ZX4分子是由粗Z提纯Z的中间产物,X的最高价氧化物对应的水化物为无机酸中的最强酸,Y的离子在同周期中离子半径最小,其氧化物有两性且可用于制造一种极有前途的高温材料,Z是无机非金属材料的主角,其单质是制取大规模集成电路的主要原料,W原子的最外层电子数小于4且W 的常见化合价有+3、+2,WX3的稀溶液呈黄色,回答下列问题:(1)X在元素周期表的位置________________,其简单阴离子的结构示意图为____________________,用电子式表示X的氢化物的形成过程______________________________。
(2)Z的氧化物在通讯领域用来作_______________。
锗与Z是同一主族元素,它可用来制造半导体晶体管。
研究表明:有机锗具有明显的抗肿瘤活性,锗不与 NaOH溶液反应但在有H2O2存在时可与NaOH溶液反应生成锗酸盐,反应的化学方程式为:_______________________________(3)W(OH)2在空气中不稳定,极易被氧化,由白色迅速变成灰绿色,最后变成红褐色,反应的化学方程式为:____________________________________,若灼烧W(OH)2固体得到___________。
【答案】第三周期ⅦA族光导纤维 Ge + 2H2O2 +2NaOH = Na2GeO3 + 3H2O 4Fe(OH)2 + O2 + 2H2O = 4Fe(OH)3 Fe2O3【解析】【分析】根据元素的性质及用途等信息分析元素的种类;根据核外电子排布情况确定在元素周期表中的位置;根据物质的性质及反应的现象书写反应方程式,及用相关化学用语表示物质的组成和结构。
【详解】Z是无机非金属材料的主角,其单质是制取大规模集成电路的主要原料,则Z为硅;ZX4分子是由粗Z提纯Z的中间产物,X的最高价氧化物对应的水化物为无机酸中的最强酸,则X 为氯;Y的离子在同周期中离子半径最小,其氧化物有两性且可用于制造一种极有前途的高温材料,则Y为铝;W原子的最外层电子数小于4且W的常见化合价有+3、+2,WX3的稀溶液呈黄色,则W为铁;(1)X为氯元素,在元素周期表的位置为:第三周期ⅦA族;氯离子的结构示意图为:;用电子式表示HCl的形成过程:;(2)Z为硅,二氧化硅在通讯领域用作光导纤维;根据题干信息知锗NaOH溶液在有H2O2存在时反应生成锗酸盐,反应的化学方程式为:Ge + 2H2O2 + 2NaOH = Na2GeO3 + 3H2O;(3)反应现象知该反应为氢氧化亚铁被氧化为氢氧化铁,反应的化学方程式为:4Fe(OH)2 + O2 + 2H2O = 4Fe(OH)3,Fe(OH)3不稳定,灼烧分解得到固体Fe2O3。
2020-2021高考化学铁及其化合物推断题综合题含答案解析
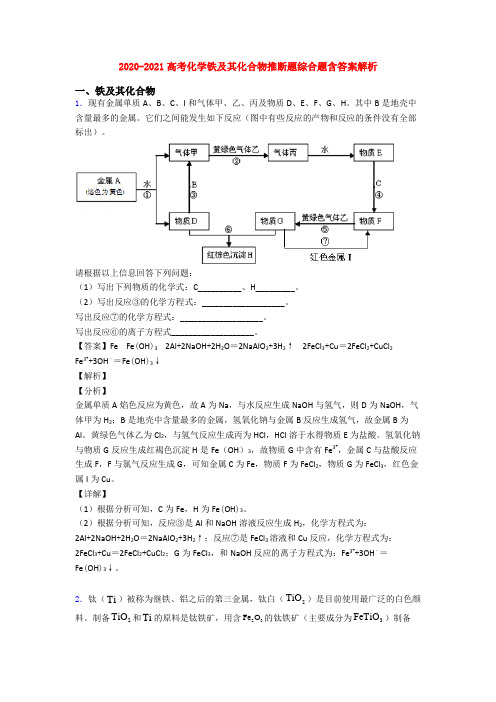
2020-2021高考化学铁及其化合物推断题综合题含答案解析一、铁及其化合物1.现有金属单质A 、B 、C 、I 和气体甲、乙、丙及物质D 、E 、F 、G 、H 。
其中B 是地壳中含量最多的金属。
它们之间能发生如下反应(图中有些反应的产物和反应的条件没有全部标出)。
请根据以上信息回答下列问题:(1)写出下列物质的化学式:C__________、H_________。
(2)写出反应③的化学方程式:___________________。
写出反应⑦的化学方程式:___________________。
写出反应⑥的离子方程式___________________。
【答案】Fe Fe (OH )3 2Al +2NaOH +2H 2O =2NaAlO 2+3H 2↑ 2FeCl 3+Cu =2FeCl 2+CuCl 2 Fe 3++3OH ﹣=Fe (OH )3↓【解析】【分析】金属单质A 焰色反应为黄色,故A 为Na ,与水反应生成NaOH 与氢气,则D 为NaOH ,气体甲为H 2;B 是地壳中含量最多的金属,氢氧化钠与金属B 反应生成氢气,故金属B 为Al 。
黄绿色气体乙为Cl 2,与氢气反应生成丙为HCl ,HCl 溶于水得物质E 为盐酸。
氢氧化钠与物质G 反应生成红褐色沉淀H 是Fe (OH )3,故物质G 中含有Fe 3+,金属C 与盐酸反应生成F ,F 与氯气反应生成G ,可知金属C 为Fe ,物质F 为FeCl 2,物质G 为FeCl 3,红色金属I 为Cu 。
【详解】(1)根据分析可知,C 为Fe ,H 为Fe (OH )3。
(2)根据分析可知,反应③是Al 和NaOH 溶液反应生成H 2,化学方程式为:2Al +2NaOH +2H 2O =2NaAlO 2+3H 2↑;反应⑦是FeCl 3溶液和Cu 反应,化学方程式为:2FeCl 3+Cu =2FeCl 2+CuCl 2;G 为FeCl 3,和NaOH 反应的离子方程式为:Fe 3++3OH ﹣=Fe (OH )3↓。
2020-2021高考化学铁及其化合物推断题综合经典题含详细答案

2020-2021高考化学铁及其化合物推断题综合经典题含详细答案一、铁及其化合物1.下列各物质是中学化学中常见的物质,甲为常见金属单质,丙为黄绿色的单质气体,乙、丁是常见无色气态非金属单质,其它均为化合物,C 常温下为一种液体,B 、D 分别为黑色粉末和黑色晶体,G 为淡黄色固体,J 为生活中常见的调味品,I 为红褐色固体,F 为棕黄色溶液。
①是实验室制取丁的反应之一。
各物质间的转化如下图所示,回答下列问题(部分生成物未列出):(1)物质I 的化学式为________;F 中阴离子是______________;(2)反应①的化学方程式为为____________;(3)B 与K 的反应是实验室制取丙的反应,其离子方程式为____________;(4)反应②的化学方程式为_____________;(5)若E 与G 以物质的量比为1:1投入足量水中,反应的化学方程式为_________;生成1mol 气体转移电子的个数为__________。
【答案】Fe(OH)3 Cl - 2H 2O 22MnO 2H 2O+O 2 MnO 2+4H ++2Cl -ΔMn 2++Cl 2↑+2H 2O 3Fe + 4H 2O(g)高温Fe 3O 4 +4H 2 4FeCl 2+4Na 2O 2 + 6H 2O = 4Fe(OH)3↓+8NaCl + O 2↑ 6N A【解析】【分析】丙为黄绿色单质气体,所以丙为Cl 2,B 与K 的反应是实验室制取丙的反应,且B 为黑色粉末,则B 为MnO 2,K 为HCl ;①是实验室制取丁的反应之一,则该反应为双氧水在二氧化锰的催化作用下制取氧气的反应,所以C 为H 2O ,丁为氧气;G 为淡黄色固体,且可以生成氧气,则G 应为Na 2O 2,则J 为生活中常见的调味品,应为NaCl ,I 为红褐色固体应为Fe(OH)3;F 为棕黄色溶液,应含Fe 3+,E 与氯气反应可生成F ,则F 为FeCl 3,E 为FeCl 2;氯化铁可以与单质铁反应生成氯化亚铁,所以甲为铁单质,Fe 可以在高温条件下与水反应生成氢气和四氧化三铁,所以乙为氢气,D 为Fe 3O 4。
2020-2021高考化学铁及其化合物推断题综合题含答案

2020-2021高考化学铁及其化合物推断题综合题含答案一、铁及其化合物1.将铁、铝的混合物进行如下实验:(1)操作X的名称是________。
(2)气体A是________(填化学式)。
(3)A与Cl2混合光照可能发生爆炸,A在该反应中作________(填“氧化剂”或“还原剂”)。
(4)溶液B中的阴离子除OH-外还有________(填离子符号,下同),溶液D中存在的金属离子为________。
(5)加入足量NaOH溶液时发生反应的离子方程式为___________;加入稀盐酸发生反应的离子方程式为_________。
(6)向溶液D中加入NaOH溶液,观察到产生的白色絮状沉淀迅速变为灰绿色,最终变为红褐色,请写出沉淀转化的化学方程式:___________。
【答案】过滤 H2还原剂 AlO2- Fe2+ 2Al+2OH-+2H2O=2AlO2-+3H2↑ Fe+2H+=Fe2++H2↑ 4Fe(OH)2+O2+2H2O=4Fe(OH)3【解析】【分析】金属混合物中Fe与NaOH溶液不反应,而Al可以与NaOH溶液反应产生NaAlO2、H2,NaAlO2易溶于水,所以气体A是H2,溶液B是NaAlO2与NaOH的混合溶液,固体C是Fe,Fe是比较活泼的金属,与HCl发生置换反应产生FeCl2和氢气,因此溶液D为FeCl2,据此分析解答。
【详解】(1)操作X的名称是分离难溶性的固体与可溶性液体混合物的方法,名称是过滤,故答案为:过滤;(2)根据上述分析可知,金属混合物中Fe与NaOH溶液不反应,而Al可以与NaOH溶液反应产生NaAlO2、H2,NaAlO2易溶于水,所以气体A是H2,故答案为:H2;(3)A是H2,H2和Cl2的混合气体光照会发生爆炸,反应生成HCl,在该反应中,氢元素的化合价升高,失去电子,被氧化,所以H2作还原剂,故答案为:还原剂;(4)溶液B是反应产生的NaAlO2与过量的NaOH的混合溶液,所以溶液B中阴离子除OH-外还有AlO2-,铁可以和盐酸反应生成FeCl2和H2,溶液D中含有的金属离子为Fe2+,故答案为:AlO2-;Fe2+;(5)加入足量NaOH溶液时,Al与NaOH溶液反应生成偏铝酸钠和氢气,反应的离子方程式为2Al+2OH-+2H2O=2AlO2-+3H2↑,加入稀盐酸,Fe与稀盐酸反应生成氢气和氯化亚铁,发生反应的离子方程式为Fe+2H+=Fe2++H2↑,故答案为2Al+2OH-+2H2O=2AlO2-+3H2↑;Fe+2H+=Fe2++H2↑;(6)溶液D为FeCl2,向溶液D加入NaOH溶液,观察到产生的白色絮状沉淀迅速变为灰绿色,最终变为红褐色,其中沉淀转化的化学方程式为4Fe(OH)2+O2+2H2O=4Fe(OH)3,故答案为4Fe(OH)2+O2+2H2O=4Fe(OH)3。
2020-2021高考化学 铁及其化合物推断题综合试题含详细答案

2020-2021高考化学 铁及其化合物推断题综合试题含详细答案一、铁及其化合物1.下列各物质是中学化学中常见的物质,甲为常见金属单质,丙为黄绿色的单质气体,乙、丁是常见无色气态非金属单质,其它均为化合物,C 常温下为一种液体,B 、D 分别为黑色粉末和黑色晶体,G 为淡黄色固体,J 为生活中常见的调味品,I 为红褐色固体,F 为棕黄色溶液。
①是实验室制取丁的反应之一。
各物质间的转化如下图所示,回答下列问题(部分生成物未列出):(1)物质I 的化学式为________;F 中阴离子是______________;(2)反应①的化学方程式为为____________;(3)B 与K 的反应是实验室制取丙的反应,其离子方程式为____________;(4)反应②的化学方程式为_____________;(5)若E 与G 以物质的量比为1:1投入足量水中,反应的化学方程式为_________;生成1mol 气体转移电子的个数为__________。
【答案】Fe(OH)3 Cl - 2H 2O 22MnO 2H 2O+O 2 MnO 2+4H ++2Cl -ΔMn 2++Cl 2↑+2H 2O 3Fe + 4H 2O(g)高温Fe 3O 4 +4H 2 4FeCl 2+4Na 2O 2 + 6H 2O = 4Fe(OH)3↓+8NaCl + O 2↑ 6N A【解析】【分析】丙为黄绿色单质气体,所以丙为Cl 2,B 与K 的反应是实验室制取丙的反应,且B 为黑色粉末,则B 为MnO 2,K 为HCl ;①是实验室制取丁的反应之一,则该反应为双氧水在二氧化锰的催化作用下制取氧气的反应,所以C 为H 2O ,丁为氧气;G 为淡黄色固体,且可以生成氧气,则G 应为Na 2O 2,则J 为生活中常见的调味品,应为NaCl ,I 为红褐色固体应为Fe(OH)3;F 为棕黄色溶液,应含Fe 3+,E 与氯气反应可生成F ,则F 为FeCl 3,E 为FeCl 2;氯化铁可以与单质铁反应生成氯化亚铁,所以甲为铁单质,Fe 可以在高温条件下与水反应生成氢气和四氧化三铁,所以乙为氢气,D 为Fe 3O 4。
2020-2021高考化学 铁及其化合物推断题 综合题附答案

2020-2021高考化学铁及其化合物推断题综合题附答案一、铁及其化合物1.常见物质A~K之间存在如图所示的转化关系,其中A、D、E、H为单质,请回答下列问题。
(1)下列物质的化学式是:C______,H______。
(2)反应“I→J”的离子方程式是____。
(3)检验J溶液中的金属离子的方法是(写出操作步骤、现象及结论)____。
【答案】AlCl3 Fe 2Fe2++Cl2=2Fe3++2Cl-在试管中取少量J溶液,向其中滴加几滴KSCN溶液,振荡,若溶液变为红色,则说明J溶液含有Fe3+【解析】【分析】溶液C与氨水反应生成白色沉淀F,白色沉淀F与氢氧化钠溶液反应生成溶液G,说明G 为NaAlO2,F为Al(OH)3,金属A与溶液B反应生成气体D,金属A为Al,气体D和黄绿色气体E(Cl2)反应生成气体B,气体B溶于水,溶液B与金属H反应生成溶液I,根据后面红褐色沉淀,得到金属H为Fe,则B为HCl,溶液C为AlCl3,则D为H2,溶液I为FeCl2,溶液J为FeCl3,K为Fe(OH)3。
【详解】(1)根据前面分析得到物质的化学式是:C为AlCl3,H为Fe;(2)反应“I→J”是Fe2+与Cl2反应生成Fe3+和Cl-,其离子方程式是2Fe2++Cl2=2Fe3++2Cl-;(3)检验J溶液中的金属离子的方法是主要是用KSCN溶液检验铁离子,变红,说明溶液中含有铁离子。
2.某工厂的工业硫酸盐废水中含有大量的Fe2+、Fe3+、较多的Cu2+和少量的Na+。
工厂计划从该废水中回收硫酸亚铁和金属铜,设计如下流程图。
回答下列问题;(1)A的化学式为_________,D的化学式为_______。
(2)在工业废水中加入过量A时,发应的离子方程式有:__________、______。
(3)得到FeSO4•7H2O晶体的操作Ⅲ为:加热浓缩、冷却结晶、______、______、干燥。
【答案】Fe H2SO4 Fe + 2Fe3+=3Fe2+ Fe + Cu2+=Fe2++ Cu 过滤洗涤【解析】【分析】工业废水中含大量Fe2+、Fe3+、Cu2+和少量的Na+,从该废水中回收硫酸亚铁和金属铜,结合流程可知,要加入铁粉,可置换出铜,同时生成硫酸亚铁,经过滤,得到的滤液C中主要含硫酸亚铁,滤渣B中含Cu、Fe,向该固体混合物中加入D为H2SO4,得到的溶液F为硫酸亚铁,得到滤渣E为Cu,将溶液C、F合并就是FeSO4溶液,溶液经蒸发、浓缩、冷却结晶、过滤,洗涤、干燥就可得到FeSO4·7H2O晶体,以此来解答。
2020-2021高考化学铁及其化合物推断题综合经典题及详细答案

2020-2021高考化学铁及其化合物推断题综合经典题及详细答案一、铁及其化合物1.下列各物质是中学化学中常见的物质,甲为常见金属单质,丙为黄绿色的单质气体,乙、丁是常见无色气态非金属单质,其它均为化合物,C 常温下为一种液体,B 、D 分别为黑色粉末和黑色晶体,G 为淡黄色固体,J 为生活中常见的调味品,I 为红褐色固体,F 为棕黄色溶液。
①是实验室制取丁的反应之一。
各物质间的转化如下图所示,回答下列问题(部分生成物未列出):(1)物质I 的化学式为________;F 中阴离子是______________;(2)反应①的化学方程式为为____________;(3)B 与K 的反应是实验室制取丙的反应,其离子方程式为____________;(4)反应②的化学方程式为_____________;(5)若E 与G 以物质的量比为1:1投入足量水中,反应的化学方程式为_________;生成1mol 气体转移电子的个数为__________。
【答案】Fe(OH)3 Cl - 2H 2O 22MnO 2H 2O+O 2 MnO 2+4H ++2Cl -ΔMn 2++Cl 2↑+2H 2O 3Fe + 4H 2O(g)高温Fe 3O 4 +4H 2 4FeCl 2+4Na 2O 2 + 6H 2O = 4Fe(OH)3↓+8NaCl + O 2↑ 6N A【解析】【分析】丙为黄绿色单质气体,所以丙为Cl 2,B 与K 的反应是实验室制取丙的反应,且B 为黑色粉末,则B 为MnO 2,K 为HCl ;①是实验室制取丁的反应之一,则该反应为双氧水在二氧化锰的催化作用下制取氧气的反应,所以C 为H 2O ,丁为氧气;G 为淡黄色固体,且可以生成氧气,则G 应为Na 2O 2,则J 为生活中常见的调味品,应为NaCl ,I 为红褐色固体应为Fe(OH)3;F 为棕黄色溶液,应含Fe 3+,E 与氯气反应可生成F ,则F 为FeCl 3,E 为FeCl 2;氯化铁可以与单质铁反应生成氯化亚铁,所以甲为铁单质,Fe 可以在高温条件下与水反应生成氢气和四氧化三铁,所以乙为氢气,D 为Fe 3O 4。
2020-2021高考化学铁及其化合物推断题综合题汇编附详细答案
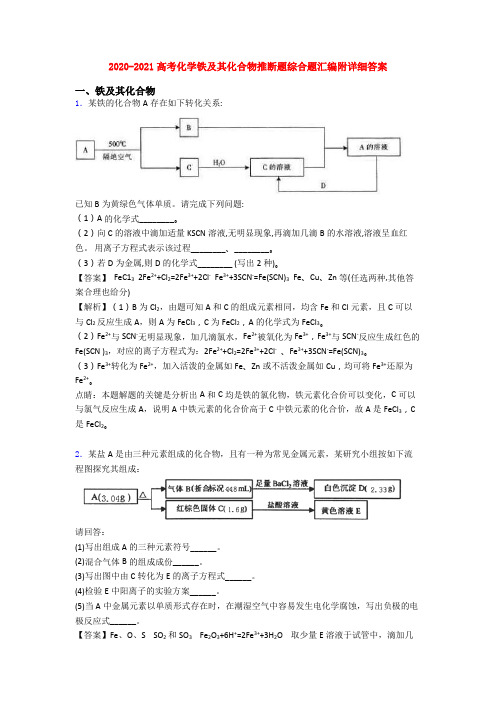
2020-2021高考化学铁及其化合物推断题综合题汇编附详细答案一、铁及其化合物1.某铁的化合物A存在如下转化关系:已知B为黄绿色气体单质。
请完成下列问题:(1)A的化学式________。
(2)向C的溶液中滴加适量KSCN溶液,无明显现象,再滴加几滴B的水溶液,溶液呈血红色。
用离子方程式表示该过程________、________。
(3)若D为金属,则D的化学式________ (写出2种)。
【答案】 FeC13 2Fe2++Cl2=2Fe3++2Cl- Fe3++3SCN-=Fe(SCN)3 Fe、Cu、Zn等(任选两种,其他答案合理也给分)【解析】(1)B为Cl2,由题可知A和C的组成元素相同,均含Fe和Cl元素,且C可以与Cl2反应生成A,则A为FeCl3,C为FeCl2,A的化学式为FeCl3。
(2)Fe2+与SCN-无明显现象,加几滴氯水,Fe2+被氧化为Fe3+,Fe3+与SCN-反应生成红色的Fe(SCN )3,对应的离子方程式为:2Fe2++Cl2=2Fe3++2Cl-、Fe3++3SCN-=Fe(SCN)3。
(3)Fe3+转化为Fe2+,加入活泼的金属如Fe、Zn或不活泼金属如Cu,均可将Fe3+还原为Fe2+。
点睛:本题解题的关键是分析出A和C均是铁的氯化物,铁元素化合价可以变化,C可以与氯气反应生成A,说明A中铁元素的化合价高于C中铁元素的化合价,故A是FeCl3,C 是FeCl2。
2.某盐A是由三种元素组成的化合物,且有一种为常见金属元素,某研究小组按如下流程图探究其组成:请回答:(1)写出组成 A的三种元素符号______。
(2)混合气体B的组成成份______。
(3)写出图中由C转化为E的离子方程式______。
(4)检验E中阳离子的实验方案______。
(5)当A中金属元素以单质形式存在时,在潮湿空气中容易发生电化学腐蚀,写出负极的电极反应式______。
【答案】Fe、O、S SO2和SO3 Fe2O3+6H+=2Fe3++3H2O 取少量E溶液于试管中,滴加几滴KSCN溶液,若溶液变为血红色,则说明E中阳离子为Fe3+ Fe-2eˉ=Fe2+【解析】【分析】由红棕色固体溶于盐酸得到棕黄色溶液,可知C为氧化铁、E为氯化铁溶液,说明A中含有铁元素和氧元素,1.6g氧化铁的物质的量为 1.6g160g/mol=0.01mol;由气体B与足量氯化钡溶液反应生成白色沉淀可知,白色沉淀D为硫酸钡、气体B中含有三氧化硫,由硫原子个数守恒可知,三氧化硫的物质的量为 2.33g233g/mol=0.01mol,气体B的物质的量为0.448 22.4/LL mol=0.02mol,由A是由三种元素组成的化合物可知,A中含有硫元素、气体B为二氧化硫和三氧化硫的混合气体,二氧化硫的物质的量为(0.02—0.01)mol=0.01mol,m (SO3)+m(SO2)+m(Fe2O3)=0.01mol×80g/mol+0.01mol×64g/mol+1.6g=3.04g,说明A 中nFe):n(S):n(O)=1:1:4,则A为FeSO4。
2020-2021高考化学 铁及其化合物推断题综合试题含答案解析

2020-2021高考化学 铁及其化合物推断题综合试题含答案解析一、铁及其化合物1.下列各物质是中学化学中常见的物质,甲为常见金属单质,丙为黄绿色的单质气体,乙、丁是常见无色气态非金属单质,其它均为化合物,C 常温下为一种液体,B 、D 分别为黑色粉末和黑色晶体,G 为淡黄色固体,J 为生活中常见的调味品,I 为红褐色固体,F 为棕黄色溶液。
①是实验室制取丁的反应之一。
各物质间的转化如下图所示,回答下列问题(部分生成物未列出):(1)物质I 的化学式为________;F 中阴离子是______________;(2)反应①的化学方程式为为____________;(3)B 与K 的反应是实验室制取丙的反应,其离子方程式为____________;(4)反应②的化学方程式为_____________;(5)若E 与G 以物质的量比为1:1投入足量水中,反应的化学方程式为_________;生成1mol 气体转移电子的个数为__________。
【答案】Fe(OH)3 Cl - 2H 2O 22MnO 2H 2O+O 2 MnO 2+4H ++2Cl -ΔMn 2++Cl 2↑+2H 2O 3Fe + 4H 2O(g)高温Fe 3O 4 +4H 2 4FeCl 2+4Na 2O 2 + 6H 2O = 4Fe(OH)3↓+8NaCl + O 2↑ 6N A【解析】【分析】丙为黄绿色单质气体,所以丙为Cl 2,B 与K 的反应是实验室制取丙的反应,且B 为黑色粉末,则B 为MnO 2,K 为HCl ;①是实验室制取丁的反应之一,则该反应为双氧水在二氧化锰的催化作用下制取氧气的反应,所以C 为H 2O ,丁为氧气;G 为淡黄色固体,且可以生成氧气,则G 应为Na 2O 2,则J 为生活中常见的调味品,应为NaCl ,I 为红褐色固体应为Fe(OH)3;F 为棕黄色溶液,应含Fe 3+,E 与氯气反应可生成F ,则F 为FeCl 3,E 为FeCl 2;氯化铁可以与单质铁反应生成氯化亚铁,所以甲为铁单质,Fe 可以在高温条件下与水反应生成氢气和四氧化三铁,所以乙为氢气,D 为Fe 3O 4。
2020-2021高考化学综合题专题复习【铁及其化合物推断题】专题解析及详细答案
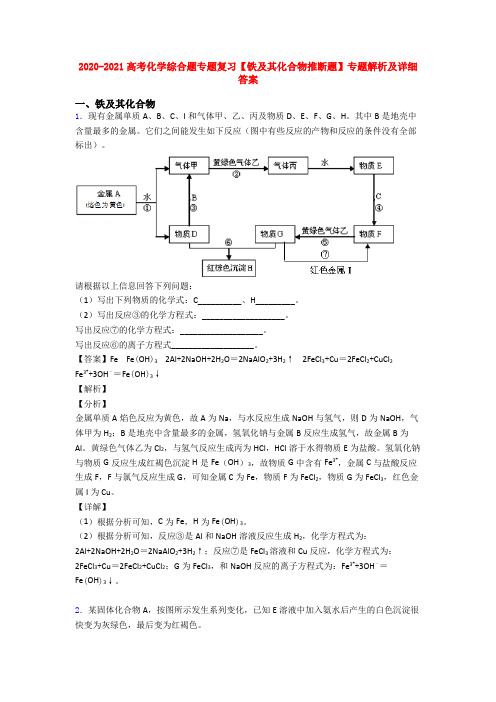
2020-2021高考化学综合题专题复习【铁及其化合物推断题】专题解析及详细答案一、铁及其化合物1.现有金属单质A、B、C、I和气体甲、乙、丙及物质D、E、F、G、H。
其中B是地壳中含量最多的金属。
它们之间能发生如下反应(图中有些反应的产物和反应的条件没有全部标出)。
请根据以上信息回答下列问题:(1)写出下列物质的化学式:C__________、H_________。
(2)写出反应③的化学方程式:___________________。
写出反应⑦的化学方程式:___________________。
写出反应⑥的离子方程式___________________。
【答案】Fe Fe(OH)3 2Al+2NaOH+2H2O=2NaAlO2+3H2↑ 2FeCl3+Cu=2FeCl2+CuCl2Fe3++3OH﹣=Fe(OH)3↓【解析】【分析】金属单质A焰色反应为黄色,故A为Na,与水反应生成NaOH与氢气,则D为NaOH,气体甲为H2;B是地壳中含量最多的金属,氢氧化钠与金属B反应生成氢气,故金属B为Al。
黄绿色气体乙为Cl2,与氢气反应生成丙为HCl,HCl溶于水得物质E为盐酸。
氢氧化钠与物质G反应生成红褐色沉淀H是Fe(OH)3,故物质G中含有Fe3+,金属C与盐酸反应生成F,F与氯气反应生成G,可知金属C为Fe,物质F为FeCl2,物质G为FeCl3,红色金属I为Cu。
【详解】(1)根据分析可知,C为Fe,H为Fe(OH)3。
(2)根据分析可知,反应③是Al和NaOH溶液反应生成H2,化学方程式为:2Al+2NaOH+2H2O=2NaAlO2+3H2↑;反应⑦是FeCl3溶液和Cu反应,化学方程式为:2FeCl3+Cu=2FeCl2+CuCl2;G为FeCl3,和NaOH反应的离子方程式为:Fe3++3OH﹣=Fe(OH)3↓。
2.某固体化合物A,按图所示发生系列变化,已知E溶液中加入氨水后产生的白色沉淀很快变为灰绿色,最后变为红褐色。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
2020-2021备战高考化学铁及其化合物推断题综合题附答案解析一、铁及其化合物1.印刷电路板(PCB)是用腐蚀液(FeCl3溶液)将覆铜板上的部分铜腐蚀掉而制得。
一种制作PCB并将腐蚀后废液(其中金属阳离子主要含Fe3+、Cu2+、Fe2+)回收再生的流程如图。
请回答:(1)腐蚀池中发生反应的化学方程式是__。
(2)上述各池中,没有发生化学变化的是__池。
(3)由置换池中得到固体的操作名称是__。
(4)置换池中发生反应的离子方程式有__。
(5)请提出利用酸从固体中回收Cu并将滤液回收利用的合理方案:__。
(6)向再生池中通入Cl2也可以使废液再生,相比Cl2,用双氧水的优点是__。
【答案】Cu+2FeCl3=CuCl2+2FeCl2沉降过滤 Fe+2Fe3+=3Fe2+、Fe+Cu2+=Fe2++Cu 用盐酸溶解固体中的Fe,过滤后得到Cu,并将滤液加入再生池避免有毒气体污染环境【解析】【分析】腐蚀液(FeCl3溶液)将覆铜板上,发生反应为:Cu+2FeCl3=CuCl2+2FeCl2,再在沉降池中沉降后加入铁粉置换出铜单质、以及铁与铁离子反应生成亚铁离子,再生池中主要指FeCl2,通入过氧化氢氧化生成FeCl3,循环利用。
【详解】(1)腐蚀液(FeCl3溶液)将覆铜板上腐蚀池中发生反应的化学方程式为:Cu+2FeCl3=CuCl2+2FeCl2;(2)腐蚀池中发生:Cu+2FeCl3=CuCl2+2FeCl2;置换池中铁粉置换出铜、以及铁与铁离子反应生成亚铁离子,再生池中过氧化氢氧化FeCl2,没有发生化学变化的是沉降池;(3)置换池中铁粉置换出铜,固液分离的操作为过滤;(4)置换池中铁粉置换出铜、以及铁与铁离子反应生成亚铁离子,其离子反应方程式:Fe+2Fe3+=3Fe2+、Fe+Cu2+=Fe2++Cu;(5)根据金属活动性顺序表可知,铁能与稀盐酸发生反应,而铜不与稀盐酸反应,所以用盐酸溶解固体中的Fe,过滤后得到Cu,并将滤液加入再生池;(6)Cl2有毒,污染环境,需要尾气处理,加双氧水氧化后生成水,避免有毒气体污染环境,故答案为:避免有毒气体污染环境。
2.物质X是某新型净水剂的中间体,它可以看成由AlCl3(在180℃升华)和一种盐A按物质的量之比1:2组成。
在密闭容器中加热X使之完全分解,发生如下转化:请回答下列问题:(1)X的化学式为__。
(2)将E混合晶体溶于水配成溶液,向溶液中加入过量稀NaOH溶液时发生的总反应的离子方程式为__。
(3)高温下,若在密闭容器中长时间煅烧X,产物中还有另外一种气体,请设计实验方案验证之_。
【答案】AlCl3·2FeSO4 Al3++2H++6OH-=AlO2-+4H2O 将气体通入足量NaOH溶液中,收集余气,把一条带火星的木条伸入其中,若复燃,则说明是O2【解析】【分析】固体氧化物B溶于稀盐酸后得到的溶液C中滴加KSCN溶液,混合液变血红色,说明B中含有Fe3+,则B为Fe2O3,C为FeCl3溶液,无色D气体能使品红褪色,则D为SO2,由元素守恒可知A中含有Fe、S、O元素,A加热分解能生成氧化铁和二氧化硫,则盐A为FeSO4,氧化铁的物质的量为3.2g160g/mol=0.02mol,生成二氧化硫为0.448L22.4L/mol=0.02mol,由Fe、S原子为1:1可知生成SO3为0.02mol,4.27g混合晶体E为AlCl3和SO3,AlCl3的物质的量为4.27g-0.02mol80g/mol133.5g/mol=0.02mol,X的组成为AlCl3∙2FeSO4,以此解答该题。
【详解】(1)根据上述分析,X的化学式为AlCl∙2FeSO4;(2)将E混合晶体溶于水配成溶液,三氧化硫反应生成硫酸,则硫酸与氯化铝的物质的量相等,逐滴加入过量稀NaOH溶液,该过程的总反应的离子方程式为:Al3++2H++6OH-=AlO2-+4H2O;(3)若在高温下长时间煅烧X,生成的三氧化硫再分解生成二氧化硫和氧气,另一种气体分子式是O2,检验氧气的方法为:将气体通入足量NaOH溶液中,收集余气,把一条带火星的本条伸入其中,若复燃,则说明是O2。
3.某盐A是由三种元素组成的化合物,且有一种为常见金属元素,某研究小组按如下流程图探究其组成:请回答:(1)写出组成 A的三种元素符号______。
(2)混合气体B的组成成份______。
(3)写出图中由C转化为E的离子方程式______。
(4)检验E中阳离子的实验方案______。
(5)当A中金属元素以单质形式存在时,在潮湿空气中容易发生电化学腐蚀,写出负极的电极反应式______。
【答案】Fe、O、S SO2和SO3 Fe2O3+6H+=2Fe3++3H2O 取少量E溶液于试管中,滴加几滴KSCN溶液,若溶液变为血红色,则说明E中阳离子为Fe3+ Fe-2eˉ=Fe2+【解析】【分析】由红棕色固体溶于盐酸得到棕黄色溶液,可知C为氧化铁、E为氯化铁溶液,说明A中含有铁元素和氧元素,1.6g氧化铁的物质的量为 1.6g160g/mol=0.01mol;由气体B与足量氯化钡溶液反应生成白色沉淀可知,白色沉淀D为硫酸钡、气体B中含有三氧化硫,由硫原子个数守恒可知,三氧化硫的物质的量为 2.33g233g/mol=0.01mol,气体B的物质的量为0.448 22.4/LL mol=0.02mol,由A是由三种元素组成的化合物可知,A中含有硫元素、气体B为二氧化硫和三氧化硫的混合气体,二氧化硫的物质的量为(0.02—0.01)mol=0.01mol,m (SO3)+m(SO2)+m(Fe2O3)=0.01mol×80g/mol+0.01mol×64g/mol+1.6g=3.04g,说明A 中nFe):n(S):n(O)=1:1:4,则A为FeSO4。
【详解】(1)由分析可知,A为FeSO4,含有的三种元素为Fe、O、S,故答案为:Fe、O、S;(2)由分析可知,三氧化硫的物质的量为 2.33g233g/mol=0.01mol,气体B的物质的量为0.448 22.4/LL mol=0.02mol,由A是由三种元素组成的化合物可知,A中含有硫元素、气体B为二氧化硫和三氧化硫的混合气体,故答案为:SO2和SO3;(3)C为氧化铁、E为氯化铁溶液,氧化铁与盐酸反应生成氯化铁和水,反应的离子方程式为Fe2O3+6H+=2Fe3++3H2O,故答案为:Fe2O3+6H+=2Fe3++3H2O;(3)E为氯化铁溶液,检验铁离子的实验方案为可取少量E溶液于试管中,滴加几滴KSCN溶液,若溶液变为血红色,则说明E中阳离子为Fe3+,故答案为:取少量E溶液于试管中,滴加几滴KSCN溶液,若溶液变为血红色,则说明E中阳离子为Fe3+;(5)铁在潮湿空气中容易发生电化学腐蚀,铁做原电池的负极,失去电子发生氧化反应生成亚铁离子,电极反应式为Fe-2eˉ=Fe2+,故答案为:Fe-2eˉ=Fe2+。
【点睛】注意从质量守恒的角度判断A的化学式,把握二氧化硫的性质、铁离子检验为解答的关键。
4.以废旧锌锰电池中的黑锰粉(MnO2、MnO(OH)、NH4Cl、少量ZnCl2及炭黑、氧化铁等)为原料制备MnCl2,实现锰的再利用。
其工作流程如下:(1)过程Ⅰ,在空气中加热黑锰粉的目的是除炭、氧化MnO(OH)等。
O 2氧化MnO(OH)的化学方程式是_______。
(2)溶液a 的主要成分为NH 4Cl ,另外还含有少量ZnCl 2等。
① 溶液a 呈酸性,原因是______。
② 根据如图所示的溶解度曲线,将溶液a______(填操作),可得NH 4Cl 粗品。
③ 提纯NH 4Cl 粗品,有关性质数据如下: 化合物ZnCl 2 NH 4Cl 熔点365℃ 337.8℃分解 沸点 732℃ -------------根据上表,设计方案提纯NH 4Cl :________。
(3)检验MnSO 4溶液中是否含有Fe 3+:取少量溶液,加入_______(填试剂和现象),证明溶液中Fe 3+沉淀完全。
(4)探究过程Ⅱ中MnO 2溶解的适宜条件。
ⅰ.向MnO 2中加入H 2O 2溶液,产生大量气泡;再加入稀H 2SO 4,固体未明显溶解。
ⅱ.向MnO 2中加入稀H 2SO 4,固体未溶解;再加入H 2O 2溶液,产生大量气泡,固体完全溶解。
① 用化学方程式表示ⅱ中MnO 2溶解的原因:________。
② 解释试剂加入顺序不同,MnO 2作用不同的原因:________。
上述实验说明,试剂加入顺序不同,物质体现的性质可能不同,产物也可能不同。
【答案】4MnO(OH)+O 2==4MnO 2+2H 2O NH 4++H 2O ⇌NH 3·H 2O+H +(或NH 4+水解产生H +) 蒸发浓缩,趁热过滤 加热NH 4Cl 粗品至340℃左右,NH 4Cl = NH 3 + HCl ;收集产物并冷却,NH 3 + HCl=NH 4Cl ,得到纯净NH 4Cl 。
KSCN 溶液,不变红MnO 2+H 2O 2+H 2SO 4==MnSO 4+2H 2O+O 2↑i 中2MnO 作催化剂,反应快,2MnO 只催化分解22H O ii 中2MnO 作氧化剂,加入稀24H SO 后,2MnO 的氧化性增强,被22H O 还原为4MnSO 。
【解析】【详解】(1)根据流程图可知,经过过程Ⅰ,得到了MnO 2粗品,则O 2将MnO(OH)氧化成MnO 2,根据得失电子守恒,1molO 2得到4mol 电子,1molMnO(OH)失去1mol 电子,则O 2和MnO(OH)的比例为1∶4,再根据原子守恒可配平方程式,答案为4MnO(OH)+O 2=4MnO 2+2H 2O ;(2)①ZnCl 2和NH 4Cl 均为强酸弱碱盐,均会水解,铵根离子水解使溶液呈酸性,答案为NH 4++H 2O ⇌NH 3·H 2O+H +(或NH 4+水解产生H +);②从曲线可以看出,随着温度的变化,NH 4Cl 的溶解度几乎没有发生太大的变化,只能蒸发溶剂得到晶体,再进行后续操作,答案为蒸发浓缩,趁热过滤;③从表格中数据可以知道,NH 4Cl 在337.8℃分解,生成NH 3和HCl ,而此温度下,ZnCl 2没有熔化,也没有分解,因此可以利用NH 4Cl 的分解,收集产物再次合成NH 4Cl ,答案为加热NH 4Cl 粗品至340℃左右,NH 4Cl = NH 3 + HCl ;收集产物并冷却,NH 3 + HCl=NH 4Cl ,得到纯净NH 4Cl ;(3)Fe 3+的检验常用KSCN 溶液,如果溶液中有铁离子,生成红色物质;没有Fe 3+就不会变红,答案为KSCN 溶液,不变红;(4)从实验ⅰ知道,先加入双氧水,MnO 2不溶解,只做催化剂,而通过实验ⅱ可知,先加入硫酸,固体溶解,且有气体冒出,气体为氧气,则MnO 2作了氧化剂,双氧水作了还原剂。
